Introducción
Se denomina aneurisma de la aorta abdominal (AAA) a la dilatación localizada de la aorta abdominal mayor de 1,5 veces el diámetro esperado (usualmente más de 2 desviaciones estándar sobre el diámetro promedio). Es una condición con una prevalencia entre 1,3 y 12,5 %, que varía con la edad 1-3 y ha ido en aumento. En Colombia, García, et al. 4, reportaron una prevalencia baja, menor del 1 %. Es la causa de alrededor de 11.000 fallecimientos por año en los Estados Unidos 5.
Las características bioquímicas y fisiopatológicas del AAA son complejas 6 y se identifican tres etapas en su formación 7: desarrollo, crecimiento y ruptura. Los factores de riesgo asociados con mayor frecuencia en la literatura son tabaquismo (considerado el de mayor importancia) 8,9, sexo masculino, edad, historia familiar de aneurismas, enfermedad pulmonar obstructiva crónica, hipercolesterolemia y presencia de calcificaciones 6-10.
Cabe resaltar que el 75 % de los pacientes son asintomáticos y el porcentaje restante desarrolla síntomas inespecíficos como: edema de miembros inferiores (MMII), dolor lumbar con eventuales síntomas urológicos, dolor abdominal y pérdida de peso. La ruptura, que es una de las formas de presentación inicial, es una emergencia quirúrgica con un alto riesgo de muerte (hasta un 90 %), donde el diámetro del aneurisma es el factor predictor más importante 11.
A pesar de los cambios en la prevalencia de AAA, desde finales del siglo pasado un buen número de países han implementado programas de tamizaje en hombres mayores de 65 años. La aplicación de medidas contra el tabaquismo y el manejo de los factores de riesgo cardiovascular, así como la realización de pruebas para la detección temprana de esta condición, han demostrado ser costo-efectivas, tal como lo reflejaron Svensjö, et al., en su estudio 12-14. El objetivo de la revisión fue describir las herramientas de tamizaje de AAA, comprender su alcance y el tipo de evidencia en relación con la literatura.
Métodos
Se realizó una búsqueda de la literatura en bases de datos electrónicas como MEDLINE (vía Pubmed y Ovid), Cochrane Library (vía Willey), EMBASE, LILACS y Google Scholar. Se tomó las publicaciones de los últimos 10 años, en inglés y español, utilizando dos ecuaciones de búsqueda que emplearon términos seleccionados a partir de los tesauros “Medical Subject Heading” (MeSH) y “Descriptores en Ciencias de la Salud” (DeCS). Tras la búsqueda, todas las citas identificadas se cotejaron y cargaron al programa bibliográfico o sistema de gestión de citas Mendeley, para eliminar los duplicados. Luego se examinaron los títulos y resúmenes, para una posterior evaluación de la calidad de los estudios encontrados con la herramienta STROBE (Strengthening the Reporting of Observational studies in Epidemiology). De la anterior evaluación se tomaron 5 ítems, título y resumen, introducción, métodos con sus respectivas divisiones, resultados con sus diferentes segmentaciones, análisis, discusión y otra información. Por último, se extrajo la información más relevante para la construcción de la revisión.
Resultados
Factores de riesgo
Posterior a la revisión de la literatura disponible y la evaluación de la calidad de los artículos encontrados con la herramienta STROBE, se identificaron los factores de riesgo asociados a AAA (Tabla 1) y a partir de estos se definieron las pautas de tamizaje.
Tabla 1. Factores de riesgo para aneurisma de aorta abdominal
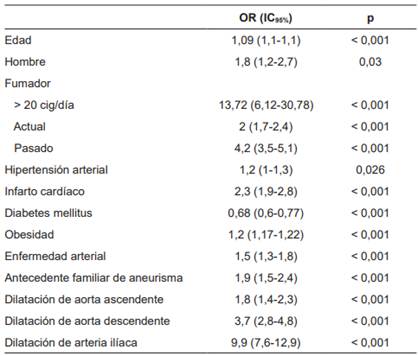
* Diabetes mellitus, hipertensión arterial, fibrilación auricular, anemia y enfermedad renal crónica no mostraron ser factores de riesgo.
La importancia de estos hallazgos tiene que ver con el diseño de procesos de tamizaje, ya que el desarrollo del AAA parece ser el resultado de la combinación de predisposición genética, factores comportamentales e individuales 15.
Herramientas de tamizaje
La Sociedad Europea de Cirugía Vascular (ESVS) publicó las guías de práctica clínica para el manejo de aneurismas abdominales aorto-ilíacos en 2019 3. Por su parte, el Grupo de Trabajo de Servicios Preventivos de Estados Unidos publicó, el mismo año, las recomendaciones para el Tamizaje de Aneurismas Aórticos 16, las cuales se encuentran consignadas en la Tabla 2.
Tabla 2. Recomendaciones para tamizaje de aneurisma de aorta abdominal (AAA) en Europa y Estados Unidos
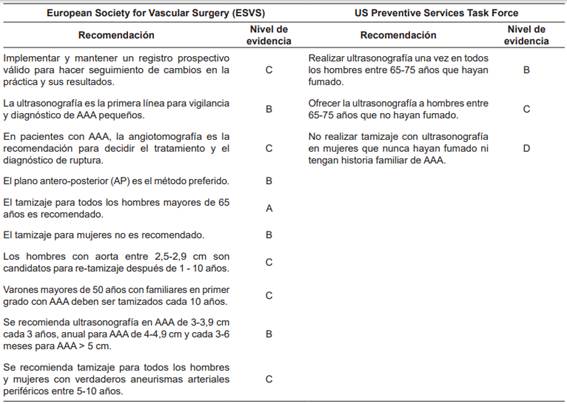
De lo anterior se pudo evidenciar que la ultrasonografía es uno de los métodos imagenológicos más usados como parte del tamizaje. Como señalaron en 2019 Blum-Gilbert, et al. 17, en su algoritmo diagnóstico no invasivo de AAA, el cirujano debe usar apropiadamente todas las herramientas a su alcance porque esto determina el pronóstico de los pacientes, sobre todo si la detección es temprana.
Discusión
Definición
Se denomina aneurisma de la aorta abdominal (AAA) a la dilatación localizada en la aorta abdominal mayor de 1,5 veces el diámetro esperado 3. Para Carino, et al. 15, la definición del AAA plantea la irreversibilidad del aumento de grosor de vaso que exceda 1,5 veces el diámetro normal, que en la aorta abdominal es mayor de 3 cm. Por otro lado, en Corea, Kim, et al. (2023), describieron tamaños de la aorta normal menores comparando con los reportados por los europeos 18.
Etiología
La etiología de AAA es multifactorial. Es decir, participan factores de orden bioquímico, metabólico, físico y hereditario, entre otros. Los diferentes modelos etiológicos incluyen teorías inflamatorias, de degradación proteica y de apoptosis de las células de la musculatura lisa 15,17. Estas influyen directamente en la estructura de la pared aórtica, causando una degeneración en la túnica media. Hao, et al. 14, en 2017, presentaron un modelo matemático que predice el desarrollo de AAA relacionando el aumento del tamaño aórtico con las concentraciones séricas de Interleucina-6.
Epidemiología
En el siglo pasado, los países desarrollados reportaron cambios sostenidos en la incidencia y la mortalidad. La prevalencia reportada en países desarrollados está alrededor de 3 al 5 %, siendo 4 veces más frecuente en hombres que en mujeres, sin embargo, con una mayor mortalidad en ellas, dado que tienen cuatro veces más riesgo de ruptura 19. Se ha demostrado, además, un aumento en la incidencia, muy posiblemente relacionado con el uso de nuevas herramientas diagnósticas, a pesar de las medidas implementadas para el control de los factores de riesgo, como el cese del tabaquismo, el aumento del ejercicio, la dieta y las medidas para el control de patologías cardiovasculares.
Powell, et al. 20, en una revisión sistemática en 2011, informaron que la tasa de ruptura de aneurismas entre 3 y 5,5 cm varió de 0 a 1,61/100 personas-año.
Factores de riesgo
Para el año 2021, Obel, et al. 21, posterior a un análisis multivariado en Dinamarca, señalaron que el factor de riesgo más importante para AAA es la documentación de una dilatación en cualquier otro segmento aórtico, incluyendo las arterias ilíacas. Sin embargo, una evaluación del tamaño aórtico de manera individualizada ayudará a distinguir los pacientes sanos con variaciones biológicas superiores a las normales de aquellos pacientes que pueden haber comenzado una dilatación aórtica patológica.
Por otro lado, el tabaquismo es uno de los factores de riesgo más importante para el desarrollo de AAA, dado que aumenta la progresión de ateroesclerosis aórtica, considerando que existe una relación lineal clara entre el número de cigarrillos fumados o el número de años fumando y la presencia de AAA 9,22. Según Howard, et al. 23, luego de 10 años de seguimiento los fumadores tuvieron un incremento en el desarrollo de ateroesclerosis, siendo el riego relativo de 1,4 (IC95% 1,0 a 2,0) entre fumadores de 1 a 9 cigarrillos diarios vs 2,3 (IC95% 1,8 a 3,0) entre fumadores de más de 20 cigarrillos diarios. No obstante, pese al abandono del consumo de tabaco se continuó observando un riesgo mayor hasta después de 10 años de 1,6 (IC95% 1,1 a 2,2).
Además, variables como hipertensión arterial, infarto de miocardio, enfermedad arterial oclusiva, antecedente familiar de aneurisma, dilatación de la aorta ascendente o descendente y obesidad se deben tener presentes para la clasificación de estos pacientes respecto al tamizaje 1,19. La diabetes mellitus, sorprendentemente, parece actuar como factor de protección 24.
Tamizaje
El concepto de tamizaje de los AAA puede ser aplicado con dos propósitos: el primero, identificar la presencia de una enfermedad aneurismática en su etapa subclínica en los grupos de mayor riesgo (tamizaje primario) y el segundo, definir un método de seguimiento intentando documentar su particular ritmo de crecimiento (tamizaje secundario).
La identificación de pacientes en una etapa subclínica, en la que aún no se presentan signos y síntomas, pretende disminuir la morbimortalidad asociada a diagnósticos tardíos por lo que los métodos de tamizaje son más útiles cuando el período prepatogénico es largo, ya que en ese momento, la intervención reduce el riesgo y la necesidad de procedimientos de urgencia, dado que estos aumentan los costos y la morbimortalidad asociada 17,25.
Para determinar la utilidad de estos tamizajes, en términos de salud pública, se deben tener en cuenta factores como dificultad de la prueba, prevalencia de la enfermedad, costo-eficacia del tratamiento temprano y los resultados a largo plazo en los sujetos no detectados 19.
Así mismo, durante años se han promovido diversas herramientas para el tamizaje, que van desde el uso de la radiografía convencional y el ultrasonido, pasando a la tomografía axial computarizada (TAC) con contraste, la resonancia magnética nuclear (RMN) contrastada, la tomografía de emisión de positrones (PET) y la ecocardiografía. Beede, et al. 22, desde finales de los años 80’s plantearon la utilidad del ultrasonido para el diagnóstico de AAA. Actualmente los datos muestran que la ultrasonografía es el método con mayor especificidad y sensibilidad para la tamización, además de ser el de más fácil acceso.
El ultrasonido realizado por personal entrenado es considerado un mecanismo apropiado de tamizaje, diagnóstico y seguimiento del AAA 16,26, con una sensibilidad de 95 % y una especificidad de 99 %, en comparación a la palpación abdominal que tiene una sensibilidad de 68 % y especificidad de 75 % 25.
Por otra parte, la angiotomografía es la herramienta más eficaz en la búsqueda activa o en pacientes con alta sospecha y es considerada el estándar de oro para el diagnóstico. Además, es la herramienta diagnostica utilizada para la toma decisiones quirúrgicas 17.
Los estudios con seguimiento superiores a los 10 años han demostrado cómo la tamización con el uso de ultrasonografía es beneficiosa para prevenir las muertes relacionadas con AAA en personas mayores de 65 años 15. Así, por ejemplo, The Multicentre Aneurysm Screening Study (MASS) es el ensayo clínico controlado más grande realizado hasta la fecha, llevado a cabo en el Reino Unido, el cual demostró el beneficio del tamizaje 27. Por su parte, Argyriou, et al. 28, en 2018, argumentaron que dado a que los pacientes llevados a ecocardiografía transtorácica en muchas ocasiones presentan un perfil de riesgo similar, estos deberían en ese mismo procedimiento ser tamizados para AAA.
En 2016, el grupo de trabajo para el cuidado de la salud canadiense hizo una revisión sistemática sobre los beneficios y los riesgos de hacer tamización con ultrasonido, encontrando que el tamizaje en mayores de 65 años disminuye significativamente la ruptura y la mortalidad asociadas a AAA en hombres. Además, concluyeron que el beneficio incluye disminución de la mortalidad postoperatoria en todos los seguimientos hasta 15 años 29.
La edad máxima considerada para el uso de la tamización con ultrasonografía es de 80 años. El estudio IMPROVE 30 demostró que la técnica es segura en esta población, por lo que propusieron aumentar la edad para tamizar dependiendo de la expectativa de vida de cada sujeto. En Chile, Poblete 31 informó en 2002 que de no tamizarse los mayores de 70 años se escaparía un porcentaje importante de pacientes con AAA, por lo cual se necesita hacer tamizaje mínimo hasta los 75 años.
Según Moxon, et al. 32, en EEUU el 40 % de las muertes y la tercera parte de las admisiones hospitalarias por ruptura de AAA ocurren en mujeres y en el Reino Unido la tasa de ruptura de AAA es tres veces mayor en este sexo 2, por lo que, ante el riesgo aumentado, algunos trabajos sugieren realizar una ultrasonografía en todas las mujeres entre 65 y 80 años con historia de tabaquismo o enfermedad cardiovascular.
También se ha demostrado que la prevalencia de AAA es mayor en parientes de pacientes con aneurismas, por lo que se sugiere realizar una ultrasonografía en parientes de primer grado de consanguinidad mayores de 55 años 33.
Por otra parte, la ultrasonografía en el sitio del paciente (Point of Care Ultrasonography - POCUS) es equivalente frente a la ultrasonografía convencional para tamizar el AAA. Los éxitos obtenidos en disminuir la mortalidad con el uso de esta modalidad imagenológica han llevado a algunos a plantear el uso del tamizaje ultrasonográfico para otras patologías vasculares 34.
En los últimos años se han planteado nuevas estrategias de tamizaje. Según Raffort, et al. 35, los riesgos de progresión y ruptura son difíciles de predecir, por lo cual propugnan por el uso de Inteligencia Artificial (machine learning) para evaluar el pronóstico y la predicción de riesgo de ruptura.
Tratamiento
El manejo del aneurisma de la aorta abdominal es quirúrgico y dependerá de su tamaño. De manera tradicional se han descrito los abordajes abiertos, pero con el avance de la tecnología, la cirugía endovascular se ha vuelto parte del pilar de manejo. El empleo de técnicas endovasculares para reparación del AAA ha mostrado un beneficio en pacientes hombres mayores de 65 años. Como ilustración, el uso del Endovascular Aneurysm Repair (EVAR), desde hace un lustro propende por el uso de imágenes tridimensionales fusionadas a la fluoroscopia tradicional, ha disminuido en un 50 % la irradiación, lo que conlleva a mejor cuidado perioperatorio 36. Los programas de tamizaje de AAA en Suecia y el Reino Unido han aumentado la aplicación de estas técnicas para la reparación 35.
En otro sentido, también se ha discutido el uso de terapias no quirúrgicas para el manejo de AAA, especialmente en sujetos con alto riesgo. Pincemail, et al. 8, en 2018, propusieron el uso de antioxidantes, pero no presentaron evidencia suficiente. Por su parte, Musumeci, et al. 37, partiendo del conocimiento de los mecanismos involucrados en el desarrollo de esta patología, en los que participan diversos mediadores inflamatorios implicados en la activación de vías que llevan a la degradación de la matriz extracelular, para reducir la progresión del AAA, en 2022 propusieron focalizar la terapia farmacológica utilizando polifenoles de la dieta para disminuir el estrés oxidativo patológico. Además, el uso de metformina dado su efecto en la disminución de fosforilación oxidativa mitocondrial, lleva a la inhibición de la inflamación y la reducción de la angiogénesis. Por último, la administración de antiplaquetarios para impedir la aparición de trombos que participan en la progresión aneurismática.
Conclusiones
El AAA es una patología con una incidencia variable a nivel mundial, que aumenta conforme con la edad. Los individuos de 60 años o más, con primer grado de consanguinidad de pacientes con AAA, deben ser sometidos a examen físico y tamizaje con ultrasonido, al igual que aquellos pacientes de 65 años o más que hayan fumado. No se recomienda el tamizaje de rutina en pacientes sin antecedente de tabaquismo. La angiotomografía se considera hoy el estándar de oro para el diagnóstico y la evaluación preoperatoria. Gracias a la resolución de los equipos actuales es posible evaluar en detalle la anatomía de la aorta y órganos relacionados, con una sensibilidad y una especificidad cercanas al 100 %. Aumentos mayores de 3 cm deben ser seguidos periódicamente y manejados de forma conservadora, incluyendo el control de los factores de riesgo modificables.
El tamizaje de AAA en un método confiable y costo-efectivo para la detección temprana de los pacientes con AAA, con lo cual se puede brindar diagnóstico temprano y plantear estrategias de tratamiento, que pueden tener beneficios para el paciente con opciones de manejo de forma oportuna que evitan la ruptura, lo que conllevaría a una mayor tasa de morbimortalidad y a un aumento muy significativo en el costo de los tratamientos.















