Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957On-line version ISSN 2500-7440
Rev. colomb. Gastroenterol. vol.38 no.3 Bogotá July/Sept. 2023 Epub Dec 15, 2023
https://doi.org/10.22516/25007440.948
Trabajos originales
Drenaje de pseudoquistes pancreáticos con stent metálico luminal de aposición (LAMS): experiencia en dos centros de referencia en Colombia
1Internist, gastroenterologist, epidemiologist. Gastroenterologist, Gastroadvanced IPS, Bogotá, Hospital Internacional de Colombia, Bucaramanga, Colombia.
2Internist, gastroenterologist, rheumatologist, Hospital Internacional de Colombia. Bucaramanga, Colombia.
3Gastroenterology fellow. Universidad Nacional de Colombia. Bogotá, Colombia.
4Surgeon. Associate physician, Gastroadvanced IPS. Bogotá, Colombia.
Introducción:
el drenaje guiado por ultrasonido endoscópico (USE) y el uso de stent metálico luminal de aposición (LAMS) son de elección en el manejo de los pseudoquistes pancreáticos sintomáticos.
Objetivo:
evaluar la efectividad y seguridad del LAMS para el drenaje por USE de pseudoquistes pancreáticos sintomáticos en dos centros de referencia en Colombia.
Materiales y métodos:
estudio de cohorte prospectivo multicéntrico entre junio de 2019 y diciembre de 2021, se incluyeron a 13 pacientes con diagnóstico de pseudoquistes pancreáticos sintomáticos sometidos a drenaje por USE con LAMS. Se evaluaron como desenlaces el éxito técnico, el éxito clínico y la extracción exitosa del stent. Y los desenlaces de seguridad incluyeron eventos adversos relacionados con el stent y los eventos adversos generales. Se realizó seguimiento a 8 semanas, en las que se recopilaron datos relacionados con el retiro del stent.
Resultados:
la edad promedio fue 53,4 años, 8/13 fueron hombres. El tamaño medio del pseudoquiste fue de 9,56 ± 2,3 cm. El éxito técnico fue del 100% y el éxito clínico fue 92,3%. Los stents fueron retirados en promedio a las 8 ± 2 semanas. El tiempo medio del procedimiento desde la punción hasta el despliegue del stent fue 3,2 ± 2,4 minutos. En el control imagenológico hubo un adecuado drenaje de las colecciones en todos los casos. Hubo baja frecuencia de complicaciones, se documentó sangrado en 1 caso con requerimiento quirúrgico.
Conclusiones:
el uso de LAMS es seguro y efectivo en el manejo de pseudoquistes pancreáticos sintomáticos, disminuye la estancia hospitalaria y sobrecostos. La sintomatología clínica prima en la decisión de intervención.
Palabras clave: Endosonografía; ultrasonografía intervencionista; endoscopia gastrointestinal; pseudoquiste pancreático; pancreatitis; stent metálico por aposición.
Introduction:
Endoscopic ultrasound (EUS)-guided drainage and luminal-apposing metal stents (LAMS) are the options for managing symptomatic pancreatic pseudocysts.
Aim:
To evaluate the effectiveness and safety of LAMS for EUS-guided drainage of symptomatic pancreatic pseudocysts in two referral centers in Colombia.
Materials and methods:
A multicenter prospective cohort study between June 2019 and December 2021 included 13 patients diagnosed with symptomatic pancreatic pseudocysts who underwent EUS-guided drainage with LAMS. Technical success, clinical success, and successful stent removal were evaluated as outcomes. Safety outcomes included stent-related adverse events and general adverse events. Follow-up was carried out for eight weeks, collecting data on stent removal.
Results:
The average age was 53.4 years; 8/13 were men. The mean size of the pseudocyst was 9.56 ± 2.3 cm. Technical success was 100%, and clinical success was 92.3%. The stents were removed on average after 8 ± 2 weeks. The mean procedural time from puncture to stent deployment was 3.2 ± 2.4 minutes. In the imaging check-up, the collections had adequate drainage in all cases. There was a low frequency of complications; bleeding was documented in one case requiring surgery.
Conclusions:
LAMS is safe and effective in managing symptomatic pancreatic pseudocysts, reducing hospital stay and cost overruns. Clinical symptomatology prevails in the surgery decision.
Keywords (DeCS): Endoscopic ultrasound; interventional ultrasonography; gastrointestinal endoscopy; pancreatic pseudocyst; pancreatitis; apposing metal stents.
Introducción
Las colecciones pancreáticas son una complicación de la pancreatitis. Más de la mitad suelen resolverse espontáneamente y, a menudo, la decisión más acertada es un manejo expectante o conservador1,2. La clasificación actualizada de Atlanta3 describe que, en la fase tardía de la pancreatitis, después de más de 4 semanas, se desarrollan los pseudoquistes pancreáticos a partir de pancreatitis edematosa intersticial o necrosis amurallada resultante de pancreatitis necrosante. Los pseudoquistes sobreinfectados o sintomáticos requieren de manejo intervencionista y las modalidades terapéuticas actuales incluyen drenaje quirúrgico, endoscópico o percutáneo4.
En la última década se ha presentado un cambio de paradigma en el manejo de las colecciones pancreáticas secundarias a la pancreatitis y el drenaje guiado por ultrasonido endoscópico (USE) se ha convertido en la técnica de elección5,6. Recientemente, se han descrito sistemas de stents ecoguiados de nueva generación y con un mayor diámetro. Estos dispositivos permiten un drenaje preciso y efectivo de las colecciones y la realización de necrosectomías endoscópicas a través de estos stents7, denominados como stent metálico luminal de aposición (LAMS). Con su implementación se ha llegado a demostrar seguridad y efectividad para el drenaje transmural de colecciones pancreáticos por vía endoscópica, con mayor éxito terapéutico, menor estancia hospitalaria y reducción de costos generales en comparación con el drenaje quirúrgico o percutáneo8-10. A nivel local, Gómez y colaboradores11 describen el uso de stents metálicos convencionales en el drenaje de 10 colecciones pancreáticas, pero no hay estudios en el medio relacionados con la efectividad y seguridad con el uso del LAMS.
El propósito de este estudio fue evaluar la efectividad y la seguridad de LAMS de nuevo diseño para el drenaje guiado por USE en el tratamiento de los pseudoquistes pancreáticos sintomáticos en dos centros de referencia de Colombia.
Materiales y métodos
Diseño del estudio y extracción de datos
Se realizó un estudio de cohorte prospectivo multicéntrico con muestreo por conveniencia. Se incluyeron a 13 pacientes con diagnóstico de pseudoquistes pancreáticos sintomáticos atendidos entre los períodos de junio de 2019 y diciembre de 2021 en dos centros de referencia en gastroenterología en Bogotá, Colombia. La población de estudio la constituyeron adultos (18 años o mayores) que desarrollaron un cuadro de pseudoquistes pancreáticos sintomáticos definidos por presencia de dolor abdominal o patrón restrictivo gástrico (disconfort posprandial con sensación de llenura precoz), con más de 8 semanas de evolución desde la documentación de la pancreatitis. Los pacientes elegibles debían tener seguimiento clínico activo en cada institución del estudio. Se excluyeron a sujetos menores de 18 años, necrosis pancreática organizada (con un mínimo componente líquido), pseudoquistes infectados, inestabilidad hemodinámica, coagulopatía grave (índice internacional normalizado [INR] > 1,5 o recuento de plaquetas < 50 × 109/L), uso de anticoagulación/antiagregación que no se pueda suspender y la negativa a dar su consentimiento informado para participar en el estudio.
Recolección de datos
Como fuente de información primaria se usaron las historias clínicas y el reporte oficial del procedimiento realizado. Los pacientes se sometieron a drenaje guiado por USE, con un LAMS de nuevo diseño (Niti-S HOT SPAXUS; Taewoong Medical Co, Ltd, Ulsan, Corea del Sur) con diámetros de 16 mm y 10 mm, con una longitud de 20 mm, de acuerdo con la disponibilidad de existencias. Las variables de los desenlaces incluyeron el éxito técnico, el éxito clínico y la extracción exitosa del stent. Los pacientes fueron seguidos prospectivamente hasta el retiro del stent.
Definiciones
El éxito técnico se definió como la adecuada liberación y posicionamiento del stent en sus 2 extremos. El éxito clínico se definió como la disminución mayor del 50% de la colección a las 4 semanas determinada por imagen de control, ya sea por USE o por tomografía axial computarizada (TAC). Se consideró fracaso clínico como la persistencia de la colección o de los síntomas luego de haber completado 4 semanas de drenaje de la colección. Si el control por imágenes no mostraba un drenaje completo o esperado de la colección, se mantenía el stent por cuatro semanas adicionales y un nuevo control imagenológico en 3 a 6 meses con USE. No se utilizaron stents plásticos. El éxito en la extracción del stent se definió como la remoción de la prótesis en ausencia de complicaciones como el sangrado. El tiempo del procedimiento se definió como el tiempo transcurrido desde la punción hasta el despliegue del stent12,13. Las medidas de seguridad incluyeron eventos adversos relacionados con el stent (EA) y los eventos adversos generales (EAG).
Análisis estadístico
Se elaboró la base de datos en Excel versión 2019. Se completaron los datos faltantes con nuevas revisiones de las fuentes de información y se realizaron al final solo análisis de datos completos. El criterio principal de valoración del estudio fue el éxito clínico al momento de la extracción del stent. Este estudio de un solo brazo tuvo como objetivo confirmar su no inferioridad con base en una comparación del éxito clínico del stent Niti-S HOT SPAXUS con valores de referencia. El promedio ponderado calculado en estudios previos fue de alrededor del 96%, lo que se estableció como el éxito clínico esperado para este estudio.
El procesamiento de datos se realizó en el programa para ciencias sociales SPSS versión 25.0. Para el análisis descriptivo de las variables cuantitativas se utilizó el promedio aritmético, el mínimo y el máximo; mientras que para las variables cualitativas se utilizaron frecuencias absolutas y relativas.
Consideraciones éticas
Este estudio fue aprobado por los comités de ética e investigación de las respectivas instituciones en Bogotá, Colombia. Ambos son hospitales de tercer nivel de atención y centros de referencia en gastroenterología. En su diseño se tuvieron en cuenta los requerimientos establecidos en la Resolución 8430 de 1993 del Ministerio de Salud de Colombia, de manera que se consideró una investigación de bajo riesgo y se garantizó la confidencialidad y reserva de la información recolectada. Todos los pacientes fueron instruidos respecto a la intervención y firmaron el consentimiento informado. Ningún registro contenía información sensible sobre la identidad de los pacientes.
Resultados
Se intervinieron 13 pacientes (edad promedio de 53,4 años, 8 fueron hombres), cuyas características clínicas se resumen en Tabla 1. El tamaño medio del pseudoquiste fue de 9,56 ± 2,3 cm.
Tabla 1 Características demográficas, clínicas y procedimentales de los pacientes
| Características (n = 13) | |
|---|---|
| Edad, media (DE) | 53,4 (8,1) |
| Sexo | |
| - Masculino, n (%) | 8 (61,5) |
| - Femenino, n (%) | 5 (38,5) |
| Características del pseudoquiste | |
| - Tamaño, media (DE) | 9,6 (2,3) |
| - Drenaje a estómago, n (%) | 13 (100) |
| Características de los stents | |
| Diámetro del stent | |
| - 15 mm, n (%) | 11 (84,6) |
| - 10 mm, n (%) | 2 (15,4) |
| Procedimiento | |
| - Tiempo de retiro (semanas), media (DE) | 8 (2) |
| - Tiempo del procedimiento (minutos), media (DE) | 3,2 (2,4) |
| Desenlaces clínicos | |
| - Éxito técnico, n (%) | 13 (100) |
| - Éxito clínico, n (%) | 12 (92,3) |
DE: desviación estándar. n: número. Tabla elaborada por los autores.
Aspectos técnicos de la colocación
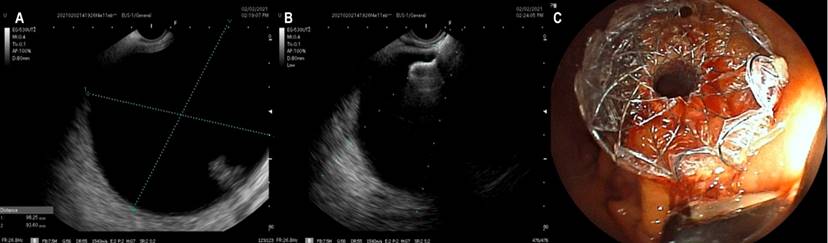
Los pacientes se realizaron con sedación asistida por anestesiología, en la que se empleó propofol, no se requirió anestesia general en ningún caso. Como profilaxis antibiótica se usó ciprofloxacina 400 mg IV (dosis única). Se usó un ecoendoscopio lineal Fujifilm EG-530UT2 con procesador de ultrasonido SONART SU-1 operado por un ecoendoscopista experto. Una vez evaluada la colección mediante USE (Figura 1A), se realizó una punción mediante una guía Doppler para comprobar la existencia de vasos interpuestos.
Todos los drenajes se realizaron al estómago. En solo 4 casos se utilizó aguja de punción 19 G y paso de guía de 0,035 bajo visión ecoendoscópica para tener mayor seguridad de no perder el trayecto; sin embargo, en los siguientes casos no se usó aguja ni guía, teniendo en cuenta una mejor familiarización con el nuevo stent y su facilidad de uso, además de una buena ventana ecográfica (Figura 1B) y tamaño mayor de 6 cm de diámetro de los pseudoquistes. En todos los casos se utilizó una unidad electroquirúrgica ERBE VIO 200 s en modo de corte puro a 200 W efecto 6. No realizamos cultivo de las muestras obtenidas. En ningún caso se documentó absceso o áreas de necrosis amurallada. Es muy importante tener en cuenta que no se usó fluoroscopia, por lo que no hubo necesidad adicional de emplear medios de contraste.
En ninguno de los casos usamos balones de dilatación. La expansión radial de estos dispositivos es adecuada y consideramos que no es necesaria para mejorar los desenlaces (Figura 1C). El diámetro más empleado fue de 15 mm (11 pacientes) y 10 mm en (2 pacientes). La decisión de usar estos calibres fue por la disponibilidad en las instituciones de estos diámetros en el momento respectivo.
Desenlaces clínicos
El éxito técnico fue del 100% (13/13) y el éxito clínico fue del 92,3% (12/13). El único caso sin éxito clínico correspondió a un paciente que presentó sangrado a las 48 horas del procedimiento por ruptura de un pseudoaneurisma de la arteria esplénica al colapsar la cavidad, que requirió intervención quirúrgica con buena evolución. Todos los stents fueron retirados con éxito usando la pinza de cuerpo extraño, en promedio a las 8 ± 2 semanas. El tiempo medio del procedimiento desde la punción hasta el despliegue del stent fue de 3,2 ± 2,4 minutos (Tabla 1). El control imagenológico (TAC, resonancia magnética [RM] o ecoendoscopia) a las 8 semanas permitió apreciar un adecuado drenaje de las colecciones (mayor del 80%) en todos los casos. No se observaron diferencias entre los diámetros empleados de los stents, posiblemente por tratarse solo de pseudoquistes sin presencia de áreas de necrosis o un mayor componente de detrito asociado.
Perfil de seguridad
En cuanto a las complicaciones, en un caso se documentó sangrado a las 48 horas de la colocación del stent, sin requerimiento transfusional, con la necesidad de intervención quirúrgica por ruptura de pseudoaneurisma de la arteria esplénica al colapsarse la cavidad del pseudoquiste, y su evolución fue satisfactoria.
Discusión
La técnica del drenaje endoscópico de los pseudoquistes pancreáticos ha evolucionado en los últimos años. Anteriormente se utilizaban múltiples stents plásticos para drenar los pseudoquistes pancreáticos, que se asociaban a migración, diámetros menores y requerimientos de múltiples accesos, lo que llevó a la búsqueda de otras alternativas, como los stents metálicos, para lograr un drenaje eficiente2. La implementación del USE como guía de punción también permite definir las características de la colección pancreática, particularmente en aquellos casos de ausencia de compresión a órganos vecinos, porque identifica la vasculatura vecina lesionable y descarta neoplasias14, lo que se asocia a una mayor seguridad y disminución de las complicaciones10. En este estudio se evidencia que el drenaje guiado por USE usando LAMS (Niti-S HOT SPAXUS; Taewoong Medical Co, Ltd, Ulsan, Corea del Sur) es una gran alternativa, debido a que disminuye las comorbilidades observadas con otras técnicas de drenaje anteriormente empleadas.
En nuestro estudio se encontró una tasa porcentual de un éxito técnico del 100% (13/13), que es consistente con lo descrito en la literatura15-17, y es probable que se relacione con la función de la experiencia del operador. También se encontró un éxito clínico del 92,3%, lo cual sugiere que a pesar de que todos los pacientes incluidos en el estudio fueron sintomáticos y de que se realizó la adecuada liberación y posicionamiento del stent (12/13), un bajo porcentaje de los casos (7,7%) no logró una disminución mayor del 50% de la colección a las 4 semanas, lo que podría afectar la práctica clínica en un futuro, ya que la sintomatología prima sobre los hallazgos radiológicos. Estos hallazgos están de acuerdo con las recomendaciones de la clasificación revisada de Atlanta3: la intervención clínica inicial para una colección pancreática debe guiarse por la sintomatología clínica y no por el tamaño del quiste. Igualmente, la sintomatología clínica debe guiar a los endoscopistas para futuras intervenciones después de la colocación del stent.
Actualmente, el drenaje endoscópico del pseudoquiste pancreático es la opción preferida en muchos centros de referencia, con reportes de éxito superiores al 93% y morbilidad inferior al 10%, sin mortalidad10,17. El drenaje por USE se asocia a un aumento del éxito técnico y disminución de la incidencia de complicaciones4. Este estudio demostró éxito técnico en el 100% (13/13) de pacientes, con pocas complicaciones relacionadas al procedimiento (1/13 pacientes) y resolución del cuadro superior al 90% (el éxito clínico fue del 92,3%); esto evidencia que el drenaje guiado por USE usando LAMS (Niti-S HOT SPAXUS; Taewoong Medical Co, Ltd, Ulsan, Corea del Sur) con diámetros de 16 mm y 10 mm y con una longitud de 20 mm es una alternativa para ser tenida en cuenta, pues es técnicamente factible y efectiva para el tratamiento de pseudoquistes pancreáticos sintomáticos, acompañada de pocas complicaciones al ser usado en nuestro medio.
En este estudio se encontró una menor estancia hospitalaria y ausencia de reintervenciones. Estos hallazgos concuerdan con las ventajas documentadas a partir de un estudio de cohortes retrospectiva por Akshintala y colaboradores18, en el que se comparó el drenaje percutáneo con el endoscópico y se encontró que los pacientes sometidos a drenaje endoscópico tuvieron menores reintervenciones (9,8% frente a 42,5%; p = 0,001), menor duración de la estancia hospitalaria (6,5 ± 6,7 días frente a 14,8 ± 14,4 días; p = 0,001) y menor cantidad promedio de imágenes de seguimiento (4 [2,5-6] frente a 6 [3,25-10]; p = 0,02). A pesar de que en el presente estudio no se pudo evaluar una posible disminución en la cantidad promedio de requerimiento de imágenes de seguimiento, ni tiempos de estancia hospitalaria o sobrecostos por complicaciones asociadas a la patología, los resultados observados en los casos son alentadores ante la baja frecuencia de complicaciones y de reintervención.
En el caso particular del paciente sin éxito clínico, el mecanismo del stent no falló sino que presentó sangrado por la arteria esplénica, por lo cual hubo éxito técnico; sin embargo, presentó sangrado a las 24 horas que requirió un control endoscópico de revisión sin poder lograr un control hemostático adecuado y ante la sospecha de lesión de vasos esplénicos fue llevado a manejo quirúrgico, en el que se encontró la etiología del sangrado a nivel de la pared gástrica, por lo que se procedió a retirar el stent, y realizar una ulterior gastrorrafia y marsupialización. El sangrado es una complicación previamente descrita en la literatura; a partir del estudio de Siddiqui y colaboradores19 se encontró que el uso de LAMS aumentaba las probabilidades de sangrado probablemente porque los rebordes son amplios y puede llevar a una erosión del stent en un vaso cuando la pared de la cavidad colapsa. Particularmente en estos casos el sangrado puede representar una complicación seria porque en muchas ocasiones los grandes vasos atraviesan los quistes y el sangrado ocurrirá en la cavidad del pseudoquiste, seguido de derrame de sangre retro- o intraperitoneal. Al compararse con los stents plásticos para el drenaje de colecciones pancreáticas, los pacientes tratados con LAMS presentan mayores cifras de sangrado20, por lo que estos procedimientos deben ser realizados en centros de referencia por personal experto en intervencionismo endoscópico y donde se cuente con el apoyo de cirugía hepatobiliar y radiología intervencionista21. En el caso ocurrido durante el estudio, la intervención quirúrgica precoz permitió una evolución adecuada sin complicaciones posoperatorias y posibilitó el alta oportuna. También es necesario mencionar el tiempo de retiro del stent: lo ideal es hacerlo a las 4 semanas y no a las 8 semanas, como ocurrió en los casos descritos22; sin embargo, pueden ocurrir barreras administrativas por parte de las aseguradoras en salud, que impiden el acceso oportuno y dificultan el cumplimiento de estos tiempos pactados. A pesar de los tiempos que se realizaron en los casos descritos, no se encontraron complicaciones asociadas.
La elección del tratamiento de los pseudoquistes pancreáticos seguirá siendo un tema controversial desde distintos puntos de vista, entre los cuales está el abordaje, que incluye observación, drenaje endoscópico guiado o no por USE, drenaje percutáneo e intervenciones quirúrgicas; y si es por vía endoscópica, incluye el requerimiento o no de stent, uso de stents plásticos o metálicos, y la forma del drenaje. En estos últimos aspectos, la evidencia ha mostrado resultados diversos en relación con características heterogéneas en los estudios. Por un lado, en el estudio de Bang y colaboradores23 se comparó el LAMS con stents plásticos para necrosis pancreática amurallada y no se observaron diferencias significativas en la cantidad de procedimientos realizados, el éxito del tratamiento, los acontecimientos clínicos adversos, los reingresos, la estancia y los costos globales del tratamiento; por otro lado, en un metaanálisis reciente, el éxito técnico, éxito clínico y eventos adversos de LAMS para colecciones pancreáticas (tanto necrosis pancreática amurallada como pseudoquistes pancreáticos) fueron del 96,2% (IC 95%: 94,6-97,4), 86,8% (IC 95%: 83,1-89,8) y 20,7% (IC 95%: 16,1-26,1), respectivamente24. Recientemente, en un reporte de caso se mostró la cistogastrostomía endoscópica guiada o no con ecoendoscopia y LAMS como una opción terapéutica viable, segura, efectiva y económica en un caso de pseudoquiste pancreático gigante25. Todos estos son hallazgos de interés y se relacionan con características propias del paciente, de la colección y del abordaje, por lo que ameritan de estudios de mayor tamaño y seguimiento, en los que se delimiten las características a considerar.
Existen algunas limitaciones del estudio. En primer lugar, se trata de un estudio retrospectivo y con una cantidad pequeña de pacientes, pues es una serie limitada de 13 pacientes consecutivos que se sometieron a colocación de LAMS en dos instituciones. Además, el muestreo por conveniencia condiciona una alta posibilidad de sesgo. Se debe mencionar que solo se realizaron estadísticas descriptivas para expresar nuestra experiencia sobre LAMS e hizo falta poder proporcionar un análisis estadístico sobre el beneficio clínico. Otra limitación es que no se pudo comparar con otros tipos de stents. El objetivo de este estudio fue demostrar la experiencia inicial en dos centros de referencia a nivel local con la descripción de la viabilidad técnica y el éxito clínico. Este estudio es concordante con otros estudios de LAMS16,26-28 acerca de su seguridad y eficacia en el manejo de pseudoquistes pancreáticos. Debido a los resultados satisfactorios, se continúa utilizando LAMS en el manejo de este tipo de pacientes. Por último, hay que mencionar que en el presente estudio no se establecieron periodos definidos para el seguimiento, por lo que no se pudieron caracterizar desenlaces de interés en periodos mayores de 8 semanas.
Entre las cuestiones específicas que es importante abordar en futuras investigaciones se encuentran: ¿cuál es la duración adecuada/segura entre la colocación y la retirada de los LAMS?, ¿cuáles son los intervalos ideales de seguimiento radiológico y endoscópico para reducir el riesgo de migración de la endoprótesis y de enterramiento de las mismas? y ¿ el uso de endoprótesis plásticas colocadas a través de una LAMS tiene algún efecto sobre el riesgo de migración, oclusión u otras complicaciones? La aplicación sistemática de protocolos desarrollados y perfeccionados deliberadamente debería contribuir a reducir las complicaciones de los LAMS, así como debería permitir una aplicación más segura de estos importantes dispositivos a medida que su uso clínico se amplíe con el tiempo.
Conclusiones
En conclusión, en el presente estudio observacional se demuestra que, en nuestro medio, el uso de LAMS es seguro y efectivo en el manejo de los pseudoquistes pancreáticos sintomáticos, y tiene una baja frecuencia de complicaciones. La decisión de intervención debe basarse netamente en la clínica por personal experto y en un centro que cuente con apoyo de cirugía y radiología intervencionista, entre otros.
REFERENCIAS
1. Law RJ, Chandrasekhara V, Bhatt A, Bucobo JC, Copland AP, Krishnan K, et al. Lumen-apposing metal stents (with videos). Gastrointest Endosc. 2021;94(3):457-70. https://doi.org/10.1016/j.gie.2021.05.020 [ Links ]
2. Giovannini M. Endoscopic Ultrasonography-Guided Pancreatic Drainage. Gastrointest Endosc Clin N Am. 2012;22(2):221-30. https://doi.org/10.1016/j.giec.2012.04.004 [ Links ]
3. Banks PA, Bollen TL, Dervenis C, Gooszen HG, Johnson CD, Sarr MG, et al. Classification of acute pancreatitis - 2012: Revision of the Atlanta classification and definitions by international consensus. Gut. 2013;62(1):102-11. https://doi.org/10.1136/gutjnl-2012-302779 [ Links ]
4. Chaves D, Mönkemüller K, Carneiro F, Medrado B, dos Santos M, Wodak S, et al. Endoscopic treatment of large pancreatic fluid collections (PFC) using self-expanding metallic stents (SEMS) - a two-center experience. Endosc Int Open. 2014;2(4):E224-9. https://doi.org/10.1055/s-0034-1390796 [ Links ]
5. Kahaleh M, Shami VM, Conaway MR, Tokar J, Rockoff T, De La Rue SA, et al. Endoscopic ultrasound drainage of pancreatic pseudocyst: A prospective comparison with conventional endoscopic drainage. Endoscopy. 2006;38(4):355-9. https://doi.org/10.1055/s-2006-925249 [ Links ]
6. Varadarajulu S, Christein JD, Tamhane A, Drelichman ER, Wilcox CM. Prospective randomized trial comparing EUS and EGD for transmural drainage of pancreatic pseudocysts (with videos). Gastrointest Endosc. 2008;68(6):1102-11. https://doi.org/10.1016/j.gie.2008.04.028 [ Links ]
7. Wrobel PS, Kaplan J, Siddiqui AA. A new lumen-apposing metal stent for endoscopic transluminal drainage of peripancreatic fluid collections. Endosc Ultrasound. 2014;3(4):203-4. https://doi.org/10.4103/2303-9027.144508 [ Links ]
8. Hao S-J, Xu W-J, Di Y, Yao L, He H, Yang F, et al. Novel and supplementary management of pancreatic fluid collections: Endoscopic ultrasound-guided drainage. World J Gastrointest Endosc. 2017;9(9):486-93. https://doi.org/10.4253/wjge.v9.i9.486 [ Links ]
9. Mangiavillano B, Pagano N, Baron TH, Arena M, Iabichino G, Consolo P, et al. Biliary and pancreatic stenting: Devices and insertion techniques in therapeutic endoscopic retrograde cholangiopancreatography and endoscopic ultrasonography. World J Gastrointest Endosc. 2016;8(3):143-56. https://doi.org/10.4253/wjge.v8.i3.143 [ Links ]
10. Siddiqui AA, Adler DG, Nieto J, Shah JN, Binmoeller KF, Kane S, et al. EUS-guided drainage of peripancreatic fluid collections and necrosis by using a novel lumen-apposing stent: A large retrospective, multicenter U.S. experience (with videos). Gastrointest Endosc. 2016;83(4):699-707. https://doi.org/10.1016/j.gie.2015.10.020 [ Links ]
11. Gómez Zuleta MA, Mindiola AL, Morales ÓFR. Case series of drainage of pancreatic pseudocysts guided by echoendoscopy without fluoroscopy. Rev Colomb Gastroenterol. 2017;32(2):160-5. https://doi.org/10.22516/25007440.143 [ Links ]
12. Johnson MD, Walsh RM, Henderson JM, Brown N, Ponsky J, Dumot J, et al. Surgical versus nonsurgical management of pancreatic pseudocysts. J Clin Gastroenterol. 2009;43(6):586-90. https://doi.org/10.1097/MCG.0b013e31817440be [ Links ]
13. Melman L, Azar R, Beddow K, Brunt LM, Halpin VJ, Eagon JC, et al. Primary and overall success rates for clinical outcomes after laparoscopic, endoscopic, and open pancreatic cystgastrostomy for pancreatic pseudocysts. Surg Endosc. 2009;23(2):267-71. https://doi.org/10.1007/s00464-008-0196-2 [ Links ]
14. Varadarajulu S, Christein JD, Wilcox CM. Frequency of complications during EUS-guided drainage of pancreatic fluid collections in 148 consecutive patients. J Gastroenterol Hepatol. 2011;26:1504-8. https://doi.org/10.1111/j.1440-1746.2011.06771.x [ Links ]
15. Patil R, Ona MA, Papafragkakis C, Anand S, Duddempudi S. Endoscopic ultrasound-guided placement of axios stent for drainage of pancreatic fluid collections. Ann Gastroenterol. 2016;29(2):168-73. https://doi.org/10.20524/aog.2016.0008 [ Links ]
16. Yoo J, Yan L, Hasan R, Somalya S, Nieto J, Siddiqui AA. Feasibility, safety, and outcomes of a single-step endoscopic ultrasonography-guided drainage of pancreatic fluid collections without fluoroscopy using a novel electrocautery-enhanced lumen-apposing, self-expanding metal stent. Endosc Ultrasound. 2017;6(2):131-5. https://doi.org/10.4103/2303-9027.204814 [ Links ]
17. Shah RJ, Shah JN, Waxman I, Kowalski TE, Sanchez-Yague A, Nieto J, et al. Safety and Efficacy of Endoscopic Ultrasound-Guided Drainage of Pancreatic Fluid Collections With Lumen-Apposing Covered Self-Expanding Metal Stents. Clin Gastroenterol Hepatol. 2015;13:747-52. https://doi.org/10.1016/j.cgh.2014.09.047 [ Links ]
18. Akshintala VS, Saxena P, Zaheer A, Rana U, Hutfless SM, Lennon AM, et al. A comparative evaluation of outcomes of endoscopic versus percutaneous drainage for symptomatic pancreatic pseudocysts. Gastrointest Endosc. 2014;79(6):921-8. https://doi.org/10.1016/j.gie.2013.10.032 [ Links ]
19. Siddiqui AA, Kowalski TE, Loren DE, Khalid A, Soomro A, Mazhar SM, et al. Fully covered self-expanding metal stents versus lumen-apposing fully covered self-expanding metal stent versus plastic stents for endoscopic drainage of pancreatic walled-off necrosis: clinical outcomes and success. Gastrointest Endosc. 2017;85(4):758-65. https://doi.org/10.1016/j.gie.2016.08.014 [ Links ]
20. Lang GD, Fritz C, Bhat T, Das KK, Murad FM, Early DS, et al. EUS-guided drainage of peripancreatic fluid collections with lumen-apposing metal stents and plastic double-pigtail stents: comparison of efficacy and adverse event rates. Gastrointest Endosc. 2018;87(1):150-7. https://doi.org/10.1016/j.gie.2017.06.029 [ Links ]
21. Umapathy C, Gajendran M, Mann R, Boregowda U, Theethira T, Elhanafi S, et al. Pancreatic fluid collections: Clinical manifestations, diagnostic evaluation and management. Dis Mon. 2020;66(11):100986. https://doi.org/10.1016/j.disamonth.2020.100986 [ Links ]
22. Nayar M, Leeds JS, Oppong K. Lumen-apposing metal stents for drainage of pancreatic fluid collections: does timing of removal matter? Gut . 2022;71(5):850-3. https://doi.org/10.1136/gutjnl-2021-325812 [ Links ]
23. Bang JY, Navaneethan U, Hasan MK, Sutton B, Hawes R, Varadarajulu S. Non-superiority of lumen-apposing metal stents over plastic stents for drainage of walled-off necrosis in a randomised trial. Gut . 2019;68(7):1200-9. https://doi.org/10.1136/gutjnl-2017-315335 [ Links ]
24. Tan S, Zhong C, Ren Y, Luo X, Xu J, Peng Y, et al. Are Lumen-Apposing Metal Stents More Effective Than Plastic Stents for the Management of Pancreatic Fluid Collections: An Updated Systematic Review and Meta-analysis. Gastroenterol Res Pract. 2020;2020:4952721. https://doi.org/10.1155/2020/4952721 [ Links ]
25. Barreto Noratto CP, Limas Solano LM. Drenaje de pseudoquiste pancreático gigante mediante cistogastrostomía endoscópica: reporte de caso. Rev Colomb Gastroenterol. 2022;37(2):210-3. https://doi.org/10.22516/25007440.734 [ Links ]
26. Sharaiha RZ, Tyberg A, Khashab MA, Kumta NA, Karia K, Nieto J, et al. Endoscopic Therapy With Lumen-apposing Metal Stents Is Safe and Effective for Patients With Pancreatic Walled-off Necrosis. Clin Gastroenterol Hepatol. 2016;14(12):1797-803. https://doi.org/10.1016/j.cgh.2016.05.011 [ Links ]
27. Whitworth PW, Holbert BL, Pawa R, Lalwani N, Tappouni R. The LACSEMS: what radiologists need to know. Abdom Radiol. 2019;44(3):976-83. https://doi.org/10.1007/s00261-019-01904-9 [ Links ]
28. Schawkat K, Luo M, Lee K, Beker K, Meir M, Berzin TM, et al. Lumen-apposing covered self-expanding metallic stent for symptomatic pancreatic fluid collections: assessment of outcomes and complications with CT and MRI. Abdom Radiol. 2021;46(2):757-67. https://doi.org/10.1007/s00261-020-02638-9 [ Links ]
Citación: Flórez-Sarmiento C, Parra-Izquierdo V, Frías-Ordoñez JS, Castillo JD, Rodríguez S. Drenaje de pseudoquistes pancreáticos con stent metálico luminal de aposición (LAMS): experiencia en dos centros de referencia en Colombia. Revista. colomb. Gastroenterol. 2023;38(3):256-263. https://doi.org/10.22516/25007440.948
Aprobación ética y consentimiento de participación Esta investigación fue revisada y aprobada por el comité de ética en investigación de cada institución participante
Consentimiento para la publicación Se tuvieron en cuenta los requerimientos establecidos en la Resolución 8430 de 1993 del Ministerio de Salud de la República de Colombia, de manera que se consideró una investigación de bajo riesgo y se garantizó confidencialidad y reserva de la información recolectada. Todos los pacientes fueron informados y firmaron el consentimiento informado. Ningún registro contenía información sensible sobre la identidad de los pacientes.
Disponibilidad de datos y material Los datos y el material disponibles para la publicación están en el manuscrito y no se omitió ninguna información
Recibido: 27 de Julio de 2022; Aprobado: 02 de Marzo de 2023











 text in
text in