INTRODUCCIÓN
El cáncer de cuello uterino es el cuarto cáncer con mayor incidencia en mujeres a nivel mundial, y es la segunda causa de muerte por cáncer en mujeres cuya edad oscila entre 15 y 44 años 1. Entre los factores de riesgo para este cáncer está el virus del papiloma humano; se ha descrito que los serotipos 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 y 68 están fuertemente asociados con NIC y cáncer invasor 2.
El cáncer de cuello uterino viene precedido por estadios preinvasores que persisten entre 10 a 20 años, lo que brinda oportunidades para su tamización, diagnóstico precoz y tratamiento oportuno 3. Es un hecho que la tamización del cáncer de cuello uterino con citología ha reducido sustancialmente la incidencia y la mortalidad de este tipo de cáncer en países desarrollados, a pesar de que su sensibilidad para detectar NIC2+ se sitúa alrededor del 66 % 4. Sin embargo, recientes avances han ocasionado un cambio de paradigma en la prevención del cáncer cervical con el uso de la prueba del ADN de VPH como método de tamización primaria en cuanto a la disminución de la incidencia de lesiones preneoplásicas y cáncer. Un metaanálisis de cuatro ensayos controlados aleatorizados informa que la tamización primaria con prueba de VPH aporta un 60 a 70 % de mayor protección que la tamización basada en citología en la prevención del cáncer invasor del cérvix 5.
Respecto a la edad en que se debería iniciar la tamización con la prueba VPH, una evaluación de tecnologías sanitarias hecha en Inglaterra en el 2014 concluyó que la tamización primaria con ADN de VPH a partir de los 25 años es más efectiva, ahorra costos y años de vida comparada con la tamización primaria con citología hasta los 30-35 años y la continuación con prueba de ADN de VPH 6. En el 2019 en los Estados Unidos de América se propone iniciar la tamización con prueba de ADN de VPH a partir de los 25 años 7. En Colombia, a partir del 2014 se incorporó la tamización primaria con prueba de VPH desde los 30 y hasta los 65 años, cuando la prueba es positiva se hace triage con citología para remisión a colposcopia 8. Con base en esta evidencia, en Colombia se discute la conveniencia de iniciar la tamización con prueba de ADN de VPH a partir de los 25 años.
De este modo, el objetivo de esta evaluación de tecnologías sanitarias es analizar la evidencia disponible en torno a la seguridad, efectividad, costo-efectividad, valores y preferencias, dilemas éticos y aspectos relacionados con la implementación para el contexto colombiano de la prueba ADN-VPH como estrategia de tamización cervical en mujeres menores de 30 años.
MATERIALES Y MÉTODOS
Diseño: evaluación de tecnología sanitaria teniendo como base los lineamientos sugeridos por el manual metodológico del Instituto de Evaluación Tecnológica en Salud (IETS) 9.
Población: mujeres menores de 30 años. Para fines de esta evaluación de tecnología sanitaria, se excluyeron estudios con participantes con riesgo diferente al promedio, pacientes con diagnóstico actual o previo de lesión invasora del cérvix o en seguimiento de una lesión preneoplásica.
Intervención: prueba de ADN-VPH por captura híbrida o reacción de cadena de la polimerasa.
Comparación: citología convencional o en base líquida.
Dominios considerados:
Efectividad de la intervención (v.g. mortalidad específica por cáncer; incidencia de carcinoma invasor; proporción de pacientes con diagnóstico de NIC2+).
Seguridad: remisión a colposcopia.
Costo-efectividad para Colombia.
Del individuo o la sociedad: valores y preferencias de las mujeres menores de 30 años en torno a la tamización cervical.
Aspectos éticos asociados a la tamización cervical en mujeres menores de 30 años.
Organizacionales: barreras y facilitadores relacionados con la implementación en el contexto colombiano de la tamización cervical en mujeres menores de 30 años.
Tipos de estudios: se priorizó la inclusión de revisiones sistemáticas para responder cada pregunta formulada, recurriendo a estudios primarios solo cuando la pesquisa no recuperó una revisión sistemática, o en su defecto, cuando esta fue baja o críticamente baja acorde al instrumento AMSTAR-2 10. Se incluyeron ensayos clínicos controlados que compararan tamización primaria con ADN-VPH frente a citología convencional o en base líquida. Se excluyeron ensayos clínicos cuasi aleatorios, dado que producen estimaciones del efecto que indican beneficios mayores cuando se comparan con ensayos clínicos aleatorios, también se excluyeron ensayos clínicos de conglomerados o de diseño cruzado en virtud de la naturaleza de la condición y de la intervención. Para los estudios de preferencias, aspectos éticos y barreras se incluyeron estudios cualitativos primarios o secundarios, guías, evaluaciones de tecnología, entrevistas con expertos o con responsables de programas.
Contexto: instituciones de atención en salud de alta, mediana o baja complejidad. Siempre que fue factible se priorizaron estudios desarrollados en el territorio colombiano.
Métodos de búsqueda para la identificación de los estudios: la búsqueda de la literatura fue realizada con apoyo de un experto en exploración de la información en las siguientes bases de datos: MEDLINE, Embase y Central; no se restringió por fecha y la búsqueda se actualizó el 30 de enero de 2022; se identificaron los términos en lenguaje libre y controlado para cada uno de los componentes claves de las preguntas PICOT (población, intervención, comparación, desenlaces y tipo de estudio) 11 (Anexo 01 Material Suplementario: Bitácora de Búsqueda).
Cada estrategia se diseñó implementando el uso de operadores booleanos, conectores de proximidad, comodines y filtros altamente sensibles 11, búsqueda que fue validada por un experto clínico, sin restricción por tipo de idioma o fecha de publicación. Adicionalmente, con el ánimo de identificar estudios relevantes en curso o no publicados, la pesquisa se extendió a expertos en la materia, la búsqueda de investigaciones a partir del listado de referencias para los estudios incluidos y en los archivos de la Revista de Colombiana de Obstetricia y Ginecología.
Desarrollo de la evaluación de tecnología sanitaria: para dar alcance al objetivo propuesto, se conformó un grupo desarrollador el cual contó con el concurso de profesionales pertenecientes al área de medicina general, ginecología, patología del tracto genital inferior, ginecología oncológica, diseño de políticas, economía de la salud y bioética. Así mismo, participaron en este proceso profesionales en epidemiología clínica, salud pública y en búsqueda sistemática de la información. Todos los integrantes declararon por escrito sus conflictos de interés, los cuales se encuentran disponibles para revisión a solicitud del autor principal.
Una vez se conformó el grupo desarrollador, se discutieron los componentes de la pregunta clínica a contestar mediante un ejercicio no formal de priorización. Se estructuró la pregunta en formato PICOT, siguiendo los lineamientos de la guía metodológica para el desarrollo de IETS 9. El protocolo de la revisión sistemática se diseñó de acuerdo con las recomendaciones del Manual Cochrane 12 y la declaración PRISMA 13 y ante el comité de ética e investigación de la Facultad de Medicina de la Universidad Nacional de Colombia (Acta 023-221).
Selección de estudios y extracción de datos: el listado de referencias se depuró utilizando el programa EndNote, y luego de eliminar duplicados, las referencias a tamizar fueron revisadas por un experto clínico y un metodólogo, quienes independientemente realizaron la lectura de títulos, resúmenes y artículos en texto completo. Las discrepancias se resolvieron mediante consenso.
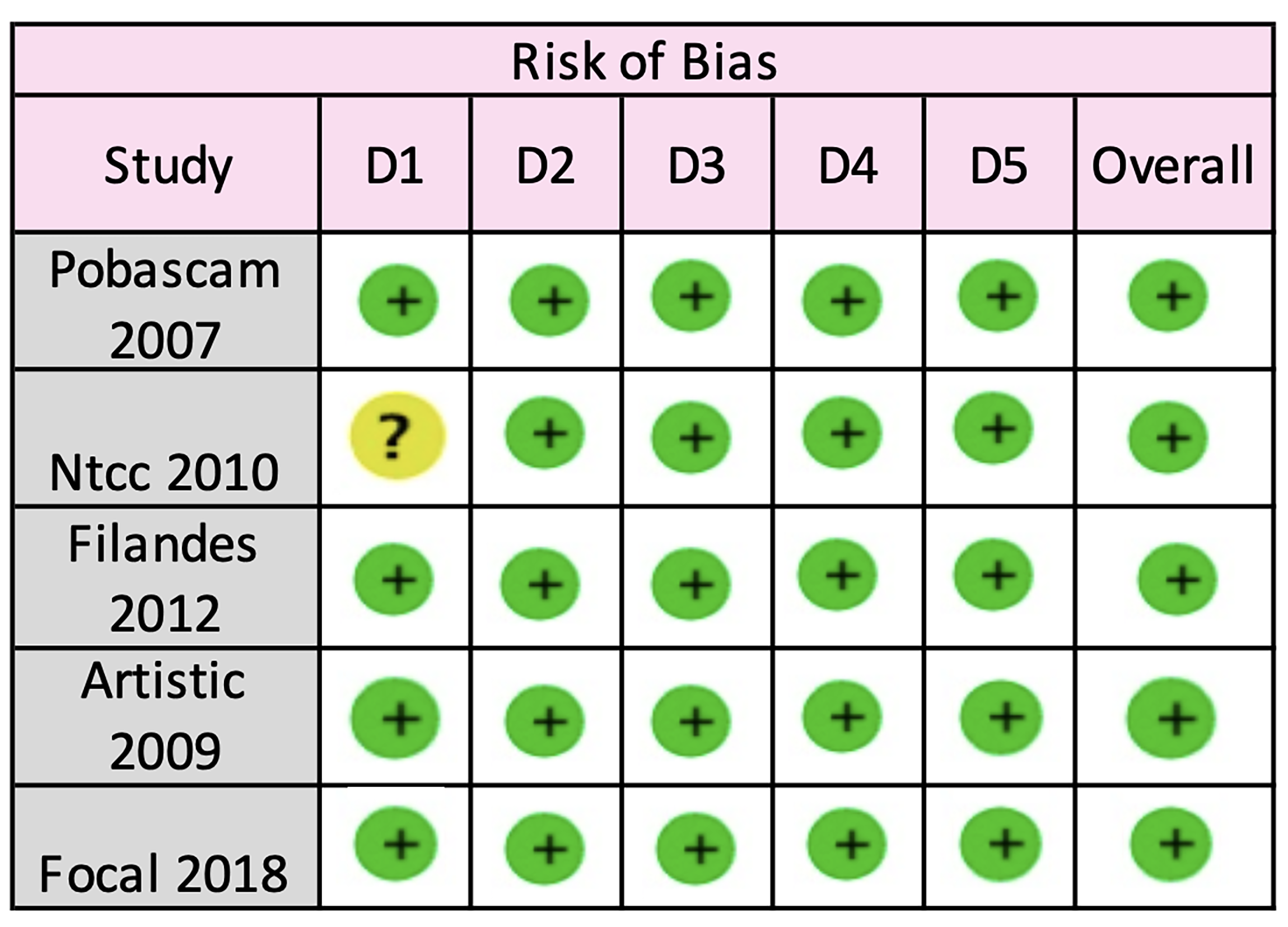
Valoración de calidad de los estudios incluidos: cuando se trató de estudios primarios, cuatro autores realizaron independientemente la evaluación de riesgo de sesgo, aplicando el instrumento Riesgo de Sesgos 2 (RoB2) 14 de Cochrane para los ensayos clínicos, la lista de verificación Consensus on Health Economic Criteria (CHEERS) 15 para los estudios económicos, y el instrumento sugerido por el Instituto Joanna Briggs para los estudios cualitativos 16. Las discrepancias se resolvieron mediante consenso o mediante consulta con un tercer autor.
Análisis y síntesis de resultados: para cada uno de los ensayos clínicos controlados incluidos, se recopiló la información relevante para esta evaluación de tecnología sanitaria en un formulario de recolección de datos diseñado para tal fin. Se digitó la información en el programa Review Manager 5 de forma pareada para verificar la calidad de los datos, se implementó como medida resumen de efecto la razón de oportunidades (OR) junto a sus respectivos intervalos de confianza (IC) del 95 % 12.
Además, se realizó, cuando fue posible, el análisis por intención de tratar, independientemente de si recibieron o no la intervención asignada. Además, se evaluó la heterogeneidad estadística en cada metaanálisis mediante el estadístico I2 y los valores de prueba Chi2, considerando heterogeneidad sustancial como la presencia de un estadístico I2 mayor del 40 % o la presencia de un valor de P en la prueba de hipótesis menor a 0,10 (prueba de heterogeneidad Chi2). Finalmente, se realizó la construcción de los diagramas de bosque utilizando el programa Review Manager 5, implementando la aproximación de efectos fijos para combinar los datos cuando fue razonable suponer que los estudios estimaban el mismo efecto subyacente del tratamiento (desde la perspectiva clínica y metodológica) 12.
Por el contrario, si el grupo clínico o metodológico o bien las pruebas estadísticas detectaron la presencia de heterogeneidad sustancial, se realizó metaanálisis de efectos aleatorios para producir un resumen general si el efecto promedio del tratamiento en todos los ensayos fue considerado clínicamente significativo 12. Si el efecto agrupado del tratamiento no fue clínicamente significativo o este fue producto de heterogeneidad sustancial, no se combinaron los estudios 12.
Se utilizó el programa GRADEpro (Universidad McMaster, ON, Canadá) para generar el respectivo perfil de evidencia 17, y se convocó a todos los integrantes del grupo desarrollador a una mesa de trabajo en donde se presentó la evidencia recuperada para cada uno de los aspectos mencionados, dando paso a la discusión y a la construcción de las conclusiones siguiendo los lineamientos de un consenso formal acorde a la metodología RAND/ UCLA 18, sopesando a lo largo de la deliberación los beneficios, los efectos adversos, los valores y preferencias de las pacientes, los aspectos éticos, las potenciales barreras y facilitadores y, finalmente, el potencial impacto de las intervención sobre los costos. Los resultados se presentan de manera narrativa.
RESULTADOS
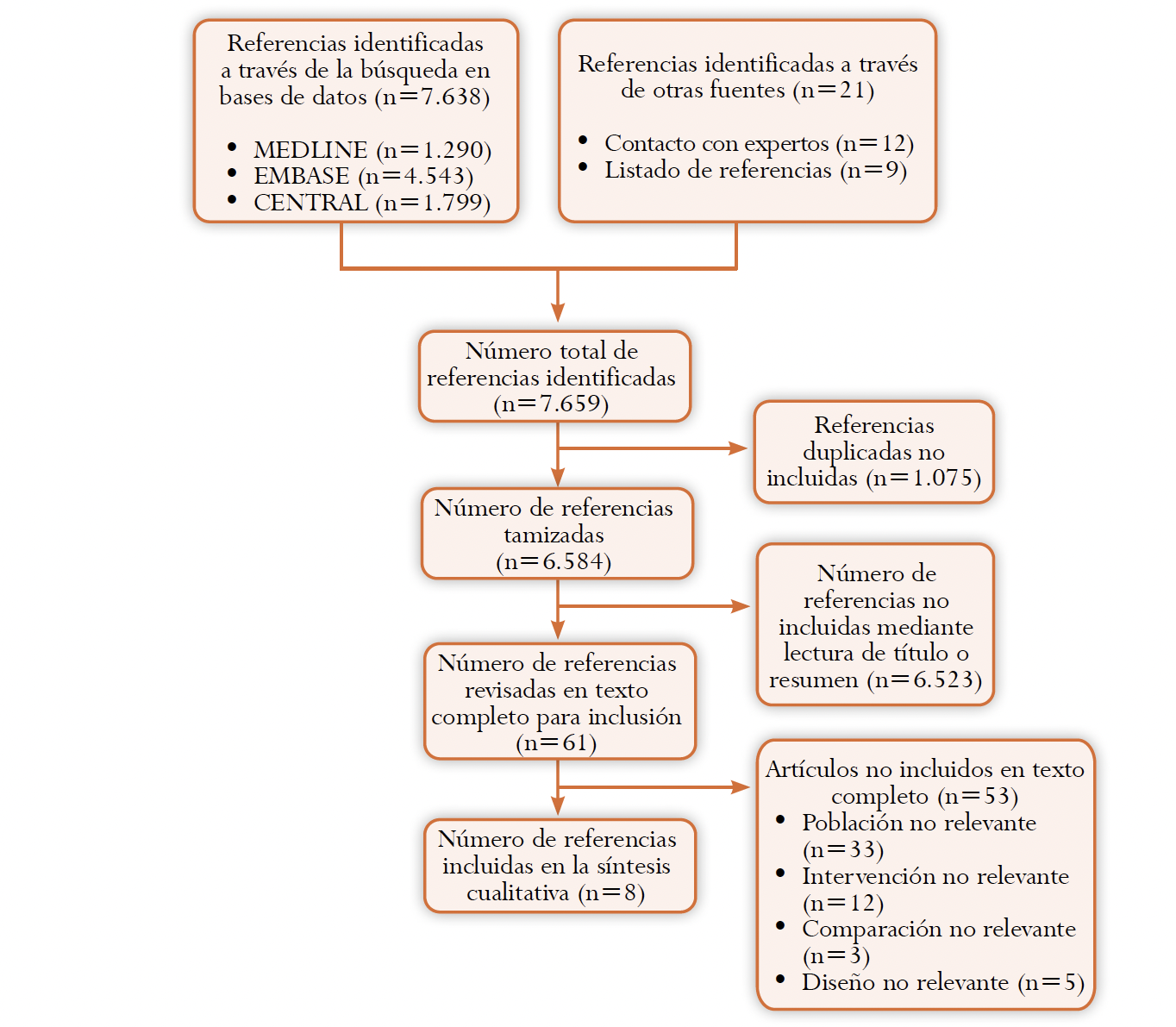
Se recuperaron 7.659 referencias, de las cuales se eliminaron 1.075 duplicadas, quedaron 6.584 títulos. De estos se descartaron 6.523 después de la lectura del título y resumen por no cumplir con los criterios de inclusión. Se examinó el texto completo de 61 documentos de los cuales ocho cumplieron con los criterios de inclusión y exclusión (Figura 1).
Se incluyeron cinco ensayos clínicos controlados que evaluaron el efecto de la intervención 19-23; un estudio de costo-efectividad 24, una revisión sistemática cualitativa que analizó la información relacionada en torno a los aspectos éticos, los valores y las preferencias para la población de interés 25, y otro de barreras y facilitadores de la prueba ADN-VPH para el contexto colombiano en mujeres menores de 30 años 26. A continuación, se presenta una síntesis de la evidencia para cada uno de los aspectos considerados.
Evidencia clínica seguridad y efectividad prueba ADN-VPH como estrategia de cribado en mujeres menores de 30 años
La búsqueda no recuperó revisiones sistemáticas que abordaran el uso de ADN-VPH en mujeres menores de 30 años. No obstante, la pesquisa identificó cinco ensayos clínicos controlados que sí abordaron esta población de 25 años.
En cuanto al desenlace primario de mortalidad específica por cáncer o la frecuencia de eventos adversos serios, asociados a la tamización, ninguno de los estudios incluidos analizó estos resultados.
Estudio Pobascam
Este ensayo clínico controlado realizado en Holanda 19) comparó la efectividad y la seguridad de la citología convencional frente a la prueba de ADN-VPH como estrategia de tamización en mujeres de 29 a 56 años, no incluyó un grupo específico de 25 a 29 años, incluyó 40.105 participantes, y fue calificado como bajo riesgo de sesgos (Anexo 02 Material Suplementario: RoB2). Los autores informan que cuando se comparó frente a la citología convencional, el uso de la prueba ADN-VPH se asoció con una mayor detección de lesiones NIC2+ durante la primera ronda (RR: 1,25; IC 95 %: 1,04 a 1,49), sin diferencias para la segunda ronda de cribado (RR: 0,88; IC 95 %: 0,71 a 1,08). El uso de la prueba de ADN-VPH redujo la incidencia de carcinoma invasor al término del seguimiento (RR: 0,29; IC 95 %: 0,09 a 0,87). En cuanto a la seguridad se evidenció una mayor de remisión a colposcopia durante la primera (RR: 1,75; IC 95 %: 1,39 a 2,19) pero no durante la segunda ronda (RR: 0,61; IC 95 %: 0,51 a 0,88).
Estudio NTCC
Ensayo clínico controlado realizado en Italia 20 analizó la efectividad y la seguridad de la prueba ADN-VPH frente al uso de citología en base líquida para la detección de lesiones preneoplásicas del cérvix en mujeres de 25 a 60 años. El estudio incluyó 94.370 participantes; el RoB2 fue calificado como de bajo riesgo. Cuando se comparó frente a la citología en base líquida, el uso de la tamización cervical con ADN-VPH se asoció con una mayor detección de lesiones NIC2+ durante la primera ronda (RR: 2,43, IC 95 %: 2,03 a 2,91) y con una menor incidencia de lesiones NIC2+ (RR: 0,55; IC 95 %: 0,36 a 0,83) y de carcinoma invasor durante al término del seguimiento (RR: 0,39; IC 95 %: 0,16 a 0,92). Este estudio documentó una mayor tasa de detección de NIC2+ durante la primera ronda de cribado, tanto en el grupo de 25 a 29 años (RR: 3,46; IC 95 %: 2,23 a 5,38) como en el de 30 a 34 años (RR: 2,74; IC 95 %: 1,88 a 3,98). Efecto que qué también se observó para carcinoma invasor al término de seguimiento (25 a 29 años RR: 2,35; IC 95 %: 1,63 a 3,37 y en mujeres de 30 a 34 años RR: 2,0; IC 95 %: 1,51 a 2,91). Respecto a la seguridad, el uso de la prueba de ADN-VPH incrementó la remisión a colposcopia durante la primera ronda (RR: 3,11; IC 95 %: 2,93 a 3,30) pero no al término del seguimiento (RR: 1,06; IC 95 %: 0,96 a 1,18).
Estudio Finlandés
Este ensayo clínico controlado 21 comparó la efectividad y la seguridad de la tamización cervical basada en ADN-VPH frente al uso de la citología convencional en mujeres de 25 a 65 años. Incluyó 132.194 participantes; el ROB2 fue calificado como de bajo riesgo. Cuando se comparó frente a la citología, la tamización cervical con ADN-VPH se asoció con una mayor frecuencia de detección de lesiones NIC2+ durante la primera ronda (OR: 1,68; IC 95 %: 1,46 a 1,92), efecto que se mantiene tanto en el grupo de 25 a 34 años (RR: 1,56; IC 95 %: 1,25 a 1,93) como en el grupo 35 o más años (RR: 1,53; IC 95 %: 1,25 a 1,87). El uso de ADN-VPH no se asoció con una mayor detección de carcinoma invasor (OR: 0,80; IC 95 %: 0,47 a 1,35). En cuanto a la seguridad no se observó diferencia en la remisión a colposcopia (OR: 1,04; IC 95 %: 0,95 a 1,15) durante la primera ronda de cribado. Este estudio no reportó rondas subsecuentes de cribado.
Estudio Artistic
Este ensayo clínico controlado hecho en el Reino Unido 22 comparó la efectividad y la seguridad de la tamización cervical basada en ADN-VPH frente a la implementación de la citología en base líquida. Este ensayo incluyó mujeres de 20 a 64 años (el grupo de 25 años se evaluó junto al de 30 a 34 años), quienes asistían rutinariamente al programa de detección cervical del servicio nacional de salud inglés. Ingresaron 24.510 participantes; el ROB2 fue calificado como bajo riesgo de sesgo. Cuando se comparó frente a la citología en base líquida, la tamización cervical con ADN-VPH no se asoció con una mayor frecuencia de detección de lesiones NIC2+ para la primera ronda (OR: 1,14; IC 95 %: 0,94 a 1,38) o para segunda ronda (OR: 0,83; IC 95 %: 0,56 a 1,23). No evaluó incidencia de cáncer invasor. Cuando se realizó análisis de subgrupos acorde a la edad de cribado, las mujeres de 20 a 34 años con resultado positivo en la prueba de ADN-VPH exhibieron una incidencia acumulada de NIC2+ del 23,9 % frente al 15,9 % en las mujeres de 35 a 49 años y de 6,4 % para mayores de 50 años. Respecto a la seguridad se informó un incremento aparente en la frecuencia de remisión a colposcopia durante la primera ronda de cribado (OR: 1,32; IC 95 %: 1,16 a 1,50).
Estudio Focal
El último ensayo clínico controlado desarrollado en Canadá 23 comparó la efectividad de la prueba ADN-VPH como estrategia de cribado frente al uso de la citología en base líquida para el diagnóstico de lesiones preneoplásicas en mujeres de 25 a 65 años. Ingresaron 9.009 participantes, el ROB2 fue calificado como de bajo riesgo de sesgo. Cuando se comparó frente al uso de la citología en base líquida, el cribado con ADN-VPH se asoció con una mayor detección de NIC2+ durante la primera ronda (RR: 1,61; IC 95 %: 1,24 a 2,09) y con una menor incidencia de lesiones NIC2+ (RR: 0,47; IC 95 %: 0,34 a 0,67) en la segunda ronda, sin que el análisis de subgrupos sugiera que el efecto de la intervención se modifique cuando se compara acorde a la edad de tamización (25 a 29 años RR: 0,52; IC 95 %: 0,27 a 0,98 y en el grupo de 30 años o más RR: 0,46; IC 95 %: 0,31 a 0,69). No se evaluó incidencia de cáncer invasor. Se reportó que el uso de la prueba de ADN-VPH incrementa la frecuencia de remisión a colposcopia durante la primera (RR: 1,85; IC 95 %: 1,61 a 2,13) pero no durante la segunda ronda (RR: 0,69; IC 95 %: 0,62 a 0,78).
Metaanálisis de todos los ensayos clínicos recuperados
El grupo desarrollador realizó un análisis integrativo de los ensayos clínicos aleatorizados recuperados. Se observa que cuando se compara frente a la citología convencional o en base líquida, la tamización primaria con ADN-VPH en mujeres menores de 30 años:
Hay posiblemente mayor frecuencia detección de lesiones NIC2+ durante la primera ronda de cribado (RR: 1,57; IC: 1,20 a 2,04; I2: 90 %; 5 estudios 310.127 participantes). Certeza en la evidencia baja (evidencia indirecta, alta heterogeneidad).
Hay posiblemente menor incidencia de NIC2+ al término del seguimiento (RR: 0,67; IC: 0,48 a 0,92; I2: 70 %; 4 estudios 166.804 participantes). Certeza en la evidencia baja (evidencia indirecta, alta heterogeneidad).
Hay menor incidencia de carcinoma invasor (RR: 0,19; IC: 0,07 a 0,53; I2: 22 %; 2 estudios 132.066 participantes) al término del seguimiento. Certeza en la evidencia alta (evidencia indirecta).
Seguridad:
d. Hay incertidumbre sobre una mayor remision a colposcopia durante la primera ronda de cribado (RR: 1,73; IC: 1,01 a 2,96; I2: 98 %; 5 estudios 287.177 participantes) y al término del seguimiento (RR: 0,79; IC 95 %: 0,56 a 1,12; I2: 94 %; 3 estudios 125.429 participantes). Certeza en la evidencia muy baja (evidencia indirecta, alta heterogeneidad). (Ver Anexo 03 Material Suplementario: Tabla SoF).
Evidencia costo-efectividad estrategias de tamización cervical en mujeres menores de 30 años
Un estudio de costo-efectividad desarrollado en la guía de manejo de cáncer invasor en Colombia 24 analizó las diferentes alternativas de tamización cervical en mujeres sexualmente activas incluyendo población menor de 30 años. Para ello, el estudio utilizó el modelo de Markov validado para Colombia que simula la historia natural de las pacientes con displasia cervical y que tiene como horizonte temporal la expectativa de vida de la mujer colombiana (76 años a la fecha del estudio). Para esta evaluación económica se propuso como resultado en salud los años de vida ganados derivados del uso de las estrategias (Tabla 1), teniendo como perspectiva el tercer pagador (v.g. costos para el sistema de salud), con una tasa de descuento anual del 3 %. Al aplicar la lista de verificación CHEERS 15, se evidenciaron algunas limitaciones en los supuestos estructurales, en los métodos de validación del modelo, la medición y valoración de los resultados, y cuestiones éticas y distributivas.
Tabla 1 Alternativas comparadas para la tamización cervical para las mujeres en Colombia.
| Estrategia de cribado / Realizada por | Periodicidad y edad de inicio |
|---|---|
| ADN-VPH (profesional de salud) | Cada 5 años, iniciando tamización a los 30 años. |
| ADN-VPH (profesional de salud) triage con citología en base líquida. | Cada 5 años, iniciando tamización a los 25 años. |
| Prueba ADN-VPH (profesional de salud) y triage con citología convencional. | Cada 5 años, iniciando tamización a los 25 años. |
| Citología en base líquida desde los 25 años continuando con prueba ADN-VPH (profesional de salud) y triage con citología en base líquida. | Cada 5 años, a partir de los 30 años. |
| Citología convencional desde los 25 años continuando con prueba ADN-VPH (profesional de salud) y triage con citología convencional. | Cada 5 años, a partir de los 30 años. |
| Prueba ADN- VPH (Autotoma). | Cada 3 años, iniciando la tamización a los 30 años. |
| Prueba ADN-VPH (Autotoma) y triage con citología en base líquida. | Cada 3 años, iniciando la tamización a los 25 años. |
| Prueba ADN-VPH (Autotoma) y triage con citología. | Convencional cada 3 años, iniciando la tamización a los 25 años. |
| Citología en base líquida desde los 25 años continuando con prueba ADN-VPH (Autotoma) y triage con citología en base líquida. | Cada 3 años, a partir de los 30 años. |
| Citología convencional desde los 25 años continuando con prueba ADN-VPH (Autotoma) y triage con citología convencional. | Cada 3 años, a partir de los 30 años. |
| No tamización cervical. |
Los costos directos fueron los derivados del valor de la contratación del personal asistencial, del tratamiento médico y del manejo de las complicaciones; los cuales se expresaron en pesos colombianos (COP) y con la metodología "tipo de caso". La valoración monetaria se realizó usando los manuales ISS (Manual de tarifas de la entidad promotora de salud) + 30 % 2001 y SOAT de acuerdo con la guía metodológica para el desarrollo de GPC en Colombia 27. En cuanto a los medicamentos, se extrajo información del SISMED (Sistema de información de precios de medicamentos) y de la resolución 4316 de 2011, que fueron actualizados a la fecha de estudio usando el índice de precios al consumidor, informado por el DANE (Departamento Administrativo Nacional de Estadística) 28.
Se estimaron las razones de costo-efectividad incremental para cada una de las alternativas en evaluación, de acuerdo con lo recomendado por IETS (Instituto de Evaluación Tecnológica en Salud 9 para este tipo de estudios. De esta manera, se implementó como umbral el producto interno bruto (PIB) per cápita, ($15.008.793 COP para 2013 y $23.050.060 COP para el año 2021) 26, considerando como alternativa costo-efectiva si el costo por año de vida adicional estaba entre dos y tres veces el PIB. A partir de los resultados de este estudio, se puede concluir que la estrategia de inicio con prueba ADN-VPH y triage con citología desde los 25 años quizás representa la alternativa más costo-efectiva para el sistema de salud colombiano (Razón costo-efectividad incremental [RCEI] $8.820.980 COP, datos 2013), en tanto que la aproximación vigente, con inicio de la tamización con citología a los 25 años, continuando con prueba de ADN-VPH y triage con citología desde los 30 años, constituye una alternativa dominada, toda vez que es más costosa y menos efectiva. Otras alternativas que eventualmente podrían resultar costo-efectivas acorde a la disponibilidad a pagar pueden ser el uso de la prueba ADN-VPH por autotoma y triage con citología convencional o base líquida cada 3 años (RCEI $17.536.200 COP y $33.094.285 COP, respectivamente).
Aspectos organizacionales y del individuo: valores y preferencias
Dos estudios recopilaron la evidencia de estos dos dominios de la prueba ADN-VPH en mujeres menores de 30 años. El primero de ellos corresponde a una revisión sistemática con metasíntesis cualitativa (AMSTAR 2 moderada) 25, en tanto que la segunda alude a un estudio cualitativo desarrollado en siete municipios de Colombia 26. Ambos involucraron mujeres menores de 30 años, capturaron las potenciales barreras y facilitadores asociados al proceso, al tiempo que recopilaron los valores, perspectivas y preferencias frente a la tamización cervical para esta población.
Implicaciones sobre la mujer individual. Un elemento que sobresale en ambas publicaciones es que las mujeres perciben y asocian un resultado positivo en la prueba a infidelidad y un diagnóstico indefectible de cáncer. La tamización cervical también genera en las mujeres la sensación de vulnerabilidad y desprotección, toda vez que se desarrolla bajo el contexto de la desnudez; percepción que se potencializa especialmente cuando las prácticas del cribado resultan contrarias a la creencia cultural. Con respecto a los elementos que impactan negativamene la aceptabilidad de la prueba, la literatura señala aspectos relevantes como la prioridad que la mujer le otorga al ámbito familiar y laboral, muchas veces sobre sus necesidades en salud 25,26.
Aspectos organizacionales
Por otra parte, la aceptabilidad se incrementa con una adecuada comunicación y empatía con el proveedor de servicio de salud y con la percepción que poseen algunas pacientes, pues entre más veces repitan la prueba, mejor será el proceso 25,26. Frente a la autotoma, la evidencia encontró que si bien esta alternativa les otorga a las pacientes comodidad y privacidad, su implementación podría estar vinculada con el temor a que la muestra no sea adecuada, dado que el procedimiento recae sobre ella 27,28.
En cuanto al entorno, la literatura señala la existencia de algunas barreras cuando las mujeres experimentan dificultades de acceso atribuibles a circunstancias de orden público (v.g. violencia o inseguridad) o bien, de carácter geográfico (v.g. largos desplazamientos, no disponibilidad de vías de acceso) 26. Barreras que podrían ser solventadas, al menos en parte, por la disponibilidad de nuevas tecnologías (autotoma) o estrategias de cribado (VIA-VILI). Como posible facilitador se destaca que el acto de involucrar nuevos actores en el marco del proceso de tamización (v.g. líderes comunitarios, profesionales de salud locales o supervivientes de cáncer) empodera a la población y fomenta el cribado, haciendo de este un proceso aceptable socialmente 26.
Cuando se trata de las barreras y facilitadores relacionados con el sistema, el principal facilitador es la inclusión de la prevención y detección temprana del cáncer del cuello uterino en la agenda de salud nacional y la incorporación de nuevas tecnologías sanitarias en el plan de beneficios en salud 26. Para el contexto colombiano, se encuentran como barrera la eficiencia del sistema de autorizaciones, el cual varía acorde al tipo de asegurador, la ausencia de registros estandarizados para los procesos de tamización y la marcada heterogeneidad que hay en la capacidad instalada, dotación y calidad de los servicios en salud implicados en la tamización, triage y manej o de los casos positivos 26. Dentro de estos desafíos propios del sistema, llama la atención las diferencias en la autorización de la colposcopia y la biopsia, debido a que en algunos casos se autorizan de forma simultánea y no es necesaria la realización de biopsia dependiendo de lo que reporta la colposcopia; o se realiza la colposcopia pero hay inoportunidad en la autorización de la biopsia, ocasionado pérdidas en el seguimiento 26.
Evidencia aspectos éticos
Una revisión sistemática de la literatura (AMSTAR 2: moderada) recuperó la evidencia disponible en torno a los aspectos éticos relacionados con la tamización cervical, cómo estos influyen sobre la adopción de estrategias 25. Al respecto, la ETS señala que todo cambio en la política pública debe incorporarse desde la perspectiva ética, los principios de beneficencia, no maleficencia, autonomía y equidad 25. El documento señala que todo programa de cribado (especialmente cuando se trata del uso de nuevas tecnologías) debe fundamentarse sobre el precepto de "compensación aceptable de daño/beneficio", el cual se enmarca en los cuatro pilares éticos y sociales previamente mencionados: la reducción de la incidencia y de la mortalidad por cáncer es éticamente y socialmente valiosa (principio de beneficencia); la tecnología seleccionada para realizar el cribado debe ser la más eficiente disponible, pues esto también engloba el principio de beneficencia (la costo-oportunidad es relevante); la estrategia seleccionada debe minimizar el daño (remisión a colposcopia y el riesgo asociado al sobrediagnóstico y sobretratamiento) sobre la población blanco (principio de no maleficencia) y todo programa debe contemplar la inclusión de alternativas seguras, efectivas y eficientes que reduzcan la inequidad en salud, protegiendo a las mujeres que se encuentran en situación de vulnerabilidad.
Para finalizar, la evaluación enfatiza que recae sobre el médico la responsabilidad de ilustrar la voluntariedad de la detección y de fomentar la elección informada (principio de autonomía), sin juicios de valor o presiones, y sin que una negativa de participación represente per se la cesación del acto médico. Los programas de cribado deben minimizar cualquier aumento de los daños relacionados con la prueba empleada para la tamización (v.g. aumento de las remisiones a colposcopias, casos falsos positivos, la estigmatización de las pacientes al ser el VPH una enfermedad de transmisión sexual) justificando de manera transparente la edad de inicio y el intervalo para ella. El médico y su paciente, correctamente informado, deben estar preparados para las posibles implicaciones de un resultado positivo 25.
CONCLUSIONES DE LA REVISIÓN SISTEMÁTICA Y MESA DE TRABAJO
El uso de la prueba ADN-VPH como estrategia de tamización en mujeres menores de 30 años es una intervención efectiva, en virtud que reduce la incidencia de carcinoma invasor en rondas subsecuente (Calidad de la evidencia alta) y posiblemente permite una mayor detección de lesiones NIC2+ durante la primera ronda de cribado (Calidad de la evidencia baja). El estudio económico disponible a la fecha, sugiere que la tamización a partir de los 25 años con prueba ADN-VPH y triage con citología cada 5 años, es quizás, la alternativa más costo-efectiva para Colombia.
Debido a la frecuencia del cáncer de cuello uterino, la existencia de una tecnología en la cual la relación de riesgo beneficio, las implicaciones económicas y éticas, así como los efectos sobre la mujer, son importantes, sería pertinente ampliar el programa de tamización con prueba ADN VPH a las mujeres desde los 25 años o más. Se requieren más estudios que evalúen la seguridad y efectividad de la tamización con ADN-VPH en mujeres menores de 30 años, prestando especial atención a los efectos no deseados de esta alternativa. Finalmente, dado que el estudio económico disponible presenta limitaciones metodológicas, al tiempo que no abordan algunas alternativas de tamización reciente, y que sus costos no se encuentran actualizados frente a una mayor cantidad de alternativas en el mercado, es necesario la actualización de este análisis costo-efectividad.
GRUPO DESARROLLADOR DE LA EVALUACIÓN TECNOLÓGICA EN SALUD EN TAMIZACION PRIMARIA CERVICAL
Carmen Doris Garzón-Olivares, MD. Profesor Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia, Bogotá (Colombia).
Carlos Fernando Grillo-Ardila, MD. Profesor Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia, Bogotá (Colombia). Instituto Nacional de Cancerología, Grupo de Investigación Clínica y Epidemiológica del Cáncer, Bogotá (Colombia).
Jairo Amaya-Guio, MD. Profesor Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia, Bogotá (Colombia).
María Teresa Vallejo-Ortega, MSc. Instituto Nacional de Cancerología. Bogotá (Colombia).
Luz Amparo Diaz-Cruz, MD. Profesor Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia, Bogotá (Colombia).
Carolina Fernández-Motta, MD. Universidad Surcolombiana, Neiva (Huila).
Alejandra del Pilar Gómez-Motta. Universidad Surcolombiana, Neiva (Huila).
Alina Tatiana Barrera. Universidad Surcolombiana, Neiva (Huila).
GRUPO PARTICIPANTE EN LA MESA DE TRABAJO
Lina Maria Trujillo-Sánchez, MD. Instituto Nacional de Cancerología, Bogotá (Colombia).
Carlos Humberto Pérez-Moreno, MD. Federación Internacional de Patología del Tracto Genital Inferior y Colposcopia, Bogotá (Colombia).
Luis Jairo Bonilla-Osma, MD. Profesor Fundación Universitaria de Ciencias de las Salud, Bogotá (Colombia). Robinson Fernández-Mercado, MD. Profesor Universidad Libre de Barranquilla.
Néstor Giraldo, MD. Subred Integrada de servicios de Salud Norte, Bogotá (Colombia).
Jorge Eduardo Caro-Caro, MD. Subred Integrada de servicios de Salud Centro-Oriente, Bogotá (Colombia).
Amparo Leonor Ramírez-Corredor, MD. Subred Integrada de Servicios de Salud Sur, Bogotá (Colombia).
Dayanne Milecsy Rodríguez-Hernández, PhD. Universidad Nacional de Colombia, Bogotá (Colombia).
ESTUDIOS ECONÓMICOS