Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombian Journal of Anestesiology
Print version ISSN 0120-3347On-line version ISSN 2256-2087
Rev. colomb. anestesiol. vol.49 no.1 Bogotá Jan./Mar. 2021 Epub Jan 04, 2021
https://doi.org/10.5554/22562087.e913
Revisión narrativa
¿Cómo evaluar la calidad metodológica de las revisiones sistemáticas a través de la herramienta AMSTAR?
a Facultad de Enfermería, Pontificia Universidad Javeriana. Bogotá, Colombia.
b Facultad de Medicina, Pontificia Universidad Javeriana. Bogotá, Colombia.
c Departamento de Epidemiología Clínica y Bioestadística, Facultad de Medicina, Pontificia Universidad Javeriana. Bogotá, Colombia.
Introducción
Tomar decisiones basadas en la evidencia ha sido un reto para profesionales de la salud; se requiere tener herramientas y habilidades para apreciar la evidencia críticamente y evaluar la validez de los resultados. Las revisiones sistemáticas de la literatura (RSL) han sido muy usadas para dar respuesta a preguntas del ámbito clínico. Se han desarrollado herramientas que apoyan la apreciación de la calidad de los estudios. El AMSTAR es una de estas, validada y soportada por evidencia reproducible que orienta la calidad metodológica de las RSL.
Objetivos
Mostrar un abordaje histórico, teórico y de guía práctica para la apreciación crítica de las revisiones sistemáticas con el AMSTAR, orientar las bases argumentales para su uso, según los componentes de esta estructura metodológica en investigación en salud, y proporcionar ejemplos prácticos sobre cómo aplicar esta lista de chequeo.
Métodos
Realizamos una revisión no exhaustiva de literatura en PubMed y The Cochrane Library con los términos libres "AMSTAR" y "revisiones sistemáticas'', sin límite de idioma o año de publicación; también, recolectamos información de expertos en evaluación de la calidad de la evidencia.
Conclusiones
El AMSTAR es un instrumento validado y soportado por evidencia reproducible para la evaluación de la validez interna de las revisiones sistemáticas de la literatura. Consiste en 16 ítems que evalúan de manera global la calidad metodológica de una RSL. Actualmente, se usa de manera indiscriminada y predilecta, pero no está exenta de limitaciones y futuras actualizaciones basadas en nuevos estudios de reproducibilidad y validación.
Palabras clave: AMSTAR; revisión sistemática; evaluación de calidad; evidencia clínica; fiabilidad; validez; métodos epidemiológicos; metaanálisis como tema
Introduction
Making decisions based on evidence has been a challenge for health professionals, given the need to have the tools and skills to carry out a critical appraisal of the evidence and assess the validity of the results. Systematic reviews of the literature (SRL) have been used widely to answer questions in the clinical field. Tools have been developed that support the appraisal of the quality of the studies. AMSTAR is one of these, validated and supported by reproducible evidence, which guides the methodological quality of the SRL.
Objectives
To show a historical, theoretical and practical guide for critical assessment of systematic reviews using AMSTAR to guide the argumental bases for their use according to the components of this methodological structure in health research, and to provide practical examples of how to apply this checklist.
Methods
We conducted a non-exhaustive review of literature in Pubmed and Cochrane Library using "AMSTAR" and "Systematic Reviews" as free terms without language or publication date limit; we also collected information from experts in the evaluation of the quality of the evidence.
Conclusions
AMSTAR is an instrument used, validated and supported by reproducible evidence for the evaluation of the internal validity of systematic reviews of the literature. It consists of 16 items that assess the overall methodological quality of a SRL. It is currently used indiscriminately and favorably, but it is not exempt from limitations and future updates based on new reproducibility and validation studies.
Keywords: AMSTAR; systematic review; quality assessment; clinical evidence; reliability; validity; epidemiological methods; meta-analysis as topic
¿Qué sabemos acerca de este problema?
Las revisiones sistemáticas de la literatura, dentro del ámbito clínico, tienen como objetivo sintetizar evidencia enfocada en la efectividad/eficiencia de tratamientos, diagnóstico y pronóstico, para apoyar la toma de decisiones en salud. Aunque existe variabilidad en criterios de apreciación metodológica y herramientas que orientan este tipo de estudios, el AMSTAR es un instrumento validado que permite apreciar críticamente la calidad, a través de dominios globales.
¿Qué aporta este estudio de nuevo?
Aunque conocemos reportes sobre la validación y estructura del AMSTAR, este manuscrito es una guía que presenta un abordaje histórico, teórico y práctico que orienta a clínicos y metodólogos sobre su uso dentro de la práctica basada en la evidencia, específicamente en la evaluación de la calidad de las revisiones sistemáticas. Esto contribuye a la resolución de preguntas en el ámbito clínico, así como apoyar la toma de decisiones basadas en la evidencia.
INTRODUCCIÓN
Las revisiones sistemáticas de la literatura (RSL) y las síntesis ampliadas han tenido gran relevancia dentro del cuidado de la salud y la toma de decisiones en la medicina basada en la evidencia (MBE) 1,2. Esta estrategia metodológica ha sido un apoyo para el desarrollo de recomendaciones de guías de práctica clínica basadas en la evidencia; además, constituyen la segunda mejor fuente de literatura científica disponible cuando las RSL están basadas en experimentos clínicos aleatorizados, según la pirámide de la evidencia 1. Este diseño de investigación secundario o integrativo permite dar respuesta a una pregunta de investigación, según su población, intervención, comparador y desenlaces 3, al analizar los resultados de un conjunto de investigaciones originales y dar respuesta en un corto tiempo y con menos costos que el que se pueda generar de un estudio primario 3. La MBE ha ido evolucionando en su concepto, y se ha convertido en un método de comunicación a escala mundial de decisiones clínicas por medio del consumo de la literatura biomédica 4. Se origina a partir de un problema de salud traducido en una pregunta clínica que guía la búsqueda del cuerpo de la evidencia 4. Una vez se identifique la literatura biomédica, es importante preguntarse a partir de los resultados de los estudios encontrados: ¿los resultados del artículo son válidos?, ¿cuáles fueron los resultados? y ¿los resultados de ese estudio son aplicables a la población en la que se identificó el caso clínico? 5. Las respuestas a estas preguntas serán la base para tomar decisiones respecto al problema de salud. Considerando la importancia de tomar decisiones basadas en la evidencia con responsabilidad, se han diseñado y validado herramientas e instrumentos soportados en listas de chequeo que apoyan la apreciación crítica de la literatura, según el tipo de diseño metodológico reportado 6. Se le sugiere al lector la escogencia de uno de los recursos disponibles para apoyarse en la apreciación crítica de la evidencia, según el tipo de investigación.
Para la evidencia basada en RSL se han desarrollado diversas herramientas, de las cuales se ha validado y actualizado una de ellas: el AMSTAR (del inglés "A Measurement Tool for Assessment of Multiple Systematic Reviews"). Esta es una de las herramientas con mayor validez y confiabilidad para el reporte de la calidad, con resultados satisfactorios de las RSL 4. Sin embargo, poco se ha divulgado sobre los principios básicos metodológicos de una RSL, y su apreciación puede variar sustancialmente entre clínicos, por lo que es necesario lograr una comprensión e interpretación de cada ítem para su implementación. El presente artículo pretende describir y orientar el uso de la herramienta AMSTAR para la evaluación de la calidad de la evidencia de una revisión sistemática de la literatura.
SOBRE LOS ESTUDIOS SECUNDARIOS O INTEGRATIVOS
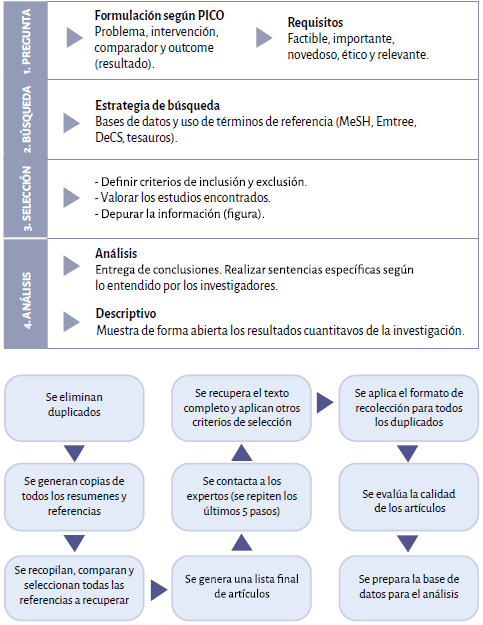
Las revisiones sistemáticas tienen como objetivo identificar, evaluar y resumir los hallazgos de todos los estudios individuales relevantes sobre un tema relacionado con la salud, y hacer que la evidencia disponible sea más accesible para los tomadores de decisiones 7. A diferencia de las revisiones narrativas, las revisiones sistemáticas de la literatura parten de una pregunta de investigación [formato PICO: P (Paciente, Población o Problema) I (Intervención) C (Comparación) O (Resultado)]; así, se realiza una búsqueda de artículos primarios, basado en una estrategia de búsqueda entendible, en diversas bases de datos (8). La etapa de selección de los artículos en la revisión sistemática tiene criterios de selección específicos y evalúa la calidad de los estudios primarios incluidos. Finalmente, el resumen de los estudios es usualmente cualitativo en la revisión narrativa, mientras que en la RSL se realiza una síntesis sistemática (cualitativo o cuantitativo - metaanálisis) 8,9(figura 1).
APRECIACIÓN CRÍTICA DE LA EVIDENCIA DE REVISIONES SISTEMÁTICAS DE LA LITERATURA
La práctica basada en la evidencia requiere el uso consciente, explícito y juicioso de la mejor evidencia disponible para tomar decisiones 10. Entonces, ¿cómo identificar, entre toda la evidencia disponible, la mejor? Para apreciarla críticamente se exige el conocimiento del tipo de diseño metodológico con el que fue respondida la pregunta de investigación 10.
Apreciación crítica de las RSL: los instrumentos para evaluar su calidad
Frente al aumento de profesionales de la salud que practican la medicina basada en la evidencia y teniendo en cuenta la responsabilidad que este proceso conlleva, se han desarrollado y validado varios instrumentos que condensan criterios para evaluar la calidad de la evidencia 11. Entre los primeros instrumentos está el "Checklist for Review Articles", desarrollado por el Departamento de Epidemiología Clínica y Bioestadística de la Universidad de McMaster y publicado en el British Medical Journal en 1994; este fue diseñado para identificar los estudios que son relevantes en el enfoque de la pregunta clínica/investigación y generar la validez del diseño escogido 12. Inicialmente fue calificado como rudimentario, por tener preguntas abiertas y carecer de un sistema de calificación objetivo 12.
En 1996, Oxman y Guyatt desarrollaron el "Cuestionario de evaluación de calidad general" (OQAQ), una herramienta validada para evaluar la calidad metodológica para las RSL de los estudios de intervención 13.
Posteriormente, en 1999, se describió el "Quality of Reporting Of Meta-analyses" (QUOROM), resultado de una conferencia de epidemiólogos, clínicos y estadísticos del Reino Unido y Norteamérica que buscaban un consenso entre disciplinas para reportar una RSL 14. El producto de esta conferencia fue una lista de comprobación estructurada con 18 ítems que los autores de un metaanálisis y también los editores de revistas deberían considerar a la hora de publicar su trabajo en forma de artículo en una revista médica. Además, incluye un diagrama de flujo que describe todo el proceso, desde la identificación inicial de los estudios potencialmente relevantes hasta la selección definitiva de estos. El objetivo de QUOROM es animar a los autores a que obtengan toda aquella información que pudiese ser esencial para interpretar y utilizar adecuadamente los resultados de un metaanálisis 14.
Al momento de su publicación, el grupo de trabajo QUOROM estableció la necesidad de una revisión y actualización programada de la herramienta, conforme con la nueva evidencia publicada. Como resultado, en julio de 2009 fue publicada la declaración PRISMA ("Preferred Reporting Items for Systematic Reviews and Meta-Analyses"), desarrollada por un grupo de 29 revisores, metodólogos, médicos, editores médicos y consumidores 15. Se utilizó un proceso de consenso basado en evidencia para desarrollar una lista de verificación de 27 ítems, la cual se ha concebido como una herramienta para contribuir a mejorar la claridad y transparencia en el reporte, y la publicación de RSL. El PRISMA no ha sido validado como instrumento para valorar la calidad de las RSL y no debería usarse como tal. Este se centra en las formas como los autores pueden garantizar la presentación de informes transparentes y completos de revisiones sistemáticas y metaanálisis 15.
No aborda directamente ni de manera detallada la realización de revisiones sistemáticas, para las cuales hay otras guías disponibles. Se consideró que fueron incluidos la mayoría de los elementos relevantes al informar revisiones sistemáticas de estudios no aleatorios que evalúan los beneficios y los daños de las intervenciones 16. Basado en los modelos previos, la evidencia empírica y los consensos de expertos, el AMSTAR nació en el 2007, en el Instituto de Investigación Bruyère en Ottawa, Ontario, Canadá; esta herramienta combina puntos del Overview Quality Assessment Questionnaire 17. El instrumento tiene como ventajas su buena correlación interevaluador, su gran fiabilidad para el análisis de las revisiones sistemáticas y su fácil entendimiento y utilización 18. Además, ha recibido el aval de la Agencia Canadiense para las Drogas y las Tecnologías en Salud (CADTH), ha sido citado aproximadamente 200 veces en los últimos tres años y una gran variedad de autores dan el aval para su uso. Otro punto para tener en cuenta es la excelente fiabilidad de la puntuación obtenida por el AMSTAR, su practicidad, simplicidad y fácil interpretación 18.
En la actualidad, la evidencia científica ha aumentado en estudios no aleatorizados, esto generó la necesidad de sintetizar dicha evidencia bajo la misma metodología de las RSL. A partir de ello, el AMSTAR ha desarrollado su segunda versión de la herramienta AMSTAR 2 que ayudará a los responsables de la toma de decisiones en la identificación de revisiones sistemáticas de alta calidad, incluidas aquellas basadas en estudios no aleatorios de intervenciones de atención médica 19.
Esta herramienta tiene como objetivo generar evaluaciones válidas, confiables y completas que ayuden a los usuarios a diferenciar la calidad entre las diversas revisiones sistemáticas de la literatura centrándose en su calidad metodológica, para así facilitar el desarrollo de revisiones de alta calidad 20. La herramienta debe ser interpretada de forma individual por cada evaluador, partiendo de que no existen resultados buenos o malos, sino un espectro muy amplio de resultados intermedios sobre la calidad metodológica de la RSL, los cuales deben correlacionarse con los objetivos y conclusiones de cada artículo para tener una visión real y concreta del contexto.
"A MEASUREMENT TOOL FOR ASSESSMENT OF MULTIPLE SYSTEMATIC REVIEWS" (AMSTAR)
Las revisiones sistemáticas de la literatura dentro del ámbito clínico tienen como objetivo sintetizar evidencia enfocada en la efectividad/eficiencia de tratamientos, diagnóstico y pronóstico. Aunque existe variabilidad en criterios de apreciación metodológica de este tipo de estudios, existe una aceptación internacional de ciertos estándares para determinar si la RSL es de calidad 21. Dentro de la variabilidad de los instrumentos desarrollados para la apreciación crítica de las revisiones sistemáticas de la literatura y metaanálisis (tabla 1), cada una puede llegar a conclusiones diferentes al evaluar una sola RSL, dependiendo del evaluador y la ponderación que tienen las herramientas, la cual puede ser difícil de interpretar por los lectores.
TABLA 1 Herramientas para evaluar la validez de los estudios científicos.
| Study type | Tool | Source |
|---|---|---|
| Experimentos clínicos aleatorizados | Herramienta Cochrane para el riesgo de sesgo. | https://training.cochrane.org/es/resource/evaluaci%c3%b3n-del-riesgo-de-sesgo-de-los-estudios-incluidos |
| Herramienta de apreciación crítica del centro de Medicina Basada en la Evidencia (MBE) de Oxford. | https://www.cebm.net/2014/06/critical-appraisal/ | |
| Lista de chequeo de apreciación crítica de literatura de Scottish Intercollegiate Guidelines Network (SIGN). | https://www.cebm.net/2014/06/critical-appraisal/ | |
| Critical Appraisal Skills Program (CASP): “Randomised Controlled Trial Appraisal Tool” | https://casp-uk.net/casp-tools-checklists/ | |
| Physiotherapy Evidence Database (PEDro) Scale Physiotherapy Evidence Database Scale | https://www.pedro.org.au/ | |
| The Jadad Scale | http://onlinelibrary.wiley.com/doi/10.1002/9780470988343.app1/pdf | |
| Graphic Approach To Evidence based practice (GATE)-Critically Appraised Topic (CAT)- Intervention Randomised Controlled Trials (RCT) Studies. Centre for Evidence Based Medicine, Oxford University. | https://www.fmhs.auckland.ac.nz/assets/fmhs/soph/epi/epiq/docs/GATE%20CAT%20Intervention%20Studies%20May%202014%20V8.docx | |
| Joanna Briggs Institute (JBI) Checklist for Randomised Controlled Trials. | http://joannabriggs.org/research/critical-appraisal-tools.htm | |
| Estudios observacionales analíticos de cohorte | Critical Appraisal Skills Program (CASP): Cohort Studies | https://casp-uk.net/casp-tools-checklists/ |
| Graphic Approach To Evidence based practice (GATE)-Critically Appraised Topic (CAT) - Intervention Cohort Studies. | https://www.fmhs.auckland.ac.nz/assets/fmhs/soph/epi/epiq/docs/GATE%20CAT%20Intervention%20Studies%20May%202014%20V8.docx | |
| Joanna Briggs Institute (JBI) checklist for Cohort Studies | https://joannabriggs.org/sites/default/files/2019-05/JBI_Critical_Appraisal-Checklist_for_Cohort_Studies2017_0.pdf | |
| Estudios observacionales analíticos de casos y controles | Critical Appraisal Skills Program (CASP): Case Control Studies | https://casp-uk.net/casp-tools-checklists/ |
| Graphic Approach To Evidence based practice (GATE)-Critically Appraised Topic (CAT) - Case Control Studies | https://www.fmhs.auckland.ac.nz/assets/fmhs/soph/epi/epiq/docs/GATE%20CAT%20Case%20Control%20Studies%20May%2 | |
| Scottish Intercollegiate Guidelines Network (SIGN) Methodology Checklist 4: Case Control Studies. | http://www.sign.ac.uk/checklists-and-notes.html | |
| Joanna Briggs Institute (JBI) Checklist for Case Control Studies. | http://joannabriggs.org/research/critical-appraisal-tools.html | |
| Pruebas diagnósticas | Critical Appraisal Skills Program (CASP) Diagnostic Critically Appraised Topic (CAT) | https://casp-uk.net/casp-tools-checklists/ |
| Graphic Approach To Evidence based practice (GATE)-Critically Appraised Topic (CAT) for Diagnostic Test Accuracy Studies. | https://www.fmhs.auckland.ac.nz/assets/fmhs/soph/epi/epiq/docs/GATE%20CAT%20Diagnostic%20Studies%20May%202014%202014%20V5.docx | |
| Joanna Briggs Institute (JBI) Checklist for Diagnostic Accuracy Studies. | http://joannabriggs.org/research/critical-appraisal-tools.html | |
| Critical Appraisal Skills Program (CASP) Diagnostic Critically Appraised Topic (CAT) | https://casp-uk.net/wp-content/uploads/2018/03/CASP-Diagnostic-Checklist-2018_fillable_form.pdf | |
| Evaluaciones económicas en salud | Critical Appraisal Skills Program (CASP):Economic Evaluation Studies. | https://casp-uk.net/wp-content/uploads/2018/01/CASP-Economic-Evaluation-Checklist-2018.pdf |
| Scottish Intercollegiate. Guidelines Network (SIGN). Methodology Checklist 6: Economic studies. | http://www.sign.ac.uk/checklists-and-notes.html | |
| Joanna Briggs Institute (JBI)Checklist for Economic Evaluations. | http://joannabriggs.org/research/critical-appraisal-tools.html | |
| Revisiones sistemáticas de la literatura y metaanálisis | Critical Appraisal Skills Program (CASP): Systematic Reviews. | https://casp-uk.net/wp-content/uploads/2018/01/CASP-Economic-Evaluation-Checklist-2018.pdf |
| A Measurement Tool for Assessment of Multiple Systematic Reviews (AMSTAR) | https://amstar.ca/Amstar_Checklist.php | |
| Scottish Intercollegiate. Guidelines Network (SIGN). Methodology Checklist 1: Systematic Reviews. | http://www.sign.ac.uk/checklists-and-notes.html | |
| Joanna Briggs Institute (JBI) Checklist for Systematic Reviews. | http://joannabriggs.org/research/critical-appraisal-tools.html | |
| Centre for Evidence Based Medicine, Oxford University. | https://www.cebm.net/2014/06/critical-appraisal/ |
FUENTE: Autores.
El AMSTAR es una herramienta utilizada para estimar la calidad metodológica de las revisiones. Inició como una herramienta para evaluar RSL de estudios de intervención; sin embargo, gracias a su evaluación y evolución metodológica se creó el AMSTAR 2, que incluye la evaluación de RSL de estudios experimentales y no experimentales 20. En 2007, B. J. Shea y colaboradores de la Universidad de Ottawa, decidieron alcanzar algo de consistencia en la evaluación de las revisiones sistemáticas, al centrar la apreciación en dos criterios de calidad de estos estudios con la primera versión del AMSTAR: la calidad metodológica con la que fue conducida la revisión y la calidad de información con que fueron reportados la metodología y los resultados. Dicho estudio prospectivo de validación externa logró demostrar la confiabilidad de la herramienta al compararla con el criterio de referencia para evaluar revisiones sistemáticas de la época, lo que dio unos resultados congruentes en la evaluación de 42 revisiones sistemáticas 22. Tres años más tarde se realizó otro estudio a cargo de los mismos autores para medir la congruencia, confiabilidad, validez y factibilidad de AM-STAR; en este se usaron 30 revisiones sistemáticas de la literatura utilizando "Overview of Quality Assessment Questionnaire" (OQAQ) 10, "The Rating Scale of Sacks y colaboradores" y la herramienta AMSTAR. El estudio mostró que AMSTAR cumplía con una buena calidad durante la evaluación de los ítems anteriormente mencionados, y obtuvo resultados superiores a las demás herramientas 23.
DOMINIOS QUE EVALÚA EL AMSTAR 2
El AMSTAR fue desarrollado con base en un cuestionario de evaluación de calidad. La lista de chequeo consta de 16 ítems que sistemáticamente guían al evaluador sobre cada uno de los factores que pueden hacer de una RSL poco válida y confiable. Adicionalmente, esta es una de las razones por las que el AMSTAR también puede ser usado como guía durante el desarrollo y reporte de RSL 18(tabla 2).
TABLA 2. Dominios del AMSTAR 1. ¿La pregunta de investigación y los criterios de inclusión para la revisión incluyen los componentes PICO?
| Para marcar sí | Opcional (recomendado) | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
√ Población √ Intervención √ Comparador √ Outcome (resultado) |
√ Tiempo de seguimiento. | La pregunta de investigación raras veces está descrita en formato de interrogación, se identifica en el título u objetivo. |
□ Sí. □ No |
Esta condición se cumple si se identifica que ¡os autores contemplaron una pregunta de investigación en la que se identifique la población, la intervención, el grupo comparador y el resultado.
2 ¿Contenía el informe de la revisión una declaración explícita de que los métodos de revisión se habían establecido antes de la realización de la revisión y justificaba el informe cualquier desviación significativa del protocolo?
| Para marcar sí parcial | Opcional (recomendado) | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
Los autores afirman que tenían un protocolo que incluye: √ Pregunta de revisión √ Estrategia de búsqueda √ Criterios de inclusión/exclusión √ Evaluación del riesgo de sesgo |
Además de lo anterior, hay registro del protocolo y se especifica: √ El plan de metaanálisis (si corresponde) √ El plan para investigar causas de heterogeneidad. √ Justificación de cualquier desviación del protocolo. |
En los antecedentes o en la sección de métodos del estudio. |
□ Sí □ Sí parcial □ No |
Este ítem evalúa si fue proporcionado un diseño 'a priori' de la revisión en el que se encuentran definidos la pregunta de investigación, los criterios de inclusión y exclusión. Orienta e indaga sobre la existencia de un protocolo de la RSL, y es importante para detectar posibles desviaciones en este durante la ejecución del estudio.
3 ¿Los autores de la revisión explicaron la selección de los diseños del estudio para su inclusión en la revisión?
| Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|
|
La revisión debe satisfacer UNO de los siguientes: □ Explicación para incluir solo experimentos clínicos aleatorizados (ECA). □ O solo estudios no aleatorizados de intervenciones (NRSI). □ O explicación para incluir ECA y NRSI. |
En la sección de métodos. |
□ Sí. □ No |
4 ¿Los autores de la revisión utilizaron una estrategia integral de búsqueda de literatura?
| Para marcar sí parcial | Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
Los autores: √ Buscaron en al menos dos bases de datos. √ Proporcionaron las palabras clave o estrategia de búsqueda. √ Añadieron las restricciones de publicación justificadas (idioma, año de publicación). |
Además de lo anterior, los autores: √ Buscaron en las referencias bibliográficas de los estudios incluidos. √ Indagaron los registros de los ensayos y estudios. √ Consultaron a expertos en el campo. √ Utilizaron literatura gris (si relevante). √ Realizaron una búsqueda dentro de los 24 meses posteriores a la finalización de la revisión. |
En la sección de métodos o en los suplementos del artículo. |
□ Sí □ Sí parcial □ No |
Cuestiona sobre las bases de datos incluidas, los años abarcados, las palabras clave; los términos MeSH y EMTREE deben estar registrados y preferiblemente debe aparecer descrita la estrategia de búsqueda que se utilizó. Además, todas las búsquedas deben ser complementadas con consulta a registros especializados o expertos en el campo de estudio, revisión de las listas de referencias en los estudios encontrados y revisión de la literatura gris.
5 ¿Los autores de la revisión realizaron la selección del estudio por duplicado?
| Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|
|
La revisión debe satisfacer UNO de los siguientes: □ Selección de estudios elegibles y alcanzaron un consenso sobre qué estudios incluir. O □ dos revisores seleccionaron una muestra de estudios elegibles y lograron un buen acuerdo (al menos el 80 %), y el resto fue seleccionado por un revisor. |
En la sección de métodos. |
□ Sí. □ No |
6 ¿Los autores de la revisión realizaron la extracción de datos por duplicado?
| Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|
|
La revisión debe satisfacer UNO de los siguientes: □ Al menos dos revisores lograron un consenso sobre qué datos extraer de los estudios incluidos. O □ dos revisores extrajeron datos de una muestra de estudios elegibles y lograron un buen acuerdo (al menos el 80 %), con el resto extraído por un revisor. |
En la sección de métodos. |
□ Sí. □ No |
7 ¿Los autores de la revisión proporcionaron una lista de estudios excluidos y justificaron las exclusiones?
| Para marcar sí parcial | Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
Los autores: √ Proporcionaron una lista de todos los estudios relevantes que se leyeron en forma de texto completo, pero se excluyeron de la revisión |
Además de lo anterior, los autores: √ Justificaron la exclusión de la revisión de cada estudio potencialmente relevante |
En la sección de métodos o en los suplementos del artículo. |
□ Sí □ Sí parcial □ No |
Ya que los sesgos se pueden introducir en varias etapas en el diseño, la planificación, la conducta y el análisis de un estudio, este punto debe ser evaluado en cada uno de los artículos primarios de la RSL.
8 ¿Los autores de la revisión describieron los estudios incluidos con el detalle adecuado?
| Para marcar sí parcial | Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
Se encuentran: √ intervenciones descritas √ Comparadores descritos √ Resultados descritos √ Diseños de investigación descritos |
√ Población descrita en detalle √ Describieron la intervención detalladamente (dosis, si pertinente) √ El comparador descrito en detalle (incluida la dosis, si relevante) √ Describieron el entorno √ Calendario para el seguimiento |
En la sección de resultados, anexos o suplementos. |
□ Sí □ Sí parcial □ No |
9 ¿Los autores de la revisión utilizaron una técnica satisfactoria para evaluar el riesgo de sesgo (ROB, por sus siglas en inglés) en los estudios individuales que se incluyeron en la revisión?
| Para marcar sí parcial | Para marcar sí | ¿Dónde buscar en el artículo? | Respuesta |
|---|---|---|---|
|
Debe haber evaluado ROB de: √ Asignación oculta, y √ falta de cegamiento de pacientes y evaluadores al evaluar los resultados. |
Además de lo anterior, debe haber evaluado ROB de: √ Secuencia de asignación que no fue realmente aleatoria, y √ selección del resultado informado entre múltiples mediciones o análisis de un resultado específico. |
En la sección de métodos, resultados, anexos o suplementos. |
□ Sí □ Sí parcial □ No |
Ya que los sesgos se pueden introducir en varias etapas en el diseño, la planificación, la conducta y el análisis de un estudio, este punto debe ser evaluado en cada uno de los artículos primarios de la RSL.
10 ¿Los autores de la revisión informaron sobre las fuentes de financiación para los estudios primarios incluidos en la revisión?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
| √ Debe haber informado sobre las fuentes de financiación para los estudios individuales incluidos en la revisión. | En las consideraciones, notas o agradecimientos. |
□ Sí. □ No |
Es importante apreciar las fuentes que financiaron los estudios, por el sesgo de publicación y/o sesgo de información.
11 Si se realizó un metaanálisis, ¿usaron los autores de la revisión los métodos apropiados para la combinación estadística de los resultados?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
|
Los autores: √ Justificaron combinar los datos en un metaanálisis. √ Utilizaron una técnica ponderada apropiada para combinar resultados del estudio y ajustarlos por heterogeneidad. √ Investigaron las causas de cualquier heterogeneidad. |
En la sección de métodos. |
□ Sí □ No □ No se realizó metaanálisis |
Se evalúa si los autores justificaron combinar los datos en un metaanálisis y si usaron una técnica ponderada apropiada para combinar resultados del estudio (ajustando por heterogeneidad y si combinaron estadísticamente las estimaciones de efectos de estudios no aleatorizados que se ajustaron por confusión), en lugar de combinar datos brutos o combinar datos sin procesar, cuando las estimaciones de efectos ajustados no estaban disponibles e informaron estimaciones de resumen para ECA y NRSI por separado (cuando ambos fueron incluidos en la revisión).
12 Si se realizó el metaanálisis, ¿los autores evaluaron el impacto potencial de riesgo de sesgo en estudios individuales sobre los resultados del metaanálisis u otra síntesis de evidencia?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
|
Los autores: √ Incluyeron un único ECA de bajo riesgo de sesgo. O √ si la estimación agrupada se basó en ECA y/o NRSI en ROB variable, los autores realizaron análisis para investigar el posible impacto de ROB en las estimaciones resumidas del efecto. |
En la sección de métodos. |
□ Sí □ No □ No se realizó metaanálisis |
Este ítem requiere que los revisores examinen cómo los resultados varían con la inclusión o exclusión de los estudios primarios que se consideran de alto riesgo de sesgo.
13 ¿Los autores de la revisión dieron cuenta de riesgo de sesgo en los estudios primarios al interpretar/discutir los resultados de la revisión?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
|
Los autores: √ Incluyeron solo un ECA de bajo riesgo de sesgo. O √ si se incluyeron ECA con ROB moderado o alto, o NRSI. √ la revisión proporcionó una discusión sobre el probable impacto de ROB en los resultados. |
En la sección de resultados. |
□ Sí □ No □ No se realizó metaanálisis |
14 ¿Los autores de la revisión proporcionaron una explicación satisfactoria y una discusión sobre cualquier heterogeneidad observada en los resultados de la revisión?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
|
√ No hubo heterogeneidad significativa en los resultados. √ O si hubo heterogeneidad, los autores realizaron una investigación de las fuentes de cualquier heterogeneidad en los resultados y discutieron el impacto de esto en los resultados de la revisión. |
En la sección de resultados o discusión. |
□ Sí □ No |
Es importante que se investiguen las posibles causas de heterogeneidad, la variación en los elementos incluidos en el marco de la pregunta PICO (ítem i) y aquellos que surgen de consideraciones metodológicas y diseño (item 9). Con la inclusión de estudios no aleatorizados, las variaciones en el diseño y el análisis pueden contribuir a la heterogeneidad.
15 Si realizó una síntesis cuantitativa, ¿ejecutaron los autores de la revisión una investigación adecuada del sesgo de publicación (sesgo de estudio pequeño) y discutieron su posible impacto en los resultados de la revisión?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
| √ Realizaron pruebas gráficas o estadísticas para el sesgo de publicación y se discutió la probabilidad y la magnitud del impacto del sesgo de publicación. | En la sección de métodos, suplementos, anexos. |
□ Sí □ No □ No se realizó metaanálisis |
El sesgo de publicación es un problema importante que ocurre cuando el resultado de un experimento o estudio influye en la decisión de publicarlo o distribuirlo. Publicar solo resultados que muestren un hallazgo significativo perturba el equilibrio de los hallazgos e inserta sesgos a favor de resultados positivos17.
16 ¿Los autores de la revisión informaron sobre posibles fuentes de conflicto de intereses, incluido el financiamiento que recibieron para realizar la revisión?
| Para marcar sí parcial | Para marcar sí | Respuesta |
|---|---|---|
|
√ Los autores informan que no hay intereses en competencia. O √ los autores describen sus fuentes de financiamiento y cómo manejaron posibles conflictos de intereses. |
En la declaración de conflicto de intereses, agradecimientos. |
□ Sí □ No □ No se realizó metaanálisis |
Al igual que con los estudios primarios, los autores de la revisión deben informar sus fuentes de financiación de la RSL.
FUENTE: Autores.
Para usar efectivamente la herramienta, el evaluador debe disponer de la mayor información disponible de la RSL y el metaanálisis (si aplica): acceso al texto completo del artículo de la RSL, anexos, tablas, figuras, material suplementario. Se recomienda una lectura inicial del artículo, seguido de la aplicación de la lista de chequeo con opciones de respuesta entre "sí", si el ítem evaluado cumple con la condición cuestionada; "no", si el ítem evaluado no cumple con la condición evaluada, y "no puede ser contestada" o "no es aplicable".
Una vez se hayan repasado los 16 ítems de la lista de chequeo en línea, la herramienta realiza la sumatoria de los puntos de manera automática; cada "sí" es el equivalente a 1 punto y "no"/"no se puede responder" equivale a 0 puntos. Al final define si el artículo es de baja, media o alta calidad 18.
Esta versión del AMSTAR nació de una reunión constituida por los autores originales y miembros del Bruyère Research Institute y el Hospital de Ottawa con experiencia en el desarrollo de estudios no aleatorizados en la cual se evaluaron diferentes estudios y encuestas sobre el uso del AMSTAR 18. Los principales cambios resaltados por el grupo investigador fueron los siguientes: simplificar las categorías de respuesta, alinear la definición de preguntas de investigación con el marco de la pregunta PICO, buscar más detalles sobre las razones para la exclusión de los estudios de la revisión, determinar si los autores de la RSL realizaron una evaluación suficientemente detallada del riesgo de sesgo para los estudios incluidos (ya sea de forma aleatoria o no aleatorizada), determinar si el riesgo de sesgo con los estudios incluidos se consideró adecuadamente durante la combinación estadística de los resultados (si esto se realizó) y determinar si el riesgo de sesgo con los estudios incluidos se consideró adecuadamente al interpretar y discutir los hallazgos de la revisión 24.
En cuanto a la similitud con la anterior herramienta, se mantuvieron diez dominios originales de la herramienta. Dos dominios recibieron una cobertura más detallada en AMSTAR 2 que en el instrumento original: la selección de estudios duplicados y la extracción de datos ahora tienen sus propios elementos (se combinaron en la herramienta original). Además, la posible influencia de las fuentes de financiación ahora se considera por separado para los estudios individuales incluidos en la revisión y para la revisión en sí misma. Fue eliminado un dominio: la consideración de la literatura gris, que anteriormente era un elemento separado, se maneja ahora en el ítem de búsqueda bibliográfica. En total, se agregaron cuatro dominios, dos de los cuales provienen de la herramienta ROBINS-I 11, la elaboración del PICO y la forma en que se manejó el riesgo de sesgo durante la síntesis de la evidencia. Uno de los otros ítems nuevos, la discusión de las posibles causas y la importancia de la heterogeneidad es una elaboración de contenido en la herramienta original AMSTAR. Otra nueva justificación de ítem de selección de diseños de estudio fue parte de la adaptación de AMSTAR para tratar diseños no aleatorios. Las preguntas de dominio en AMSTAR 2 están enmarcadas de modo que una respuesta "sí" denota un resultado positivo; se eliminaron las opciones "no aplicable" y "no puedo responder" en el instrumento AMSTAR original, de tal forma que si no se proporciona información para calificar un ítem, los autores de la revisión no deben recibir el beneficio de la duda y el ítem debe ser calificado como "no". Por último, se ha proporcionado una respuesta de "sí" parcial en algunos casos en los que consideramos que vale la pena para identificar el cumplimiento parcial de la norma 24.
CONCLUSIONES
Una herramienta comúnmente utilizada por su eficacia para la evaluación de la validez interna de las revisiones sistemáticas de la literatura es el AMSTAR. Consiste en 16 ítems que evalúan de manera global la calidad metodológica de una revisión, y se encuentra actualmente validada. Es deber de cada revisor aplicar de manera exhaustiva, cuidadosa y responsable la lista de chequeo para establecer la calidad metodológica de la revisión y evitar el sesgo de clasificación al subestimar o sobreestimar. Aunque actualmente se usa de manera indiscriminada y predilecta, esta herramienta no está exenta de limitaciones y futuras actualizaciones basadas en nuevos estudios de re-producibilidad y validación.
RECONOCIMIENTOS
Contribución de los autores
AB-L: Concibió la idea presentada así como el diseño y estructura del manuscrito.
ABP y AB-L: Realizaron la estrategia de búsqueda e interpretación de la literatura seleccionada.
ABP y SC: Seleccionaron los estudios y extrajeron los datos.
AB-L, SC y ABP: Contribuyeron con sugerencias y comentarios críticos durante la escritura del manuscrito.
Agradecimientos
Ninguno
REFERENCIAS
1. Gaitán Duarte HG, Rojas Reyes MX, Feliciano-Alfonso J. Búsqueda, evaluación y síntesis de la evidencia de efectividad y seguridad en evaluaciones de tecnología: Manual metodológico. Washington, D.C.; BID; 2017. DOI: http://dx.doi.org/10.18235/0000748. [ Links ]
2. Higgins JP, Green S. Cochrane handbook for systematic reviews of interventions Version 5.1.0. The Cochrane Collaboration; 2011. [ Links ]
3. Cañón M, Buitrago-Gómez Q. La pregunta de investigación en la práctica clínica: guía para formularla. Rev Colomb Psiquiatr. 2018;47(3):193-200. DOI: 10.1016/i.rcp.2016.06.004. [ Links ]
4. Beltrán Ó. Revisiones sistemáticas de la literatura. Rev Colomb Gastroenterol.2005;(20):60-9. [ Links ]
5. Sackett DL, Rosenberg WMC, Gray JAM, Haynes RB, Richardson WS. Evidence based medicine: what it is and what it isn't. BMJ. 1996 312(7023)71-2. DOI: 10.1136/bmj.312.7023.71. [ Links ]
6. Al-Jundi A, Sakka S. Critical appraisal of clinical research. J Clin Diagn Res. 2017;11(5):JE01-5. DOI: 10.7860/JCDR/2017/26047.9942. [ Links ]
7. Gopalakrishnan S, Ganeshkumar P Systematic reviews and meta-analysis: understanding the best evidence in primary healthcare. J Fam Med Prim Care. 2013. DOI: 10.4103/22494863.109934. [ Links ]
8. Robinson P, Lowe J. Literature reviews vs systematic reviews. Aust N Z J Public Health. 2015;39(2):103. DOI: 10.1111/1753-6405.12393. [ Links ]
9. Evidence-Based Medicine Working Group. Evidence-based medicine. A new approach to teaching the practice of medicine. JAMA. 1992;268(17):2420-5. DOI: 10.1001/jama.1992.03490170092032. [ Links ]
10. Ruiz Morales A, Gómez-Restrepo C. Epidemiología clínica: investigación clínica aplicada. Bogotá: Médica Panamericana; 2015. [ Links ]
11. Guyatt G, Rennie D, Meade M, Cook D. Users' Guides to the medical literature: A Manual for evidence-based clinical practice, 3rd ed. McGraw-Hill Medical; 2008. [ Links ]
12. Oxman AD. Checklists for review articles. BMJ.1994;309(6955):648-51. DOI: 10.1136/bmj.309.6955.648. [ Links ]
13. Oxman AD, Guyatt GH. Validation of an index of the quality of review articles. J Clin Epidemiol. 1991;44(11):1271-8. DOI: 10.1016/0895-4356(91)90160-b. [ Links ]
14. Moher D, Cook DJ, Eastwood S, Olkin I, Rennie D, Stroup DF. Improving the quality of reports of meta-analyses of randomised controlled trials: the QUOROM statement. Quality of Reporting of Meta-analyses. Lancet (London, England). 1999;354(9193):1896-900. DOI: 10.1016/s0140-6736(99)04149-5. [ Links ]
15. Pussegoda K, Turner L, Garritty C, Mayhew A, Skidmore B, Stevens A, et al. Identifying approaches for assessing methodological and reporting quality of systematic reviews: a descriptive study. Syst Rev. 2017;6(1):117. DOI: https://doi.org/10.1186/s13643-017-0507-6. [ Links ]
16. Shea B, Dub C, Moher D. Assessing the quality of reports of systematic reviews: The QUOROM statement compared to other tools. En: Systematic reviews in health care. London, UK: BMJ Publishing Group; 2001. p. 122-39. [ Links ]
17. Pussegoda K, Turner L, Garritty C, Mayhew A, Skidmore B, Stevens A, et al. Systematic review adherence to methodological or reporting quality. Syst Rev . 2017;6(1):131. DOI: 10.1186/s13643-017-0527-2. [ Links ]
18. Pieper D, Koensgen N, Breuing J, Ge L, Wegewitz U. How is AMSTAR applied by authors - a call for better reporting. BMC Med Res Methodol. 2018. DOI: https://doi.org/10.1186/s12874-018-0520-z. [ Links ]
19. Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, et al. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017;58:j4008 DOI: https://doi.org/10.1136/bmj.j4008. [ Links ]
20. AMSTAR Assesing the Methodological Quality of Systematic Reviews The Development of Amstar [Internet]. Bruyère Research Institute, Ottawa, ON Canada; c2017 [citado 2020 ene. 9]. Disponible en: Disponible en: https://amstar.ca/contactus.php . [ Links ]
21. Egger M, Schneider M, Davey Smith G. Spurious precision? Meta-analysis of observational studies. BMJ. 1998;316(7125):140-4. DOI: 10.1136/bmj.316.7125.140. [ Links ]
22. Shea BJ, Bouter LM, Peterson J, Boers M, Andersson N, Ortiz Z, et al. External validation of a measurement tool to assess systematic reviews (AMSTAR). Gagnier J, editor. PLoS One. 2007;2(12):e1350. DOI: 10.1371/journal.pone.0001350. [ Links ]
23. Shea BJ, Hamel C, Wells GA, Bouter LM, Kristjansson E, Grimshaw J, et al. AMSTAR is a reliable and valid measurement tool to assess the methodological quality of systematic reviews. J Clin Epidemiol . 2009;62(10):1013-20. DOI: 10.1016/j.jclinepi.2008.10.009. [ Links ]
24. Sterne JAC, Egger MMD. Chapter 10: Addressing reporting biases. En: Higgins JPT, S (editors). Cochrane handbook for systematic reviews of intervention. 2011. [ Links ]
Conflictos de interés Los autores han declarado que no existen conflictos de intereses con las ideas y opiniones presentadas en este artículo.
Cómo citar este artículo: Pizarro AB, Carvajal S, Buitrago-López A. Assessing the methodological quality of systematic reviews using the AMSTAR tool. Colombian Journal of Anesthesiology. 2021;49(1):e913.
Este es un artículo de acceso abierto bajo la licencia CC BY-NC-ND (https://creativecommons.org/licenses/by-nc-nd/4.0/).
Recibido: 01 de Noviembre de 2019; Aprobado: 29 de Enero de 2020; : 19 de Agosto de 2020











 text in
text in