Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957On-line version ISSN 2500-7440
Rev. colomb. Gastroenterol. vol.38 no.1 Bogotá Jan./Mar. 2023 Epub June 07, 2023
https://doi.org/10.22516/25007440.866
Reporte de caso
Diagnóstico de un caso de hepatotoxicidad por fármacos y suplementos herbales en un hospital de Pasto, Colombia
1Specialist Physician in Toxicology, Department of Toxicology, Hospital Universitario Departamental de Nariño. Pasto, Colombia
2 Surgeon, Emergency Physician, Hospital Universitario Departamental de Nariño. Pasto, Colombia
3General Physician, Hospital Universitario Departamental de Nariño. Pasto, Colombia
4Specialist Physician in Epidemiology, Universidad de Caldas. Manizales, Colombia
El hígado es un órgano crucial en el metabolismo y algunas sustancias pueden inducir hepatitis toxica con alta morbimortalidad. La enfermedad hepática inducida por sustancias químicas y medicamentos es un desafío tanto diagnostico como terapéutico, puesto que requiere la realización de estudios de extensión para descartar otras entidades. A continuación se presenta el caso de una paciente femenina de 51 años sin comorbilidades de base, ingresada por clínica de 2 días de evolución consistente en ictericia progresiva, episodios diarreicos sin acolia ni otra manifestación adicional. Aparentemente, su cuadro fue provocado por la administración de nimesulida, 2 tabletas al día por 2 días, contra el dolor secundario a un quiste mandibular diagnosticado en días anteriores. Durante su ingreso a urgencias la paciente describió consumo crónico, a diario desde hace 4 años, de productos de Herbalife®. Cursa con elevación de transaminasas, prolongación del tiempo de protrombina (TP) e hiperbilirrubinemia directa. Se descartan enfermedades infecciosas e inmunológicas. Se decidió iniciar el cubrimiento antibiótico y vitamina K. Finalmente y por exclusión, se realizó una biopsia hepática que sugirió un proceso inflamatorio compatible con hepatitis inducida por fármacos. La mujer evolucionó favorablemente al suspender la medicación y el suplemento dietético referido. En conclusión, el caso expuesto constituye un punto inicial en el avance hacia la investigación en hepatotoxicidad por mecanismos compartidos de diversas sustancias simultáneamente, como lo sucedido a la paciente con el uso paralelo de Herbalife® y de nimesulida.
Palabras clave: Hepatitis tóxica; analgésicos; antiinflamatorios no esteroideos; ictericia; suplementos dietéticos; reporte de caso
The liver is a crucial organ in metabolism, and some substances can induce toxic hepatitis with high morbidity and mortality. Chemical and drug-induced liver disease is a diagnostic and therapeutic challenge since it requires extension studies to rule out other entities. We present the case of a 51-year-old female patient without underlying comorbidities, admitted due to symptoms of two-day evolution consisting of progressive jaundice, diarrheal episodes without acholia, or any other additional manifestation. Her condition was caused by the intake of nimesulide, two tablets a day for two days, for pain secondary to a mandibular cyst diagnosed in previous days. During her admission to the emergency room, the patient described chronic consumption of Herbalife® products daily for four years. She presented with elevated transaminases, prolonged prothrombin time (PT), and direct hyperbilirubinemia. Infectious and immunological diseases were ruled out. We decided to start antibiotic and vitamin K coverage. Finally, and by exclusion, a liver biopsy suggested an inflammatory process compatible with drug-induced hepatitis. The woman evolved favorably when the medication and dietary supplement were discontinued. In conclusion, this case constitutes an initial point in advancing research into hepatotoxicity by shared mechanisms of various substances simultaneously, such as what happened to the patient with the parallel use of Herbalife® and nimesulide.
Keywords: Toxic hepatitis; analgesics; nonsteroidal anti-inflammatory drugs; jaundice; dietary supplements; case report
Introducción
El hígado es un órgano crucial encargado de la síntesis proteica y del almacenamiento de glucógeno y vitaminas liposolubles, y también descompone los compuestos xenobióticos, incluidos fármacos1. Algunos medicamentos y sustancias de amplio consumo y de venta libre pueden inducir hepatitis tóxica2.
La enfermedad hepática inducida por sustancias y drogas es una entidad que mimetiza en diferentes grados de gravedad a los síntomas de patologías agudas y crónicas del hígado3-6. Aunque es una entidad poco frecuente en su reporte, la hepatitis tóxica tiene una alta morbimortalidad y es un desafío tanto en su diagnóstico como en su tratamiento oportuno por detectarse cuando ya ha ocurrido el daño hepático3,4. La lesión hepática inducida por medicamentos es una de las reacciones adversas más graves y el motivo más frecuente de hepatotoxicidad en muchos lugares5.
La adjudicación de hepatotoxicidad a los suplementos y fármacos requiere exclusión previa de otras causas como virus, bacterias, autoinmunidad, enfermedades metabólicas y vasculares, alcohol, patología biliar y neoplasias4,6. En específico, existen escasos reportes acerca de la hepatotoxicidad inducida por productos naturales con un creciente interés para los clínicos2,3 y pues es importante documentar nuevos casos. En cuanto a los medicamentos antiinflamatorios no esteroideos (AINE), algunos se retiraron del mercado por hepatotoxicidad grave; 7 de los AINE son responsables de casi del 10% de los casos de enfermedad hepática inducida por fármacos7.
Con respecto a otros AINE, es notable que la nimesulida ocasione tanto mayor proporción como mayor gravedad de eventos hepáticos adversos8. El riesgo de hepatotoxicidad por nimesulida también incrementa con un mayor tiempo de consumo y con dosis más altas que las convencionales8,9.
Por todo lo anterior, se presenta el caso de una mujer con hepatitis tóxica relacionada con el consumo de un suplemento herbal (Herbalife®) con antecedente de uso concomitante de nimesulida en una institución de alto nivel de complejidad de Pasto, Colombia.
Caso clínico
Se trata de una paciente femenina, profesional de 51 años, con índice de masa corporal (IMC) de 25,64 (sobrepeso) y sin antecedentes personales de relevancia que consultó a medicina interna por la aparición de un nódulo mandibular. Al comienzo se consideró un proceso inflamatorio y se prescribió nimesulida, 2 tabletas de 100 mg al día por dos días. Luego, al tercer día del cuadro la mujer presentó náuseas e ictericia; negó otros síntomas como emesis, dolor abdominal, diarrea o fiebre. Durante su ingreso a urgencias, la paciente comentó el consumo crónico de suplementos dietéticos de marca Herbalife® desde hace 4 años, con un patrón de ingesta diaria en forma de batidos. Consultó a la institución de tercer nivel de atención en salud por la exacerbación de síntomas y por el abordaje clínico inicial se contempló en el diagnóstico diferencial procesos de origen inflamatorio y viral.
Se decidió un enfoque intrahospitalario para realizar varios estudios de extensión, los cuales evidenciaron elevaciones de transaminasas, de tiempos de coagulación y de otros marcadores hepáticos (Tabla 1). El hemograma no reportó leucocitosis y la lipasa solicitada no se procesó por dificultades con los reactivos. Es de anotar que en el examen físico se identificaron adenomegalias en la región mandibular y se corroboró la ausencia de otro tipo de lesión en la piel o de sangrado agudo. Los servicios de toxicología y de medicina interna valoran el caso y emiten como impresión diagnóstica un síndrome ictérico con posible hepatotoxicidad.
Tabla 1 Exámenes séricos complementarios realizados a la paciente
| Parámetro de laboratorio | Ingreso | Día 7 | Día 10 | Egreso |
|---|---|---|---|---|
| Fosfatasa alcalina | 341 U/L | 298 U/L | 258 U/L | 86 U/L |
| Amilasa~ | 22,5 U/L | Sin dato | Sin dato | Sin dato |
| Colesterol total | 175 mg/dL | Sin dato | Sin dato | 172 mg/dL |
| Triglicéridos | 167 mg/dL | Sin dato | Sin dato | 180 mg/dL |
| GGT | 109 U/L | 95 U/L | Sin dato | 60 U/L |
| Bilirrubina total | 10,8 mg/dL | 2,90 mg/dL | Sin dato | 2,0 mg/dL |
| Bilirrubina directa | 6,7 mg/dL | 0,00 mg/dL | Sin dato | 1,2 mg/dL |
| Bilirrubina indirecta | 4,1 mg/dL | 1,10 mg/dL | Sin dato | 0,8 mg/dL |
| Glicemia | 88 mg/dL | 110 mg/dL | Sin dato | Sin dato |
| Creatinina | 0,69 mg/dL | Sin dato | Sin dato | Sin dato |
| ALT | 1160 U/L | 987 U/L | 574 U/L | 272 U/L |
| AST | 786 U/L | 780 U/L | 513 U/L | 180 U/L |
| TP | 15,8 s | 16,7 s | 13 s | Sin dato |
| TPT | 65 s | 31 s | 31 s | Sin dato |
| Leucocitos | 8,555 10³/μL | Sin dato | Sin dato | 6,700 10³/μL |
| Hb | 14,6 g/dL | Sin dato | Sin dato | 12 g/dL |
| Hto | 43,4% | Sin dato | Sin dato | 40,2% |
| Plaquetas | 130 10³/μL | Sin dato | Sin dato | 150 10³/μL |
| *Hepatitis B y C negativo Antígeno carcinoma embrionario CA 19 negativo Ac antimúsculo liso negativo | VIH - serología negativa | CMV IgG- IgM negativo | Epstein-Barr IgG-IgM negativo | Ac antinucleares, mitocondriales y microsomales negativo |
~No se dispone de seguimiento de amilasa dado que no se contaba con reactivo en la institución. *Las pruebas para hepatitis B y C (además de la última fila) fueron reportadas en la historia clínica como no reactivas sin parámetro numérico, no es posible acceder a su valor dada la realización externa por la aseguradora del paciente y por el reporte institucional cualitativo. Ac: anticuerpos; ALT: alanina-aminotransferasa; AST: aspartato-aminotransferasa; CA: cáncer; CMV: citomegalovirus; GGT: gamma-glutamil transferasa; Hb: hemoglobina; Hto: hematocrito; IgG: inmunoglobulina G; IgM: inmunoglobulina M; TP: tiempo de protrombina; TPT: tiempo de tromboplastina parcial; VIH: virus de la inmunodeficiencia humana. Fuente: Laboratorio clínico HUDN (Hospital Universitario Departamental de Nariño).
Para el caso en mención, se consideraron como diagnósticos diferenciales, entre los más relevantes, a la hepatitis autoinmune, lesiones derivadas de plaguicidas (descartadas por antecedentes y clínica), virus hepatotropos, hepatitis alcohólica y patología biliar.
El estudio del caso inició con una ecografía de cuello en la que se evalúo el nódulo mandibular y se detectó como hallazgo incidental un nódulo tiroideo derecho subcéntrico, acompañado de adenomegalias redondeadas en la región submandibular derecha con pérdida de la relación corteza-médula sospechosas. A continuación se solicitaron estudios para virus hepatotropos y otros, los cuales fueron negativos. Se realizó una biopsia por aspiración con aguja fina (BACAF) del nódulo submandibular que evidenció atipia indeterminada de células linfoides. Con estos resultados se decidió un tratamiento con vitamina K (10 mg intravenoso/día), hidratación (lactato de Ringer) y antibióticos (ampicilina/sulbactam 3 g intravenoso cada 6 horas).
Posteriormente, en la ecografía de hígado y vías biliares se describió esteatosis hepática, colecistitis y barro biliar; por esto, cirugía valoró y solicitó tomografía abdominal (Figura 1) y colangiorresonancia (Figura 2). Al persistir la hiperbilirrubinemia a expensas de la directa, gastroenterología evaluó y realizó una colangiopancreatografía retrógrada endoscópica (CPRE) que reportó papila de Váter en la segunda porción duodenal plana, ingreso selectivo a la vía biliar con papilótomo de arco más guía hidrofílica, colangiografía en la que se contrastó la vía biliar de calibre normal sin cálculos, exploración de la vía biliar con canastilla de Dormia y extracción de barro biliar y bilis retenida, y lavado de vía biliar hasta el drenaje de bilis clara.
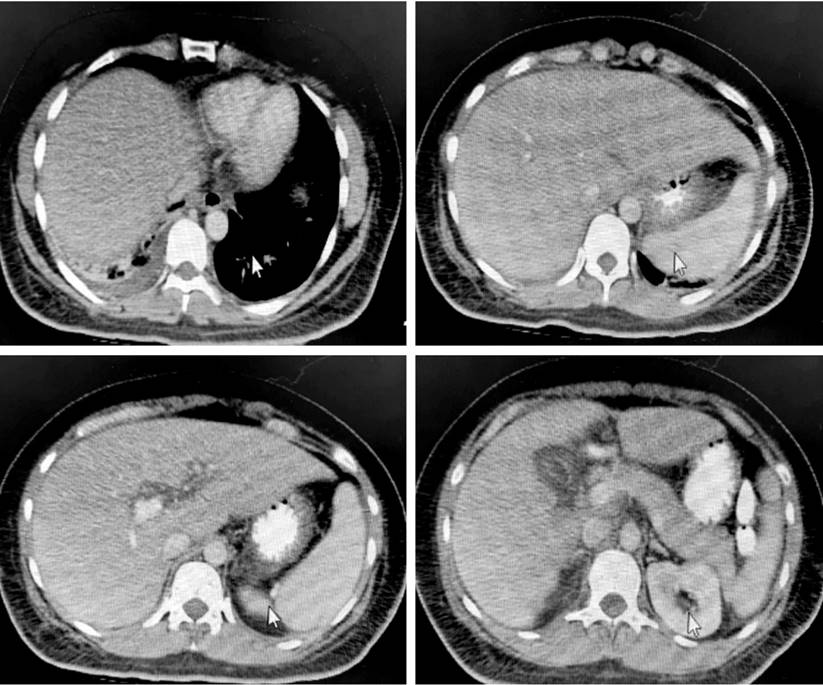
Figura 1 Tomografía axial computarizada (TAC) de abdomen de la paciente. Derrame pleural laminar derecho con atelectasias subsegmentarias. Esteatosis hepática difusa sin lesiones focales. Hallazgos descritos a nivel pancreático que sugieren proceso edematoso intersticial Balthazar C. Índice de gravedad 2. Imagen nodular hipodensa renal derecha compatible con quiste. Liquido laminar intraabdominal. Cortesía del departamento de radiología HUDN.
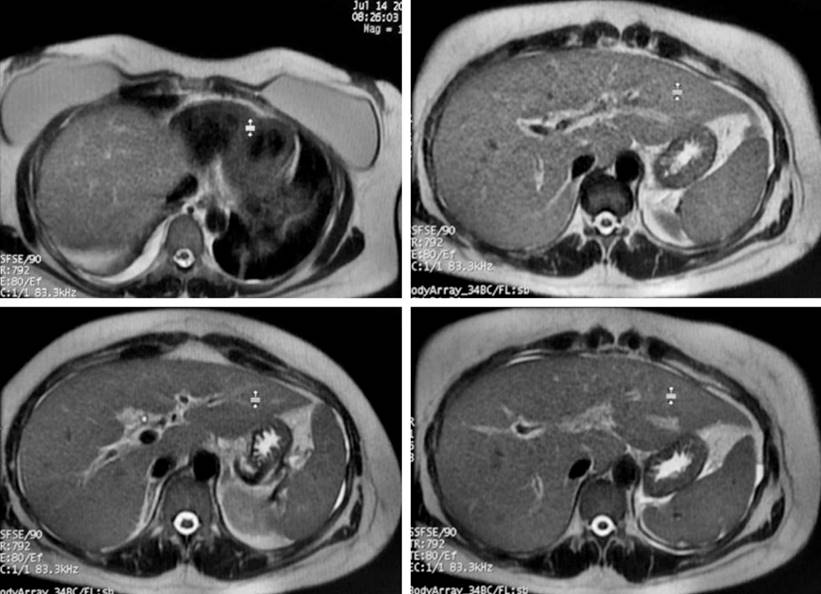
Figura 2 Colangiorresonancia de la paciente. Edema de las paredes de la vesícula y barro biliar en su interior sin observar cálculos en la luz vesicular ni en la vía biliar que originen obstrucción. Líquido libre en el espacio de Morrison y gotera parietocólica derecha. Líquido libre en la base pulmonar derecha. Hepatomegalia leve. Cortesía del departamento de radiología HUDN.
La paciente padeció una patología hepática no obstructiva, con vía biliar sin cálculos, y evolucionó de modo favorable por estar asintomática, con estabilidad hemodinámica, con descenso en los valores de paraclínicos de control (en específico, bilirrubinas y transaminasas), sin proceso infeccioso evidente y con resolución de la adenopatía mandibular.
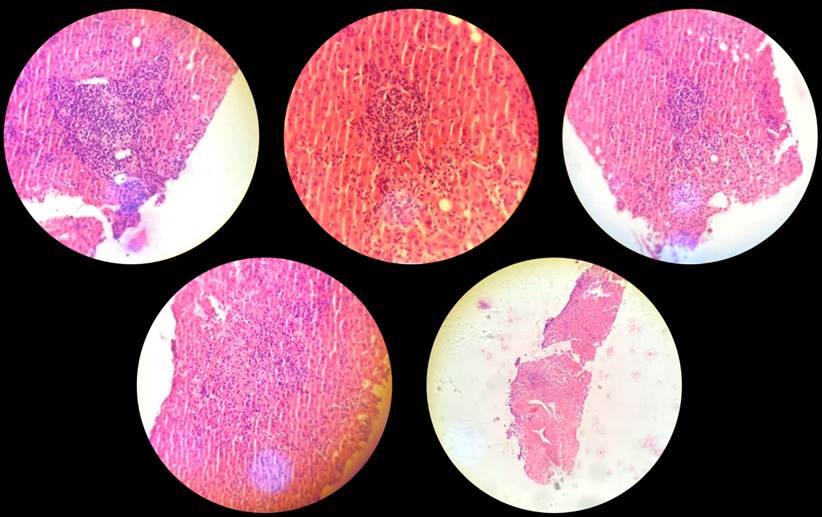
Finalmente, se realizó una biopsia hepática (Figura 3), cuyo diagnóstico histopatológico señaló un proceso inflamatorio de células de línea blanca compatible con un patrón de hepatitis aguda con necrosis pericentral y hepatocitos apoptóticos. Es de anotar que la evolución clínica de la paciente hacia la mejoría con total recuperación se evidencia secundaria a la suspensión de la medicación de nimesulida y del suplemento dietético, con controles de función hepática y transaminasas dentro de los parámetros normales a los 30 días posteriores al egreso; esto, en conjunto con la biopsia hepática, indica que el origen del proceso patológico fue el inducido por medicamentos.
Discusión
La hepatitis toxica tiene etiologías diversas, entre ellas el consumo de medicamentos o xenobióticos como inmunosupresores, antituberculosos, antibióticos y AINE10. Los analgésicos abarcan la mayor parte de los casos relacionados con efectos adversos hepáticos por fármacos10. En efecto, hasta el 15% de los pacientes que emplean AINE experimentan al menos una elevación transitoria de las transaminasas11. Los factores de riesgo relacionados con el desarrollo de lesiones hepáticas por medicamentos son edad avanzada (60 a 70 años de edad), sexo femenino, enfermedad hepática previa y polimorfismo genético de las vías del metabolismo de fármacos según la etnia5,8.
Así mismo, el uso de los suplementos dietéticos y herbales ha aumentado con un consecuente impacto como causa de daño hepático12. Por ejemplo, los productos Herbalife® se asocian con diversos grados de daño hepático, desde mínimos cambios hasta hepatitis fulminante que requiere trasplante13. Los suplementos herbales y dietéticos engloban muchos ingredientes como vitaminas, minerales, proteínas, hierbas y otros productos botánicos13,14. En específico, la información nutricional del conjunto de compuestos describe una mezcla de minerales (citrato de calcio, óxido de magnesio, fumarato ferroso, selenito de sodio, óxido de zinc, carbonato de manganeso, cloruro de cromo [III], yoduro de potasio, citrato cúprico), fosfato potásico, antiaglomerante (dióxido de silicio) y productos botánicos (hongo shiitake, hoja de té verde, hoja de té oolong, hoja de té negro, cáscara de granada, perejil, diente de león, extracto de cardo mariano, Echinacea purpurea, Echinacea angustifolia, Astragalus, Schisandra)15.
Aunque estas sustancias parecen ser naturales y seguras, existe controversia sobre su seguridad por la escasa evidencia disponible sobre su eficacia y toxicidad14. La hepatotoxicidad secundaria a productos herbales se origina con mayor frecuencia por una reacción idiosincrática que por daño tóxico13.
Publicaciones recientes informan sobre casos de toxicidad por suplementos herbales en Asia (dada la medicina tradicional china), América (incluidos Estados Unidos y Latinoamérica) y Europa (como en España, Islandia y Francia)14,16. En concreto, los productos Herbalife® contienen como agentes sospechosos de hepatotoxicidad el extracto de té verde, ginkgo y palma enana americana12. Todavía más, el mecanismo predominante de daño hepático por estos es el hepatocelular, seguido del mixto, entre otros12,13,16. En cuanto a la gravedad del daño hepático por suplementos herbales, esta varía de leve a grave e incluso con casos de cirrosis e insuficiencia hepática que requieren trasplante hepático13.
Los suplementos herbales y dietéticos provocan la activación metabólica mediada por el complejo citocromo P450 hepático o por bacterias intestinales; dicha activación produce metabolitos tóxicos que se unen al glutatión celular reducido y tales metabolitos forman aductos de proteína/ácido desoxirribonucleico (ADN) que pueden resultar tóxicos17.
Un estudio afirma que, entre los pacientes con insuficiencia hepática aguda, aquellos cuya etiología es la de suplementos herbales y dietéticos presentan mayor probabilidad de requerir trasplante hepático en comparación con los casos a causa de la prescripción de medicamentos18,19. El análisis de la toxicidad por Herbalife® es complejo debido a que podría contener componentes químicos no herbales adicionales que deben evaluarse como precursores de hepatotoxicidad20. A saber, la contaminación con Bacillus subtilis de productos de Herbalife® podría considerarse una causa potencial del perfil de hepatotoxicidad de dicho suplemento herbal18.
En lo que concierne a la nimesulida, su empleo se relaciona con una mayor frecuencia de hepatotoxicidad al compararse con otros AINE21,22. De hecho, en un estudio integrativo, alrededor del 45% de los pacientes con reacción adversa hepática por nimesulida requirieron trasplante hepático o fallecieron por insuficiencia hepática fulminante21; además, la latencia de toxicidad hepática por nimesulida puede ocurrir en períodos de 90 días a 6 meses8. La mayoría de los pacientes con hepatotoxicidad por nimesulida son mujeres, presentan ictericia y son de edad avanzada acorde a estudios recientes8,21 y en concordancia con la situación expuesta en este reporte.
El mecanismo de daño hepático por nimesulida es deconocido y no se han realizado estudios de asociación genética al respecto a la fecha8. Se ha propuesto la participación del sistema inmune adaptativo, la bioactivación con producción de estrés oxidativo por nitrorreductasas y la hipótesis metabólica idiosincrática como posibles mecanisos de hepatotoxicidad8.
Ahora bien, se requieren más estudios que evalúen el riesgo de hepatotoxicidad específica por nimesulida según determinadas características como edad, sexo, dosis del medicamento y duración del tratamiento21. Además, es importante considerar que al compartir algunas vías entre medicamentos y xenobióticos se podría potencializar el efecto hepatotóxico; por ejemplo, al igual que Herbalife®, la nimesulida presenta metabolismo por las isoenzimas citocromo P45017,22.
Con respecto a la biopsia hepática realizada a la paciente, esta reporta la presencia de infiltrado inflamatorio mononuclear y zonas de necrosis en el tejido hepático que, en conjunto con el contexto clínico, concluye que el diagnóstico histopatológico es de hepatitis aguda inducida por medicamentos. Se reconoce como limitación que no fue posible ampliar hallazgos que soporten con exactitud desde la patología el diagnóstico indicado; sin embargo, la elevación de ambas transaminasas junto a una relación ALT/AST de 1,4 a 1,5 permiten inferir que la afección hepática pudo ser mixta de predominio colestásico, de acuerdo con López-Gil y colaboradores23.
El análisis de este caso propone un posible mecanismo hepatotóxico sinérgico con el uso concomitante de nimesulida y suplemento dietético de Herbalife® dado que se descartaron otras causas posibles de hepatotoxicidad. A la fecha no se cuenta con estudios que evalúen un posible mecanismo conjunto de toxicidad hepática, como el evidenciado en este caso. De la misma forma, se pretende insistir en la regulación de la prescripción de medicamentos hepatotóxicos y del consumo de productos sin indicación médica a largo plazo, los cuales de forma sinérgica afectan órganos relacionados con el metabolismo y la excreción de xenobióticos.
Conclusión
El caso expuesto constituye un punto inicial en el avance hacia la investigación en hepatotoxicidad por mecanismos compartidos de diversas sustancias simultáneamente (vía compartida citocromo P450, por ejemplo), como lo sucedido a la paciente con el uso simultáneo de Herbalife® y de nimesulida.
Agradecimientos
A la paciente y a la institución de tercer nivel de complejidad de Pasto (Nariño). Al doctor Ronald Gilberto Bastidas Gustín, médico especialista en patología referente de la línea de cáncer del Instituto Departamental de Salud de Nariño, por la ampliación de lectura de biopsia hepática.
REFERENCIAS
1. Trefts E, Gannon M, Wasserman DH. The liver. Curr Biol. 2017;27(21):R1147-R1151.https://doi.org/10.1016/j.cub.2017.09.019 [ Links ]
2. Woo S, Davis W, Aggarwal S, Clinton J, Kiparizoska S, Lewis J. Herbal and dietary supplement induced liver injury: Highlights from the recent literature. World J Hepatol. 2021;13(9):1019-1041. https://doi.org/10.4254/wjh.v13.i9.1019 [ Links ]
3. Bessone F, García-Cortés M, Medina-Caliz I, Hernandez N, Parana R, Mendizabal M, et al. Herbal and Dietary Supplements-Induced Liver Injury in Latin America: Experience From the LATINDILI Network. Clin Gastroenterol Hepatol. 2022;20(3):e548-e563. https://doi.org/10.1016/j.cgh.2021.01.011 [ Links ]
4. Garcia-Cortes M, Robles-Diaz M, Stephens C, Ortega-Alonso A, Lucena M, Andrade R. Drug induced liver injury: an update. Arch Toxicol. 2020;94(10):3381-3407. https://doi.org/10.1007/s00204-020-02885-1 [ Links ]
5. Bessone F, Hernandez N, Tagle M, Arrese M, Parana R, Méndez-Sánchez N, et al. Drug-induced liver injury: A management position paper from the Latin American Association for Study of the liver. Ann Hepatol. 2021;24:100321. https://doi.org/10.1016/j.aohep.2021.100321 [ Links ]
6. Andrade R, Chalasani N, Björnsson E, Suzuki A, Kullak-Ublick G, Watkins P, et al. Drug-induced liver injury. Nat Rev Dis Primers. 2019;5(1):58. https://doi.org/10.1038/s41572-019-0105-0 [ Links ]
7. Meunier L, Larrey D. Recent Advances in Hepatotoxicity of Non Steroidal Anti-Inflammatory Drugs. Ann Hepatol. 2018;17(2):187-191. https://doi.org/10.5604/01.3001.0010.8633 [ Links ]
8. Bessone F, Hernandez N, Mendizabal M, Ridruejo E, Gualano G, Fassio E, et al. Serious liver injury induced by Nimesulide: an international collaborative study. Arch Toxicol. 2021;95(4):1475-1487. https://doi.org/10.1007/s00204-021-03000-8 [ Links ]
9. Donati M, Conforti A, Lenti M, Capuano A, Bortolami O, Motola D, et al; DILI-IT Study Group. Risk of acute and serious liver injury associated to nimesulide and other NSAIDs: data from drug-induced liver injury case-control study in Italy. Br J Clin Pharmacol. 2016;82(1):238-48. https://doi.org/10.1111/bcp.12938 [ Links ]
10. Björnsson H, Björnsson E. Drug-induced liver injury: Pathogenesis, epidemiology, clinical features, and practical management. Eur J Intern Med. 2021;S0953-6205(21)00375-7. https://doi.org/10.1016/j.ejim.2021.10.035. [ Links ]
11. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases; 2012-. Nimesulide. [Updated 2016 Mar 1]. Available from: Available from: https://www.ncbi.nlm.nih.gov/books/NBK547948/ [ Links ]
12. Zheng E, Sandhu N, Navarro V. Drug-induced Liver Injury Secondary to Herbal and Dietary Supplements. Clin Liver Dis. 2020;24(1):141-155. https://doi.org/10.1016/j.cld.2019.09.009 [ Links ]
13. Jurčić D, Gabrić M, Troskot R, Liberati A, Mirat J, Včev A, et al. Herbalife® associated severe hepatotoxicity in a previously healthy woman. Acta Clin Croat. 2019;58(4):771-776. https://doi.org/10.20471/acc.2019.58.04.26 [ Links ]
14. Santos G, Gasca J, Parana R, Nunes V, Schinnoni M, Medina-Caliz I, et al. Profile of herbal and dietary supplements induced liver injury in Latin America: A systematic review of published reports. Phytother Res. 2021;35(1):6-19. https://doi.org/10.1002/ptr.6746 [ Links ]
15. LiverTox: Clinical and Research Information on Drug-Induced Liver Injury [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases; 2012-. Herbalife. [Updated 2018 Apr 11]. Available from: Available from: https://www.ncbi.nlm.nih.gov/books/NBK548447/ [ Links ]
16. Grewal P, Ahmad J. Severe liver injury due to herbal and dietary supplements and the role of liver transplantation. World J Gastroenterol. 2019;25(46):6704-6712. https://doi.org/10.3748/wjg.v25.i46.6704 [ Links ]
17. Wang Y, Li W, Xia S, Guo L, Miao Y, Zhang B. Metabolic Activation of the Toxic Natural Products From Herbal and Dietary Supplements Leading to Toxicities. Front Pharmacol. 2021;12:758468. https://doi.org/10.3389/fphar.2021.758468 [ Links ]
18. de Boer YS, Sherker A. Herbal and Dietary Supplement-Induced Liver Injury. Clin Liver Dis. 2017;21(1):135-149. https://doi.org/10.1016/j.cld.2016.08.010 [ Links ]
19. Hillman L, Gottfried M, Whitsett M, Rakela J, Schilsky M, Lee W, et al. Clinical Features and Outcomes of Complementary and Alternative Medicine Induced Acute Liver Failure and Injury. Am J Gastroenterol. 2016;111(7):958-965. https://doi.org/10.1038/ajg.2016.114 [ Links ]
20. Ballotin V, Bigarella L, Brandão A, Balbinot R, Balbinot S, Soldera J. Herb-induced liver injury: Systematic review and meta-analysis. World J Clin Cases. 2021;9(20):5490-5513. https://doi.org/10.12998/wjcc.v9.i20.5490 [ Links ]
21. Kwon J, Kim S, Yoo H, Lee E. Nimesulide-induced hepatotoxicity: A systematic review and meta-analysis. PLoS One. 2019;14(1):e0209264. https://doi.org/10.1371/journal.pone.0209264 [ Links ]
22. Zhou L, Pang X, Xie C, Zhong D, Chen X. Chemical and Enzymatic Transformations of Nimesulide to GSH Conjugates through Reductive and Oxidative Mechanisms. Chem Res Toxicol. 2015;28(12):2267-77. https://doi.org/10.1021/acs.chemrestox.5b00290 [ Links ]
23. López-Gil S, Nuño-Lámbarri N, Chávez-Tapia N, Uribe M, Barbero-Becerra VJ. Liver toxicity mechanisms of herbs commonly used in Latin America. Drug Metab Rev. 2017;49(3):338-356. https://doi.org/10.1080/03602532.2017.1335750 [ Links ]
Citación:
3Yalila Andrea Ordóñez-Zarama YA, Muñoz-Delgado ER, Ruiz-Ruiz JA, José Alirio Risueño-Blanco JA. Diagnóstico de un caso de hepatotoxicidad por fármacos y suplementos herbales en un hospital de Pasto, Colombia. Revista. colomb. Gastroenterol. 2023;38(1):65-72. https://doi.org/10.22516/25007440.866
Recibido: 27 de Diciembre de 2021; Aprobado: 08 de Septiembre de 2022











 text in
text in