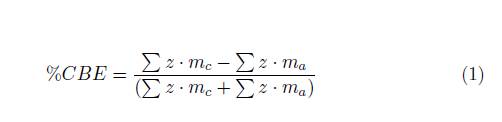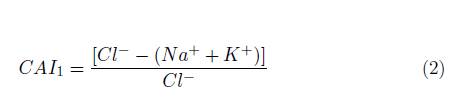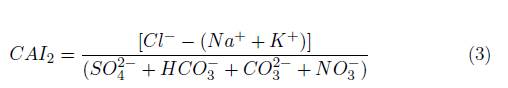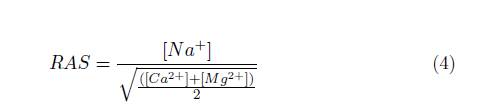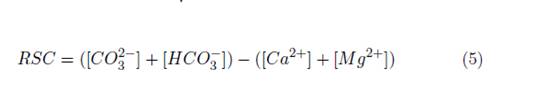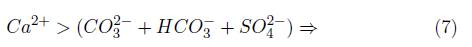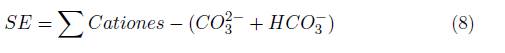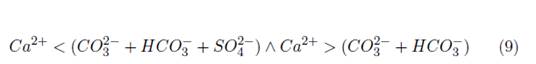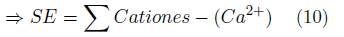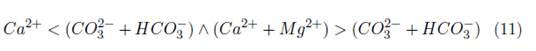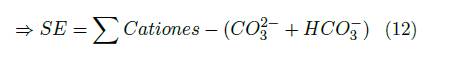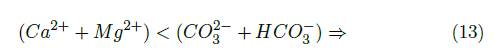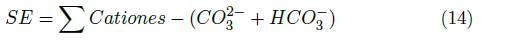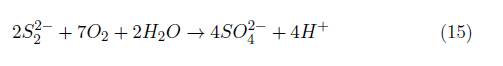1 Introducción
El acceso libre y seguro del agua es esencial para el mantenimiento del valor ecológico en el planeta y para la subsistencia de la vida [1],[2],[3], razón por la cual, su calidad debe encontrarse dentro de los estándares propuestos para su uso. Dado el crecimiento de la población y el correspondiente desarrollo de actividades agropecuarias, ganaderas, industriales, domésticas y, en particular, en sectores rurales de países latinoamericanos, tales como Colombia, donde se evidencia la ausencia de acueductos y redes de distribución en adecuadas condiciones de operación [4], se ha recurrido a la extracción de agua subterránea, considerada por presentar menor contaminación por su limitado contacto con las actividades que se desarrollan en la superficie y el proceso de filtración natural durante su percolación [2].
No obstante, el incremento de la demanda, su extracción, consumo y la limitada oferta del recurso, ha generado un desequilibrio insostenible [1], agravado por el detrimento de su calidad, la cual no solo depende de factores naturales, sino de las actividades antrópicas que han generado efecto sobre el ciclo hidrológico, alterando este frágil sistema [5], por ejemplo: la lixiviación a través de la zona no saturada de contaminantes originados por derrames accidentales, fugas o aplicación inapropiada de sustancias químicas en la superficie del suelo, entre otras [6]. Ante esta problemática, se hace necesario determinar las condiciones de calidad y evolución hidroquímica, buscando generar información que haga evidente los impactos generados por la actividad antrópica, y sirvan para la adecuada planeación y uso sostenible, en pro de prevenir y evitar riesgos a la salud de los asentamientos humanos que hacen uso de este recurso.
En el presente documento, se muestran los resultados del estudio hidroquímico del acuífero del Neógeno - Cuaternario, enmarcado por la cuenca del Río Chicú, cuya localización se encuentra al noroeste de la ciudad de Bogotá D.C., Colombia. En trabajos antecedentes sobre el área, realizados por el Servicio Geológico Colombiano (1990) se señala que el agua subterránea extraída reúne características de impotabilidad por presentar altas concentraciones de iones en solución [7]. Además en un segundo estudio realizado por la Corporación Autónoma Regional de Cundinamarca (2008), concluye que el agua subterránea extraída presenta una tendencia iónica bicarbonatada sódica o cálcica, y valores medios de DBO entre 5.7 - 8.6 mg O 2/L y DQO entre 21.7 - 41.7 mg O 2/L [8].
Para entender adecuadamente los procesos hidroquímicos que gobiernan la calidad del agua subterránea, una variedad de métodos estadísticos han sido aplicados para el análisis de datos hidroquímicos, tales como los métodos estadísticos multivariantes [5],[9],[10],[11], entre los que se encuentran el análisis de conglomerados (CA), análisis de varianza (ANOVA) y análisis de componentes principales/análisis de factores (ACP/AF), que permiten analizar conjuntos de datos sin perder información, con el objetivo de verificar la existencia de variaciones espaciales y temporales importantes, así como la interdependiencia entre las variables [6],[12]. En este estudio se analizaron los procesos de interacción roca - agua y la calidad del agua subterránea extraída de la cuenca del Río Chicú, por medio de análisis descriptivos, y de igual manera se llevó a cabo un análisis de componentes principales (ACP) para reducir la dimensionalidad del conjunto de datos analizado, con el fin de explicar la correlación existente entre las variables determinadas [5]. Se propone en el presente documento: [1] comparar las muestras de agua extraídas en la cuenca del Rio Chicú, usando métodos gráficos convencionales, indicadores hidroquímicos y análisis de componentes principales (ACP) para trazar su evolución hidrogeoquímica en la cuenca estudiada; [2] comparar las variables fisicoquímicas determinadas en las muestras de agua subterránea, con la normatividad Colombiana de Calidad para consumo humano y para irrigación.
2 Materiales y métodos
2.1 Área de estudio
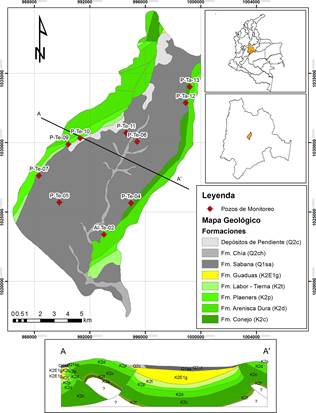
La cuenca hidrográfica del Rio Chicú se encuentra localizada sobre los municipios de Tabio y Tenjo, ubicados en el departamento de Cundinamarca, Colombia [13], con una altura entre los 2510 msnm y 3140 msnm [Figura 1.). Económicamente es un agro - ecosistema de tendencia ecoturística y de economía manufacturera [14], donde se produce mayoritariamente papa, flores y otros productos como hortalizas y cebada, así mismo, existen actividades relacionadas con la ganadería lechera y el cultivo de pastos.
Geográficamente, se encuentra limitada al este por la Serranía de Cota- Chía y al oeste por la Serranía de Tabio-Tenjo, que conforman la zona montañosa que bordea el valle intramontano, extenso y plano, localizado en el centro de la cuenca [7],[13], [15],[16],[17].
El clima se caracteriza por ser frio semihúmedo (FsH), según la clasificación de Caldas-Lang, con valores de temperatura medios mensuales de 13.7 ± 0.2 ◦ C y una precipitación media anual de 749.7 ± 156.8 mm de comportamiento bimodal, con periodos de exceso hídrico en los meses de abril - mayo y octubre - noviembre [13],[17].
2.2 Geología e hidrogeología
Se presentan dos grandes zonas geológicas: la zona exterior conformada por rocas de edad cretácica (formaciones Conejo, Arenisca Dura, Plaeners y Labor y Tierna) y edad terciaria (formación Guaduas), conformadas por areniscas grises o amarillentas, con intercalaciones de arcillolitas, liditas, o limolitas, entre otras [7],[18], y en algunos sectores presencia de minerales ricos en sulfuro, tales como la pirita; y calcio, tales como calizas, entre otras [18],[19]; y la zona interior, que corresponde al valle intramontano de origen lacustre, compuesto por depósitos no consolidados arcillosos con intercalaciones lenticulares de arenas finas y niveles delgados de gravas y turbas y localmente limos, áreas fangosas y arcillas orgánicas diatomíticas [18], correspondientes a las Fm. Sabana, Fm. Chía y depósitos de pendiente, que conforman el acuífero libre a confinado del Neógeno - Cuaternario [13] [Figura 1].
Tabla 1 Características hidrogeológicas de la Cuenca del Río Chicú
| Formación | Espesor (m) | Caracteristicas Hidrogeologicas | ||||
| Clas | T (m2/día) | K (m/día) | S | Q (L/s) | ||
| Depositos Coluviales | 1-12a,c | D | N.D. | N.D. | N.D. | N.D. |
| Formacion Chia | 2-15a,c; <30b | B | N.D. | N.D. | N.D. | N.D. |
| Formacion Sabana | <200a,c; <500b | B | 5-20a; 7.3-52.45b | 0.4-4.5a; 0.11-3.5b | 5:5x10-3- 4:5x10-5 a; (1:3 - 2:8) x10-3 b | <1a; 0.03-0.8b |
| Formacion Guaduas | 150-500a; 600b | C | 2.3-20.4b | N.D. | (1:16 - 7:2)x10-3 b | 1.6-4b |
| Formacion Labor -Tierna | 100a,c; 220b | A | 50-270a; 16.24-360b | 1-3.5a; 1 - 8b | 5x10-4 a; 5:9x10-3 - 2:5x10-4 b | 3-15a; 2-30b |
| Formacion Plaeners | 120a,c; 60b | C | 9.6b (D.P.) | 0.3b (D.P.) | N.D. | 2-14b |
| Formacion Arenisca Dura | 350a; 400b | A | 15-60a; 22-356b | 0.3-1a; 0.8b | 5x10-4 a | 7-20a; 2-14b |
| Formacion Chipaque | >400a; 130b | D | N.D. | N.D. | N.D. | N.D. |
T: Transmisividad; K: Conductividad Hidraulica; S: Coeficiente de Almacenamiento; Q: Caudal de Extraccion; Clas: Clasificacion; A: Rocas porosas/fracturadas con gran a moderada importancia hidrogeologica; B: Sedimentos no consolidados con moderada importancia hidrogeologica; C: Rocas porosas/fracturadas con poca importancia hidrogeologica; D: Sedimentos y rocas porosas/fracturadas sin importancia hidrogeologica; N.D.: Dato no reportado; D.P.: Dato Puntual
Fuente: a(7), b(20), c(8).
Acorde a la litología, el grado de fracturamiento de las rocas, la capacidad específica, conductividad hidráulica, entre otros aspectos, las formaciones geológicas presentes en el área de estudio se dividen en las unidades hidrogeológicas [Tabla 1] [7],[13]: rocas porosas/fracturadas con gran a moderada importancia hidrogeológica, integradas por la Fm. Arenisca Dura y la Fm. Labor y Tierna; sedimentos no consolidados con moderada importancia hidrogeológica conformados por la Fm. Sabana y la Fm. Chía; rocas porosas/fracturadas con poca importancia hidrogeológica, compuesto por la Fm. Guaduas, la Fm. Plaeners y por último, se encuentran los sedimentos y rocas porosas/fracturadas sin importancia hidrogeológica, conformados por los depósitos Coluviales y Cuaternarios sin diferenciar, y la Fm. Chipaque.
2.3 Muestreo y Análisis de Datos
Tabla 2 Ubicación y altura de los puntos de muestreo
| Punto de Muestreo | X | Y | Altura |
| msnm | |||
| Al-Te-02 | 993029.6 | 1023371.2 | 2600.7 |
| P-Te-04 | 994977.3 | 1025644.2 | 2606.6 |
| P-Te-05 | 989812.9 | 1025693.9 | 2559.4 |
| P-Te-06 | 995418.3 | 1030070.5 | 2592.4 |
| P-Te-07 | 988337.2 | 1027620.1 | 2587.2 |
| P-Te-09 | 990457.5 | 1029877.5 | 2602.2 |
| P-Te-10 | 991311.0 | 1030319.7 | 2619.2 |
| P-Te-11 | 994629.5 | 1030706.4 | 2585.3 |
| P-Te-12 | 998921.7 | 1032874.9 | 2580.4 |
| P-Te-13 | 999211.4 | 1034023.7 | 2603.3 |
Fuente: elaboración propia
La recolección de muestras fue realizada en diez [10] puntos que extraen agua del acuífero, de los cuales 9 eran pozos de extracción y el décimo un [1] aljibe [Tabla 2]. Estos puntos fueron seleccionados, buscando capturar la variación espacial de la calidad del agua subterránea en el área estudiada [Figura 1]. Los muestreos se realizaron en el segundo semestre del año 2014, el primero en meses con reducción en la precipitación (Julio - M 1) y el segundo en meses de exceso hídrico (Octubre - M 2). Previo a la toma de las muestras, se procedió a desalojar por 45 min aproximadamente el agua presente dentro del punto de extracción. Las muestras fueron conservadas en recipientes color ámbar previamente purgados, refrigerados a 4 ◦ C en oscuridad, y trasportadas al laboratorio para su posterior análisis.
A la totalidad de las muestras se analizó in situ temperatura (T ) y pH, y en laboratorio, los iones mayoritarios (calcio (Ca 2+), magnesio (Mg 2+), sodio (Na +), potasio (K+) , bicarbonato (HCO3−), carbonato (CO 2− ), sulfato (SO 2− ), cloruro (Cl − ) y nitrato (NO − )). Adicionalmente se cuantificó la presencia de hierro total (Fe T ), plomo total (Pb T ) y cobre total (Cu T ). El pH fue determinado usando un pH-metro (Rocker pH5011). Los elementos metálicos se analizaron por medio de espectrofotometría de absorción atómica de llama (Perkin Elmer 2380 Atomic), siguiendo el método 3111 Metals by Flame Atomic Absorption Spectrometry CC [21]. El HCO3−y CO 2− , fueron determinados por titrimetría, usando ácido sulfúrico (H 2 SO 4(0.010mol/L)), siguiendo el método 2320 B [21]. El SO 2− , fue analizado mediante gravimetría usando Cloruro de Bario (BaCl 2 H 2 O (10 %m/v)) como agente precipitante e indicador rojo de metilo, siguiendo el método 4500-SO 2− Sulfate B [21]. El análisis de Cl − se efectuó por potenciometría de ion selectivo (Electrodo Ión Cloro Orión 94-17B), siguiendo el método 4500-Cl − Chloride C [21] y finalmente, el N NO3 se analizó mediante espectrofotometría UV/VIS (Hitachi U-1800 UV/VIS Spectrophotometer), utilizando radiación ultravioleta a la longitud de onda de 220 nm y realizando una corrección de la absorbancia a 275 nm, siguiendo el estándar 4500-NO3− Nitrogen B [21]. Los valores de STD consignados se obtuvieron como la suma de la concentración de aniones y cationes analizados, expresados en mg/L [22].
2.4 Balance iónico
Para validar los resultados obtenidos, se realizó el balance iónico tradicional ( % CBE, por sus siglas en inglés: percent charge-balance error) basado en la diferencia entre las cargas totales positivas y las cargas totales negativas expresado en unidades de porcentaje [23],[24]. El nivel de error de los datos fue calculado usando la siguiente ecuación [1] [25]:
Dónde: z es el valor absoluto de la carga del ion; m c y m a son las concentraciones en meq g/L de las especies catiónicas y aniónicas respectivamente. El criterio para la aceptación de los datos analíticos fue de ±10 %, debido a la utilización de diversas técnicas para la determinación de los numerosos parámetros analizados, las cuales traen consigo un aumento en la incertidumbre del análisis y en la precisión de los datos obtenidos en el mismo. Acorde al %CBE, la totalidad de las muestras de agua para los dos periodos de muestreo se encontraban dentro de este rango.
2.5 Análisis de datos
Se determinaron los parámetros estadísticos descriptivos (media, desviación estándar, rango, entre otros), para cada variable hidroquímica obtenida, con el supuesto que estos datos son espacialmente independientes. Este proceso se realizó usando el software R [26], y el paquete Psych [27]. Adicionalmente, aceptando la hipótesis que la composición química del agua subterránea refleja la composición mineralógica de las rocas en el acuífero [28], se realizó el análisis de las facies hidroquímicas del agua subterránea presente en el acuífero estudiado.
2.5.1 Relaciones iónicas
Se determinaron las relaciones iónicas existentes entre las variables analizadas para cada pozo, al comparar diferentes masas de agua y trazar la evolución hidrogeoquímica del agua subterránea [13]. Como primera aproximación se generó la correlación estadística entre los iones mayoritarios y minoritarios analizados, usando el coeficiente de Pearson, y posteriormente, las relaciones entre (Ca 2+ + Mg 2+) (HCO3− + SO 2− ) y (Na ++K +) Cl − fueron analizadas, buscando determinar la existencia del proceso de intercambio catiónico en el sistema agua-sedimento [29],[30]. Adicionalmente se estimaron los índices cloro alcalinos (CAI) [2] y [3], para constatar las posibles reacciones de intercambio iónico [31],[30].
Para identificar la existencia de procesos de la meteorización presentes en la matriz arcillosa que conforma los sedimentos del acuífero, se analizó la relación entre los cationes mayoritarios (Na + , K + , Ca 2+ , Mg 2+) y el ion bicarbonato y entre los cationes mayoritarios y la suma de los iones bicarcarbonato y sulfato [30]. Para evaluar el rol de la disolución de los minerales de carbonato y sulfato en el sistema, se determinó la relación (Ca 2+ + Mg 2+) contra (HCO 3 - SO 2− ). Por último, se evaluaron los procesos de disolución de los minerales de carbonato y sulfato, y su mediación por la presencia de sus especies acidas correspondientes, el ácido carbónico (H 2 CO 3) y el ácido sulfúrico (H 2 SO 4).
2.5.2 Análisis de componentes principales
Para confirmar las tendencias evolutivas del agua subterránea identificadas a través de los indicadores hidroquímicos, se usaron los datos de cada parámetro fisicoquímico analizado, ajustados a la distribución normal por medio de su log- normalización, evaluando su homogeneidad mediante el test de Shapiro - Wilk. También, se usó el test de esfericidad de Bartlett para determinar si la matriz de datos es significativamente diferente de una matriz de identidad [32], es decir si las variables no se relacionan y, por lo tanto, son inadecuadas para la detección de estructuras [33]. Posteriormente, los datos fueron estandarizados a sus correspondientes z-scores. La estandarización de los datos es esencial para el análisis multivariante, debido que garantiza que la totalidad de los parámetros se encuentran cercanos en términos de sus varianzas [10]. El análisis de componentes principales (ACP) fue realizado mediante el programa R [26] y las librerías Psych [26] y Ade4 [34].
2.5.3 Comparación con normatividad colombiana e indicadores para riego
Los datos fisicoquímicos obtenidos, fueron comparados con los parámetros máximos permisibles del Agua para Consumo Humano señalados en el capítulo II de la Resolución 2115 de 2007 [35], de igual manera, con los criterios de calidad admisibles para la destinación del recurso para uso agrícola señalados en el literal 2.2.3.3.9.5. del Decreto único Reglamentario del Sector Ambiente y Desarrollo Sostenible 1076 de 2015 [36]. Acorde al Parágrafo 2 del presente Decreto, se aplicaron los indicadores: relación de absorción de sodio [4] [37], carbonato sódico residual [5] [37], porcentaje de sodio posible [6] [37] y la salinidad efectiva [7][9][11][13] [13], cuyas concentraciones están expresadas en meq − g/L.
3 Resultados y discusión
La Tabla 3, presenta los estadísticos sumarios de la concentración de variables hidroquímicas determinadas en la cuenca del Rio Chicú para los muestreos realizados. Los valores variables en la desviación estándar de algunos parámetros muestran que la concentración de estos, no presentan un comportamiento homogéneo a nivel espacial. Los valores de asimetría obtenidos, muestran que los parámetros analizados no se ajustan a una distribución normal, al presentar asimetrías positivas (γ 1 > 0) y asimetrías negativas (γ 1 < 0) [Figura 2].
Tabla 3 Concentración de los parámetros hidroquímicos en la Cuenca del Río Chicú
| Muestreo | M1 | M2 | ||||||||
| Parametro | X | σ | Max | Min | γ1 | X | σ | Max | Min | γ1 |
| pH | 6.4 | 0.6 | 7.0 | 5.0 | -1.4 | 6.1 | 0.5 | 6.9 | 5.1 | -0.9 |
| T (°C) | 16.9 | 1.3 | 19.0 | 15.0 | -0.2 | 18.7 | 1.1 | 20.0 | 16.0 | -2.1 |
| STD (mg/L) | 276.1 | 178.5 | 615.3 | 59.3 | 0.5 | 263.9 | 165.3 | 525.9 | 56.2 | 0.3 |
| Na+ (mg/L) | 48.2 | 51.8 | 157.8 | 5.7 | 1.3 | 33.5 | 31.7 | 107.3 | 3.6 | 1.5 |
| K+ (mg/L) | 11.8 | 17.8 | 60.6 | 1.3 | 2.8 | 11.7 | 17.6 | 60.6 | 1.5 | 2.9 |
| Ca2+ (mg/L) | 12.4 | 12.9 | 43.1 | 1.7 | 1.6 | 14.1 | 12.0 | 41.3 | 3.1 | 1.3 |
| Mg2+ (mg/L) | 3.1 | 1.6 | 6.3 | 0.9 | 0.6 | 3.6 | 3.6 | 14.5 | 1.3 | 2.8 |
| FeT (mg/L) | 7.4 | 5.2 | 17.3 | 1.1 | 1.2 | 12.3 | 7.6 | 24.6 | 3.3 | 0.3 |
| CuT (mg/L) | 0.7 | 0.1 | 0.8 | 0.5 | 0.6 | 0.6 | 0.1 | 0.9 | 0.5 | 1.3 |
| Alc (mg/L) | 122.9 | 94.0 | 290.0 | 20.0 | 0.5 | 117.1 | 94.0 | 276.7 | 20.0 | 0.5 |
| HCO- 3 (mg/L) | 149.9 | 114.7 | 353.8 | 24.4 | 0.5 | 142.9 | 114.7 | 337.5 | 24.4 | 0.5 |
| SO2- 4 (mg/L) | 41.7 | 32.0 | 120.8 | 11.0 | 1.9 | 43.0 | 31.0 | 120.8 | 8.2 | 1.9 |
| Cl- (mg/L) | 0.4 | 0.1 | 0.6 | 0.2 | 0.0 | 0.4 | 0.1 | 0.7 | 0.2 | 0.1 |
| N-NO- 3 (mg/L) | 0.4 | 0.4 | 1.6 | 0.4 | 3.1 | 1.7 | 1.5 | 4.5 | 0.9 | 0.6 |
| PbT (mg/L) | <0.5 | SD | SD | SD | SD | <0.5 | SD | SD | SD | SD |
| CBE (%) | 2.4 | 8.1 | 9.6 | -9.1 | -0.7 | -0.8 | 7.2 | 7.8 | -8.0 | 0.2 |
X: Media; σ: Desviación estándar de la muestra; γ1: coeficiente de asimetría de Fisher;
Max: Valor Máximo; Min: Valor Mínimo; SD: sin datos.
Fuente: elaboración propia.
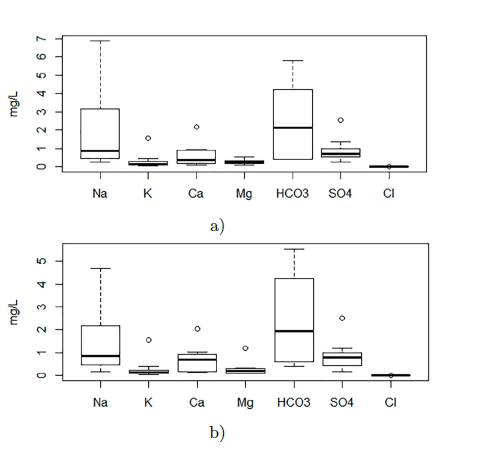
Figura 2 Box-plot: resultados de concentraciones de iones mayoritarios de muestras de agua de pozo extraída en el muestreo de a) julio de 2014 (M1); y b) octubre de 2014 (M2).
3.1 Facies hidroquímicas del acuífero
Al caracterizar hidroquímicamente las muestras de agua subterránea para los dos muestreos realizados [Figura 3], se evidencia que el acuífero estudiado presenta facies bicarbonatadas a sulfatadas sódicas o cálcicas según el caso. Con base en el diagrama de piper, se generaron cuatro grupos G1, G2, G3 y G4 con características hidroquímicas similares.
El grupo G1, conformado por el punto P-Te-10 en el muestreo M 1, se caracteriza por tener agua con facies hidroquímicas sulfatada sódico- cálcica, dado el proceso de recarga lateral de agua de recorrido intermedio proveniente de las rocas que conforman la zona exterior del acuífero, sobre el piedemonte de la Serranía Tabio - Tenjo [7],[13], y la limitada recarga de agua meteórica, debido al déficit hídrico que se genera en el mes de muestro [13],[17].
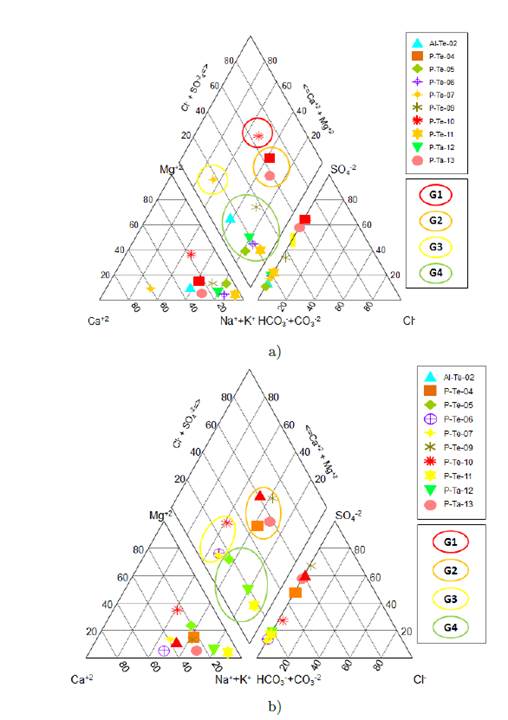
Figura 3 Diagrama de Piper para las muestras tomadas del Acuífero de Sedimentos Chía y Sabana, Cuenca del Río Chicú en a) julio de 2014 (M1); b) octubre de 2014 (M2).
El grupo G2, reúne puntos de muestreo con agua de facies hidroquímicas sulfatada sódica, dispersos a nivel espacial en áreas donde se presenta recarga lateral de aguas provenientes de las rocas del cretácico y actividades agrícolas intensivas, cuya composición química se encuentra enriquecida con iones sulfato, producto de la interacción y disolución de iones sulfuro (S 2− ) provenientes de minerales, tales como la pirita (FeS), cuyo origen fue en ambientes de deposición marinos someros o cercanos al continente, por reacción del ácido sulfhídrico (H 2 S), generado por la actividad bacteriana sobre la materia orgánica, con los compuestos ferrosos del agua marina [19], y su respectiva oxidación en iones sulfato por su interacción con aguas de recarga meteórica ricas en oxígeno disuelto [15], asimismo, por el uso el uso de fertilizantes inorgánicos ricos en iones sulfato, en especial en el muestreo M 2, dados los procesos de recarga generados, por el periodo de exceso hídrico que se produce la zona [13].
El grupo G3, agrupa puntos de muestreo con facies bicarbonatada cálcica, ubicados sobre las zonas potenciales de recarga, con agua de origen meteórico y corto tiempo de residencia en el acuífero, que encuentran su máxima representatividad en el muestreo M 2, dado el exceso hídrico que se produce en este mes de muestreo. Por último, el grupo G4, con facies hidroquímicas bicarbonatada sódica, se encuentran dispersos sobre la cuenca media y baja; el predominio del ion sodio se debe a los procesos de intercambio catiónico reverso que se producen entre los sedimentos arcillosos que proveen este ion y los iones calcio y magnesio presentes en el agua subterránea.
3.2 Relaciones iónicas
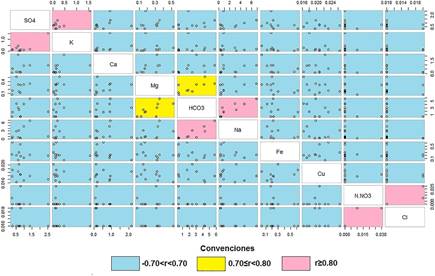
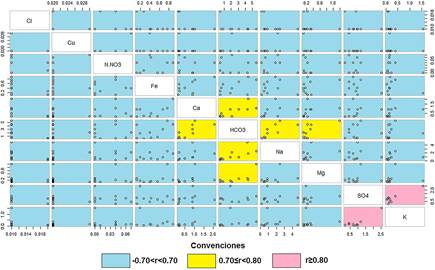
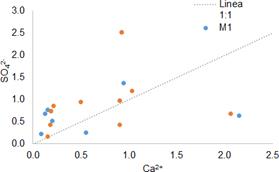
Como primera aproximación, se determinó [Figura 4 y Figura 5] la dependencia lineal entre las variables Na+ - HCO3- (rM1 = 0.89; rM2 = 0.74), K+ - SO2- 4 (rM1 = 0.84; rM2 = 0.89), N - NO3 - - Cl- ((rM1 = 0.87), Mg2+ - HCO3 - (rM1 = 0.71; rM2 = 0.71) y Ca2+ - HCO3 - (rM2 = 0.75), mostrando que la hidrogeoquímica de la zona estudiada es gobernada mayormente por los iones Na+, Mg2+, Ca2+, SO2− y HCO−, con presencia minoritaria de los iones Cl− y N − NO3−.
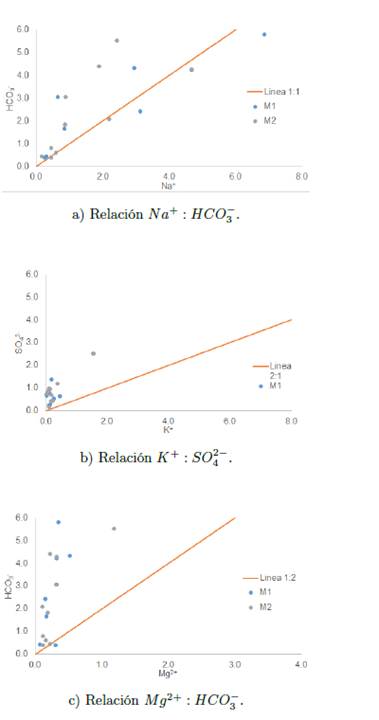
Al analizar las mayores correlaciones (r > 0.70), y comparándolas con las líneas de relación molar, generadas al asumir que la composición del agua es formada únicamente por la disolución de la sal pura correspondiente, lo cual queda representado por la relación molar de los iones N +: HCO3 - es 1:1; de K+: SO4 2− es 2:1 y de Mg2+: HCO− es 1:2. De la Figura 6, se evidencia una marcada tendencia de los datos a encontrase encima o debajo de sus respectivas equilineas, indicando la existencia de procesos adicionales a la disolución de sales que gobiernan la hidroquímica del acuífero estudiado, tales como el enriquecimiento de iones sodio y magnesio, aludida al intercambio catiónico que se produce en la matriz mineral de carácter arcilloso con intercalaciones lenticulares de arenas y gravas que conforman los sedimentos del acuífero [7],[20].
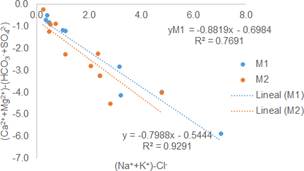
Para evaluar el posible rol del intercambio catiónico en la hidroquímica del agua subterránea, se determinó la relación entre (Ca 2+ + Mg 2+) + SO 2− ) - (HCO3 -+ SO2- 4)y (Na + + K +) - Cl − [Figura 7]; el primer indicador, ubicado en el eje de las ordenadas, provee la suma de los cationes calcio y magnesio de fuentes distintas que sus respectivos bicarbonatos y sulfatos; el segundo indicador ubicado en el eje de las abscisas, provee la concentración total de cationes potasio y sodio de otras fuentes que sus respectivos cloruros en el sistema [13]. Si el intercambio catiónico implica el ion sodio y los otros cationes mayoritarios que se encuentran en el sistema, se espera una línea de pendiente aproximada -1. En ausencia de estas reacciones en cantidades significativas para influenciar la hidroquímica del acuífero, todos los puntos se encontrarán graficados cerca del origen [10],[29].
Con base en las pendientes obtenidas a través de las líneas de tendencia (m M 1 = -0.88; m M 2 = -0.798), se evidencian valores cercanos a -1, lo cual implica un incremento en la concentración de iones Na + y K + y una reducción en la concentración de los iones Ca 2+ y Mg 2+, dada la existencia de un proceso de intercambio catiónico en el sistema [Figura 7].
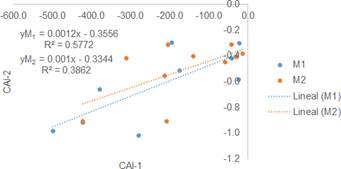
Para constatar las posibles reacciones de intercambio iónico que toman lugar en el sistema, fueron usados los índices cloro alcalinos (CAI): cuando el intercambio catiónico ocurre entre Ca 2+ y Mg 2+ en la roca huésped y Na + y K + en el agua, ambos indicadores se espera que sean positivos. Por otro lado, si ambos índices son negativos, este comportamiento indica un intercambio catiónico reverso [31],[10]. Con base en la Figura 8, se encuentra que la totalidad de las muestras presenta valores negativos de los dos índices, sugiriendo que se produce el intercambio catiónico reverso en el sistema.
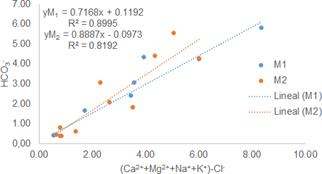
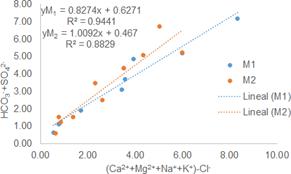
Por otro lado, analizando la presencia de los aniones mayoritarios, al graficar la relación entre la suma de los cationes mayoritarios obtenidos por disolución de minerales diferentes a los cloruros contra el ion bicarbonato Figura 10 y contra la suma de los iones bicarbonato y sulfato [Figura 9] se determina la relación (r2 M1> 0.89; r2 M2> 0.81) entorno a los procesos de meteorización de minerales, los cuales favorecen la presencia y disolución de minerales de carbonato y sulfato, que conforma los sedimentos del acuífero estudiado.
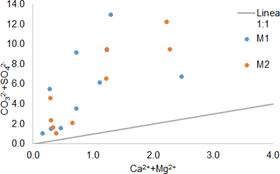
Al analizar el rol de la disolución de los minerales de carbonato y sulfato en el sistema, se realizó la gráfica del (Ca 2+ + Mg 2+) contra (CO 2− + SO 2− ), entendiendo que la relación estequiométrica entre los iones HCO 3 - y CO3 2- en meq -g es de 2:1, y que los puntos que están a lo largo o cerca de la línea de relación molar 1:1 son atribuidos a la meteorización de los minerales de carbonato y sulfato; los puntos que caen debajo de la equilínea son considerados como resultado de la disolución de carbonatos o sulfatos y los valores por encima son producto del intercambio catiónico y la meteorización de los minerales de silicato [10], tales como las arcillas orgánicas diatomíticas.
En la Figura 11, se observa que la totalidad de los puntos de muestreo se encuentan sobre la equilínea, permitiendo confirmar que el intecambio catiónico y la meteorización de los silicatos, son los procesos que rigen la hidroquímica del acuifero objeto de estudio.
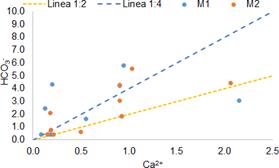
Respecto a la meteorización de silicatos y a los minerales ricos en carbonato y sulfato presentes en la matriz sedimentaria del acuífero, se analizará la mediación por la presencia de sus especies ácidas correspondientes, el ácido carbónico (H 2 CO 3) y el ácido sulfúrico (H 2 SO 4). Para el caso de los minerales de carbonato tales como la calcita (CaCO 3) y dolomita (CaMg(CO 3)2), si el ácido carbónico es el agente meteorizador, la relación molar de los iónes Ca 2+: HCO3−es 1:2 para la calcita, mientras que la meteorización de la dolomita es 1:4 [38].
En la Figura 12, se evidencia que los puntos de muestreo se ubican sobre o cerca de las líneas 1:2 y 1:4, haciendo evidente la mediación generada por la presencia de ácido Carbónico (H2CO3), en la meteorización y disolución de minerales de calcita y dolomita presentes en la matriz sedimentaria del acuífero. Así mismo, en la Figura 13 se muestra una mediación del ácido sulfúrico, originado en las aguas de recarga lateral, provenientes de las rocas que conforman la zona exterior del acuífero [15], ricas en iones sulfato (en el 70 % de los puntos de muestreo) en la meteorización de la calcita, mostrada por los puntos de muestreo cercanos a la línea de relación molar 1:1 de la relación iónica Ca2+: SO2− [38].
3.3 Análisis por componentes principales
Previo al análisis, los datos fueron log-normalizados y al aplicar el test de shapiro-wilk, se obtuvo que los datos no presentan una diferencia estadísticamente significativa (p > 0.05), por lo cual se acepta la hipótesis nula que estos datos provienen de una población normalmente distribuida. El test de esfericidad de Barlett fue calculado con los datos obtenidos para los dos muestreos, y se obtuvo que los datos presentan una diferencia estadísticamente significativa (p < 0.05; df = 78), por lo cual la aplicación de un análisis de componentes principales genera una reducción significativa de la dimensionalidad de los datos originales.
El ACP fue llevado a cabo por la diagonalización de la matriz de correlación; las variables fueron autoescaladas a media cero y unidad de varianza, evitando los problemas debido a las diferentes escalas de medición y rangos numéricos variables que presentan los parámetros analizados. La Tabla 4 presenta los valores propios (eigenvalues) y la varianza acumulada de cada factor para los dos periodos de muestreo. Los primeros 3 factores considerados en el ACP, con valores propios > 1 presentan una varianza acumulada del 75 % (M1) y 71 % (M2).
Tabla 4 Valores propios y varianza acumulada para cada factor en los periodos de muestreo M 1 y M 2
| Factor | M1 | M2 | ||
| VP | VA | VP | VA | |
| 1 | 5.16 | 0.40 | 4.98 | 0.38 |
| 2 | 2.59 | 0.60 | 2.60 | 0.58 |
| 3 | 2.06 | 0.75 | 1.67 | 0.71 |
| 4 | 1.24 | 0.85 | 1.16 | 0.80 |
| 5 | 0.99 | 0.93 | 0.99 | 0.87 |
| 6 | 0.61 | 0.97 | 0.83 | 0.94 |
| 7 | 0.24 | 0.99 | 0.65 | 0.99 |
| 8 | 0.06 | 1.00 | 0.14 | 1.00 |
| 9 | 0.06 | 1.00 | 0.01 | 1.00 |
*VA: Varianza Acumulada; VP: Valor propio
La Tabla 5 muestra las cargas de cada variable fisicoquímica analizada en cada factor, y en cuyo análisis se tuvo en cuenta que las cargas de las variables analizadas presentaran valores > 0.5, lo que genera una única contribución a la discriminación de los procesos que controlan la hidroquímica del agua subterránea en el área, y el porcentaje de la varianza total contabilizada en cada factor del modelo de 3 componentes principales.
Tabla 5 Matriz de coordenadas Varimax para los Muestreos M 1 y M 2
| Variables | M1 | M2 | ||||
| PC1 | PC2 | PC3 | PC1 | PC2 | PC3 | |
| Na+ | 0.69 | -0.35 | 0.46 | 0.60 | -0.11 | 0.46 |
| K+ | 0.41 | 0.63 | -0.54 | 0.33 | 0.73 | -0.35 |
| Ca2+ | 0.64 | 0.04 | -0.41 | 0.76 | -0.07 | 0.12 |
| Mg2+ | 0.59 | -0.09 | 0.54 | 0.68 | -0.13 | 0.26 |
| HCO3 - | 0.87 | -0.35 | 0.31 | 0.92 | -0.22 | 0.30 |
| SO4 2- | 0.54 | 0.58 | -0.27 | 0.42 | 0.74 | -0.30 |
| Cl- | -0.28 | 0.53 | 0.55 | -0.63 | 0.28 | 0.60 |
| N-NO3 - | -0.48 | 0.55 | 0.52 | -0.28 | -0.56 | 0.26 |
| pH | 0.80 | -0.35 | -0.35 | 0.65 | -0.34 | -0.64 |
| T | 0.58 | 0.70 | -0.13 | 0.23 | 0.60 | 0.34 |
| STD | 0.93 | -0.17 | 0.20 | 0.96 | 0.00 | 0.21 |
| FeT | -0.60 | -0.52 | -0.28 | 0.52 | -0.56 | -0.18 |
3.3.1 Muestreo julio (M1)
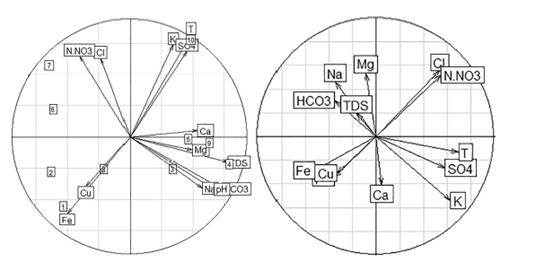
Para el muestreo 1 [Figura 14 a,b y Tabla 5], el primer factor (PC1) explica el 39.6 % del total de la varianza, presentando una fuerte asociación con valores positivos (> 0.6) de las variables Na+, Ca2+, HCO3 -, pH y STD, siendo las variables relacionadas con los procesos de interacción entre la matriz agua-sedimento, y en específico del proceso de intercambio catiónico reverso que se desarrolla en la matriz sedimentaria del acuífero, disolución de minerales carbonatados y la influencia que presenta el pH en estos procesos. Así mismo, la asociación avalores negativos (< -0.6) de las variables FeT y N - NO3 -, estaría relacionada con el proceso de enriquecimiento iónico y su baja concentración en la matriz agua - suelo.
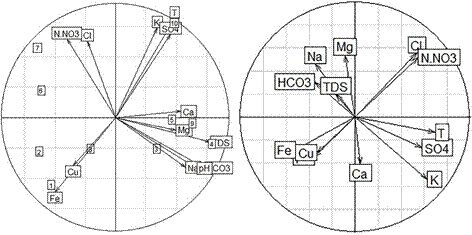
Nota: 1: Al-Te-02; 2: P-Te-04; 3: P-Te-05; 4: P-Te-06; 5: P-Te-07; 6: P-Te-09; 7: P-Te-10; 8: P-Te-11; 9: P-Ta-12; 10: P-Ta-13
Figura 14 Diagrama de dispersión para a) las componentes PC1 y PC2; b) las componentes PC2 y PC3, en el muestreo M1.
El segundo factor (PC2) explica el 19.9 % del total de la varianza, con fuerte asociación al K+ y T (valor > 0.6), al FeT (valor < −0.6) y a SO4 2- y N - NO3 - (valor > 0.55), relacionado con procesos antrópicos que afectan las características hidroquímicas del agua subterránea, tales como el uso fertilizantes ricos en sulfato y compuestos nitrogenados, tales como el sulfato de amonio ((NH4)2SO4) o potasio, tales como el óxido de potasio (K2O), en los cuales la temperatura juega un papel importante, dado que facilita los procesos de meteorización y dilución de estos en la matriz sedimentaria. El tercer factor (PC3) explica el 15,8 % del total de la varianza; este presenta asociaciones débiles (|0.5| < |x| < |0.6|) positivas con las variables Mg2+, Cl−, N − NO3− y negativas con K+.
En la Figura 14a y b, se evidencia un primer agrupamiento de los puntos de muestreo P-Te-05, P-Te-06, P-Te-07 y P-Ta-12, localizados en la cuenca media, sobre el PC1, mostrando su relación a nivel espacial con los procesos de intercambio catiónico reverso; un segundo grupo, conformado por los puntos de muestreo Al-Te-02; P-Te-04 y P-Te-11, ubicados mayormente en el flanco sureste de la cuenca, sobre el piedemonte de la Serranía Cota- Chía, relacionados por sus elevadas concentraciones de los parámetros Fe T y Cu T , en comparación a los restantes puntos de monitoreo. Además, se observa una relación entre el punto P-Ta-13 con las variables K +, SO 2− y T, mostrando la existencia en este punto de procesos de disolución de minerales ricos en estos iones, tales como la pirita y el uso de fertilizantes inorgánicos ricos en sulfato o potasio, mediados por la temperatura.
3.3.2 Muestreo octubre (M2)
Para el muestreo 2 [Figura 15a,b y Tabla 5], el primer factor (PC1) explica el 38.3 % del total de la varianza, presentando una fuerte asociación de los iones Na +, Ca 2+, Mg 2+, Fe T , HCO3− y los parámetros pH y STD asociados a los procesos de intercambio catiónico y enriquecimiento iónico. Además, una fuerte relación negativa (< 0.6) con el ion Cl − . El segundo factor (PC2) explica el 20.0 % del total de la varianza, con fuerte asociación con T, K +, SO 2− (< 0.7), reflejando la influencia de la temperatura con los procesos de meteorización y disolución de los minerales ricos en sulfato presentes en la matriz sedimentaria del acuífero y la dilución de compuestos ricos en sulfato o potasio por el uso de fertilizantes agrícolas inorgánicos, adicionalmente, presenta una relación débil con el ion N - NO 3 - (< - 0.5), manifestando los efectos que sufre el acuífero respecto a la ganancia y enriquecimiento de estos iones, por efectos antrópicos que suprayacen el acuífero estudiado. Por último, el tercer factor (PC3) explica el 12.9 % del total de la varianza, presentando asociaciones débiles con el ion Cl − (> 0.6) y con el pH (< −0.6).
En las Figura 15a y b, se evidencia un primer agrupamiento de los puntos de muestreo P-Te-05, P-Te-06, P-Te-07 y P-Ta-12, ubicados en la cuenca media, sobre el PC1, mostrando su relación a nivel espacial con los procesos de intercambio catiónico reverso, siendo esta una relación recurrente entre los dos periodos de muestreo; un segundo grupo, conformado por los puntos de muestreo Al-Te-02 y P-Te-11, se relacionan por sus concentraciones de los parámetros N - NO3−, Fe T y Cu T , las cuales se relacionan en el segundo factor (PC2) [Figura 15a y b), en comparación a los restantes puntos de monitoreo, evidenciando mayores efectos, relacionados con los procesos de interacción entre las actividades agrícolas que suprayacen en el área de estudio y su efecto sobre la calidad del agua subterránea. Además, se observa una relación entre el punto P-Ta-13 con las variables K +, SO 2− y T, las cuales presentan una alta relación con el PC2, siendo esta una característica recurrente en los dos periodos de muestreo.
3.4 Comparación con la normatividad colombiana
Tabla 6 Agua para uso agrícola
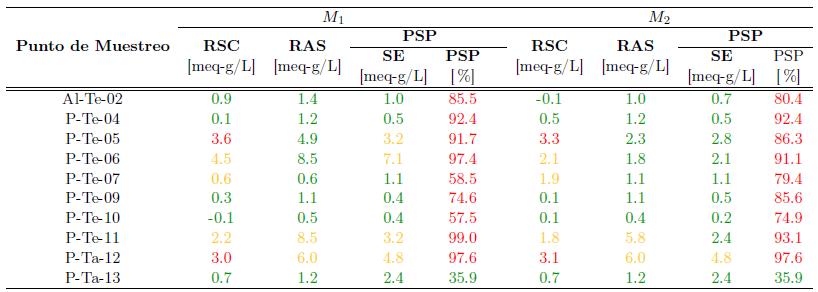
Nota: Los indicadores determinados fueron propuestos en el literal 2.2.3.3.9.5. del Decreto 1076 de 2015. El color rojo indica clases de agua no recomendadas, el color amarillo clases de agua condicionadas, y el color verde clases de agua recomendadas para riego. RSC: Carbonato sódico residual; PSP: Porcentaje de Sodio posible; SE: Salinidad Efectiva; RAS: Relación de absorción del Sodio.
Fuente: elaboración propia
Comparando los parámetros químicos obtenidos en los muestreos con los valores máximos aceptables para agua de consumo humano para la normatividad colombiana, se encuentra que la totalidad de los puntos de muestreo analizados superan el límite permisivo para el hierro (0.3 mg Fe/L) y 3 puntos de muestreo el límite de alcalinidad total (200 mg CaCO3/L). Con respecto al plomo, los valores obtenidos no permiten hacer comparación con la normativa estudiada, al estar por debajo de los límites de detección del equipo (< 0.5 mg Pb/L). Con base en estos resultados, para la potabilización de este tipo de aguas, se recomienda la aplicación de un tratamiento convencional y la determinación de parámetros microbiológicos para las mismas.
En relación con los valores máximos admisibles para el uso agrícola, se por encima de los valores máximos permisibles (5 mg Fe/L; 0.2 mg Cu/L) encuentra que el agua extraída presenta concentraciones de hierro y cobre reportados en este decreto. Se realizó la determinación de los indicadores propuestos [Tabla 6], encontrado que, a excepción del pozo P-Te-13, los pozos muestreados presentan características condicionadas o no recomendadas para riego en uno o más de los indicadores analizados.
Conclusiones
El Agua subterránea en la Cuenca del Río Chicú, fue caracterizada hidroquímicamente en dos periodos de muestreo. Se determinaron las facies hidroquimicas del acuífero, que en general son bicarbonatadas a sulfatadas sódicas o cálcicas según el caso, las cuales varían entre los periodos analizados, debido al régimen de precipitación que se desarrolla en la zona (déficit hídrico para el muestreo M1 y exceso hídrico para el muestreo M2). Se identificaron cuatro [4] grupos de facies hidroquímicas: 1) el grupo G1, conformado por muestras de agua sulfatada sódico-cálcica, responde a un proceso de recarga lateral de agua proveniente de las rocas que conforman la zona exterior del acuífero; 2) el grupo G2, reúne agua sulfatada sódica, cuyo comportamiento hidroquímico responde a un proceso de enriquecimiento con iones sulfato, dada la interacción, disolución y oxidación de iones sulfuro (S2−) provenientes de minerales, tales como la pirita (FeS), en las rocas que conforman la zona exterior del acuífero y el uso el uso de fertilizantes inorgánicos ricos en iones sulfato; 3) el grupo G3, que agrupa agua bicarbonatada cálcica, de origen meteórico y corto tiempo de tránsito en el acuífero, ubicados sobre las zonas potenciales de recarga; por último 4) el grupo G4, con facies hidroquímicas bicarbonatada sódica, cuyo predominio del ion sodio se debe a los procesos de intercambio catiónico reverso que se desarrollan en la matriz sedimentaria.
En cuanto a los indicadores analizados, se encuentra que los procesos de intercambio catiónico reverso y de meteorización de los minerales presentes en el sedimento, mediados por la presencia de oxácidos (H2CO3 y H2SO4), rigen la hidrogeoquímica de la zona estudiada, lo cual se confirma por el análisis de componentes principales, al corroborar la existencia de procesos hidroquímicos que afectan a la calidad del agua subterránea. De igual manera, se encuentra que dichos procesos son recurrentes en una agrupación de pozos ubicados en el área de tránsito del agua subterránea, además, que en el pozo P-Ta-13 los procesos de enriquecimiento iónico de minerales ricos en Potasio y Sulfato, dominan la hidroquímica de este punto de muestreo, por la interacción de las aguas subterráneas con los minerales presentes en las rocas del cretácico y por el uso de fertilizantes inorgánicos ricos en sulfato y potasio.
En comparación con las normativas ambientales colombianas para los periodos de muestreo, se encuentra que la totalidad de las muestras no proveen agua de buena calidad para propósitos de consumo, al sobrepasar los límites permisivos en hierro y alcalinidad total; se recomienda la aplicación de un tratamiento convencional de potabilización para su consumo, que busque reducir las características no deseables del agua. En adición, se evidencia en el muestreo 2, un aumento en la concentración del ion N - NO3 - y CuT, el cual no sobrepasa los límites permisivos establecidos para agua potable. Aunque su presencia en el área puede ser considerada como indicador de impacto antropíco leve, se requiere hacer un continuo seguimiento a estos parámetros, con el fin de identificar las áreas donde las actividades antrópicas que suprayacen al acuífero puede generan efectos significativos sobre su calidad y, determinar la probable existencia de procesos de dilución de este parámetro, dados los procesos de recarga que se hacen evidentes en los meses de exceso hídrico, manifestados por la reducida concentración de N - NO3 - y CuT en el muestreo 1. Por último, respecto a su uso para riego, las muestras estudiadas no son recomendadas al presentar clasificación condicionada o no recomendada en uno o más de los indicadores analizados.