I. INTRODUCCIÓN
El acceso a agua potable segura es un importante aspecto de la salud y el desarrollo en los niveles nacional, regional y local. En algunas regiones se ha evidenciado que inversiones en abastecimiento de agua y saneamiento pueden producir un beneficio económico neto, al sopesar los costos producto de realizar las intervenciones del caso, frente a los efectos adversos y cuidados de la salud humana[1].
De acuerdo con las estimaciones realizadas por Naciones Unidas, la población mundial de 7,2 billones de habitantes registrada en 2013 tiene una proyección de crecimiento de 1 billón de personas en los próximos 20 años, para alcanzar un valor del orden de 8,1 billones en 2025 y posteriores incrementos hasta 9,6 billones en 2050 y 10,9 billones de habitantes en el año 2100[2]. Las poblaciones urbanas tienen una proyección de crecimiento de 2,9 billones de personas, para pasar de los 3,4 billones registrados en 2009 a 6,3 billones en 2050, lo que implica que las áreas urbanas del mundo deberán absorber la gran mayoría del crecimiento poblacional de las próximas cuatro décadas[3]. Con base en lo anterior, es de esperar un gran aumento en las necesidades de agua potable, que sumado a la creciente presión que han experimentado las diferentes fuentes de agua en términos de su uso y contaminación, establece nuevos retos en el tratamiento del líquido disponible.
Según Rodrigues, Milhomem, Magalhães, Cavalcanti & Daniel[4], el proceso de tratamiento del agua puede ser visto como un conjunto de operaciones aplicadas al líquido en sus más diversas fuentes con el objetivo de hacerla apta para el abastecimiento público; por lo tanto, significa afirmar que su calidad físico-química y microbiológica atiende ciertos estándares de calidad definidos por los entes reguladores.
Los administradores de sistemas de potabilización de agua trabajan en medio de un mundo cargado de incertidumbres. Su primera prioridad es garantizar la seguridad del abastecimiento del líquido y dependen de parámetros geofísicos que definen la disponibilidad del agua (precipitación, escorrentía, infiltración) y los determinantes de actividades humanas que afectan la calidad y flujo natural del agua (como por ejemplo, el uso del suelo que afecta la escorrentía superficial) así como su distribución en el tiempo y el espacio[3].
En términos generales, el color en el agua puede resultar de procesos de descomposición de la materia orgánica, de la presencia de iones metálicos naturales como el hierro y el manganeso, así como del vertimiento de diversos tipos de efluentes industriales; en particular, el color natural en las aguas, principalmente el color verdadero, presenta como agentes causadores las sustancias húmicas (SH) y fúlvicas, las cuales se presentan siempre en estado coloidal[5].
La coagulación química con sales metálicas ha sido usada tradicionalmente en el tratamiento para remoción de la turbidez; sin embargo, la coagulación es también capaz en cierto grado de remover la materia orgánica natural, la cual puede funcionar como un precursor de la formación de subproductos de la desinfección[6]. En los últimos años ha tomado relevante importancia la remoción de materia orgánica natural del agua, la cual está asociada a la producción de olores y gustos desagradables, constituye un sustrato para el crecimiento bacteriano e incrementa la necesidad de insumos; pero lo más importante es que genera en el tratamiento de potabilización subproductos de la desinfección potencialmente cancerígenos[7].
Las tecnologías de tratamiento del agua pueden resumirse en dos grupos, sin coagulación y con coagulación química. Dependiendo de la calidad del agua cruda, ambas pueden o no ser precedidas de pre-tratamiento, el agua químicamente coagulada puede seguir varios caminos hasta llegar a los filtros, toda vez que la calidad del agua cruda debe ser el factor decisivo en la selección de la tecnología de tratamiento[8].
Según Di Bernardo[9], la filtración directa presenta diversas ventajas en relación con tratamiento convencional, entre las que se encuentra el menor número de unidades involucradas, pues la primera presenta solamente presenta las unidades de coagulación, floculación (eventualmente) y filtración; el menor consumo de productos químicos durante el proceso de tratamiento; mayor facilidad de operación y mantenimiento e menor generación de lodo.
La electrólisis se refiere a la separación de sustancias por medio del uso de la electricidad. El proceso ocurre en un electrolito, una solución acuosa que brinda la posibilidad de transferir iones entre dos electrodos; cuando se aplica una corriente eléctrica, los iones positivos se desplazan hacia el cátodo mientras que los iones negativos se mueven hacia el ánodo[10].
Los procesos de tratamiento electroquímico se han utilizado tradicionalmente para la depuración de aguas residuales trabajando como unidades individuales o acoplados a reactores de tratamiento biológico, pues una de sus principales aplicaciones consiste en servir como pre-tratamiento de compuestos tóxicos y no biodegradables para que estos sean posteriormente tratados por medio de sistemas biológicos convencionales. Entre las características que hacen atractivo el tratamiento electroquímico se destacan su versatilidad, eficiencia en el uso de la energía, facilidad de automatización y bajo costo efectivo[11].
Esta investigación tuvo como objetivo, evaluar el desempeño del proceso electrolítico, seguido de filtración directa en la remoción de diversos niveles de color de muestras provenientes del río Paraná, en inmediaciones de la ciudad de Ilha Soleira (São Paulo). La evaluación se efectuó para el agua en condiciones de color natural y para valores aumentados por medio de la adición de sustancias húmicas, utilizando como coagulante sulfato de aluminio; adicionalmente, se evaluó la eficiencia de remoción de la turbidez y se monitorearon los valores de pH.
II. METODOLOGÍA
El experimento se realizó en el Laboratorio de Saneamiento de la Facultad de Ingeniería de la Universidade Estadual Paulista -UNESP-, campus de Ilha Solteira, estado de São Paulo, Brasil. El método aplicado para purificación del agua involucró dos tecnologías, donde primero se aplicó el proceso electrolítico con el propósito de mitigar los picos de color y posteriormente se ejecutó el ensayo de filtración directa en el equipo de ensayo de jarras para determinar la dosis de coagulante más favorable para el proceso.
El agua utilizada en el estudio fue colectada en el río Paraná en un tramo cercano a la ciudad de Ilha Solteira, estado de São Paulo, Brasil; se adicionaron cantidades controladas de SH, las cuales según Campos, Di Bernardo & Vieira [12], son de utilidad para preparar aguas de estudio con miras a evaluar la remoción del color por parte de sistemas de tratamiento que involucran la coagulación. Las muestras del líquido fueron sometidas a proceso electrolítico en el que a los electrodos de aluminio se aplicó una tensión de 25 V y corriente de 0,9 Amperios.
Se realizaron ensayos preliminares que permitieron determinar que el proceso de tratamiento electrolítico se aplicaría durante una hora y que para el ensayo de filtración directa se utilizarían dosis de 6, 8, 10, 12, 14 y 16 mg/L de coagulante sulfato de aluminio anhidro (Al2(SO4)3), con una concentración de 2,0 mg/mL. Posteriormente, con tal tiempo de reacción electrolítica y dichas dosis de coagulante se realizaron 7 ensayos, que determinaron 4 fases del experimento, cuyas características básicas fueron:
En la primera etapa, se aplicó el proceso de tratamiento electrolítico y la filtración sobre el agua cruda del río Paraná.
En la segunda etapa se realizaron dos ensayos con adición de 60 mL de SH para aumentar los niveles de color; allí también se agregó 1 g/L de dióxido de titanio (TiO2).
En la tercera fase hubo una adición de 125 mL de SH para ambos ensayos, para el segundo de ellos se añadió 1 g/L de TiO2.
En la cuarta fase se adicionaron 250 mL de SH y en el segundo ensayo se adicionó TiO2 en una concentración de 1 g/L.
El proceso electrolítico se efectuó en un reactor rectangular de acrílico transparente de 40 cm de largo, 30 cm de alto, 20 cm de ancho y volumen útil de 20 L. Los electrodos del reactor estuvieron compuestos por 6 placas de aluminio de 30 cm de altura, 39 cm de longitud y 0,5 mm de espesor. Se utilizó una fuente alimentadora de corriente continua, rectificadora con 25 Voltios nominales y corriente máxima de 5 Amperios, marca Labo, modelo FR 25 50 y para el cableado se utilizaron cables y caimanes N° 10.
Los ensayos de coagulación se efectuaron mediante la prueba de jarras en un equipo de reactores estáticos marca Nova Ética (Brasil), compuesto por seis jarras, dispuestas en paralelo con agitación mecánica variable. Dado que la tecnología utilizada en el estudio fue la de filtración directa, se utilizó un gradiente de velocidad que simuló alta agitación en un corto intervalo de tiempo. En la Fig. 1 se presenta una fotografía en la que se ilustran los elementos constitutivos del reactor electrolítico con su fuente alimentadora.
La Fig. 2 presenta una imagen relativa al equipo de prueba de jarras y de filtración directa.
En cada ensayo para tratamiento electrolítico se lavaron el reactor y los electrodos con agua de grifo y se secaron con un paño limpio; se ubicaron los electrodos en sus respectivas posiciones y se fijaron los caimanes a su parte superior; en el reactor se vertían 19 L de agua a ser tratada (según el caso, con SH o SH + TiO2) y se cronometraban 60 minutos de exposición, tiempo después del cual se colectaba el líquido para la prueba de jarras mediante una manguera fijada con un soporte; al final del ensayo nuevamente se lavaban el reactor y los electrodos.
El agua efluente del reactor era vertida en las jarras de forma aleatoria, hasta completar los 2 L; para los ensayos de coagulación se utilizó un gradiente de velocidad de 600 s-1 y tiempo de mezcla rápida de 5 min; a cada jarra se le adicionó entre 6 y 16 mg/L de Al2(SO4)3; después del proceso de mezcla rápida se suspendió la agitación y el efluente fue sometido al proceso de simulación de la filtración directa a través de filtros de arena; durante los primeros 5 min de filtración se descartaron los efluentes y después de ese tiempo se colectaron muestras para realizar la medición de los parámetros turbidez, color aparente, color verdadero y pH.
Las muestras se colectaron en frascos de plástico y se transportaron para su análisis después de cada ensayo. Para medir la turbidez se utilizó un turbidímetro HACH 2100 AN, con lecturas 30 s después de insertar la muestra. Los análisis de color aparente y verdadero se hicieron con espectrofotómetro HACH DR 5000 con longitud de onda de 455 nm; para analizar color verdadero se realizó centrifugación del líquido por 3 min mediante una centrífuga marca FANEM, Excelsa II modelo 206 BL, con rotación de 3500 rpm. La medición del pH se hizo con un pHmetro DIGIMED DM 22, con tiempo de espera para estabilización de la lectura de 10 min.
III. RESULTADOS
A. Primera etapa, agua cruda del río Paraná
El agua cruda presentó turbidez y color relativamente altos puesto que el día previo a la colecta se presentaron precipitaciones del orden de 15,2 mm en el municipio de Ilha Solteira. Los valores iniciales fueron de 8,23 unidades nefelométricas de turbidez (UNT), 41 unidades Hazen (uH) de color aparente, 12 uH de color verdadero y pH de 7,7; después del proceso electrolítico se midieron niveles de turbidez de 2,54 UNT, 14 uH de color aparente, 3 uH de color verdadero y un pH de 7,87.
Los efluentes del proceso de coagulación y filtración directa reportaron en todos los casos valores de color aparente menores al máximo nivel permitido para agua potable de 15 uH, establecido por la legislación Brasilera en la Portaria del Ministerio de la Salud No. 2914 [13], con valor mínimo de 3 uH para 14 mg/L de Al2(SO4)3, que también presentó la mayor remoción de turbidez con 0,54 UNT, ligeramente superior al máximo definido por la Portaria 2914 de 0,50 uT.
Todas las dosis de coagulante generaron valores de color aparente <1 uH, lo que demostró su eficiencia en la remoción de los elementos disueltos en el agua. Los valores de pH en los efluentes variaron entre 7,8, para una dosis de 6 mg/L de coagulante y 7,64, para 16 mg/L, enmarcándose en los límites de 6,5 a 9,0 definidos por la norma Brasilera.
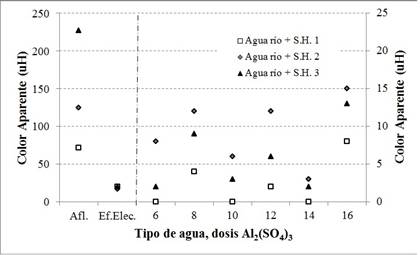
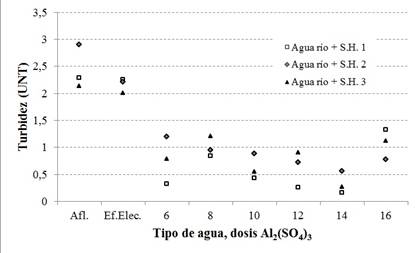
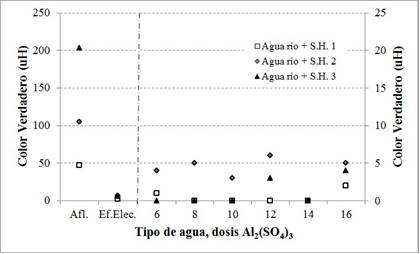
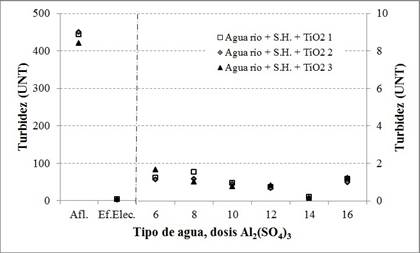
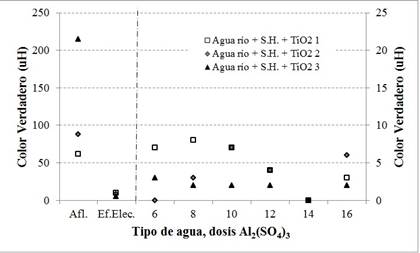
En los siguientes párrafos se presentarán los resultados del monitoreo de los parámetros en la segunda, tercera y cuarta etapas. Las Fig. 3, 4 y 5 ilustran respectivamente las mediciones del color aparente, turbidez y color verdadero para los ensayos efectuados sobre agua cruda con adición de SH, donde las leyendas Agua río + S.H.1, S.H.2 o S.H.3 representan cada una la adición de 60 mL de SH (segunda etapa), 125 mL de SH (tercera etapa) y 250 mL de SH (cuarta etapa). Las Fig. 6, 7 y 8 grafican los resultados para los ensayos con SH en las cantidades ya mencionadas y 1 mg/L de TiO2. Dada la alta eficiencia de remoción de color o turbidez por el proceso electrolítico, se estableció para las Figs. 3, 5, 6, 7 y 8 dos escalas verticales separadas por una línea discontinua, que en su lado derecho representa la escala para los resultados obtenidos después de la filtración.
B. Segunda etapa, agua cruda del río Paraná + 60 mL de SH + 1 g/L de TiO 2
En el ensayo con agua cruda + SH se registró color aparente inicial de 72 uH, color verdadero de 47 uH, turbidez de 2,29 UNT y pH de 7,65.
Como se puede apreciar en la Fig. 3, el tratamiento electrolítico removió de manera eficiente el color aparente (72,2%), que complementado por la filtración directa garantizó valores muy por debajo de las 8 uH, encontrándose así dentro de los limites definidos por la legislación brasilera.
En lo que respecta a la turbidez, la Fig. 4 evidenció que fue fundamentalmente la filtración el proceso que realizó su remoción. En el ensayo se lograron valores menores a 0,5 UNT, con excepción de las dosis de 8 y 16 mg/L de coagulante.
Tal como lo indica la Fig. 5, el color verdadero fue principalmente removido por el proceso electrolítico, con una eficiencia del 95,7%. Para las seis cantidades de coagulante evaluadas se obtuvo en el líquido filtrado valores menores a 3 uH; el mejor desempeño se obtuvo para una dosis de 14 mg/L de Al2(SO4)3.
En las pruebas con SH y TiO2 la presencia del dióxido de titanio aumentó los niveles del material fino en suspensión, con color aparente inicial de 425 uH (Fig. 6), turbidez inicial de 443 UNT (Fig. 7) y color verdadero de 62 uH (Fig. 8), además de un pH inicial de 7,71.
El tratamiento electrolítico reportó remociones del 95,8% para el color aparente, del 99,2% para turbidez y del orden del 83,9% para color verdadero, lo que evidenció una alta eficiencia en la remoción de material en suspensión y disuelto, como se puede apreciar en las Figuras 6, 7 y 8.
La filtración realizó remoción adicional de los parámetros, con mayor eficiencia para la dosis de 14 mg/L de Al2 (SO4)3 que simultáneamente permitió ajustar los valores de turbidez y color aparente en lo establecido por la norma Brasilera, con 0,2 UNT y 4 uH de color aparente. El más bajo valor de pH lo presentó el agua filtrada proveniente de la jarra con 16 mg/L de coagulante.
C. Tercera etapa, agua cruda del río Paraná + 125 mL de SH + 1 g/L de TiO 2
En la prueba con agua cruda + SH se midió color aparente inicial de 125 uH, turbidez de 2,9 UNT, color verdadero de 105 uH y pH de 7,66.
El tratamiento electrolítico removió de manera eficiente el color aparente (86,4%); la filtración directa redujo los niveles hasta por debajo de las 15 uH, con mejor desempeño para una dosis de 14 mg/L (Fig. 3). Situación similar se presentó para el color verdadero, cuya eficiencia de remoción en el reactor electrolítico fue del 93,3% (Fig. 5).
El proceso electrolítico únicamente removió 23,8% de la turbidez, hasta un valor de 2,21 UNT, la coagulación y la filtración removieron fracciones adicionales de material en suspensión, pero el desempeño fue insuficiente para ajustarse a lo estipulado por la Portaria No. 2914 [13], pues el valor más cercano al límite máximo permitido se obtuvo con una dosis de 14 mg/L de coagulante, que reportó 0,56 UNT (Fig. 4).
En el ensayo con SH y TiO2 nuevamente se registró alto color aparente y turbidez iniciales (440 uH y 450 UNT), con color verdadero de 88 uH y pH de 7,72.
Con el proceso electrolítico se lograron remociones de 96,4% de color aparente, 99,5% de turbidez y 90,9% de color verdadero, evidenciando alta eficiencia en la remoción de material en suspensión. Todas las dosis de sulfato de aluminio usadas en la coagulación, junto con la filtración garantizaron que el color aparente se ajustase a los valores de la norma; sin embargo, solamente el tratamiento con 14 mg/L de coagulante garantizó simultáneamente el cumplimiento de los valores de turbidez junto con el mínimo nivel de color aparente, tal como puede apreciarse en las Fig. 6 y 7. El menor valor de pH se midió en el agua filtrada previa coagulación con 16 mg/L de Al2 (SO4)3.
D. Cuarta etapa, agua cruda del río Paraná + 250 mL de SH + 1 g/L de TiO 2
El agua cruda + SH registró valores de color aparente de 227 uH, turbidez de 2,14 UNT, color verdadero de 203 uH y 7,66 unidades de pH. Dados los bajos niveles iniciales de material en suspensión, el proceso electrolítico registró baja eficiencia de remoción de turbidez (6,1%), mientras que para el color aparente y verdadero se contabilizaron eficiencias de 91,2 y 97,0% (Fig. 3 y 5), evidenciando un buen desempeño para remover material disuelto.
La coagulación y la filtración garantizaron valores de color aparente dentro de los permitidos por la norma, con mejor desempeño para la unidad con 14 mg/L de coagulante, que además de reportar valor final de 2 uH también fue el único que se enmarcó en la Portaria en cuanto a turbidez, con 0,27 UNT (Fig. 4). Todos los valores de pH de los efluentes finales se encontraron por encima de 7,5, permaneciendo así dentro de los límites recomendados por la norma.
En la prueba con SH y TiO2 se registraron valores iniciales de 495 uH de color aparente, 420 UNT y 215 uH de color verdadero. El tratamiento electrolítico redujo un alto porcentaje del material en suspensión y disuelto (f6, 7 y 8), con remociones de 99,3% de la turbidez, 96,4% del color aparente y 97,7% del color verdadero. Como resultado de la filtración directa, las seis unidades de coagulación y filtración enmarcaron los niveles de color aparente en la norma, con mejor desempeño para una dosis de 14 mg/L de Al2 (SO4)3, con 2 uH, que a su vez fue el único que cumplió la norma en términos de turbidez pues el valor medido fue de 0,13 UNT.
El sistema de tratamiento generó, en los seis casos, valores finales de color verdadero inferiores a 3 uH y el menor pH registrado fue de 7,49, en la unidad con dosis de coagulante de 16 mg/L.
IV. CONCLUSIONES
El proceso electrolítico seguido de filtración directa fueron eficientes en la remoción de color y turbidez tanto para la condición natural del río Paraná como para valores muy elevados de dichos parámetros; permitiendo en la mayoría de los casos, principalmente para color aparente, su reducción hasta los niveles permitidos por las directrices de agua potable Brasileras.
El uso de sulfato de aluminio como coagulante demostró una alta eficiencia en la remoción de color aparente, turbidez y color verdadero, con mejores resultados para una dosis de 14 mg/L.
La utilización de TiO2 en el tratamiento no reportó resultados que justifiquen su uso versus los beneficios que representaría para el sistema de tratamiento.