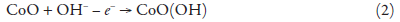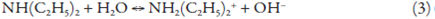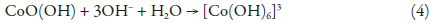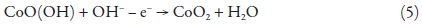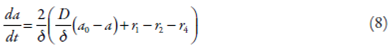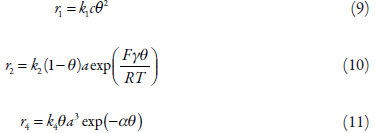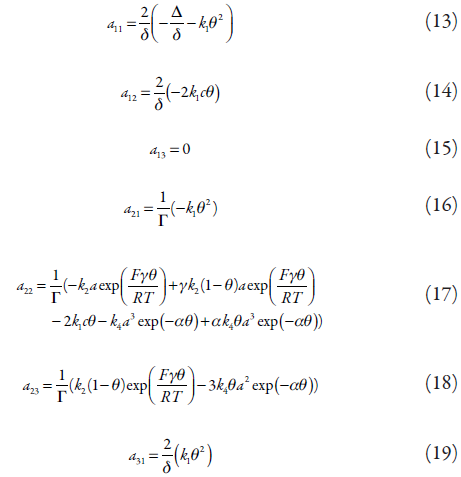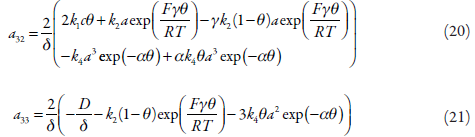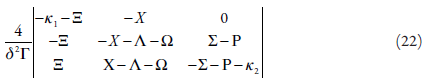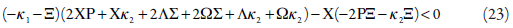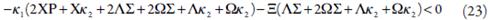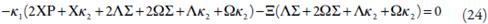INTRODUÇÃO
Hodiernamente, o uso dos métodos eletroquímicos na detecção de presença e(ou) concentração de fármacos tornou-se um dos apetrechos analíticos flexíveis, baratos, e eficientes [1-10]. Dentre eles, um lugar especial ocupam os elétrodos quimicamente modificados (EQM) [5-10], pois o serem capazes de combinar a precisão, exatidão, rapidez e ainidade aos analitos lhes dá um amplo espectro de uso.
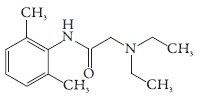
Por outro lado, a lidocaína 2-(dietilamino)-N-(2,6-dimetilfenil) acetamida é um dos anestéticos locais mais usados hoje em dia [11-18] (fig. 1), podendo ser aplicado mesmo em pequenas intervenções cirúrgicas. Sintetizado em 1946 e comercializado em 1948, ele é também utilizado para o tratamento de taquicardia ventricular [19,20] e fibrilação ventricular [21,22]. Quanto ao mecanismo da sua ação, ela é um bloqueador rápido dos canais de sódio, activados ou inactivados, existentes nos miócitos especializados do sistema de condução (coração) ou nervos periféricos. Impede a condução de potencial de ação nos axônios sensitivos dos nervos periféricos, quando usada topicamente.
Não obstante que a lidocaína seja considerada um fármaco relativamente seguro, a sua atividade no corpo humano depende fortemente da sua concentração. Ademais, o seu uso excessivo e duradouro pode provocar hipotensão arterial, a dita sensação de cabeça leve, ziziamento no ouvido e parestesias [23,24]. Outrossim, no caso do uso indevido ele pode causar excitação do sistema nervoso central (SNC), depressão e reação alérgica [25-27]. Destarte, o desenvolvimento de um método eficiente e rápido da detecção da sua presença e concentração segue sendo uma tarefa atual ainda hoje [28-32].
Como a lidocaína é um composto eletroquimicamente ativo, foram desenvolvidos vários métodos da sua quantificação mediante o uso de EQM. Dentre os modificadores destacam-se o boro [33], materiais de carbono [34,35] e os polímeros condutores [36,37]. O oxihidróxido de cobalto, um material semicondutor do tipop-, visto por alguns pesquisadores como alternativa ao dióxido de titânio [38-40], veio a ser usado em sistemas eletroanalíticos apenas recentemente [41,42]. No entanto, em princípio, ele poderia ser usado na quantificação da lidocaína, já que as substâncias, para as quais o seu desempenho eletroanalítico eficiente foi observado experimentalmente [41,42] ou previsto teoricamente [43-46] são oxidadas nas condições, semelhantes às da lidocaína, descritas na literatura [33-37].
No entanto, a possível aplicação de oxihidróxido de cobalto como modificador do ânodo na detecção de lidocaína pode enfrentar os problemas como:
- o pouco conhecimento do comportamento exato do material no ânodo e, por conseguinte, do mecanismo mais provável de ação eletroanalítica de CoO(OH) com o lidocaína nas condições da análise;
- a possibilidade das instabilidades eletroquímicas, que podem acompanhar tanto o processo da eletrossíntese de CoO(OH) [47,48], como o da eletrooxidação de várias substâncias orgânicas [49], inclusive a eletropolimerização.
A resolução de ambos os problemas não pode ser realizada sem o desenvolvimento de um modelo matemático, capaz de descrever adequadamente os processos neste sistema.
Assim, o objetivo geral deste trabalho é a avaliação mecanística da possibilidade de o CoO(OH) ser modificador do elétrodo para auxiliar a oxidação da lidocaína, para fins eletroanalíticos, ou eletrocatalíticos. A realização deste objetivo requer o alcance dos objetivos específicos:
- A sugestão do mecanismo da reação, incluindo o desempenho de CoO(OH) no processo;
- O desenvolvimento de modelo, na base deste mecanismo;
- Análise de estabilidade do estado estacionário neste sistema (na base do modelo);
- Verificação da possibilidade das instabilidades eletroquímicas nele;
- Comparação do seu comportamento com o dos sistemas semelhantes [41-46].
O SISTEMA E O SEU MODELO
A obtenção de CoO(OH) para modificar o ânodo pode ser realizada tanto de via química [41,42], como da eletroquímica [42,47,48]. Neste caso, ela se dá mediante a eletrooxidação dos compostos do cobalto bivalente (geralmente, CoO, Co(OH)2 ou Co2+), e naquele, por meio de uma síntese coloidal. As reações da eletrossíntese de CoO(OH) também se usam para manter a reversibilidade do elétrodo, o que será descrito abaixo.
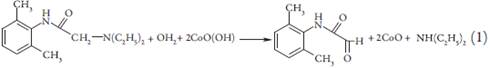
O mecanismo da eletrooxidação de lidocaína sobre o oxihidróxido de cobalto(III) inclui a sua hidrólise e pode ser apresentado abaixo:
É preciso observar, também, a formação de uma amina secundária durante o processo da oxidação. Haja vista a aparição da dietilamina, o meio da solução torna-se mais alcalino, haja vista a reação
o que serve para melhorar o desempenho eletroanalítico de CoO(OH) com a lidocaína. No entretanto, em meio fortemente alcalino, CoO(OH) tende a dissolver, formando o complexo
Destarte, o uso de soluções fortemente alcalinas com o pH superior a 11 - 12, como nos sistemas semelhantes [41-46], prejudicará a estabilidade do material e, por conseguinte, o processo eletroanalítico. No caso da lidocaína, o pH da solução cresce ao longo do processo da oxidação, e a análise deve ser realizada com muito cuidado, para impedir a dissolução do oxihidróxido de cobalto.
Aplica-se ao ânodo o potencial não superior a 1,7 V, já que neste potencial o próprio CoO(OH) pode sofrer oxidação até formar compostos de cobalto (IV):
Haja vista o supracitado, conclui-se que o sistema é descrito pelo conjunto de três equações diferenciais, cujos variveis são:
c - a concentração da lidocaína na camada pré-superficial da solução;
9 - o grau de recobrimento da superfície com o oxihidróxido de cobalto trivalente;
a - a concentração da hidroxila na camada pré-superficial da solução.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente (para menosprezar o fluxo de convecção), que o eletrólito de suporte esteja em excesso (para menosprezar o fluxo de migração). Também é suposto que a distribuição con-centracional na camada pré-supericial seja lineal, e a sua espessura, constante, igual a S. Supõe-se, também, que, no início da reação, o oxido de cobalto bivalente cubra a superfície inteira. Outrossim, para efeitos de modelagem, as reações (1) e (3) dar-se-ão como uma reação única.
O analito entra na camada pre-superficial por meio da sua difusão, entrando, ulteriormente, na reação com o oxihidroxicomposto de cobalto (III). Destarte, a sua equação de balanço descrever-se-á como:
Em que Δ e o seu coeficiente de difusão, c0 e a concentração da lidocaína no interior da solução, e r1, a velocidade da sua reação com o oxihidroxido de cobalto, incluindo a ionização da amina.
O oxihidróxido de cobalto forma-se durante a reação (2) e desaparece durante a reação (1). Ele também sofre a dissolução, reagindo com o excesso do álcali. Posto assim, a sua equação de balanço obter-se-á como:
Em que r 2 e r 4 são as reações da formação e da dissolução de CoO(OH), e Γ é a sua concentração máxima superficial.
A hidroxila entra na camada pré-superficial durante a difusão do álcali. Além disso, ela é formada durante a reação (3), precedida pela reação (1). Assim sendo, a sua equação de balanço será descrita como:
em que D é o coeficiente da difusão da hidroxila, e a 0 , a sua concentração no interior da solução.
As velocidades das respectivas reações podem ser calculadas como:
Em características gerais, o comportamento deste sistema não difere muito do dos semelhantes. No entretanto, haja vista a formação de uma amina secundária, um composto expressamente básico, o pH cresce ao longo da reação, o que não pode não dar influências ao sistema eletroanalítico. Estas influências pôr-se-ão em discussão abaixo.
RESULTADOS E DISCUSSÃO
Para investigar teoricamente o comportamento do processo da detecção eletroquímica da lidocaína sobre o oxihidróxido de cobalto trivalente, analisamos o conjunto de equações diferenciais (6 - 8) mediante a teoria de estabilidade linear. Os elementos estacionários da matriz funcional de Jacobi descrever-se-ão como:
Em que:
Observando os membros da diagonal principal da matriz (13), (17) e (21), é possível ver que eles contêm expressões, capazes de ter valores positivos. Elas descrevem a positiva conexão de retorno, e isto significa que o comportamento oscilatório, neste caso, é possível.
Como em sistemas semelhantes [41-49], ele é causado pela influência dos fatores superficiais (atração das partículas adsorvidas) e eletroquímicos (influências dos processos eletroquímicos na dupla camada elétrica (DCE)). Elas se representam pela positividade dos elementos 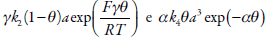 , descrevendo as influências superficial e eletroquímica, correspondentemente. As oscilações esperam-se frequentes e de curta amplitude. Quanto mais cresce o pH, tanto maior é a probabilidade do comportamento oscilatório, haja vista a ocorrência dos dois processos pH-dependentes, relacionados às oscilações, contra um no caso do pH neutro ou levemente alcalino.
, descrevendo as influências superficial e eletroquímica, correspondentemente. As oscilações esperam-se frequentes e de curta amplitude. Quanto mais cresce o pH, tanto maior é a probabilidade do comportamento oscilatório, haja vista a ocorrência dos dois processos pH-dependentes, relacionados às oscilações, contra um no caso do pH neutro ou levemente alcalino.
Para investigar a estabilidade do estado estacionário, aplicamos ao conjunto das equações diferenciais de balanço (6 - 8) o critério de Routh-Hurwitz. Para evitar a aparição de expressões grandes, introduzimos as novas variáveis, de modo que o determinante se descreve como:
Abrindo os parênteses, e aplicando o requisito Det J<0, saliente do critério, obteremos a condição da estabilidade do estado estacionário como:
Ao rearranjarmos a inequação (23), com a eliminação dos elementos iguais com signos contrários, obter-se-á o requisito de estabilidade de forma ainda mais clara:
Este requisito de estabilidade do estado estacionário, que, para efeitos eletroanalíticos, é correspondente à linearidade da dependência entre a concentração da lidocaína e o parâmetro eletroquímico medido, é fácil de implementar. Sabendo que a maioria das novas variáveis só pode ter valores positivos (sendo apenas os parâmetros A e O capazes de ficar negativos), no caso da repulsão das partículas adsorvidas (descrita pela positividade do parâmetro O) e da fraqueza das influências do processo eletroquímico na capacitância da DCE (descrita pela positividade do parâmetro A), o valor da expressão do lado esquerdo da inequação (23) deslocar-se-á para valores mais negativos, o que significará a pequenez dos desvios do estado estacionário e, por conseguinte, a sua estabilidade. Como isto acontece em soluções neutras e levemente alcalinas, haja vista a cinética das reações (1 - 5), o melhor desempenho do sensor espera-se no valor de pH≈8, o que é condizente com os valores, obtidos na literatura tanto para a detecção eletroquímica da lidocaína [33-37], como para o desempenho eletroanalítico de CoO(OH) [41-46]. Disso é possível fazer conclusão de que CoO(OH) pode ser um modificador excelente de elétrodo para a eletrooxidação de lidocaína em meio levemente alcalino, quando mesmo o crescimento de pH da solução não influencia sobremaneira o processo eletroanalítico.
A reação realiza-se como um processo, controlado pela difusão do analito, ou pela reação deste com o oxihidróxido de cobalto (no caso da presença das concentrações relativamente grandes).
Já no caso da aplicação do pH inicial mais alto, especialmente em concentrações relativamente grandes do analito, e com um elétrodo relativamente pequeno, o estado estacionário desvia-se da estabilidade, porque o pH atinge os valores suficientes para dissolver CoO(OH), conforme a reação (4).
No caso da igualdade das influências desestabilizadoras superficiais e eletroquímicas às estabilizadoras, realiza-se a instabilidade monotônica, cuja aparição se dá, caso
Esta instabilidade se manifesta pelo trecho N-formado do voltamperograma, correspondente à existência de três estados estacionários num ponto, cada um instável.
Do ponto de vista eletroanalítico, a instabilidade é correspondente ao limite da detecção. Outrossim, neste sistema, é facilmente realizada no caso do uso de pH elevado, servindo de sinal de que o pH, crescendo ao longo da reação, atingiu o valor marginal, depois do qual a estabilidade do estado estacionário é comprometida.
No caso de meio neutro e levemente alcalino, é possível, também, simplificar este modelo generalista, eliminando dele a reação (4). A análise do modelo simplificado descrever-se-á num dos nossos próximos trabalhos.
CONCLUSÕES
A análise da possibilidade do uso de oxihidróxido de cobalto (III) deixou concluir que:
CoO(OH) pode ser um excelente modificador de elétrodo para a eletrooxidação de lidocaína em meio levemente alcalino. No processo eletroanalítico, a estabilidade do estado estacionário é fácil de manter e dá-se na vastidão da zona topológica de parâmetros, no caso da repulsão de partículas de CoO(OH) durante a sua dissolução, caso se realize, e na fraqueza da outras influências.
Dependendo da concentração do analito, do pH, do tamanho do elétrodo e do grau do recobrimento dele por CoO(OH), o processo é controlado pela difusão, ou pela reação.
O uso das soluções fortemente e, em alguns casos, moderadamente alcalinas pode levar à destrução do material e, como resultado, à ineficiência eletroanalítica do processo. O crescimento do pH é perigoso para a eficiência da análise com concentrações grandes e elétrodos pequenos. O estado estacionário será desestabilizado pelas influências superficiais e eletroquímicas.
O comportamento oscilatório neste sistema é possível, podendo, como em sistemas semelhantes, ser causado por influências superficiais da atração das partículas de CoO(OH) durante a sua dissolução, bem como pelas eletroquímicas das capacitâncias da dupla camada elétrica (DCE).
A amplitude e a frequência das oscilações neste sistema depende do pH da solução, sendo as oscilações mais prováveis no caso dos valores altos do potencial de hidrogênio.
A instabilidade monotônica, neste caso, é possível. Sendo correspondente ao limite de detecção, a sua ocorrência também indica a passagem do valor crescente do pH pela margem de estabilidade do estado estacionário.
No caso de meio neutro e levemente alcalino, o modelo generalista simplificar-se-á, eliminando-se-lhe a expressão, referente à reação (4).