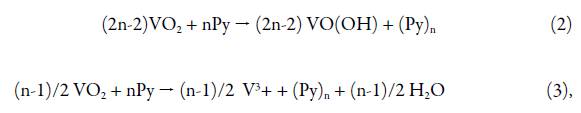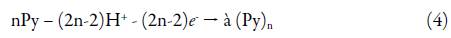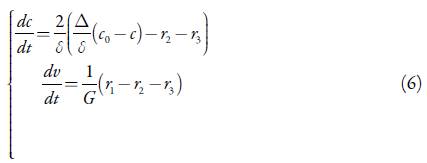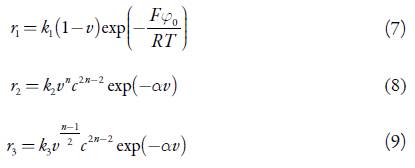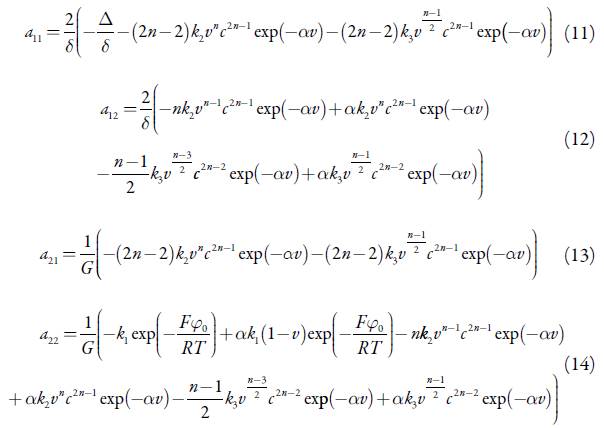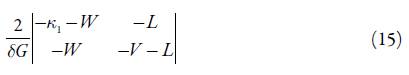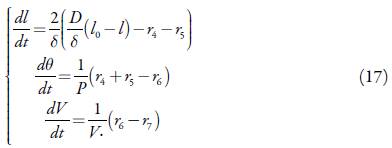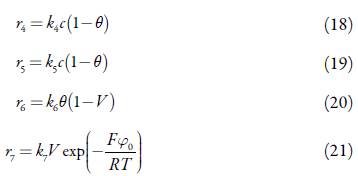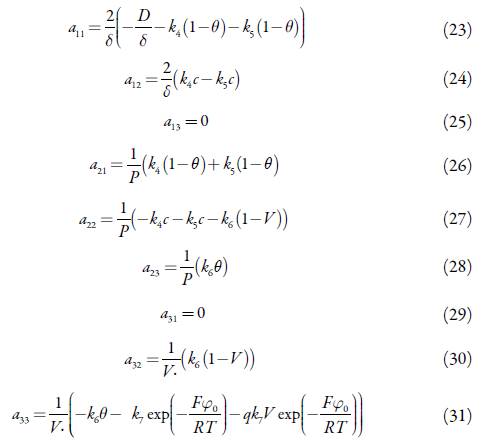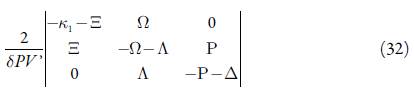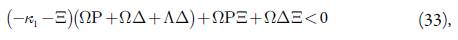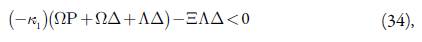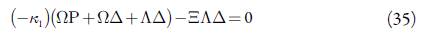INTRODUÇÃO
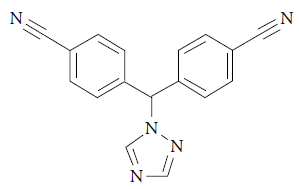
Letrozol, isto é 4-4'-((1H-1,2,4-triazol-1-il)metileno)dibenzonitrila, número CAS 112809-51-5, masa molar 285,303 g/mol (figura 1) é um composto inibidor de aroma-tases, usado para tratamento de diferentes tipos de câncer do pulmão [1-4]. Do ponto de vista químico, é um derivado triazólico, que contém dois grupos nitrila:
Além do seu uso no tratamento de câncer, o letrozol é amplamente usado, também, no tratamento de infertilidade como estimulador ovariano [5, 6] até por ter menos efeitos colaterais que clomifeno e, outrossim, por dar menos chances de gestação múltipla. Sem embargo, além da sua ação direta, o fármaco possui diferentes efeitos colaterais [7-10], como artralgia e fadigas. O seu uso excessivo em mulheres pode provocar a síndrome de hiperestimulação ovariana [9, 10]. Ademais, o seu uso duradouro e excessivo pode provocar osteoporose [11]. Destarte, o desenvolvimento de métodos da sua determinação é, deveras, uma tarefa atual [12-14], e o desenvolvimento de métodos eletroquímicos servir-lhe-iam de boa solução.
Existem trabalhos, em que o letrozol tem sido determinado eletroquimicamente [15-19]. O processo eletroanalítico estava sendo realizado mediante a redução catódica dos grupos nitrile laterais.
Um dos modificadores de elétrodo, capazes de ser usados na detecção eletroanalítica do letrozol pode ser polipirrol, que é um dos polímeros condutores mais usados nas cinco últimas décadas. Ele foi o primeiro polímero condutor, que veio a ser sintetizado química [20], e eletroquimicamente [21] e até agora ele e seus compósitos são amplamente usados na eletroanalítica como modificadores de elétrodos, agindo como substâncias ativas e(ou) mediadores de transferência de elétrons.
O desempenho do polipirrol ter-se-ia feito mais eficaz, se este fosse combinado com o oxihidróxido de vanádio (VO(OH)), um composto com comportamento eletroquí-mico flexível, mas mais acentuado para as propriedades redutoras [21]. No entretanto, por ora, nenhum trabalho acerca da modificação do elétrodo por VO (OH) para fins eletroanalíticos tem sido publicado (à exceção de alguns trabalhos teóricos do nosso grupo [22, 23], num dos quais foi comprovada a sua eficácia justamente com o letrozol [23]), e a introdução de um novo modificador de elétrodo pode acarretar os problemas como:
- Dependência entre a maneira de sintetizar o compósito e as suas propriedades (isto se refere não só à questão eletroanalítica em particular, senão às propriedades químicas em geral, bem como ao estado físico, em que o compósito está presente no elétrodo).
- A indecisão acerca do mecanismo mais eficiente-tanto da síntese do compósito (qual técnica é mais eficaz para o material ser utilizado em sensores-síntese eletroquímica ou química; e se for eletroquímica, se é codeposição anódica com polimerização direta, ou catódica, com a indireta?), como das questões comportamentais.
- A possibilidade das instabilidades eletroquímicas, características não só para a eletros-síntese e desempenho eletroanalítico dos polímeros condutores [24-26], como para a obtenção do oxihidróxido de cobalto [27-29], que é composto relacionado.
Para a resolução destes problemas na etapa do desenvolvimento da metodologia de produção do sensor e do seu desempenho, uma análise teórica a priori do comportamento de ambos os processos faz-se necessária-não só para compreender melhor os processos que ocorrem no sistema eletroanalítico, mas também para fazer o elétrodo resultante mais eficaz. Outrossim, mediante esta avaliação far-se-á possível comparar o comportamento do processo de eletrossíntese e detecção eletroanalítica do letrozol com os análogos.
Destarte, o objetivo geral deste trabalho é avaliar, mecanisticamente, o comportamento dos sistemas da preparação e desempenho do sensor, baseado no compósito de poli-pirrol com o oxihidróxido de vanádio, obtido, mediante uma metodologia de eletro-deposição catódica. Na primeira seção do presente trabalho, analisa-se o processo da eletrossíntese do compósito, e na segunda, analisar-se-á o desempenho do compósito.
SEÇÃO I. A ELETROSSÍNTESE
A eletrossíntese do compósito de polipirrol far-se-ia por uma técnica, parecida com a usada pelo grupo de pesquisadores sul-coreanos em [29], mas com o composto iniciador inserto na matriz, que cobre o cátodo. Na etapa inicial, o íon pervanadilo VO2+ é catodicamente reduzido, para formar o dióxido, conforme (1):
De fato, a depender do pH da solução e da concentração do monômero, existem dois cenários da polimerização do pirrol, que se divergem apenas pela forma, em que o vanádio trivalente aparece na superfície do cátodo:
podendo, inté, dar origem a um compósito ternário.
Tem-se em conta, também, a equação geral da polimerização do pirrol:
Destarte, para descrever o sistema da eletrossíntese do compósito polipirrol-oxihidró-xido de vanádio, por via catódica, considerando que, no início da reação, todos os sítios ativos do cátodo são ocupados pelo íon VO2+, introduzimos duas variáveis:
c: a concentração do monomer na camada pré-superficial
v: o grau do recobrimento da superfície pelo dióxido de vanádio.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente, o que nos deixa menosprezar o fluxo de convecção. Outrossim, supomos que o eletrólito de suporte esteja em excesso, o que nos deixa menosprezar o fluxo de migração. Ademais, considera-se que o perfil concentracional na camada pré-superficial seja lineal, e a sua espessura, constante, igual a 8.
É possível mostrar que o comportamento do sistema da eletrossíntese se pode descrever conforme o conjunto de equações diferenciais bivariante (5):
sendo c 0 a concentração do pirrol no interior da solução, Δ o seu coeficiente de difusão, G a concentração máxima do dióxido de vanádio e os parâmetros r, as velocidades das respectivas reações, que se podem calcular conforme (7-9):
sendo os parâmetros k as constantes das respectivas reações, a, o parâmetro, que relaciona o comportamento da dupla camada elétrica (DCE), com o grau do recobrimento do dióxido de vanádio, F é o número do Faraday, φ 0 é o salto do potencial na DCE, relativo ao potencial da carga zero, R é a constante universal de gases e T é a temperatura absoluta no sistema.
Neste caso, a eletrossíntese do compósito de polipirrol terá o comportamento mais dinâmico que nós já descritos [29, 30] processos catódicos, mas, por não haver instabilidades superficiais, menos dinâmica que durante a polimerização anódica direta [31]. As diferenças comportamentais entre esses processos descrever-se-ão abaixo.
RESULTADOS E DISCUSSÃO (SEÇÃO I)
Para investigar o comportamento do sistema com a eletrodeposição do compósito de polipirrol com os compostos de vanádio trivalente, analisamos o conjunto de equações diferenciais (6), haja vista as relações algébricas (7-9), mediante a teoria de estabilidade linear e análise de bifurcações. Os elementos estacionários da matriz funcional de Jacobi podem ser descritos como:
em que:
As condições principais dos pontos singulares para sistemas bivariantes são reunidas na tabela 1:
Tabela 1 As principais condições para sistemas bivariantes.
| Estabilidade do estado estacionário | Tr J<0, Det J>0 | |
| Comportamento oscilatório | Tr J=0, Det J>0 | |
| Instabilidade monotónica | Tr J<0, Det J=0 |
Para evitar as expresses grandes durante a análise da matriz, nós introduzimos as novas variáveis, de modo que os elementos da matriz se descrevem como:
Observando as expressões (11) e (14), pode-se ver que o comportamento oscilatório neste sistema é mais provável que no caso da presence do iniciador na solução [28, 29], mas menos prováveis que durante a eletropolimerização direta [30, 31], visto que a DCE é influenciada por mais de um processo, mas a instabilidade superficial é ausente.
Além das influências, que a DCE sofre durante a etapa eletroquímica (que produz o iniciador do crescimento do polímero), descritas pela positividade de
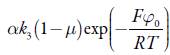 , o comportamento oscilatório pode, também, ser causado pelas influências da iniciação, que leva à apariçaõ do composto de vanádio trivalente e radi-cal-cátion do polipirrol. Essas influências são descritas pela positividade dos elementos
, o comportamento oscilatório pode, também, ser causado pelas influências da iniciação, que leva à apariçaõ do composto de vanádio trivalente e radi-cal-cátion do polipirrol. Essas influências são descritas pela positividade dos elementos
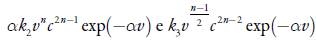 .
.
A condição de estabilidade do estado estacionário, para este sistema pode ser descrita conforme: Tr J<0, Det J>0 (vide a tabela 1). Abrindo os parênteses, obtê-la-emos conforme:
E esta condição é satisfeita de forma garantida, no caso da possibilidade dos parâmetros V e L, que descrevem a fraqueza das influências na DCE da formação do iniciador e da iniciação do crescimento da cadeia. O processo da eletrossíntese é controlado pela difusão do monômero, e a morfologia polimérica será menos desenvolvida que em [28, 29], sendo mais centrada aos sítios ativos de VO2+, posteriormente transformado em VO2 e VO(OH), na superfície, mas mais desenvolvida que em [30, 31], por a eletrodeposição anódica do polímero condutor sofrer influências das instabilidades superficiais.
A instabilidade monotônica, neste sistema, é possível, contrariamente ao caso, descrito em [28]. Isto é causado pela igualdade entre as influências estabilizadoras e desestabili-zadoras na DCE. A sua condição para a eletrossíntese do compósito pode ser descrita como:
CONCLUSÕES (SEÇÃO I)
Da análise da eletrossíntese teórica do compósito de polipirrol com os compostos do vanádio trivalente, principalmente, com o seu oxihidróxido VO(OH), é possível concluir que:
- A deposição catódica é realizada de forma eficiente, mas a morfologia do polímero resultante diferir-se-á tanto da obtida durante a codeposição anódica, como durante a deposição catódica com o iniciador na superfície.
- O processo da eletrossíntese é controlado pela difusão, e o estado estacionário estável é fácil de obter e manter.
- Contrariamente ao caso da presença do iniciador do crescimento da cadeia poli-mérica na solução, neste caso as instabilidades eletroquímicas são possíveis, sendo causadas única e exclusivamente pelas influências dos processos da eletrorredu-ção e da iniciação nas capacitâncias da DCE.
SEÇÃO II. DESEMPENHO
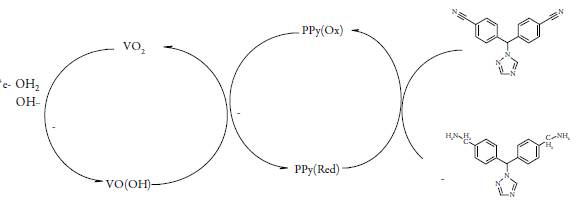
Como o letrozol contém os dois grupos nitrila, a sua detecção eletroquímica sobre o compósito polipirrol-VO(OH) dar-se-á conforme:
A redução eletroquímica far-se-á, prioritariamente, pelos grupos nitrila. No caso da aplicação dos potenciais catódicos mais baixos, o anel triazólico também será reduzido.
Neste caso, o polímero condutor age como substância ativa, e o oxihidróxido de vanádio, como mediador. O polímero condutor, além de reinforçar o desempenho do VO(OH), aumenta a sua estabilidade face os meios ácidos.
Destarte, para descrever o desempenho deste compósito, supondo o suposto na seção anterior, introduzimos as três variáveis:
l: a concentração do letrozol na camada pré-superficial
p: o grau do recobrimento da superfície pelo polímero condutor
V: o grau do recobrimento da superfície pelo dióxido de vanádio.
As equações de balanço, no modelo mais geral, incluirão, também a redução do anel triazólico e descrever-se-ão como:
Sendo as velocidades das respectivas reações:
Sendo os significados dos parâmetros análogos aos descritos na seção anterior.
RESULTADOS E DISCUSSÃO (SEÇÃO II)
Os membros estacionários da matriz de Jacobi para o sistema com o desempenho do compósito polipirrol-VO(OH) na detecção eletroanalítica de letrozol podem ser descritos como:
em que:
Aplicando o mesmo procedimento da seção anterior, observamos que o comportamento oscilatório neste sistema é possível; como nos sistemas análogos [32-35], ele é causado apenas pelas influências da etapa eletroquímica na dupla camada elétrica.
Para investigar a estabilidade do estado estacionário, aplicamos ao conjunto de equações diferenciais (17) o critério Routh-Hurwitz. Evitando as expressões grandes, introduzimos as novas variáveis, reescrevendo o determinante do jacobiano conforme:
Aplicando a condição Det J<0, saliente do critério, obtemos o requisito de estabilidade do estado estacionário como:
que se rearranja para:
e que é garantidamente satisfeito no caso da ausência ou fraqueza das influências da etapa eletroquímica na dupla camada elétrica. Deveras, no caso da satisfação da exigência supracitada, o parâmetro Δ terá valores positivos, e a expressão do lado esquerdo da inequação (34) desviar-se-á para valores mais negativos, o que é correspondente à estabilização do estado estacionário.
Do ponto de vista eletroanalítico, a estabilidade do estado estacionário é correspondente à dependência linear entre a concentração do analito (letrozol) e o parâmetro eletroquímico (neste caso, a corrente). Por isso, é possível concluir que o sistema eletro-analítico é eficiente. O processo eletroanalítico é controlado pela difusão.
A instabilidade monotônica, correspondente ao limite de detecção do ponto de vista eletroanalítico, também é possível para este sistema, e as suas condições descrevem-se como:
CONCLUSÕES (SEÇÃO II)
A investigação mecanística teórica do sistema da eletrorredução da letrozol, assistida pelo compósito de VO(OH) com o polipirrol deixou concluir que:
- O oxihidróxido de vanádio trivalente pode ser usado como um perfeito modificador de elétrodo para a quantificação de letrozol em meios neutro, leve e moderadamente ácido.
- O estado estacionário no sistema é fácil de obter e manter. A estabilidade do estado estacionário só pode ser atrapalhada por impactos da reação eletroquímica na DCE, que causam o comportamento oscilatório.
- A zona topológica da estabilidade do estado estacionário é muito vasta e a dependência linear entre o parâmetro eletroquímico e a concentração mantém-se facilmente.
- O comportamento oscilatório neste sistema é possível, mas menos provável que nos semelhantes, haja vista a ausência das instabilidades superficiais. Ele pode ter como única causa as influências da reação eletroquímica nas capacitâncias da DCE.
Do ponto de vista geral, ambos os sistemas se apresentam eficientes. Assim, do ponto de vista teórico existe pretexto forte de uso destes dois processos não só para a determinação do letrozol, mas também para outros fármacos com grupos aceptadores de elétrons.