Introducción
En el perro (Canis lupus familiaris), las articulaciones de la región del codo tienen elevado interés veterinario, debido a la cantidad de patologías que allí se diagnostican. Tanto por el número de casos como por los graves problemas locomotores que puede ocasionar en el paciente, la patología más importante del miembro torácico es de naturaleza congénita y se denomina displasia de codo (DC).
Los huesos de las articulaciones involucradas son tres: húmero, ulna y radio (1,2,3,4,5,6,7,8), que forman tres articulaciones (9,1,2,3,4,5,6,7,8,10,11):
Humeroradial: entre el capitulum humeri (cabecita del húmero) y la fovea capitis radii (fosita de la cabeza del radio); es la que transmite la mayor parte del peso soportado por el miembro torácico.
Humeroulnar: entre la trochlea humeri (tróclea del húmero) y la incisura trochlearis (incisura troclear) de la ulna; estabiliza y restringe el movimiento de la articulación a un plano sagital, es decir, flexión y extensión.
Radioulnar: entre la circumferentia articularis (circunferencia articular) del radio y la incisura radialis (incisura radial) de la ulna; permite la rotación del antebrazo (pronación y supinación).
La cápsula fibrosa de la sinovial es común a las tres articulaciones. En la parte craneal, se inserta proximalmente al foramen supratrochleare (foramen supratroclear). Caudalmente, la cápsula forma una bolsa que se inserta distalmente al foramen supratroclear, por lo que no hay comunicación entre las dos partes a este nivel (9,1,2,3,4,5,6,7,8,10,11). Distalmente, sobrepasa la incisura radial de la ulna y la circunferencia articular del radio.
Displasia del codo (DC) es un término general, usado para designar una enfermedad hereditaria poligénica del codo de los perros. Cuatro procesos la configuran, y pueden encontrarse independientemente o en combinación:
Fractura del processus coronoides medialis (proceso coronoides medial) (FPCM).
Osteocondritis disecante del condylus humeri (cóndilo del húmero) (ODCH).
No unión del processus anconeus (proceso ancóneo) (UPA).
Incongruencia entre radio y ulna.
Se da por hecho que la etiología de la DC es multifactorial. Según Morgan et al (12) y Degner (13), entre las principales causas que provocarían la aparición de los procesos antes enumerados (FPCM, ODCH, UPA e incongruencia), destacan las siguientes:
Elevada tasa de crecimiento: esta a su vez, estaría influenciada por la genética propia del animal y por la nutrición.
Microtrauma: debido a una concentración de fuerzas de apoyo en zonas determinadas del aparato locomotor.
Malformaciones congénitas
Todas ellas dan lugar a la aparición de osteocondrosis. Patología del cartílago que, mediante una de las cuatro formas de DC, progresa hasta la osteoartrosis, de la cual se derivan todos los problemas clínicos.
A partir de lo expuesto y con el objetivo de contribuir al mejor conocimiento de esta enfermedad, surge el interés por averiguar si hay alguna asociación entre la mecánica del funcionamiento de las articulaciones del codo y la DC. Planteamiento sintético, ya que desde la biomecánica es posible reunir aspectos morfológicos y funcionales, mediante un lenguaje físico, que abre la vía a la cuantificación de las observaciones mediante escalas numéricas.
Materiales y métodos
Se utilizó el miembro torácico derecho de un perro mestizo de 13 kg, proporcionado por el Servicio Municipal de Protección Animal del Ayuntamiento de Zaragoza, eutanasiado por causas ajenas a la investigación. No presentó externamente signos de anormalidad o alteración clínica. Sus características morfológicas fueron similares al promedio de los animales empleados en la disección de músculos y articulaciones, para obtener datos de referencia. La preparación del cuerpo fue llevada a cabo por el personal técnico del Departamento de Anatomía, en la sala de disección de la Facultad de Veterinaria de Zaragoza.
Modelización
El objetivo de esta etapa, conllevó la construcción de un modelo tridimensional, capaz de proporcionar información suplementaria acerca de la distribución de las fuerzas que actúan en la superficie articular del codo, en función de su estructura y de la disposición de sus materiales. A continuación, se presenta un diagrama que reúne los pasos que se siguieron:
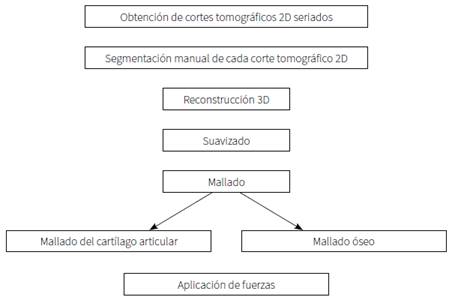
Obtención de cortes tomográficos 2D seriados
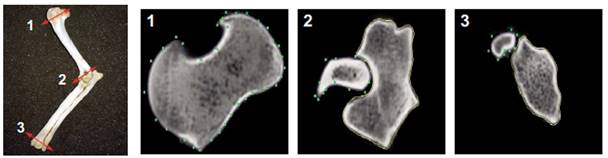
Se realizó un estudio de tomografía computarizada (TC) a los tres huesos implicados en la articulación del codo: húmero, radio y ulna. Se usó un tomógrafo multicorte Philips® para generar casi 600 láminas transversales, con una separación de 0.6 mm entre cada una de ellas (Figura 1).
Segmentación manual de cada corte tomográfico 2D
El contorno de las estructuras óseas se llevó a cabo mediante un programa informático, elaborado para ese fin, por el Grupo de Ingeniería Gráfica (GIGA) del Centro Politécnico Superior (CPS) de la Universidad de Zaragoza. Fue un proceso manual que hubo que realizar en cada uno de los casi 600 cortes tomográficos.
Reconstrucción 3D
La superposición ordenada de las tomografías 2D ya segmentadas permitió construir, mediante el programa I-DEAS 9.0, un primer armazón de lo que sería el modelo 3D.
I-DEAS 9.0 es un programa asistido por ordenador (CAD) que, habitualmente se emplea en ingeniería para diseño y cálculo de estructuras. Esto lo hace adecuado para el estudio biomecánico de las estructuras óseas del codo. En su aplicación se contó con el asesoramiento del Grupo de Estándares y Modelado de Materiales (GEMM) del CPS de la Universidad de Zaragoza. Este grupo tenía experiencia previa en el uso del software para el estudio de prótesis ortopédicas en medicina humana (Figura 2).
Aplicación de fuerzas
A los modelos de huesos 3D mallados mediante I-DEAS 9.0, se les aplicaron varios pesos para calcular la distribución de fuerzas a través de las mallas. El cálculo se realizó mediante el programa ABAQUS 6.3 (14). Los resultados se pueden visualizar mediante un código de colores.
Cada uno de los tres huesos: húmero, radio y ulna fueron considerados como cuerpos rígidos, y los cartílagos articulares como elásticos lineales, isótropos y homogéneos. La actuación de los músculos fue modelizada mediante la aplicación de las cargas equivalentes a sus fuerzas, aplicadas en sus respectivas inserciones.
Las fuerzas fueron aplicadas sobre el húmero mediante compresión, simulando la carga que tiene que soportar el miembro torácico durante la fase de apoyo, con la articulación del codo formando un ángulo de aproximadamente 135º.
Para definir el comportamiento de los diferentes materiales del modelo (hueso, cartílago articular, etc.) y aproximarlos lo más posible a su comportamiento fisiológico, fue preciso definir tanto su módulo elástico como su coeficiente de Poisson. Estos módulos son los que caracterizan el comportamiento ante las fuerzas de cada parte del modelo y permiten la simulación biomecánica, lo más cercana posible al comportamiento de los tejidos vivos.
Rango de fuerzas aplicadas
Según fuentes consultadas (15), el porcentaje de carga del peso del animal, que tienen que soportar los miembros torácicos, corresponde al 60 %. Por lo tanto, si queremos calcular que peso soporta uno de los miembros, habrá que usar al menos el 30 % del peso del animal. En este ejemplar, con un peso de 13 kg, corresponde a unos 4 kg. El rango de fuerzas añadidos al modelo, parte de un valor de 2 kg, inferior al que el miembro soportará cuando este animal está apoyado y en reposo. Incrementándolo kilo a kilo, se llegó a cargar con 14 kg, es decir, un 350 % superior a los 4 kg, que sirven como referencia. De esta manera, se dispuso de datos suficientes para conocer el rango completo de trabajo.
Resultados
El modelo biomecánico aplicado sobre el:
Húmero : (Figura 3a) muestra en todos los casos, que las regiones de la epífisis distal de este hueso, vinculada a la DC, están entre las que soportan menos esfuerzos. Por lo tanto, no se ve afectado de forma primaria por la biomecánica de la carga.
Radio : (Figura 3b) muestra que, de las tres partes de este hueso que acumulan las mayores concentraciones de cargas, solo dos están vinculadas a la DC. Una se puede relacionar con la explicación de la FPCM, por causas biomecánicas (16). La otra se relaciona con la interpretación de la incongruencia entre radio y ulna, por causas biomecánicas.
Ulna: (Figura 3c) muestra en todos los casos, que las regiones de la epífisis proximal de este hueso, vinculadas a la DC, están entre las que soportan menos esfuerzos. Consecuentemente, no se ve afectada de forma primaria por la biomecánica de la carga. Sin embargo, si se deforma por esta, como ocurre en los casos de incongruencias entre radio y ulna, debe existir previamente otra causa.
Cartílagos: (Figura 3d) en los datos referidos a ellos, se encuentra una concentración de tensiones, que no la hay en otros lugares de la articulación, precisamente, en el proceso coronoides medial. Lugar causal de la FPCM en la DC. Los datos procedentes del cartílago articular proximal de la ulna y radio, así como los procedentes del cartílago articular distal del húmero, ambos aislados del hueso, complementan los anteriores, ya que indican moderados incrementos de las cargas, en las zonas donde los huesos contactan, y elevadas, precisamente en el proceso coronoides medial, lugar ya resaltado antes.
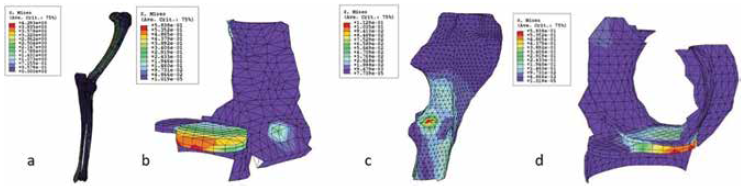
Fuente: elaboración propia
Figura 3 Modelo biomecánico aplicado sobre los componentes. Los colores rojo y morado visualizan respectivamente los mayores y menores esfuerzos mecánicos soportados, existiendo una gradación entre ambos
Compendiando los datos generales a todas las opciones revisadas, se encuentra que interpretar esta situación, desde el presupuesto de la bondad en la metodología seguida para construir y manipular el modelo, abre dos opciones, que además no son incompatibles:
El modelo no es capaz de cuantificar, el efecto de ciertos cambios.
La falta de continuidad en algunos resultados, se debe a cambios en las propiedades elásticas de los huesos estudiados. De manera que la ausencia de cambios, indica la absorción de las cargas mediante deformaciones microscópicas de la estructura ósea. Cuando los cambios son manifiestos, se ha superado la capacidad de absorción elástica por parte del hueso. Como consecuencia, en el hueso real se habrían producido microfracturas acumuladas, por causa de las grandes fracturas.
Discusión
Mediante el uso del modelo biomecánico, se han encontrado varias asociaciones entre el funcionamiento de las articulaciones del codo y las lesiones óseas de la DC. Ello confirma una de las etiologías propuestas para la DC, que con este trabajo ha pasado de ser meramente especulativa, a estar apoyada por su cuantificación.
La modelización informatizada, mediante reconstrucción 3D y control de la gestión de cargas, nos ha permitido conocer detalles biomecánicos precisos sobre la localización de las zonas óseas de las articulaciones del codo, que soportan más presiones durante su funcionamiento y que son coincidentes con los lugares lesionados en una DC. Esto será de utilidad a la hora de buscar lesiones mediante radiografías, en los animales con posible DC, así como para focalizar tratamientos, y plantear ejercicios paliativos y/o de recuperación, destinados a cada una de las posibles lesiones óseas asociadas a una DC.
Una limitación de esta metodología es que solo nos ha permitido cuantificar las cargas totales soportadas en zonas muy concretas del hueso. Una posible mejora sería poder modificar por separado la influencia de los músculos y tendones, con el objetivo de matizar los cambios que se producen bajo sus actuaciones.
Las conclusiones de este trabajo justifican plantear a futuro un estudio clínico-epidemiológico. Ello conlleva, entre otras cosas, desarrollar un procedimiento que automatice las medidas obtenidas y de esa forma, inferir conclusiones estadísticamente sostenibles.