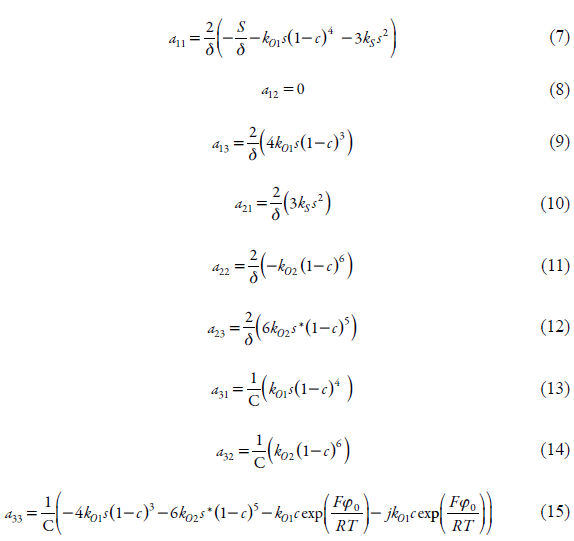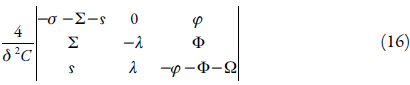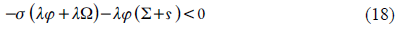INTRODUCCIÓN
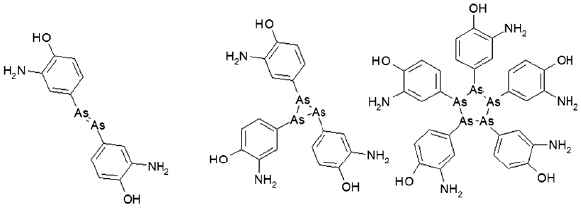
Arsfenamina, 3-3'diamino-4-4-dihidroxiarsenobenceno (figura 1, a la izquierda) (CAS: 139-93-5, M = 368 g/mol comercializada como Salvarsano y hasta como "compuesto 606", es uno de los fármacos ampliamente utilizados en el tratamiento de sífilis [1-5], siendo uno de los primeros desarrollados y usados para tratar esta enfermedad. Estudios recientes han mostrado que la arsfenamina suele entrar en la reacción de ciclooligomerización, formando un trímero y un pentámero (figura 1, al centro y a la derecha).
El compuesto fue desarrollado en 1910. Dos años más tarde apareció su derivado neo-salvarsano, más soluble en el agua y fácil de preparar. Ambos compuestos han sido usados no solo en el tratamiento de sífilis, sino en la cura de tripanosomiasis [5, 6]. Sin embargo, a pesar de su eficacia, el salvarsano y derivados no se pueden usar en grandes cantidades, por presencia de arsénico, cuyos compuestos son famosos por su toxicidad [7-10]. Además, hay dificultades en almacenar el salvarsano y derivados por su facilidad de oxidar (se usa la atmosfera de nitrógeno o gases nobles). Por eso el uso de salvarsano disminuyó en 1940 con el descubrimiento de penicilina. Hoy en día, el salvarsano solo se usa en algunos países de América Latina, de África subsahariana y de Asia. Por eso, el desarrollo de un método de su detección cualitativa y cuantitativa permanece actual [11-14].
Por ahora, no hay métodos electroquímicos de la detección de salvarsano. Sin embargo, los otros compuestos de arsénico han sido detectados electroquímicamente [15, 16]. Para tal, se han usado varios modificadores, incluyendo el oxihidróxido de cobalto [17-20], que es un semiconductor del tipo p, visto por investigadores como alternativa al dióxido de titanio.
Sin embargo, el uso de nuevos procesos electroanalíticos, antes de implementarlo debe ser analizado teóricamente. Esto resolvería problemas como:
- La indecisión acerca del mecanismo más probable de las etapas químicas y electroquímicas, que llevan a la aparición de la señal electroanalítica.
- La indecisión acerca de la secuencia y orden de reacciones, con las que se da el proceso electroanalítico.
- La posibilidad de realización de inestabilidades oscilatoria y monotónica, características para sistemas análogos [21-26].
Para resolver los tres problemas mencionados es importante llevar a cabo una investigación teórica a priori del comportamiento del sistema electroanalítico. Así, en este trabajo se investiga desde punto de vista matemático la posibilidad de determinación electroquímica del salvarsano en la presencia del oxihidróxido de cobalto, depositado sobre un colorante escuárico. Por el desarrollo del modelo y su análisis se verifican los requisitos de estabilidad de estado estacionario, como las condiciones de las inestabilidades oscilatoria y monotónica. Además, mediante el análisis teórico se compara (con exactitud y sin ensayos experimentales adicionales) el comportamiento de este sistema con los semejantes [27, 28].
Como la molécula de salvarsano contiene un exceso de electrones se oxida fácilmente. El oxihidróxido de cobalto podrá participar de su oxidación de diferentes maneras. En el caso de la oxidación del o-aminofenol se formará el CoO:
EL SISTEMA Y SU MODELO
El trímero cíclico, que se forma según la reacción (figura 3) se oxida por el oxihidróxido de cobalto con una facilidad aún mayor (figura 4).
Así, el comportamiento en el sistema se describirá por un conjunto de ecuaciones diferenciales de tres variables:
s: la concentración del salvarsano en la capa presuperficial.
s*: la concentración del ciclotrímero (sesquímero) de salvarsano en la capa presuperficial.
c: el grado de recubrimiento de la superficie de electrodo por el óxido de cobalto.
Para simplificar el modelo, suponemos que el reactor se agita intensamente, lo que permite ignorar el flujo de convección. Además, suponemos que el electrólito de soporte está presente en su exceso, dejándonos menospreciar el flujo de migración. Suponemos, también, que el perfil concentracional de las sustancias en la capa presuperficial es lineal, y su espesor, constante e igual a δ.
Se puede verificar que el comportamiento del sistema se describe por el conjunto de ecuaciones diferenciales (1):
Siendo S el coeficiente de difusión del salvarsano, s0 su concentración en el interior de la solución, C es la concentración superficial máxima del óxido de cobalto, rS es la velocidad de la sesquimerización (trimerización cíclica) y rO 1 , rO 2 y r 2 son velocidades de oxidaciones químicas y electroquímica. Las velocidades de reacciones respectivas se pueden calcular conforme:
En donde los parámetros k son constantes de velocidad de las respectivas reacciones, F es el número de Faraday, φ 0 es el salto de potencial en la doble capa eléctrica (DCE), relacionado al potencial de carga cero, R es la constante universal de gases y J es la temperatura absoluta.
En general, el comportamiento de este proceso se hace semejante al observado en estudios previos [17, 18]. Sin embargo, la presencia de dos formas de una sustancia impactará el comportamiento del sistema, conforme se describirá en el siguiente apartado.
RESULTADOS Y DISCUSIÓN
Para investigar el comportamiento del sistema con la detección electroanalítica del salvarsano, analizamos el conjunto de ecuaciones diferenciales (1) mediante la teoría de la estabilidad lineal. Los elementos estacionarios de la matriz Jacobiana se describen como:
Siendo:
Analizando las expresiones (7), (11) y (15), podemos averiguar que la inestabilidad oscilatoria en este sistema se puede realizar. Para que la bifurcación de Hopf, correspondiente a la inestabilidad oscilatoria, se lleve a cabo es necesario que haya elementos positivos en la diagonal principal de la matriz. El único elemento, que puede ser positivo, es
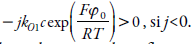 Así como en estudios previos [27, 28], esta positividad solo se obtiene con las influencias fuertes de la reacción electroquímica a la capacitancia de la DCE, que llevaran a cambios periódicos de la capacitancia y de la conductividad de la capa. Las oscilaciones son frecuentes y de poca amplitud.
Así como en estudios previos [27, 28], esta positividad solo se obtiene con las influencias fuertes de la reacción electroquímica a la capacitancia de la DCE, que llevaran a cambios periódicos de la capacitancia y de la conductividad de la capa. Las oscilaciones son frecuentes y de poca amplitud.
Para investigar la estabilidad de estado estacionario de este sistema, aplicamos al conjunto de ecuaciones diferenciales (2) el criterio Routh-Hurwitz. Simplificando el análisis de la matriz, introducimos nuevas variables, de modo que se describa su determinante conforme:
Abriendo los paréntesis y aplicando el requisito Det/<0, se obtendrá, después de reagrupados los elementos, la condición de estabilidad conforme (17):
Que solo puede no se realizarse si Ω <0, por causa de las influencias en la DCE ya descritas. Como la realización de esas influencias se da en condiciones bastante específicas, se puede afirmar que se trata de un sistema electroanalítico eficiente, que se controla tanto por la difusión como por las reacciones. Como no hay reacciones laterales capaces de comprometer la estabilidad y eficiencia del proceso electroanalítico, la estabilidad de estado estacionario describe la dependencia lineal entre el parámetro electroquímico y la concentración de fármaco.
Cuando el estado estacionario está en vigor, el determinante tiene valores negativos. Cuando el determinante se anula, se obtiene el límite de detección, descrito por la inestabilidad monotónica. Su punto sirve de margen entre estados estacionarios estables e inestables y, para el caso, se describe como:
La ciclooligomerización del salvarsano también se puede dar con la formación de un pentágono (figura 5).
Así, el modelo (2) se rectifica, incluyendo la formación del pentámero cíclico, alterándose las expresiones rS y rO2. Por lo demás, el comportamiento del sistema será el mismo.
CONCLUSIONES
A partir del análisis teórico de la detección electroquímica de salvarsano sobre el oxihidróxido de cobalto, en la presencia de ciclooligómeros, se concluye que:
- Pese que el mecanismo de la detección del analito sea híbrido, se trata de un sistema electroanalítico eficiente de un complejo estable.
- El proceso electroanalítico se controla de igual manera por la difusión o por la
- El comportamiento oscilatorio en este sistema es posible, porque la etapa electroquímica puede influir en la capacitancia, la conductividad y la fuerza iónica de la doble capa eléctrica.