Introducción
Los insectos escama (Hemiptera: Coccomorpha) son interesantes por su impacto en las actividades agrícolas (Dhaliwal et al. 2010): excretan sustancias azucaradas que sirven de medio de crecimiento de hongos causantes de fumagina, se alimentan de savia elaborada, poseen protección cerosa que los protege del ambiente y de los insecticidas, tienen asociación con hormigas, permiten el ingreso de patógenos y, en algunos casos, trasmiten toxinas o virus (McKenzie 1967; Kosztarab y Kozár 1988; Williams y Granara de Willink 1992; Gullan 1997; Gullan y Kosztarab 1997; Ramos y Serna 2004; Kondo et al. 2008a).
A nivel mundial, los insectos escama constituyen un importante grupo de plagas del café (Coffea spp.) (James 1935; Le Pelley 1973; Watson y Cox 1990; Culik et al. 2006; Barrera 2008; Sousa et al. 2012). En Colombia, desde 1930 se consideran el segundo grupo más importante de insectos plaga en este cultivo (Federación Nacional de Cafeteros 1932), destacándose Puto antioquensis (Murillo, 1931) (Putoidae) y Planococcus citri (Risso, 1813) (Pseudococcidae). En la década de los 70, se encontró en altas poblaciones en cafetales de Antioquia y Caldas (Benavides-Gómez y Cárdenas-Murillo 1977) a Neochavesia caldasiae (Balachowsky, 1957) (Rhizoecidae). Recientemente, las poblaciones de cocomorfos de raíz se han incrementado, tanto en etapa de almácigo como en establecimiento del cultivo, generando, en algunos casos, la muerte de las plantas antes del inicio de su producción, lo que obliga a llevar a cabo resiembras que aumentan los costos de producción (Villegas et al. 2009; Villegas-García y Benavides-Machado 2011; Federación Nacional de Cafeteros 2013; Gil et al. 2015).
Las siguientes especies están registradas en raíces de café en Colombia: Toumeyella coffeaeKondo, 2013 de la familia Coccidae; Puto barberi (Cockerell, 1895) y P. antioquensis (Murillo, 1931) de Putoidae; Neochavesia caldasiae (Balachowsky, 1957), N. eversi (Beardsley, 1970), Rhizoecus americanus (Hambleton, 1946), R. coffeae Laing, 1925 y Geococcus coffeaeGreen, 1933 de Rhizoecidae y Dysmicoccus brevipes (Cockerell, 1893), D. caribensisGranara de Willink, 2009, D. neobrevipes Bearsdley, 1959, D. texensis (Tinsley, 1900), D. varius Granara de Willink, 2009, Planococcus citri (Risso, 1813) y Pseudococcus jackbeardsleyiGimpel y Miller, 1996 de Pseudococcidae (Murillo 1931; Hambleton 1946; Balachowsky 1959; Benavides-Gómez y Cárdenas-Murillo 1977; Williams y Granara de Willink 1992; Gimpel y Miller 1996; Kondo 2001; Kondo et al. 2008b; Granara de Willink 2009; Villegas et al. 2009; Kondo 2013).
Pese a la importancia de estos insectos en el café y al desconocimiento taxonómico de las especies asociadas, hasta la fecha no se ha realizado un muestreo con los métodos adecuados que permita reconocer las especies que se alimentan de este cultivo. Por esta razón, el objetivo de esta investigación es aportar al conocimiento fitosanitario del cultivo de café en Colombia por medio de la determinación taxonómica de insectos escamas recolectados de raíces de café en los departamentos de Norte de Santander y Valle del Cauca.
Materiales y métodos
El muestreo se desarrolló por parte del Servicio de Extensión Rural de la Federación Nacional de Cafeteros (FNC), entre junio y septiembre de 2013. Los especímenes se recolectaron manualmente de raíces de plantas de café menores a 24 meses de establecimiento, en 73 fincas de los departamentos de Norte de Santander y Valle del Cauca. Los predios se seleccionaron aleatoriamente a partir del Sistema de Información Cafetera SICA de FNC. Las muestras se conservaron en etanol (76 %) y se rotularon con datos de campo.
El montaje de los especímenes en láminas para microscopía se realizó empleando el protocolo del Systematic Entomology Laboratory (SEL-USDA) (2014): evisceración con hidróxido de potasio al 10 %, deshidratación progresiva con etanol al 75, 86 y 96 %, tinción con fucsina ácida, aclarado con aceite de clavo y sellado permanente con bálsamo de Canadá. El estudio de morfología e identificación se realizó en el Museo Entomológico Agronomía Bogotá (UNAB) de la Facultad de Ciencias Agrarias Universidad Nacional de Colombia, en el Museo Entomológico “Marcial Benavides” (MEMB, Centro Nacional de Investigaciones de Café-Cenicafé), Landscape and Ornamental Pests Laboratory (Purdue University, EE.UU.) y SEL-USDA (EE.UU.). Para la observación macroscópica se emplearon estereomicroscopios Nikon MSZ-1. La observación microscópica se hizo en microscopios de contraste de fases Zeiss LSM 880, Olympus IX51 y Nikon Eclipse E6000. Las imágenes se tomaron y analizaron con los programas Axion Vision e Image-Pro Insigth 8.0.
Las identificaciones fueron corroboradas según su especialidad, por Dr. Takumasa Kondo (Corporación Colombiana para la Investigación-Corpoica, Colombia), Dra. Lucía Claps (Universidad de Tucumán, Argentina), Dr. Douglass Miller (USD-SEL, EE.UU.) y Scott Schneider (Universidad de Massachusetts, EE.UU.). Los especímenes estudiados y el material tipo de la especie descrita están depositados en el museo UNAB (números de catálogo para cada especie en la Tabla 1) y se dispusieron láminas de respaldo en MEMB.
La terminología morfológica sigue las propuestas de Hambleton (1946, 1977a, 1977b), Williams y Granara de Willink (1992), Kozár y Konczné (2007), Schneider y Lapolla (2011) y Ramos-Portilla y Caballero (2016). La descripción de la nueva especie se basa en la morfología externa de la hembra adulta. El material tipo está conformado por seis especímenes. Las medidas se presentan en orden holotipo y entre paréntesis paratipos; no todas las medidas consideran los seis especímenes. La longitud de antena, escudo clipeolabral, labio y trocánter corresponde a la parte media de cada segmento; la longitud de cada segmento de la pata corresponde a su margen externo y la longitud total de cada pata corresponde a la suma de fémur, tibia, tarso y uña. El largo y ancho de cada estructura corresponde a la sección más amplia marcada por una línea recta de cada segmento.
Resultados y discusión
Se procesaron e identificaron 768 especímenes a partir de 85 muestras. Se determinaron 21 especies en 12 géneros y cinco familias (Tabla 1). Pseudococcidae fue la familia más representativa con 10 especies, seguida por Rhizoecidae (7), Coccidae (1), Ortheziidae (1) y Putoidae (1). Estos resultados son los esperados, dado que las especies de Pseudococcidae tienen una alta plasticidad biológica que les permite habitar en estructuras aéreas y subterráneas y alimentarse de diferentes tejidos de la planta (McKenzie 1967; Williams y Granara de Willink 1992), de allí que existan cerca de 314 especies asociadas a raíces (McKenzie 1967; Williams 1985; Watson y Cox 1990; Ben-Dov 1994; Gimpel y Miller 1996; Kosztarab 1996; Miller y Arapu 1997; Hara et al. 2001; Culik et al. 2007; Danzig 2007; Kondo et al. 2008b; Granara de Willink 2009; Kaydan y Gullan 2012; Malumphy 2014; García-Morales et al. 2016; Gavrilov-Zimin y Kurochkin 2016), mientras que Rhizoecidae está compuesta exclusivamente por especies rizófagas (Hambleton 1946; Kozár y Konczné 2007; Schneider y Lapolla 2011).
Por otro lado, aunque Coccidae es la tercera familia más diversa de Coccomorpha (Ben-Dov y Hodgson 1997; García-Morales et al. 2016), las especies que la componen tienden a alimentarse de estructuras aéreas de la planta (Kosztarab y Kozár 1988), muestra de ello es que solo 32 especies han sido registradas alimentándose de tejido radical (Gill 1988; Kosztarab y Kozár 1988; Ben-Dov 1994; Kosztarab 1996; Kondo y Gullan 2004; Ben-Dov 2012; Kondo 2013; Moghaddam 2013; García-Morales et al. 2016). El número bajo de especies de Ortheziidae y Putoidae probablemente se debe a que son familias compuestas por menos especies respecto a Pseudococcidae y Coccidae y todavía existen vacíos en la información de su ecología y biología (Kozár 2004; Williams et al. 2011; Vea 2014). Por otra parte, Rhizoecidae tiene como mayor centro de diversidad el Neotrópico, mientras que para Ortheziidae es el Paleartico (Kozár 2004; Kozár y Konczné 2007).
Respecto a los hallazgos a nivel de género, en las cochinillas harinosas (Pseudococcidae, Putoidae y Rhizoecidae) se observa que los géneros con más especies correspoden a aquellos que mundialmente son más diversos, como Dysmicoccus Ferris, Puto Signoret y Rhizoecus Künckel d’Herculais (Hambleton 1976; Williams y Granara de Willink 1992; Kozár y Konczné 2007; Granara de Willink 2009; Williams et al. 2011; Ramos-Portilla y Caballero 2016).
Los resultados a nivel de especie muestran a Puto barberi como la más recurrente, presente en 64 (75 %) de las 85 muestras; este porcentaje es similar a los resultados reportados por Villegas-García y Benavides-Machado (2011) para los departamentos de Caldas, Cauca, Cundinamarca, Norte de Santander, Risaralda, Santander y Tolima, lo cual hace pensar que P. barberi es la especie con mayor distribución en Colombia. Toumeyella coffeae y Dysmicoccus varius representan el 40 % del total de los especímenes analizados. Estas especies no están registradas en trabajos previos, excepto aquellos en donde se describen, por lo que su hallazgo muestra que son potenciales nuevas plagas del café.
Se hace el primer registro de Dysmicoccus mackenziei, D. radicis y Mixorthezia minima para Colombia. Dysmicoccus mackenziei se lista con amplia distribución en Centro América y en Ecuador mientras que D. radicis tiene distribución restringida en Sur América (Surinam y Brasil) (Williams y Granara de Willink 1992; Granara de Willink 2009) y M. minima está registrada para Brasil (Kozár 2004).
Se registra por primera vez a M. minima y Phenacoccus solani Ferris asociadas a café. En el caso de M. minima no se registra información de asociación con plantas, aunque Kozár (2004) menciona haber recolectado los especímenes en musgo y hojarasca. Ph. solani está asociada a 29 familias botánicas, pero no existen registros de especies de Rubiaceae como hospedante (Williams y Granara de Willink 1992; Ben-Dov 1994; Granara de Willink y Szumik 2007).
Tabla 1 Listado de especies de insectos escama asociados a raíces de café en Norte de Santander (NS) y Valle del Cauca (VC). Se referencia información de la familia, especie, departamento donde fue recolectado en este estudio, además del número de catálogo del Museo Entomológico UNAB, distribución y hospedantes.
| Taxón | Departamento | N° Cat. UNAB | Distribución | Hospedante | Referencia bibliográfica |
|---|---|---|---|---|---|
| Coccidae | |||||
| Toumeyella coffeae Kondo, 2013 (Fig. 1A) | NS, VC | 1412 | Neotrópico | Coffea sp. | 32, 36 |
| Ortheziidae | |||||
| Mixorthezia minima Konczné y Kozár, 2004 1, 2 (Fig. 1B) | NS | 1806 | Neotrópico (Colombia1) | Suelo, Coffea arabica 2 | (22) |
| Pseudococcidae | |||||
| Dysmicoccus brevipes (Cockerell, 1893) | NS, VC | 1390 | Cosmopolita | [Polífaga] | 5, 6, 13, 14, 15, 23, 26, 30, 31, 34, 37 |
| Dysmicoccus caribensis Granara de Willink, 2009 | NS, VC | 1391 | Neotrópico | Café | 31 |
| Dysmicoccus mackenziei Beardsley, 1965 1 (Fig. 1C) | NS | 1393 | Cosmopolita (Colombia1) | [Polífaga] | 6, 8, 14, 15, 31 |
| Dysmicoccus neobrevipes Beardsley, 1959 | VC | 1394 | Cosmopolita | [Polífaga] | 10, 14, 15, 19, 20, 30, 31, 35 |
| Dysmicoccus radicis (Green, 1933) 1 (Fig. 1D) | NS | 1399 | Neotrópico (Colombia1) | Coffea sp., Cyperus hermaphroditus (Jacq.) Standl., 1916 | 1, 15, 31 |
| Dysmicoccus texensis (Tinsley, 1900) | VC | 1397 | Neártico, Neotrópico | [Polífaga] | 6, 14, 15, 19, 21, 30, 31 |
| Dysmicoccus varius Granara de Willink, 2009 (Fig. 1E) | NS | 1395 | Neotrópico | Coffea sp. | 31 |
| Phenacoccus solani Ferris, 1918 2 (Fig. 1F) | VC | 1404 | Cosmopolita | [Polífaga], Coffea arabica 2 | 6, 14, 15, 17, 30, 37 |
| Planococcus minor (Maskell, 1897) | VC | 1403 | Cosmopolita | [Polífaga] | 12, 14, 15, 21, 30, 37, 38 |
| Pseudococcus elisae Borchsenius, 1947 | NS, VC | 1405 | Neotrópico | [Polífaga] | 11, 14, 16, 27 |
| Pseudococcus landoi (Balachowsky, 1959) | VC | 1406 | Neártico, Neotrópico | 4, 14,15, 16 | |
| Putoidae | |||||
| Puto barberi (Cockerell, 1895) (Fig. 1G) | NS, VC | 1408 | Neotrópico | [Polífaga] | 6, 14, 15, 19, 30, 33 |
| Rhizoecidae | |||||
| Geococcus coffeae Green, 1933 (Fig. 1H) | NS, VC | 1400 | Cosmopolita | [Polífaga] | 1, 7, 25, 28, 29 |
| Neochavesia caldasiae (Balachowsky, 1957) (Fig. 1I) | VC | 1401 | Neotrópico | Musa sp., Coffea arabica | 3, 18, 24, 29, 32 |
| Pseudorhizoecus bari n. sp. Caballero y Ramos (Fig. 1J) | NS | 1807 | Colombia | Coffea arabica | |
| Rhizoecus americanus (Hambleton, 1946) | VC | 1326 | Cosmopolita | [Polífaga] | 2, 9, 14, 15, 19, 25, 29, 39 |
| Rhizoecus coffeae Laing, 1925 | NS | 1409 | Neotrópico | [Polífaga] | 1, 14, 15, 29 |
| Rhizoecus colombiensis Ramos y Caballero, 2016 (Fig. 1K) | VC | 678 | Neártico, Neotrópico | [Polífaga] | 40 |
| Ripersiella andensis (Hambleton, 1946) | VC | 1411 | Neotrópico | Musa sp., Coffea arabica | 2, 14, 15, 29 |
1Nuevo registro de especie para el país; 2Nuevo registro de hospedante. Referencias bibliográficas: 1. Green (1933). 2. Hambleton (1946). 3. Balachowsky (1957). 4. Balachowsky (1959). 5. Beardsley (1959). 6. McKenzie (1967). 7. Williams (1968). 8. Williams y McKenzie (1971). 9. Hambleton (1976). 10. Beardsley et al. (1982). 11. Beardsley (1986). 12. Cox (1989). 13. Orellana y Vera (1989). 14. Williams y Granara de Willink (1992). 15. Ben-Dov (1994). 16. Gimpel y Miller (1996). 17. Kosztarab (1996). 18. Johnson et al. (2001). (19. Kondo (2001). (20. Miller y Williams (2002). 21. Santa-Cecilia et al. (2002). 22. Kozár (2004). 23. Ramos y Serna (2004). 24. Williams (2004a). 25. Williams (2004b). 26. Watson y Kubiriba (2005). 27. Culik et al. (2006). 28. Kianek et al. (2007). 29. Kozár y Konczné (2007). 30. Kondo et al. (2008b). 31. Granara de Willink (2009). 32. Villegas-García y Benavides-Machado (2011). 33. Williams et al. (2011). 34. Ben-Dov (2012). 35. Tanaka y Uesato (2012). 36. Kondo (2013). 37. Moghaddam (2013). 38. Malumphy (2014). 39. Ramos-Portilla et al. (2014). 40. Ramos-Portilla y Caballero (2016).
Pseudorhizoecus bari n. sp. Caballero y Ramos (Fig. 1J)
Material tipo
Pseudorhizoecus bari n. sp. HOLOTIPO: ♀ adulta, en raíces de café, Coffea arabica L., 1753 (Rubiaceae). COLOMBIA. Norte de Santander. Convención, Vda. El Retiro, Fca. Monte Cristo, 1242 msnm. Captura manual. 11-jun-2013 [UNAB]. PARATIPOS: 3 ♀ adultas + 2 ♀ de tercer instar ninfal, datos iguales al holotipo [UNAB]. Machos no observados.
Etimología. Esta especie es nombrada en homenaje a la etnia indígena Barí, quienes habitan la región donde se recolectó el material tipo, nombre en aposición.
Descripción
En vivo de color blanco o blanco cremoso, circular, sin recubrimiento de cera (Fig. 1J). En lámina de microscopia: Cuerpo (Fig. 2) subcircular, 1,2 (0,7-1,1) mm de largo, 1 (0,5-0,9) mm de ancho. Órgano genital visible en dos paratipos (75 y 87 µm de largo).
Dorso. Ostiolos ausentes. Ano: anillo anal circular u ovalado, 80 (67-75) µm de diámetro, rodeado por un área esclerosada delgada con 23 (21) setas flageladas, 35-60 µm de largo, sin celdas, con dos o tres protuberancias. Lóbulos anales no diferenciables en Holotipo y ligeramente desarrollados en hembras adultas tenerales, con setas no diferenciables a otras del segmento. Setas corporales flageladas, en bandas intrasegmentales desde mesotórax hasta cauda; cefálicas y protorácicas en un único grupo; longitud de setas en últimos segmentos abdominales progresivamente más largas. Conductos tubulares, bitubulares y tritubulares ausentes. Poros triloculares 3-4 µm de diámetro, distribuidos en toda la superficie; poros discoidales y multiloculares ausentes. Espículas presentes, evidentes en abdomen posterior.
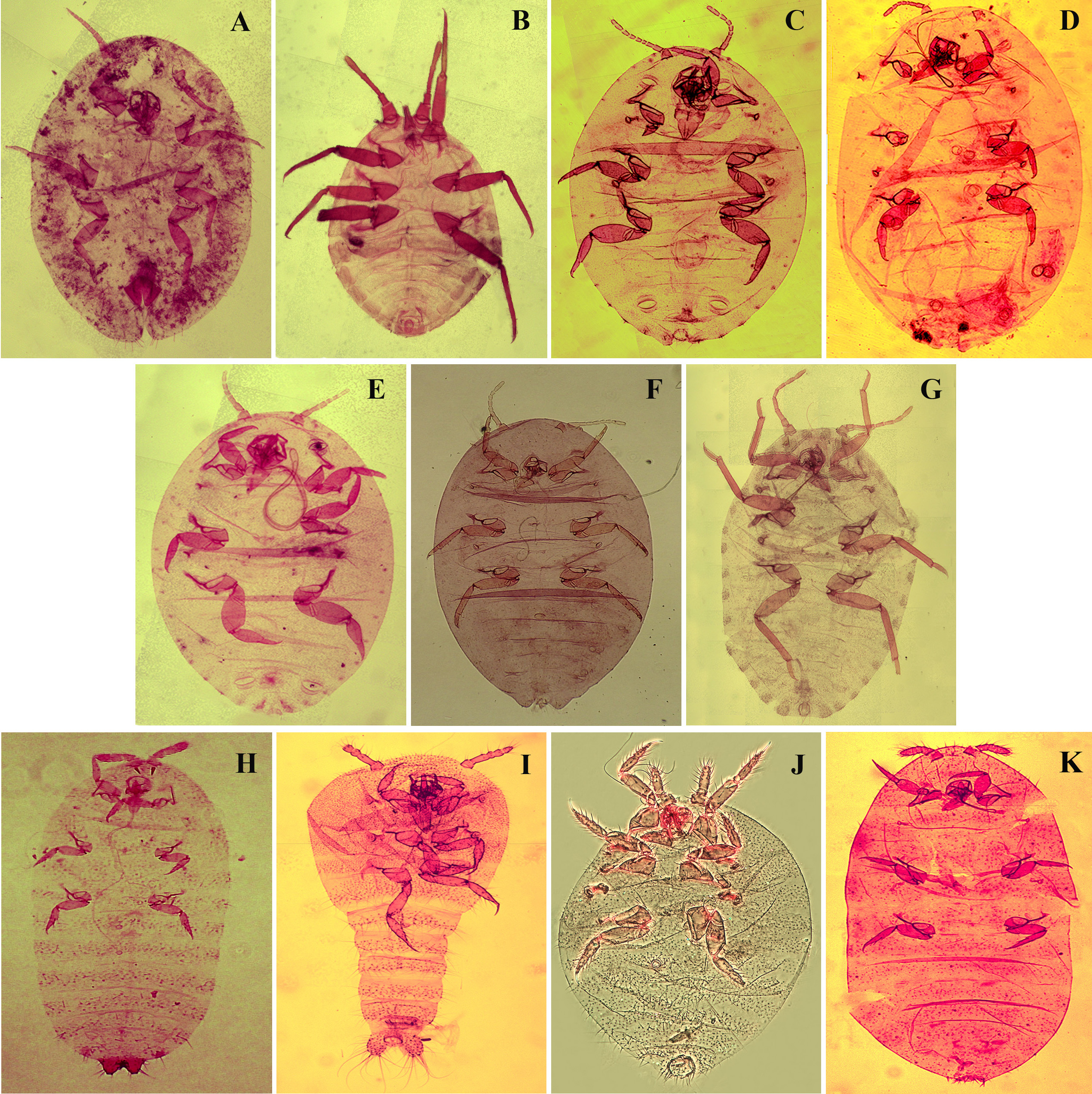
Figura 1 Hábitus de A. Toumeyella coffeae. B. Mixorthezia minima. C. Dysmicoccus mackenziei. D. Dysmicoccus radicis. E. Dysmicoccus varius. F. Phenacoccus solani. G. Puto barberi. H. Geococcus coffeae. I. Neochavesia caldasiae. J. Pseudorhizoecus bari n. sp. K. Rhizoecus colombiensis.
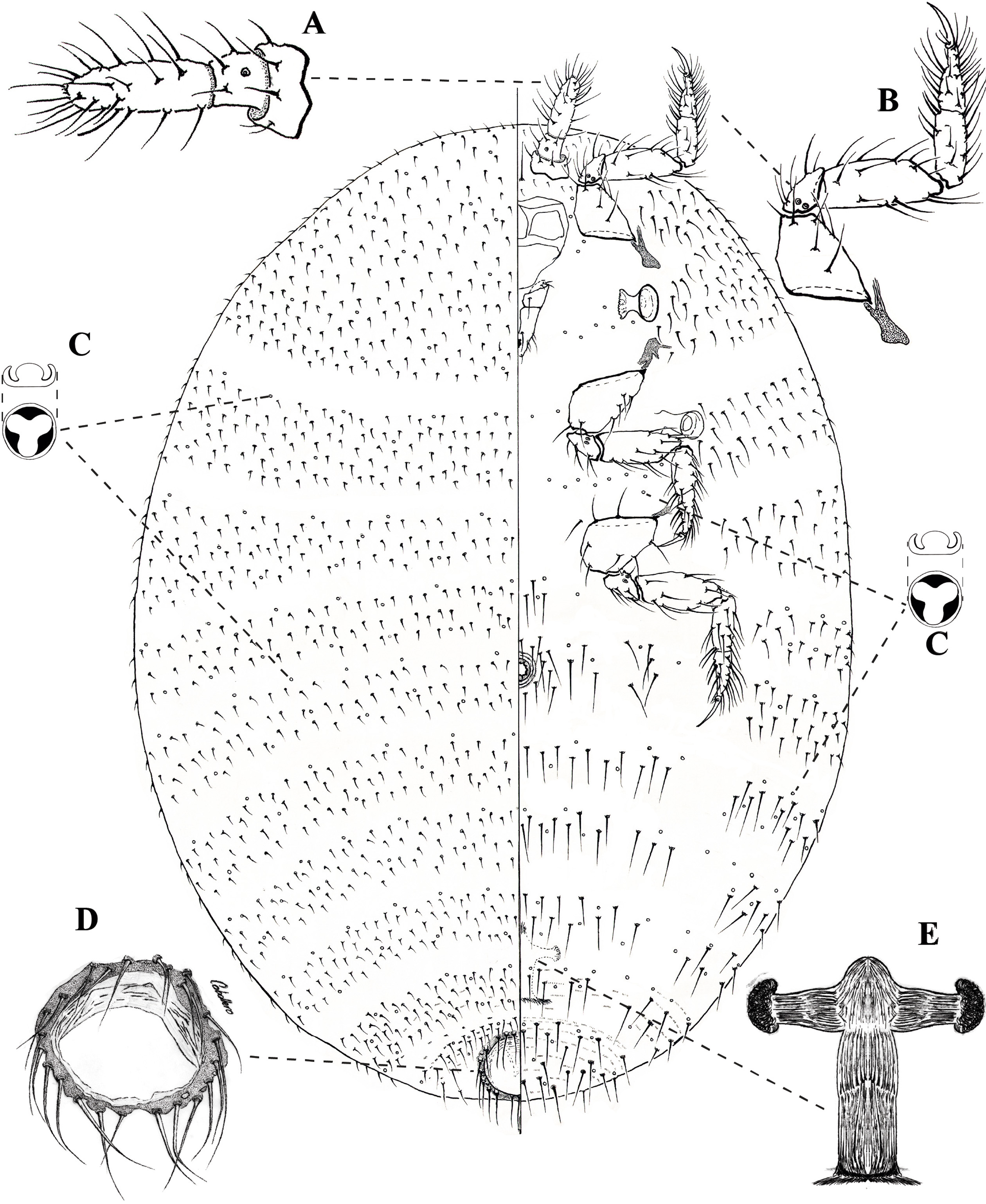
Figura 2 Pseudorhizoecus bari n. sp. Caballero y Ramos, hembra adulta. Ampliación de: A. Antena. B. Pata anterior. C. Poro trilocular. D. Anillo anal. E. Cámara genital.
Vientre: Ojos ausentes. Placa cefálica no visible. Antena de tres segmentos, 127 (130-133) µm de largo: segmento I: largo 33 (29-32) µm, ancho 53 (47-53) µm, cinco setas flageladas; segmento II: largo 21 (20-21) µm, ancho 31 (31-35) µm, tres setas flageladas y un sensorio campaniforme; segmento III: largo 82 (80-81) µm, ancho 27 (28-31) µm, dos setas de ápice truncado, apicales, 5 µm de largo, dos sensorios filiformes delgados, de ápice redondeado, distales, en margen externo, 33 µm de largo, 23 setas flageladas. Escudo clipeolabral: largo 102 µm, ancho 108 µm. Labio de tres segmentos: basal membranoso, medio y apical esclerosados; tres, uno y siete pares de setas flageladas respectivamente; largo 96 µm. Patas caminadoras; coxas con 11 setas flageladas; trocánteres con cinco setas flageladas y cuatro sensorios campaniformes; todos los tarsos con una sensorio campaniforme basal en margen externo; uñas con digítulos setosos, delgados, más cortos que la uña, 10-12 µm de largo, dentículo ausente. Propatas: largo 273 (233-289) µm; fémur: largo 106 (109-115) µm, ancho 42 (38-44) µm, 15 setas flageladas; tibia: largo 53 (65-73) µm, ancho 30 (26-30) µm, 14 setas flageladas, en filas longitudinales y dos espuelas preapicales en margen interno; tarso: largo 49 (49-51) µm, ancho 25 (22-25) µm, 20 setas flageladas, en filas longitudinales y una espuela en margen interno; uña: largo 52 (48-50) µm. Mesopata: largo 281 (274-286) µm: fémur: largo 111 (108-115) µm, ancho 41 (44-50) µm, 15 setas flageladas; tibia: largo 68 (62-70) µm, ancho 32 (28-30) µm, 15 setas flageladas y dos espuelas preapicales marginales internas (una más robusta que la otra); tarso: largo 52 (50-52) µm, ancho 25 (23-25) µm, 20 setas flageladas, una espuela preapical en margen interno; uña: largo 50 (47-52) µm. Metapata: largo 287 (287-297) µm; fémur: largo 106 (114-117) µm, ancho 48 (45-54) µm, 16 setas flageladas; tibia: largo 67 (66-74) µm, ancho 33 (32-38) µm, 16 setas flageladas y dos espuelas preapicales en margen interno; tarso: largo 56 (52-56) µm, ancho 25 (24-28) µm, cada una con 19 setas flageladas y una espuela proximal en margen interno; uña: largo 58 (50-55) µm. Círculo en segmento abdominal III, protruido, en forma de cono truncado, cima irregular, diámetro basal 42 (40-42) µm, diámetro apical 30 (21-28) µm. Vulva mesial entre segmentos abdominales VII y VIII (evidente en paratipos).
Poros triloculares: diámetro 3-4 µm; distribuidos en la superficie. Poros multiloculares y discoidales ausentes. Conductos tubulares, bitubulares y tritubulares ausentes. Setas corporales flageladas: en cabeza, dos setas flageladas, anteromesiales, de 35 (35-42) µm, en el espacio interantenal, las demás setas son flagelas, conspicuamente más cortas que las anteriormente descritas; en tórax, ausentes en área mesial, submesial y áreas intersegmentales, presentes en áreas submarginales y marginales, formando grupos en cada segmento torácico, el grupo del segmento protorácico se une a las setas cefálicas; en abdomen se presentan dos tipos de setas flageladas: I) setas conspicuamente largas (30-40 µm), rectas y robustas presentes en mesón y submesón, en filas transversales a cada segmento, II) setas cortas (5-10 µm), curvas y delgadas, intrasegmentales desde el submargen hasta el margen, ausentes de áreas laterales y espacios intersegmentales. Espículas presentes en toda la superficie.
Diagnosis
Pseudorhizoecus bari n. sp. puede ser diferenciado de Pseudorhizoecus proximusGreen, 1933 porque el primero presenta antena con tres segmentos, círculo presente y anillo anal con más de 20 setas flageladas; en tanto que P. proximus presenta antenas de 5 segmentos, círculo ausente y anillo anal con 2-5 setas. También puede ser confundido con Ripersiella colombiensis (Hambleton, 1946) por la forma del cuerpo, la abundancia de setas corporales y la presencia de círculo; sin embargo, R. colombiensis posee antenas con 5 segmentos y un anillo anal con seis setas flagelas y dos bandas de celdas anales evidentes.
Esta especie presenta tres atributos poco frecuentes dentro de la familia Rhizoecidae: ausencia de conductos de cualquier tipo, antena de tres segmentos y anillo anal sin celdas, con más de 20 setas rodeando la apertura. Dentro de la subfamilia Rhizoecinae Williams, donde se ubica Pseudorhizoecus Green, la ausencia de conductos tubulares, bi o tritubulares es característico únicamente de géneros monotípicos como Brevicoccus Hambleton, Capitisetella Hambleton y Lepthorhizoecus Williams y la especie R. colombiensis (Green 1933; Hambleton 1946; Hambleton 1977a; Williams 1998; Kozár y Konczné 2007), es decir, solo en cinco especies de las cerca de 200 que componen a la subfamilia. Por otro lado, en la misma subfamilia no existen especies descritas con antenas de tres segmentos; este atributo se presenta sólo en el género Eumyrmococcus Silvestri, perteneciente a la subfamilia Xenococcinae (Tang) (Kozár y Konczné 2007; Schneider y Lapolla 2011). El anillo carente de celdas también es atípico, presente solo en P. proximus pero este último posee 2-5 setas anales (Green 1933; Williams 1998; Kozár y Konczné 2007; Schneider y Lapolla 2011).
Pseudorhizoecus Green, antes de esta publicación, pertenecía a un grupo de géneros monotípicos de la subfamilia Rhizoecinae; su especie Tipo, P. proximus Green, está restringida a la región Neotropical y está registrada en Colombia, Costa Rica, Ecuador, Guatemala y Surinam; asociada con Coffea sp., C. arabica, C. liberica, Musa sapientum, Musa sp. y Theobroma cacao (Williams y Granara de Willink 1992; Kozár y Konczné 2007).
Debido a los argumentos arriba explicados, la clasificación taxonómica de Pseudorhizoecus bari n. sp. está abierta a la discusión; su ubicación temporal dentro de Pseudorhizoecus se debe a la semejanza en la mayoría de caracteres morfológicos, datos de ubicación y hospedantes. Se espera que el incremento de especímenes recolectados, a través de muestreos más detallados, puedan ayudar a la clarificación de la ubicación taxonómica de esta especie.
Conclusiones
Esta investigación proporciona información necesaria para actualizar la lista de especies asociadas a la rizósfera de café. Actualmente Puto barberi es la especie de cocomorfos, de hábito rizófago, de mayor distribución en la caficultura de los departamentos de Norte de Santander y Valle del Cauca.
Especies de reciente descripción como Dysmicoccus varius y Toumeyella coffeae, están presentando una distribución más amplia, en comparación con investigaciones recientes donde D. texensis y D. brevipes eran las más distribuidas; esto demuestra que las dinámicas poblacionales de cocomorfos son variables espacio-temporalmente. El hábito hipogeo de estos insectos los hace pasar desapercibidos y son difíciles de detectar en campo; sin embargo, los nuevos registros para el cultivo del café y para Colombia, soportan la idea de Kozár y Konczné (2007) y Villegas et al. (2009) que los insectos escama de raíces son insectos que aún carecen de estudios de taxonomía. Esta investigación puede ser un ejemplo metodológico para conocer la fauna de cocomorfos hipogeos asociados a cultivos.














