Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Acta Medica Colombiana
versão impressa ISSN 0120-2448
Acta Med Colomb vol.48 no.1 Bogotá jan./mar. 2023 Epub 29-Mar-2024
https://doi.org/10.36104/amc.2023.2635
Presentación de Casos
Movimientos coreiformes y calcificaciones ganglio basales como presentación de la enfermedad de Fahr
cResidente de Psiquiatría. Universidad del Norte. Barranquilla (Colombia).
Las calcificaciones ganglio basales pueden ser un hallazgo radiológico en la población general alrededor de 20%. Cuando se asocia a síntomas neuropsiquiátricos y motores y se presenta de forma idiopàtica, se le conoce como enfermedad de Fahr. Se le denomina síndrome de Fahr en el caso que sea secundario a una causa identificable y potencialmente tratable. Presentamos en este reporte un caso clínico de una mujer de 69 años con la aparición de una corea subaguda, sin otra sintomatologia asociada, en la que se encontró en la neuroimagen calcificaciones ganglio basales extensas, y por esta razón posteriormente se descartaron alteraciones metabólicas. El objetivo es aportar a la caracterización de las manifestaciones motoras que pueden aparecer e incitar a la sospecha clínica. Debido a la baja incidencia y a los pocos datos sobre esta entidad clínica en la región, queremos motivar a la documentación de otros casos y el proceso para descartar otros diagnósticos diferenciales, con el fin de obtener mayores datos sobre su epidemiología real y semiología en Colombia. (Acta Med Colomb 2022; 48. DOI:https://doi.org/10.36104/amc.2023.2635).
Palabras clave: enfermedades de los ganglios basales; calcio; enfermedades neurodegenerativas; corea; encefalopatías
Basal ganglia calcifications may be a radiological finding in approximately 20% of the general population. When they are associated with neuropsychiatric and motor symptoms in an idiopathic form, they are known as Fahr's disease. They are termed "Fahr's syndrome" when they are secondary to an identifiable and potentially treatable cause. In this report, we present the clinical case of a 69-year-old woman with the onset of subacute chorea, with no other associated symptoms, in whom extensive basal ganglia calcifications were found on neuroimaging, due to which metabolic disorders were subsequently ruled out. The objective is to contribute to the characterization of the potential motor manifestations which would give rise to clinical suspicion. Due to its low incidence and the little information on this condition in the region, we want to encourage documentation of other cases and the process for ruling out other differential diagnoses, in order to obtain more information on its actual epidemiology and signs and symptoms in Colombia. (Acta Med Colomb 2022; 48. DOI:https://doi.org/10.36104/amc.2023.2635).
Keywords: basal ganglia diseases; calcium; neurodegenerative diseases; chorea; encephalopathies
Introducción
Las calcificaciones ganglio basales pueden ser un hallazgo radiológico en la población general alrededor de 20% y una variedad de condiciones médicas se han documentado en las que pueden estar presentes, tanto idiopáticas como secundarias a otros trastornos 1,2. Tal es el caso de la enfermedad de Fahr, el cual es un trastorno neurodegenerativo poco común y que existen muy pocas publicaciones en Colombia 3. Consiste en calcificaciones idiopáticas bilaterales de los ganglios basales que se expresan clínicamente con manifestaciones neuropsiquiátricas y/o síntomas motores. Por lo general, la edad de inicio es entre los 30 y 60 años con progresión gradual de la sintomatologia, no se ha identificado una correlación entre la edad de aparición, la extensión de los depósitos de calcio y los déficits neurológicos 4. A través de los años ha sido también conocida cómo calcificación ganglio basal idiopàtica, calcinosis bilateral estriato pálido dentada (BSPDS por sus siglas en inglés) y calcificación cerebral familiar primaria (PFBC, por sus siglas en inglés) 2. Por otro lado, la denominación de síndrome de Fahr se le atribuye a aquel con una causa etiológica identificable y potencialmente tratable, este se ha asociado mayormente a enfermedades endocrinas que afectan el metabolismo del calcio y fósforo como el hipoparatiroidismo, pero también a infecciones, neuroinfecciones, exposición a tóxicos, patologías inmunológicas, entre otras causas 2.
Presentamos el caso de una paciente que presentó movimientos coreicos como única manifestación clínica y hallazgo tomográfico de calcificaciones en los ganglios de la base extensas.
Presentación del caso
Paciente mestiza de 69 años de edad natural de Tubará, Atlántico, residente y procedente del municipio de Galapa, Atlántico. Ingresa por presentar aparición súbita de movimientos estereotipados de alta amplitud, arrítmicos, sin ningún propósito en las cuatro extremidades y región orolingual con predominio en el hemicuerpo derecho, que no cedían durante el sueño. Antecedente de diabetes mellitus tipo 2 en manejo con esquema de insulinas basal bolos de reciente instauración a dosis total de 36 unidades diarias, metformina 850 mg/día y glibenclamida 5 mg/cada 12 horas
Al examen físico se encontró en buenas condiciones generales, signos vitales dentro de la normalidad, alerta y orientada, pupilas isocóricas, normorreactivas a la luz, sin disminución de la fuerza muscular en las cuatro extremidades, normorrefléxica, sin déficit sensitivo. A la evaluación motora se observaron movimientos involuntarios, arrítmicos, de frecuencia errática y de alta amplitud en extremidades superiores e inferiores, de predominio en hemicuerpo derecho, que no alteraban la aprehensión: los cuales se describieron como corea.
Se solicitaron paraclínicos iniciales de valoración encontrándose hemograma, electrolitos séricos, función renal, tiempos de coagulación, bilirrubinas, colesterol y transaminasas dentro de la normalidad, glicemia en rangos de hipoglucemia, y valores elevados de hemoglobina glicada. A continuación los resultados: hemograma: leucocitos 4740/ uL, glóbulos rojos 4.620.000/uL, hemoglobina 12.7 g/dL, hematocrito 35.6%, volumen corpuscular medio 76.9 fL, hemoglobina corpuscular media 27.4 pg, concentración de hemoglobina corpuscular media 35.5 g/dL, ancho de distribución eritrocitaria 13.1%, amplitud de distribución eritrocitaria 2.84 g/dL, plaquetas 211 x10.e3 /uL, volumen medio plaquetario 8.0 fL, ancho de distribución plaquetario 59.4%, porcentaje de granulocitos 67.0%, porcentaje de linfocitos 24.7%, porcentaje de monocitos 4.4%, porcentaje de eosinófilos 1.5%, porcentaje de basófilos 0.4%, porcentaje células grandes no teñidas (LUC) 2.0, recuento de granulocitos totales 3.18 x10.e3 /uL, recuento de linfocitos totales 1.17 x10.e3 /uL, recuento de monocitos 0.21 x10. e3 /uL, recuento de eosinófilos 0.07 x10.e3 /uL, recuento de basófilos 0.02 x10.e3 /uL, recuento células grandes no teñidas 0.09 x10.e3 /uL; potasio en sangre: 4.16 meq/L; sodio en sangre: 139.6 meq/L; nitrógeno uréico: 11.21 mg/ dL; urea: 24 mg/dL; creatinina en sangre: 1.28 mg/dL; microalbuminuria: 10 mg/L; tiempo parcial de tromboplastina: 25.7 seg; tiempo de protrombina: 10.3 seg; bilirrubina total: 0.96 mg/dL; bilirrubina directa: 0.43 mg/dL; bilirrubina indirecta: 0.53 mg/dL; aspartato aminotransaminasa (AST): 15 U/L; alanina aminotransaminasa (ALT): 21 U/L; colesterol total: 208 mg/dL; colesterol HDL: 49.5 mg/dL; colesterol LDL: 128 mg/dL; Triglicéridos: 145 mg/dL; hemoglobina glicosilada: 6.4%; glicemia: 38 mg/dL.
La tomografia de cráneo simple mostró signos de atrofia cortical leve. A nivel del tallo cerebral, ganglios basales y ventrículos laterales se observan hiperdensidades de forma anular de bordes irregulares bilaterales, comprometiendo: corteza cerebelosa de predominio en el hemisferio izquierdo, cabeza del núcleo caudado, cápsula interna y núcleo lenticular de predominio en el hemisferio derecho (Figura 1). Se inició manejo sintomático con haloperidol vía oral a dosis de 2.5 mg/cada 8 horas y se decidió diferir los hi-poglucemiantes orales estableciendo control glucométrico. Se solicitaron pruebas de valoración de la homeostasia del calcio y tiroides con la finalidad de descartar causa orgánica, encontrándose niveles de vitamina D, calcio iónico, fósforo, magnesio, hormona estimulante de la tiroides (TSH) y paratohormona (PTH) sin alteraciones; tiroxina libre (T4L): 1.14 ng/dL; TSH : 1.772 UI/mL; calcio iónico: 1.17 mmol/L; vitamina D 25-OH: 47.6 ng/mL; fósforo:3.71 mg/dL; mag-nesio:2.03 mg/dL; PTH: 37.7 pg/mL. Dada la persistencia de la sintomatologia durante su estancia se hizo ajuste de la dosis inicialmente instaurada a 5 mg en la mañana y 2.5 mg por la noche, con lo cual hubo adecuada respuesta clínica.
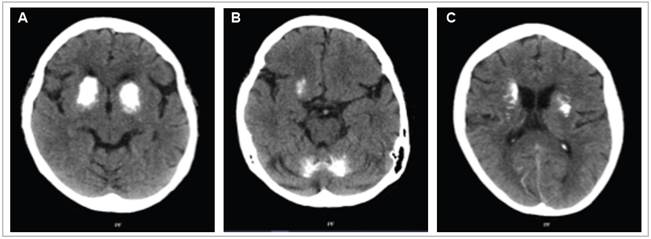
Figura 1 Tomografia de cráneo simple axial que evidencia marcadas calcificaciones intraparenquimatosas que ocupan casi la totalidad de los ganglios basales bilaterales y región central de lóbulos cerebelosos.
Teniendo en cuenta la lateralización de la sintomatologia y lo súbito del cuadro para descartar una causa isquémica, se solicitó resonancia magnética cuyos hallazgos fueron: cambios de señal de intensidad de ganglios basales y a nivel de ambos hemisferios cerebelosos, en relación a enfermedad por depósito mineral y/o calcio, cambios microangiopáticos de curso crónico, atrofia cortical moderada, engrasamiento perimetral mucoso del seno maxilar izquierdo. Constatándose con los resultados de ésta los hallazgos previamente mencionados en la TAC de cráneo simple y estableciendo entonces el diagnóstico de enfermedad de Fahr. Tras excluir causas secundarias de la sintomatologia descrita y teniendo en cuenta los resultados de los estudios imagenológicos se decide dar egreso con haloperidol a la dosis de respuesta clínica, se ajustó tratamiento hipoglucemiante y se ordenó citar a control en un mes por consulta externa, en donde se evidenció mejoría del cuadro inicial y adecuado control metabólico (Figura 2).
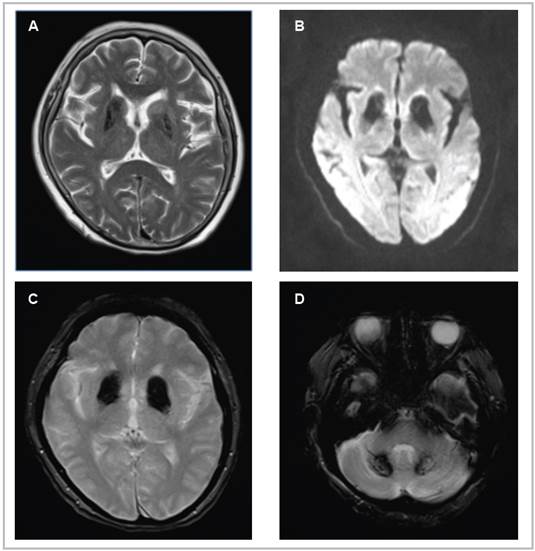
Figura 2 Resonancia magnética del cerebro en secuencias T2 (A), Difusión (B), T2 GRE (C,D) del plano axial. Se observa hipointensidad en cabeza del caudado y putamen bilaterales por depósito de material ferromagnético (A), hiperintensidad de igual localización (B), hiperintensidad simétrica en ganglios de la base (C) e hiperintensidad en núcleos dentados de cerebelo (D).
Discusión
Según la literatura existente, la enfermedad de Fahr se manifiesta clínicamente en forma de alteraciones neurológicas heterogéneas(torpeza, fatiga, marcha inestable, habla lenta o arrastrada, movimientos involuntarios, bradicinesia, rigidez, marcha festinante, hipofonía, facies en forma de máscara, distonia, temblor, coreoatetosis, convulsiones, signos piramidales o cerebelosos), psiquiátricas (deterioro cognitivo, trastornos del estado de ánimo, síntomas psicóticos y síntomas obsesivo-compulsivos) y radiológicamente como calcificaciones bilaterales de predominio gangliobasal 2,3. Esto concuerda con el cuadro clínico de la paciente, la cual presentó movimientos coreicos en las cuatro extremidades, pero de mucha mas amplitud en hemicuerpo derecho. No se encontraron síntomas psiquiátricos; sin embargo, dado el carácter neuroprogresivo de la patología no se descarta la aparición de estos en el futuro.
Para llegar al diagnóstico, se usó la evidencia actual de la enfermedad, que consiste en la presencia de calcificaciones gangliobasales bilaterales, el deterioro neurológico progresivo, la ausencia de alteraciones metabólicas y de otra enfermedad infecciosa, traumática, tóxica o heredofamiliar. En este caso, el primer recurso radiológico usado fue la TAC de cráneo sin contraste que es la herramienta que aporta mayor sensibilidad y especificidad para la detección de las calcificaciones 5,6,8.
En el paciente con síndrome psicótico, es de gran relevancia descartar la etiología orgánica, puesto que hay reportes de casos 7, que indican que algunos pacientes debutan con síntomas psiquiátricos aislados de instauración aguda. Por esta razón, cuando haya una leve sospecha de etiología orgánica o cuando la sintomatologia del paciente sea refractaria a varios niveles de tratamiento, es indispensable la realización de una neuroimagen que permita el correcto enfoque clínico del paciente y un pronóstico más favorable.
No se dispone actualmente de un tratamiento que retrase o revierta el curso de la enfermedad por lo que el pronóstico de ésta es variable. El tratamiento es únicamente sintomático: anticonvulsivantes, antipsicóticos, estabilizadores del estado de ánimo como el carbonato de litio, clonazepam, antidepresivos, han mostrado efectividad en varios reportes de casos 1,3, especialmente en aquellos pacientes con predominancia de síntomas neuropsiquiátricos. En nuestro caso, el uso de haloperidol logró disminuir la frecuencia y amplitud de los movimientos coreicos. Dada la mejoría clínica de la paciente y su adecuada respuesta a la medicación, se dio egreso con la misma dosis de haloperidol.
Quedan algunos interrogantes en este caso: uno de ellos es si la presentación se debe a una aparición esporádica de la patología o ligada a una herencia autosómica dominante o recesiva. Se ha descrito que están involucradas mutaciones en los genes SCL20A2, PDGFB, PDGFRB y XPR1, por lo cual son necesarios estudios genéticos moleculares para establecer la etiología. Adicionalmente, es de vital importancia brindar consejería genética a los familiares directos, ya que si existe alto riesgo de presentación de la enfermedad, se ha planteado la realización de TAC de cráneo en forma de tamizaje 5.
Falta aún mucho para avanzar en el estudio de esta patología, principalmente el desarrollo de medicamentos eficaces que impidan la neuroprogresión de ésta y todas las catastróficas consecuencias para la calidad de vida, de la persona que la padece. Nos queda a nosotros como profesionales de la salud, sospechar e identificar correctamente esta patología, brindarle un tratamiento sintomático al paciente, y una correcta asesoría multidisciplinar que le permita llevar a cabo, de mejor manera las actividades de su vida diaria.
References
1. Zavatta G, Clarke BL. Basal ganglia calcification in hypoparathyroidism and pseudohypoparathyroidism: local and systemic metabolic mechanisms. J Endocrinol Invest. 2021 Feb; 44(2):245-53. [ Links ]
2. Donzuso G, Mostile G, Nicoletti A, Zappia M. Basal ganglia calcifications (Fahr's syndrome): related conditions and clinical features. Neurol Sci Off J Ital Neurol Soc Ital Soc Clin Neurophysiol. 2019 Nov;40(11):2251-63. [ Links ]
3. Cassiani-Miranda CA, Herazo-Bustos M, Cabrera-González A, Cadena-Ramos I, Barrios-Ayola F. [Psychosis Associated With Fahr's Syndrome: A Case Report]. Rev Colomb Psiquiatr. 2015;44(4):256-61. [ Links ]
4. Ramos EM, Oliveira J, Sobrido MJ, et al. Primaiy Familial Brain Calcification. 2004 Apr 18 [Updated 2017 Aug 24]. In: Adam MP, Ardinger HH, Pagon RA, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2021. Available from: https://www.ncbi.nlm.nih.gov/books/NBK1421/ [ Links ]
5. Zavatta G, Clarke BL. Basal ganglia calcification in hypoparathyroidism and pseudohypoparathyroidism: local and systemic metabolic mechanisms. J Endocrinol Invest. 2021 Feb; 44(2):245-53. [ Links ]
6. Latre EML, Sánchez E, Jaime P, Barlés R. Imagen. 2016;7(2):74-5. [ Links ]
7. Gülsün M, Baykiz AF, Kabata§ S, Belli H. Fahr syndrome: Three cases presenting with psychiatric signs. Eur J Gen Med. 2006;3(1):35-10. [ Links ]
8. Otu AA, Anikwe JC, Cocker D. Fahr's disease: a rare neurological presentation in a tropical setting. Clin Case Rep. 2015 Oct;3(10):806-8. doi: 10.1002/ccr3.349. Epub 2015 Aug 26. PMID: 26509011; PMCID: PMC4614644. [ Links ]
Recibido: 24 de Abril de 2022; Aprobado: 24 de Octubre de 2022











 texto em
texto em 


