Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Colombian Journal of Anestesiology
versão impressa ISSN 0120-3347
Rev. colomb. anestesiol. vol.48 no.1 Bogotá jan./mar. 2020 Epub 28-Fev-2020
https://doi.org/10.1097/cj9.0000000000000130
Artículo de revisión
Recuperación intensificada en cirugía abdominal mayor en pediatría: revisión narrativa de la literatura
a Posgrado de Anestesiología de la Universidad de Caldas, Manizales, Caldas.
b Programa de Medicina de la Universidad de Manizales, Manizales, Caldas.
c Hospital Infantil Rafael Henao Toro, Manizales, Caldas.
d Servicios Especiales de Salud (S. E. S.) - Hospital de Caldas, Manizales, Caldas.
e Cirugía Pediátrica - Universidad de Antioquia, Medellín, Colombia.
Introducción:
Los programas de recuperación intensificada después de cirugía (ERAS, por sus siglas del inglés enhanced recovery after surgery) en adultos han impactado positivamente en morbilidad, mortalidad y costos en salud. Es conocido su efecto respecto a su efectividad en población pediátrica.
Objetivo:
Elaborar una revisión narrativa respecto a la evidencia actual de las diferentes estrategias en el marco de programas de recuperación intensificada en cirugía pediátrica (ERPS, por sus siglas del inglés enhancing recovery in pediatric surgery), en el contexto de cirugía abdominal mayor.
Métodos:
Se realizó una búsqueda sobre la evidencia científica disponible en bases de datos (Pubmed/Medline, Science Direct, OVID, SciELO) para elaborar una revisión narrativa de la literatura.
Conclusiones:
Aunque existe evidencia limitada sobre la utilidad de los protocolos ERAS en la población pediátrica sometida a cirugía abdominal mayor, podrían lograrse mejores resultados si se adoptan estas estrategias en pacientes pediátricos.
Palabras clave: Cirugía; Pediatría; Recuperación; Anestesia
Introduction:
Enhanced recovery after surgery (ERAS) programs in adults have positively impacted morbidity, mortality, and healthcare costs. Its effects on the pediatric population is recognized.
Objective:
To prepare a narrative review on the current evidence of the various strategies within the framework of enhancing recovery after pediatric surgery, in the context of major abdominal surgery.
Methods:
A search was conducted on the scientific evidence available in databases (Pubmed/Medline, Science Direct, OVID, SciELO), in order to prepare a narrative literature review.
Conclusion:
Notwithstanding the limited evidence on the practicality of the ERAS protocols in the pediatric population undergoing major abdominal surgery, better results could be accomplished if these strategies are adopted.
Keywords: Pediatric surgery; Recovery; Anesthesia
Introducción
El programa de recuperación intensificada después de cirugía (ERAS, por sus siglas del inglés enhanced recovery after surgery) abarca estrategias e intervenciones orientadas a atenuar la respuesta al estrés quirúrgico y a permitir que el paciente retorne a su estado basal y a las actividades familiares y sociales en el menor tiempo posible. Los elementos clave son la evidencia científica, el trabajo multidisciplinario, la adecuada comunicación entre los actores implicados en la atención y manejo de los pacientes, y los procesos de auditoría sobre la aplicación de las diferentes estrategias.1 Se han publicado protocolos para diferentes procedimientos diagnósticos y terapéuticos en el adulto. En general, contienen entre 17 y 23 estrategias que involucran todo el proceso perioperatorio, las cuales han impactado positivamente en las complicaciones, en la morbilidad yenloscostosensalud.2
Debido a las diferencias fisiológicas y a menores tasas de morbimortalidad en niños, es difícil adaptar protocolos ERAS del adulto en la población pediátrica.3 Sin embargo, estudios observacionales en cirugía colorrectal con ERAS4 han documentado desenlaces similares a los observados en el adulto. Así, la aplicabilidad y la adaptación de estas estrategias es eficaz en la reducción de complicaciones posoperatorias, disminución del tiempo de estancia hospitalaria, inicio más temprano de la nutrición enteral y menores costos en salud en niños.
El objetivo del presente artículo fue realizar una revisión narrativa de la literatura respecto a la evidencia actual de las diferentes estrategias en el marco de programas de recuperación intensificada en cirugía pediátrica (ERPS, por sus siglas del inglés enhancing recovery in pediatric surgery), específicamente en el contexto de cirugía abdominal mayor y orientada más hacia cirugía colónica.
Métodos
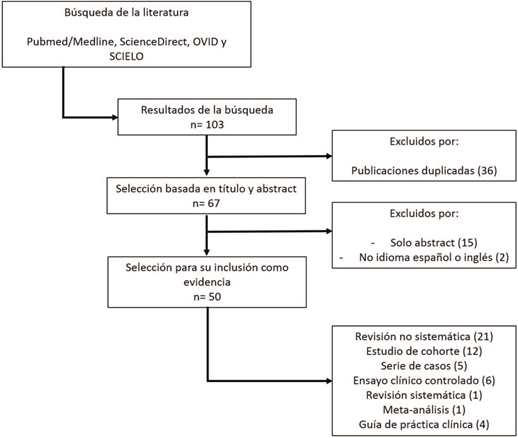
Se realizó una búsqueda de literatura en bases de datos Pubmed/Medline, ScienceDirect, OVID, Scielo, usando las palabras "surgery", "pediatric", "recovery", "anesthesia", "anaesthesia", "analgesia", "enhanced recovery", "fast track", "ERAS programme" y "major abdominal procedures". La búsqueda y selección de artículos se realizaron de forma independiente, incluidos metaanálisis, revisiones sistemáticas, ensayos clínicos, estudios observacionales y artículos de revisión. No se consideró límite la fecha de publicación. Se incluyeron artículos en español e inglés. No se tuvo en cuenta literatura gris (Figura 1).
Evolución histórica
Henrik Kehlet introdujo el concepto de ERAS. Él atribuyó la recuperación prolongada a las alteraciones en la función orgánica ocasionadas por el estrés quirúrgico y cambios endocrinometabólicos.2 Al reconocer que ninguna intervención perioperatoria de forma individual puede modificar estos trastornos fisiológicos, Kehlet y Mogensen publicaron un estudio sobre la viabilidad y la eficacia de un régimen de rehabilitación multimodal para promover la recuperación posoperatoria de los pacientes sometidos a sigmoidectomía abierta. Mediante la utilización de una combinación de analgesia regional, ingesta oral y deambulación posoperatoria temprana demostraron una reducción en la estancia hospitalaria de diez a dos días.5,6
Desde la creación en el 2010 de la sociedad ERAS se han realizado varias publicaciones con recomendaciones específicas para diferentes procedimientos quirúrgicos.7 Desde hace algunos años la atención en la adaptación de estrategias ERAS se ha centrado en la población pediátrica. Aunque la evidencia es escasa, recientemente se publicó no solo el desarrollo de un protocolo de recuperación intensificada para niños sometidos a cirugía gastrointestinal,8 sino los resultados de su aplicación, que evidencia disminución en el volumen de líquidos endovenosos administrados, reducción en dosis de opioides, inicio más rápido de la vía oral, tiempos de estancia hospitalaria más cortos y reducción en costos en salud.4
Contexto fisiológico
Uno de los objetivos fundamentales de los ERPS es disminuir la respuesta al estrés quirúrgico. Dicha respuesta está representada por cambios hormonales y metabólicos que resultan en alteraciones hematológicas, inmunológicas y endocrinas; se caracteriza por una elevación en las hormonas contrarreguladoras (cortisol, hormona del crecimiento, glucagón y catecolaminas) inducida por la activación del eje hipotálamo-hipófisis-suprarrenal, y un predominio inicial de citocinas proinflamatorias (IL-1 e IL-6), seguidas de citocinas antiinflamatorias. Esta respuesta será mayor cuanto más grande sea el trauma quirúrgico, y explica el desarrollo de resistencia a la insulina de algunos pacientes.7
Estrategias
A continuación se discutirán algunas de las estrategias más importantes incluidas en protocolos de ERPS en el contexto de cirugía abdominal mayor (Tabla 1).
Educación de padres y pacientes
Los niños son más vulnerables al estrés emocional que genera una cirugía, por lo cual la preparación preoperatoria es importante no solo como medida de ansiolisis, sino, también, para facilitar la recuperación posoperatoria (adherencia a indicaciones de deambulación temprana, terapia respiratoria, cuidado de heridas, entre otros). Es indispensable involucrar a los padres en el proceso de educación, ya que su propio estrés puede ser transferido al niño, lo que aumenta su ansiedad. Debe mencionarse el procedimiento quirúrgico por realizar, la técnica anestésica, la posibilidad de dolor posoperatorio, el área de manejo posterior a la cirugía y posibles riesgos y complicaciones esperados. Sin embargo, debe asegurarse que el método educativo sea específico, exacto y apropiado para la edad.9,10
Preparación de colon
La anastomosis intestinal electiva es un procedimiento quirúrgico frecuentemente utilizado en cirugía pediátrica. Pretende restaurar la continuidad intestinal (cierre de ileostomía o colostomía), curar una enfermedad inflamatoria o la malformación congénita anatómica o funcional de la región colorrectal.11
La preparación intestinal (PMI) en cirugía colorrectal se lleva a cabo usando antibióticos y/o enemas orales o rectales para la limpieza intestinal mecánica. Sin embargo, hoy se cuestiona esto, argumentando mayores riesgos colaterales, así como la carencia de respaldo científico.12 Dicha práctica ha ido cambiando, y se calcula que solo una cuarta parte de los pacientes recibe preparación mecánica antes de cirugía colorrectal.
Estudios que comparan las complicaciones infecciosas en pacientes con preparación mecánica del colon sin la administración simultánea de antibióticos orales en cirugía colorrectal,13 cierre de colostomía14 y cistoplastia de aumento15 no encontraron diferencias en la incidencia de infección del sitio operatorio, abscesos intraabdominales y fugas anastomóticas, pero sí una mayor estancia hospitalaria y mayor grado de incomodidad. Otros estudios en cirugía de colon sin preparación intestinal mecánica (PIM) encontraron que no aumenta el riesgo de infección del sitio operatorio, ni de filtraciones anastomóticas, pero sí disminuye la estancia y la incomodidad en los pacientes.16,17
En 2015, Rangel publicó una revisión de la literatura, e informó la mejor evidencia actual para la prevención de complicaciones infecciosas en cirugía colorrectal en niños; así, concluyó que la PMI no tiene beneficios. Además, el uso de antibióticos orales no absorbibles previamente a la cirugía (neomicina y el metronidazol) sin PMI disminuye significativamente las complicaciones infecciosas y la estancia hospitalaria.18,19
Ayuno preoperatorio
El ayuno prolongado es peligroso, puede generar una respuesta metabólica e inmunológica que desencadena catabolismo proteico, resistencia a la insulina y disminución del volumen intravascular.20 Además, genera estrés, irritabilidad e incomodidad en los niños. Incentivar la ingesta de líquidos claros con carbohidratos (3 ml/kg o 1 onza por cada 10kg de peso) hasta una hora antes de la inducción de anestesia evita estos efectos indeseables y mejora la satisfacción de los pacientes.21,22 Dichos beneficios se extienden al posoperatorio, al disminuir la estancia hospitalaria y favorecer el funcionamiento intestinal.20,23 Por ello, es importante prescribir como una orden médica la hora, el tipo y la cantidad de líquido que se debe administrar al paciente antes de cirugía.
Ansiolisis
Controlar la ansiedad preoperatoria disminuye el consumo de analgésicos, la frecuencia de delirium y comportamientos mal adaptativos posoperatorios.24,25 Los medicamentos más utilizados en pediatría para este propósito son: el midazolam, la clonidina y la dexmedetomidina26,27 (Tabla 1). También son efectivas medidas no farmacológicas, como el uso de videos y la musicoterapia.26
Evaluación del riesgo de tromboembolismo
Se debe determinar el riesgo de tromboembolismo venoso en niños para decidir qué medidas preventivas son las más apropiadas (farmacológicas y no farmacológicas). Guías internacionales sugieren el uso de medias con gradiente de presión o dispositivo de compresión neumática en mayores de 13 años, independientemente del riesgo de evento tromboembólico. Se recomienda iniciarla deambulación de forma temprana en el posoperatorio.28
Prevención de la infección del sitio operatorio (ISO)
La ISO es la infección más común asociada con el cuidado de la salud. Prolonga la estancia hospitalaria, aumenta dos a once veces el riesgo de mortalidad e incrementa los costos. Las instituciones de salud deben implementar guías de profilaxis antibiótica preoperatoria con base en el procedimiento quirúrgico, los patógenos más frecuentemente asociados con ISO y el perfil propio de resistencia bacteriana.29 Además, se recomienda: mantener la normotermia, bañar con clorhexidina la noche previa al procedimiento quirúrgico, preparar la piel de forma metódica con un tiempo de duración determinado en sala de cirugía con clorhexidina y cambiar los guantes después de completar ciertas etapas del procedimiento que pueden causar contaminación (por ejemplo, después de anastomosis intestinales).
Técnica mínimamente invasiva
El empleo de técnicas mínimamente invasivas, como la laparoscopia, ha demostrado disminuir la inflamación, reducir la estancia hospitalaria y la morbilidad perioperatoria; así, es un predictor independiente para tolerancia temprana de líquidos y sólidos, tránsito intestinal más rápido y tiempo menor a la primera defecación.30
Uso de sondas gástricas y drenes
Las sondas gástricas se usan para disminuir la distensión abdominal por aire y secreciones en el posoperatorio, y con la intención de prevenir náuseas, vómito, complicaciones pulmonares, desarrollo de fístulas, complicaciones de la herida y días de estancia hospitalaria. Sin embargo, publicaciones recientes no han demostrado los beneficios descritos.11,4,31-33 Estudios en cirugía de resección de colon en los que se evitó el uso de sondas y drenes informan un inicio de la vía oral más temprano, más confort para el paciente y disminución de la estancia hospitalaria.34
Las sondas gástricas y catéteres urinarios podrían retirarse en el posquirúrgico inmediato, o máximo a las 24 horas después de cirugía, sin que esto ponga en riesgo la seguridad del paciente; además, mejora su comodidad. Respecto al uso de drenes abdominales en cirugía colorrectal, no existen estudios específicos que demuestren mejores resultados con o sin su uso; sin embargo, en todas las investigaciones que aplican ERAS como protocolo para cirugía pediátrica dichos drenes se retiraron en un plazo máximo de 48 horas sin que se hayan generado complicaciones asociadas con su retiro.
Analgesia: uso de técnicas regionales y ahorro de opioides
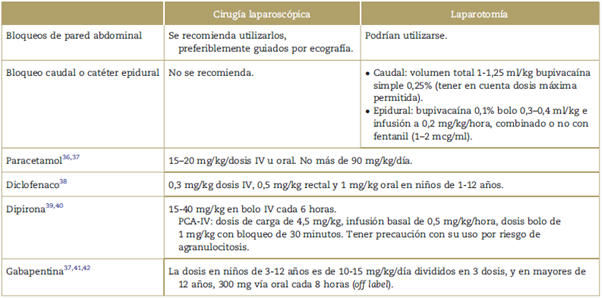
Los opioides tienen efectos secundarios que prolongan la recuperación posquirúrgica, y retrasan el alta hospitalaria y el retorno al estado basal. Los anestesiólogos podemos influir en el éxito de los protocolos ERPS con un adecuado control del dolor, al emplear una estrategia analgésica multimodal para disminuir el consumo de opioides3,35-42 (Tabla 2).
Normotermia
La hipotermia en el perioperatorio, al ser un evento prevenible, es un factor de riesgo de incremento de sangrado y necesidad de transfusión sanguínea, trastornos hidroelectrolíticos, complicaciones cardiovasculares por aumento de concentraciones de catecolaminas séricas, incremento de ISO, entre otros. Se recomienda el uso de diversas técnicas de calentamiento, tanto pasivas como activas, y la monitorización de la temperatura en el intraoperatorio.43
Uso de líquidos en el perioperatorio
El objetivo del uso de soluciones hidroelectrolíticas es mantener la perfusión tisular sin producir edema. Tanto el exceso como el déficit de líquidos tienen efectos deletéreos en la homeostasis del paciente. Debe evitarse la deshidratación preoperatoria e incentivar la ingesta de líquidos claros, como se explicó previamente. Las necesidades basales (NB) deben ser cubiertas según la fórmula del 4-2-1 de Holliday-Segar, con soluciones isotónicas (SI). En neonatos debe adicionarse dextrosa entre 1-2,5% para cubrir las necesidades basales y evitar la hipoglucemia (3 mg/kg/min). Se debe evitar el uso de electrolitos en dextrosa por el riesgo de hiponatremia.44-46
El déficit de líquido intraoperatorio debe ser reemplazado con SI, con preferencia por las soluciones balanceadas. Las cargas de líquidos deben administrarse durante 20 minutos, pues su rápida administración lleva a mayor distribución de líquido en el espacio intersticial, a menor éxito en la expansión del volumen intravascular, a daño del glucocálix y a desarrollo de edema. En cirugía, la base exceso, el delta de CO2 y el lactato son itiles para guiar la reposición hídrica. Las medidas de la variabilidad de la onda del pulso y el test de la elevación de los miembros inferiores son poco útiles en menores de 5 años. En niños, el mejor parámetro para predecir quién será respondedor a volumen es la variación de la velocidad del flujo pico aórtico.47,48
Los líquidos deben ser administrados en bombas de infusión, y debe usarse una línea para las NB y otra diferente para la administración de bolos.
Un aumento mayor al 10% del peso corporal por sobrecarga hídrica (SH) está asociado con mayor estancia en cuidados intensivos, más días de ventilación mecánica, infección del sitio quirúrgico y costos de la atención médica. Por ello, se recomienda hacer seguimiento diario del total de líquidos administrados (LA) y eliminados (LE), de acuerdo con la siguiente fórmula:
SH = (LA - LE en litros)/Peso del paciente en kg x 100.
En el posoperatorio, los líquidos endovenosos deben ser formulados cada 12 horas y no cada 24 horas, como tradicionalmente se hace, para ajustar permanentemente la dosis de acuerdo con el estado del paciente.49 En este periodo, se recomienda administrar solo el 70% de las NB de líquidos y suspenderlos tan pronto se inicie la vía oral.
Prevención de náuseas y vómito
Se recomienda el uso de la escala de Eberhart para determinar el riesgo de náuseas y vómito posoperatorio, y el uso de estrategias farmacológicas de acuerdo con el riesgo y características de los pacientes.50
Conclusiones
Los protocolos ERAS han demostrado tener un impacto positivo en la recuperación de los pacientes adultos. Existe evidencia limitada sobre la utilidad de estos protocolos en la población pediátrica sometida a cirugía abdominal mayor, dado que se han ido construyendo a partir de los resultados mostrados con ERAS del adulto y no a partir de la pregunta fundamental que lleva a su desarrollo y que fue planteada desde el inicio por Henrik Kehlet: ¿por qué está el paciente quirúrgico hospitalizado hoy?
Adicionalmente, hay gran disparidad entre el número de estudios que evalúan la efectividad de los protocolos ERAS en adultos y niños. Existen estudios que demuestran la efectividad de algunas estrategias individuales, pero no se han evaluado cuando se integran junto con otras estrategias en un mismo protocolo. Tampoco está claro si dichos protocolos son aplicables en todos los rangos de edad en los que hay marcadas diferencias; por ejemplo, en la respuesta fisiológica al estrés, en el riesgo de tromboembolismo venoso y en la capacidad de deambulación.
También existen controversias sobre la utilización de insulina para la corrección de la hiperglucemia intraoperatoria en este grupo de pacientes, pues no está claro si el beneficio justifica el riesgo. Además, medicamentos como la bupivacaína liposomal no han sido integrados aún en estos protocolos, por lo que se desconoce su impacto.
A pesar de lo anterior, la evidencia apunta a lograrse mejores resultados en niños cuando se adoptan las estrategias de los protocolos ERPS.
Es fundamental que las instituciones fomenten la creación de grupos quirúrgicos y que estos desarrollen, adopten y apliquen este tipo de protocolos en los sitios de atención pediátrica del país. La experiencia obtenida debe ser seguida periódicamente, al evaluar los resultados obtenidos dentro de una estrategia de mejoramiento y autoevaluación continua.
REFERENCIAS
1. Scott MJ, Baldini G, Fearon KCH, et al. Enhanced recovery after surgery (ERAS) for gastrointestinal surgery, Part 1: Pathophysiological considerations. Acta Anaesthesiol Scand 2015;59:1212-1231. [ Links ]
2. Casans Francés R, Ripollés Melchor J, Abad-Gurumeta A, et al. The role of the anaesthesiologist in enhanced recovery programs. Rev Española Anestesiol Reanim (English Edition) 2016;63:273-288. [ Links ]
3. George JA, Koka R, Gan TJ, et al. Review of the enhanced recovery pathway for children: perioperative anesthetic considerations. Can J Anesth 2018;65:569-577. [ Links ]
4. Short HL, Heiss KF, Burch K, et al. Implementation of an enhanced recovery protocol in pediatric colorectal surgery. J Pediatr Surg 2018;53:688-692. [ Links ]
5. Elhassan A, Ahmed A, Awad H, et al. The evolution of surgical enhanced recovery pathways: a review. Curr Pain Headache Rep 2018;22:74. [ Links ]
6. Kehlet H, Mogensen T. Hospital stay of 2 days after open sigmoidectomy with a multimodal rehabilitation programme: rehabilitation after sigmoidectomy. Br J Surg 1999; 86:227-230. [ Links ]
7. Ljungqvist O, Scott M, Fearon KC. Enhanced recovery after surgery: a review. JAMA Surg 2017;152:292. [ Links ]
8. Raval MV, Heiss KF. Development of an enhanced recovery protocol for children undergoing gastrointestinal surgery. Curr Opin Pediatr 2018;30:399-404. [ Links ]
9. Li HCW. Evaluating the effectiveness of preoperative interventions: the appropriateness of using the children’s emotional manifestation scale. J Clin Nurs 2007;16:1919-1926. [ Links ]
10. Li HCW, López V, Lee TLI. Psychoeducational preparation of children for surgery: the importance of parental involvement. Patient Educ Counsel 2007;65:34-41. [ Links ]
11. Dávila-Pérez R, Bracho-Blanchet E, Fernández-Portilla E, et al. Evidence based improvements in elective bowel anastomoses in children. Cir Cir 2013;81:548-555. [ Links ]
12. Cordero Castro S. Benefits and risks of preoperative bowel cleansing in the pediatric population. Enfermería Actual de Costa Rica 2013;1-9. [ Links ]
13. Aldrink JH, McManaway C, Wang W, et al. Mechanical bowel preparation for children undergoing elective colorectal surgery. J Pediatr Gastroenterol Nutrit 2015;60:503-507. [ Links ]
14. Serrurier K, Liu J, Breckler F, et al. A multicenter evaluation of the role of mechanical bowel preparation in pediatric colostomy takedown. J Pediatr Surg 2012;47:190-193. [ Links ]
15. Víctor D, Burek C, Corbetta JP, et al. Augmentation cystoplasty in children without preoperative mechanical bowel preparation. J Pediatr Urol 2012;8:201-204. [ Links ]
16. Leys CM, Austin MT, Pietsch JB, et al. Elective intestinal operations in infants and children without mechanical bowel preparation: a pilot study. J Pediatr Surg 2005;40:978-982. [ Links ]
17. Shinnick JK, Short HL, Heiss KF, et al. Enhancing recovery in pediatric surgery: a review of the literature. J Surg Res 2016; 202:165-176. [ Links ]
18. Pennington EC, Feng C, St Peter SD, et al. Use of mechanical bowel preparation and oral antibiotics for elective colorectal procedures in children: is current practice evidence-based? J Pediatr Surg 2014;49:1030-1035. [ Links ]
19. Rangel SJ, Islam S, Peter SD, et al. Prevention of infectious complications after elective colorectal surgery in children: an American Pediatric Surgical Association Outcomes and Clinical Trials Committee comprehensive review. J Pediatr Surg 2015;50: 192-200. [ Links ]
20. Rove KO, Edney JC, Brockel MA. Enhanced recovery after surgery in children: promising, evidence-based multidisciplinar care. Pediatr Anesth 2018;28:482-492. [ Links ]
21. Kelly CJ, Walker RWM. Perioperative pulmonary aspiration is infrequent and low risk in pediatric anesthetic practice. Pediatr Anesth 2015;25:36-43. [ Links ]
22. Habre W, Disma N, Virag K, et al. Incidence of severe critical events in paediatric anaesthesia (APRICOT): a prospective multicenter observational study in 261 hospitals in Europe. Lancet Respir Med 2017;5:412-425. [ Links ]
23. Thomas M, Morrison C, Newton R, et al. Consensus statement on clear fluids fasting for elective pediatric general anesthesia. Pediatr Anesth 2018;28:411-414. [ Links ]
24. Hilly J, Hórlin A-L, Kinderf J, et al. Preoperative preparation workshop reduces postoperative maladaptive behavior in children. Pediatr Anesth 2015;25:990-998. [ Links ]
25. Fincher W, Shaw J, Ramelet A-S. The effectiveness of a standardized preoperative preparation in reducing child and parent anxiety: a single-blind randomized controlled trial: preoperative preparation for children. J Clin Nurs 2012; 21:946-955. [ Links ]
26. Strom S. Preoperative evaluation, premedication, and induction of anesthesia in infants and children. Curr Opin Anaesthesiol 2012;25:321-325. [ Links ]
27. Rosenbaum A, Kain ZN, Larsson P, et al. The place of premedication in pediatric practice. Pediatr Anesth 2009;19:817-828. [ Links ]
28. Morgan J, Checketts M, Arana A, et al. Prevention of perioperative venous thromboembolism in pediatric patients: Guidelines from the Association of Paediatric Anaesthetists of Great Britain and Ireland (APAGBI). Pediatr Anesth 2018; 28:382-391. [ Links ]
29. Ban KA, Minei JP, Laronga C, et al. American College of Surgeons and Surgical Infection Society: Surgical Site Infection Guidelines, 2016 Update. J Am Coll Surg 2017;224:59-74. [ Links ]
30. Van Bree SH, Vlug MS, Bemelman WA, et al. Faster recovery of gastrointestinal transit after laparoscopy and fast-track care in patients undergoing colonic surgery. Gastroenterology 2011;141: 872-880. [ Links ]
31. Sangkhathat S, Patrapinyokul S, Tadyathikom K. Early enteral feeding after closure of colostomy in pediatric patients. J Pediatr Surg 2003;38:1516-1519. [ Links ]
32. Reismann M, von Kampen M, Laupichler B, et al. Fast-track surgery in infants and children. J Pediatr Surg 2007;42:234-238. [ Links ]
33. Reismann M, Dingemann J, Wolters M, et al. Fast-track concepts in routine pediatric surgery: a prospective study in 436 infants and children. Langenbeck’s Arch Surg 2009;394:529-533. [ Links ]
34. Mattioli G, Palomba L, Avanzini S, et al. Fast-track surgery of the colon in children. J Laparoendoscopic Adv Surg Tech 2009;19 (s1): s7-s9. [ Links ]
35. López-García JC, Castejón J, Moreno M. Anestesia multimodal infantil: analgesia epidural. Rev Soc Esp Dolor 2004;11:10. [ Links ]
36. Chiaretti A, Pierri F, Valentini P, et al. Current practice and recent advances in pediatric pain management. Eur Rev Med Pharmacol Sci 2013;17 (suppl 1):112-126. [ Links ]
37. Shay JE, Kattail D, Morad A, et al. The postoperative management of pain from intracranial surgery in pediatric neurosurgical patients. Pediatr Anesth 2014;24:724-733. [ Links ]
38. Standing JF, Tibboel D, Korpela R, et al. Diclofenac pharmacokinetic meta-analysis and dose recommendations for surgical pain in children aged 1-12 years: Diclofenac pooled PK in children. Pediatr Anesth 2011;21:316-324. [ Links ]
39. De Leeuw TG, Dirckx M, Gonzalez Candel A, et al. The use of dipyrone (metamizol) as an analgesic in children: what is the evidence? A review. Pediatr Anesth 2017;27:1193-1201. [ Links ]
40. Sener M, Kocum A, Caliskan E, et al. Administration of paraceta-mol versus dipyrone by intravenous patient-controlled analgesia for postoperative pain relief in children after tonsillectomy. Braz J Anesthesiol 2015;65:476-482. [ Links ]
41. Konijnenbelt-Peters J, van der Heijden C, Ekhart C, et al. Metamizole (Dipyrone) as an alternative agent in postoperative analgesia in patients with contraindications for nonsteroidal anti-inflammatory drugs. Pain Pract 2017; 17:402-408. [ Links ]
42. Baxter KJ, HaflingJ, Sterner J, et al. Effectiveness of gabapentin as a postoperative analgesic in children undergoing appendectomy. Pediatr Surg Int 2018;34:769-774. [ Links ]
43. Bayter-Marín JE, Rubio J, Valedón A, et al. Hypothermia in elective surgery: the hidden enemy. Col J Anesthesiol 2017;45:48-53. [ Links ]
44. Hahn RG. Fluid therapy might be more difficult than you think. Anesth Analg 2007;105:304-305. [ Links ]
45. Edjo Nkilly G, Michelet D, Hilly J, et al. Postoperative decrease in plasma sodium concentration after infusion of hypotonic intravenous solutions in neonatal surgery. This article is accompanied by Editorial III. Br J Anaesth 2014;112:540-545. [ Links ]
46. Jansen L, Safavi A, Lin Y, et al. The Canadian Pediatric Surgery Network (CAPSNet) Preclosure fluid resuscitation influences outcome in gastroschisis. Am J Perinatol 2012;29:307-312. [ Links ]
47. Gan H, Cannesson M, Chandler JR, et al. Predicting fluid responsiveness in children: a systematic review. Anesth Analg 2013;117:1380-1392. [ Links ]
48. Hahn RG. Volume kinetics for infusion fluids. Anesthesiol 2010; 113:470-481. [ Links ]
49. Lander A. Updated guidelines for the management of fluid and electrolytes in children. Surgery 2016;34:213-216. [ Links ]
50. Höhne C. Postoperative nausea and vomiting in pediatric anesthesia. Curr Opin Anaesthesiol 2014;27:303-308. [ Links ]
Cómo citar este artículo: Trujillo-Mejía A, Zapata-Contreras L, Melo-Aguilar LP, Gil-Montoya LF. Enhancing recovery in pediatric major abdominal surgery: a narrative review of the literature. Colombian Journal of Anesthesiology. 2020;48:30-37.
Copyright © 2019 Sociedad Colombiana de Anestesiología y Reanimación (S.C.A.R.E.). Published by Wolters Kluwer. This is an open access article under the CC BY-NC-ND license (https://creativecommons.org/licenses/by-nc-nd/4.0/).











 texto em
texto em