Introducción
La enfermedad de Pompe (EP) se suele clasificar en tres formas, dependiendo de la edad de inicio y la severidad clínica: de inicio infantil (clásica y no clásica) y de inicio tardío. La rehabilitación hace parte del tratamiento integral y multidisciplinario de esta condición.
En la actualidad, la terapia de remplazo enzimático (TRE) representa la mayor herramienta terapéutica para la EP, lo que ha reducido la mortalidad a corto plazo por cambios en su expresión fenotípica, y esto ha permitido la autonomía del paciente y el logro de nuevas habilidades motrices 1,2. La TRE ha cambiado la perspectiva de los pacientes con EP en los últimos años, ya que mejora la supervivencia, mantiene la fuerza muscular y estabiliza la función pulmonar, aunque no todos los pacientes responden de igual manera a este tratamiento, debido a que no se resuelve el daño muscular instaurado ni la limitación funcional motora, lo cual lleva a la evaluación y el abordaje de nuevas dificultades clínicas en la rehabilitación primaria.
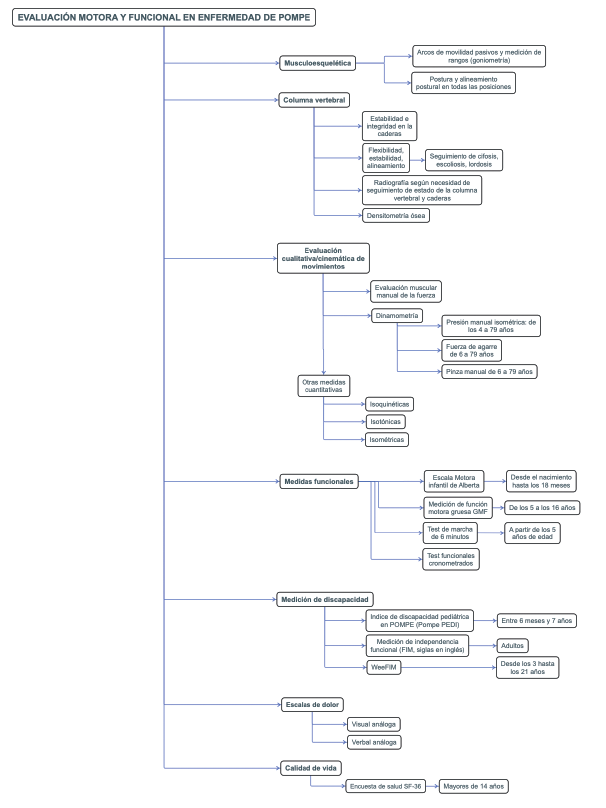
Para el abordaje y el seguimiento funcional del paciente con EP, como complemento del examen físico general y neurológico, se recomienda utilizar escalas de movilidad como la Medición de Función Motora Gruesa (GMFM, por sus siglas en inglés); pruebas funcionales cronometradas como el test de marcha en 6 minutos, que fue desarrollada por la Academia Americana de Tórax para medir la capacidad de ejercicio en pacientes con enfermedad cardiopulmonar, pero ha sido adoptada para la evaluación, el seguimiento funcional y la capacidad de ejercicio en enfermedades neuromusculares. Existen también escalas de discapacidad, escalas visuales análogas para medición del dolor y de calidad de vida 3. Aunque la mayoría de las escalas no tienen un alto nivel de evidencia ni de recomendación, debido a la falta de estudios con muestras grandes aleatorizadas, las que presentan mejor medición de la funcionalidad motora y discapacidad en la EP son la Escala Motora Infantil de Alberta y el Inventario de Evaluación Pediátrica de Discapacidad (PEDI, por sus siglas en inglés), con una versión adaptada para EP (recomendación C: respaldada en investigaciones de ensayos aleatorizados con una muestra pequeña y resultados inciertos, con riesgo de errores alfa o beta) 4. A grandes rasgos, estas escalas funcionales informan sobre las actividades motoras que el niño o adolescente domina, aquellas que están en desarrollo y las que no se han alcanzado de acuerdo con la edad; adicionalmente, permiten monitorear la función motora inicial; cambios a lo largo del tiempo y después de intervenciones terapéuticas; y también hacen posible crear objetivos de intervención de acuerdo con el nivel de función motora y psicológica de cada paciente (figura 1) 5,6.
Dentro de las pruebas funcionales principales para monitoreo y seguimiento funcional de la EP se sugiere realizar el test de marcha de 6 minutos después de los 5 años, con seguimiento cada 6 a 12 meses, y las pruebas de función motora cada 3 meses en el primer año de diagnóstico; posteriormente, cada 6 a 12 meses. Se sugiere hacer seguimiento a la deglución en cada evaluación clínica de seguimiento 7.
Hay distintos estudios que describen el espectro clínico de la EP y la interacción entre la disfunción muscular, la estructura ósea, el efecto de la TRE, así como la intervención con ejercicio para mejorar la función motora 8. Por esta razón, no hay guías establecidas para el cuidado primario, por lo cual en la práctica clínica se siguen recomendaciones generales para la enfermedad neuromuscular. No obstante, este cuidado primario, que es multidisciplinario, es de alta importancia para optimizar la condición general del paciente mientras se realiza el tratamiento con la TRE, pues previene el daño y la pérdida de capacidad funcional de distintos sistemas como el respiratorio, el muscular, el óseo, el auditivo, el lenguaje, la deglución y el renal, de manera que se mejora o mantiene la calidad de vida 9. Los efectos fisiológicos de la EP pueden variar de un paciente a otro, motivo por el cual los planes de intervención en rehabilitación se deben personalizar según la funcionalidad y las necesidades de cada individuo, por lo cual es relevante hacer un seguimiento clínico y funcional periódico para evaluar la evolución y hacer ajustes en estas intervenciones en caso de requerirlas. Con respecto al seguimiento clínico para la EP en pacientes asintomáticos (es decir, sin TRE), este se hace cada 3 meses durante el primer año posterior al diagnóstico, luego cada 3 a 12 meses según evolución clínica si son asintomáticos; para los pacientes con inicio de síntomas y TRE, el seguimiento se realiza mensualmente durante 3 a 4 meses, posteriormente cada 3 meses -de 4 a 12 meses-, y finalmente cada 3 a 6 meses, después del primer año 7.
En cualquier edad, en cualquier estadio de la enfermedad se debe apoyar, según la estabilidad clínica lo permita, la participación del individuo en todos los aspectos de la vida en los cuales esté interesado, de modo que se provea la máxima independencia funcional en actividades de la vida diaria, mediante la adaptación para la función y la educación a la familia.
Intervenciones de rehabilitación
Manejo de contracturas y deformidades
Se define contractura como la incapacidad para completar un arco de movilidad en forma activa o pasiva debido a una alteración articular, muscular o de los tejidos blandos. Las contracturas producen un desbalance entre los músculos agonistas y los antagonistas, lo cual ocasiona cambios biomecánicos que generan posturas compensatorias, de manera que se altera la postura y el posicionamiento; por lo tanto, se deben adoptar medidas de prevención mediante un diagnóstico temprano, inicio de fisioterapia con movilizaciones pasivas, estiramiento y adecuado posicionamiento con cambios de posición, principalmente en los pacientes con mayor debilidad, ya que la principal causa de contracturas es el posiciona-miento estático de las articulaciones por debilidad; se debe tener presente, además, que las contracturas ya instauradas tienen respuesta limitada a los programas de estiramientos 10.
En principio, las modalidades de fisioterapia deben prevenir o retrasar la instauración de deformidades de las extremidades 11:
Proveer el posicionamiento y apoyo para aumentar las ventajas biomecánicas (periodos de bipedestación y marcha si el paciente tiene la capacidad).
Minimizar la fuerza de la gravedad deformante.
Minimizar la contractura promoviendo la extensión.
Estiramientos: pasivos y activos asistidos de baja intensidad.
Hay pocas recomendaciones sobre el beneficio de las intervenciones quirúrgicas para el manejo de las contracturas 12.
Formulación de ayudas técnicas de posicionamiento y marcha
Los dispositivos de asistencia para el posicionamiento y la marcha deben tener como propósito mantener el nivel máximo de independencia, de manera que apoyen la función, mejoren el posicionamiento para prevenir contracturas, permitan cambios de posición y reduzcan los puntos de presión para el mantenimiento de la integridad de la piel 11.
Dentro de los dispositivos ortésicos se encuentran las órtesis fijas de tobillo y pie, que previenen principalmente las contracturas del tendón de Aquiles (contractura en plantiflexión); los fijadores de caderas para prevenir las contracturas de la banda ilioti bial; férulas en las rodillas, codos, muñecas y manos para prevenir las deformidades en flexión, y corsé lumbar para el manejo del dolor de espalda. En la EP no hay evidencia del uso de estos dispositivos durante la noche 12.
En dispositivos para asistencia de la marcha, dependiendo del grado de debilidad y patrón de marcha, se encuentran los caminadores fijos y con llantas, bastones canadienses y de cuatro puntos. Al progresar la enfermedad se debe adaptar la movilidad a la silla de ruedas, con sistemas de sedestación adecuados para prevenir deformidades en las extremidades y la columna. Es preciso tener en cuenta que también se deben hacer adaptaciones al entorno del paciente para la realización de sus actividades básicas cotidianas, como puntos de apoyo en el baño con barandas de sujeción y sillas de ducha, con el fin de mejorar la seguridad y la independencia mientras se reducen las complicaciones.
También están los equipos de bipedestación, que tienen dos objetivos principales: el primero es el estiramiento de las articulaciones de los miembros inferiores, para mejorar la elongación muscular, y el segundo, contribuir al manejo de la osteoporosis, ya que el bípedo induce la remodelación ósea 12.
Como todos estos dispositivos son formulados, se debe proveer al paciente y a los cuidadores la educación y el entrenamiento necesarios sobre su utilización, con el fin de maximizar la función, la independencia, la seguridad, el acceso y la participación en las actividades de la vida diaria.
Con respecto a la deformidad vertebral y la escoliosis, se debe hacer vigilancia radiológica, principalmente cuando el paciente realiza la transición a la silla de ruedas, ya que debido a la debilidad proximal y del tronco, con atrofia de los músculos paraespinales, algunos pacientes presentan lordosis compensatoria durante la bipedestación, mientras que otros pueden presentar síndrome de espina rígida. Las deformidades en la columna pueden llegar a ser muy severas y producir distintas complicaciones, sobre todo la exacerbación de la restricción en la ventilación. En la actualidad, el tratamiento más efectivo es la intervención quirúrgica para las enfermedades neuromusculares progresivas que conllevan deformidades vertebrales 5.
Ejercicio aeróbico y de fortalecimiento
Antes de iniciar el entrenamiento físico se debe estudiar la función cardiopulmonar, con el fin de establecer la seguridad de la respuesta cardiovascular y pulmonar, para iniciar el ejercicio terapéutico y garantizar la estabilidad clínica de la enfermedad, de modo que se evite la debilidad por sobreesfuerzo y se conserve la energía celular, principalmente en los pacientes con EP de inicio infantil 11.
El ejercicio aeróbico, que consiste en una actividad rítmica, prolongada, suficiente para proveer un estímulo cardiopulmonar y muscular debajo del umbral anaeróbico, aumenta la densidad capilar y la función mitocondrial. El ejercicio de anaeróbico (fortalecimiento) se recomienda que sea submáximo y que se suspenda en caso de fatiga 13,14.
En el mayor estudio aleatorizado realizado en el 2015 15 en pacientes con EP, de 23 de 25 pacientes en TRE completaron 3 sesiones semanales de entrenamiento aeróbico y de fortalecimiento. Los autores reportaron pequeñas pero significativas mejorías en la resistencia, la fuerza y la función muscular, como también mayor estabilidad de los músculos axiales.
Estudios pequeños no controlados han documentado los beneficios del ejercicio aeróbico y de fortalecimiento con mejoría en la distancia en el test de marcha de 6 minutos. Otros incluso han demostrado estabilización en la progresión de la enfermedad en pacientes sin TRE 16.
También se pueden explorar otras modalidades de ejercicio, principalmente en los pacientes con mayor debilidad o que no puedan realizar marcha, como el entrenamiento acuático que limita la fuerza de gravedad y activa el sistema cardiovascular 10.
Es importante educar a los pacientes en el monitoreo de su frecuencia cardiaca y la respiración antes de la fatiga y disminuir las complicaciones por la debilidad.
Entrenamiento de los músculos respiratorios
Hay estudios que demuestran que el entrenamiento en la musculatura inspiratoria mejora apreciablemente la presión inspiratoria máxima, sobre todo en pacientes que aun no dependen de ventilación mecánica. Entre las recomendaciones terapéuticas de la vía respiratoria se encuentra el manejo de las secreciones bronquiales mediante terapia respiratoria con técnicas aspirativas, asistencia en la tos y monitoreo continuo de problemas ventilatorios durante el sueño 1. En este suplemento se encuentra un capítulo dedicado a toda la función y la rehabilitación respiratoria en la EP.
Deglución y lenguaje
Los pacientes con EP, en particular con enfermedad de inicio infantil, presentan dificultad para el lenguaje y la deglución debido a hipotonía facial, macroglosia con debilidad de los músculos linguales y limitación de los movimientos orofaciales. Los pacientes presentan dificultades en el manejo de la saliva y las secreciones, que suelen acumularse en los pliegues vocales, lo que puede conllevar complicaciones respiratorias adicionales como microaspiraciones y neumonía aspirativa. Adicionalmente, se puede presentar debilidad de la musculatura gastrointestinal, lo que produce reflujo gastroesofágico, gastroparesia y disminución de los movimientos intestinales. Por lo tanto, estos pacientes requieren intervención por gastroenterología, piscología, nutricional y fonoaudiología 3. Este último servicio también estimula la musculatura orofacial en la articulación del lenguaje y las funciones comunicativas. Para este punto es importante realizar una valoración anual de la audición, la cual se puede ver afectada.
Nutrición
La mayoría de los pacientes con EP tienen obesidad sarcopénica (baja masa muscular y alto porcentaje graso); por lo general, presentan un índice de masa corporal bajo, lo que puede ser precursor de osteoporosis e incrementa el riesgo de fractura, por lo cual se debe hacer control con densitometría ósea anual. Debido a esta composición física se presentan alteraciones en el consumo de proteínas (subóptimo), combinadas con un consumo energético alto a nivel muscular. Por consiguiente, estos pacientes deben ser valorados nutricionalmente y optimizar la síntesis de proteínas musculares mediante el consumo de proteínas de alto valor biológico. Asimismo, también presentan déficits de vitaminas, especialmente la vitamina D en los más inactivos, por lo cual se debe dar un buen suplemento. Aun no se ha evaluado el suplemento de aminoácidos 17.
Manejo del dolor
Por lo general, no hay dolor en la valoración inicial, y se ha visto que es más común en la EP de inicio tardío. Los mecanismos del dolor son multifactoriales, como inflamación en los músculos y en los nervios, fatiga y deformidades musculoesqueléticas como la escoliosis, que contribuyen a una alta prevalencia de dolor de espalda. Adicionalmente, la escoliosis puede producir rigidez de la columna cervical y dorsal, lo que a su vea ocasiona síndrome de espina rígida y una sensación de fatiga crónica que interfiere con las actividades de la vida diaria. Aun no hay ensayos clínicos con la TRE que tengan como desenlace terapéutico el dolor, pero revisiones iniciales demuestran que la percepción del dolor puede variar por depresión, fatiga y calidad de vida. Con frecuencia, para el manejo del dolor en la EP se utilizan AINE y acetaminofén (paracetamol), sin embargo, la terapia física mejora la fatiga y la sensación de dolor. Los pacientes con miopatías metabólicas deben evitar situaciones que produzcan esfuerzo muscular, deshidratación o temperaturas extremas, a fin de prevenir la fatiga y el dolor 18.
Apoyo psicológico
El diagnóstico de la EP no solo afecta al individuo, sino también a su familia, que debe involucrarse en el cuidado. La aceptación de la enfermedad por parte del paciente y su familia puede requerir intervención psicológica individual o familiar, y también se puede dar consejería para que se involucren con alguna asociación de afectados por EP, quienes tienen programas de acompañamiento y apoyo psicológico, no solo de la enfermedad sino también del tratamiento con TRE, lo que le permite al paciente comprometerse con las intervenciones terapéuticas y mejorar su calidad de vida 6.
Cuidados paliativos
Al presentarse un franco deterioro funcional, con dependencia severa en todas las actividades básicas de la vida diaria por limitación postural y en la movilidad, en esta fase se tiene como objetivo mantener las mejores condiciones hasta el final de la vida, de manera que se manejen los síntomas y se dé apoyo integral al paciente y a su familia 19.
En este momento se evalúa el requerimiento de traqueostomía y gastrostomía, con el propósito de asegurar la ventilación pulmonar y el aporte nutricional. Al presentarse el deterioro pulmonar y cardiaco se decide iniciar manejo con ventilación mecánica invasiva o no invasiva, según las indicaciones del grupo interdisciplinario, principalmente el neumólogo.
La rehabilitación tiene como propósito el manejo domiciliario, con intervenciones dirigidas a la familia, con el fin de evitar la aparición de complicaciones derivadas de los cuidados generales, como deformidades osteomusculares que dificulten el posicionamiento y las actividades de higiene 20.
Conclusiones y recomendaciones
La EP requiere un manejo de rehabilitación integral, ya que se deben abordar las múltiples necesidades de cada individuo según la edad de inicio y la severidad clínica. De acuerdo con el inicio de la TRE y la capacidad funcional de cada paciente, el equipo de rehabilitación permite estructurar los objetivos de las diversas intervenciones y cuidados.
Es recomendable contar con un grupo de manejo interdisciplinario, con una comunicación constante, para abarcar el compromiso en la fisiología de los diferentes sistemas, a fin de reducir el impacto en la independencia funcional y en la calidad de vida de cada paciente, como también de su entorno biopsicosocial.