Introducción
La falla cardiaca es un síndrome clínico en el cual múltiples etiologías convergen en una sintomatología común 1,2, está ampliamente descrito el aumento gradual en su incidencia de presentación correlacionado con los cambios en la pirámide poblacional 3. En las últimas décadas, se ha definido una nueva clasificación ecocardiográfica con base en la medición de la fracción de eyección del ventrículo izquierdo (FEVI) que ha demostrado presentar amplias diferencias en cuanto a sus estrategias de manejo farmacológico y diversos desenlaces en los estudios experimentales 4. Se habla entonces de falla cardiaca con fracción de eyección preservada (ICFEp) cuando la FEVI es ≥50 %, reducida (ICFEr) ≤ 40 % y en rango medio (ICFEm) entre 40-50 % 5. No es infrecuente abordar este tipo de pacientes en el ámbito operatorio y anestésico, además poco se ha descrito del manejo óptimo de esta entidad y sus complicaciones en un contexto preoperatorio 6. El objetivo de la siguiente revisión es realizar una recopilación de la literatura actual para el abordaje y manejo de los pacientes con ICFEp en el pre, intra y posoperatorio.
Metodología
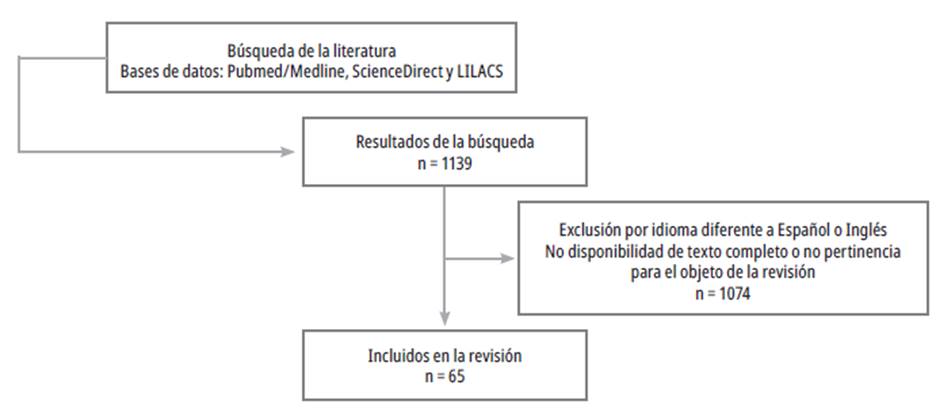
Se consultaron las bases de datos Pubmed/Med-line, ScienceDirect y LILACS con los términos "heart failure with preserved ejection fraction" "perioperative" "heart failure and anesthesia" "perioperative diastolic disfuction", en idioma inglés o español, y cuyo texto completo estuviera disponible. Los artículos fueron seleccionados por los autores de acuerdo con el objetivo de la revisión incluyendo metaanálisis, revisiones sistemáticas, ensayos clínicos y artículos de revisión. Se encontraron 1139 artículos, de los cuales se seleccionaron 65 (Figura 1).
Epidemiología
La prevalencia de falla cardiaca en general puede variar desde el 1 % hasta el 14 % en EE. UU. y Europa 4,7. En Colombia según un estudio publicado en 2012, la insuficiencia cardiaca tiene una prevalencia en la población general de 2,3 % 8 y de este porcentaje el 67,5 % corresponde a ICFEp 9. La falla cardiaca con fracción de eyección preservada en la actualidad no solamente es frecuente sino que su incidencia aumenta a razón de 1 % por año 10; en las grandes cohortes cardiovasculares se ha encontrado que su presentación varía entre 36,9 % hasta más del 50 % del total de los pacientes con falla cardiaca 11-13, es más frecuente en población anciana y de sexo femenino y se ha asociado con comorbilidades como la obesidad, la hipertensión arterial, las taquiarritmias supraventriculares como la fibrilación auricular y, en menor medida, la cardiopatía isquémica 14. La tasa de mortalidad intrahospitalaria varía entre 2,4 15 y 4,9 % 16 y el pronóstico de la enfermedad no es bueno, pues a los 5 años más de la mitad de los pacientes han fallecido; esto se correlaciona de manera directa con la carga de comorbilidades asociadas 17,18. En el ámbito perioperatorio, el panorama es similar puesto que se ha identificado la falla cardiaca como un fuerte predictor de complicaciones cardiovasculares mayores y además cada día se da más importancia a la disfunción diastólica como predictor independiente de complicaciones mayores como falla cardiaca aguda y edema agudo de pulmón 19, tanto en cirugía cardiaca 20 como no cardiaca 21.
Fisiopatología
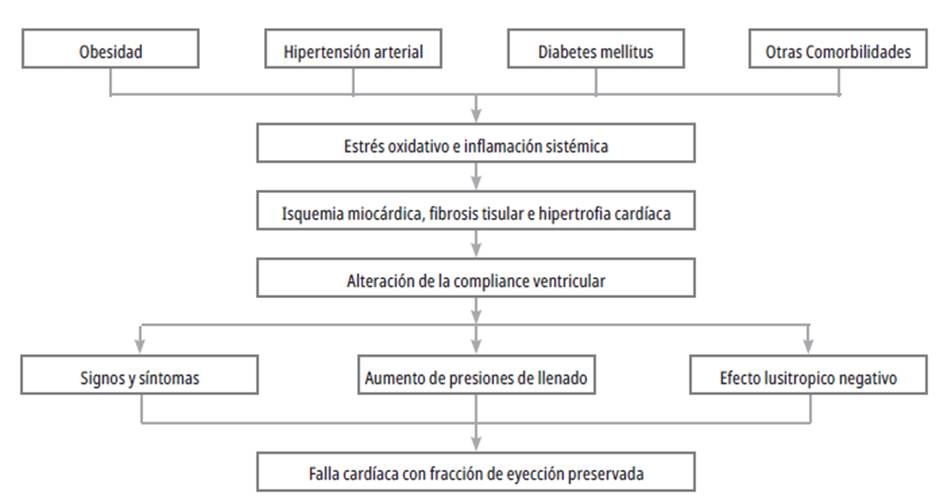
El sustrato fisiopatológico de la ICFEp en su totalidad no es bien conocido, sin embargo en la actualidad se acepta que interviene en mecanismos diastólicos y no diastólicos 22. En condiciones normales, la fase diastólica representa 2/3 partes del total del ciclo cardiaco y constituye el trabajo interno miocárdico que tiene lugar en cuatro fases: relajación isovolumétrica, llenado rápido, llenado lento o diástasis y sístole auricular 23. Las comorbilidades que acompañan a la enfermedad como la hipertensión arterial, diabetes mellitus y obesidad generan un ambiente de estrés oxidativo endotelial que ocasiona daños al cardiomiocito sufriendo apoptosis y fibrosis, lo que a su vez ocasiona rigidez, remodelación ventricular y disminución de la compliance que ocasiona disfunción diastólica 22-24; como consecuencia de este fenómeno, las cuatro fases diastólicas se ven alteradas y las presiones de llenado auricular izquierdo aumentan con el fin de compensar y mantener el volumen de fin de diástole estable. En etapas iniciales este mecanismo es eficiente, sin embargo el aumento de presiones de manera retrógrada repercute en la circulación pulmonar y en las cavidades derechas que terminan sufriendo remodelación en estadios más tardíos 25,26. Por el aumento de la presión en el circuito pulmonar, estos pacientes pueden desarrollar hipertensión pulmonar y concomitar con disfunción ventricular derecha, lo que se traduce en síntomas congestivos, disminución de la tolerancia al ejercicio e insuficiencia cronotrópica 27. (Figura 2).
Cuadro clínico y diagnóstico
Para el diagnóstico se deben correlacionar los hallazgos de la historia clínica, la presencia de signos o síntomas de la enfermedad y el hallazgo de una fracción de eyección preservada usualmente medido por ecocardiografía transtorácica 28.
Los métodos no invasivos como la ecocardiografía transtorácica son utilizados con frecuencia, puesto que además ayudan a excluir causas como valvulopatías, derrame pericárdico, hipertensión pulmonar e insuficiencia cardiaca con FEVI reducida 29. En la radiografía de tórax se puede encontrar cardiomegalia o signos de congestión pulmonar y en el electrocardiograma los hallazgos son inespecíficos pudiéndose encontrar fibrilación auricular o signos de isquemia antigua 30. Los péptidos natriuréticos en estos pacientes tienen valores menores que en el paciente con falla cardiaca y fracción de eyección ventricular reducida 31, aunque se acepta que valores por encima de 100 pg/ml para el péptido natriurético cerebral (BNP) o un péptido natriurético cerebral N- terminal mayor de 300 pg/ml se asocian con desenlaces cardiovasculares adversos 32, sin olvidar que valores inferiores no descartan la presencia del síndrome 29.
La ecocardiografía es la herramienta no invasiva más útil en el abordaje de estos pacientes, la fracción de eyección ventricular izquierda estima la función sistólica global pero no indica volumen ventricular izquierdo o volumen latido. A pesar de una FEVI preservada, los pacientes con ICFEp pueden presentar alteraciones que pueden ser medidas usando la excursión sistólica del anillo mitral o velocidades sistólicas como el strain longitudinal global. Un índice E/e' mayor o igual a 15 en reposo tiene buen valor diagnóstico para identificar una presión en cuña pulmonar elevada que apoye el diagnóstico. La IC-FEp no puede ser diagnosticada con un parámetro ecocardiográfico único, sino que requiere una combinación de parámetros estructurales y funcionales. Recientemente la Sociedad Europea de Cardiología describe criterios funcionales y morfológicos mayores y menores para facilitar el abordaje de estos pacientes, desde el punto de vista funcional. Criterios mayores: e' septal < 7 cm/s o e' lateral < 10 cm/s, relación E/ e' > 15, velocidad de regurgitación tricuspidea > 2,8 m/s (PSAP > 35 mmHg). Criterios menores: E/ e' promedio 9-14, strain longitudinal global < 16 %. También se han descrito como criterios morfológicos mayores: índice volumen aurícula izquierda > 34 ml/m2 o índice de masa ventrículo izquierdo ≥ a 149 (hombres) y ≥ 122 (mujeres) gr/m2, grosor relativo de la pared (RWT) mayor a 0,42. Criterios menores: índice volumen aurícula izquierda 29-34 ml/m2 o índice masa ventrículo izquierdo 115 gr/m2 (hombres) 95 gr/m2 (mujeres), RWt > 0,42 o grosor de la pared del ventrículo izquierdo > 12 mm 29.
El cateterismo cardiaco izquierdo que demuestra presiones de llenado ventricular en reposo ≥ a 16 mmHg confirma el diagnóstico de ICFEp, al igual que una presión en cuña media en reposo ≥ a 15 mmHg 29.
Para facilitar el abordaje diagnóstico, se han desarrollado herramientas como el Score H2FPEF (por la Clínica Mayo) utilizando seis variables clínicas y ecocardiográficas. Al asignar diferentes puntajes a cada uno de ellos (Tabla 1), se pueden obtener puntajes de 0-9 y los bajos valores (0-1) descartan el síndrome, mientras puntajes altos (69) pueden establecer el diagnóstico y los valores intermedios 2-5 pueden sugerir la realización de test adicionales 33.
Tabla 1 Score H2FPEF para el diagnóstico de ICFEp
| Variable clínica | Parámetro | Puntos | |
|---|---|---|---|
| H2 | Peso | Índice de masa corporal mayor de 30 kg/m2. | 2 |
| Hipertensión arterial | Dos o más medicamentos antihipertensivos. | 1 | |
| F | Fibrilación auricular | Paroxística o persistente. | 3 |
| P | Hipertensión pulmonar | Presión sistólica de la arteria pulmonar > 35 mm Hg (Doppler ecocardiográfico). | 1 |
| E | Edad | Edad mayor de 60 años. | 1 |
| F | Presión | E/ e'> 9 (Doppler ecocardiográfico). | 1 |
Fuente: tomado de Reddy YN, Carter R, Obokata M, Redfieid MM, Boriaug, BA. Circulation. 2018;138(9):861-870. Doi: https://doi.org/10.1161/CIRCULATIONAHA.118.034646 33
Tratamiento
El tratamiento de este síndrome en la actualidad está dirigido a mejorar los estilos de vida, el manejo óptimo de las comorbilidades y la mejoría de los síntomas congestivos usualmente con el uso de diuréticos 22,34. Pese a los múltiples estudios realizados en busca de algún tratamiento farmacológico que impacte en el curso de la enfermedad, hasta el momento este objetivo no se ha logrado, a diferencia de lo que ocurre con la insuficiencia cardiaca con fracción reducida 35,36. La inhibición del sistema renina-angiotensina-aldosterona (IECAS y ARA II) no ha demostrado impactar en morbimortalidad en estos pacientes 37-39, los antialdosterónicos parecieran tener mejor perfil y algunos estudios indican que pueden asociarse con disminución de la mortalidad y hospitalización por falla cardiaca; dicho efecto no es reproducible a todas las poblaciones 40. Por su parte, la utilidad y eficacia de los betabloqueantes no es clara, se han realizado diversos estudios con resultados contradictorios por lo que se considera que actualmente su utilidad y efecto aún son inciertos y no se recomiendan de manera rutinaria 41, lo mismo sucede con la ivabradina 42 y la digoxina 43 que no han demostrado mejoría en el pronóstico de la enfermedad. Otras terapias farmacológicas que se han considerado para el tratamiento del síndrome son el uso de nitratos 44, inhibidores de la fosfodiesterasa 5 45, inhibidores del receptor de angiotensina II y neprilisina 46 y ranolazina 47; sin embargo, los resultados no son concluyentes por lo que se necesitan estudios posteriores para emitir recomendaciones sólidas respecto al uso de los medicamentos en mención. En la actualidad se estudia el uso de hierro parenteral en el tratamiento y los desenlaces de pacientes con ICFEp, dos ensayos clínicos se encuentran en curso: el PREFER HF y el FAIR HFpEF cuyos resultados pueden orientar nuevos horizontes terapéuticos 48.
Abordaje perioperatorio
El abordaje de estos pacientes constituye un reto para el anestesiólogo considerando las implicaciones fisiopatológicas del síndrome, las comorbilidades existentes, las escasas herramientas terapéuticas y las limitadas recomendaciones perioperatorias a la luz de la evidencia actual (Tabla 2). La valoración preanestésica debe incluir la descripción y optimización de las patologías concomitantes, pues es bien sabido que la enfermedad está asociada usualmente con la presencia de comorbilidades como la fibrilación auricular, anemia, diabetes mellitus, hipertensión arterial y obesidad 49,50. En aquellos pacientes con disfunción diastólica severa o sometidos a cirugía mayor, se debe considerar una evaluación detallada que puede incluir la realización de ecocardiografía de stress, resonancia magnética cardiaca, cateterismo cardiaco derecho e izquierdo, además del concepto especializado de cardiología 51.
Tabla 2 Recomendaciones para el abordaje de pacientes con falla cardiaca y fracción de eyección preservada en el perioperatorio
1 Equivalentes metabólicos.
Fuente: elaboración propia.
La valoración cardiovascular debe ser completa e incluir la capacidad funcional en equivalentes metabólicos (METs), y se ha demostrado que un hallazgo < 4 METs es un fuerte predictor de eventos cardiacos posoperatorios 52. Se debe indagar sobre la terapia farmacológica actual, pues aunque ningún medicamento ha demostrado impactar fuertemente en el pronóstico y la mortalidad de estos pacientes, las comorbilidades usualmente obligan a la utilización de terapias con betabloqueantes, IECAS, ARA II o diuréticos 53,54. El anestesiólogo debe considerar dar continuidad a la terapia con betabloqueantes incluso el día de la cirugía en aquellos pacientes que ya tienen el tratamiento instaurado 55,56; en cuanto la terapia con IECAS y ARA II, la decisión está condicionada por las cifras tensionales y el riesgo de hipotensión intraoperatoria pudiéndose continuar la terapia o suspenderla previo al procedimiento 56.
Paraclínicos como el hemograma, la radiografía de tórax y la función hepática y tiroidea pueden ser tomados dependiendo de las particularidades y los objetivos que se quieren alcanzar en cada paciente. Algo para considerar es el uso crónico de diuréticos, por lo que es importante la toma de electrolitos previa al procedimiento y la corrección de los disturbios de estos 10, particularmente la hipocalemia que puede ser resultado del consumo crónico de furosemida y que se asocia con desenlaces adversos intraoperatorios 57,58.
La elección de la técnica anestésica va estar determinada por varios factores entre ellos el tipo de procedimiento, las preferencias del paciente y la experiencia del anestesiólogo; sin embargo, lo que sí es claro es que independientemente de la técnica anestésica, se deben perseguir los siguientes objetivos: control de la respuesta cronotrópica, mantenimiento de estabilidad hemodinámica así como el ritmo sinusal, evitar la congestión pulmonar y mantener adecuadas presiones de llenado 10,59. Se pone énfasis en el control de la respuesta cronotrópica, pues la taquicardia se traduce en disminución del tiempo de diástole y esto sumado a la disminución de la compliance ventricular hace que se comprometa la perfusión miocárdica de manera crítica llegando incluso a desencadenar un episodio de falla cardiaca aguda; de ahí la importancia de que el anestesiólogo sea cuidadoso en aquellas situaciones que pudiesen desencadenar taquicardia tales como: el dolor, el proceso de inducción, la ansiedad, la hipovolemia, la anemia aguda y la hipercapnia 60.
Deben tenerse consideraciones con el uso de ciertos medicamentos tanto para la inducción, el mantenimiento y la analgesia del paciente, ya que el impacto en la función diastólica difiere entre unos y otros; por ejemplo, la ketamina y los barbitúricos inhiben el transporte de calcio en el sarcómero y pueden tener un efecto negativo sobre la compliance ventricular empeorando la disfunción basal del paciente, motivo por el cual deben evitarse en la medida de lo posible, a diferencia del uso de otros medicamentos como el sevoflurano, desflorane, isoflorane, propofol, etomidato, midazolam, morfina y remifentanil que parecen ser seguros y tener un perfil diastólico neutro 10,61-63.
La monitoria va a variar en función del procedimiento y del grado de disfunción diastólica. Si se considera cirugía de alto recambio sanguíneo, lo mejor es contar con monitoría invasiva de la presión arterial, mediciones indirectas de precarga y otras variables hemodinámicas de ser posible, todo esto con el fin de mantener adecuada presión arterial evitando reducciones mayores del 20 % del valor basal; además, la titulación de los líquidos debe ser cuidadosa, lo suficiente para mantener presiones de llenado adecuadas pero sin llevar el paciente a edema pulmonar 60,64.
En el período posoperatorio se pueden presentar complicaciones como en otros pacientes; aunque la fibrilación auricular, hipoxemia y descompensación de falla cardiaca usualmente son las más comunes, se debe tener en cuenta que en el momento de la emergencia anestésica aumenta el tono simpático y el volumen intravascular pudiendo llevar a descompensación aguda y edema pulmonar. El manejo óptimo del dolor es fundamental, como ya se explicó previamente, con el fin de evitar la respuesta simpática y aumentar la sobrecarga miocárdica por los mecanismos ya descritos.
Conclusiones
Como conclusiones, se podría considerar que la falla cardiaca con fracción de eyección preservada en el perioperatorio es un síndrome no infrecuente, más frecuente en mujeres y ancianos, asociado con múltiples etiologías, comorbilidades y complicaciones y mal pronóstico. El ecocardiograma transtorácico con base en mediciones de función y morfología apoyados por parámetros específicos por doppler tisular, speckle tracking y strain longitudinal global asociadas con elevaciones de biomarcadores como el BNP y NT-proBNP han permitido calcular y establecer scores diagnósticos como el HFA-PEFF (puntajes ≥ 5), que sugieren falla cardiaca con FEVI preservada. En ocasiones debemos recurrir a la resonancia magnética cardiaca para establecer patología miocárdica y pericárdica específica y en casos de incertidumbre diagnóstica recurrir al ecoestrés diastólico y confirmar mediante pruebas hemodinámicas invasivas en reposo y ejercicio el diagnóstico definido de falla cardiaca con FEVI preservada. A diferencia del manejo con falla cardiaca con FEVI reducida, no existen estudios confirmatorios de disminución de la mortalidad por lo que se requieren nuevos estudios clínicos de fármacos que mejoren las perspectivas anestésicas y el abordaje terapeútico perioperatorio, nuevos paradigmas en el conocimiento de la fisiopatología de la remodelación y disfunción ventricular 65, así como el entendimiento de las manifestaciones clínicas y el abordaje perioperatorio guiado por metas fisiológicas que continúan siendo los pilares en la actualidad.