Introducción
De acuerdo con la Organización Mundial de la Salud, el tabaquismo encabeza la lista de las sustancias de abuso que causan más enfermedades y muertes relacionadas con drogas en el mundo 1. Las muertes atribuidas al tabaquismo se relacionan principalmente con cáncer, enfermedades respiratorias, enfermedades cardiovasculares, deterioro de la salud mental e incremento en el uso de otras drogas 2)(3.
La nicotina es el principal componente adictivo del tabaco, actúa través de receptores nicotínicos expresados en regiones del cerebro involucradas en los sistemas de recompensa, emoción, aprendizaje y memoria de la corteza prefrontal y del sistema límbico, áreas implicadas en la conducta adictiva 4.
Las intervenciones psicoterapéutica, ambiental y farmacológica son útiles para apoyar a las personas que desean dejar de fumar, siendo la combinación de consejería y farmacoterapia la opción más efectiva 2. Aunque las tasas de abstinencia con tratamiento farmacológico superan en mucho a las obtenidas con placebo, hasta el 50% de los pacientes han recaído a los 90 días de seguimiento y no más 42% y del 19% de quienes dejaron el cigarrillo siguen en abstinencia seis y doce meses después, respectivamente 5. Esto muestra la necesidad de descubrir tratamientos más efectivos, lo cual requiere entender mejor los factores contribuyentes a la adicción a la nicotina y a la respuesta a los medicamentos.
Existen tres medicamentos aprobados internacionalmente para tratamiento del tabaquismo: la nicotina, la vareniclina y el bupropion, lo que constituye un escaso número de opciones terapéuticas; la citisina ha mostrado beneficios, pero su rol en los protocolos de tratamiento aún no está definido 6.
Se acepta que en la severidad de la adicción la heredabilidad (la fracción de riesgo atribuible a factores genéticos) es del 40% al 70% 7. Son numerosos los genes que aparecen como candidatos a influir en la adicción a la nicotina y en la respuesta al tratamiento del tabaquismo, pero la mayor atención se ha enfocado en los genes que codifican para las principales enzimas responsables del metabolismo de la nicotina (CYP2A6) y del bupropion (CYP2B6), así como en los genes que codifican los receptores nicotínicos 8.
La variante CYP2B6*4 (rs2279343, c785 A>G) conduce a mayor expresión de la enzima, de modo que los individuos con los genotipos mutados AG y GG tienen acelerado el metabolismo del bupropion, en comparación con los portadores del genotipo nativo AA. En consecuencia, a dosis similares de bupropion, los homocigotos nativos tendrían concentraciones séricas más elevadas y persistentes del fármaco, en comparación con los metabolizadores más rápidos que tienen el alelo G; esto explicaría el mayor éxito en el abandono del tabaquismo en los pacientes portadores del genotipo nativo AA que son tratados con bupropion 9. El gen CYP2A6 también es polimórfico y, en comparación con el genotipo nativo, algunos alelos se relacionan con menor respuesta a nicotina, particularmente aquellos que se traducen en un fenotipo “deficiente metabolizador”, entre ellos los que portan el SNP rs56113850 y los que comparten el polimorfismo rs1137115 (51G>A) 10.
El creciente problema de abuso del tabaco y la efectividad limitada de los actuales protocolos de tratamiento, justifican la búsqueda de nuevas alternativas terapéuticas que mejoren las tasas de adherencia y minimicen las recaídas y la morbimortalidad asociadas con esta adicción. La identificación de marcadores genéticos influyentes en la respuesta a las diferentes opciones farmacológicas representa una promisoria estrategia para alcanzar una medicina de precisión más efectiva. En esta serie de pacientes tratados con enfoque farmacogenético encontramos que mejoraron las tasas de retención, abstinencia, recaídas y tolerabilidad, en comparación con los resultados reportados en los tratamientos convencionales.
Descripción de los casos
Se incluyeron 21 pacientes, el 67% de ellos de sexo masculino (14/21), con edades entre 27 y 64 años (46,2±11,7 años) e índice de masa corporal de 24±3. Solamente 6 personas no tenían otros factores de riesgo cardiovascular y 15 no consumían medicamentos.
La edad de inicio en el consumo regular de cigarrillo fue de 17,8±6,4 años, la duración del tabaquismo era de 28±13,4 años y los pacientes consumían un promedio de 17±12 CPD, habían hecho 3,7±2 intentos previos por dejar de fumar y el puntaje NDSS fue de 22,4±4,8. El 62% de los individuos (13/21) tenía un entorno familiar o laboral proclive al tabaquismo. En la tabla 1 se muestran estas mismas variables discriminadas por género, donde se aprecia que entre hombres y mujeres no hubo diferencias significativas con respecto al fenotipo de fumador.
Tabla 1 Fenotipos de los fumadores, discriminados por género.
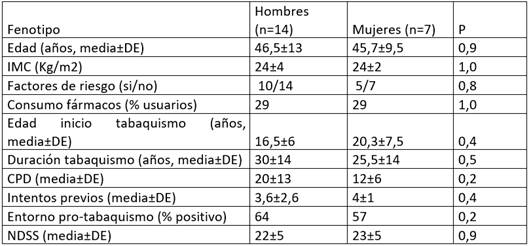
IMC: índice de masa corporal; CPD: cigarrillos por día; NDSS: escala breve de evaluación de dependencia de la nicotina.
P: Chi cuadrado o Mann-Whitney, según el tipo de variable.
Los pacientes fueron prescritos con nicotina o bupropion según los genotipos CYP2A6 (que codifica la enzima que metaboliza la nicotina) y CYP2B6 (que codifica la enzima que metaboliza el bupropion). El tratamiento con nicotina se realizó con parches transdérmicos de 14 mg el primer mes y luego de 7 mg el segundo mes, complementados con chicles para manejo del síndrome de abstinencia, mientras que a los pacientes tratados con bupropion se les indicó formas de liberación regulada por 300 mg, 1-2 veces al día. Todos los pacientes recibieron consejería una vez a la semana y tenían acceso telefónico al médico tratante. Después de 8 semanas de tratamiento y 4 de observación, 15 sujetos (71,4%) respondieron en forma parcial/total. El consumo de CPD bajó de 17±12 al inicio del estudio, a 2,2±3,5 al final del estudio, que corresponde a una reducción de 195 cigarrillos/día. Siete de ocho pacientes tratados con bupropion (87,5%) y siete de trece tratados con nicotina (54%) tuvieron respuesta parcial/total.La tasa de recaídas, evaluada un mes después del tratamiento farmacológico, fue de cero. Se encontró buena correlación genotipo-fenotipo en los individuos tratados con bupropion, pero no en los tratados con nicotina.
Los pacientes refirieron satisfacción respecto al tratamiento; solo un paciente formulado con nicotina suspendió el medicamento por intolerancia gastrointestinal (náusea y vómito).
Discusión
El fenotipo de los fumadores del estudio, correspondiente a individuos de edad media, con predominio masculino, prevalencia relativamente alta de factores de riesgo cardiovascular (71%) e inicio en el tabaquismo a los 17 años coincide con los reportes de numerosas investigaciones.
Los promedios de años del consumo de cigarrillos (~28 años), del número de cigarrillos consumidos por día (~17), de los intentos fallidos por dejar de fumar (~4) y de los puntajes NDSS (~22) muestran un grupo de personas con características de tabaquismo severo, pero motivados para dejar de fumar.
La tasa de retención lograda en esta serie de casos (71,4%) es similar o superior a la reportada en otros estudios y corresponde a los 15 individuos que al final de la octava semana de tratamiento habían suspendido totalmente el consumo de cigarrillos (7/15), o solamente lo habían disminuido (8/15), lo cual también está descrito, pues casi nunca se alcanza un 100% de abstención 11. De todos modos, una reducción del consumo de 195 cigarrillos/día en nuestra serie de casos es importante desde el punto de vista clínico y se ajusta a la estrategia de reducción del daño en el consumo de psicoactivos.
El hecho de que solo uno de los pacientes haya tenido que suspender el tratamiento por intolerancia a la nicotina, que no hubo reacciones adversas severas y que cuatro semanas después de terminada la medicación ningún participante del estudio haya recaído, refleja el buen margen de seguridad de los dos fármacos usados y refuerza la opinión de que los programas de dejación de tabaquismo son relativamente sencillos de implementar, no requieren recursos ni personal altamente calificado y resultan costo-efectivos, aunque está claro que las tasas de recaídas en el tabaquismo son altas y se incrementan con el tiempo 5.
La mejor respuesta terapéutica al bupropion (7 de 8 pacientes) que a la nicotina (7 de 13 pacientes) ha sido documentada en algunos estudios 12, aunque en otros encuentran que la nicotina y el bupropion son equiefectivos 6)(13.
Al incluir la variable genética en el análisis de los resultados, encontramos que ninguno de los dos polimorfismos del gen CYP2A6 se asoció con alguna de las características fenotípicas de los fumadores, ni con la respuesta a nicotina, pues el 50% de los pacientes con el genotipo nativo (6/12) no respondió al fármaco, que es un porcentaje de respuesta similar al reportado en los tratamientos con nicotina que no tienen en cuenta el genotipo. Con respecto a esta falta de correlación fenotipo-genotipo no existe consenso, ya que algunos estudios encuentran correlación y otros no 14)(15)(16.
Por el contrario, en el caso del bupropion, 7 de los 8 pacientes tratados según el genotipo (homocigotos o heterocigotos nativos para el gen CYP2B6) concluyeron el tratamiento con éxito, lo cual coincide con otros reportes 12)(17 y apoya la propuesta de que el genotipo CYP2B6 es un buen predictor de respuesta a este fármaco.
Se espera que los resultados presentados generen interés para la formulación de investigaciones más potentes, que exploren el papel de la farmacogenética en la respuesta a los medicamentos utilizados en los programas de dejación del tabaquismo.
Conclusión
La inclusión de marcadores farmacogenéticos para la elección de nicotina o bupropion en un programa de dejación de tabaquismo puede mejorar la adherencia al programa y la tolerabilidad al fármaco y, en el caso del bupropion, la efectividad del tratamiento.
Aspectos legales
El estudio fue aprobado por el Comité de Ética de la Universidad Tecnológica de Pereira. Se obtuvo consentimiento escrito para la genotipificación, el tratamiento y la publicación de los resultados, conservando la confidencialidad de los datos de los pacientes. Copias de los consentimientos firmados están disponibles para la revisión del Editor en Jefe de esta revista.















