Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Ciencias Químico - Farmacéuticas
Print version ISSN 0034-7418
Rev. colomb. cienc. quim. farm. vol.44 no.2 Bogotá May/Aug. 2015
https://doi.org/10.15446/rcciquifa.v44n2.56293
Microencapsulación de aceite esencial de tomillo (Thymus vulgaris) en matrices poliméricas de almidón de ñame (Dioscorea rotundata) modificado
Microencapsulation of thyme (Thymus vulgaris) essential oil in polymeric matrices based on modified yam (Dioscorea rotundata) starch
Germán Eduardo Matiz Melo a
Katerin Fuentes López b
Glicerio León Méndez c
a Grupo de Investigación en Tecnología de Productos Naturales (Tecprona), Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia, sede Bogotá, Cra. 30 No. 45-03, Bogotá, D. C., Colombia. Autor correspondiente. Correo electrónico: gematizm@unal.edu.co.
b c Grupo de Investigación en Tecnología Farmacéutica, Cosmética y de Alimentos (Gitfca), Facultad de Ciencias Farmacéuticas, Universidad de Cartagena, Cartagena, Colombia. Tel.: (1)3165000. Ext.: 14620. Correo electrónico: gleonm1@unicartagena.edu.co y kfuentesl@unicartagena.edu.co.
Recibido para evaluación: 20 de enero de 2015.
Aceptado para publicación: 2 de julio de 2015.
Resumen
Los aceites esenciales son conocidos por sus numerosas actividades biológicas y organolépticas, pero su empleo suele verse limitado por su alta volatilidad y tendencia a degradarse. La microencapsulación es una estrategia válida para superar estos inconvenientes. En este trabajo se empleó almidón de ñame (D. rotundata), el cual fue sometido a procesos de hidrólisis y lipofilización, empleando anhídrido dodecenilsuccínico (DDSA); esto incrementó significativamente las capacidades captadora de aceite y emulsificante (tensoactiva) del almidón nativo, el cual se empleó para microencapsular aceite esencial de tomillo, que en estudios previos demostró potente actividad antibacteriana sobre las cepas involucradas en el desarrollo del acné. La microencapsulación se llevó a cabo por microparticulación lipídica sólida, seguida de emulsificación. Esta alcanzó una eficiencia superior al 98%, y el producto obtenido, desafiado en diversas pruebas, demostró capacidad de retener más del 90% del aceite esencial en condiciones de evaporación, evitando su oxidación y el cambio en su perfil de composición. Finalmente, las microcápsulas de aceites esenciales de tomillo, al ponerse en contacto con las bacterias del acné, mantuvieron su actividad bactericida. Los resultados de este trabajo aportan al desarrollo de formulaciones farmacéuticas, cosméticas y alimentarias estables y funcionales de aceites esenciales, al protegerlos de la evaporación y degradación.
Palabras clave: almidones modificados, microencapsulación, Thymus vulgaris, hidrólisis, lipofilización, DDSA, acné.
Summary
Essential oils are known for their numerous biological and organoleptic activities, but their use is often limited by high volatility and tendency to degrade. Microencapsulation is a valid strategy to overcome these drawbacks. In this paper starch yam (D. rotundata) was used, which was subjected to hydrolysis processes and lipophilization using dodecenyl succinic (DDSA) anhydride, this significantly increased the scavenging capacity of oil and emulsifier (surfactant) of native starch, which was used to microencapsulate thyme essential oil, that in previous studies showed potent antibacterial activity on strains involved in the development of acne. Microencapsulation was conducted by microparticulation solid lipid, followed by emulsification. This reached an efficiency of over 98%, and the product obtained, challenged by various trials, demonstrated ability to hold more than 90% of essential oil under evaporation conditions, avoiding oxidation and change in composition profile. Finally, the microcapsules of essential oil of thyme at contact the acne bacteria, maintained its bactericidal activity. The results of this study contribute to the development of pharmaceutical, cosmetic and food formulations stable and functional based on essential oils, to protect degradation and evaporation.
Key words: Modified starches, microencapsulation, Thymus vulgaris, hydrolysis, lipophilization, DDSA, acne.
Introducción
Los aceites esenciales (AA. EE.) son mezclas complejas de sustancias químicas biosintetizadas fundamentalmente por las plantas, que les proporcionan su aroma característico. Muchos poseen actividades biológicas reconocidas como antisépticas, antiinflamatorias y repelentes de insectos, entre otras, amén de que otros son empleados como sazonadores. Con gran frecuencia, dichas propiedades no se aprovechan plenamente debido a su gran volatilidad y tendencia a oxidarse [1], por lo cual es necesario fijarlos a un transportador para proporcionarles una adecuada estabilidad y vida útil. Una de las mejores alternativas para llevar a cabo esto es la microencapsulación, para lo cual pueden emplearse biopolímeros de origen natural [2-5]. Generalmente, los materiales de pared usados para microencapsulación son goma arábiga, maltodextrina, carbometilcelulosas y almidón [6].
Colombia, dentro de su gran riqueza natural, posee numerosas fuentes de almidones nativos que han sido muy poco estudiados para fines no alimentarios. Estudios previos [7] permitieron desarrollar una serie de almidones lipofílicos a partir de fuentes propias de las regiones Caribe y Andina (ñame, batata, yuca, plátano, maíz, arracacha, achira, arroz, etc.), que probaron una importante capacidad emulsificante. Estos almidones, mediante procedimientos microtecnológicos posteriores son capaces de encapsular eficientemente AA. EE., con potenciales aplicaciones farmacéuticas, cosméticas y alimentarias. La microencapsulación se realiza empleando numerosos procesos [6, 8, 9], entre ellos el secado por aspersión o Spray Drying, la coacervación, formación de liposomas, entre muchos otros. Según las condiciones de elaboración y el tipo de material encapsulante, es posible obtener materiales capaces de retener AA. EE. y liberarlos en el momento de su uso. Estos productos pueden ser empleados como transportadores de aceites esenciales capaces de brindar protección a los mismos frente a la oxidación, la evaporación y el mantenimiento de su perfil cromatográfico, así como el control de su liberación.
Materiales y métodos
Reactivos y solventes: el etanol se adquirió de JT Baker (Phillipsburg, USA), anhídrido docecenil succínico caldo de Sigma-Aldrich (Saint Louis, USA). Medios de cultivo: Müeller Hinton (caldo MH), agar Müeller Hinton (agar MH), caldo Tripticasa Soya (caldo TSA), agar Tripticasa Soya (agar TSA), caldo Lutia Bertani (caldo LB) y agar Lutia Bertani (agar LB) se obtuvieron de Merck KGaA (Darmstadt, Alemania), gentamicina sulfato de Biopex SAC (estándar secundario lote: 10C256). Las cepas bacterianas se adquirieron de la American Type Culture Collection (ATCC): Propionibacterium acnes (P. acnes) ATCC 11827, Staphylococcus aureus (S. aureus) ATCC 25923 y Staphylococcus epidermidis (S. epidermidis) ATCC 12228. El aceite esencial de tomillo (Thymus vulgaris L.) se obtuvo en Green Andina Ltda. (Bogotá, Colombia).
El almidón de ñame (Dioscorea rotundata, var. espino) se obtuvo de tubérculos del mismo que se compraron en el municipio de San Juan Nepomuceno, norte del departamento de Bolívar (9° 37 latitud norte y 74° 15 longitud oeste), a 72 km de la ciudad de Cartagena. Se adquirieron en la parcela de un particular, 20 kilogramos de material vegetal fresco, entero, sin señales de deterioro y en estado de madurez para consumo humano. El proceso de extracción del almidón corresponde al método convencional de rallado y precipitación [10]. Inicialmente, con un lavado se retira la tierra y suciedad en general, seguido de un descortezado y nuevo lavado; luego se realiza un troceado y licuado con agua potable para obtener una lechada, esta se filtra por medio de una tela para eliminar las fibras de celulosa. El filtrado se deja en reposo y luego se decanta, el sobrenadante se elimina y el sedimento se lava con agua desionizada y se filtra al vacío, se seca a 50 °C por 24 horas, luego se muele y finalmente se empaca en recipientes herméticos. Aproximadamente un 10% de almidón seco es obtenido a partir del material vegetal, es decir, 2 kilogramos.
Caracterización del almidón
Contenido de amilosa: se disolvieron 20 mg de almidón (base seca) en 8 mL de dimetilsulfóxido (DMSO) al 90%, se agitó vigorosamente en un Vórtex por 20 minutos y posteriormente se calentó la dispersión en un baño de maría Memmet a 85 °C por 15 minutos. En seguida se enfrió la mezcla y se aforó a 25 mL con agua destilada. Se tomó 1 mL de esta dispersión y se transfirió a un matraz aforado de 50 mL, al cual se le había agregado 40 mL de agua destilada y 5 mL de una solución de yodo/yoduro de potasio (0,0025 M - 0,0065 M). Finalmente se aforó con agua, se homogenizó y se dejó en reposo por 15 minutos antes de leer en el espectrofotómetro a 630 nm, usando una curva patrón de almidón soluble (amilosa) estandarizado para la realización de los cálculos [11, 12].
Determinación de pH: se preparó una suspensión de 10 g de almidón en un vaso de precipitado de 100 mL y se adicionaron 50 mL de agua destilada, en agitación constante a una rata moderada por 5 minutos. Se determinó el pH empleando un potenciómetro previamente calibrado [13].
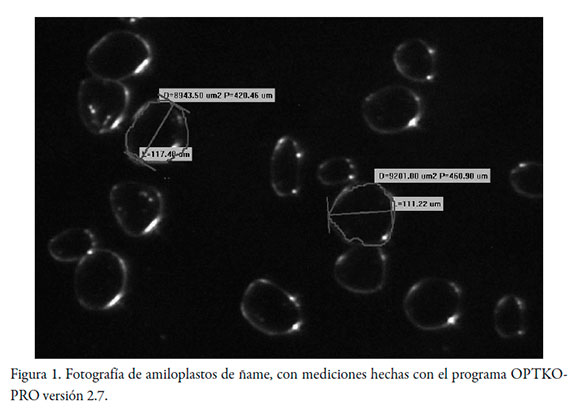
Tamaño de partícula: el tamaño medio de partícula se determinó según metodología de Edmundson [14]. Para la medición de las partículas se empleó un estéreo-microscopio NIKON SMZ745T (lente de 5X). Muestras muy pequeñas de almidón se pusieron sobre portaobjetos que posteriormente eran ubicados en la platina del equipo. Se observó la morfología, tamaño y bordes de las partículas para cada almidón y se tomaron varias fotografías. De cada una se escogieron 20 partículas que fueron analizadas y medidas empleando el programa OPTKO-PRO versión 2.7. Un mínimo de 200 partículas se analizaron por muestra.
Modificación química del almidón
Hidrólisis: a una suspensión de almidón nativo (40 g de almidón en 100 mL de agua desionizada) se añadió ácido clorhídrico hasta alcanzar una proporción de 3,4 g respecto de la base seca, con agitación constante por 6 horas; manteniendo la temperatura en 50 °C en un baño termostatado. Cumplido el tiempo, se neutralizó el sistema con NaOH al 10% hasta pH 6,5; se filtró al vacío y el residuo se lavó 4 veces con agua destilada, se secó a 50 °C por 24 horas y finalmente el almidón hidrolizado obtenido se molió y almacenó en bolsas plásticas herméticas hasta su uso [15].
Lipofilización: una suspensión de almidón nativo o hidrolizado a 25 °C (40 g de almidón en 100 mL de agua desionizada), se ajustó a pH 8,5 con NOH 3% con agitación constante por 30 minutos. En ensayos independientes se agregaron 10 o 15 mL de anhídrido dodecenil succínico (DDSA) diluido en 75 mL de etanol 96%, para alcanzar dos niveles diferentes de sustitución. Debido a que durante la reacción el pH de la solución tiende a descender, este se mantuvo entre 8,5 y 9,0 con pequeñas adiciones de NaOH 3%. Una vez que el reactivo límite se terminó, esto es, cuando el pH no desciende más, la solución se ajustó a un valor de 6,5 con HCl al 10%. El material se filtró a vacío y se resuspendió en agua desionizada para nuevamente ser filtrado. Esta operación se repitió por tres veces. Finalmente se dispuso en capas delgadas sobre bandejas y se secó en un horno de laboratorio (Memmert SNE 400) a 50 °C por 24 horas [16].
Para garantizar la remoción total del ácido dodecenil succínico libre, los almidones lipofilizados se sometieron a un lavado con ayuda de un extractor Soxhlet empleando 300 mL de etanol al 96% como solvente, y un mínimo de 10 recirculaciones; luego, el almidón fue filtrado y secado durante 24 horas a 50 °C.
Determinación del porcentaje de sustitución (PS): el PS representa el número promedio de grupos hidroxilos sustituidos por mol de anhidroglucosa (AG) [17]. El PS de los almidones succinatados se determinó por titulación ácido-base, toda vez que el residuo de ácido docecenil succínico unido a la cadena de almidón, posee un grupo carboxilo libre. Se pesaron 5 g de almidón modificado en un vaso de precipitado de 50 mL, a los que se adicionaron 25 mL de solución de HCl 0,01 N; para asegurar que los residuos se encontraran protonados (remineralización). Esta suspensión se agitó durante 30 minutos. La suspensión se filtró y la torta húmeda se lavó con agua desionizada hasta que no se detectaron cloruros en las aguas de lavado (utilizando solución de AgNO3 0,1 N). La torta húmeda se transfirió cuantitativamente a un vaso precipitado de 900 mL, añadiendo 100 mL de agua desionizada con posterior agitación. A continuación se incorporaron 200 mL de agua desionizada a ebullición. La solución se colocó en un baño de agua hirviendo durante 30 minutos, después de enfriada, y con adición de 2-3 gotas de fenolftaleína al 1% como indicador, se tituló con NaOH 0,01 N. El PS se calculó mediante la siguiente ecuación:
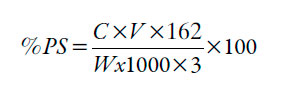
Donde:
C = normalidad de la solución de NaOH utilizado durante la titulación.
V = volumen consumido de la solución de NaOH.
W = peso de la muestra analizada.
162 es el peso molecular de la unidad AG.
3 es el número de hidroxilos presentes en cada unidad de AG.
Propiedades de los almidones modificados
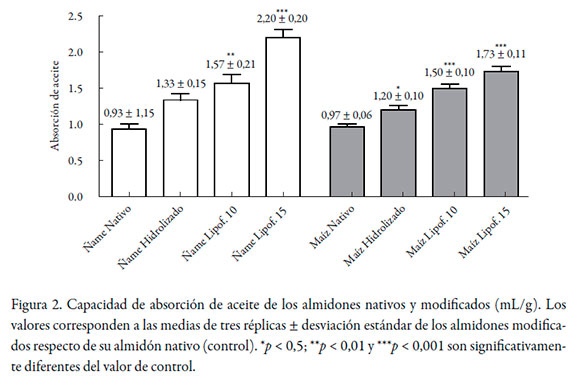
Absorción de aceite: este ensayo mide el cambio en la capacidad de los almidones modificados para absorber aceite. Para determinarla, se tomó 1 g de almidón y se mezcló con 10 mL de aceite de maíz en Vórtex durante 30 segundos. Las muestras se dejaron en reposo durante 30 minutos a una temperatura ambiente (25 +/- 2 °C). Luego se centrifugaron a 3.000 rpm durante 15 minutos, midiéndose el volumen del sobrenadante obtenido en una probeta de 10 mL. Los resultados se obtuvieron restando los 10 mL iniciales de aceite con el volumen después de la centrifugación, reportándose la capacidad de absorción de aceite en mL/g de muestra [18].
Absorción de agua: este ensayo es homólogo al anterior, pero orientado a la absorción o captación de agua, y se desarrolla de manera similar a la prueba de absorción de aceite, pero empleando agua en su lugar. Los resultados se obtuvieron restando los 10 mL iniciales de agua con el volumen de la misma después de la centrifugación. Se reporta la capacidad de absorción de agua en mL/g de muestra [18].
Capacidad emulsificante: los almidones tienen capacidad anfifílica frente al agua y el aceite, pero escaso poder tensoactivo. Al lipofilizar los almidones, esta propiedad cambia y debe ser evaluada. Para ello se mezcló 1 g de almidón con 25 mL de agua a 25 °C, agitándose manualmente durante 15 minutos; posteriormente se mezcló esta suspensión con 25 mL de aceite de maíz con ayuda de un homogenizador ultra turrax IKA T10 a 1.300 rpm por 3 minutos y se dejó en reposo a temperatura ambiente por 24 horas, al cabo de las cuales, se midió la cantidad de emulsión remanente (ER). Esta se expresó en términos de porcentaje, como volumen de la capa emulsificada (VCE) con respecto al total del líquido (VTL) empleando la siguiente expresión [19]:
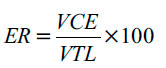
Microencapsulación de aceites esenciales
La microencapsulación se realizó mediante microparticulación lipídica sólida (MLS). Se tomaron 15 g de almidón (nativo, hidrolizado, lipofilizado), y se mezclaron manualmente en un vaso de precipitado con ayuda de una varilla de vidrio en seco con 3,2 g de aceite esencial disueltos en 3,2 g de aceite mineral, dejando en reposo por 24 horas en un frasco de cierre hermético. Al cabo de este tiempo, se añadieron 50 mL de agua desionizada, y la mezcla resultante se sometió a emulsificación con ayuda de un homogenizador ultra turrax IKA T10 a 5.000 rpm por 10 minutos. El producto obtenido se almacenó emulsionado en frascos herméticos y así se empleó.
Eficiencia de la encapsulación
Para evaluar la eficiencia de la encapsulación se empleó un equipo de hidrodestilación tipo Clevenger, en el que se pusieron 20 g de emulsión de microencápsulas en 300 mL de agua desionizada en un balón de 500 mL. Después de destila por 3 horas, se cuantificó el aceite esencial obtenido, el cual corresponde a un porcentaje de material inicial [20].
Análisis de composición del aceite esencial
La composición del aceite esencial de tomillo se analizó mediante técnica instrumental de gromatografía de gases acoplada a espectrometría de masa (GC/MS), en un equipo GC/MS 7890A/5975C Agilent (USA), en interfase con un detector selectivo de masas HP5973 Network conectado en línea con un sistema HP-MS ChemStation y la base de datos NIST-2008. Condiciones: como muestra se tomaron 50 µL de cada aceite esencial que se disolvieron en 450 µL de diclorometano, inyectándose 1,0 µL a modo split (20:1), la temperatura inyector fue de 250 °C, se utilizó una columna capilar HP-5MS 5% Phenyl Methyl Silox (30 m à 250 µm à 0,25 µm), utilizándose helio (Aga-Fano) como gas de arrastre, a flujo constante de 1 mL/min, presión del gas 7,6354 psi y velocidad lineal de 36 cm/seg. La temperatura inicial fue de 45 °C y la temperatura de la línea de transferencia de 280 °C [21, 22]. La identidad de los componentes se asignó por comparación de los espectros de masas obtenidos con los presentes en la base de datos.
Actividad antibacteriana in vitro
La actividad antibacteriana del aceite esencial de tomillo microencapsulado en el almidón lipofilizado de ñame, se realizó de la manera que se describe a continuación.
Cepas de S. aureus, S. epidermidis y P. acnes se inocularon en caldos MH, LB, TSA, respectivamente, de acuerdo con las indicaciones establecidas por la CLSI [23], tomando entre 3 y 4 colonias bien diferenciadas y morfológicamente similares de las bacterias previamente sembradas en placas de Petri con agares homólogos, incubándose a 35 ± 2 °C y verificando sistemáticamente la densidad óptica a 620 nm (DO620) en lector de microplacas (Multiscan EX Thermo®, USA), hasta que la suspensión bacteriana alcanzara una DO620 entre 0,08 y 0,1 equivalente a 0,5 en la escala de McFarland (1 à 108 UFC/mL) [24]. Una vez alcanzado este valor, 5 mL de caldo se mezclaron con 5 mL de emulsión de microcápsulas empleando un agitador Vórtex, en tubos de ensayo microbiológico con tapa estériles, dejándose en incubación por 24 horas a 35 ± 2 °C en agitación constante. Finalizado este tiempo, y para evaluar la capacidad bactericida de las microcápsulas, asadas tomadas de los tubos se sembraron en los agares específicos para las tres cepas y nuevamente se incubaron a las mismas condiciones por 24 horas.
Análisis estadístico
Los resultados obtenidos para cada uno de los almidones bajo estudio, fueron recolectados y comparados mediante evaluación estadística según los comportamientos observados para materiales de referencia tales como el almidón de maíz. Todos los ensayos se realizaron por triplicado siguiendo los protocolos establecidos anteriormente. El análisis estadístico se realizó comprobando los supuestos de normalidad de datos para el empleo de modelos paramétricos (distribución normal, igualdad de varianza e independencia de datos). El análisis estadístico se orientó a comparar los valores de medios de los resultados obtenidos. Los resultados obtenidos fueron sometidos a análisis de varianza ANOVA, seguido de la prueba de Dunnet para determinación de diferencias significativas. Los datos se ordenaron empleando el programa MS Excel 365, y los análisis estadísticos se hicieron con el paquete GraphPad Prisma V 5.0.
Resultados y discusión
Los ensayos se realizaron sobre almidones nativos y modificados de ñame (D. rotundata). Se emplearon almidones homólogos de maíz USP (Z. mays), como referencia.
La tabla 1 presenta los resultados de la caracterización básica de los almidones de ñame y maíz. El valor de pH para cada uno se encontró dentro de los límites esperados de 5,5 a 7,5 [25]. De igual manera, tanto el tamaño de partícula como el contenido de amilosa se corresponden con los valores reportados por la literatura [2, 12, 26, 27]. La figura 1 presenta una imagen de los amiloplastos de ñame con la forma en que se hicieron las medidas.

Una micropartícula lipídica sólida se asimila a una emulsión del tipo agua en aceite, excepto que la parte lipídica se mantiene sólida [28]. La microencapsulación de aceites esenciales empleando almidones, utiliza los amiloplastos como microcontenedores, ajustándose a esta definición. El objetivo, por tanto, es "rellenar" los amiloplastos individuales con aceite esencial en una matriz sólida, para lo que se necesitan dos cosas: incrementar la lipofilicidad y conservar la integridad del amiloplasto para que retenga al aceite. Numerosos estudios se centran hoy en la preparación de este tipo de micropartículas para vehiculizar y proteger los AA. EE. [29-33].
La lipofilización de los almidones para hacerlos más afines a los aceites esenciales se puede lograr de varias maneras. La primera, es realizando una hidrólisis ácida parcial del almidón. Zambrano y Camargo [15] optimizaron las condiciones de dicha hidrólisis sobre almidón de yuca (Manihot esculenta), como sustituto de grasas en alimentos procesados. Consecuencia de la hidrólisis, ocurre un incremento en la lipofilicidad del material resultante, junto con una disminución significativa de la viscosidad de sus dispersiones. La segunda, consiste en introducir grupos lipofílicos a las cadenas poliméricas del almidón. Una forma de hacerlo, es mediante reacciones de sustitución con anhídridos orgánicos de cadenas carbonadas largas. En este trabajo se empleó anhídrido dodecenil succínico, el cual tiene una cadena de doce carbonos. La tabla 2 presenta los porcentajes de sustitución alcanzados a los dos niveles de cantidad de reactivo empleado. En todos los casos se utilizaron almidones hidrolizados. Almidones nativos no se sustituyeron debido a que sus dispersiones son muy viscosas.

Como consecuencia de la hidrólisis y la sustitución lipofílica, los almidones presentaron cambios en la capacidad captadora de aceite, cuyos valores se presentan en la figura 2. Es notable para ambos almidones, que en la medida que se hidroliza y sustituye con DDSA, la lipofilicidad aumenta, llegando a duplicarse con la mayor sustitución.
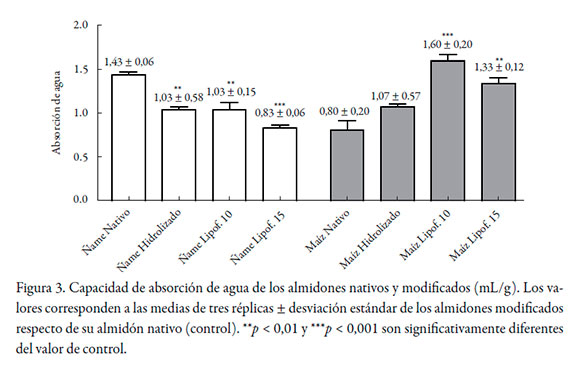
Un comportamiento un poco más errático se verifica con la capacidad de captación de agua (véase figura 3). El ñame tiende a reducir esta capacidad a medida que se lipofiliza, en tanto que en el maíz, con la hidrólisis y primera sustitución, esta se aumenta, mientras que con la segunda sustitución se disminuye. Esto puede deberse al hecho de que con las primeras modificaciones ocurre una desorganización de las cadenas poliméricas, lo que permite una mayor entrada de agua al amiloplasto. Con el segundo nivel de sustitución, este se hace más hidrorrepelente y, por tanto, su capacidad de captar agua disminuye. Por tener un tamaño de partícula más pequeño que el ñame, la desorganización de las cadenas es más probable.
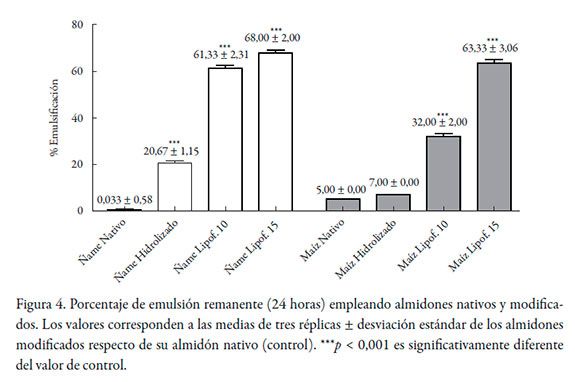
Los almidones son anfifílicos en su estado natural (nativo), pero con una pobre capacidad emulsificante, pues su actividad tensoactiva es muy limitada; no obstante, como se observa en la figura 4, en la medida que los almidones se sustituyen con cadenas carbonadas largas, la capacidad tensoactiva, y por tanto emulsificante, se incrementa [28, 29, 34]. El balance hidrofílico-lipofílico (HLB) de los almidones obtenidos probablemente tienda a ser bajo, puesto que las emulsiones que se forman en el ensayo de capacidad emulsificante fueron del tipo agua en aceite (W/O).
Para la encapsulación del aceite esencial de tomillo, se escogió el almidón de ñame hidrolizado/lipofilizado, que mostró la mayor capacidad tanto lipofílica como emulsificante.
La absorción del aceite esencial en la matriz lipofílica rinde un material de aspecto seco, que se embebe fácilmente sin ser grasoso al tacto. El propósito de suspender/emulsificar estas partículas, se orienta la formación de una cubierta acuosa alrededor de las mismas, que por hidrorrepelencia, ayude a mantener al aceite esencial dentro de las microcápsulas de almidón modificado, que como se indicó previamente, corresponden a los amiloplastos nativos originales. La emulsión obtenida, correspondió a una de tipo aceite en agua (O/W), sin sensación grasosa y de fácil lavado, lo que permite concluir que al incrementar la proporción de agua en la emulsión mediada por estos almidones lipofílicos, ocurre una inversión de fases.
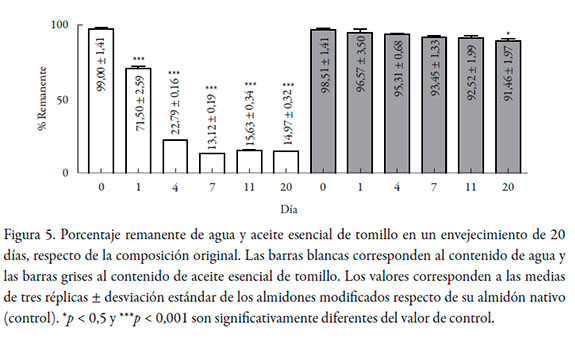
Para evaluar la capacidad de las microcápsulas de retener el aceite esencial, se tomaron 10 cuerpos de cajas de Petri, donde se vertieron 20 mL de emulsión, que se dejaron expuestas al ambiente (temperatura 25 ± 2 °C, HR 60%) durante 20 días, evaluando por triplicado de manera seriada. La figura 5 presenta los resultados. El día cero, corresponde a la composición inicial de la preparación, donde se pone de manifiesto que la eficiencia de la encapsulación es mayor del 98,5%. Al día 4, se ha perdido cerca del 77% del agua, pero apenas un 3,2% de aceite esencial. Para el día 20, hay un remanente del 15% de humedad, y más del 91% de aceite, es decir, una pérdida del 7%. Estos resultados ponen de manifiesto la eficiencia del sistema de retener el componente volátil bajo las condiciones extremas de libre evaporación.
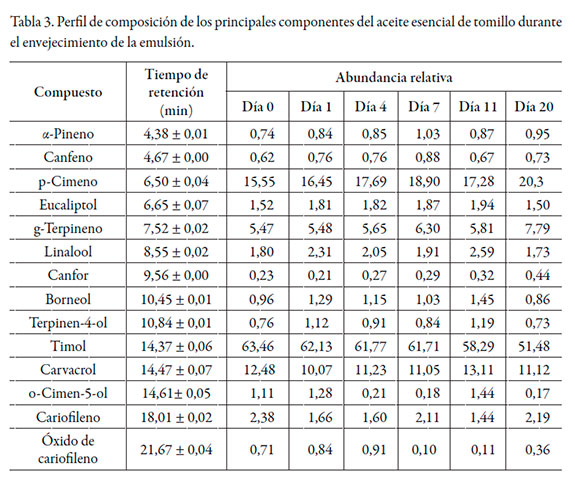
Dado que los objetivos de la microencapsulación de los aceites esenciales no es solo retenerlos sino también mantener su composición invariable, evitando oxidaciones, polimerizaciones y otras reacciones degradativas, se realizaron análisis de cromatografía GM a los destilados anteriores. Los perfiles de composición durante el envejecimiento se presentan en la tabla 3. De los principales componentes, se destaca que el timol se reduce en un 10%, en tanto que el carvacrol lo hace en un 1%, que es consistente con la pérdida global del 7% de aceite, y no se evidencia la aparición de nuevas especies químicas, lo que significa que hubo una pequeña pérdida de material, pero no se evidenció deterioro de los componentes constitutivos.
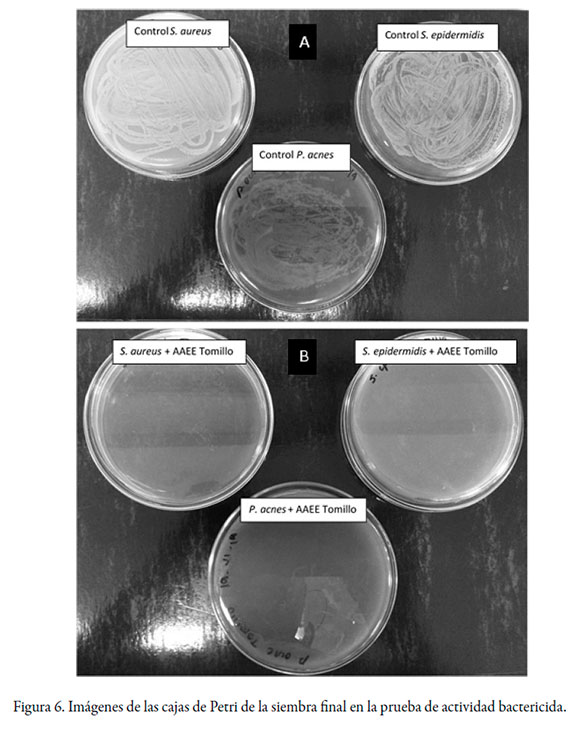
El aceite esencial de tomillo (T. vulgaris), ha demostrado ser muy promisorio para el tratamiento del acné, gracias a sus propiedades antibacterianas sobre las cepas vinculadas a la fase infectiva del mismo (P. acnes, S. epidermidis, S. aureus) [29, 30, 35]; por tal razón, fue elegido como aceite modelo. Para probar si sus propiedades bactericidas se mantenían aún después de encapsulado, se evaluó la emulsión del mismo frente a las cepas de acuerdo con la metodología descrita. En el modelo empleado, se evidenció que por efecto de la dilución, la emulsión deja de ser propiamente líquida, las microcápsulas quedan en suspensión, de allí la necesidad de la agitación constante.
La figura 6 corresponde a las imágenes de las cajas de Petri donde se sembraron asadas de la mezcla de cepas con la emulsión del aceite microencapsulado. La parte A de la figura corresponde al control, y la parte B al ensayo con aceite. Se evidencia que no hubo ningún crecimiento, y que por tanto, el aceite esencial se liberó suficientemente, para ser eficaz frente al crecimiento de las bacterias.
Conclusiones
La hidrólisis y posterior lipofilización del almidón de ñame (D. rotundata), permite la microencapsulación de aceite esencial de tomillo (T. vulgaris) con una eficiencia mayor al 98%, en donde el amiloplasto nativo original se constituye en un microrreservorio de este aceite. Su posterior emulsificación lo estabiliza y lo mantiene confinado, aislado del oxígeno y la luz, elementos importantes en la degradación de estos materiales. No obstante lo anterior, al ser aplicado en un sistema diluido, las microcápsulas se liberan de la emulsión y, a su vez, liberan el aceite, virtualmente intacto, que mantiene y ejerce sus actividades biológicas conocidas.
Agradecimientos
Los autores agradecen a Colciencias por el apoyo recibido para el desarrollo de este trabajo, por sus programas de apoyo a jóvenes investigadores e innovadores, y por la ayuda integral en el marco de la convocatoria 521 de 2010. Igualmente, a la Universidad de Cartagena y la Universidad Nacional de Colombia sede Bogotá, por facilitar espacio, recursos y tiempo de los investigadores.
Referencias
1. C. Turek, F.C. Stintzing, Impact of different storage conditions on the quality of selected essential oils, Food Research International, 46(1), 341-353 (2012). [ Links ]
2. R. Acosta, El cultivo del maíz, su origen y clasificación. El maíz en Cuba, Cultivos tropicales, 30(2), 113-120 (2009). [ Links ]
3. R.V. de Barros Fernandes, S.V. Borges, D.A. Botrel, Gum arabic/starch/maltodextrin/inulin as wall materials on the microencapsulation of rosemary essential oil, Carbohydrate polymers, 101, 524-532 (2014). [ Links ]
4. C. Dima, M. Cotârlet, P. Alexe, S. Dima, Microencapsulation of essential oil of pimento [Pimenta dioica (L) Merr.] by chitosan/k-carrageenan complex coacervation method, Innovative Food Science & Emerging Technologies, 22, 203-211 (2014). [ Links ]
5. E.A. Soliman, A.Y. El-Moghazy, M.M. El-Din, M.A. Massoud, Microencapsulation of essential oils within alginate: Formulation and in vitro evaluation of antifungal activity, Journal of Encapsulation and Adsorption Sciences, 3(1), 48-55 (2013). [ Links ]
6. J.E. Camacho, L.F. Villamizar, M.I. Gómez, Selección de un sistema de atomización para la formación de micropartículas de Eudragit® S100 en lecho fluido, Nova, 8(13), 87-100 (2010). [ Links ]
7. G. Matiz, M. Osorio, G. León, Lipofilización de almidones nativos como posibles agentes emulsificantes en cosméticos, Arte y Ciencia Cosmética, 56, 25-39 (2013). [ Links ]
8. Y. Yeo, N. Baek, K. Park, Microencapsulation methods for delivery of protein drugs, Biotechnology and Bioprocess Engineering, 6(4), 213-230 (2001). [ Links ]
9. M. Lopretti, F. Barriero, I. Fernandes, A. Damboriarena, C. Ottati, A. Olivera, Microencapsulación de compuestos de actividad biológica, INNOTEC, 2(2), 19-23 (2007). [ Links ]
10. J. Aristizábal, T. Sánchez, D. Mejía Lorío, "Guía técnica para producción y análisis de almidón de yuca", Boletín de Servicios Agrícolas 163, FAO Editor, Roma, 2007. [ Links ]
11. R. Hoover, W. Ratnayake, Determination of total amylose content of starch, Current protocols in food analytical chemistry, E2.3.1-E2.3.5 (2001). [ Links ]
12. C.R.V. Tovar, El ñame espino (Dioscorea rotundata Poir.): una opción en la producción de jarabes edulcorantes intermedios para la industria alimentaria, Agraria y Ambiental, 2(1), 19-28 (2010). [ Links ]
13. USP36. The United States Pharmacopeial Convention. Rockville, 2012. [ Links ]
14. P. Sinko, "Martin's Physical pharmacy and pharmaceutical sciences", Lippincott, Williams and Wilkinson, Baltimore, 2006. [ Links ]
15. F. Zambrano, C. Camargo, Otimização das condições de hidrólise ácida de amido de mandioca para obtenção de substituto de gordura, Brazilian Journal of Food Technology, 4, 147-154 (2001). [ Links ]
16. Y. Jeon, A. Lowell, R. Gross, Studies of starch esterification: Reactions with alkenylsuccinates in aqueous slurry systems, Starch - Stärke, 51(2-3), 90-93 (1999). [ Links ]
17. L. Bello, S. Contreras, R. Romero, J. Solorza, A. Jiménez, Propiedades químicas y funcionales del almidón modificado de plátano Musa paradisiaca L. (var. Macho), Agrociencia, 36(2), 169-180 (2002). [ Links ]
18. S. Chaparro, J. Gil, I. Aristizábal, Efecto de la hidratación y la cocción en las propiedades físicas y funcionales de la harina de vitabosa (Mucuna deeringiana), Vitae, 18(2), 133-143 (2011). [ Links ]
19. M. Granito, M. Guerra, A. Torres, J. Guinand, Efecto del procesamiento sobre las propiedades funcionales de Vigna sinensis, Interciencia, 29(9), 521-526 (2004). [ Links ]
20. B. Murúa, C. Beristain, F. Martínez, Preparation of starch derivatives using reactive extrusion and evaluation of modified starches as shell materials for encapsulation of flavoring agents by spray drying, Journal of Food Engineering, 91(3), 380-386 (2009). [ Links ]
21. S. Baharum, M. Bunawan, M. Ghani, W. Mustapha, N. Noor, Analysis of the chemical composition of the essential oil of Polygonum minus Huds. using twodimensional gas chromatography-time-of-flight mass spectrometry (GC-TOF MS), Molecules, 15(10), 7006-7015 (2010). [ Links ]
22. G.T. Tomy, G.A. Stern, D.C. Muir, A.T. Fisk, C.D. Cymbalisty, J.B. Westmore, Quantifying C10-C13 polychloroalkanes in environmental samples by highresolution gas chromatography/electron capture negative ion high-resolution mass spectrometry, Analytical Chemistry, 69(14), 2762-2771 (1997). [ Links ]
23. CLSI. "Normas para realizar las pruebas de sensibilidad a los antimicrobianos con discos". Pennysylavania: Clinical and Laboratory Standards Institute, 2009. [ Links ]
24. S. Sutton, Measurement of cell concentration in suspension by optical density, Pharmaceutical Microbiology Forum Newsletter, 12(8), 3-13 (2006). [ Links ]
25. A.M. Rincón, B. Rached, L.E. Aragoza, F. Padilla, Efecto de la acetilación y oxidación sobre algunas propiedades del almidón de semillas de fruto de pan (Artocarpus altilis), Archivos Latinoamericanos de Nutrición, 57(3), 287-294 (2007). [ Links ]
26. D. Kuakpetoon, Y.-J. Wang, Structural characteristics and physicochemical properties of oxidized corn starches varying in amylose content, Carbohydrate Research, 341(11), 1896-1915 (2006). [ Links ]
27. V. González, E. María, El ñame (Dioscorea spp.). Características, usos y valor medicinal. Aspectos de importancia en el desarrollo de su cultivo, Cultivos Tropicales, 33(4), 5-15 (2012). [ Links ]
28. P. Ekambaram, A.A.H. Sathali, K. Priyanka, Solid lipid nanoparticles: A review, Scientific Reviews and Chemical Communications, 2(1), 80-102 (2012). [ Links ]
29. D.F. Cortés-Rojas, C.R. Souza, W.P. Oliveira, Encapsulation of eugenol rich clove extract in solid lipid carriers, Journal of Food Engineering, 127, 34-42 (2014). [ Links ]
30. R.V. de Barros Fernandes, G.R. Marques, S.V. Borges, D.A. Botrel, Effect of solids content and oil load on the microencapsulation process of rosemary essential oil, Industrial Crops and Products, 58, 173-181 (2014). [ Links ]
31. F. Donsì, M. Annunziata, M. Sessa, G. Ferrari, Nanoencapsulation of essential oils to enhance their antimicrobial activity in foods, LWT-Food Science and Technology, 44(9), 1908-1914 (2011). [ Links ]
32. E. Frascareli, V. Silva, R. Tonon, M. Hubinger, Effect of process conditions on the microencapsulation of coffee oil by spray drying, Food and Bioproducts Processing, 90(3), 413-424 (2012). [ Links ]
33. V. Silva, G. Vieira, M. Hubinger, Influence of different combinations of wall materials and homogenisation pressure on the microencapsulation of green coffee oil by spray drying, Food Research International, 61, 132-143 (2014). [ Links ]
34. C. Bernal, A. Leal, J. Garzón, Obtención a escala laboratorio del octenilsuccinato alumínico de almidón de quinua con miras a su utilización en un producto cosmético, Virtual Pro, 95, 16-32 (2009).
35. G. Matiz, M. Osorio, G. León, Actividad antibacteriana in vitro de diecinueve aceites esenciales frente a bacterias asociadas al acné, Revista Cubana de Farmacia, 49(1), en prensa (2015).













