Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista de la Facultad de Medicina
Print version ISSN 0120-0011
rev.fac.med. vol.53 no.1 Bogotá Jan. 2005
ACTUALIZACIÓN ELECTROFISIOLOGÍA
Guillermo Mora Pabón1
1.Profesor Asociado, Especialista en Medicina Interna (Cardiología y electrofisiología), Facultad de Medicina, Universidad Nacional de Colombia Bogotá.
Correspondenciagmorap@unal.edu.co
Resumen
La terapia eléctrica en cardiología está encaminada a transferir electrones al miocardio, su mayor utilidad está dada en la cardioversión y desfibrilación. La terapia eléctrica cumple las leyes de la electricidad y el mayor factor a vencer es la impedancia o resistencia al flujo de electrones. Para mejorar la efectividad de la terapia eléctrica se han ideado diferentes formas en la onda de choque, en la duración y la polaridad. La terapia eléctrica ha logrado consolidarse como el tratamiento de elección del paro cardiorrespiratorio secundario a fibrilación ventricular y taquicardia ventricular sin pulso.
Es igualmente el tratamiento de elección en taquiarritmias con compromiso hemodinámico. Pese a sus grandes ventajas tiene efectos secundarios que se deben conocer adecuadamente para dar un tratamiento oportuno.
Palabras clave: electrones, conductividad eléctrica, estimulación eléctrica, energía eléctrica, electro shock, paro cardíaco, fibrilación ventricular, taquicardia ventricular.
Summary
Electrical shock in cardiology are pursuid transfer of electrons to the myocardium. Its main indications are`s cardioversion and defibrillation.
The electrical shock therapy follows laws of electricity laws and consequently, its main difficulty is the impedance or resistance of electrons flow. To make better the effectiveness of this therapy, a number of improvements have been made on the shock wave, its duration, and polarity. The electric shock therapy has become the preferred treatment when dealing with cardiorespiratory arrest secondary, ventricular fibrillation and pulseless ventricular tachycardia. Similarly, it is the preferred treatment for ventricular tachyarrhythmia associated with hemodynamic compromise. Despite its significant advantages, this treatment causes secondary effects, which should adequately be known in order to provide a timely treatment.
Key words: electrons, electric conductivity, electric stimulation, electricity, electroshock, heart arrest, ventricular fibrillation, tachycardia, ventricular.
Terapia eléctrica en cardiología
Los fenómenos eléctricos se caracterizan por el flujo de electrones a través de un medio conductor. Entre las múltiples aplicaciones de estos fenómenos a la salud una de las más importantes es la terapia eléctrica. En este grupo se incluyen aquellas modalidades que transfieren electrones al cuerpo y que desde el punto de vista cardiovascular son: el marcapaso cardíaco, la cardioversión y la desfibrilación. En el presente artículo revisaremos los conceptos básicos, indicaciones y complicaciones de los últimos dos tipos de terapia eléctrica.
Historia
Es posible que la relación del hombre con la electricidad se haya iniciado en épocas prehistóricas al conocer los rayos y tener contacto con animales tales como el pez gato eléctrico (Malapterurus electricus) y la raya eléctrica (Torpedo mamorata). Sin embargo sólo hasta el siglo XVIII, gracias a la invención de Germán Otto von Gueike, se produjo la primera máquina eléctrica (1). En 1791 Galvani publicó Die Vivibus Electricitates in Motu Commentarius, en esta monografía describió la relación de corriente eléctrica y contracción muscular a través de los nervios en un espécimen de rana (2).
Esta es la primera descripción de la relación de fisiología y electricidad. Pese a ello sólo hasta la segunda guerra mundial Léneyre y Mamice describieron la actividad eléctrica en las cámaras cardíacas (3).
La utilidad de la terapia eléctrica en reanimación puede remontarse a 1796 cuando Richard Fowler le aplicó corriente galvánica al vago y al simpático en el corazón de una rana, en asistolia, y produjo una contracción normal (4). Los intentos por aplicar electricidad para reanimación en humanos no tardaron e incluso se idearon aparatos relativamente pequeños para reanimación (5). En l872 T. Green reportó seis sobrevidas de paro cardiorrespiratorio en pacientes anestesiados con cloroformo con corriente proveniente de baterías galvánicas (6). Pese a este éxito dado que el conocimiento de la fibrilación ventricular (FV) era precario solo hasta 1886 John McWilliam describió sus efectos hemodinámicos y sus características clínicas (7).
Igualmente describió como un choque eléctrico podía revertirla (8). Su experiencia fue demostrada en mamíferos y en humanos (9).
A principios del siglo XX se hacieron aportes valiosos a la terapia eléctrica al confirmar que el choque eléctrico revertía la FV, al desarrollar aparatos de desfibrilación e introducir las técnicas de masaje cardíaco externo (10).
Beck y col (11) se encargaron de extender la utilidad de la desfibrilación en el mundo acuñando la famosa frase "corazones demasiado buenos para morir", con la cual hacían referencia a pacientes con corazones con adecuada función ventricular izquierda que podían desarrollar fibrilación ventricular y muerte súbita. Una vez establecida la desfibrilación como una herramienta terapéutica útil, el siguiente mayor avance fue el desarrollo del cardiodesfibrilador implantado, trabajo hecho gracias a la tenacidad de Michael Mirowsky (12). Los avances tecnológicos con la aparición de los cardiodesfibriladores implantados han hecho cada vez más efectiva la desfibrilación.
Principios básicos
La terapia eléctrica se rige por las leyes de la electricidad. En primer término daremos algunas definiciones:
Corriente: volumen de flujo de electrones Amperios-(A)
Voltaje: fuerza que mueve la corriente Voltios-(V)
Carga: cantidad de electrones por tiempo Coulumbos-(Col)
Energía: voltaje por carga Julios-(J) Impedancia: Resistencia al flujo Ohmios-(Ohm)
La ley básica de la electricidad es la ley de Ohm

De esta forma el flujo de electrones es directamente proporcional al voltaje e inversamente proporcional a la resistencia al flujo (13).
Mecanismo de acción
El mecanismo por el cual la desfibrilación termina la fibrilación ventricular no está totalmente aclarado y se han desarrollado tres hipótesis para explicarlo.
Teoría de la masa crítica. Esta teoría propone que el choque necesita sólo eliminar ondas fibrilatorias en una cantidad crítica de miocardio para que la arritmia se extinga. Una forma de demostrarla es que la desfibrilación es más exitosa, en modelos experimentales en perros, si los electrodos están en el ápex del ventrículo derecho y la pared posterior del ventrículo izquierdo, que si se colocan sólo en el ventrículo derecho (14).
Teoría del límite superior de vulnerabilidad. Un hallazgo importante ha sido que, en algunos experimentos el choque eléctrico termina la FV pero luego de una pausa eléctrica se reinicia la arritmia; se ha creído que es el mismo choque eléctrico el que reinduce la fibrilación ventricular (15). Los experimentos demostraron que la FV se reiniciaba en zonas diferentes a donde terminaba con el choque, en sitios de más baja intensidad de corriente.
Nuevos estudios demostraron que choques con un gradiente de potencial menor que un mínimo valor crítico, llamado límite superior de vulnerabilidad (6 V/cm para choques monofásicos o 4 V/cm para choques bifásicos) podrían inducir FV en el miocardio durante su período vulnerable (16).
Choques de baja energía sobre la onda T inducen FV, mientras que choques por encima del límite superior de vulnerabilidad no lo hacen. Así que choques por encima del límite superior de vulnerabilidad cruzarán el miocardio sin reinducir FV y terminarán el evento (17).
Teoría de la despolarización progresiva. Es también conocida como teoría de la extensión del período refractario. Un estudio encontró que si se aplican choques de suficiente intensidad se pueden despolarizar fibras miocárdicas aún en período refractario absoluto, de manera tal que se prolonga la duración del potencial de acción y se extiende el período refractario (18). Como el choque abre canales de sodio en el miocardio en repolarización y también en despolarización, induce resincronización eléctrica miocárdica. Al sincronizar la despolarización también lo hace en la repolarización de manera tal que no hay miocardio excitable para sostener la FV.
Características de la onda de choque
La eficacia de la onda de choque de desfibrilación es dependiente de varios factores como duración, inclinación, polaridad, número de fases y tiempo de desfibrilación.
Duración de la onda. La cantidad de electrones (corriente) que cruzan el miocardio depende de la fuerza (voltios) y de la duración del impulso.
Los pulsos monofásicos (Figura1) requieren más corriente para desfibrilar a corta duración que a larga duración (19). Cuando la segunda fase de una onda bifásica (Figura 2) se mantiene constante, la primera fase genera una curva fuerzaduración semejante a la de la onda monofásica (20). En cardiodesfibriladores implantados de gran tamaño la desfibrilación es más exitosa si la duración de la segunda fase es igual o más corta que la duración de la primera fase (21).
En la medida que el tamaño del cardiodesfibrilador ha disminuido se necesita, para que la desfibrilación sea exitosa, que la segunda fase sea más larga que la primera (22). Si la duración del choque es muy larga se produce una "cola" de bajo voltaje que puede inducir refibrilación, por ello las ondas usadas clínicamente se truncan con lo que súbitamente desaparece el flujo de electrones (por ejemplo ondas monofásicas rectangulares truncadas) para disminuir el bajo voltaje final (23).
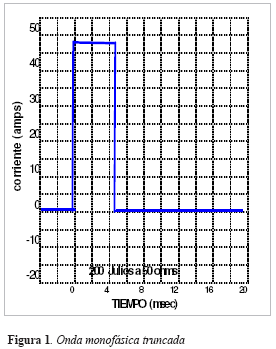
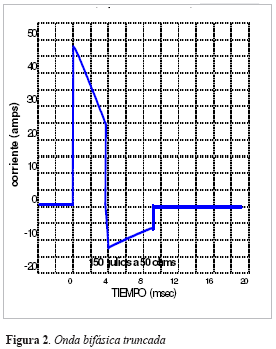
Inclinación de la onda. La inclinación de la onda es la expresión del porcentaje de caída del voltaje inicial. Es función del tamaño del capacitor usado, de la resistencia al flujo de corriente y de la duración del pulso.
% inclinación = (V inicial-V final)/V inicial x 100% (24)
Los desfibriladores monofásicos o bifásicos tienen fija la inclinación de la onda o la duración de ella. En sistemas con inclinación fija la duración de la onda cambiará dependiendo de la impedancia del choque. Para los equipos de duración fija la inclinación de la onda dependerá de la impedancia del choque, de manera tal que a alta impedancia la inclinación es pequeña y viceversa (25).
Para las ondas monofásicas la inclinación ideal es de 50-80% (24), para las ondas bifásicas con igual inclinación de la primera y segunda fase la inclinación ideal es de 40-65% (22,26,27).
Polaridad de la onda. En general la desfibrilación es más exitosa si el electrodo sobre el ápex del ventrículo derecho es el ánodo (28), sobretodo en ondas monofásicas. Con ondas bifásicas los resultados son menos uniformes (29-31) sin embargo todos los estudios encontraron que en la primera fase el ánodo debe ser el ventrículo derecho.
Número de fases. Las ondas bifásicas han demostrado ser mejores, para producir adecuada desfibrilación, que las ondas monofásicas y además requieren menos energía (27). Un estudio con 115 pacientes demostró que desfibrilar con ondas bifásicas exponenciales truncadas de 150 J era mejor que dosis escaladas de ondas monofásicas (200, 300 y 360 J). El éxito del grupo de ondas bifásicas fue de 98%, mientras que para ondas monofásicas fue de 69% (32). Igualmente fue mayor el grupo que alcanzó circulación espontánea (76% vs 54% p = 0.01) y tenían mejor rendimiento cerebral. En la cardioversión las ondas bifásicas son igualmente más efectivas, en un estudio reciente el éxito en cardioversión de fibrilación auricular fue de 97% con choques de 360 J con ondas bifásicas exponenciales truncadas, mientras que las ondas monofásicas tenían éxito del 90% (33). En el desfibrilador bifásico la onda rectilínea utiliza menos energía que la exponencial truncada. Los desfibriladores que usan ondas rectilíneas tienensal idas máximas de 200 J, mientras que los que usan ondas exponenciales truncada tienen salidas máximas de 360 J. En la actualidad muchos de los desfibriladores externos bifásicos ajustan la duración de las ondas de acuerdo a la impedancia transtorácica del paciente con lo cual mejoran la eficacia y la seguridad.
La causa del mayor éxito de las ondas bifásicas no está totalmente aclarada, se ha postulado que la primera fase hiperpolariza el tejido cerca al ánodo reactivando canales de sodio inactivos y que esto facilita la excitación de la siguiente fase (34). Otra hipótesis es que la primera fase acorta el período refractario de la células miocárdicas facilitando el reclutamiento de canales de sodio por la segunda fase (35). Una última ventaja de la onda bifásica es que produce menor daño en los tejidos posiblemente porque al revertir la polarización durante el choque reorienta los daños de la membrana disminuyendo el efecto tóxico (36).
Tiempo. El tiempo desde el inicio de la FV y el momento de la descarga es uno de los factores primordiales en el éxito de la desfibrilación. Al realizar estudios electrofisiológicos se puede inducir FV si la desfibrilación ocurre a los pocos segundos se obtiene un éxito mayor al 99%. Sin embargo estos son pacientes que generalmente están estables y no representan necesariamente a aquellos que desarrollan muerte súbita en el ámbito clínico. Los pacientes a quienes se les implanta un cardiodesfibrilador son de alto riesgo para muerte súbita, en este grupo también la desfibrilación es muy exitosa ya sea para tratar FV o taquicardia ventricular y en ellos la descarga sucede a los pocos segundos del inicio de la arritmia. En la medida que el tiempo pasa hay deterioro celular electrofisiológico que incluye lentificación de la frecuencia de las ondas de despolarización de la FV debido a falla de la conducción y refractariedad posrepolarización (37). Igualmente se produce aumento de la resistencia tisular por desacople celular que es mediado por apertura de canales de potasio dependientes de ATP, sobrecarga de calcio y falla contráctil (38). Todos estos cambios, unidos a la isquemia global y la acidosis, hacen menos exitosa la desfibrilación.
Efectos deletéreos del choque eléctrico
Cerca del electrodo de desfibrilación se produce un alto gradiente de potencial que lleva a efectos deletéreos como bradicardia (39), bloqueo AV (40), bloqueo de conducción (41), taquiarritmias (42), fibrilación (43), necrosis (44) y muerte (25). Con gradientes mayores de 100 V/cm se producen latidos ectópicos que pueden reinducir fibrilación (41).
La desfibrilación produce necrosis miocárdica y hace el diagnóstico de infarto un poco más difícil. La nueva definición de infarto (45) da un importante valor al hallazgo de troponina positiva, haciendo de ella el patrón de oro para el diagnóstico clínico. No está totalmente aclarada la relación de aumento de troponina con desfibrilación pero parece que la cardioversión o desfibrilación no aumenta sus niveles (46,47).
Realización de la desfibrilación eléctrica
La terapia eléctrica tiene como objetivo llevar electrones desde el desfibrilador hasta el miocardio, así que el mayor problema a vencer es la impedancia o resistencia al flujo de estos electrones. Los factores que afectan la impedancia transtorácica son: nivel de energía seleccionada, tamaño de las palas de desfibrilación, material de acople piel-palas (gel conductor), choques previos, fase de la ventilación, distancia entre electrodos (tamaño del tórax) y presión sobre las palas (48-50). La principal fuente de aumento de la impedancia es el aire, por lo que no se puede desfibrilar sin poner en contacto las palas con el paciente. Para disminuir la impedancia el operador debe presionar firmemente las palas sobre el tórax y usar gel o solución salina. Es importante tener en cuenta que no debe haber contacto entre el gel de cada una de las palas ya que los electrones pasarían por la pared del tórax y no por el miocardio. En los hombres con abundante vello torácico se debe rasurar la zona donde se colocarán las palas, ya que entre los vellos se atrapa aire y esto aumenta la impedancia.
La posición de las palas en el tórax está establecida, una se coloca en región subclavia derecha (marcada en la pala como esternón) y la otra en la región medio axilar izquierda a la altura del ápex cardíaco (marcada como ápex). Cuando el paciente tiene un marcapaso o un cardiodesfibrilador implantado, las palas deben quedar al menos a 12 cm del dispositivo y una vez recuperado el paciente se debe revisar el adecuado funcionamiento de estos aparatos (51). Tomadas las medidas para disminuir la impedancia, se debe elegir cual será la energía del choque.
Las dos indicaciones de desfibrilación son la FV y la taquicardia ventricular sin pulso (52), en estos casos la dosis inicial será 200 J en los desfibriladores monofásicos (los más comúnmente encontrados en las salas de urgencias de nuestro hospitales) (53). Si no hay mejoría del ritmo inicial se usará una segunda dosis, esta dosis será más efectiva ya que hay disminución de la impedancia, siempre y cuando no se retiren las palas del tórax, y por ello se reco mienda entre 200 y 300 J (49,52). Si el ritmo de FV o TV sin pulso persiste se realiza una tercera descarga de 360 J, nuevamente sin retirar las palas del tórax entre cada descarga.
Si la FV o la TV sin pulso revertió y recurre se usará como carga inicial la última que haya sido efectiva. Si el paciente persiste en FV o TV sin pulso se iniciaran otras medidas de reanimación como intubación orotraqueal, masaje cardíaco y uso de drogas vasoconstrictoras y antiarrítmicas, que pretenden sensibilizar al miocardio a nuevas desfibrilaciones. Para ello se debe seguir, durante el proceso de reanimación, la secuencia de droga - masaje - descarga, haciendo esta última a la dosis máxima de 360 J (52).
Los desfibriladores externos bifásicos tienen menor tiempo de uso, sin embargo es claro que a partir del éxito de los cardiodesfibriladores implantados, las ondas bifásicas son tan o más efectivas que las monofásicas. Un estudio encontró que choques bifásicos de 150 J eran tan efectivos como los monofásicos de 200 J (50), y sugiere que los choques repetitivos bifásicos (menores a 200 J) son tan efectivos como choques (200, 300 y 360 J) monofásicos (54).
Cardioversión
Durante la desfibrilación el choque eléctrico ocurrirá en cualquier fase del potencial de acción del miocardio y pretenderá la resincronización eléctrica. Sin embargo si tenemos una actividad eléctrica organizada (por ejemplo un flutter auricular) y el choque cae en el período refractario relativo (cerca al pico de la onda T) se puede generar FV (55). Para evitar ello se utiliza la cardioversión. En ella el desfibrilador externo sincroniza el choque con la R del QRS del ritmo del paciente.
La principal indicación de cardioversión eléctrica es la taquiarritmia, ya sea ventricular o supraventricular, con inestabilidad hemodinámica (52). Esta inestabilidad es definida por la presencia de hipotensión sintomática, choque, edema pulmonar o síndrome coronario agudo. Generalmente la taquiarritmia cursará con frecuencias cardíacas mayores a 150 latidos por minuto. Existe otra indicación de cardioversión eléctrica y es la necesidad de volver a ritmo sinusal un paciente estable que no lo ha logrado por otros métodos (52).
Para la realización de la cardioversión se deben tomar las mismas medidas para disminuir la impedancia transtorácica, que las tomadas para desfibrilar. La ubicación de las palas será igual (infraclavicular derecha y en ápex), aunque se han utilizado otras como anteroposterior (región precordial y en la zona infraescapular derecha o izquierda) o ápex infraescapular derecha (56), sin que alguna haya demostrado una clara superioridad sobre la convencional.
La cardioversión eléctrica es un proceso muy doloroso por lo que los pacientes sometidos a ella deben recibir adecuada analgesia y sedación (comúnmente con midazolam y fentanyl® o propofol®). Se debe realizar en un sitio con los implementos necesarios para reanimación cardiopulmonar avanzada, como intubación, acceso fácil a drogas como adrenalina, atropina, etc.
La dosis de energía depende de la taquiarritmia a tratar. En fibrilación auricular y en TV polimorfa la dosis inicial es de 200 J, en TV monoforma 100 J (57) y en otras taquiarritmias supraventriculares se inicia con 50 J (57,58).
Estas dosis iniciales son con choques con onda monofásica, no hay datos disponibles aún para ondas bifásicas.
Es importante recordar que los pacientes con fibrilación auricular o flutter auricular son de particular cuidado a la hora de cardiovertir por el riesgo de tromboembolismo (59). En el paciente hemodinámicamente inestable la cardioversión es una urgencia por lo que se debe realizar prontamente, pero el paciente debe recibir una dosis inicial de heparina de 120 UI/Kg (52). En los pacientes en los cuales la cardioversión no es una urgencia, y tienen más de 48 horas de la fibrilación o flutter auricular, se puede realizar ecocardiograma transesofágico y si no hay trombos en la aurícula izquierda iniciar heparina IV y cardiovertir (60). Si hay trombos se debe anticoagular por tres semanas con warfarina, manteniendo el INR entre 2-3, y luego cardiovertir. Si no hay disponibilidad de ecocardiograma transesofágico se anticoagula al paciente por tres semanas antes de la cardioversión (61). Es fundamental entender que una vez realizada la cardioversión el paciente sigue en riesgo de embolismo, ya que aunque se recupera eléctricamente el ritmo sinusal, la aurícula puede quedar aturdida y recuperar su adecuada contracción hasta cuatro semanas después por lo que al menos durante este tiempo debe continuarse la anticoagulación (62).
Procedimiento
Durante los cursos de reanimación cardiopulmonar avanzada realizados en el CEMU (Centro de Estudios de la Medicina de Urgencias) de la facultad de Medicina de la Universidad Nacional de Colombia, sugerimos a nuestros estudiantes el siguiente protocolo de actuación al momento de realizar la cardioversión o la desfibrilación:
Comprobar la seguridad del paciente y el reanimador, por lo cual el paciente no debe estar húmedo y no debe él ni el reanimador estar en contacto con superficies metálicas.
Aplicar el gel conductor a las palas del desfibrilador.
Encender el desfibrilador.
Elegir el nivel de energía
Cargar el acumulador
Colocar las palas en el tórax del paciente con presión firme pero sin apoyarse en ellas, para no resbalar, y comprobando que no hay contacto del gel conductor entre las palas.
Retirarse (el operador) de la camilla para no tener contacto con ella ni con el paciente.
Asegurar visualmente que no haya otras personas en contacto con el paciente o la camilla y avisar en voz alta que se va a realizar la descarga eléctrica.
Presionar los dos botones de descarga en forma simultánea verificando previamente en el monitor que persiste el ritmo eléctrico a tratar.
Complicaciones de la cardioversión
La cardioversión esta contraindicada en pacientes con intoxicación digitálica ya que puede producir arritmias ventriculares malignas; si es estrictamente necesaria se deben primero corregir estados hipocalémicos o hipomagnesémicos (63). Igualmente está absolutamente contraindicada en caso de FV ya que para que se produzca la descarga el aparato necesita detectar los QRS y si no lo hace, por ser muy pequeños como en FV, no se producirá el choque. En caso de FV el tratamiento es la desfibrilación.
Nuevas ondas
Experimentalmente se han empezado a evaluar los choques trifásicos, sin que hayan mostrado ventajas sobre los bifásicos en los estudios iniciales (64) aunque sí cuando las tres fases tienen la misma duración y se aplican energías bajas (menores a 65 J) (65).
Conclusiones
La terapia eléctrica ha adquirido un papel preponderante, desde su descubrimiento, en el manejo de pacientes en paro cardiorrespiratorio por FV o TV sin pulso o con taquiarritmias inestables. Su adecuado uso la hace una herramienta muy útil para todo médico, independiente de la especialidad que maneje. Con el advenimiento de los cardiodesfibriladores implantados ha surgido gran investigación en esta terapia haciéndola cada vez más segura y efectiva.
Referencias
1. Acierno L. The history of cardiology. Ed Roche. New York 1994; 239-64. [ Links ]
2. Galvani L. De viribus electricitatis in motu muscularicommentaries. De Bononienssi Scientarium et Artium Instituto atque Academia Commentarii 7, 363-418. [ Links ]
3. Lénegre J, Maurice P. De qualques resultats obtenus par la derivation directe intracavitaire des courants électriques de l'oreillette et du ventricule droit. Arch. Mal. Coeur 1945; 38: 298-302. [ Links ]
4. Fowler R. Experiments and observations relative to the influence lately discovered by Mr Galvani, and commonly called animal electricity. Bibl Br 1786; 11. (1). [ Links ]
5. Reece R. Medical Guide for the use of the clergy, heads of families, and junior practitioners in medicine and surgery. Herst and Co London, 1824. [ Links ]
6. Green T. On death from chloroform: its prevention by galvanism. Br Med J 1872 1: 551-3. [ Links ]
7. MacWilliam J. Fibriller condestion of the heart. J Physol 1887; 8; 296. [ Links ]
8. MacWilliam J. On electrical stimulation of the mammalian heart. Trans Int Med Congress, 9th session. Washington 1887 vol III p.253. [ Links ]
9. MacWilliam J. Electrical stimulation of the heart in man. Br Med J. 1889; 1:348. [ Links ]
10. Kouwenhoven WB. The development of the defibrillator. Ann Intern Med 1969 71: 449-58. [ Links ]
11. Beck CS, Patchard W, Feil HS. Ventricular fibrillation of long duration abolished by electric shock. JAMA 1947; 135: 985-8. [ Links ]
12. Mirowsky M, Mower M, Staewen M, et at. Standby automatic defibrillator an approach to prevention of sudden coronary death. Arch. Intern Med 1970; 126: 158-61. [ Links ]
13. Barold S, Stokes K, Byrd C, McVenes R. Energy parameters in cardiac pacing should be abandoned. PACE 1997; 20: 112-21. [ Links ]
14. Zipes DP, Fisher J, King RM, Nicoll A de B, Jolly W. Termination of ventricular fibrillation in dogs by depolarizing a critical amount of myocardium. Am J Cardiol 1975; 36: 37-44. [ Links ]
15. Chen PS, Shibata N, Dixon EG, et al. Activation during ventricular defibrillation in open-chest dogs. Evidence of complete cessation and regeneration of ventricular fibrillation after unsuccessful shocks. J Clin Invest 1986; 77: 810-23. [ Links ]
16. Frazier D, Wolf P, Wharton J, et al. Stimulus-induced critical point. Mechanism for electrical initiation of reentry in normal canine myocardium. J Clin Invest 1989; 83: 1039-52. [ Links ]
17. Chen PS, Feld GK, Kerett J, et al. Relation between upper limit of vulnerability and defibrillation threshold in humans. Circulation 1993; 88: 186-92. [ Links ]
18. Sweeney R, Gill R, Steinberg M, Reid P. Ventricular refractory period extension caused by defibrillation shocks. Circulation 1990; 82: 965-72. [ Links ]
19. Bourland J, Tacker W, Geddes L. Strength-duration curves for trapezoidal waveforms of various tilts for transchest defibrillation in animals. Med Instrum 1978; 12: 38-41. [ Links ]
20. Kroll M. A minimal model of the monophasic defibrillation pulse. PACE 1993; 16: 769-77. [ Links ]
21. Feeser SA, Tang A, Kavanagh K, et al. Strengthduration and probability of success curves for defibrillation with biphasic waveforms. Circulation 1990; 82:2128-41. [ Links ]
22. Swerdlow C, Kass R, Davie S, et al. Short biphasic pulses from 90 microfarad capacitors lower defibrillation threshold. PACE 1996; 19: 1053-60. [ Links ]
23. Schuder JC, Gold JH, Warwill M, Transthoracic ventricular defibrillation in the 100 Kg calf with untruncated and truncated exponential stimuli. IEEE Trans Biomed Eng 1980; 27: 37-43. [ Links ]
24. Lloyd M, Hayes D, Friedman P. Clinical relevants basics of pacing and defibrillation. In: Hayes F, Lloyd M, Friedman P. Cardiac Pacing and defibrillation: A Clinical Approach. Futura Publishing. Armonk NY 2000. 1-52. [ Links ]
25. White J, Ideker R. Roles of schock characteristics in successful ventricular defibrillation. In Zipes D, Jalife J. Cardiac electrophysiology from cell to bedside. Saunders Company. Philadelphia 1999. 440-6. [ Links ]
26. Shorofsky S. Effect of waveform tilt on defibrillation thresholds in humans J Cardiovasc Electrophysiol 1997; 8: 496-501. [ Links ]
27. Natale A, Sra J, Krum D, et al. Relative efficacy of different tilts with biphasic defibrillation in humans. PACE 1996; 19: 197-206. [ Links ]
28. Strickberger S, Hummel J Horwood L, et al. Effect of shock polarity on ventricular defibrillation threshold using a transvenous lead system. J Am Coll Cardiol 1994; 24: 1069-72. [ Links ]
29. Strickberger S, Man K, Daoud E, et al. Effect of first-phase polarity of biphasic shocks on defibrillation threshold with single transvenous lead system. J Am Coll Cardiol 1995; 25: 1605-8. [ Links ]
30. Natale A, Sra J, Dhata A, et al. Effects of initial polarity on defibrillation threshold with biphasic pulses. PACE 1995; 18: 1809-93. [ Links ]
31. Shorofsky S, Gold M. Effects of waveform and polarity on defibrillation thresholds in humans using transvenous leads system. Am J Cardiol 1996; 78: 313-6. [ Links ]
32. Schneider T, Martens P, Paschen H, et al. Multi- center randomized, controlled trial of 150 J biphasic shocks compared with 200 to 360 J monophasic shocks in the resuscitation of out-of-hospital cardiac arrest victims. Circulation 2000; 102: 1780-7. [ Links ]
33. Koster RW, Dorian P, Chapman FW, et al. A randomized trial comparing monophasic and biphasic waveform shocks for external cardioversión of atrial fibrillation. Am Heart J 2004; 147: e1-7. [ Links ]
34. Zhou X, Smith W, Justice R, Wayland J, Ideker R. Transmembrane potencial changes caused by monophasic and biphasic shocks. Am J Physiol 1998; 275: H 1798-1807. [ Links ]
35. Tang A, Yabe S, Wharton J, et al. Ventricular defibrillation using biphasic waveforms: the importance of phasic duration. J Am Coll Cardiol 1989; 13: 207-14. [ Links ]
36. Jones J, Jones R. Decreased defibrillation-induced dysfunction with biphasic rectangular waveforms Am J Physiol 1984; 247: H 792-6. [ Links ]
37. Tovar O, Noe W, Jones J, et al. At long fibrillation durations actino potencials are more frequent and fractionated in the right ventricle than in the left ventricle. PACE 1998; 21: 931. [ Links ]
38. Tovar O, Wang Y, Jones J. Deterioration of contractile function during the first five minutes of ischemic ventricular fibrillation. Circulation 1999; 100: I317. [ Links ]
39. Waldecker B, Brugada P, Zehender M, et al. Dysrhythmias after direct-current cardioversion. Am J Cardiol 1986; 57: 120-3. [ Links ]
40. Stoeckle H, Nellis SH, Schuder JC. Incidence of arrhythmias in the dog following transthoracic ventricular defibrillation with unidirectional rectangular stimuli. Circ Res 1968; 23: 343-8. [ Links ]
41. Yabe S, Smith W, Daubert J et al. Conduction disturbances caused by high current density electric fields. Circ Res 1990; 66: 1190-1203. [ Links ]
42. Peleska B. Cardiac arrhythmias following condenser discharges and their dependence upon strength of current and phase of cardiac cycle. Cir Res 1963; 13: 21-32. [ Links ]
43. Lesigne C, Levy B. Saumont R, et al. An energytime analysis of ventricular fibrillation and defibrillation thresholds with interval electrodes. Med Biol Eng 1976; 14: 617-22. [ Links ]
44. Dahl CF, Ewy GA, Warner E, Thomas E. Myocardial necrosis from direct current countershock: effect of paddle size and time interval between discharge. Circulation 1974; 50: 956-61. [ Links ]
45. Joint European Society of Cardiology/American College of Cardiology Committee. Myocardial infarction redefined a consensus document of the Joint European Society of Cardiology/ American College of Cardiology Committee for the redefinition of myocardial infarction. Eur Heart J 2000; 21: 1502-13. [ Links ]
46. Goktein O, Molok M, Gorenek B, et al. Cardiac troponin T and cardiac enzymes after external transthoracic cardioversion of ventricular arrhythmias in patients with coronary artery disease. Chest 2002; 122:2050-4. [ Links ]
47. Grubb N, Cuthbert D, Cawood P, Flapan AD, Fox K. Effect of DC schock on serum levels of total creatine kinase, MB-creatine kinase mass and troponin T. Resuscitation 1998; 36: 193-9. [ Links ]
48. Kerber RE, Grayzel J, Hoyt R, Marcus M, Kennedy J, Transthoracic resistance in human defibrillation: influence of body weight, chest size, serial schocks, paddle size and paddle contact pressure. Circulation 1981; 63: 676-82. [ Links ]
49. Sirna SJ, Ferguson D, Charbonnier F, Kerber RE,Factors affecting transthoracic impedance during electrical cardioversion. Am J Cardiol 1988; 62: 1048-52. [ Links ]
50. Ewy GA, Hellman D, McClung S, Taren D. Influence of ventilation phase on transthoracic impedance and defibrillation effectiveness. Crit Care Med 1980; 8: 164-6. [ Links ]
51. Levine PA, Barold SS, Fletcher R, Talbot P. Adverse acute and chronic effects of electrical defibrillation and cardioversion on implanted unipolar cardiac pacing systems. J Am Coll Cardioll 1983; 1: 1413-22. [ Links ]
52. The americam heart association in collaboration with the international liason committee on resuscitation (ILCOR). Guidelines 2000 for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation 2000; 102: I-1-384. [ Links ]
53. Weaver WD, Cobb LA, Copass MK, Hallstrom AP. Ventricular defibrillation: a comparative trial using 175- J and 320-J shocks. N Eng J Med 1982; 307: 1101-6. [ Links ]
54. Bardy GH, Marchlinski F, Sharma A, et al. Transthoracic Investigators. Multicenter comparison of truncated biphasic shocks and standard damped sine wave monophasic shocks for transthoracic ventricular defibrillation. Circulation 1996; 94: 1507-14. [ Links ]
55. Lown B. Electrical reversion of cardiac arrhythmias. Br Heart J 1967; 29: 469-89. [ Links ]
56. Kerber RE, Grayzel J, Kennedy J, Jensen SR: Elective cardioversion: influence of paddle electrode location and size on success rates and energy requirements. N Eng J Med 1981; 305: 658-62. [ Links ]
57. Kerber RE, Kienzle M, Olshansky B, et al. Ventricular tachycardia rate and morphology determine energy and current requirements for transthoracic cardioversion. Circulation 1992; 85: 158-63. [ Links ]
58. Pinski S, Sgarbosa E, Ching E, Trohman R. A comparison of 50 J versus 100 J shocks for direct-current cardioversion of atrial flutter. Am Heart J. 1999; 137: 439-42. [ Links ]
59. Bgerkelund C, Orning M. The efficacy of anticoagulant therapy in preventing embolism related to DC cardioversion of atrial fibrillation. Am J Cardiol 1969; 23: 208-15. [ Links ]
60. Klein A, Grimm R, Block W, et al. Cardioversion guided by transesophageal echocardiography: the ACUTE pilot study. Ann Intern Med 1997; 126: 200-9. [ Links ]
61. Mancini GBJ, Goldberger AI. Cardioversion of atrial fibrillation: consideration of embolization, anticoagulation, prophylactic pacemaker and long-term success. Am Heart J 1982; 104: 617-21. [ Links ]
62. Omran H, Jung W, Rabahich R, et al. Left atrial chamber and appendage function after internal atrial defibrillation a prospective and serial transesophageal echocardiographic study. J Am Coll Cardiol 1997; 29: 131-138. [ Links ]
63. Fuchs T. Cardioversion and defibrillation. In Podrid P. Kowey P. Cardiac arrhythmia. Mechanisms, diagnosis, and treatment. Williams and Wilkins. Baltimore 1995; 726-37. [ Links ]
64. Kidway B, McIntyre A, Anderson J, et al. Optimization of transthoracic ventricular defibrillation-biphasic and triphasic shocks, waveform rounding, and synchronized shock delivery. J Electrocardiol 2002; 35: 235-44. [ Links ]
65. Zhang Y, Ramabadran RS, Boddicker K, et al. Triphasic waveforms are superior to biphasic waveforms for transthoracic defibrillation. J Am Coll Cardiol 2003; 42: 568-75. [ Links ]













