Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Entomología
Print version ISSN 0120-0488On-line version ISSN 2665-4385
Rev. Colomb. Entomol. vol.31 no.2 Bogotá July/Dec. 2005
Articulo de revision
Resistencia a insecticidas en mosquitos (Diptera: Culicidae): mecanismos, deteccion y vigilancia en salud publica
Inseclicide resistance in mosquitoes (Diptera: Culicidae): mechanisms, detection and monitoring in public health
IDALYD FONSECA1. MARTHA L. QUINOÑES2
1 Programa de Estudio y Control de Enfermedades Tropicales - PECET. Facultad de Medicina, Universidad de Antioquia. Calle 62 No 52-59. Edificio de Sede de Investigacion Universitaria. Medellin. Colombia. A. A 1226. Fax: (4) 210 6502. E-mail: idalydfin@guajiros.udea.edu.co
2 Autor para correspondencia: Martha L. Quiñones P. Programa de Estudio y Control de Enfermedades Tropicales - PECET. Sede de Investigacion Universitaria Universidad de Antioquia. Lab 632. A. A 1226. Medellin. Colombia. Fax: (4) 210-6502. E-mail: mquinones@guajiros.udea.edu.co
Resumen. Uno de los obstaculos mas serios en los programas de control de vectores de enfermedades humanas es el desarrollo de resistencia a los insecticidas usados. Segun la Organizacion Mundial de la Salud, aproximadamente el 40% de los 506 artropodos de importancia medica presentan algun grado de resistencia a insecticidas. De estas especies. cerca del 50% son especies de mosquitos vectores de malaria, dengue, fiebre amarilla y filariasis. Los dos principales mecanismos de resistencia a insecticidas son las alteraciones en el sitio blanco y un incremento en la tasa de detoxificacion de los insecticidas. Una vez se detectan niveles de resistencia en una poblacion de vectores es fundamental determinar su base bioquimica y molecular. La identificacion de los mecanismos de resistencia permite la seleccion de los insecticidas a usar en los programas de control y la evaluacion del potencial desarrollo de resistencia a insecticidas alternativos. Esta revision presenta informacion basica acerca de los principales mecanismos de resistencia a insecticidas identificados en mosquitos vectores de enfermedades humanas y las metodologias mas usadas para su vigilancia y deteccion.
Palabras clave: Mecanismos moleculares. vectores. Control Quimico. Vigilancia.
Summary. Among the most serious obstacles in vector controlprograms for human diseases is the development of resistance to the insecticides used. According to WHO, approximately 40% of the 506 medically important arthropods show some degree of insecticide resistance. Of these species, about 50% arc species of mosquitoes that vector malaria, dengue, yellow fever and filariasis. The two principal mechanisms of insecticide resistance are alterations in the target site or an increase in the detoxification rate ofthe insecticide. Once resistance is detected in a vector population it is crucial to determine its molecular and biochemical basis. Identification of resistance mechanisms permits the selection of insecticides to use in control programs and the evaluation of potential development of resistance to alternative insecticides. This review presents basic information regarding the main mechanisms of insecticide resistance identifico in mosquito vectors of human diseases and the methodologies most used to monitor and detect them.
Key words: Molecular mechanisms. Vectors. Chemical Control, monitoring.
Introduccion
Cada año, millones de personas alrededor del mundo se enferman y mueren por enfermedades transmitidas por insectos vectores, como malaria, dengue, leishmaniosis y tripanosomiasis. Estas enfermedades causan gran impacto economico y social, particularmente en paises tropicales como Colombia. Actualmente, ningun metodo efectivo de inmunizacion esta disponible para controlar dichas enfermedades y la unica forma de controlar la transmision esta dirigida hacia sus vectores. El uso de insecticidas quimicos ha sido la forma mas utilizada en los programas de Control. Estos se han empleado por mas de 60 años con resultados variables. Inicialmente se usaron piretrinas, de corto efecto de noqueo. Posteriormente se introdujeron insecticidas de mayor accion residual como los organoclorados, carbamatos y organofosforados. A partir de 1990, el desarrollo de piretroides sinteticos fotoestables y las presiones de grupos ambientalistas desplazaron el uso del DDT (Dicloro-difenil-tricloroetano) para la fumigacion intradomiciliar en los programas de control de malaria, siendo en la actualidad el tipo de insecticida mas usado tanto en rociamientos intradomiciliares como en la impregnacion de toldillos (Lengeler etal. 1996; Phillips 2001).
En 1947, tan solo un año despues de la introduccion de insecticidas para el control de vectores, se notificaron los primeros casos de resistencia a DDT en Aedes tritaeniorhynchus (Weidemann) y Ae. solicitans (Walker) (Brown 1986). Desde entonces se han señalado mas de 100 especies de mosquitos resistentes a uno o mas insecticidas, de las cuales 56 son Anophelinos y 39 Culicinos, ademas de triatomineos, pulgas, piojos y garrapatas (WHO 1992). Actualmente, el Comite de Accion para la Resistencia a Insecticidas (IRAC) cita en su pagina web (http://www.plantprotection.org/irac) resistencia en 21 especies de Aedes, entre ellas el vector de dengue Ae. aegypti (Linnaeus) (resislente a 16 insecticidas) y 63 especies de Anopheles, incluyendo Anopheles albimanus Weidemann, An.darlingi Root, An. pseudopunctipenis Theobald y An. rangeli Gabaldon, Cova Garcia & Lopez, todas estas importantes en la transmision de malaria en Colombia.
En Colombia, la descentralizacion de los programas de control de malaria y dengue desde 1992 ha dificultado la vigilancia permanente del estado de la resistencia a insecticidas en las poblaciones vectoras. No obstante, existen registros de resistencia al DDT y Temelos en diferentes especies de Anopheles y Ae. aegypti en el pais, respectivamente (Quiñones et a 1.1987; Suarez et al. 1990), los cuales sugieren que las poblaciones de vectores presentan caracteristicas geneticas favorables para la emergencia de resistencia cuando estas sean presionadas por insecticidas. Sin embargo, debido a que no hay conocimiento de los mecanismos bioquimicos que generaron la resistencia al DDT y a otros quimicos, se desconoce el impacto que podria tener el uso de otros insecticidas que compartan el mismo mecanismo de accion, causado por efectos de resistencia cruzada.
La resistencia a insecticidas o resistencia fisiologica se define como la capacidad de una poblacion de insectos de tolerar dosis de un insecticida que serian letales para la mayoria de los individuos en una poblacion normal de la misma especie y es el resultado de la presion de seleccion positiva ejercida por el insecticida (WHO 1975) sobre genes inicialmente en baja frecuencia. Los genes de resistencia pueden luego dispersarse en la poblacion local de insectos e incluso en el mundo. Los patrones de distribucion de estas variantes geneticas en poblaciones naturales son el efecto conjunto de varias fuerzas evolutivas y factores demograficos como la seleccion, mutacion y el ciclo de vida (Gazave et al. 2001).
numerosos factores influyen en la evolucion de la resistencia a insecticidas, los cuales pueden agruparse en tres categorias: factores geneticos, biologicos y operacionales. Los factores geneticos se relacionan principalmente con la frecuencia y dominancia de los alelos de resistencia, en tanto que los biologicos incluyen el ciclo de vida, el numero de descendientes por generacion y las tasas de flujo genico. Los factores geneticos y biologicos son intrinsecos a las especies y por lo tanto se escapan del control humano Los factores operacionales si pueden ser manejados a fin de evitar o retardar el desarrollo de resistencia. Estos factores se asocian directamente con el tiempo, dosis y formulacion del insecticida, el estadio seleccionado y el uso previo de insecticidas relacionados (Georghiou 1990).
Mecanismos de Resistencia
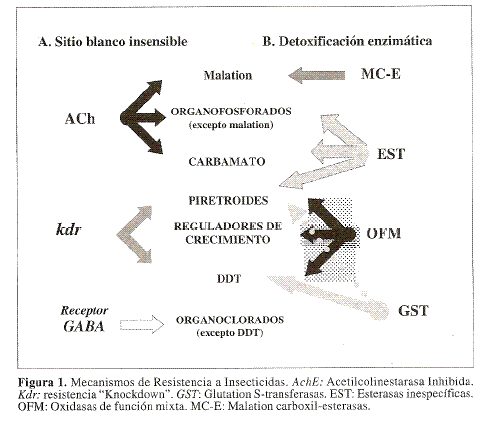
Los dos principales mecanismos de resistencia a insecticidas son las alteraciones en el sitio blanco y un incremento en la tasa de detoxificacion de los insecticidas. Se proponen tambien mecanismos basados en la respuesta al estres termico (Patil et al. 1996), penetracion disminuida, incremenlo en las tasas de excrecion y cambios de comportamiento que eviten el contacto con los insecticidas aunque los vectores sean susceplibles a estos (Brogdon y McAllister 1998a).
La resistencia mediada por el sitio blanco ocurre cuando el insecticida no logra unirse a su sitio de accion ya sea porque hay disminucion en la sensibilidad del sitio blanco o modificacion de este (Hemingway y Ranson 2000). La resistencia basada en enzimas detoxificantes se presenta cuando niveles elevados o actividades modificadas de estas enzimas contribuyen a disminuir la dosis efectiva de un insecticida evitando que llegue a su sitio de accion (Ranson et al. 2002a). (Fig. 1).
1. Alteraciones en el sitio blanco
La causa mas comun de resistencia en el sitio blanco es la presencia de mutaciones puntuales no silentes en genes estructurales. Para que dichas mutaciones sean seleccionadas favorablemente, el cambio en el aminoacido debe disminuir la union al insecticida sin causar perdida de la funcion primaria del sitio blanco. Por lo tanto, el numero de posibles sustituciones de aminoacidos es limitado y comunmente se encuentran mutaciones identicas asociadas con resistencia a traves de taxa altamente divergentes. El grado de deterioro de la funcion, ocasionado por la mutacion que confiere resistencia, se refleja en la eficacia biologica de los individuos resistentes en ausencia de seleccion por el insecticida. Este costo en la eficacia biologica ticne importantes implicaciones para la persistencia de resistencia y/o reversion a la susceptibilidad en poblaciones de campo (Berticat et al. 2002).
1.1. Cambios en el Receptor GABA (Acido 7 -aminobutirico)
En insectos, el receptor GABA es un canal heleromultimerico abierto por el ion cloro, un inhibidor de canales de neuro-transmision en el sistema nervioso y las uniones neuromusculares (Bermudez et al 1991).
El receptor GABA es el sitio de accion para ciclodienos y avermectinas al igual que para fipronil (Ffrench-Constant et al. 1993a). La resistencia esta dada por el gen Rdl (Resistencia a dieldrin), el cual codifica para la subunidad RDL del receptor GABA. La sustitucion Ala302Scr confiere insensibilidad al insecticida al interactuar directamente con el sitio de union del insecticida dentro del poro del canal ionico y alostericamente, desestabilizando la conformacion preferida del insecticida, a traves de un fenomeno conocido comodesensibilizacion (Ffrench-Constant et al. 1998). En Drosophila se identificaron por primera vez subunidades del receptor GABA conteniendo Rdl, las cuales se han encontrado expresadas en el sistema nervioso de insectos resistentes a dieldrin, entre ellos Ae. aegypti (Thompson et al. 1993). En Drosophila simulans Sturtevant y Myzus persicae (Sulzer) (Hemiptera: Aphididae), el mismo residuo es rcemplazado por glicina (Ffrench-Constant et al. 1993b).
1.2. Canales de sodio dependientes de voliaje (kdr)
Los canales de sodio dependientes de voltaje son el blanco de accion del DDT y piretroides. Estos insecticidas actuan sobre el sistema nervioso del insecto causando decaidas lenlas del potencial de accion, generando la iniciacion de descargas repetitivas en los axones motores y sensoriales (Sodcrlund y Bloomquist 1989). Estudios eletrofisiologicos en Ae. aegypti y An. stephensi Liston han demostrado que estos fenomenos resultan de la modificacion en la cinetica de apertura de estos canales (Hemingway et al. 1989;Vatandoost et al. 1996).
El para-canal de sodio es un complejo de proteinas de mas de 2000 aminoacidos, compuesto por 4 dominios homologos separados por enlaces hidrofilicos. Cada uno de estos dominios contiene 6 ochelices hidrofobicas extendidas sobre la membrana (S1-S6) y cuyas secuencias contribuyen a las propiedades funcionales del canal (Loughney et al. 1989).
El gen Para, el cual codifica el canal de sodio, se clono originalmente de D. melanogaster (Loughney et al. 1989) pero la primera mutacion confiriendo resistencia, denominada "Resistencia Knockdowm" o kdr, se identifico en Musca domestica Linnaeus (Williamson et al. 1993). Los fenotipos kdr poseen una mutacion puntual (Leul014Fen) en el segmento transmembranal S6 del dominio II, la cual produce 10-30 veees resistencia a DDT y piretroides en M. domestica (Williamson et al. 1996). Esla mutacion se ha identificado en insectos resistentes a piretroides pertenecienles a los ordenes Diptera (M. domestica, An. gambiae Giles). Blattodea (Blatella germanica (Linnaeus)) (Dong 1997), Lepidoptera (Plutella xylostella Linnaeus) (Schulcr et al. 1998) y Hemiptera (M. persicae) (Martinez-Torres et al. 1999). Otras mutaciones puntuales en el mismo nueleotido (Leul014His: An. gambiae. Leu 1014Ser: An. gambiae, Culex pipiens Linnaeus) tambien confieren resistencia a DDT y piretroides, aunque con menor frecuencia (Martinez-Torres et al. 1998; Ranson et al. 2000a).
Una sustitucion adicional encontrada en cepas de M. domestica, Metionina 918-Treonina, cerca al dominio IIS4-S5, en combinacion con la mutacion Leu 1014-Fen, presenta niveles elevados de resistencia a piretroides (mas de 500 veces), denominandose resistencia super-kdr (Williamson et al. 1996). Esta mutacion no tiene efecto sobre la dependencia de vollaje del canal de sodio pero si reduce la disponibilidad de los canales e incrementa la tasa de inicio y recuperacion de la inactivacion (Vais et al. 2001).
Martinez-Torres et al. (1998) desarrollaron una prueba diagnostica basada en la amplificacion por PCR de alelos especificos, la cual permite discriminar entre individuos homocigoticos susceptibles, homocigoticos resistentes y heterocigoticos con la mutacion Leul014Fen. Debido a que el fenotipo kdr es semi o tolalmente recesivo (Paton et al. 2000), con genes de resistencia en bajas frecuencias, la capacidad de identificar heterocigoticos es importante en la deteccion temprana y manejo de la resistencia en el campo. Esta prueba diagnostica ha sido modificada por Ranson et al. (2000a) para identificar la mutacion Leul014Ser en An. gambiae.
En Drosophila se ha usado un enfoque diferente para aislar mutantes tipo kdr utilizando un metodo basado en el fenotipo de sensibilidad a la temperatura. De esta forma se han identificado dos clases de mutaciones ubicadas en posiciones equivalentes a las mutaciones kdr y super-kdr pero hasta la fecha no se ha establecido su papel en el desarrollo de resistencia (Ffrench-Constant et al. 1998).
1.3. Acetilcolinesterasas (AchE)
La acetilcolinesterasa es una enzima clave en el sistema nervioso al catalizar la hidrolisis del neurotransmisor Acetilcolina sobre las membranas de los nervios post-sinapticos. En insectos, la forma molecular predominante es un dimero anfifilico globular anclado en la membrana mediante un glicolipido (Vontas et al. 2002). AchE es el principal blanco para organofosforados y carbamatos, los cuales inhiben la actividad enzimatica mediante fosforilacion covalente o carbamilatando el residuo de serina dentro del sitio activo (Corbett 1974).
La resistencia a insecticidas mediada por AchE esta relacionada con cambios cualitativos y cuantitativos en la enzima y con mutaciones puntuales generalmente acompañadas por modificacion de los parametros cineticos de la hidrolisis de acetilcolina. Tales mutaciones involucran sustituciones de aminoacidos en el sitio activo de la enzima (Walsh et al. 2001).
En general, los niveles de insensibilidad a insecticidas conferidos por cada sustitucion individual son bajos pero en combinacion producen enzimas altamente resistentes. El alto numero de mutaciones puntuales en AchE contrasta con las pocas mutaciones responsables para resistencia fuerte, encontradas en otros sitios blancos alterados (GABA o kdr). Este numero elevado de mutaciones presentes en AchE se atribuye a la comunalidad sustrato-analogo insecticida y los receptores de acetilcolina (Vontas et al. 2002). Se han registrado mutaciones especificas en AchE que confieren resistencia en D. melanogaster Meigen (Mutero et al. 1994) y M. domestica (Walsh et al. 2001).
En Cx. pipiens existen minimo dos genes, AchE 1 y AchE 2 , los cuales se diferencian en su especificidad de sustrato, sensibilidad y patrones dc migracion electroforetica (Malcolm et al. 1998). AchE2 es ligado al sexo pero aun no ha sido asociado con resistencia. En Ae. aegypti y An. stephensi, tambien sehan identificado genes AchE aunque son pocas las referencias de mecanismos de resistencia basados en AchE en estas especies (Vaughan et al. 1998). Estos genes tambien estan ligados al sexo. Esto sugiere que los genes clonados a partir de estos mosquitos no representan el sitio blanco del insecticida o por el contrario, si existe la resistencia basada en AchE alterada, esta debe estar ligada al sexo en estas especies (Hemingway y Ranson 2000).
En Drosophila se han identificado cinco mutaciones puntuales dentro del gen AchE asociadas con resistencia a organofosforados y carbamatos (Mutero et al. 1994). Estas mutaciones tambien se han identificado mediante estudios de mutagenesis sitio-dirigida en el gen AchE de Ae. aegypti (Milatovic et al. 1997), pero ninguna de ellas se ha identificado en cepas coleccionadas en el campo o seleccionadas en el laboratorio.
2. Incremento en la tasa de detoxificacion de los insecticidas
En el metabolismo de los insecticidas se involucran principalmente tres familias enzimaticas: carboxilesterasas, glutation S-transferasas (GST) y monooxigenasas. La aclividad de una o mas de eslas enzimas a menudo es clevada en poblaciones de insectos resistentes, pero en contraste con la resistencia dada por alteraciones en el sitio blanco, no se conocen totalmenle los mecanismos moleculares de esta resistencia metabolica. La identificacion de enzimas involucradas en la resistencia a insecticidas se complica ademas por la complejidad de tales familias enzimaticas y las dificultades para identificar genes ortologos entre diferentes especies de insectos (Ranson et al, 2002a).
2.1 Carboxil-esterasas
Estas enzimas catalizan la hidrolisis de esteres carboxilicos y se han asociado como primer mecanismo de resistencia a organofosforados, carbamatos y en menor proporcion a piretroides (Hemingway y Karunaratne 1998). Se han encontrado niveles elevados de esterasas inespecificas en el 90% de los casos de tolerancia a insecticidas y en mas de 30 especies de insectos resistentes (Hemingway et al. 2000).
Las esterasas comprenden seis familias proteicas pertenecientes a la superfamilia a/b hidrolasas (Cygler et al. 1993). En Diptera, estas enzimas son codificadas por un grupo de genes sobre el mismo cromosoma (Cr. 3R), donde cada uno de sus miembros pucde sufrir modificaciones que confieren resistencia. Tales modificaciones pueden ser cambios aminoacidicos que altcrcn la especificidad del sustrato (encontrado en An. arabiensis Patton, An. stephensi, An. culicifacies Giles), presencia de multiples copias genicas amplificadas en insectos resistentes (Cx. quinquefasciatus Say, Cx. tarsalis Coquillett, Cx. pipiens, Cx. tritaeniorhynchus Giles), mutaciones puntuales (An. arabiensis, An. culicifacies, An. stephensi) o sobre produccion constitutiva (An. albimanus, An. culicifacies, Cx. quinquefasciatus, Cx. tarsalis) (Hemingway y Ranson 2000).
Bioquimicamente, las esterasas actuan uniendose rapidamente al insecticida pero liberando lentamente los metabolitos de este, es decir, secuestrando el insecticida antes que llegue a su sitio de accion. Lo anterior requiere altas cantidades de estas enzimas debido a la estequiometria de la reaccion, desencadenando la sobreproduccion enzimatica y por ende el desarrollo de resistencia (Karunaratne et al. 1993). Molecularmente, el mecanismo mas comun de resistencia mcdiado por esterasas es la co-amplificacion de los genes est a1' y est b2', los cuales presentan distribucion mundial y cuya base bioquimica y molecular de resistencia ha sido bien caracterizada en el mosquito Cx. quinquefasciatus (Vaughan et al. 1997).
La alta homologia entre los genes est a y est b sugiere que estos han surgido como resultado de un evento ancestral de duplicacion genica (Raymond et al. 1991). Los genes est a2' y est b2'se encuentran en el mismo amplicon alejados 2.7 kb en insectos resistentes y solo 1.7 kb en insectos susceptibles. La diferencia esta dada por la presencia de tres inserciones en el espacio intergenico amplificado (Vaughan et al. 1997). Las inserciones pueden haber introducido clementos reguladores adicionales (Hemingway etal. 1998).
Recientemente se ha descrito co-amplificacion de est a2 y est b2' ligada a un tercer gen, aldehido oxidasa, el cual a su vez se encuentra co-elevado dentro del mismo amplicon con tales alelos pero no con otros genolipos de esterasas (Hemingway et al. 2000).
El analisis de fragmentos de restriccion y homologia de secuencias en cepas de insectos resistentes procedentes de distintos continentes, ha permitido confirmar que la co-amplificacion de est a2` y est b2', posee un origen unico y se ha propagado mundialmente (Hemingway y Karunaratne 1998; Raymond et al. 1998). Esta rapida e inesperada migracion de insectos resistentes sugiere una gran ventaja en la eficacia biologica de los portadores de este amplicon en presencia del insecticida (Hemingway y Karunaratne 1998), resultando en serias implicaciones para el control del vector y la enfermedad.
Otros fenotipos de resistencia mas variables y menos comunes involucran coamplificacion de est a3 y est b1, o amplificacion individual de est b1, o est a1 y est a5', los cuales presentan distribucion gcografica restringida (Guillemaud et al. 1997; Severini et al 1997; Vaughan et al. 1997). La region cromosomica que contiene estos genes de esterasas, presumiblemente representa un punto susceptible de amplificacion, una teoria sustentada por la amplificacion de genes esterasa P homologos en Cx. tritaeniorhyncus (Karunaratne etal. 1998).
2.2. Glutation-S-transferasas
La enzima Glutation S-transferasa (GST) pertenece a una gran familia de isoenzimas multifuncionales involucradas en el metabolismo, detoxificacion y excrecion de un amplio rango de xenobiolicos incluyendo los insecticidas. Ellas se encargan de proteger a las celulas del estres oxidativo y de los toxicos quimicos, catalizando la conjugacion de los componentes electrofilicos con el grupo tiol de la glutation reducida (GSH), obteniendo productos mas hidrosolubles y de mayor excrecion (Salinas y Wong 1999).
En eucariontes se han identificado mas de 40 genes GST clasificados en 13 grupos segun la identidad de sus secuencias, propiedades inmunologicas y en algunos casos, especificidad de sustrato (Shechan etal. 2001). En insectos se han reconocido solo tres clases: Delta. Sigma y Epsilon (Ranson et al. 2001), las cuales estan potencialmente relacionadas con el desarrollo de resistencia a insecticidas.
GST se asocia principalmente con resistencia a DDT (catalizando la dehidroclorinacion del DDT a su metabolito menos toxico DDE) (Clark y Shamaan 1984), organofosforados y recientemente piretroides (Kostaropoulos et al. 2001; Vontas et al. 2001), a traves de mecanismos de cambio en la especificidad del sustrato (An. gambiae), niveles elevados de actividad (An. gambiae, An. dims Peyton & Harrison, An. stephensi, An. subpictus Grassi, An. culicifacies y Aedes aegypti) y regulacion genica (con posible amplificacion) (An. gambiae. An. dirus y Ae. aegypti), aunque los elementos reguladores que controlan la expresion de GST no se han identificado aun (Hemingway y Ranson 2000).
GST de la clase Delta son codificadas por una familia multigenica. En D. melanogaster y An. gambiae tal familia se encuentra agrupada (Toung et al. 1993; Ranson et al. 1998), en contraste con M. domestica, donde estos genes se encuentran dispersos a traves de todo el genoma (Zhou y Syvanen 1997). Los genes de esta subfamilia han sido localizados sobre el cromosoma 2R, division 18B y 19D y se expresan en niveles elevados tanto en larvas como adultos de An. gambiae (Ranson et al. 1998; Ranson et al. 2001). La familia GST de la clase Sigma consiste de un unico gen en todas las tres especies (Beall et al. 1992; Reiss y James 1993). Se ha observado que la resistencia a DDT en An. gambiae es diferencial dependiendo del estadio de su ciclo de vida; asi, el gen GSTsl se expresa en larvas pero su deteccion es escasa en insectos adultos, estadio responsable de la transmision de malaria (Reiss y James 1993). Recientemenle se ha descrito GST clase Epsilon en An. gambiae y se sugiere que representa la mayor familia enzimatica confiriendo resistencia a DDT en este vector. Se han identificado dos genes codificando enzimas funcionales GSTel y GSTe2. Uno de estos genes, GSTe2, presenta actividad dehidroclorinasa y niveles de sobre-expresion cinco veces mayores en cepas resistentes que en cepas susceptibles (Ranson et al 2001). Estos genes se ubican en la division 33B sobre el cromosoma 3R que contiene uno de los dos mayores loci {rtdl) para rasgos cuantitalivos asociados con resistencia a DDT (Ranson etal. 2000b). Ranson etal. (2001) propusieron que rtdl podria ser un elemenlo regulador actuando en Cis, el cual estaria controlando la expresion de los genes GST clase Epsilon. Si multiples miembros de esta familia genica estan bajo el control de un factor regulador comun, una mutacion en este factor podria explicar la elevada actividad de GST observada en ensayos bioquimicos (Ding etal. 2003).
Un estudio sobre las propiedades bioquimicas e inmunologicas de la subfamilia Epsilon identifico un alelo GSTelK, el cual presento altos niveles de actividad peroxidasa (Ortelli et al. 2003). En Nilaparvata lugens Stal (Hemiptera: Delphacidac) se ha demostrado que la actividad de peroxidasa protege contra daños causados por productos de la peroxidacion lipidica inducidos por la exposicion a piretroides (Vontas et al. 2001). Aunque este mecanismo no se ha identificado en mosquitos, es posible que insectos portadores de este alelo posean ventajas en su eficacia biologica en presencia de insecticidas (Ortelli etal. 2003).
2.3. Citocromos P450
Los citocromos P450 son una super familia de hemoproteinas responsables del metabolismo oxidativo de una amplia variedad de componentes exogenos (alcloquimicos vegetales, promutagenos e insecticidas) y endogenos (hormonas juveniles, ecdiesteroides, feromonas) del metabolismo (Scott y Wen 2001). P450 han sido encontrados en todos los sistemas vivos y en un rango diverso de especies de insectos, incluyendo Diptera (Scott 1999), Lepidoptera (Rose et al. 1997) y Coleoptera (Sharf et al. 2001).
Se ha identificado resistencia mediada por P450 para casi todas las clases de insecticidas, principalmente piretroides (Berge et al. 1998), organoclorados y reguladores decrecimiento (Brogdon y McAllister 1998a). Se proponen dos posibles mecanismos geneticos: (1) Cambios estructurales en P450s especificos o (2) Niveles elevados de expresion de P450s. Mutaciones puntuales dentro de genes estructurales P450 pueden resultar en actividades cataliticas incrementadas o alta afinidad por el insecticida (Scott y Wen 2001). Algunos estudios han registrado sobre-expresion constitutiva (CYP6G1, CYP12D1) e induccion post exposicion a DDT (CYP12D1) en cepas de insectos resistentes (Brandt etal. 2002), pero en pocos casos se ha establecido conexion definitiva entre la expresion elevada de un gen P450 especifico y el desarrollo de resistencia.
En D. melanogaster se han aislado 83 genes putativos para codificar P450s funcionales. Estos han sido clasificados en 25 familias, pero mas del 50% pertenece a las familias CYP4 o CYP6 (Tijet et al. 2001). Recicntemente, Daborn et al. (2002) utilizando analisis de microarreglos sobre todos los P450s de D. melanogaster demostraron que DDT-R, un gen que confiere resistencia a DDT, esta asociado con un incremento en la transcripcion del gen Cyp6g1. Esto se confirmo mediante analisis transgenicos de Cyp6g1, los cuales demostraron que la transcripcion es necesaria y suficiente para el desarrollo de resistencia.
En An. albimanus se identificaron 17 genes que codifican proteinas de las familias CYP4 y CYP9. En An. gambiae se identificaron 34 genes P450: 14 genes pertenecientes a la familia CYP6, 18 genes para CYP4 y 2 para CYP9. Estos genes se localizan en el cromosoma 3R, division 30A (CYP6), cromosoma 2R, division 13C (CYP6P) y division 12C (CYP4H) (Ranson et al. 2002b). Loanterior se relaciona con la identificacion de dos loci de resistencia para permetrina, uno de los cuales se localiza en el cromosoma 3R, division 30 (Ranson et al. 2002b). La co-localizacion de este loci de resistencia con un grupo de genes P450, plantea el papel de una o mas de estas proteinas en conferir resistencia a piretroides en An. gambiae.
2.4. Aldehido Oxidasa
En vertebrados superiores, la enzima aldehido oxidasa esta involucrada en el metabolismo oxidativo de xenobioticos y en la reduccion de nitrosaminas, acidos hidroxamicos, N-òxidos, hidrocarbonos aromaticos nitropoliciclicos, colorantes azo y sulfoxidos (Calzi et al. 1995), pero existen pocos estudios sobre su papel en el metabolismo de los insectos.
Esta enzima pertenece al grupo de hidrolasas que contienen Molibdeno. Se asume que para todas las enzimas de este grupo, los sustratos acluan en el molibdeno central, reduciendolo del estado Mo(VI) a Mo(IV). Posteriormente, los equivalentes reductores son transferidos via centros de sulfuro de hierro y la enzima es reoxidada por interaccion con el oxigeno (Turner et al. 1995).
Esta enzima se describio por primera vez para insectos en la cepa PELRR resistente de Cx. quinquefasciatus (Hemingway et al. 2000). El gen que codifica esta enzima fue identificado en ligamiento con el gen esta, dentro del amplicon de 30 kb asociado con resistencia a insecticidas el cual contiene los genes est a2' y est b2'. Lo anterior coincide fuertemente con estudios previos de mapeo genetico en An. albimanus (Narang y Seawright 1983) y sugiere una ventaja selectiva de los individuos portadores de este amplicon con respecto a los amplicones que contienen otras esterasas (Coleman et al. 2002).
Coleman et al. (2002), mediante analisis de secuenciamiento y donacion, identificaron para aldehido oxidasa una secuencia de 1266 aminoacidos, la cual transcribe una proteina de 150 kDa. Analisis por RT-PCR en cepas susceptibles y resistentes sugieren que el gen amplificado es transcrito en todas las fases del ciclo de vida de los mosquitos, presentando mayor actividad en larvas resistentes, con un pico en los estadios 3 y 4, disminuyendo progresivamenteen pupas y adultos.
Aunque el papel especifico del gen aldehido oxidasa en la resistencia a insecticidas no se ha determinado totalmente, se ha demostrado que insecticidas como el paracion y herbicidas conteniendo el grupo aldehido son reconocidos como sustratos o inhibidores enzimaticos (Hemingway etal. 2000). Trabajos realizados en mamiferos han involucrado esta enzima en el desarrollo del sistema nervioso central, uno de los principales blancos de accion de los insecticidas (Calzi et al. 1995), lo cual es otra evidencia de su posible papel en la resistencia a insecticidas.
Resistencia Cruzada
La resistencia cruzada implica el mismo mecanismo de resistencia para dos clases de insecticidas no relacionados (Najera y Zaim 2002). Este tipo de resistencia se presenta principalmente entrc piretroides y DDT en diferentes especies de insectos. Registros de resistencia tipo kdr en An. gambiae en Africa oriental postulan que la resistencia ha sido seleccionada por el uso temprano de DDT y/o el uso agricola de piretroides (Chandre et al. 1999). La resistencia cruzada es especffica de producto mas no del tipo de insecticida, lo cual se ha demostrado en An. stephensi donde la resistencia a permetrina no confiere resistencia cruzada a deltametrina en larvas y adultos pero si a otros cianopiretroides (Curtis y Townson 1998) y Etofenprox (Curtis 1993). Recientemente se ha registrado resistencia cruzada tipo kdr en Ae. aegypti (Brengues et al. 2003). La presencia de resistencia cruzada tipo kdr entre DDT y piretroides amenaza el uso de piretroides tanto en rociamientos intradomiciliares como en toldillos impregnados para el control de malaria.
Un estudio realizado en An. funestus Giles demostro elevados niveles de resistencia a piretroides pero no a DDT (Hargreaves et al. 2000). Estas evidencias han motivado la idea de restaurar los program as de rociamiento con DDT en paises como Madagascar y en la provincia dc Kwazulu/Natal en Sur Africa, en areas donde se advierte alta transmision de malaria (Brooke et al. 2001). El impacto del uso reciente de DDT ha sido asociado con una reduccion del 60% de los casos de malaria durante el 2001 en Sur Africa (Curtis 2002).
Deteccion y Vigilancia de la Resistencia
La capacidad de prevenir o retardar la evolucion del desarrollo de resistencia a insecticidas se fundamenta en la implementacion de estrategias para el manejo y vigilancia de la resistencia. Tres aspectos importantes en el diseno de tales estrategias son (1) el establecimiento de lineas-base dc susceptibilidad, (2) la identificacion de los mecanismos de resistencia y (3) el uso de metodos que vigilen las frecuencias de resistencia y el efecto de las estrategias de control (Brogdon y McAllister 1998a).
La identificacion de los mecanismos de resistencia determina el espectro de resistencia cruzada, facilita la escogencia de insecticidas alternativos y permite el mapeo detallado de areas con poblaciones resistentes. Los bioensayos o pruebas biologicas tienen la capacidad de encontrar casos de resistencia producidos por cualquiera de los diferentes mecanismos bioquimicos o neurofisiologicos. La OMS (WHO 1981) implemento el uso de papeles impregnados con insecticidas o sinergistas en dosis estandarizadas, basados en la correlacion entre mortalidad vs tiempo de exposicion y mortalidad vs dosis letales. Otra alternativa para la realizacion de los bioensayos es el uso de botellas de vidrio impregnadas con insecticidas la cual ha sido estandarizada por el Centro para el Control y Prevencion de Enfermedades en Estados Unidos (CDC). Esta aproximacion simplifica el procedimiento de los bioensayos convencionales e incrementa la cantidad de informacion que puede obtenerse de un grupo limitado de mosquitos (Brogdon y McAllister 1998b).
Debido a que los piretroides causan induccion de paralisis temporal, mas conocida como "knockdown", se ha asociado la resistencia a piretroides con un incremento significativo en el tiempo de noqueo antes de disminuir la mortalidad, por lo que dicho tiempo es un bucn indicador para la deteccion temprana de resistencia a piretroides (WHO 1992) y puede incluirse en los programas de vigilancia de resistencia a estos insecticidas al aportar informacion inicial acerca de la resistencia basada en cl gen kdr (Chandre et al. 1999).
Los metodos bioquimicos y moleculares pueden identificar mecanismos especificos de resistencia y detectar genes de resistencia cuando estos aun esten en bajas frecuencias y utilizando un numero minimo de insectos (Brogdon 1984). Las pruebas bioquimicas estan disponibles para la evaluacion de esterasas inespecificas, oxidasas de funcion mixta, glutation S-transferasas y acetilcolinesterasas inhibidas, las cuales pueden ser detectadas en un mismo individuo. Aunque las pruebas estan inicialmente diseñadas para realizarse en condiciones de laboratorio, pueden estandarizarse bajo condiciones de campo directamente en las areas de vigilancia.
Actualmente se dispone de estudios comparativos de la estructura y funcion de los genomas totales de An. gambiae y D. melanogaster (Ranson et al. 2000b). Estos analisis permitiran descubrir nuevas moleculas hormonales, neuronales y reguladoras que puedan utilizarse como blancos para el desarrollo de nuevas clases de insecticidas; Igualmente, los avances recientes en genomica funcional permitiran determinar los cambios moleculares precisos que resulten en fenotipos de resistencia, contribuyendo asi al manejo de la resistencia en las poblaciones de campo (Hemingway et al. 2002).
Para el manejo de la resistencia se estan desarrollando numerosas herramientas, desde nuevos insecticidas quimicos hasta mosquitos transgenicos. Se han considerado tambien distintas estrategias, entre ellas el uso de mezclas de insecticidas con diferentes modos de accion (Corbel et al. 2002), las cuales deben producirse industrialmente. Entre las estrategias mas comunes se encuentran la aplicacion de insecticidas en mosaico y rotaciones. La aplicacion en mosaico consiste en dividir el area a tralar en zonas, seleccionar dos insecticidas de resistencia no cruzada y aplicar en cada zona uno de estos (Ej., alternando piretroides y organofosforados). En la estrategia de rotacion se aplica un insecticida en un ciclo y otro, que no sea de resistencia cruzada, en el ciclo siguiente. (Por Ej., piretroides - organofosforados /carbamalos) (Penilla et al. 1998).
Se han desarrollado modelos matematicos y simulaciones in vitro de la evolucion de los genes de resistencia asociados a diferentes patrones de usos de los insecticidas (Tabashnik 1990), pero estos modelos no han sido aplicados en estudios de campo dada la dificultad practica de estimar correctamente los cambios en las frecuencias de los genes de resistencia en los programas de control quimico aplicados en gran escala (Penilla et al. 1998; Hemingway y Ranson 2000).
Conclusiones
Todos los insecticidas quimicos ejercen, en mayor o menor extension, presiones selectivas sobre las poblaciones de insectos que intentan controlar; por lo cual, en un tiempo las poblaciones resistentes comienzan a emerger. El tiempo necesario para el desarrollo de resistencia depende de numerosos factores incluyendo la frecuencia y naluraleza de los genes de resistencia, las estrategias para su manejo, las dosis y frecuencias de aplicacion de los insecticidas y la eficacia biologica de las poblaciones resistentes en relacion con las susceptibles. Mientras no haya alternativas efectivas al uso del control quimico, este debe enmarcarse en programas de control integrado, adaptandose a las condiciones locales con enfasis en la rotacion de insecticidas a fin de prevenir, retardar o revertir el desarrollo fuluro de resistencia en las poblaciones de insectos vectores. Es indispensable en los programas de control de las enfcrmedades transmitidas por vectores el uso de metodos quo vigilen las Frecuencias de resistencia y el efecto de las estrategias de control. Todas las deeisiones sobre el uso de insecticidas deben tomarse considerando los componentes del manejo de la resisteneia y el impacto minimo sobre los humanos, los organismos no blanco y el ambiente.
Literatura citada
BEALL. C; FYRBERG. C: SONG. S.: FYRBERG, E. 1992. Isolation of a Drosophila gene encoding glutathione S-transferase. Biochemical Geneties 30: 515-527. [ Links ]
BERGE, J. B.; FEYEREISEN. R.: AMI-CHOT, M. 1998. Cylochrome P450 monooxygenases and insecticide resistance in insects. Philosophical Transaccions of the Royal Society of London. Series B, Biological Sciences 353: 1701-1705. [ Links ]
BERMUDEZ, I.; HAWKINS. C. A.; TAYLOR. A. M.; BEADLE. D. J. 1991. accions of insecticides on the insect GAB A receptor complex. Journal of Receptor Researchi:221-232. [ Links ]
BERTICAT, C; BOQUIEN. G.; RAYMOND, M.; CHEVILLON, C. 2002. Insecticide resistance genes induce a mating competition cost in Culex pipiens mosquitoes. Genelical Research 79:41 -47. [ Links ]
BRANDT, A.; SHART. M.: PEDRA, J. H. R; HOLMES, G.; DEAN. A.; KREITMAN. M.; PITTENDRIGH, B. R. 2002. Differential expression and induction of two Drosophila cylochrome P450 genes near the Rst(2)DDi locus. Insect Molecular Biology 11:337-341. [ Links ]
BRENGUES, C.; HAWKES. N. J.: CHANDRE, F.; MCCARROLL. L.; DUCHON. S.; GUILLET, P.: MANGUIN, S.; MORGAN, J. C.: HEMINGWAY. J. 2003. Pyrethroid and DDT cross-resistance in Aedes aegypti is correlated with novel mutations in the voltage-gated sodium channel gene. Medical and Veterinary Entomology 17:87-94. [ Links ]
BROGDON, W. G. 1984. Mosquito protein microassay. I. Protein determinations from small portions of single-mosquito homogenates. Comparative Biochemistry and Physiology. B, Comparative Biochemistry 79: 457-9. [ Links ]
BROGDON. W. G; MCALLISTER, J. C. 1998a. Insecticide Resistance and Vector Control. Emerging Infectious Diseases 4: 605-613. [ Links ]
BROGDON, W. G; MCALLISTER, J. C.1998b. Simplification of adult mosquito bioassays through use of time-mortality determinations in glass bottles. Journal of the American Mosquito Control Association 14: 159-164. [ Links ]
BROOKE. B. D.-. KLOKE, G.; HUNT. R. H.; KOEKEMOER, L. L.; TEMU, E. A.; TAYLOR, M. E.; SMALL, G.: HEMINGWAY. J.; COETZEE, M. 2001. Bioassay and biochemical analysis of insecticide resistance in southern African Anophelesfunestus (Diplera: Culicidae). Bulletin of Entomological Research 91: 265-272. [ Links ]
BROWN, A. W. A. 1986. Insecticide resistance in mosquitoes: a pragmatic review. Journal of the American Mosquito Control Association 2: 123-140. [ Links ]
CALZI, M.; RAVILO, C; GHIBAUNDI, E.; DEGIOIA. L.; SALMONA, M.; CAZZA-NIGA. G.; KUROSAKI. M.;TERAO, M.; GARATTINI, E. 1995. Purification,cDNA cloning and tissue distribution of bovine liver aldehyde oxidase. The Journal of Biological Chemistry 270:31037-31045. [ Links ]
CHANDRE, F.; DARRIER. R; MANGA. L.; AKOGBETO, M.; FAYE, O.; MOU-CHET. J.; GUILLET, P. 1999. Status of pyrethorid resistance in Anopheles gambiae sensu lalo. Bulletin of the World Health Organization 77(3): 230-234. [ Links ]
CLARK, A. G.; SHAMAAN, N. A. 1984. Evidence that DDT-dehydrochlorinase from the housefly is a glutathione S-transferase. Pesticide Biochemistry and Physiology 22: 249-261. [ Links ]
COLEMAN. M.; VONTAS, J. G.; HEMINGWAY, J. 2002. Molecular characterization of the amplified aldehyde oxidase from insecticide resistant Culex quinquefasciatus. European Journal of Biochemistry 269: 768-779. [ Links ]
CORBEL, V; DARRIET. R; CHANDRE, R; HOUGARD, J. M. 2002. Insecticide Mixtures for Mosquito Net Impregnation Against Malaria Vectors. Parasite 9:255-259. [ Links ]
CORBETT, J. R. 1974. The Biochemical mode of accion of pesticides. Academic Press, London, UK. pp. 102-130. [ Links ]
CURTIS. C. R 1993. Workshop on bednets at the International Congress of Tropical Medicine. Japanese Journal of Sanitary Zoology. 44: 65-68. [ Links ]
CURTIS. C. R 2002. Should the use of DDT be revived for malaria vector control? Biomedica 22:455-61. [ Links ]
CURTIS. C. R;TOWNSON, H. 1998. Malaria: existing methods of vector control and molecular entomology. British Medical Bulletin 54: 311-325. [ Links ]
CYGLER, M.; SCHRAG, J. D.: SUSSMAN, J. L.; HAREL, M.: SILMAN, I.; GENTRY, M. K. 1993. Relationship between sequence conservation and three-dimensional structure in a large family of esterases, lipases and related proteins. Protein Science 2: 366-82. [ Links ]
DABORN, P. J.: YEN, J. L.: BOGWITZ. M. R.; LEGOFF, G.; FEIL, E.; JEFFERS. S.; TIJET, N.; PERRY, T.; HECKEL, D.; BATTERMAN, P.; FEYEREISEN, R,; WILSON, T. G.; FFRENCH-CONSTANT, R. H. 2002. A single P450 allele associated with insecticide resistance in Drosophila. Science 297: 2253-2256. [ Links ]
DING, Y.; ORTELLI, R; ROSSITER. L. C; HEMINGWAY, J.; RANSON. H. 2003. The Anopheles gambiae glutathione transferase supergene family: annotation. phylogeny and expression profiles. Genomies 13:4-35. [ Links ]
DONG, K. 1997. A single amino acid change in thepara sodium channel protein isassociated with knockdown-resistance (kdr) to pyrethroid insecticides in German cockroaches. Insect Molecular Biology 27:93-100. [ Links ]
FFRENCH-CONSTANT, R. H.; STEICHEN, J.;ROCHELAU,T.A.:ARONSTEIN. K.; ROUSH, R. T. 1993a. A single aminoacid substitution in a g-aminobulyric acid subtype. A receptor locus associated with Ciclodiene insecticide resistance in Drosophila populations. Proceedings of the National Academy of Sciences of the United States of America 90: 1957-1961. [ Links ]
FFRENCH-CONSTANT, R. H.: ROCHELAU, T. A.; STEICHEN, J. C; CHALMERS. A. E. 1993b. A point mutation in a Drosophila GABA receptor confers insecticide resistance. Nature 363:449-451. [ Links ]
FFRENCH-CONSTANT. R. H.: PITTENDRIGH. B.: VAUGHAN, A.: ANTHONY, N. 1998. Why are there so few resistance-associated mutations in insecticide target genes? Philosophical Transaccions of the Royal Society of London. Series B, Biological Sciences. 353: 1685-1693. [ Links ]
GAZAVE, E.: CHEVILLON. C: LENOR-MAND, T.; MARQUINE, M.; RAYMOND. M. 2001. Dissecting the cost of insecticide resistance genes during the overwintering period of the mosquito Culexpippiens. Heredity 87: 441-448. [ Links ]
GEORGHIOU, G. P. 1990. Overview of insecticide resistance. Pages 18-41. In: M. B. Green, H.M. LeBaron and W. K. Moberg (eds.). Managing resistance to agrochemical from fundamental research to practical strategies. American Chemical Society Series. 421, Washington. DC. 421 p. [ Links ]
GUILLEMAUD, T.; MAKATE, N.; RAYMOND, M.; HIRST. B.; CALLAGHAN, A. 1997. Esterase gene amplification in Culex pipiens. Insect Molecular Biology 6:319-327. [ Links ]
HARGREAVES, K.: KOEKEMOER, L. L.; BROOKE, B. D.; HUNT, R. H.; MTHEMBU, J.: COHETES, M. 2000. Anopheles funestus resistant to pyrethorid insecticidas in South Africa. Medical and Veterinary Entomology 14: 181-189. [ Links ]
HEMINGWAY, J.; BODDINGTON, R. G.; HARRIS, J.; DUNBAR, S. J. 1989. Mechanisms of insecticide resistance in Aedes aegypti (L.) (Diptera: Culicidae) from Puerto Rico. Bulletin of Entomological Research 79: 123-130. [ Links ]
HEMINGWAY, J.; HAWKES, N.; PRAPAN-THADARA, L.; JAYAWARDENA. K. G. I.; RANSON, H. 1998. The role of gene splicing, gene amplification and regulation in mosquito insecticide resistance. Philosophical Transaccions of the Royal Society of London. Series B, Biological Sciences 353: 1695-1699. [ Links ]
HEMINGWAY, J.; KARUNARATNE, S. H. P. P. 1998. Mosquito carboxylesterases: a review of molecular biology and biochemistry of a major insecticide resistance mechanism. Medical and Veterinary Entomology 12: 1-12. [ Links ]
HEMINGWAY, J.; RANSON, H. 2000. Insecticide Resistance in Insect Vectors of Human Disease. Annual Review of Entomology 45: 371-391. [ Links ]
HEMINGWAY, J.: COLEMAN, M.; PATON, M.; MCCARROLL, L.; VAUGHAN, A.; DESILVA, D. 2000. Aldehyde Oxidase is coamplified with the World's most common Culexmosquito insecticide resistance-associated eslerases. Insect Molecular Biology 9: 93 99. [ Links ]
HEMINGWAY, J.; FIELD, L.; VONTAS, J. 2002. An Overview of Insecticide Resistance. Science 298: 96-97. [ Links ]
KARUNARATNE, S. H. P. P.; JAYAWARDENA, K. G. I.; HEMINGWAY, J.; KETTERMAN, A. J. 1993. Characterization of a B-type esterase involved in insecticide resistance from the mosquito Culex quinquefasciatus. The Biochemical Journal 294: 575-579. [ Links ]
KARUNARATNE, S. H. P. P.; VAUGHAN, A.; PATON, M. G.; HEMINGWAY, J. 1998. Amplification of a serine esterase gene is involved in insecticide resistance in Sri Lankan Culex tritaeniorhynchus. Insect Molecular Biology 7: 307-315. [ Links ]
KOSTAROPOULOS, I.; PAPADOPOULOS, A. I.; METAXAKIS, A.; BOUKOUVALA, E.; PAPADOPOULOU—MOURKIDOU, E. 2001. Glutathione S-transferase in the defense against pyrethroid insecticides. Insect Molecular Biology 31:313-319. [ Links ]
LENGELER, C; CATTANI, J.; DE SAVIGNY, D. 1996. Net Gain: A New Method for preventing malaria deaths. International Development Research Center, Olawa and World health Organization, Geneva. [ Links ]
LOUGHNEY, K.; KREBER, R.; GANETZ-KY. B. 1989. Molecular analysis of the para locus, sodium channel gene in Dwsophila. Cell 58: 1143-1154. [ Links ]
MALCOLM, C. A.; BOURGUET, D.; ASCOLILLO. A.; ROOKER, S. J.: GARVEY, C. F. 1998. A sex linked Ace gene, not linked to insensitivity acetylcholinesterase-mediated insecticide resistance in Culex pipiens. Insect Molecular Biology 7: 107-20. [ Links ]
MARTINEZ-TORRES, D.; CHANDRE, E; WILLIAMSON, M. S.; DARRIET, F.; BERGE, J. B.; DEVONSHIRRE, A. L.; GUILLET, P.; PASTEUR, N.; PAURON, D. 1998. Molecular characterization of pyrethroid knockdown resistance {kdr) in the major malaria vector Anopheles gambiae s.s. Insect Molecular Biology 7: 179-184. [ Links ]
MARTINEZ-TORRES, D.; FOSTER, S. P.; FIELD, L. M.; DEVONSHIRRE, A. L.; WILLIAMSON, M. S. 1999. A sodium channel point mutation is associated with resistance to DDT and pyrethroid insecticides in the peach-potato aphid, Myzus penicae (Hemiptera: Aphididae). Insect Molecular Biology 8: 339-346. [ Links ]
MILATOVIC, D.; MORETTO, A.; OSMAN, K. A.; LOTTI, M. 1997. Phenyl valerate esterases other than neuropathy target esterase and the promotion of organo-phosphate polyneuropathy. Chemical Research in Toxicology 10(9): 1045-1048. [ Links ]
MUTERO, A.; PRALAVORIO, M.; BRIDE, J. M.; FOURNIER, D. 1994. Resistance-associated point mutations in insecticide insensitive acetylcholinesterase. Proceedings of the National Academy of Sciences of the United States of America 91:5922-5926. [ Links ]
NAJERA, J. A.; ZAIM, M. 2002. Malaria Vector Control: Decision making criteria and procedures for judicious use of insecticides. WHO Pesticide Evaluation Scheme (WHOPES), World Health Organization, Geneva. [ Links ]
NARANG, S.: SEAWRIGHT, J. A. 1983. Genetic mapping and characterization of an aldehyde oxidase of Anopheles albimanus. Biochemical Geneties 21:653-660. [ Links ]
ORTELLI, F.; ROSITER, L. C; VONTAS, L; RANSON, H.; HEMINGWAY, J. 2003. Heterologous expression of four glutathione transfera.se genes genetically linked to a major insecticide resistance locus, from the malaria vector Anopheles gambiae. The Biochemical Journal 373: 957-963. [ Links ]
PATIL, N. S.; LOLE, K. S.; DEOBAGKAR, D. N. 1996. Adaptive larval ihermo-tolerance and induced cross-tolerance to propoxur insecticide in mosquitoes Ano pheles stephensi and Aedes aegypti. Medical and Veterinary Entomology 10: 277-82. [ Links ]
PATON, M. G.; KARUNARATNE, S. H. P. P.; GIAKOUMAKI, E.; ROBERTS, N.; HEMINGWAY, J. 2000. Quantitative analysis of gene amplification in insecticide resistant Culex mosquitoes. The Biochemical Journal 346: 17-24. [ Links ]
PENILLA, R. P.; RODRIGUEZ, A. D.; HEMINGWAY, J.; TORRES, J. L.; ARREDONDO-JIMENEZ, J. I.; RODRIGUEZ, M. H. 1998. Resistance management strategies in malaria vector mosquito control. Baseline data fora large-scale field trial against Anopheles albimanus in Mexico. Medical and Veterinary Entomology 12: 217-233. [ Links ]
PHILLIPS. R. S. 2001. Current status of malaria and potential for control. Clinical Microbiology Reviews 14:208-226. [ Links ]
QUINOÑES, M. L.; SUAREZ, M. R; FLEMING, G.A. 1987. Estado de la susceptibilidad al DDTde los principales vectores de malaria en Colombia y su implicacion epidemiologica. Biomedica 7: 81-86. [ Links ]
RANSON, H.; COLLINS, F. H.; HEMINGWAY, J. 1998. The role of alternative mRNA splicing in generating heterogeneity with in Anopheles gambiae class I GST family. Proceedings of the National Academy of Sciences of the United States of America 95: 14284-14289. [ Links ]
RANSON, H.; JENSEN. B.;VULULE, J. M.; WANG, X.; HEMINGWAY, J.; COLLINS, F. H. 2000a. Identification of a novel mutation in the voltage-gated sodium channel gene of Anopheles gambiae associated with resistance to pyrethroid insecticides. Insect Molecular Biology 9: 491-497. [ Links ]
RANSON, H.; JENSEN, B.; WANG, X.; PRA-PANTHADARA, L.; HEMINGWAY, J.; COLLINS, F. H. 2000b. Genetic mapping of two loci affecting DDT resistance in the malaria vector Anopheles gambiae. Insect Molecular Biology 9:499-507. [ Links ]
RANSON, H.; ROSSITER, L.; ORTELLI, F.; JENSEN, B.; WANG, X.; ROTH. C. H.; COLLINS, F. H.; HEMINGWAY, J. 2001. Identification of a novel class of insect glutathione S-transferases involved in resistance to DDT in the malaria vector Anopheles gambiae. The Biochemical Journal 359: 295-304. [ Links ]
RANSON, H.; CLAUDIANOS, C; ORTELLI. F; ABGRALL. C; HEMINGWAY, J.; SHARAKHOVA, M. V; UNGER, M. E; COLLINS, F. H.; FEYEREISEN, R. 2002a. Evolution of supergene families associated with insecticide resistance. Science 298: 179-181. [ Links ]
RANSON, H.; NIKOU, D; HUTCHINSON, M.; WANG, X.; ROTH, C. W.; HEMINGWAY, J.; COLLINS, F. H. 2002b. Molecular analysis of multiple Cytochrome P450 genes from the malaria vector Anopheles gambiae. Insect Molecular Biology 11 (5): 409-418. [ Links ]
RAYMOND, M.; CALLAGHAN, A.; FORT, P.; PASTEUR, N. 1991. Worldwide migration of amplified insecticide resistance genes in mosquitoes. Nature 14; 350: 151-3. [ Links ]
RAYMOND, M.; CHEVILLON, C; GUI-LLEMAUD, T.; LENORMAND, T: PASTEUR, N. 1998. An overview of the evolution of overproduced esterases in the mosquito Culex pipiens. Philosophical Transaccions of the Royal Society of London. Series B, Biological Sciences 353; 1707-1711. [ Links ]
REISS, R. A.; JAMES, A. A. 1993. A glutathion S-transferase gene of the vector mosquito Anopheles gambiae. Insect Molecular Biology 2: 25-32. [ Links ]
ROSE, R. L.; GOH. D.; THOMPSON, D. M.; VERMA, K. D.; HECKEL, D. G.; GAHAN, L. J.; ROE. R. M.; HODGSON, E. 1997. Cytochrome P450 CYP9A1. Heliothis virescens: the first member of a new CYP family. Insect Biochemistry and Molecular Biology 27:605-615. [ Links ]
SALINAS, A. E.; WONG, M. G. 1999. Glutathione S-transferases - a review. Current Medicinal Chemistry 6:279-309. [ Links ]
SCHULER,T. H.; MARTINEZ-TORRES, D.; THOMPSON, A. J.; DENHOLM, I.; DEVONSHIRE, A. L.; DUCE, I. R.; WILLIAMSON, M. S. 1998. Toxico-logical,electrophysiological, and molecular characterization of knockdown resistance to pyrethroid insecticides in the dia-mondback moth, Plutella xylostella (L.). Pesticide Biochemistry and Physiology 59: 169-182. [ Links ]
SCOTT, J. G. 1999. Cytochromes P450 and Insecticide Resistance. Insect Biochemistry and Molecular Biology 29:757-777. [ Links ]
SCOTT, J. G.; WEN, Z. 2001. Cytochromes P450 of insects: the tip of the iceberg. Pest Management Science 57: 958-967. [ Links ]
SEVERINI, C. ; ROMI, R.; MARINUCCI, M.; GUILLEMAUD, T; RAYMOND, M. 1997. Esterases A5-B5 in organophos-phate-resistant Culex pipiens from Italy. Medical and Veterinary Entomology 11: 123-126. [ Links ]
SHARF M. E.; PARIMI, S.; MEINKE, L. J.; CHANDLER, L. D.; SIEGFRIED, B. D. 2001. Expression and induction of three family cytochrome P450 genes identified from insecticide-resistant and susceptible western corn rootworms. Insect Molecular Biology 10: 139-146. [ Links ]
SHEEHAN, D.; MEADE, G.; FOLEY, V. M.; DOWD, C. A. 2001. Structure, function and evolution of glutathione transferase: implications for classification of non mammalian members of an ancient enzyme superfamily. The Biochemical Journal 360: 1-16. [ Links ]
SODERLUND, D. M.; BLOOMQUIST, J. R. 1989. Neurotoxic accion of pyrethroid insecticides. Annual Review of Entomology 34: 77-96. [ Links ]
SUAREZ, M. F; QUINONES, M. L.; PALACIOS, J. D.; CARRILLO, A. 1990. First Record of DDT Resistance in Anopheles darlingi. Journal of the American Mosquito Control Association 6:72-74. [ Links ]
TABASHNIK, B.E. 1990. Implications of gene amplification for evolution and management of insecticide resistance. Journal of Economic Entomology 83: 1170-1176. [ Links ]
THOMPSON, M.; SHOTKOSKI, F.: FFRENCH-CONSTANT, R.H. 1993. Cloning and sequencing of the cyclodiene insecticide resistance gene from the yellow fever mosquito Aedes aegypti. FEBS Letters (Netherlands). 325: 187-190. [ Links ]
TIJET, N.; HELVIG, C; FEYEREISEN, R. 2001. The cytochrome P450 gene superfamily in Drosophila melanogaster: annotation, intron-exon organization and phylogeny. Gene 262:189-198. [ Links ]
TOUNG, Y-P. S.; HSIEH, T; TU, C-P. D. 1993. The glutathione S-transferase D genes: a divergently organized, intronless gene family in Drosophila melanogaster. The Journal of Biological Chemistry 268: 9737-9746. [ Links ]
TURNER, A.; DOYLE, W. A.; VENTOM, A. M.; BRAY, R. C. 1995. Properties of rabbit liver aldehyde oxidase and the relationship of the enzyme to Xanthine Oxidase and dehydrogenase. European Journal of Biochemistry 232:646-657. [ Links ]
VAIS, H.; WILLIAMSON, M. S.; DEVONSHIRE, A. L.; USHERWOOD, P. N. R. 2001. The molecular interaccions of pyrethroid insecticides with insect and mammalian sodium channels. Pest Management Science 57:877-888. [ Links ]
VATANDOOST, H.; MCCAFFERY, A. R.; TOWNSON, H. 1996. An electrophysiological investigation of target site insensivity mechanisms in permethrin-resistant and susceptibility strains of Anopheles stephensi. Transaccions of the Royal Society of Tropical Medicine and Hygiene 90: 216. [ Links ]
VAUGHAN, A.; HAWKES, N.; HEMINGWAY, J. 1997. Co-amplification explains linkage disequilibrium of two mosquito esterase genes in insecticide resistance Culex quinquefasciatus. The Biochemical Journal 325: 359-365. [ Links ]
VAUGHAN, A.; CHADEE, D. D.; FFRENCH-CONSTANT, R. H. 1998. Biochemical monitoring of organophosphorus and carbamate insecticide resistance in Aedes aegypti mosquitos from Trinidad. Medical and Veterinary Entomology 12:318-321. [ Links ]
VONTAS, J. G.; SMALL. G. J.; HEMINGWAY, J. 2001. Glutathione S-transferase as antioxidant defense agents confers pyrethroid resistance in Nilaparvata lugens. The Biochemical Journal 357:365-372. [ Links ]
VONTAS, J. G.; HEJAZI, M. J.; HAWKES. N. J.; COSMIDIS, N.; I.OUKAS, M.; HEMINGWAY, J. 2002. Resistance-associated point mutations of organophosphate insensitive acetylcholinesterase in the olive fruit fly Bactrocera oleae. Insect Molecular Biology 11:329-336. [ Links ]
WALSH, S. B.; DOLDEN, T. A.; MOORES, G. D.; KRISTENSEN, M.; LEWIS, T; DEVONSHIRE, A. L.; WILLIAMSON, M. S. 2001. Identification and characterization of mutations in house fly (Musca domestica) acetylcholinesterase involved in insecticide resistance. The Biochemical Journal 359: 175-181. [ Links ]
WHO. 1975. Manual on Practical Entomology in Malaria. Part II. Methods and Techniques. World Health Organization, Geneva. [ Links ]
WHO. 1981. Resistance of vectors and reservoirs of disease to pesticides. WHO Technical Report Series No 737, 87 pp. World Health Organization, Geneva. [ Links ]
WHO. 1992. Vector resistance to pesticides. Fifteenth report of the expert committee on vector biology and control. WHO Technical Report Series No 818,55 pp World Health Organization, Geneva. [ Links ]
WILLIAMSON, M. S.; DENHOLM, I.; BELL, C. A.; DEVONSHIRE, A. L. 1993. Knockdown resistance (kdr) to DDT and pyrethroid insecticides maps to a sodium channel gene locus in the housefly (Musca domestica). Molecular and General Geneties 240: 17-22. [ Links ]
WILLIAMSON, M. S.; MARTINEZ-TORRES, D.; HICK, C. A.; DEVONSHIRE, A. L. 1996. Identification of mutations in the housefly para-type sodium channel gene associated with knockdown resistance (kdr) to pyrethroids insecticides. Molecular and General Geneties 252:51 -60. [ Links ]
ZHOU, Z. H.; SYVANEN, M. 1997. A complex glutathione transferase gene family n the housefly Musca domestica. Molecular and General Geneties 256: 187-194. [ Links ]