Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Medica Colombiana
Print version ISSN 0120-2448
Acta Med Colomb vol.49 no.4 Bogotá Oct./Dec. 2024 Epub Nov 21, 2024
https://doi.org/10.36104/amc.2024.3259
Presentación de Casos
Entrelazo vascular. Síndrome de May-Thurner como causante de tromboembolia venosa
a Dr. Eduard Orlando Vargas-Plazas: Residente de Medicina Interna, Universidad Libre
b Dra. Milena Luz Reales-Acuña y Dra. Olivia Del Carmen Silva-Sánchez: Médicas Especialistas en Medicina Interna, Organización Clínica General del Norte-Zentria
c Dr. Luis Antonio Díaz-Ariza: Médico Especialista en Medicina Interna y Epidemiología. Barranquilla (Colombia)
d Dra. María Paula Caro-Angulo: Médica Especialista en Epidemiólogía, Villavicencio (Colombia)
El síndrome de May-Thurner (SMT), también llamado síndrome de Cockett, es una condición anatomopatológica que conduce a obstrucción del flujo venoso debido a compresión externa en la zona venosa iliocava, por parte de la arteria ilíaca común derecha (AICD o RICA en inglés) y la columna lumbar inferior, generalmente a nivel de la quinta vértebra lumbar. Puede ser asintomática y desapercibida durante la vida, o causar morbilidad vascular, incluyendo trombosis venosa profunda (TVP), descrita sobre todo en mujeres en etapa fértil.
Se reporta caso de una mujer añosa, con diagnóstico de TVP no provocado, hallazgo de Tromboembolismo Pulmonar (TEP) en estudios complementarios y de trombosis en vena iliaca y vena ileofemoral izquierda. Se sospechó SMT a través de una angiotomografía toracoabdominal, la cual se confirmó por estudio endovascular, seguido de tratamiento por misma vía y manejo médico. El reporte destaca una causa subdiagnosticada de TEV en un grupo etario inusual. (Acta Med Colomb 2024; 49. DOI: https://doi.org/10.36104/amc.2024.3259).
Palabras clave: síndrome de May-Thurner; síndrome de Cockett; síndrome venoso compresivo; trombosis venosa profunda; tromboembolismo pulmonar
May-Thurner syndrome (MTS), also known as Cockett's syndrome, is an anatomical-pathological condition that leads to obstructed venous flow due to external compression on the iliocaval venous area by the right common iliac artery (RCIA) and the lower lumbar spine (usually the 5th lumbar vertebra). It can be asymptomatic and undetected throughout life or cause vascular morbidity, including deep vein thrombosis (DVT), especially reported in women of reproductive age. We report the case of an older woman diagnosed with an unprovoked DVT, a pulmonary thromboembolism (PTE) found on complementary tests and thromboses of the iliac and left iliofemoral veins, with suspected MTS on thoracoabdominal angiography tomography. This was confirmed through an endovascular study and treated endovascularly and medically. This report highlights an underdiagnosed cause of VTE in an unusual age group. (Acta Med Colomb 2024; 49. DOI: https://doi.org/10.36104/amc.2024.3259).
Keywords: May-Thurner syndrome; Cockett's syndrome; venous compression syndrome; deep vein thrombosis; pulmonary thromboembolism
Introducción
La tromboembolia venosa (TEV) es una entidad que interrelaciona la trombosis venosa profunda (TVP) y el tromboembolismo pulmonar (TEP). Aunque usualmente a la TVP ocurre en extremidades inferiores, puede presentarse también en el lecho esplácnico, miembros superiores y a nivel cerebral 1. Es una patología frecuente afecta a 10 millones de personas por año (1-2 casos por cada 1000 personas) en el mundo, siendo la tercera causa principal de enfermedad cardiovascular, después de la cardiopatía isquémica y la enfermedad cerebro vascular 2. La incidencia global está creciendo junto con la expectativa de vida; de hecho, a partir de los 45 años, el riesgo de presentar TEV es de 8% 3. El incremento de comorbilidades asociadas (como la obesidad, insuficiencia cardíaca, cáncer, etc.), junto con el mayor uso de pruebas imagenológicas, aumentan detección de TEV 4.
La probabilidad de cursar TEV no varía según sexo, aunque puede ser dos veces mayor en hombres que en mujeres, excluyendo causas relacionadas al embarazo y la terapia estrogénica 5. Las causas han sido delimitadas de múltiples maneras. Recientemente, se ha instado a identificar factores etiológicos provocadores y/o desencadenantes en últimos tres meses, tales como inmovilización, traumatismo, cirugía, cáncer, etc. Por otro lado, los eventos embólicos no provocadas ocurren en ausencia de estos sucesos 1. Entre un tercio a la mitad de los episodios de TEV no tienen un factor desencadenante identificable y, por tanto, permanecen como no provocados 6. La alteración de alguno de los tres factores descritos por Virchow desde 1856 con su triada (daño endotelial, estasis sanguínea e hipercoagulabilidad), ayuda a la identificación etiopatogénica 7.
En 1957, R. May y J. Turner, describieron una condición anatómica que presentaba las tres alteraciones descritas por Virchow 8. Cockett y Thomas, lo representaron clínicamente en 1965. El Síndrome de May-Thurner (SMT) se describe como una compresión de la vena ilíaca común izquierda (VICI) por la arteria ilíaca común derecha (AICD), contra la quinta vértebra lumbar, lo que puede causar obstrucción del flujo venoso y provocar dolor en la extremidad inferior izquierda, edema y TVP 9. De forma más anecdótica, puede comprometer la vena ilíaca derecha o incluso ser bilateral 10. Es prevalente en mujeres (5:1), generalmente en edad reproductiva 11. La incidencia y prevalencia del SMT son desconocidas y su subdiagnóstico es común, aunque corresponde a 2-5% de los casos de TVP (9). No existen criterios de diagnósticos estandarizados. Las imágenes diagnósticas tienen un papel fundamental en la identificación, en pacientes con signos y síntomas sugestivos 12. A continuación, se describe caso inusual de una mujer añosa con reporte imagenológico compatible con la entidad.
Presentación de caso
Mujer de 71 años que acudió a urgencias por dolor y edema duro de miembro inferior izquierdo, de inicio súbito, condicionando limitación funcional. En revisión por sistemas, indicaba que tres días atrás presentó dolor en hemitórax derecho, de características pleuríticas, intensidad moderada, sin disnea, palpitaciones, ortopnea, fiebre y/o pérdida de peso. Como antecedentes patológicos destaca diabetes mellitus tipo 2, tratada con insulina glargina, glulisina y dapagliflozina, además de insuficiencia venosa crónica sin seguimiento ni tratamiento, además de ceguera bilateral por glaucoma. No tenía antecedentes quirúrgicos, alérgicos o exposicionales de importancia. Su última hospitalización fue hace seis años por infección de vías urinarias que generó cetoacidosis diabética. Negaba abortos o mortinatos en antecedentes ginecobstétricos (G3P3).
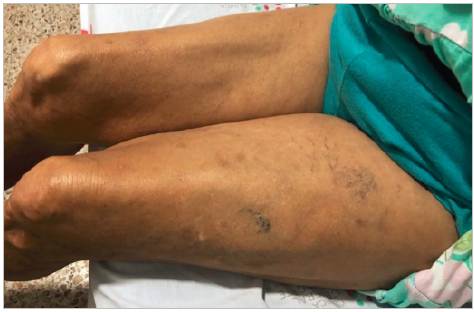
Al ingreso los signos vitales fueron normales. En el examen físico, a nivel de tórax, no se palparon nódulos en mamas. En extremidades inferiores, se evidenciaba asimetría por edema en miembro inferior izquierdo, de predominio crural, con telangiectasias (Figura 1). Los signos de Homans y Pratts fueron positivos en dicho miembro. Pulsos poplíteos y pedios preservados.
Los paraclínicos iniciales reportaron hemograma, electrolitos y pruebas de función renal sin alteraciones, destacando solo glicemia central al azar (319 mg/dL) y los niveles elevados de proteína C reactiva (PCR) de 7.19 mg/dL (rango de referencia 0-0.5). El electrocardiograma no mostró taquicardia, sin datos de sobrecarga de cavidades ni signos de lesión, isquemia o necrosis. La troponina T fue negativa (0.009 ng/ mL, referencia 0-0.0014).
Se realizó doppler venoso de miembros inferiores, confirmando a nivel de la vena femoral común, la presencia de material trombótico oclusivo. Se hospitalizó con diagnóstico de TVP no provocada y se inició tratamiento con enoxaparina ajustada a 1 mg/Kg (50 IT subcutánea cada 12 horas), se ajustó el manejo insulínico y se solicitaron estudios complementarios.
Se realizaron tomografías contrastadas (TC) en tórax y abdomen. El estudio de tórax mostró asimetría al realce del parénquima basal derecho y área de hipoperfusión hacia el aspecto medial de atelectasia ipsilateral, concluyente con TEP agudo en arteria segmentaria basal posterior derecha con aparente infarto basal posterior ipsilateral (Figura 2).
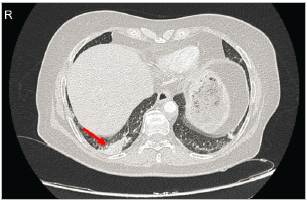
Figura 2 Corte axial de TC torácico contrastado, evidenciando área de hipoperfusión basal derecha (flecha blanca), concluyente para TEP agudo de arteria segmentaria basal posterior derecha con aparente infarto basal posterior derecho.
En la TAC de abdomen, se observó un incremento del calibre de la vena iliaca común izquierda que se extiende hacia la vena ileofemoral ipsilateral. Llamó la atención la aparente disminución de la luz de vena iliaca común por debajo de la AICD, evidenciando un trombo mural hacia confluencia de venas iliacas en vena cava inferior, concluyendo en trombosis de vena iliaca y vena ileofemoral izquierda, con sospecha de síndrome de May-Thurner (SMT) (Figuras 3a y 3b).
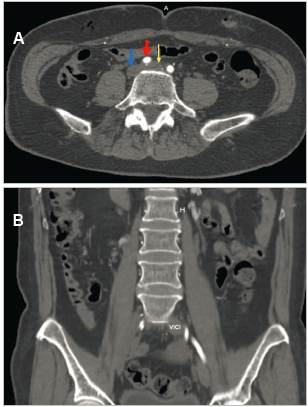
Figura 3 A (Arriba): compresión de vena iliaca común izquierda (flecha amarilla) por la arteria iliaca común derecha (flecha roja), condicionando dilatación de la vena (16 mm), con trombos murales en el interior. Vena cava inferior (flecha azul). B (Abajo): corte coronal abdomino-pélvico, evidencia trombosis de la vena iliaca común izquierda (VICI), con aumento de diámetro respecto a contralateral.
Se realizaron marcadores tumorales de screening (Alfa-fetoproteína -AFP-, antígeno carcinoembrionario - ACE-, CA 125, CA 19-9), dentro de rangos normales. Las pruebas de autoinmunidad negativos (anticuerpos antinucleares -ANA-, anti SCL 70, anti-centrómero, anti Beta2 glicoproteína -IgM/ IgG- y factor reumatoide), niveles de complemento C3 y C4 sin alteraciones. La prueba de tamizaje para anticoagulante lúpico se encontraba prolongado según el rango de referencia (48.8 con control de 34.9), con tiempos de coagulación sin alteraciones. El uroanálisis descartó presencia de proteinuria.
El ecocardiograma transtorácico mostró hipertrofia concéntrica leve de ventrículo izquierdo (VI) con función sistólica conservada y disfunción diastólica tipo I (Fracción de eyección del VI -FEVI-) de 62%, ventrículo derecho con función sistólica conservada, sin signos indirectos de hipertensión pulmonar.
Se solicitó intervencionismo endovascular, reportando oclusión completa y múltiples colaterales de aspecto crónico a nivel de la femoral común e iliaca primitiva en su extensión izquierda, compatible con oclusión crónica secundaria a compresión vascular, compatible con síndrome de May-Turner (SMT). Se decidió no realizar tromboembolectomía y, en su lugar, se repararon vasos de mediano calibre con recanalización a través de guía hidrofílica Stiff y catéter multipropósito, realizándose angioplastia con Stent venoso de 12x100mm, logrando adecuada permeabilidad a nivel de la vena iliaca común izquierda.
La paciente ingresa a la unidad de cuidados intensivos para vigilancia, trasladándose a las 24 horas a sala general por evolución satisfactoria, manteniendo doble antiagregación (ácido acetilsalicílico tableta 100 mg y clopidogrel tableta 75 mg cada 24 horas vía oral) y anticoagulación (enoxaparina 60 mg cada 12 horas subcutánea) por siete días. Posteriormente, fue dada de alta con antiagregante oral (clopidogrel) y anticoagulante directo (rivaroxabán) por tiempo indefinido y condicionado a seguimiento ambulatorio por cirugía vascular, cardiología y medicina interna.
Discusión
El SMT afecta predominantemente a mujeres entre la tercera y quinta década de vida, con pocos casos fuera de estos rangos 13. La enfermedad puede tener un curso asintomático, o presentar característicamente, dolor y edema en miembro inferior (usualmente izquierdo), claudicación y progresión hacia insuficiencia venosa crónica, manifiesta en cambios de coloración en piel y venas varicosas 14 (Figura 1). En el caso descrito, la paciente tenía antecedentes de insuficiencia venosa crónica no estudiada ni tratada. A pesar de no referir datos de síndrome constitucional, se solicitaron imágenes tomográficas apuntando inicialmente a causa neoplásica, con hallazgo de TEP de bajo riesgo y alteración estructural-anatómica a nivel vascular ilíaco, altamente sugestiva para SMT.
El SMT resulta de la compresión de la VICI por parte de la AICD, ubicada justo después de su origen en aorta abdominal y antes de unión con la vena ileofemoral. La presión permanente ejercida por la arteria provoca compresión de la vena contra estructuras óseas, comúnmente vértebras lumbares inferiores, dando lugar a la formación de "espolones" o estenosis a nivel venoso. Aunque la afectación izquierda es la más frecuente como nuestro caso, también es posible compromiso venoso contralateral en menor frecuencia 15.
El diagnóstico de esta entidad es principalmente imagenológico. De forma inicial, se emplea la ecografía doppler para visualizar defecto vascular a nivel de la vena ilíaca común; sin embargo, por profundidad anatómica y depender de operador, la sensibilidad es de apenas 47% 16. En nuestro caso, el diagnóstico se realizó mediante tomografía de vasos abdominopélvicos. Los hallazgos se pueden confirmar con ultrasonido intravascular (Intravascular Ultrasound -IVUS-), considerado recientemente como el posible estándar de oro. Este permite evaluar la presencia de trombos en luz vaso y caracterizarlos, ayudando a definir el requerimiento de manejo trombolítico. Adicionalmente, favorece la selección adecuada del Stent mediante medición de diámetros luminales e identificación de confluencia de vena iliaca 12.
En el tratamiento es fundamental la anticoagulación; un retraso en su inicio se encuentra asociado a mayor riesgo de TEP, evento que se presentó en el caso. Se sugiere continuar anticoagulación posterior a la terapia endovascular, durante 6 - 12 meses para prevenir un nuevo evento tromboembólico 16. No existe preferencia de un anticoagulante sobre otro. Las heparinas gozan de igual eficacia en comparación a anticoagulantes cumarínicos u orales directos (ACOD), por lo que pueden emplearse 17. Prácticamente, la elección de la anticoagulación estará regida de acuerdo al manejo individualizado, teniendo en cuenta aspectos como el escenario clínico, tasa de filtración glomerular (TFG), disponibilidad y riesgo de sangrado individual de cada paciente 18.
Se prefiere comúnmente la combinación de tratamiento endovascular (mediante trombectomía, trombólisis y/o angioplastia con colocación de Stent) junto con anticoagulación, en lugar de depender únicamente del manejo farmacológico en pacientes sintomáticos 12, reportándose tasas de TEV en terapia combinada menores de 10% versus 80-90% con solo tratamiento médico (19). En nuestro reporte, no se realizó tromboembolectomía por cambios crónicos endovasculares, optándose por reparación y recanalización a través de angioplastia con Stent en colaterales. Una vez realizado el manejo endovascular, los pacientes deben recibir terapia antiagregante preferiblemente con clopidogrel por seis semanas a tres meses y aspirina a dosis bajas de manera indefinida, con seguimiento periódico mediante ecografía o venografía por tomografía para confirmar permeabilidad del Stent 14.
Conclusión
El artículo remarca la importancia de considerar el SMT como causa subdiagnosticada de TEV, inclusive en grupos etarios inusuales, teniendo en cuenta que suelen existir antecedentes de insuficiencia venosa previa, muchas veces desapercibida. El abordaje de las causas, tomando en cuenta las condiciones de riesgo para TEV (triada de Virchow) puede ser claves. La identificación oportuna de la condición, respaldada por imágenes diagnósticas, es crucial para un manejo adecuado, que requiere combinar tratamiento médico (anticoagulantes) y endovascular, con menor tasa de síndrome postrombótico. No existe consenso de tratamiento respecto a anticoagulante y antiagregantes, por lo que deberá hacerse de manera individualizada, teniendo en cuenta guías o recomendaciones locales.
References
1. Lutsey PL, Zakai NA. Epidemiology and prevention of venous thromboembolism. Nat Rev Cardiol. 2023;20(4):248-62. doi: 10.1038/s41569-022-00787-6. [ Links ]
2. Khan F, Tritschler T, Kahn SR, Rodger MA. Venous thromboembolism. Lancet. 2021;398(10294):64-77. doi: 10.1016/S0140-6736(20)32658-1 [ Links ]
3. Bell EJ, Lutsey PL, Basu S, Cushman M, Heckbert SR, Lloyd-Jones DM, et al. Lifetime Risk of Venous Thromboembolism in Two Cohort Studies. Am J Med. 2016;129(3):339.e19-26. doi: 10.1016/j.amjmed.2015.10.014. [ Links ]
4. Di Nisio M, van Es N, Büller HR. Deep vein thrombosis and pulmonary embolism. Lancet. 2016;388(10063):3060-73. doi: 10.1016/S0140-6736(16)30514-1. [ Links ]
5. Roach REJ, Lijfering WM, Rosendaal FR, Cannegieter SC, le Cessie S. Sex difference in risk of second but not of first venous thrombosis: paradox explained. Circulation. 2014;129(1):51-6. doi: https://doi.org/10.1161/CIRCULATIONAHA.113.004768 [ Links ]
6. Kearon C, Ageno W, Cannegieter SC, Cosmi B, Geersing GJ, Kyrle PA, et al. Categorization of patients as having provoked or unprovoked venous thromboembolism: guidance from the SSC of ISTH. Journal of Thrombosis and Haemostasis. 2016;14(7):1480-3. doi: https://doi.org/10.1111/jth.13336 [ Links ]
7. Wolberg AS, Rosendaal FR, Weitz JI, Jaffer IH, Agnelli G, Baglin T, et al. Venous thrombosis. Nat Rev Dis Primers. 2015;1(1):15006. doi: https://doi.org/10.1038/nrdp.2015.6 [ Links ]
8. Matos ML, Matos MITS, Grijó CMSPM, Patacho MFS, Almeida AJS. May-Thurner syndrome: a case report. Porto Biomed J. 2023;8(4):e224. doi: 10.5152/eajm.2011.29 [ Links ]
9. Harbin MM, Lutsey PL. May-Thurner syndrome: History of understanding and need for defining population prevalence. J Thromb Haemost. 2020;18(3):534-42. doi: https://doi.org/10.1111/jth.14707 [ Links ]
10. Radaideh Q, Patel NM, Shammas NW. Iliac vein compression: epidemiology, diagnosis and treatment. Vasc Health Risk Manag. 2019;15:115-22. doi: 10.2147/VHRM.S203349. [ Links ]
11. Zucker EJ, Ganguli S, Ghoshhajra BB, Gupta R, Prabhakar AM. Imaging of venous compression syndromes. Cardiovasc Diagn Ther. 2016;6(6):519-32. doi: 10.21037/cdt.2016.11.19. [ Links ]
12. Knuttinen MG, Naidu S, Oklu R, Kriegshauser S, Eversman W, Rotellini L, et al. May-Thurner: diagnosis and endovascular management. Cardiovasc Diagn Ther . 2017;7(Suppl 3):S159-64. doi: 10.21037/cdt.2017.10.14. [ Links ]
13. Xu J, Alach A, Behseresht J, Hsu J, Tayyarah M, Vo T, et al. May-Thurner syndrome is not only a left-sided condition-Consideration of venous anatomical variations. Annals of Vascular Surgery - Brief Reports and Innovations. 2023;3(4):100235. doi: https://doi.org/10.1016/j.avsurg.2023.100235 [ Links ]
14. Poyyamoli S, Mehta P, Cherian M, Anand RR, Patil SB, Kalva S, et al. May-Thurner syndrome. Cardiovasc Diagn Ther . 2021;11(5):1104-11. doi: 10.21037/cdt.2020.03.07 [ Links ]
15. Abboud G, Midulla M, Lions C, El Ngheoui Z, Gengler L, Martinelli T, et al. «Right-sided» May-Thurner syndrome. Cardiovasc Intervent Radiol. 2010;33(5):1056-9. doi: https://doi.org/10.1016/jjvscit2021.10.005 [ Links ]
16. Hng J, Su S, Atkinson N. May-Thurner syndrome, a diagnosis to consider in young males with no risk factors: a case report and review of the literature. J Med Case Rep. 2021;15(1):141. [ Links ]
17. Franchini M, Mannucci PM. Direct oral anticoagulants and venous thrombo-embolism. European Respiratory Review. 2016;25(141):295-302. doi: 10.1186/s13256-021-02730-8. [ Links ]
18. Salahuddin T, Armstrong EJ. Intervention for Iliofemoral Deep Vein Thrombosis and May-Thurner Syndrome. Interv Cardiol Clin. 2020;9(2):243-54. doi: 10.1016/j.iccl.2019.11.003. [ Links ]
19. Armenta Flores R, Armenta-Villalobos D, Ramirez-Centeno E, Harrison-Ragle D, Carrillo LGD. May Thurner syndrome: Sixty years later. Phlebology. 2022;37(1):5-13. doi: 10.1177/02683555211045202. [ Links ]
Recibido: 16 de Mayo de 2024; Aprobado: 02 de Septiembre de 2024











 text in
text in