Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biomédica
Print version ISSN 0120-4157On-line version ISSN 2590-7379
Biomédica vol.24 no.2 Bogotá June 2004
Anticuerpos anti-CCP en artritis reumatoidea: relación con características clínicas, citocinas Th1/Th2 y HLA-DRB1
Paula A. Correa 1,2, Gabriel J. Tobón 1,2, Gustavo Citera 3, José Cadena 1, Emilce Schneeberger 3, José F. Camargo 1, José A. Maldonado-Cocco 3, Juan Manuel Anaya 1,2
1 Unidad de Biología Celular e Inmunogenética, Corporación para Investigaciones Biológicas, Medellín, Colombia.
2
Clínica Universitaria Bolivariana, Facultad de Medicina, Universidad Pontificia Bolivariana, Medellín, Colombia.3
Instituto de Rehabilitación, Buenos Aires, Argentina.En el presente estudio se examinó la especificidad y la sensibilidad de los anticuerpos antipéptidos citrulinados cíclicos (CCP) en pacientes latinoamericanas con artritis reumatoidea (AR), así como su relación con la actividad de la enfermedad, manifestaciones extraarticulares (MEA), síntesis de citocinas (IL-4, IL-10, IL-12, TNF-
µ e IFN-g ) y factor reumatoideo (FR) IgM e IgA, y con el polimorfismo del HLA-DRB1. Se examinaron 79 pacientes con AR (69 con AR establecida y 10 con AR temprana sin previo tratamiento), 56 pacientes con espondilitis anquilosante (EA), 25 con lupus eritematoso sistémico (LES), 50 con síndrome de Sjögren primario (SSp) y diez individuos sanos. De las 69 pacientes con AR establecida, 36 fueron reevaluadas 2 años después. La actividad de la AR se examinó según los criterios del Colegio Americano de Reumatología. Los anticuerpos anti-CCP2, el FR y los niveles de citocinas se determinaron mediante inmunoensayo, y la genotipificación del HLA se llevó a cabo por reacción en cadena de la polimerasa utilizando mezclas de iniciadores específicos. Los anticuerpos anti-CCP se observaron en 96% de los pacientes con AR en la primera evaluación y en 86% en la segunda ( p=0,12), sin modificación significativa en los valores (131±58,7 vs. 130,6±67,1 UI). Su sensibilidad y especificidad global fue de 94% y 92%, respectivamente, pero cuando sólo se consideraron los niveles altos (>60 UI) fueron de 84% y 95%, respectivamente. La razón de probabilidades (RP) positiva fue de 12 y la RP negativa de 0,06. El valor predictivo (VP) positivo fue de 87% y el VP negativo de 96%. Los anticuerpos anti-CCP se observaron en 12% de los pacientes con LES y con SSp, en 2% de los de EA y en 10% de los controles sanos. En los pacientes con AR no se asociaron con la actividad de la enfermedad, MEA y alelos del HLA-DRB1. Tampoco se observaron correlaciones significativas entre sus valores y los niveles de citocinas. En conclusión, los anticuerpos anti-CCP tienen un interés diagnóstico para la AR en nuestra población, pero su utilidad en el seguimiento clínico es limitada y su síntesis es independiente del HLA-DRB1 y no se correlacionan con niveles de citocinas Th1/Th2.Palabras clave: artritis reumatoidea, anticuerpos antipéptidos citrulinados cíclicos, factor reumatoideo, HLA-DRB1, citocinas, lupus eritematoso sistémico, síndrome de Sjögren, espondilitis anquilosante.
Anti-cyclic citrullinated peptide antibodies in rheumatoid arthritis: relation with clinical features, cytokines and HLA-DRB1
The specificity and sensitivity of anti-cyclic citrullinated peptide antibodies (anti-CCP) was examined in Latin-American patients with rheumatoid arthritis (RA). The variables considered included: 1) relation with the activity of disease, 2) extra-articular manifestations (EAM), 3) synthesis of cytokines (IL-4, IL-10, IL-12, TNF-
a , and IFN-g ) and IgM and IgA rheumatoid factor (RF), and 4) the association with HLA-DRB1 polymorphism. Seventy-nine RA patients were assessed (69 with established RA, and 10 with recent-onset RA not receiving any treatment), 56 with ankylosing spondylitis (AS), 25 with systemic lupus erythematosus (SLE), 50 with primary Sjögren's syndrome (pSS), and 10 healthy individuals. Of the 69 patients with established RA, 36 were reexamined 2 years later. The activity of the RA was measured by criteria adopted by the American College of Rheumatology. Anti-CCP2, RF and cytokines levels were determined by ELISA. HLA genotypes were established by first, PCR sequence amplification using sequence-specific primers and then, complete sequencing of the product. Anti-CCP antibodies were observed in 96% of patients with RA during the first evaluation and in 86% at the second evaluation ( p=0.12). No significant change in antibody titre was observed between the two evaluations (131±58.7 and 130.6±67.1 IU, respectively). The overall sensitivity and specificity was 94% and 92%, respectively; however, at titres >60 IU, the values were 84% and 95%, respectively. The anti-CCP likelihood ratio positive test was 12 and the likelihood ratio negative test was 0.06. The positive predictive value was 87%, and the negative predictive value was 96%. Anti-CCP antibodies were observed in 12% of SLE and pSS patients, in 2% of AS patients, and in 10% of healthy controls. In RA patients, these antibodies were not associated with the activity of disease, EAM or HLA-DRB1 alleles; no significant correlation was observed between antibody titre and cytokines level. Although anti-CCP antibodies have potential as a diagnostic tool for RA, they are not useful for monitoring clinical activity or predicting the clinical course of disease. Antibody synthesis is HLA-DRB1 independent and not correlated with Th1/Th2 cytokines.Key words: rheumatoid arthritis, anti-cyclic citrullinated peptide antibodies, rheumatoid factor, HLA-DRB1, cytokines, systemic lupus erythematosus, Sjögren's syndrome, ankylosing spondylitis.
La artritis reumatoidea (AR) es una enfermedad articular autoinmune, inflamatoria y crónica, que afecta principalmente a las mujeres. Frecuentemente compromete otros órganos distintos a las articulaciones y tiene un impacto adverso en la esfera biopsicosocial. Su causa es desconocida No obstante, se han identificado factores endocrinos, ambientales y genéticos involucrados en el desarrollo de la misma, los cuales son variables de una población a otra (1).
Se ha sugerido una variedad de autoantígenos como inductores de la respuesta autoinmune en la AR (2-5). Hasta hace poco, la determinación sérica del factor reumatoideo (FR), una inmunoglobulina dirigida contra la fracción constante (Fc) de las inmunoglobulinas de clase IgG, era la única prueba utilizada para el estudio de esta patología. De hecho, su presencia es considerada como criterio de clasificación de la enfermedad (6). Sin embargo, el FR no es altamente sensible ni específico (sensibilidad 66%; especificidad, 87%) (7), y puede encontrarse en otras enfermedades autoinmunes, enfermedades neoplásicas, infecciones crónicas e, incluso, en personas sanas.
Nienhuis y Mandema, en 1964, fueron los primeros en describir autoanticuerpos específicos en pacientes con AR, distintos al FR (8). El primero de este grupo de autoanticuerpos se denominó factor antiperinuclear (FAP), por dirigirse contra el factor perinuclear, un componente de los gránulos queratohialinos que rodean el núcleo de las células de la mucosa oral humana en diferenciación. Estos autoanticuerpos se reportaron como positivos muy temprano en el curso de la enfermedad, con una frecuencia de 49% a 91% y con una especificidad entre el 73% y el 99%, lo cual los convertía en posibles marcadores diagnósticos confiables (8). No obstante, dado que no todas las células de la mucosa oral humana expresan el sustrato antigénico y a que la prueba se realiza mediante inmunofluorescencia indirecta (IFI), en la cual los resultados dependen en gran parte del observador, su determinación cayó en desuso.
En 1979, Young et al. describieron, mediante IFI, otro tipo de autoanticuerpos que parecían ser específicos en AR (9). Éstos reaccionaban contra proteínas presentes en el epitelio estratificado del esófago de rata y se denominaron anticuerpos antiqueratina (AKA). Se reportaron como positivos en el 40% de los pacientes, con una alta especificidad. Incluso, se podían encontrar positivos antes del inicio de los síntomas osteoarticulares (10). En un estudio previo, observamos la presencia de AKA en el 61% de los pacientes con AR establecida (11).
El antígeno reconocido por los AKA y el FAP es el mismo y corresponde a la (pro)filagrina (12-16), la cual se expresa en diferentes sustratos (15). Por lo tanto, estos anticuerpos se denominan actualmente anticuerpos anti-filagrina o antiprofilagrina (17). La filagrina ( filament aggregating protein) es una proteína producida durante las fases finales de diferenciación de las células epiteliales de los mamíferos. Es sintetizada como un precursor proteico (profilagrina) que contiene entre 10 y 12 moléculas de filagrina (18). Posteriormente, se demostró que cerca del 20% del aminoácido arginina de la filagrina se convertía a citrulina por la enzima peptidil arginina deaminasa (PAD) (18). Este cambio pequeño, relacionado con la masa molecular, genera importantes cambios en la carga eléctrica, lo cual produce diferencias en la interacción de la proteína con otras moléculas. Además, la citrulina es esencial para el reconocimiento antigénico por los anticuerpos antifilagrina (19). No obstante, la AR no afecta los tejidos que contienen normalmente la filagrina, como la piel o la mucosa oral, y no se encuentra en la membrana sinovial. Sin embargo, la membrana sinovial de pacientes con AR está infiltrada por células plasmáticas productoras de anticuerpos antifilagrina, lo cual sugiere la presencia en dicho tejido de un autoantígeno reconocido por estos anticuerpos (19). En este sentido, se observaron en la membrana sinovial de los pacientes con AR proteínas intracelulares citrulinadas, que no eran reconocidas por anticuerpos monoclonales contra la filagrina, y no se encontraron en los controles (20). Recientemente, un estudio demostró la citrulinación de proteínas sinoviales en los modelos murinos de AR, como un proceso activo, debido a la presencia de PAD4, y sugirió que la inducción de autoanticuerpos contra estos nuevos antígenos (proteínas citrulinadas) es específica de los humanos (21). En resumen, las proteínas citrulinadas de la membrana sinovial, no relacionadas con la filagrina, podrían disparar respuestas autoinmunes en la AR.
Schellekens et al. desarrollaron una prueba de inmunoanálisis ligada a enzimas (ELISA) para la detección de anticuerpos contra péptidos cíclicos citrulinados derivados de la filagrina (anti-CCP1) (22). El estudio con este método reveló una sensibilidad del 68% y una especificidad del 98% en pacientes con AR (22). Como la filagrina no se expresa en la membrana sinovial, se escogieron posteriormente otros péptidos no relacionados con ella para mejorar la técnica, la cual se conoce como CCP2 (23). Su uso en población caucásica ha mostrado una sensibilidad que oscila entre el 66% y el 82% y una especificidad que oscila entre el 90% y el 98% (23,24). Por lo tanto, su determinación ha mostrado ser de interés diagnóstico (23-26). No obstante, su valor pronóstico es controvertido.
El objetivo del presente estudio fue evaluar la sensibilidad, la especificidad y los niveles de los anticuerpos anti-CCP2 en pacientes con AR, y examinar su relación con la actividad de la enfermedad y con sus características inmunogenéticas y fenotípicas (FR, alelos HLA, citocinas proinflamatorias y antiinflamatorias).
Materiales y métodos
Pacientes y controles
Se estudiaron 79 pacientes con AR (69 con enfermedad establecida y 10 con AR temprana, vistos en la primera consulta y que no habían recibido ningún tratamiento para su enfermedad). En todos los casos, las pacientes cumplieron los criterios de clasificación para AR (6). La actividad de la enfermedad en el momento del estudio se registró y evaluó de acuerdo con el número de articulaciones con sinovitis activa y los parámetros clínicos y biológicos sugeridos por el Colegio Americano de Reumatología, previamente descritos en detalle (27). De acuerdo con su actividad, la AR se clasificó como muy activa, moderadamente activa y en remisión (27).
Se incluyeron también 56 pacientes con espondilitis anquilosante (EA) definida (28), 25 pacientes con lupus eritematoso sistémico (LES) (29), 50 pacientes con síndrome de Sjögren primario (SSp) (30) y diez individuos sanos. Todos los pacientes con AR, LES, SSp e individuos sanos fueron mujeres atendidas en la Clínica Universitaria Bolivariana, en Medellín, Colombia. El 91% de los pacientes con EA fueron hombres atendidos en el Instituto de Rehabilitación, en Buenos Aires, Argentina. Esta investigación se llevó a cabo de acuerdo con la Resolución No 008430 de 1993 del Ministerio de Salud de la República de Colombia y se consideró como de riesgo mínimo. El estudio contó con la aprobación del comité de ética de la Corporación para Investigaciones Biológicas.
Determinación de anticuerpos anti-CCP
Las muestras de sangre se tomaron en el momento de la evaluación clínica, en horas de la mañana y sin ayuno. De éstas se obtuvo el suero, el cual se almacenó a -20o C hasta su procesamiento. La detección de anticuerpos anti-CCP2 se realizó mediante ELISA, utilizando el estuche Quanta Lite (Inova Diagnostics Inc., San Diego, CA, USA). En este estuche, la placa se encuentra sensibilizada con un péptido citrulinado cíclico. El suero de los pacientes, diluido 1:101, se agregó a los pozos por separado, lo que permitió que los anti-CCP presentes en dicho suero se unieran al antígeno inmovilizado. Luego, cada pozo se lavó con solución tamponada de fosfatos (PBS), eliminando los residuos de muestra y las uniones inespecíficas antígeno-anticuerpos, y se procedió a agregar un conjugado de anti-IgG humana marcado con enzima. Una segunda incubación le permitió a este conjugado unirse a los anticuerpos que se habían adherido previamente al pozo. Luego de lavar el conjugado no fijado, la actividad enzimática se midió agregando un sustrato cromogénico y se determinó por el cambio en la intensidad del color que se produjo. Los sueros se examinaron por duplicado, y la lectura se hizo en el lector Bio-Rad modelo 550, California, EE.UU. Los resultados se expresaron en unidades internacionales (UI) y se clasificaron de acuerdo con los títulos de la prueba, definidos por la curva de calibración y por las instrucciones de la casa comercial, así: negativo, si era menor de 30 UI; levemente positivo, entre 30 y 39 UI; moderadamente positivo, entre 40 y 59 UI, y fuertemente positivos cuando eran mayores de 60 UI. El valor negativo (<30 UI) se reconsideró luego de obtener el promedio más dos veces la desviación estándar del resultado observado en los controles sanos.
Se calcularon la sensibilidad, la especificidad, las razones de probabilidades y los valores predictivos de los anti-CCP de acuerdo con las fórmulas previamente descritas (31).
Determinación del FR
El FR IgA e IgM se analizó mediante ELISA utilizando los estuches Quanta Lite (Inova Diagnostics Inc., San Diego, CA, USA), según las instrucciones de la casa comercial. Los resultados se hicieron en el lector Bio-Rad modelo 550. Los valores inferiores a 20 UI se consideraron negativos tanto para el FR IgA como IgM.
Determinación de citocinas
Simultáneamente, en las mismas muestras en las que se determinaron los anti-CCP y el FR, se examinaron las concentraciones séricas de interleucina 4 (IL-4), 10 (IL-10), 12 (IL-12-p70-), factor de necrosis tumoral alfa (TNF-
a ) e interferón gamma (IFN-g ) mediante ELISA de captura, utilizando los reactivos OptEIA (Pharmingen, BD Biosciences, San Diego, California, USA), los cuales utilizan un anticuerpo monoclonal específico para cada citocina. Estos anticuerpos se fijan a cada uno de los pozos del plato (Nalgen Nunc International - Brand Products, Illinois, USA) con incubación de 12 horas a 4oC, y con el objeto de capturar la citocina de la muestra. Luego de eliminar el posible exceso de anticuerpo monoclonal, mediante lavado con 10 mM PBS, a pH 7,0 con 0,05% de Tween 20, se realizó el bloqueo de uniones inespecíficas adicionando el diluyente (10 mM PBS, pH 7,0 con 10% de suero bovino fetal) e incubando durante una hora a temperatura ambiente. Posteriormente, se agregó suero total (100 µl) de pacientes a los pozos, y se incubó durante dos horas a temperatura ambiente. Luego de lavar los pozos, se agregó un segundo anticuerpo específico por cada citocina humana, esta vez conjugado con peroxidasa de rábano, y se incubó durante una hora más. Finalmente, se reveló la unión antígeno-anticuerpo con el sustrato (ABTS Chromogen/Substrate Solution for ELISA, Zymed Laboratories, San Francisco, California, USA). La reacción se detuvo con 0,01% de azida de sodio en 0,1 M de ácido cítrico. La lectura de los platos se realizó en los 30 minutos siguientes, a una longitud de onda de 415 nm en el lector Bio-Rad modelo 550. Se realizaron los controles apropiados de calidad, según las instrucciones del estuche. Los valores se determinaron por regresión lineal teniendo en cuenta la absorbancia y las concentraciones en pg/ml de las soluciones estándar.Determinación de HLA
Los alelos HLA-DRB1 se determinaron en AND genómico usando la técnica de reacción en cadena de polimerasa, con iniciadores específicos (UCLA HLA-DR, UCLA Tissue Typing Laboratory, Los Angeles, CA, USA), tal como se describió anteriormente (11). Se evaluó la presencia del epítopo compartido, que corresponde a las secuencias de aminoácidos en las posiciones 70 a 74 de la cadena â del HLA-DRB1 (11).
Análisis estadístico
Los resultados individuales se recolectaron y analizaron con el paquete SPSS versión 9.05 para Windows (Chicago, IL). Se utilizaron porcentajes y medidas de tendencia central para describir las variables, cuyos resultados se reportan en promedios y desviaciones estándar, o en mediana y rango intercuartil, dependiendo de su distribución, la cual se evaluó mediante la prueba de Kolmogorov-Smirnov.
Las diferencias entre los promedios se examinaron mediante la prueba de Mann-Whitney a dos colas, y aquéllas entre porcentajes mediante las pruebas de ÷2 o Fisher a dos colas. Las diferencias entre los niveles de anticuerpos anti-CCP en las dos evaluaciones realizadas se examinaron mediante la prueba t pareada. Las correlaciones entre los niveles de citocinas, autoanticuerpos y la duración de la enfermedad se calcularon mediante la prueba de Spearman a dos colas. En todos los casos, el valor de p<0,05 se consideró significativo.
Resultados
Se realizaron tres determinaciones de anticuerpos anti-CCP en pacientes con AR. En la primera evaluación se examinaron los anticuerpos anti-CCP en 69 pacientes con AR establecida, de las cuales en 66 (96%) fueron positivos, así: 4 (5,8%) positivos bajos (rango: 31-36 UI), 4 (5,8%) moderados (rango: 43-55 UI) y 58 (84,1%) positivos altos (rango: 68-222 UI). En 3 (4,3%) pacientes fueron negativos (7, 9 y 15 UI, respectivamente).
En una segunda oportunidad (intervalo de 2 años), se evaluaron 36 de las 69 pacientes del grupo inicial, de las cuales en 31 (86%) los anti-CCP fueron positivos. En estas últimas pacientes, 25 (81%) tuvieron niveles altos. No hubo diferencia significativa entre la sensibilidad de los anti-CCP en las dos mediciones ( p=0,12), como tampoco en sus niveles (131±58,7 vs. 130,6±67,1 UI, p=0,6). Las características generales de estas pacientes y los resultados obtenidos se muestran en el
cuadro 1.
Se evaluaron también 10 pacientes con AR temprana (atendidos por primera vez luego de la presentación de los síntomas), en quienes la seropositividad para anti-CCP fue de 80%, en todos los casos con valores positivos altos (rango: 77-168). Los niveles negativos de las dos pacientes en este grupo fueron 15 y 24 UI, respectivamente.
De los 56 pacientes con EA, sólo uno presentó anticuerpos anti-CCP (53 UI) ( p<0,001 comparado con el grupo de AR). En 25 pacientes con LES, los anti-CCP fueron positivos en tres (12%) ( p<0,001 comparado con el grupo de AR). Dos presentaron niveles positivos altos (66 y 111 UI, respectivamente), y una niveles positivos bajos (39 UI). De las 50 pacientes con SSp, 6 presentaron anticuerpos anti-CCP (12%) ( p<0,001 comparado con el grupo de AR). Cinco de éstas tuvieron niveles altos y una, nivel bajo. En el grupo de control sano, sólo un caso (10%) fue positivo (37 UI) ( p<0,001 comparado con el grupo de AR).
Al evaluar en conjunto las 79 pacientes con AR, la sensibilidad de los anti-CCP fue del 94% y la especificidad diagnóstica del 92%. La razón de probabilidades positiva fue de 12 y la razón de probabilidades negativa fue de 0,06. El valor predictivo positivo fue de 87% y el valor predictivo negativo de 96,3%. Cuando se consideraron sólo los individuos con títulos altos (66 de 79 pacientes con AR, 2 de 25 pacientes con LES, 5 de 50 pacientes con SSp y ningún control sano ni con EA), la sensibilidad fue de 84% y la especificidad de 95%.
El análisis de las manifestaciones clínicas de la AR en función de los niveles de anticuerpos anti-CCP no mostró asociación significativa en ninguna de las evaluaciones. De la misma manera, no se observaron diferencias significativas entre la presencia o los valores de estos anticuerpos y la actividad de la enfermedad.
La presencia y los valores de estos anticuerpos se comparó con los valores de citocinas (IL-4, IL-10, IL-12, IFN
g , TNF a ) y los valores de FR isotipos IgM e IgA. Los anticuerpos anti-CCP se correlacionaron con los niveles de FR IgA y FR IgM. Las principales correlaciones entre los valores de los anticuerpos anti-CCP con otras variables se muestran en el cuadro 2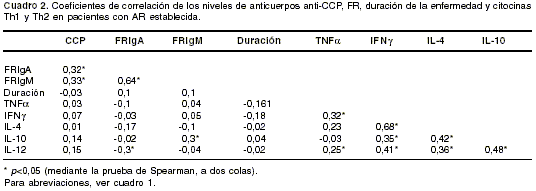
La genotipificación del HLA-DRB1 se realizó en las 69 pacientes con AR establecida. No se observaron asociaciones significativas entre alelos del HLA-DRB1 o el epítopo compartido y la presencia de anticuerpos anti-CCP. De las 66 pacientes anti-CCP positivo, 32 (48%) fueron HLADRB1* 04, 23 (35%) presentaron el epítopo compartido 70QRRAA74 y 3 (4,5%) el epítopo 70QKRAA74.
Discusión
En este estudio se encontró una alta sensibilidad (94%) y especificidad (92%) de los anticuerpos anti-CCP en pacientes con AR. Estos anticuerpos se mantuvieron estables durante la evolución de la enfermedad y no se asociaron con la actividad de la misma, manifestaciones extraarticulares, niveles de citocinas, HLA-DRB1 ni epítopo compartido. La razón de probabilidades positiva indica que un resultado de anticuerpos anti-CCP superior a 30 UI es 12 veces más probable que corresponda a un paciente con AR que sin esta enfermedad. De manera similar, la probabilidad de que un individuo con resultado negativo no padezca AR es del 96,3% (valor predictivo negativo). Es importante anotar que cuando se consideraron sólo los niveles altos (>60 UI), la sensibilidad fue de 84% y la especificidad de 95%.
El daño articular en la AR puede presentarse de manera temprana, incluso antes de que se detecten cambios erosivos o disminución del espacio articular mediante los métodos radiológicos convencionales (32). Se ha propuesto que el progreso radiológico en la AR no sigue un curso lineal y que, por el contrario, puede comportarse como una cinética de primer orden, en la que dicho daño podría ocurrir en los primeros años de la enfermedad (33). Sin embargo, no hemos observado una correlación significativa entre la duración de la enfermedad y el progreso radiológico (Anaya et al., datos sin publicar).
A pesar de esto, los cambios radiológicos se incluyen en los actuales criterios de clasificación de la AR (6), lo cual indica que su diagnóstico puede ser tardío si se tiene en cuenta este criterio. Por otro lado, el único criterio serológico es el FR, una prueba con moderada especificidad (87%) y sensibilidad (80%). Por lo tanto, es necesaria la modificación de los actuales criterios de clasificación de la AR para poder considerar como tales a pacientes con enfermedad temprana, y así iniciar un tratamiento precoz que permita prevenir el progreso de la misma.
La sensibilidad encontrada en este estudio para los anti-CCP fue del 94%, cifra superior a la observada en algunos estudios previos (24-26). Este resultado se podría explicar por las diferencias en el tamaño de la muestra, el origen de las poblaciones estudiadas, por tratarse, en su mayoría, de pacientes con AR establecida y por los niveles que se consideraron como positivos. Cuando se consideraron sólo aquellos individuos con niveles positivos altos, la sensibilidad de la prueba fue de 84%. Dubucquoi et al. compararon la positividad de anticuerpos anti-CCP en pacientes con AR en función de la linealidad del péptido citrulinado (34). El uso de péptidos citrulinados cíclicos mostró mejor sensibilidad y especificidad que los AKA y que el péptido citrulinado lineal (34). Igualmente, este estudio mostró una menor sensibilidad de los anticuerpos anti-CCP al inicio de la enfermedad que en pacientes con AR establecida (34).
En los pacientes con AR temprana se observó una sensibilidad de los anticuerpos anti-CCP de 80%. Sólo se incluyeron 10 pacientes con estas características debido a que éstos rara vez acuden al reumatólogo. En el
cuadro 3 se resumen los resultados de los estudios relacionados con la sensibilidad y la especificidad de estos anticuerpos. Van Gaalen et al. mostraron que éstos tienen un alto valor predictivo de AR en pacientes con artropatía indiferenciada (35). Estos resultados fueron confirmados por Rantapää-Dahlqvist et al. (38), quienes, además, observaron un alto valor predictivo para el FR IgA. En el presente estudio se observó una mayor prevalencia de anti-CCP (94%) que de FR IgA (86%). La prevalencia de FR IgA fue idéntica a la anteriormente reportada en otro grupo de pacientes con AR de Medellín (11). Dado que la distribución de los isotipos de autoanticuerpos puede variar con la raza (11), la evaluación del valor predictivo entre anti-CCP y FR IgA en nuestra población podría ser objeto de futuras investigaciones.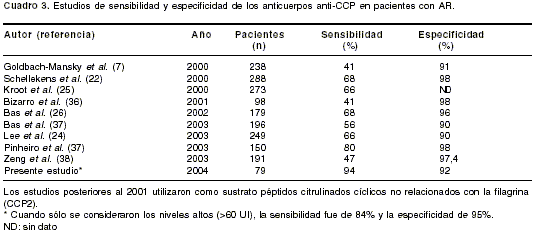
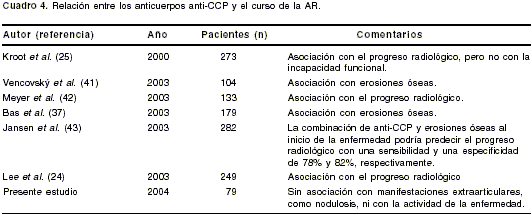
No se observaron diferencias significativas entre la presencia y los niveles de anti-CCP en las dos evaluaciones, separadas por un periodo de 2 años. Por lo tanto, y dada la ausencia de asociación con la actividad de la enfermedad y las manifestaciones extraarticulares, la utilidad de estos anticuerpos parece ser únicamente diagnóstica. Pinheiro et al. reportaron una correlación, mas no asociación, entre los niveles de anticuerpos anti-CCP y la actividad de la AR en pacientes con larga duración (promedio, 12 años) (39). En el presente estudio no se consideró el progreso radiológico como marcador pronóstico. No obstante, otros trabajos han mostrado una asociación entre estos anticuerpos y erosiones óseas (
cuadro 4).
Los anticuerpos anti-CCP se correlacionaron con el FR IgA e IgM (
cuadro 2). El tener resultados positivos para anti-CCP y FR aumenta la especificidad aunque, en conjunto, posean una sensibilidad baja (cuadro 5).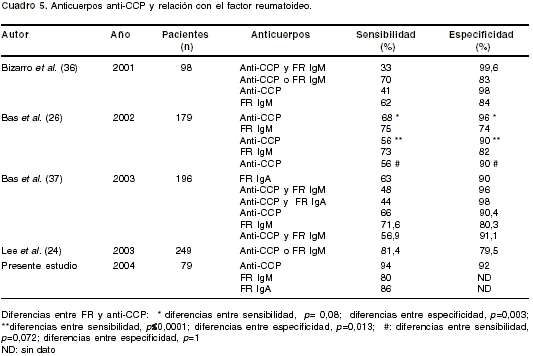
La AR ha sido descrita clásicamente como una enfermedad autoinmune, en la cual la respuesta predominante es conducida por células con patrón de citocinas T helper (Th) 1 (44). Más que la dominancia de un tipo de citocinas, existe una compleja interacción entre éstas. Ciertas características generales de las citocinas, como su pleiotropismo y redundancia biológica, dificultan el entendimiento de los mecanismos involucrados en la interacción Th1-Th2. Por otro lado, hay que tener en cuenta que el patrón de citocinas varía en función de múltiples factores, como el estado de actividad de la enfermedad, el tiempo de evolución de la misma y la existencia o no de un tratamiento instaurado (44). Los anticuerpos anti-CCP no se relacionaron con los niveles de citocinas en el presente estudio (cuadro 2). Las principales correlaciones entre citocinas fueron concordantes con los patrones de respuesta linfocitaria Th1 y Th2. Por un lado, los niveles de IFN
g , TNFa e IL-12 (características del patrón Th1) se correlacionaron entre sí. Se encontraron hallazgos similares para las citocinas del patrón Th2, IL-4 e IL-10. Por el carácter inflamatorio de la AR, era de esperarse detectar valores altos de las citocinas proinflamatorias en el suero de estos pacientes, del mismo modo que elevación de las citocinas contrareguladoras del proceso inflamatorio crónico, como un mecanismo de defensa, aunque generalmente éste sea insuficiente (44). Consecuente con lo anterior, los valores de IFNg se correlacionaron con los valores de IL-4 e IL-10. Así mismo, los niveles de IL-12 se correlacionaron con los de IL-10 (cuadro 2).La presencia y los niveles de anticuerpos anti-CCP fueron independientes del HLA-DRB1 y del epítopo compartido. Los principales estudios que han investigado la relación entre HLA y los anticuerpos anti-CCP, incluso el nuestro, muestran una ausencia de asociación entre el HLA-DRB1 y los anti-CCP. En la población colombiana, el epítopo compartido 70QRRAA74 en los alelos DRB1*04 confiere un riesgo 23 veces mayor de desarrollar AR (45). El HLA-DRB1*0401, portador del epítopo 70QKRAA74, y considerado el alelo de mayor riesgo de gravedad de la enfermedad, es escaso en poblaciones de Suramérica (46-48), particularmente en Antioquia, Colombia, de donde provinieron los pacientes con AR (45). Esto podría explicar, en parte, la ausencia de asociación no sólo entre el HLA y los anticuerpos anti-CCP, sino también entre éstos y las características clínicas de la AR.
La susceptibilidad genética a desarrollar anticuerpos anti-CCP podría estar asociada con el polimorfismo de los genes de las enzimas responsables de la citrulinación, en particular, con el gen PADI 4, situado en el cromosoma 1 (1p36), y cuyo producto 'citrulina' los residuos de arginina. Este hallazgo, inicialmente descrito en población japonesa (49), no se replicó en población caucásica inglesa (50), lo cual confirma la necesidad de realizar estudios de inmunogenética en cada población, antes de extrapolar resultados obtenidos en poblaciones distintas a la nuestra (1).
Se han descrito cinco tipos de PAD, las cuales son reguladas por estrógenos y activadas durante la apoptosis (51,52). Nissinen et al. demostraron la presencia de anticuerpos anti-PAD en el 88% de pacientes con AR en fases iniciales, pero sólo en el 22% en AR de larga duración (53). A diferencia de los anti-CCP, los anticuerpos anti-PAD se encontraron en una alta proporción de pacientes con otras enfermedades reumatológicas autoinmunes, como LES y SSp (44% y 84%, respectivamente), pero no en otras enfermedades autoinmunes como la esclerosis múltiple. Por lo tanto, los anticuerpos anti-PAD podrían ser marcadores de autoinmunidad en general.
En el presente estudio observamos anticuerpos anti-CCP en un solo paciente (2%) con EA definida. Este resultado, original y no publicado previamente, indica que la respuesta autoinmune articular en pacientes con EA, en cuanto a la citrulinación de péptidos se refiere, es distinta en AR que en EA. También se estudiaron 3 pacientes con artropatía psoriásica y uno con EA asociada con una enterocolopatía. En todos estos casos los resultados de anti-CCP fueron negativos (no se muestran los resultados).
Se observó una prevalencia de anticuerpos anti-CCP en el 12% de los pacientes con LES y SSp, no significativamente diferente al 10% observado en la población sana. Estudios previos señalaron una prevalencia de hasta el 20% en pacientes con LES (54) y del 4% en pacientes con SSp (34). Además del origen racial que pudiera explicar la diferencia entre los resultados, los criterios de selección de los pacientes deben ser también considerados en la interpretación de los mismos. Los pacientes incluidos en el presente estudio cumplieron criterios estrictos de clasificación que incluyeron la ausencia de erosiones óseas en los pacientes con LES y SSp, y una biopsia de glándula salivar positiva en aquéllos con SSp. Los resultados indican que los anticuerpos anti-CCP son de ayuda diagnóstica diferencial entre AR y otras enfermedades reumatológicas tales como LES, SSp y EA.
En resumen, los anticuerpos anti-CCP tienen un interés diagnóstico para la AR en nuestra población. Sin embargo, su utilidad en el seguimiento clínico es limitada y su síntesis es independiente del HLA-DRB1 y no se correlacionan con niveles de citocinas Th1/Th2. Los anticuerpos anti-CCP son el resultado de una respuesta autoinmune específica generada contra péptidos citrulinados en la membrana sinovial de los pacientes con AR (
figura 1). Es posible que la citrulinación de proteínas genere alteraciones cualitativas o cuantitativas que participen en la pérdida de la tolerancia inmunológica y en el desarrollo de enfermedad autoinmune (55). Esta hipótesis es sustentada por la presencia de anticuerpos anti-CCP varios años antes de la evidencia clínica de AR (56). No obstante, el papel patogénico de estos autoanticuerpos es todavía incierto.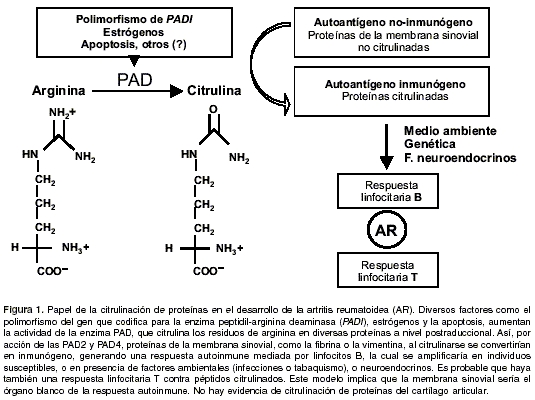
Agradecimientos
Los autores agradecen la participación de los pacientes en el presente estudio, a los dos revisores anónimos por sus comentarios útiles y a S. Ahuja por su apoyo. Este estudio fue financiado en parte por Colciencias (22130412672).
Igualmente, declaran no tener ningún conflicto de interés con las compañías mencionadas en este trabajo.
Correspondencia:
Juan Manuel Anaya, Corporación para Investigaciones Biológicas (CIB),
Cra. 72 A N° 78 B-141, Medellín, Colombia.
Teléfono: (4) 441 0855 y 441 8846; fax:(4) 441 5514
Recibido: 27/10/03; aceptado: 27/05/04
Referencias
1. Anaya JM. Genes y artritis reumatoidea. Rev Colomb Reumatol 1999;6:240-50. [ Links ]
2. Verheijden GFM, Rijnders AWM, Bos E, Coenen-de Roo CJJ, van Staveren CJ, Miltenburg AMM, et al. Human cartilage glycoprotein-39 as a candidate autoantigen in rheumatoid arthritis. Arthritis Rheum 1999; 40:1115-25. [ Links ]
3. Blass S, Meier C, Vohr HW, Schwochau M, Specker C, Burmester GR. The p68 autoantigen characteristic of rheumatoid arthritis is reactive with carbohydrate epitope specific autoantibodies. Ann Rheum Dis 1998; 57:220-5. [ Links ]
4. Guerassimov A, Zhang Y, Banerjee S, Cartman A, Leroux JY, Rosenberg LC, et al. Cellular immunity to the G1 domain of cartilage proteoglycan aggrecan is enhanced in patients with rheumatoid arthritis but only after removal of keratan sulfate. Arthritis Rheum 1998; 41:1019-25. [ Links ]
5. Després N, Boire G, Lopez-Longo FJ, Ménard HA. The Sa system: a novel antigen-antibody system specific for rheumatoid artritis. J Rheumatol 1994;21:1027-33. [ Links ]
6. Arnett FC, Edworthy SM, Bloch DA, McShane DJ, Fries JF, Cooper NS, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum 1988;31:315-24. [ Links ]
7. Goldbach-Mansky R, Lee J, McCoy A, Hoxworth J, Yarboro C, Smolen JS, et al. Rheumatoid arthritis associated autoantibodies in patients with synovitis of recent onset. Arthritis Res 2000;2:236-43. [ Links ]
8. Nienhuis RLF, Mandema EA. A new serum factor in patients with rheumatoid arthritis. The antiperinuclear factor. Ann Rheum Dis 1964;23:302-5. [ Links ]
9. Young BJJ, Mallya RK, Leslie RDG, Clark CJM, Hamblin TJ. Anti-keratin antibodies in rheumatoid arthritis. Br Med J 1979;2:97-9. [ Links ]
10. Kurki P, Aho K, Palosuo T, Heliövaara M. Immunopathology of rheumatoid arthritis: antikeratin antibodies precede the clinical disease. Arthritis Rheum 1992;35: 914-7. [ Links ]
11. Anaya JM, Correa PA, Mantilla RD, Jimenez F, Kuffner T, McNicholl JM. Rheumatoid arthritis in African Colombians from Quibdo. Semin Arthritis Rheum 2001;31: 191-8. [ Links ]
12. Hoet RM, Boerbooms AM, Arends M, Ruiter DJ, van Venrooij WJ. Antiperinuclear factor, a marker autoantibody for rheumatoid arthritis: colocalisation of the perinuclear factor and profilaggrin. Ann Rheum Dis 1991; 50:611-8. [ Links ]
13. Girbal E, Sebbag M, Gomès-Daudrix V, Simon M, Vincent C, Serre G. Characterisation of the rat oesophagus epithelium antigens defined by the so-called "antikeratin antibodies", specific for rheumatoid arthritis. Ann Rheum Dis 1993;52:749-57. [ Links ]
14. Simon M, Girbal E, Sebbag M, Gomes-Daudrix V, Vincent C, Salama G, et al. The cytokeratin filamentaggregating protein filaggrin is the target of the so-called "antikeratin antibodies," autoantibodies specific for rheumatoid arthritis. J Clin Invest 1993;92:1387-93. [ Links ]
15. Sebbag M, Simon M, Vincent C, Masson-Bessiere C, Girbal E, Durieux JJ, et al. The antiperinuclear factor and the so-called antikeratin antibodies are the same rheumatoid arthritis-specific autoantibodies. J Clin Invest 1995;95:2672-9. [ Links ]
16. Schellekens GA, de Jong BAW, van den Hoogen FHJ, van de Putte LBA, van Venrooij WJ. Citrulline is an essential constituent of antigenic determinants recognized by rheumatoid artritis-specific autoantibodies. J Clin Invest 1998;101:273-81. [ Links ]
17. Vincent C, Simon M, Sebbag M, Girbal-Neuhauser E, Durieux JJ, Cantagrel A, et al. Immunoblotting detection of autoantibodies to human epidermis filaggrin: a new diagnostic test for rheumatoid arthritis. J Rheumatol 1998;25:838-46. [ Links ]
18. van Venrooij WJ, Pruijn GJM. Citrullination: a small change for a protein with great consequences for rheumatoid arthritis. Arthritis Res 2000;2:249-51. [ Links ]
19. Masson-Bessiere C, Sebbag M, Durieux JJ, Nogueira L, Vincent C, Girbal-Neuhauser E, et al. In the rheumatoid pannus, anti-filaggrin autoantibodies are produced by local plasma cells and constitute a higher proportion of IgG than in synovial fluid and serum. Clin Exp Immunol 2000;119:544-52. [ Links ]
20. Baeten D, Peene I, Union A, Meheus L, Sebbag M, Serre G, et al. Specific presence of intracellular citrullinated proteins in rheumatoid arthritis synovium. Arthritis Rheum 2001;44:2555-62. [ Links ]
21. Vossenaar ER, Nijenhuis S, Helsen MMA, van der Heijden A, Senshu T, van den Berg WB, et al. Citrullination of synovial proteins in murine models of rheumatoid arthritis. Arthritis Rheum 2003;48:2489-500. [ Links ]
22. Schellekens GA, Visser H, de Jong BAW, van de Hoogen FHJ, Hazes JMW, Breedveld FC, et al. The diagnostic properties of rheumatoid arthritis antibodies recognizing a cyclic citrullinated peptide. Arthritis Rheum 2000;43:155-63. [ Links ]
23. van Venrooij WJ, Hazes JM, Visser H. Anticitrullinated protein/peptide antibody and its role in the diagnosis and prognosis of early rheumatoid arthritis. Neth J Med 2002; 60:383-8. [ Links ]
24. Lee DM, Schur PH. Clinical utility of the anti-CCP assay in patients with rheumatic diseases. Ann Rheum Dis 2003; 62:870-4. [ Links ]
25. Kroot EJ, de Jong BA, van Leeuwen MA, Swinkels H, van den Hoogen FH, van't Hof M, et al. The prognostic value of anti-cyclic citrullinated peptide antibody in patients with recent-onset rheumatoid arthritis. Arthritis Rheum 2000;43:1831-5. [ Links ]
26. Bas S, Perneger TV, Seitz M, Tiercy JM, Roux-Lombard P, Guerne PA. Diagnostic tests for rheumatoid arthritis: comparison of anti-cyclic citrullinated peptide antibodies, anti-keratin antibodies and IgM rheumatoid factors. Rheumatology 2002;41:809-14. [ Links ]
27. Cadena J, Vinaccia S, Pérez A, Rico MI, Hinojosa R, Anaya JM. The impact of disease activity on the quality of life, mental health status, and family dysfunction in Colombian patients with rheumatoid arthritis. J Clin Rheumatol 2003;9:142-50. [ Links ]
28. van der Linden S, Valkenburg HA, Cats A. Evaluation of diagnostic criteria for ankylosing spondylitis. A proposal for modification of the New York criteria. Arthritis Rheum 1984;27:361-8. [ Links ]
29. Tan EM, Cohen AS, Fries JF, Masi AR, McShane DJ, Rothfield NF, et al. The 1982 revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum 1982;25:1271-7. [ Links ]
30. Vitali C, Bombardieri S, Jonsson R, Moutsopoulos HM, Alexander EL, Carsons SE, et al. Clasification criteria for Sjögren's syndrome. A revised version of the European criteria proposed by the American-European Consensus Group. Ann Rheum Dis 2002;61:554-8. [ Links ]
31. Jaeschke R, Guyatt GH, Sackett DL. Users' guides to the medical literature. III. How to use an article about a diagnostic test. B. What are the results and will they help me in caring for my patients? The Evidence-Based Medicine Working Group. JAMA 1994;271:703-7. [ Links ]
32. Ory PA. Interpreting radiographic data in rheumatoid arthritis. Ann Rheum Dis 2003;62:597-604. [ Links ]
33. Fuchs HA, Pincus T. Radiographic damage in rheumatoid arthritis: description by nonlinear models. J Rheumatol 1992;19:1655-8. [ Links ]
34. Dubucquoi S, Solau-Gervais E, Lefranc D, Marguerie L, Sibilia J, Goetz J, et al. Evaluation of anti-citrullinated filaggrin antibodies as hallmarks for the diagnosis of rheumatic diseases. Ann Rheum Dis 2004;63:415-9. [ Links ]
35. van Gaalen FA, Linn-Rasker SP, van Venrooij WJ, de Jong BA, Breedveld FC, Verweij CL, et al. Autoantibodies to cyclic citrullinated peptides predict progression to rheumatoid arthritis in patients with undifferentiated arthritis. Arthritis Rheum 2004;50:709-15. [ Links ]
36. Bizarro N, Mazzanti G, Tonutti E, Villalta D, Tozzoli R. Diagnostic accuracy or the anti-citrulline antibody assay for rheumatoid arthritis. Clin Chemistry 2001;47: 1089-93. [ Links ]
37. Bas S, Genevay S, Meyer O, Gabay C. Anti-cyclic citrullinated peptide antibodies, IgM and IgA rheumatoid factors in the diagnosis and prognosis of rheumatoid arthritis. Rheumatology 2003;42:677-80. [ Links ]
38. Rantapää-Dahlqvist S, de Jong BAW, Berglin E, Hallmans G, Wadell G, Stenlund H, et al. Antibodies against cyclic citrullinated peptide and IgA rheumatoid factor predict the development of rheumatoid arthritis. Arthritis Rheum 2003;48:2741-9. [ Links ]
39. Pinheiro GC, Scheinberg MA, Aparecida da Silva M, Maciel S. Anti-cyclic citrullinated peptide antibodies in advanced rheumatoid arthritis (carta). Ann Int Med 2003; 139:234-5. [ Links ]
40. Zeng X, Ai M, Tian X, Gan X, Shi Y, Song Q, et al. Diagnostic value of anti-cyclic citrullinated peptide antibodody in patients with rheumatoid arthritis. J Rheumatol 2003;30:1451-5. [ Links ]
41. Vencovsky J, Machacek S, Sedova L, Kafkova J, Gatterova J, Pesakova V, et al. Autoantibodies can be prognostic markers of an erosive disease in early rheumatoid arthritis. Ann Rheum Dis 2003;62:427-30. [ Links ]
42. Meyer O, Labare C, Dougados M, Goupille Ph, Cantagrel A, Dubois A, et al. Anticitrullinated protein/peptide antibody assays in early rheumatoid arthritis for predicting five year radiographic damage. Ann Rheum Dis 2003:62:120-6. [ Links ]
43. Jansen L-MA, van Schaardenburg D, van der Horst-Bruinsma IE, van de Stadt RJ, de Koning M-HMT, Dijkmans B- AC. The predictive value of anti-cyclic citrullinated peptide antibodies in early arthritis. J Rheumatol 2003;30:1691-5. [ Links ]
44. Camargo JF, Correa PA, Vélez-Castrillón S, Anaya JM. Citoquinas en artritis reumatoide. En: Ramírez LA, Anaya JM, editores. Artritis reumatoide. Segunda edición. Medellín: Editora Médica Colombiana S.A.; 2004. p.53-80. [ Links ]
45. Anaya JM, Correa PA, Mantilla RD, Arcos-Burgos M. Rheumatoid arthritis association in Colombian population is restricted to HLA-DRB1*04 QRRAA alleles. Genes Immun 2002;3:56-8. [ Links ]
46. Gonzalez A, Nicovani S, Massardo L, Aguirre V, Cervilla V, Lanchbury JS, et al. Influence of the HLADR beta shared epitope on susceptibility to and clinical expression of rheumatoid arthritis in Chilean patients. Ann Rheum 1997;56:191-3. [ Links ]
47. Citera G, Padulo LA, Fernández G, Lazaro MA, Rosemffet MG, Maldonado JA. Influence of HLA-DR alleles on rheumatoid arthritis: susceptibility and severity in Argentine patients. J Rheumatol 2001;28:1486-91. [ Links ]
48. Castro F, Acevedo E, Ciusani E, Angulo JM,Wollheim FA, Sandberg-Wollheim M. Tumour necrosis factor microsatellites and HLA-DRB1*, HLA-DQA1*, and HLADQB1* alleles in Peruvian patients with rheumatoid arthritis. Ann Rheum Dis 2001;60:791-5. [ Links ]
49. Suzuki A, Yamada R, Chang X, Tokuhiro S, Sawada T, Suzuki M, et al. Functional haplotypes of PADI4, encoding citrullinating enzyme peptidylarginine deiminase 4, are associated with rheumatoid arthritis. Nat Genet 2003;34:395-402. [ Links ]
50. Barton A, Bowes J, Eyre S, Spreckley K, Hinks A, John S, et al. A functional haplotype of the PADI4 gene associated with rheumatoid arthritis in a Japanese population is not associated in a United Kingdom population. Arthritis Rheum 2004;50:1117-21. [ Links ]
51. Takahara H, Kusubata M, Tsuchida M, Kohsaka T, Tagami S, Sugawara K. Expression of peptidylarginine deiminase in the uterine epithelial cells of mouse is dependent on estrogen. J Biol Chem 1992;267:520-5. [ Links ]
52. Senshu T, Akiyama K, Nagata S, Watanabe K, Hikichi K. Peptidylarginine deiminase in rat pituitary: sex difference, estrous cycle-related changes, and estrogen dependence. Endocrinology 1989;124:2666-70. [ Links ]
53. Nissinen R, Paimela L, Julkunen H, Tienari PJ, Leirisalo-Repo M, Palosuo T, et al. Peptidylarginine deiminase, the arginine to citrulline converting enzyme, is frequently recognized by sera of patients with rheumatoid arthritis, systemic lupus erythematosus and primary Sjögren syndrome. Scand J Rheumatol 2003; 32:337-42. [ Links ]
54. Mediwake R, Isenberg DA, Schellekens GA, van Venrooij WJ. Use of anti-citrullinated peptide and anti-RA33 antibodies in distinguishing erosive arthritis in patients with systemic lupus erythematosus and rheumatoid arthritis. Ann Rheum Dis 2001;60:67-8. [ Links ]
55. Yamada R, Suzuki A, Chang X, Yamamoto K. Peptidylarginine deiminase type 4: identification of a rheumatoid arthritis-susceptible gene. Trends Mol Med 2003;9:503-8. [ Links ]
56. Nielen MMJ, van Schaardenburg D, Reesink HW, van de Stadt RJ, van der Horst-Bruinsma IE, de Koning MHMT, et al. Specific autoantibodies precede the symptoms of rheumatoid arthritis. Arthritis Rheum 2004; 50:380-6
. [ Links ]













