Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Biomédica
Print version ISSN 0120-4157On-line version ISSN 2590-7379
Biomédica vol.25 no.4 Bogotá Dec. 2005
Control de la infección por Trypanosoma cruzi en
donantes de sangre de Colombia, 2003
Mauricio Beltrán, María Isabel Bermúdez, María Cristina Forero, Maribel Ayala, Magda Juliana Rodríguez
Instituto Nacional de Salud, Red Nacional de Bancos de Sangre, Bogotá, D.C., Colombia.
Introducción. La enfermedad de Chagas es un problema de salud pública en Latinoamérica. Después de la vectorial, la segunda fuente de transmisión es la transfusional; en Colombia el tamizaje para este marcador es obligatorio en los bancos de sangre desde 1995.
Objetivo. Evaluar el comportamiento de algunas estrategias de control de la infección en donantes y estimar el riesgo transfusional por enfermedad de Chagas.
Materiales y métodos. Se analizaron los datos de cobertura de tamizaje y reactividad para anticuerpos anti- Trypanosoma cruzi; los resultados de los bancos de sangre en el Programa de Evaluación Externa del Desempeño de Serología (PEED) y los reportes de los Laboratorios de Salud Pública sobre pruebas confirmatorias de serología en donantes.
Resultados. En 2003, los bancos de sangre del país captaron 482.371 unidades, 99,91% fueron analizadas para anti- T.cruzi, resultando reactivas 0,42%. Casanare presentó la mayor reactividad con 107/1.487 (7,2%), de los cuales se confirmaron como positivos 75. En el PEED participaron 45,5% bancos, la totalidad de los cuales utilizó ELISA para tamizaje; se hallaron 1,1% resultados falsos positivos y ningún falso negativo. En 12 departamentos que analizaron 338.563 unidades para anti- T.cruzi, 1.298 casos fueron notificados como reactivos y 1.108 (85,4%) se confirmaron por la prueba de IFI, registrando una positividad de 0,33%.
Conclusiones. Aunque la cobertura del tamizaje llegó a 99,91%, existe aún riesgo de infección por T.cruzi. Los casos de T.cruzi en donantes oscilan entre 0 y 50 por cada mil, y como ya se mencionó, Casanare es el departamento con mayor riesgo de adquirir Chagas transfusional. Los bancos participantes en el PEED no mostraron resultados falsos negativos.
Palabras clave: bancos de sangre, Trypanosoma cruzi, enfermedad de Chagas, Colombia, control de calidad.
Control of infection for the Trypanosoma cruzi in blood donors
Introduction. Chagas disease is a public health problem in Latin America. Whereas the primary source of transmission is the insect vector, the second is by blood transfusion. Consequently, in Colombia, screening for trypanosomiasis has been obligatory for blood donors since 1995.
Objective. The effectiveness ot current strategies for infection control in donors was evaluated in order to estimate the risk of blood stock contamination with Chagas disease. The screening data came from the blood banks in the Program of External Evaluation in the Performance of Serology and the reports of the Laboratories of Public Health on confirming donor serology tests.
Results. In 2003, 482,371 units of blood were collected in all of Colombia Of these, 99.9% were analyzed for anti-T.cruzi reactivity, with a positives of 0.42% detected. The Casanare Province presented the biggest number of reactive donors 107/1,487 (7.2%), with 75 confirmed positive. In the Program of External Evaluation in the Performance of Serology, 45.5% of all banks participated-all used ELISA for screening of anti-T.cruzi. 1.1% false positives and nofalse negatives were indicated in 12 provinces, where 338,563 units were analyzed for anti- T.cruzi, 1,298 units were reactive and 1,108 (85.4%) were confirmed by the IFI test. This indicated a rate of Chagas positives of 0.33%.
Conclusions. Although the analysis covered arrived at 99.9% of the blood units, a small degree of infection risk for T.cruzi still remains. The cases of T.cruzi in donors oscillate between 0 and 50 per thousand. This rate is highest in Casanare with a concomitantly high risk for acquisition of transfusional Chagas. ot show negative false results.
Key words: Blood banks, Trypanosoma cruzi, Chagas disease, Colombia, quality control.
La enfermedad de Chagas representa un serio problema de salud pública en muchos países de Latinoamérica; se estima que al menos 90 millones de personas están expuestas al riesgo de infección (1). Esta enfermedad se transmite al ser humano y a animales mamíferos a través de insectos triatominos y es la cuarta causa de pérdida económica por morbilidad en Latinoamérica (2,3). En Colombia existe transmisión vectorial de Trypanosoma cruzi principalmente en los departamentos de Arauca, Boyacá, Casanare, Cundinamarca, Santander y Norte de Santander; aproximadamente, 7% de la población nacional presenta la enfermedad y 23% de la población esta en riesgo de infección (4).
La segunda fuente de transmisión de T. cruzi se debe a las transfusiones sanguíneas. Excepto los liofilizados de plasma y los hemoderivados, todos los componentes de la sangre son infectantes (5-7). Se estima que el riesgo de adquirir la enfermedad de Chagas al recibir una unidad infectada oscila entre 20% y 40%, cifras que pueden incrementarse, entre otras causas, por la elevada prevalencia en la población, por el largo tiempo de latencia de la infección, que para el caso de Chagas puede ser de varios años, la elevada prevalencia en donantes de sangre, la baja cobertura del tamizaje de las unidades de sangre donadas, el número de unidades de sangre transfundidas, la larga supervivencia del parásito en las unidades de sangre almacenadas en refrigeración, la falta de canalización y confirmación de donantes reactivos sospechosos de estar infectados, y la deficiencia en los controles de calidad durante el procesamiento de la sangre y sus componentes (8,9).
Sin embargo, la seguridad de las transfusiones sanguíneas en el país ha mejorado considerablemente en los últimos años, debido a la implementación de estrategias como las siguientes: 1) la obligatoriedad del tamizaje para anti- T.cruzi en todas las unidades de sangre para transfusión desde 1995; 2) la inclusión en la encuesta de selección del donante de preguntas relacionadas con el posible contacto que tenga el individuo con la enfermedad o con el vector, por ejemplo: "¿Conoce o ha sido picado por un insecto llamado pito, chupasangre, tábano, chipo, rondador, vinchuco o chinche besador o picudo?"; "¿Ha padecido enfermedad de Chagas?", o "¿Ha vivido en zona endémica para el insecto vector?", cuya respuesta afirmativa excluye a la persona; 3) la captación de unidades de sangre de donantes voluntarios y, más recientemente, voluntarios habituales; 4) el incremento en la cobertura del tamizaje para este marcador; 5) la implementación de la técnica de ELISA para el tamizaje de donantes y la evaluación a través del Programa de Evaluación Externa del Desempeño de Serología, PEED, que permite a los bancos de sangre comparar los resultados reales o del laboratorio organizador con los suyos, y tomar las medidas de corrección pertinentes (autoevaluación), y, además, recibir asesoría y capacitación; 6) la confirmación de los casos reactivos detectados por el banco de sangre por parte de los Laboratorios de Salud Pública (LSP) y la remisión de los casos positivos a los centros asistenciales para asesoría, tratamiento o manejo clínico pertinente (10-14), y finalmente: 7) las acciones de vigilancia y control sobre la infección y el vector realizados por los centros de investigación, el INS y los entes territoriales que participan en el Programa Nacional de Prevención y Control de la Enfermedad de Chagas y Cardiopatía Infantil. Esta combinación de estrategias permite reducir el riesgo de infección vía transfusión y cortar la cadena de transmisión de la infección (15,16).
El objetivo de este trabajo consistió en evaluar el comportamiento de algunas de estas estrategias y estimar el riesgo transfusional por enfermedad de Chagas para el año 2003 en la Red Nacional de Bancos de Sangre de Colombia.
Materiales y métodos
Se analizaron los reportes de la vigilancia de la seguridad transfusional sobre cobertura de tamizaje y reactividad para los anticuerpos anti- T. cruzi enviados mensualmente a través de las coordinaciones seccionales de los 143 bancos de sangre de Colombia; los resultados del Programa de Evaluación Externa en el Desempeño de Serología (PEED), y los reportes de los LSP sobre realización de pruebas confirmatorias, para lo cual el protocolo nacional de diagnóstico define como caso confirmado de infección por Chagas aquel que demuestra una positividad en dos pruebas serológicas que se basen en diferentes principio como IFI y ELISA.
Las variables por banco de sangre analizadas fueron: cobertura de tamizaje para anticuerpos anti- T.cruzi; reactividad a estos anticuerpos en las unidades de sangre recolectadas; método de tamizaje utilizado y concordancia en la evaluación externa; comfirmación por parte de los LSP por medio de pruebas confirmatorias de las muestras reactivas acorde con el tamizaje de los bancos. Todos los datos analizados correspondieron al 2003. Se estimó, además, el número de individuos que pudo haber sido infectados por no tamizar todas las unidades de sangre para T.cruzi, asumiendo que las unidades no fueron fraccionadas y se transfundieron como sangre total al menos a un individuo, con base en la formula de infectividad sugerida por la OPS y en un riesgo de 20% de adquirir la infección por Chagas al recibir una unidad infectada.
Resultados
En el 2003, los 143 bancos de sangre del país recolectaron 482.371 unidades de sangre, se analizó 99,9% de ellas para detectar la presencia de anticuerpos anti- T. cruzi (
cuadro 1). La cobertura de tamizaje tuvo un rango entre 99,4% y 100%; las 430 unidades de sangre no tamizadas se distribuyeron en 44 (31%) del total de bancos de sangre. Las coberturas más bajas se presentaron en los departamentos de Valle del Cauca (99,3%) Chocó (99,4%) y Cesar (99,5%). De las 481.941 unidades tamizadas para T.cruzi, 0,42% resultaron reactivas; el mayor porcentaje de reactividad se presentó en Casanare con 7,2% y en Arauca con 2,7%, y el más bajo se registró en Cauca con 0,03%, y en Putumayo y Guainía con 0%.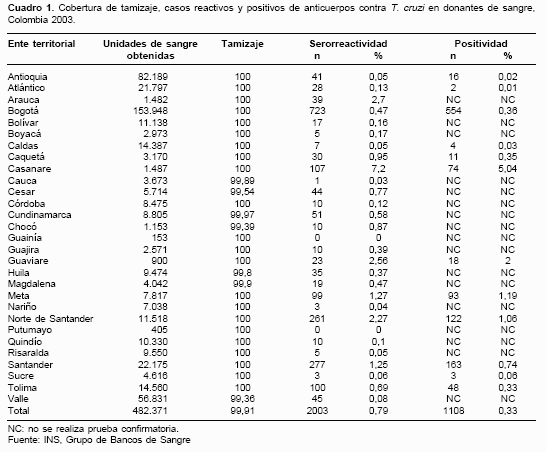
Según el PEED se halló que participaron 65 de los 143 bancos (los cuales recolectan 56,2% de la sangre del país), cuyos resultados mostraron 8 falsos positivos (1,1%) en 716 determinaciones para los sueros negativos y ningún resultado falso negativo en 64 sueros positivos enviados. Se encontró, además, que todos los bancos participantes utilizaron ensayos inmunoenzimáticos de tipo ELISA para el tamizaje de Chagas; los reactivos de ELISA empleados por los bancos de sangre estaban constituidos por antígenos purificados de cepas de T. cruzi en 94,59% de los casos y solo 5,41% utilizaron antígenos recombinantes; entre las marcas utilizadas se contaban Tecnosuma, Biomerieux, Abbott para los antígenos purificados, y Wiener para los recombinantes (17-18).
De los 29 LSP departamentales donde existen bancos de sangre, 17 (58,6%) enviaron información sobre la realización de pruebas complementarias para anticuerpos contra Chagas; de éstos, 12 realizaron prueba confirmatoria por inmunofluorescencia indirecta (IFI), los restantes realizaron una segunda prueba de ELISA. Un total de 2.003 sueros fueron reportados por los bancos de sangre como reactivos a T.cruzi, de los cuales 1.339 fueron notificados como reactivos por los LSP; se realizó prueba confirmatoria (IFI) a 1.298 del total de sueros originalmente reportados como reactivos por los bancos de sangre (64,8%), y resultaron positivos 1.108, situación que muestra un ligero avance respecto a anteriores estudios en que sólo 33,2% de los sueros reactivos fueron confirmados. Sin embargo, únicamente 41,4% de los LSP confirmaron a sus donantes, 17,2% realizaron sólo una prueba adicional tipo ELISA y 41,4% no hicieron confirmación de donantes reactivos (
cuadro 1).Los LSP de los departamentos de Sucre y Guaviare confirmaron el total de las unidades halladas reactivas en sus bancos de sangre mediante técnica de IFI, seguidos de Tolima (98%), Meta (97%) y Bogotá (94%). En total, 1.108 casos fueron confirmados serológicamente por IFI, indicando una positividad de 3 casos por cada mil donaciones. Los departamentos con mayor número de casos confirmados como positivos por cada mil donaciones fueron Casanare con 50; Guaviare, 20; Meta, 12; Norte de Santander, 11, y Santander, 7. A pesar de que el tamizaje promedio nacional es superior a 99,9% existe aún la posibilidad de que un individuo por cada millón de transfusiones realizadas pueda ser infectado con T. cruzi, riesgo que difiere de un departamento a otro, dado que el porcentaje de tamizaje presenta variaciones y que no se tuvo en cuenta que una unidad de sangre puede transfundirse, al menos, a 3 personas.
Discusión
La seguridad de la sangre en Colombia ha mejorado notablemente, en especial cuando se hace la comparación con los datos reportados en 1996, y se observa un incremento en la cobertura de tamizaje de 99,6% en 1996 a 99,9% en 2003, y una reducción en las demás variables como el número de unidades no tamizadas, que pasó de 6.557 a 430; el número de individuos que pudieron haber sido infectados con T.cruzi vía transfusión, que disminuyó de 26 a menos de un caso, y la reactividad en donantes, que pasó de 1,0% a 0,42%.
Estos hallazgos podrían explicarse por el fortalecimiento de las estrategias de seguridad transfusional descritas, en especial las referentes a la selección del donante y a las técnicas de tamizaje utilizadas por los bancos de sangre, así como a las acciones de prevención de la enfermedad y de control del vector realizadas gracias a la identificación de áreas endémicas para determinadas especies de triatominos y zonas de mayor riesgo de la enfermedad por parte de los grupos de trabajo del Programa Nacional de Control de la Enfermedad de Chagas; sin embargo, es de anotar que estas acciones de control se realizan de forma puntual, pues muchas áreas endémicas coinciden con zonas de conflicto armado (18-19).
La presencia de un porcentaje mínimo de resultados falsos positivos y ningún falso negativo en el PEED de este año podría explicarse por el uso de la técnica ELISA en 100% del tamizaje, lo que difiere de lo hallado en 1998 (uso de técnica ELISA en 91% y 2,38% de resultados falsos negativos). Este hecho, además, responde al impacto que el PEED ha generado en los bancos participantes, permitiéndoles conocer, comparar y mejorar su desempeño respecto al tamizaje, y acceder a asesoría y capacitación, situación que en cambio no se da en cerca de 50% de los bancos de sangre que no participan en el Programa (13,18).
Acorde con la recomendación de la OMS, en Colombia se utiliza una prueba de tamizaje tipo inmunoensayo (ELISA), idealmente con antígenos recombinantes o péptidos sintéticos que incluyan antígenos como Ag1, Ag2, Ag30, SAPA, Ag13 y Ag36, pues han mostrado mejor desempeño que aquellos reactivos que utilizan antígenos crudos o proteínas purificadas de los estadios epimastigote y tripomastigote de T. cruzi, los cuales presentan reacciones cruzadas que alteran la especificidad y no ofrecen una buena sensibilidad. (1,17,20-21).
Es importante destacar que sólo tenemos una visión parcial de lo que ocurre con respecto a la vigilancia realizada por los LSP, dado que no se realiza confirmación a todas las unidades reactivas y la información no es enviada a tiempo, lo que resulta en menos oportunidad o pérdida para el diagnóstico, asesoria y tratamiento de estas personas, y facilita la difusión de esta infección a la población general en caso de tratarse de donantes verdaderamente infectados, dificultando así el control epidemiológico de la enfermedad (18,22-24).
Esta situación puede deberse a causas como el desconocimiento de las responsabilidades de los bancos de sangre y los LSP respecto a los donantes de sangre; falta de recursos de los LSP, dado que el proceso de confirmación de casos reactivos en donantes de sangre no está incluido en las estrategias de prevención del Plan de Atención Básica a cargo de los entes territoriales y, finalmente, a la escasa coordinación entre las redes de LSP y los bancos de sangre.
Bogotá, Santander, Norte de Santander, Meta y Casanare presentaron 90,7% del total de casos de infección por T.cruzi (1.005/1.108), situación que ratifica lo descrito en diferentes estudios sobre una mayor endemia y riesgo de transmisión de esta infección debida a la movilización de personas hacia estos departamentos (4,18).
Casanare y Arauca tamizaron todas sus unidades de sangre, pero presentaron reactividad elevada a T. cruzi (7,2% y 2,7%, respectivamente). Sólo Casanare realizó confirmación de donantes reactivos mientras que Arauca no confirmó ninguno de sus 40 casos; además, sólo uno de los tres bancos de estos departamentos evaluó su desempeño a través del PEED; estos hallazgos permiten deducir que el mayor riesgo de adquirir una infección por Chagas transmitida por transfusión (ITT) y de difundirla en la comunidad se presenta en estos departamentos (4,9,18-19).
Finalmente, la seguridad transfusional en Colombia podría mejorar si el total de los bancos evaluaran su desempeño a través del PEED y se fortaleciera la vigilancia epidemiológica mediante la confirmación de 100% de los casos de donantes reactivos por parte de los LSP.
Agradecimientos
Agradecemos la colaboración de los bancos de sangre, los LSP y los entes territoriales por la información enviada.
Conflicto de intereses
Los autores manifiestan que no existe ningún conflicto de intereses.
Financiación
El presente estudio se desarrolló gracias a la financiación del Instituto Nacional de Salud de Colombia.
Correspondencia:
Fax 2 20 77 00 Extensión 420 o 421
Avenida El dorado Número 51-60
Bogotá, Colombia
Recibido:10/03/05; aceptado: 16/09/05
Referencias
1. World Health Organization. Control of Chagas disease. Second report of the WHO expert committee: Technical reports series 905. Geneva: WHO;2002. [ Links ]
2. World Health Organization. Important progress in the control of Chagas disease in South America. Geneva: WHO; 1997. [ Links ]
3. Cortés A, Guhl F, Barraza M. Enfermedad de Chagas transfusional en Cali, Colombia. Colombia Médica 1995: 26:6-11. [ Links ]
4. Organización Mundial de la Salud. Universidad de los Andes. Instituto Nacional de Salud. Manual de procedimientos para el diagnóstico de la enfermedad de Chagas. Bogotá: Universidad de los Andes; 2001. p.67-72. [ Links ]
5. Grijalva MJ, Rowland EC, Powell MR, McCormick TS, Escalante L. Blood donors in a vector-free zone of Ecuador potentially infected with Trypanosoma cruzi. Am J Trop Med Hyg 1995;52:360-3. [ Links ]
6. Langhi DM Jr, Bordin JO, Castelo A, Walter SD, Moraes-Souza H, Stumpf RJ. The application of latent class analysis for diagnostic test validation of chronic Trypanosoma cruzi infection in blood donors. Braz J Infect Dis 2002;6:181-7. [ Links ]
7. Schmunis GA. Prevention of transfusional Trypanosoma cruzi infection in Latin America. Mem Inst Oswaldo Cruz 1999;94:93-101. [ Links ]
8. Oelemann W, Texeira M, Peralta J. Screening and confirmation in Chagas disease serology: a contribution. Mem Inst Oswaldo Cruz 1999;94:307-8. [ Links ]
9. Guhl F, Vallejo GA. Interruption of Chagas disease transmission in the Andean countries: Colombia. Mem Inst Oswaldo Cruz 1999;94:413-5. [ Links ]
10. Schmunis GA. Riesgo de la enfermedad de Chagas a través de las transfusiones en las Américas. Medicina 1999;59:125-34. [ Links ]
11. Beltrán M. La donación de sangre en Colombia. Boletín Red de Banco de Sangre, Instituto Nacional de Salud. 1998;2:1-2. [ Links ]
12. Ministerio de Salud. República de Colombia. Sangre segura para todos. Decreto 1571. Bogotá, Colombia; 1993. [ Links ]
13. Ministerio de Salud. República de Colombia. Resolución 01738. Bogotá, Colombia; 1995. [ Links ]
14. Beltrán M, Raad J, Ayala M, Ching R. Tamizaje de enfermedades infecciosas en bancos de sangre, Colombia, 1995. Biomédica 1997;17:137-42. [ Links ]
15. Beltrán M, Ayala M. Evaluación externa de los resultados serológicos en los bancos de sangre de Colombia. Rev Panam Salud Pública 2003;13:138-42. [ Links ]
16. Cruz JR. Basic components of a national blood system. Pan Am J Public Health 2003;13:79-84. [ Links ]
17. Saéz-Alquézar A, Otani M, Sabino E, Ribeiro do Santos G, Salles N, Chamone D. Evaluation of the performance of Brazilian blood banks in testing for Chagas disease. Vox Sang 1998;74:228-31. [ Links ]
18. Behrend M, Kroeger A, Beltrán M, Restrepo M. Control de la enfermedad de Chagas en bancos de sangre de Colombia. Biomédica 2002;22:39-45. [ Links ]
19. Guhl F. Estado actual del control de la enfermedad de Chagas en Colombia. Medicina 1999;59:125-34. [ Links ]
20. Oelemann WM, Teixeira MD, Verissimo da Costa GC, Borges-Pereira J, De Castro JA, Coura JR et al. Evaluation of three commercial enzyme-linked immunosorbent assays for diagnosis of Chagas disease. J Clin Microbiol 1998;36:2423-7. [ Links ]
21. Umezawa E S, Bastos SF, Camargo ME, Yamauchi LM, Santos MR, González A et al. Evaluation of recombinant antigens for serodiagnosis of Chagas´ disease in South and Central America. J Clin Microbiol 1999;37:1554-60. [ Links ]
22. Hamerschlak N, Pasternak J, Amato Neto V, de Carvalho MB, Guerra CS, Coscina AL et al. Chagas disease: an algorithm for donor screening and positive donor counseling. Rev Soc Bras Med Trop 1997;30: 205-9. [ Links ]
23. Mendes R, Hoshino-Shimizu S, Moura da Silva A, Mota I, Heredia R, Luquetti AO et al. Serological diagnosis of Chagas disease: a potential confirmatory assay using preserved protein antigens of Trypanosoma cruzi. J Clin Microbiol 1997;37:1829-34. [ Links ]
24. Organización Panamericana de Salud. División de Prevención y Control de Enfermedades Transmisibles, División de Sistemas y Servicios de Salud. Manual de procedimientos de control de calidad para los Laboratorios de Serología de los Bancos de Sangre.Washington DC: PAHO; 1994 (PAHO/HPC/HCT/94.21). [ Links ]














