Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biomédica
Print version ISSN 0120-4157On-line version ISSN 2590-7379
Biomédica vol.31 no.2 Bogotá Apr./June 2011
ARTÍCULO ORIGINAL
1Grupo de Investigación de Farmacoepidemiología y Farmacovigilancia, Universidad Tecnológica de Pereira, Pereira, Colombia
2Audifarma, S. A., Pereira, Colombia
Institución donde se llevó a cabo el estudio: Universidad Tecnológica de Pereira
Recibido: 21/08/10; aceptado:25/03/11
Introducción. Los inhibidores del factor de necrosis tumoral alfa han presentado un consumo creciente y generan una importante carga económica para los sistemas de salud.
Objetivo. Determinar los patrones de prescripción de inhibidores del factor de necrosis tumoral en una población de personas afiliadas al Sistema General de Seguridad Social en Salud de Colombia.
Materiales y métodos. Se trata de un estudio descriptivo observacional, de 316 pacientes que recibieron inhibidores del factor de necrosis tumoral, entre enero de 2008 y junio de 2009. Se consideraron las indicaciones, criterios de inclusión, tiempo de evolución de enfermedad, enfermedades concomitantes y reacciones adversas. Se utilizaron las pruebas t de Student y de ji al cuadrado, para la comparación de variables cuantitativas y categóricas respectivamente; se hizo un análisis multivariado.
Resultados. La edad promedio fue de 44,6±13,9 años; 63,9 % de los participantes fueron mujeres. El 17,1 % de los pacientes recibía monoterapia. El orden de prescripción de los medicamentos fue: adalimumab (37,3 %), infliximab (37,3 %) y etanercept (25,4 %), todos a dosis diarias definidas adecuadas. La medicación concomitante más frecuente fue: antirreumáticos modificadores de enfermedad (82,9 %), AINE (29,1 %), omeprazol (22,5 %), antihipertensivos (21,2 %) y ácido fólico (19,9 %). El 10,4 % de los pacientes tenía registro de alguna reacción adversa a los medicamentos. El costo promedio del tratamiento por paciente y año, fue de $23.464 dólares.
Conclusiones. Los anti-TNF se emplearon a las dosis recomendadas, principalmente en artritis reumatoide y en combinación con otros antirreumáticos. El costo directo del tratamiento se consideró elevado para el sistema sanitario del país.
Palabras clave: agentes antirreumáticos, factor de necrosis tumoral alfa, artritis reumatoide, artritis reumatoide juvenil, espondilitis anquilosante, psoriasis, Colombia.
Profile of use of anti tumor necrosis factor in Colombian patients
Introduction. Tumor necrosis factor-alpha antagonists (anti-TNFα) have shown an increasing consumption and generate a significant economic burden on health systems.
Objectives. The prescribing patterns of tumor necrosis factor-alpha antagonists were determined in a patient population associated with the Sistema General de Seguridad Social en Salud in Colombia.
Materials and methods. A descriptive observational study was conducted in 316 patients with respect to use of tumor necrosis factor-alpha antagonists during a treatment period from January 2008 to June 2009. The database examined contained indications of use, inclusion criteria to medication, duration of illness, co-morbidities and adverse reactions. The data were retrieved from the clinical histories. Student´s t test was used for the comparison of quantitative variables, and the chi-square test was used to establish associations between categorical variables and multivariate analysis were used.
Results. Mean age was 44.613.9 years; 63.9% of participants were female. Of the 316 patients, 17.1% received monotherapy. The order of prescription drugs was as follows: adalimumab (37.3%), infliximab (37.3%) and etanercept (25.4%), all were prescribed in appropriately defined daily doses. Co-medication drugs most frequently prescribed were: disease-modifying anti-rheumatic (82.9%), NSAIDs (29.1%), omeprazole (22.5%), antihypertensives (21.2%), folic acid (19.9%) calcium plus vitamin D (9.8%), calcitriol (6.0%). 10.4% of patients had a record of some adverse drug reaction. The average cost of therapy per patient per year was US$23,464.
Conclusions. Anti-TNFα are being used at recommended doses, particularly in rheumatoid arthritis and in combination with other anti-rheumatic drugs. The direct cost of therapy was high for the country´s health system.
Key words: Antirheumatic agents, tumor necrosis factor-alpha; arthritis, rheumatoid; arthritis, juvenile rheumatoid; spondylitis, ankylosing; psoriatic, Colombia.
El factor de necrosis tumoral alfa (TNFα) es una citocina proinflamatoria producida por monocitos activados, macrófagos y linfocitos T, como respuesta a diversos estímulos inflamatorios (1). El TNFα ejerce, a su vez, diversos estímulos inflamatorios en una gran diversidad de células del sistema inmunitario; dichos efectos son el producto de su potencial de actividad autocrina, así como de su capacidad paracrina para estimular la producción de otras potentes citocinas proinflamatorias, tales como IL-1, IL-6, IL-8 y el factor estimulante de colonias de granulocitos y macrófagos (2-4). El TNFα también promueve la inflamación al inducir la producción de fibroblastos y moléculas de adhesión en el endotelio y en los leucocitos (5).
El papel del TNFα en la patogénesis de enfermedades autoinmunitarias y autoinflamatorias, como artritis reumatoide, enfermedad de Crohn, espondilitis anquilosante, artritis reumatoide juvenil, psoriasis cutánea y artritis psoriásica, entre otras, está bien establecido. En artritis reumatoide y artritis reumatoide juvenil, el TNFα es un potente inductor de metaloproteinasas de matriz, que son moléculas efectoras finales en el proceso de daño articular; se sabe que los pacientes con artritis reumatoide tienen elevación de las concentraciones de la citocina en el líquido sinovial, las cuales, a su vez, se relacionan de manera directa con la aparición de erosiones óseas y con el daño radiológico (6-8). El mecanismo de lesión de la mucosa intestinal en la enfermedad de Crohn no es del todo claro; no obstante, el reporte de diversas investigaciones ha demostrado que el TNFα juega un rol central en dicho proceso (9).
Con base en el papel que juega el TNFα, como citocina proinflamatoria en las enfermedades mencionadas, parece razonable que su bloqueo pueda tener efectos favorables en el mecanismo de control de la enfermedad. Los medicamentos inhibidores del factor de necrosis tumoral (anti-TNF) se recomiendan para el tratamiento de artritis reumatoide grave activa, después de que una adecuada utilización de antirreumáticos modificadores de la enfermedad ha fallado, en espondilitis anquilosante, artritis reumatoide juvenil y artritis psoriásica resistente a los fármacos convencionales, y para el manejo de la enfermedad de Crohn de moderada a grave, en pacientes que responden en forma inadecuada a los tratamientos clásicos (10-13).
En Colombia existen varios fármacos anti-TNFα, a saber: etanercept, que es una proteína de fusión recombinante, que simula el receptor de tipo 2 del TNFα de alta afinidad y está ligado a la porción Fc de la IgG1 humana; infliximab, un anticuerpo monoclonal quimérico que liga TNFα soluble y unido a membranas, y adalimumab, un anticuerpo monoclonal humanizado que liga TNFα soluble y unido a membranas de forma similar a infliximab (10-13).
Más recientemente han aparecido otros, como certolizumab, golimumab y afelimomab. Este nuevo grupo de moléculas está por fuera del listado de medicamentos esenciales a los cuales tiene acceso la población afiliada al Sistema General de Seguridad Social en Salud (SGSSS) y sólo se puede acceder a ellos mediante solicitudes hechas por los comités técnico-científicos de los aseguradores o mediante fallos judiciales de tutela (14).
Con el objetivo de determinar el perfil de utilización de los anti-TNF y de la medicación concomitante empleada con mayor frecuencia en estos pacientes, se llevó a cabo esta investigación en personas que los estaban recibiendo para el manejo de su enfermedad, afiliadas al régimen contributivo del SGSSS en Colombia. La implantación de sistemas de información sobre las prescripciones realizadas por los médicos, ha sido fundamental para lograr una mayor calidad terapéutica de la formulación. Estas investigaciones contribuyen al uso racional de los medicamentos.
Materiales y métodos
Se hizo un estudio descriptivo observacional de corte transversal sobre la utilización de medicamentos, en una población de 1´503.678 personas en cuatro ciudades de Colombia (Barranquilla, Bogotá, Medellín y Pereira) afiliadas al régimen contributivo del SGSSS en dos diferentes Empresas Promotoras de Salud (EPS).
Los datos se recolectaron desde la revisión de las prescripciones médicas efectivamente dispensadas y se revisaron las historias clínicas durante el período comprendido entre enero de 2008 y junio de 2009.
Se incluyeron en el estudio los datos de los individuos de cualquier edad y de ambos sexos que hubiesen recibido adalimumab, etanercept o infliximab. Los nuevos anti-TNF no se incluyeron en las bases de datos de las EPS participantes por su uso muy poco frecuente.
Se recolectaron todas las variables sociodemográficas, diagnósticos que motivaron el uso del anti-TNF, tiempo de evolución de la enfermedad, los datos de medicaciones concomitantes, tipo de anti-TNF y reacciones adversas a los mismos medicamentos, en una base de datos diseñada para tal fin. Además, se registraron los datos sobre la variable dosis diaria definida, dosis por 100.000 habitantes/día y costo por mil habitantes/día (CHD) (CHD= (costo/365 x No. habitantes) x 1.000), el cual se obtuvo de los registros de facturación de cada paciente en cada una de las EPS participantes y hace referencia sólo al costo directo del medicamento.
Se aceptó la medicación concomitante como un indicador sustituto de enfermedad asociada con el diagnóstico principal, en las siguientes circunstancias: antihipertensivos/hipertensión arterial, digitálicos/insuficiencia cardíaca o fibrilación auricular, anti-diabéticos/diabetes mellitus, nitratos/enfermedad coronaria, y antiinfecciosos/infección. Por último, se revisaron las combinaciones de medicamentos que pudieran ocasionar interacciones potencialmente riesgosas, con el propósito de recomendar algunas medidas correctivas.
El protocolo fue sometido a revisión científico-técnica y bioética por las instancias correspondientes de la Facultad de Ciencias de la Salud de la Universidad Tecnológica de Pereira, y de las EPS participantes, en la categoría de investigación sin riesgo. A los pacientes participantes se les pidió su consentimiento informado para poder obtener la información de sus historias clínicas.
Los datos se analizaron con el paquete estadístico SPSS®, 18.0, para Windows. Se utilizaron las pruebas t de Student y ji al cuadrado para la comparación de las variables cuantitativas y categóricas, respectivamente. Se aplicaron modelos de regresión logística binaria. Se determinó como nivel de significancia estadística una p<0,05.
Resultados
De una población afiliada de 1´503.678 en el año 2009 en cuatro ciudades de Colombia, se encontraron 6.726 pacientes con medicamentos antirreumáticos (el 4,4 % de los afiliados). De éstos, 316 pacientes recibían alguno de los anti-TNF (4,6 % de los pacientes).
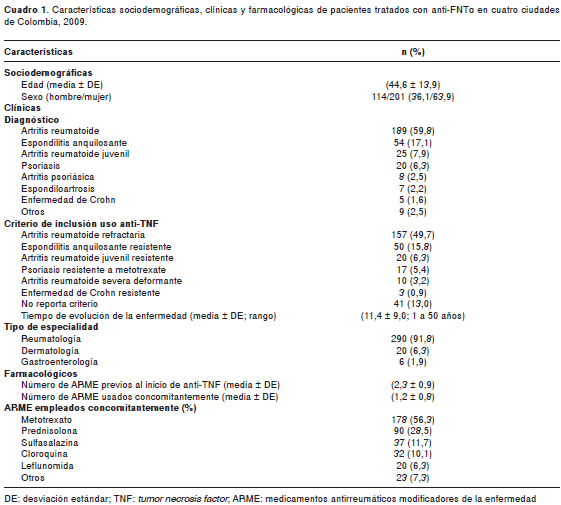
En el cuadro 1 se pueden observar las características sociodemográficas, clínicas y farmacológicas de estos pacientes. Se encontraron diferencias estadísticamente significativas entre el promedio de edad según el sexo (hombres: 41,514,5 Vs. mujeres: 46,413,4 años; p=0,003) y hubo 11 menores de 18 años (3,5 %) que recibían anti-TNF.
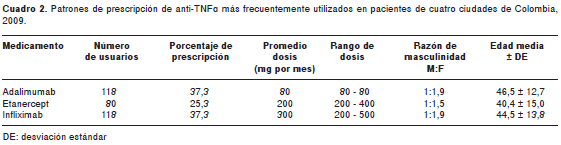
En el cuadro 2 se resumen los patrones de prescripción de los tres anti-TNF estudiados, con los cuales se estaban manejando los pacientes con artritis reumatoide y otras enfermedades articulares e inflamatorias.
Monoterapia versus asociaciones con antirreumáticos modificadores de enfermedad
Del total de pacientes del estudio, 17,1 % (n=54) recibía monoterapia con sólo un anti-TNF, mientras que 53,8 % (n=170) recibía poliquimioterapia concomitantemente con un antirreumático modificador de enfermedad, 21,8 % (n=69) recibía dos, 6,3 % (n=20) recibía tres fármacos y 0,9 % (n=3) recibía cuatro. El antirreumático modificador de enfermedad más frecuentemente empleado fue metotrexato, seguido de prednisolona; su frecuencia de uso puede observarse en el cuadro 1. El anti-TNF más utilizado en monoterapia fue etanercept (n=24, 30 % de los pacientes con este fármaco; p=0,009).
Las variables que se asociaron con una mayor probabilidad de ser tratado con poliquimioterapia, fueron: los diagnósticos de artritis reumatoide (p<0,001), psoriasis (p<0,001) o espondilitis anquilosante (p=0,002), vivir en las ciudades de Barranquilla (p<0,001) o Pereira (p=0,012), y ser tratado con adalimumab (p=0,005); mientras que no se asociaron con una mayor probabilidad de ser manejados con poliquimioterapia, las variables: diagnóstico de artritis reumatoide juvenil, enfermedad de Crohn o artritis psoriásica, vivir en Bogotá, Medellín, o ser tratado con infliximab, ni hubo diferencias con la edad o el tiempo de evolución de la enfermedad.
Al analizar mediante regresión logística binaria, la relación entre el empleo o no de politerapia anti-rreumática y otras variables, se encontró que la poliquimioterapia era más frecuente en los pacientes con artritis reumatoide que en aquellos con espondilitis anquilosante y las otras enfermedades (93,1 % frente a 68,5 %; RR=0,317; IC95%: 0,117-0,860; p=0,024), y era menos frecuente en los que vivían en Barranquilla que en otras ciudades (59,4 % frente a 90,5 %; RR=4,76; IC95%:1,916-11,755; p=0,001).
Medicación concomitante
Entre los pacientes incluidos en este estudio, 241 (76,3 %) recibían concomitantemente uno o varios de los siguientes grupos de medicamentos que reflejan enfermedad simultánea o pudieran generar interacciones con los antirreumáticos: AINE (n=92, 29,1 %), omeprazol (n=71, 22,5 %), antihipertensivos (n=67, 21,2 %), ácido fólico (n=63, 19,9 %), calcio más vitamina D (n=31, 9,8 %) y calcitriol (n=19, 6,0 %). Los AINE más frecuentemente utilizados fueron: naproxeno (n=42, 13,3 %), diclofenaco (n=28, 8,9 %) e ibuprofeno (n=9, 2,8 %).
Al analizar mediante regresión logística la relación entre el empleo o no de medicación concomitante y otras variables, se encontró que no hubo diferencias en el sexo, la edad, el anti-TNF empleado, ni la ciudad donde fue tratado. La medicación concomitante era estadísticamente significativa menos frecuente en pacientes con psoriasis que con artritis reumatoide (30,0 % frente a 80,4 %; RR=9,811; IC95%: 3,009-31,990; p<0,001) y, también, era menor en enfermedad de Crohn en comparación con artritis reumatoide (20,0 % frente a 80,4 %; RR=4,410; IC95%: 1,487-139,682; p=0,021).
Reacciones secundarias a medicamentos
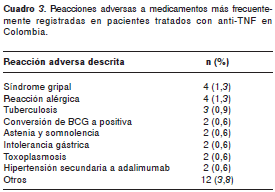
Del total de casos, un grupo de 33 pacientes (10,4 %) tenía registro de alguna reacción adversas, o secundaria, a los medicamentos, asociada con el uso de los anti-TNF. Los eventos que aparecieron con mayor frecuencia pueden observarse en el cuadro 3. No se presentaron diferencias estadísticamente significativas entre el reporte de reacciones adversas y el uso de poliquimioterapia antirreumática (p=0,86).
Comparación entre ciudades
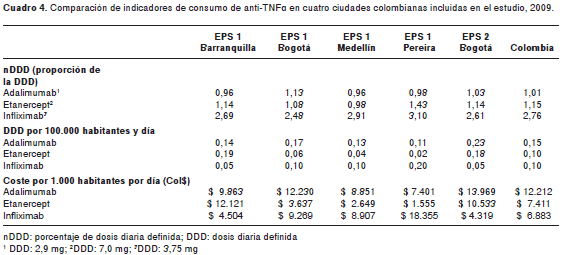
Se compararon también los indicadores asociados a la prescripción de los anti-TNF entre las cuatro ciudades colombianas incluidas en el estudio, presentados mediante los indicadores porcentaje de dosis diaria definida, dosis diaria definida por 100.000 habitantes y costo por 1.000 habitantes y día (cuadro 4) para que puedan ser útiles en comparaciones posteriores.
Costos
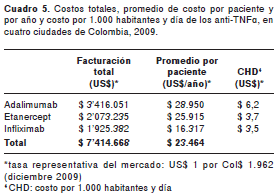
En el cuadro 5 pueden observarse los costos totales en que incurrieron las EPS, a cuenta de cada uno de los anti-TNF empleados. Se describen el costo promedio por paciente/año y el costo total por cada fármaco.
Discusión
El presente estudio representa una de las primeras aproximaciones realizadas en Colombia, soportada en una base extensa de población en el sistema de aseguramiento contributivo, sobre el perfil de prescripción de los llamados agentes biológicos; en particular, los inhibidores de citocinas proinflamatorias tales como el TNFα, los cuales han representado un gran avance en mejorar los signos, los síntomas y la calidad de vida de pacientes con artritis reumatoide, espondilitis anquilosante, enfermedad de Crohn y artritis psoriásica, y han representado un cambio dramático en la aproximación terapéutica de dichas enfermedades en los últimos años. Hoy en día, la meta deseable de los tratamientos es la remisión de la enfermedad, pese a sus elevados costos (15).
No obstante los grandes beneficios terapéuticos de etanercept, infliximab y adalimumab en las diversas enfermedades, su uso genera grandes costos a los sistemas de salud de todas las naciones (16-18). En Estados Unidos, un año de tratamiento estándar para artritis reumatoide con etanercept y adalimumab varía aproximadamente entre US$ 15.680 y US$ 22.531, costo comparable con el de infliximab, el cual oscila entre US$ 10.450 y US$ 18.110. Por esta razón, es de vital importancia para el SGSSS en Colombia, conocer los patrones de prescripción, con el propósito de analizar en ulteriores modelos farmacoeconómicos, las alternativas más costo-efectivas para apoyar la toma de decisiones (15,16,19,20).
Cabe aclarar que los anti-TNF han mostrado un importante crecimiento en su consumo en muchos de los países de altos ingresos, pero, por otro lado, algunos estudios publicados no siempre han demostrado que los costos adicionales de los productos biológicos sean compensados por la prevención de discapacidad futura, con lo que los beneficios clínicos de estos tratamientos vienen asociados a costos mayores (15,21). Algunos estudios han mostrado mejores relaciones de costo-efectividad para etanercept y adalimumab comparados con infliximab (15,22,23).
Se encontró que los hombres que recibían anti-TNFα eran significativamente más jóvenes que las mujeres, pero no se hallaron otras diferencias en cuanto a las variables sociodemográficas, lo cual difiere de algunos hallazgos hechos por Sarzi-Puttini et al., que muestran un mucho mayor predominio de mujeres, diferencias en el uso concomitante de otros ARME y en la frecuencia de enfermedades concomitantes (24). Como era de esperarse, dada la alta prevalencia de artritis reumatoide, fue ésta la enfermedad en la cual se encontró mayor utilización de anti-TNFα comparativamente con las otras enfermedades autoinflamatorias y autoinmunitarias, y es precisamente en las que las decisiones basadas en guías con soporte farmacoeconómico deberían centrarse en el futuro cercano, con el fin de evitar elevados costos al SGSSS en Colombia (15).
El perfil de medicamentos concomitantes refleja tanto el tratamiento de condiciones comórbidas, no infrecuentes en las enfermedades autoinmunitarias y autoinflamatorias, así como el tratamiento coadyuvante en el manejo de las mismas enfermedades, tal como ocurre con el uso de metotrexato en la artritis reumatoide, el cual mejora la efectividad de los mismos y disminuye la presencia de tolerancia por anticuerpos contra el medicamento (20,25,26). La monoterapia fue más común en los casos de artritis reumatoide juvenil, enfermedad de Crohn y artritis psoriásica, de acuerdo a como lo plantea la literatura científica (9,12,23). Sería importante estudiar la razón que explique el elevado uso de omeprazol, si sólo 0,6 % de los pacientes tiene registro de intolerancia gástrica.
Como efectos adversos por el uso de fármacos anti-TNFα se han reportado, fundamentalmente, procesos infecciosos, como los producidos por micobacterias atípicas, tuberculosis, listeriosis, aspergilosis, histoplasmosis, coccidioidomicosis, criptococosis y citomegalovirus (27-29). No obstante lo anterior, en nuestra población se demostró sólo tres casos de tuberculosis y dos casos de toxoplasmosis; eventualmente, este hallazgo pudiera estar reflejando una mejor selección de la condición inmunológica de los pacientes y una tamización adecuada para descartar tuberculosis latente antes del inicio del tratamiento.
Otros efectos adversos reportados con frecuencia con el uso de los anti-TNFα son enfermedad desmielinizante, síndrome similar al lupus, vasculitis, anormalidades hematológicas como anemia aplástica y linfomas (30,31), ninguno de los cuales fue encontrado en nuestra población de estudio. Sin embargo, dado el bajo número de reportes de efectos indeseados asociados a la medicación, podría interpretarse que existe un bajo registro de estos en las historias clínicas por parte de algunos de los especialistas encargados de la atención de estos pacientes.
Los tres medicamentos estaban siendo empleados a las dosis diarias definidas y recomendadas para esta indicación por la Organización Mundial de la Salud, y no se presentaron diferencias entre ciudades en este indicador. Pero sí se encontró que había diferencias en la frecuencia de uso de algunos medicamentos entre las distintas ciudades, como puede observarse en el cuadro 3, lo cual también explica las diferencias halladas entre los costos por 1.000 habitantes y día, como en el caso de infliximab en Pereira, o de, adalimumab en la EPS2 de Bogotá. Las diferencias en los patrones de prescripción entre las diferentes ciudades colombianas del estudio, no son sorprendentes, ya que la variabilidad en la atención médica, en particular en los hábitos de prescripción, es un hallazgo frecuente en los estudios farmaco-epidemiológicos (32). Estas variaciones, de importancia por sus implicaciones médicas, sociales, económicas y de salud pública, están relacionadas con características de los pacientes (edad, sexo, enfermedades concomitantes) y con estilos de práctica profesional que también resultan de factores personales y de la formación y del entrenamiento de quien prescribe (32).
Basándose en los patrones de prescripción encontrados en el presente estudio, puede afirmarse que, en general, predominan los hábitos de prescripción racional, con el empleo de medicamentos de un importante valor terapéutico, en dosis recomendadas, con diagnóstico de artritis reumatoide resistente, lo cual está de acuerdo con las recomendaciones internacionales (21) y tratados con poliquimioterapia antirreumática. Este trabajo abre la puerta para recomendar que se hagan estudios de evaluaciones económicas donde se involucren los anti-TNF que faciliten análisis de costo-beneficio y costo-efectividad, facilitando a los clínicos y a los administradores de los servicios de salud la toma de decisiones frente al mejor tratamiento para sus pacientes y al costo más racional posible.
Conflicto de intereses
Los tres autores tienen una relación contractual con Audifarma, S. A., pero expresan que esto no genera ningún conflicto de intereses, ni hubo injerencia externa en los resultados ni la presentación del estudio.
Financiación
Este trabajo fue financiado por Audifarma, S.A., y la Universidad Tecnológica de Pereira.
Correspondencia: Jorge Enrique Machado, Calle 105Nº14-140, Pereira, Colombia. Teléfono: (6) 313 7800; fax: (6) 313 7822 machado@utp.edu.co
Referencias
1. McGeehan GM, Becherer JD, Bast RC Jr, Boyer CM, Champion B, Connolly KM, et al. Regulation of tumour necrosis factor-alpha processing by a metalloproteinase inhibitor. Nature. 1994;370:558-61. [ Links ]
2. Nawroth PP, Bank I, Handley D, Cassimeris J, Chess L, Stern D. Tumor necrosis factor/cachectin interacts with endothelial cell receptors to induce release of interleukin 1. J Exp Med. 1986;163:1363-75. [ Links ]
3. Butler DM, Maini RN, Feldmann M, Brennan FM. Modulation of proinflammatory cytokine release in rheumatoid synovial membrane cell cultures. Comparison of monoclonal anti TNF-alpha antibody with the interleukin-1 receptor antagonist. Eur Cytokine Netw. 1995;6:225-30. [ Links ]
4. Haworth C, Brennan FM, Chantry D, Turner M, Maini RN, Feldmann M. Expression of granulocyte-macrophage colony-stimulating factor in rheumatoid arthritis: Regulation by tumor necrosis factor-alpha. Eur J Immunol. 1991;21:2575-9. [ Links ]
5. Chin JE, Winterrowd GE, Krzesicki RF, Sanders ME. Role of cytokines in inflammatory synovitis: The coordinate regulation of intercellular adhesion molecule 1 and HLA class I and class II antigens in rheumatoid synovial fibroblasts. Arthritis Rheum. 1990;33:1776-8. [ Links ]
6. Saxne T, Palladino MA Jr, Heinegard D, Talal N, Wollheim FA. Detection of tumor necrosis factor alpha but not tumor necrosis factor beta in rheumatoid arthritis synovial fluid and serum. Arthritis Rheum. 1988;31:1041-5. [ Links ]
7. Chu CQ, Field M, Feldmann M, Maini RN. Localization of tumor necrosis factor alpha in synovial tissues and at the cartilage pannus junction in patients with rheumatoid arthritis. Arthritis Rheum. 1991;34:1125-32. [ Links ]
8. Neidel J, Schulze M, Lindschau J. Association between degree of bone-erosion and synovial fluid-levels of tumor necrosis factor alpha in the knee-joints of patients with rheumatoid arthritis. Inflamm Res. 1995;44:217-21. [ Links ]
9. van Dullemen HM, van Deventer SJ, Hommes DW, Bijl HA, Jansen J, Tytgat GN, et al. Treatment of Crohn´s disease with anti-tumor necrosis factor chimeric monoclonal antibody (cA2). Gastroenterology. 1995;109:129-35. [ Links ]
10. Chen Y, Jobanputra P, Barton P, Jowet S, Bryan S, Clark W, et al. A systematic review of the effectiveness of adalimumab, etanercept and infliximab for the treatment of rheumatoid arthritis in adults and an economic evaluation of their cost-effectiveness. Health Technol Assess. 2006;10:1-248. [ Links ]
11. Jacobsson LT, Turesson C, Nilsson JA, Petersson IF, Lindqvist E, Saxne T, et al. Treatment with TNF blockers and mortality risk in patients with rheumatoid arthritis. Ann Rheum Dis. 2007;66:670-5. [ Links ]
12. Lee TW, Fedorak RN. Tumor necrosis factor -alpha monoclonal antibodies in the treatment of inflammatory bowel disease: Clinical practice pharmacology. Gastroenterol Clin North Am. 2010; 39: 543-57. [ Links ]
13. Sandborn WJ. State-of-the-art: Immunosuppression and biologic therapy. Dig Dis. 2010;28:536-42. [ Links ]
14. Ministerio de la Protección Social. Comisión de Regulación en Salud. Acuerdo 08 de 2009. Fecha de consulta: 1° de agosto de 2010. Disponible en: http://www.pos.gov.co/Documents/Acuerdo%20008%20Dic%2029-09.pdf. [ Links ]
15. Doan QV, Chiou CF, Dubois RW. Review of eight pharmacoeconomic studies of the value of biologic DMARDs (adalimumab, etanercept, and infliximab) in the management of rheumatoid arthritis. J Manag Care Pharm. 2006;12:555-69. [ Links ]
16. Kavanaugh A, Cohen S, Cush J. The evolving use of TNF inhibitors in rheumatoid arthritis. J Rheumatol. 2004;31:1881-4. [ Links ]
17. Wong J. Cost-effectiveness of anti-tumor necrosis factor agents. Clin Exp Rheumatol. 2005;22:S65-70. [ Links ]
18. Lambert CM. Medical therapy for rheumatoid arthritis-value for money? Rheumatology. 2001;40:961-4. [ Links ]
19. Hurst NP, Forbes J. Does economic evaluation have anything to offer the rheumatologist? Rheumatology. 1999;38:2-5. [ Links ]
20. Rat AC, Boissier MC. Rheumatoid arthritis: Direct and indirect costs. Joint Bone Spine. 2004;71:518-24. [ Links ]
21. Bertele V, Assisi A, Di Muzio V, Renzo D, Garattini S. New antirheumatic drugs: Any real added value? A critical overview of regulatory criteria for their marketing approval. Eur J Clin Pharmacol. 2007;63:879-89. [ Links ]
22. McLeod C, Bagust A, Boland A, Dagenais P, Dickson R, Dundar Y, et al. Adalimumab, etanercept and infliximab for the treatment of ankylosing spondylitis: A systematic review and economic evaluation. Health Technol Assess. 2007;11:1-158. [ Links ]
23. Bravo Y, Hawkins NS, Claxton K, Asseburg C, Palmer S, Woolacott N, et al. The cost-effectiveness of etanercept and infliximab for the treatment of patients with psoriatic arthritis. Rheumatology (Oxford). 2007;46:1729-35. [ Links ]
24. Sarzi-Puttini P, Antivalle M, Marchesoni A, Favalli EG, Gorla R, Filippini M, et al. Efficacy and safety of anti-TNF agents in the Lombardy rheumatoid arthritis network (LORHEN). Reumatismo. 2008;60:290-5. [ Links ]
25. Weinblatt ME, Kremer JM, Bankhurst AD, Bulpitt KJ, Fleischmann RM, Fox RI, et al. A trial of etanercept, a recombinant tumor necrosis factor receptor: Fc fusion protein, in patients with rheumatoid arthritis receiving methotrexate. N Engl J Med. 1999;340:253-9. [ Links ]
26. Maini R, St Clair EW, Breedveld F, Furst D, Kalden J, Weisman M, et al. Infliximab (chimeric anti-tumour necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: A randomized phase III trial. ATTRACT Study Group. Lancet. 1999;354:1932-9. [ Links ]
27. Warris A, Bjørneklett A, Gaustad P. Invasive pulmonary aspergillosis associated with infliximab therapy. N Engl J Med. 2001;344:1099-100. [ Links ]
28. Kamath BM, Mamula P, Baldassano RN, Markowitz JE. Listeria meningitis after treatment with infliximab. J Pediatr Gastroenterol Nutr. 2002;34:410-2. [ Links ]
29. Nakelchik M, Mangino JE. Reactivation of histoplasmosis after treatment with infliximab. Am J Med. 2002;112:78. [ Links ]
30. Brown SL, Greene MH, Gershon SK, Edwards ET, Braun MM. Tumor necrosis factor antagonist therapy and lymphoma development: Twenty-six cases reported to the Food and Drug Administration. Arthritis Rheum. 2002;46:3151-8. [ Links ]
31. Shakoor N, Michalska M, Harris CA, Block JA. Drug-induced systemic lupus erythematosus associated with etanercept therapy. Lancet. 2002;359:579-80. [ Links ]
32. Machado JE, Alzate JA. Patterns of antiretroviral drug prescription in 997 Colombian patients. Biomédica. 2008;28:78-86. [ Links ]














