Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Biomédica
Print version ISSN 0120-4157
Biomédica vol.32 no.2 Bogotá Apr./June 2012
REVISIÓN DE TEMA
Instituto de Zoología y Ecología Tropical, Laboratorio Biología de Vectores y Parásitos, Centro de Ecología y Evolución,Universidad Central de Venezuela, Caracas, Venezuela
Contribución de los autores: Manuel Muñoz recopiló gran parte de la parte de la información bibliográfica y del contenido en las tablas, escribió parte del manuscrito y propuso ideas de discusión general.
Juan Carlos Navarro propuso y asesoró la revisión, sugirió referencias, estilo, orden y estructura de los temas, escribió parte de las discusiones filogenéticas, epidemiológicas, de los vectores, modelos de nicho y corrigió el manuscrito.
Recibido: 12/10/11; aceptado:11/02/12
El virus Mayaro produce una enfermedad de síntomas inespecíficos y subletales, frecuentemente confundida con dengue, con síntomas de artralgias que pueden generar incapacidad laboral. Los brotes han sido esporádicos y localizados en la región selvática de la Panamazonia, posterior a su primer aislamiento en 1954 (Trinidad y Tobago). La información en la literatura científica es escasa, diversa y dispersa.
El virus Mayaro es un alfavirus filogenéticamente relacionado con el complejo del virus Semliki Forest (SFV); con el UNA, son los únicos virus de dicho complejo aislados en el Nuevo mundo. Está conformado por ARN de cadena simple de carga positiva, con longitud de 12 kb con la región 42S y 26S, que codifican para proteínas no estructurales y estructurales. El virus Mayaro presenta gran adaptabilidad para la infección en vertebrados y especificidad hacia la familia Culicidae (mosquitos) como vectores u hospedadores invertebrados.
Los factores de riesgo están asociados a zonas boscosas de la región septentrional de Suramérica y en temporada lluviosa. Se conocen dos genotipos, L (Belterra, Brasil) y D (distribución panamazónica). El ciclo enzoótico es similar al de la fiebre amarilla, que involucra a mosquitos del género Haemagogus y, como reservorios, a monos, sin descartar la participación de vectores secundarios y otros hospedadores que pudieran participar en la diseminación del virus.
El humano puede presentar viremia elevada y se ha demostrado la transmisión experimental en Aedes aegypti, Ae. scapularis y Ae. albopictus, constituyendo un riesgo para la salud pública en centros urbanos y zonas rurales cercanas a focos de virus Mayaro.
Palabras clave: Aedes, alfavirus, ecosistema amazónico, arbovirus, artralgia, filogenia, Culicidae, virus del bosque Semliki, Togaviridae
Mayaro: A re-emerging Arbovirus in Venezuela and Latin America
Mayaro virus produces nonspecific, sublethal disease symptoms, often confused with dengue, but with symptoms of arthalgias that can cause incapacitating disability. Outbreaks have been localized and sporadic in the Pan-Amazonia forest since its first isolation in 1954 (Trinidad and Tobago). The literature available is scarce, diverse and dispersed.
Mayaro virus is an alphavirus, phylogenetically related to the Semliki forest antigenic complex. UNA and Mayaro viruses are the only viruses of this complex that have been isolated in the New World. Mayaro consists of single-stranded RNA of positive charge, length of 12 kb, subdivided into genomic and subgenomic regions, which encode nonstructural and structural proteins respectively. Mayaro shows a great plasticity in vertebrate host infection, whereas high specificity in the family Culicidae (mosquitoes).
Risk factors of infection are associated with forest areas of northern South America and the rainy season. Two genotypes of MAYV have been identified, L (Belterra, Brazil) and D (widely distributed in the Pan-Amazonia). The enzootic cycle is similar to the jungle cycle of yellow fever, which involves Haemagogus mosquitoes and monkeys as reservoirs. However, the involvement of other secondary vectors and other hosts may be important in spread of the virus.
Humans may have high levels of viremia, and efficient experimental transmission has been demonstrated in Aedes aegypti, Aedes albopictus and Aedes scapularis, suggesting a significant risk to public health in urban, rural and peridomestic locations close to enzootic foci of Mayaro virus.
Key words: Aedes, alphavirus, Amazonian ecosystem, arboviruses, arthralgia, phylogeny,Culicidae, Semliki forest virus, Togaviridae.
Los virus de la familia Togaviridae y, en especial, aquellos pertenecientes al género alfavirus, han sido objeto de múltiples estudios en las décadas recientes debido, en gran medida, a su importancia como agentes causales de algunas zoonosis que han generado epizootias y epidemias recurrentes como, por ejemplo, la encefalitis equina venezolana, del este y oeste (1,2). Muchos de estos virus circulan de manera permanente en un ciclo enzoótico que involucra animales silvestres que habitan en ambientes cercanos donde se desarrollan actividades antrópicas (1-4). Si bien en muchas ocasiones es difícil identificar las causas que ocasionan un brote en una localidad específica, se sabe que factores tales como las mutaciones ocurridas entre hospedadores, las modificaciones antrópicas (uso de la tierra y actividades turísticas y económicas), el cambio climático, el crecimiento de la población, las malas condiciones sanitarias y la carencia de servicios básicos, pueden llegar a jugar un papel importante en la emergencia y reemergencia de las zoonosis causadas por estos virus (3-8).
Los factores implicados en la transmisión de virus se caracterizan por ser dinámicos e interdependientes. Este hecho hace necesario evaluar el problema epidemiológico como un sistema complejo que involucra varios niveles, todos ellos interconectados y relacionados. Con esta visión surge la eco-epidemiología, la cual se aproxima a las enfermedades con una perspectiva integral, concibiendo a las mismas como procesos complejos y diversos (9). Entre estos parámetros presentamos una revisión de los puntos más sobresalientes de la ecología, transmisión, evolución, estructura y sintomatología del virus Mayaro, de importancia en la actualidad debido a las brotes intermitentes en la zona septentrional de Suramérica, en especial en la localidades rurales cercanas a la selva amazónica (10-12).
El virus Mayaro, cuyo nombre se debe a la localidad donde fue aislado por primera vez, en Trinidad y Tobago en 1954, pertenece a la familia Togaviridae, género Alfavirus, el cual incluye a otros 29 virus, entre ellos los agentes causales de la encefalitis equina del este, la encefalitis equina venezolana, la encefalitis equina del oeste y la fiebre Chikungunya (1,2,13). El virus Mayaro es un arbovirus (Arthropod Borne Virus, dado que intervienen artrópodos en su ciclo de transmisión como vectores o transmisores) que se mantiene en la naturaleza en un ciclo que involucra principalmente a primates no humanos de vida silvestre y a mosquitos de la familia Culicidae (Diptera: Nematocera) de hábito selvático, en especial, especies pertenecientes al género Haemagogus. Sin embargo, no se descarta la posibilidad de que intervengan, en forma secundaria, otros vectores y hospedadores (1,2,10-13).
Estructura molecular del virus y sus relaciones con otros alfavirus
El virus Mayaro, como todos los alfavirus, posee material genético que está conformado por ARN monocatenario de sentido positivo, el cual posee una longitud de 11.429 nucléotidos (14). El hecho de poseer ARN de material genético, le da a este virus una gran adaptabilidad debido a la alta tasa de mutaciones, lo que aumenta la probabilidad de adaptación a nuevos organismos, tanto vertebrados como invertebrados, que pueden servir de hospedadores (1,2,15-22).
El material genómico de los alfavirus, incluyendo al virus Mayaro, puede subdividirse en dos regiones: la subregión genómica, o región subgenómica 5´, que constituye dos tercios del genoma y codifica para proteínas no estructurales (nsP1, nsP2, nsP3 y nsP4), y la subregión subgenómica 3´, que representa un tercio del genoma y codifica para proteínas estructurales (E1, E2, E3, C, y 6K) (15-21). En la figura 1 se presenta de manera esquemática el genoma de los alfavirus. La región no estructural suele ser más conservada que la región estructural, entre los diferentes virus del género alfavirus, encontrándose, al menos, 60 % de similitud en cuanto a secuencias de aminoácidos en la primera subregión, en comparación con el 45 % encontrado en la región subgenómica (2).
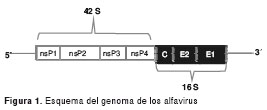
El genoma de estos virus forma un complejo con la proteína del núcleo (proteína C), formando una nucleocápside icosaédrica (15-21). Las proteínas de envoltura celular que rodean la cápside, están formadas por restos de la membrana plasmática de células hospedadoras y por dos glucoproteínas, E1 y E2 (espículas); usualmente, la E3 se desprende de la mayoría de los alfavirus (15-19). Las glucoproteínas de envoltura se insertan en la membrana lipídica, proyectándose hacia el 11,9 para asociarlos fenotípicamente en grupos. A partir de pruebas inmunoquímicas, como la fijación del complemento, la inhibición de hemaglutinación y la prueba de neutralización por reducción de placas, se han podido determinar siete complejos antigénicos (1,2,15-17). El virus Mayaro se encuentra dentro del complejo del virus del Semliki Forest (SFV), junto con los virus Chikungunya, O´nyongnyong, del río Ross, el Getah, el Sagiyama, el Bebaru, el UNA y el SFV (1,2,10).
Las relaciones evolutivas (métodos bayesiano y de parsimonia máxima) entre secuencias de la glucoproteína E1 de diferentes alfavirus (1), la cual tiene actividad de hemaglutinina y contiene epítopos responsables de la reacción cruzada, se muestra en la figura 2. La topología del árbol sugiere que el “clado” (clade) para el virus Mayaro (1) es similar a la agrupación por complejos antigénicos encontrados al emplear pruebas inmunoquímicas.
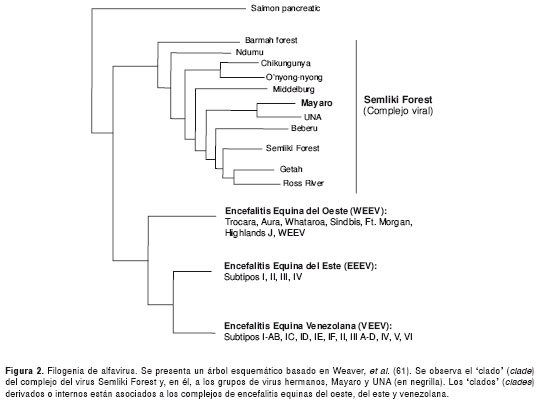
Biogeográficamente, a excepción de los virus Mayaro y UNA, la mayoría de los virus pertenecientes al “clado” (clade) del Mayaro en la figura 2 y al complejo antigénico del virus del Semliki Forest, han sido localizados únicamente en el Viejo Mundo (1). Algunos autores proponen que el virus Mayaro fue introducido en el Nuevo Mundo después de la divergencia de los complejos antigénicos virus del bosque Semliki y virus Sindbis (WEEV complex) hace 2.000 a 3.000 años. En este contexto, los autores postulan que las aves migratorias y los humanos jugaron un papel importante en la dispersión. No obstante, esta posición parafilética desde el punto de vista biogeográfico podría explicarse por la introducción de un grupo viral ancestral para ambos virus (Mayaro y UNA), por la ausencia de aislamiento viral de un ancestro de este grupo en el Nuevo Mundo, o por ambas circunstancias.
Replicación del virus
La entrada del virus en la célula hospedadora es mediada por receptores y ocurre mediante un proceso de endocitosis. La glucoproteína E2 es responsable del contacto entre partículas virales y la superficie celular, ya que los anticuerpos anti-E2 pueden neutralizar la capacidad de infección viral, lo cual no se observa al emplear anticuerpos anti-E1 (2,15-21). Una vez que la E2 interactúa con el receptor específico, el virus es introducido en una vesícula endocítica. A continuación, la envoltura vírica se fusiona a la membrana del endosoma, una reacción que es mediada por E1 y que es dependiente de un proceso de acidificación de la vesícula. Estas alteraciones en el pH y los cambios en la concentración iónica intracelular, favorecen la replicación viral (15-19). Estas reacciones permiten la liberación de la nucleocápside, que al perderla libera el genoma viral al citoplasma celular. Una vez en el citoplasma, el genoma del alfavirus se une a los ribosomas para sintetizar las proteínas no estructurales (15-19).
El aumento de la permeabilidad de la membrana de la célula hospedadora y los cambios de concentración iónica alteran la actividad enzimática de la célula, lo cual favorece la traducción del ARN vírico sobre el ARNm celular, que impide la reconstrucción y el mantenimiento de la célula, y es la causa principal de la muerte de la células infectadas (17); además, la nsP2 o cápside entra al núcleo e interfiere con la transcripción de la célula hospedera.
Ciclo de transmisión del virus Mayaro, artrópodos vectores
El virus Mayaro, como arbovirus, se caracteriza por ser transmitido por un artrópodo, conocido como vector (10-12,22). Los artrópodos presentan una gran capacidad adaptativa, que se manifiesta en su distribución cosmopolita, que favorece la diseminación y la presencia de arbovirus en gran parte del planeta. Los insectos vectores presentan un hábito hematófago, esencial para la producción de huevos y la oviposición, por lo que su capacidad reproductiva está muy influenciada por la frecuencia de la ingestión, lo cual favorece la capacidad de contacto entre los arbovirus y los hospedadores vertebrados (23-26).
En el caso del virus Mayaro y de casi todos los alfavirus, 80 % de los artrópodos capaces de actuar como vectores pertenecen a los mosquitos de la familia Culicidae, lo que revela una estrecha relación evolutiva entre ambos grupos (1). Esto trae como consecuencia directa que el combate de las patogenias causadas por estos virus se asocie al control de las poblaciones de los insectos vectores y a la disminución del contacto potencial con vertebrados domésticos y humanos. Se reportó el contagio del virus Mayaro por vía aérea o aerosol en un trabajador de laboratorio que preparaba antígenos virales (27,28), lo cual se considera una vía epidemiológicamente no significativa.
No obstante tener una alta tasa de mutación que incrementa la posibilidad de replicarse en distintos hospedadores, los alfavirus son específicos en cuanto a los vectores empleados. Esta especificidad se debe a un largo proceso de evolución y adaptación del virus a vectores eficientes (1,18,22,28). El punto clave de esta especificidad, probablemente, son los receptores localizados en el intestino medio (mesenterón) de los mosquitos hematófagos, que les permite atravesar diferentes barreras dentro del vector y pasar al sistema circulatorio (29-33).
Los mosquitos hembra adquieren los alfavirus al alimentarse de un hospedador infectado que presenta concentraciones del virus en sangre lo suficientemente altas para que el insecto hematófago lo ingiera (umbral de infección) (31-33). Una vez que el virus ha sido ingerido, infecta las células epiteliales del intestino medio, o mesenterón, del mosquito; los virus se multiplican y posteriormente atraviesan la lámina basal para alcanzar la hemolinfa. Luego, invaden las glándulas salivales, donde establecen una infección persistente y se multiplican. En las glándulas salivales, el virus es liberado junto con la saliva cuando los mosquitos tienen otra ingestión sanguínea; este período se llama período de incubación extrínseca (17,29-33). Para que un mosquito en particular sea considerado vector natural y comprobado de cualquier virus, es necesario que el ciclo descrito anteriormente se cumpla totalmente.
Entre 1977 y 1978 ocurrió un brote de virus Mayaro en Belterra, Brasil, el cual coincidió con una epidemia de fiebre amarilla en la zona, por lo que existió la sospecha de que estuvieran involucrados los mismos vectores (27,34). En la zona, se procesaron 9.000 mosquitos de 26 especies, pero el virus Mayaro sólo se aisló en Haemagogus janthinomys (Dyar), el principal vector de la fiebre amarilla en su ciclo selvático (22,27,35-38). Se recolectaron 736 mosquitos de esta especie, en los que se aislaron nueve cepas de virus Mayaro y dos de fiebre amarilla (22,27). Una proporción importante se recolectó a nivel del suelo, lo que sugiere una mayor probabilidad de contacto de estos mosquitos infectados con los humanos (10,33). La tasa mínima de infección por virus Mayaro se estimó en 1:82, mientras que la de fiebre amarilla fue de 1:368 (27). Estos resultados parecen indicar que Hg. janthinomys fue el principal vector del virus en Belterra (27).
Varios estudios han coincidido y han identificado como los principales vectores del virus Mayaro a los mosquitos del género Haemagogus (1,10-13,22,33,39), en los cuales se ha logrado aislar al menos 38 cepas del virus, mientras que en cinco aislamientos se logró recuperar, entre otros, cuatro géneros pertenecientes a cuatro tribus de Culicidae: Culex, Sabethes, Psorophora y Coquillettidia (33,40). La mayoría de los aisla-mientos del virus Mayaro en mosquitos se obtuvo a partir de Haemagogus recolectados en Brasil durante períodos interepidémicos, lo cual sugiere que podrían estar desempeñando un importante papel en el mantenimiento del virus en su ciclo enzoótico (33) (figura 3). Por otra parte, en muchas localidades donde abundan estas especies se ha encontrado alta seroprevalencia de anticuerpos contra virus Mayaro en monos de vida silvestre, que son la fuente alimentaria predilecta de los mosquitos Haemagogus; en los humanos, existe mayor seroprevalencia contra el virus Mayaro en la población de trabajadores agrícolas y exploradores (10-13,33,39), patrón similar al que se presenta con el virus de la fiebre amarilla.
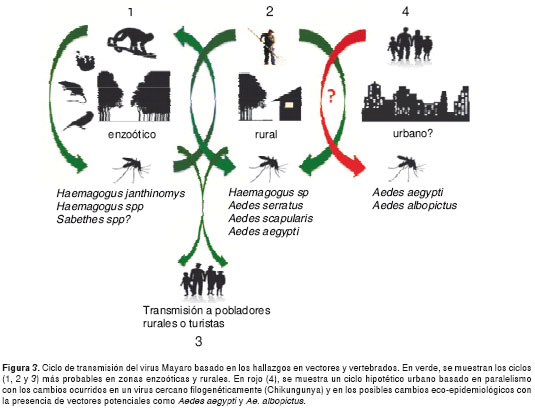
Los mosquitos del género Haemagogus presentan un hábito selvático, en bosques tropicales lluviosos o de galería, con hábito de alimentación diurno, mayores densidades arborícolas en la cercanía al dosel de los árboles, y coinciden temporal y espacialmente con el nicho de los monos, su principal fuente de ingestión sanguínea (41-43). Las hembras ponen los huevos en huecos de árboles y bambús rotos (35,42,44-48), pero también pueden utilizar recipientes artificiales, como cauchos, latas, tobos y otros que acumulan agua en zonas rurales y periurbanas (42,43,46).
Con bajo grado de antropofilia, los mosquitos Haemagogus presentan adaptabilidad alimentaria y en condiciones excepcionales o en temporadas de lluvia, en horas de baja humedad relativa en el dosel del bosque, o cuando aumentan sus densidades, pueden encontrarse a nivel de la tierra, alimentándose de humanos y animales silvestres cuando estos invaden su nicho biológico o habitan en zonas aledañas (10,33,43,49). Los mosquitos de este género presentan una gran capacidad de vuelo. En zonas abiertas se ha observado que son capaces de recorrer entre 250 y 350 metros; sin embargo, algunos estudios han encontrado que son capaces de recorrer distancias cercanas a los 11 km en búsqueda de alimento, longitud que puede aumentar según las condiciones ambientales, a un estimado de 50 km o más (22,33). Este hecho implica que estos mosquitos presentan un área de actividad muy amplio, la cual muchas veces coincide con caseríos rurales y tierras explotadas agrícolamente, lo cual aumenta su probabilidad de contacto con humanos y animales domésticos (49). En algunos estudios se ha reportado recolección de estas especies en las cercanías de viviendas rurales cercanas a áreas boscosas (43,49).
En otros mosquitos de la familia Culicidae se ha logrado aislar el virus Mayaro en condiciones ambientales: Psorophora ferox (Humboldt), Coquillettidia venezuelensis (Theobald), Culex spp.,con aislamientos fortuitos en muestras provenientes de Panamá, Trinidad-Tobago y Brasil, respectivamente, y Sabethes spp., del cual se recuperaron dos aislamientos en Brasil (33,40,50). Sabethes spp. tiene un comportamiento similar a Haemagogus, ambos vectores secundarios del virus de la fiebre amarilla (35,38,42,49,51). En otros artrópodos, el virus también fue aislado en un pool de ácaros pertenecientes al género Gigantolaelaps, asociados a cuatro roedores del género Oryzomys en Belém, Brasil (33,40) y en Ixodes spp. en el estado de Pará (10). Sin embargo, no existen suficientes indicios que permitan suponer que estos ácaros estén involucrados de manera preponderante en el ciclo de transmisión y de mantenimiento del virus Mayaro en la naturaleza.
Uno de los pocos indicios que podrían sugerir la posible participación de otros mosquitos en la transmisión del virus Mayaro, es el reporte que hacen del primer brote de la enfermedad generada por este agente causal en Venezuela (52). Los primeros casos de infección por virus Mayaro en este país se presentaron en cuatro familiares que compartieron una cena fuera de las viviendas en las cercanías a la Estación Agrícola Padrón, en el estado Miranda, localidad enzoótica para el virus de encefalitis equina venezolana (52,53). Los pacientes relataron que fueron picados múltiples veces por mosquitos durante la cena, lo que condujo a los autores a asociar la enfermedad con este hecho. Basándose en el estudio y en el muestreo de mosquitos realizado previamente para encefalitis (53) en la localidad, los autores concluyeron que los pacientes contrajeron el virus como consecuencia de las picaduras de mosquitos Hg. celeste (Dyar y Núñez-Tovar). El hábito diurno de este género no coincide con la asociación descrita, por lo que es posible que un mosquito de hábitos nocturnos o crepusculares sea competente para transmitir el virus de Mayaro de forma ocasional. Entre los candidatos a esta transmisión están Aedes scapularis (Rondani), Ae. serratus (Theobald), Ps. cyanescens (Coquillet) y los mosquitos de los géneros Mansonia, Culex y Coquillettidia de los capturados en la zona (53). Otra posible explicación a este reporte de posible transmisión atípica (52), es que este sea realmente causado por virus UNA, el cual fue aislado en la misma localidad (53), cepa que fue utilizada para enraizar los análisis filogenéticos por Powers, et al. (10). En las pruebas ELISA de captura no se usaron antígenos contra el virus Mayaro, lo que podría subestimar una posible reacción cruzada entre los virus UNA y Mayaro (52).
Mediante inoculación por vía parenteral, mosquitos de las especies Ae. serratus, Culex quinquefasciatus (Say), Mansonia arribalzagai (Theobald), Mansonia wilsoni (Barreto y Coutinho), Ps. ferox y Cq. venezuelensis, son capaces de albergar al virus Mayaro por 12 días; sin embargo, ninguna ha sido capaz de trasmitirlo (33,37,50), acción que sí se logra con las especies Ae. scapularis, Ae. aegypti (L.) y Ae. albopictus (Skuse) (33,40,50,54). Este hecho sugiere a Ae. scapularis como un vector potencial en brotes epidémicos donde la densidad de Haemagogus sea baja, mientras que Ae. albopictus podría ser también un vector potencial debido a su creciente dispersión e invasión en varios países de América del Sur, como Brasil, Colombia, Trinidad y Venezuela (54-59).
La capacidad vectorial del género Aedes es un factor epidemiológico que aumentaría la probabilidad de introducir al virus en un ciclo domiciliario. Ae. scapularis y Ae. albopictus son especies originalmente silvestres. Sin embargo, se encuentran en franca expansión geográfica; pueden aprovechar distintos y diversos tipos de hábitats, y presentan una gran capacidad adaptativa a ambientes con perturbación antropogénica, y pueden utilizar como criaderos desde bambús rotos y hojas caídas hasta recipientes artificiales como cauchos y floreros (54-60). Ambas especies presentan adaptabilidad alimentaria y, si bien se alimentan principalmente de otros mamíferos diferentes al hombre, han sido capturados con hábito endofílico y endófago (54-59). Aedes albopictus, que se ha reportado en, al menos, 28 países, se considera el segundo vector más importante de los virus causales del dengue y vector comprobado de otros 20 virus (54-57). Por sus hábitos, estas especies representan, potencialmente, un puente ideal entre el ciclo selvático y el entorno doméstico.
Un caso interesante, con posiblemente muchos paralelismos eco-epidemiológicos, lo representa el virus Chikungunya, originario de África tropical y también perteneciente al complejo SFV, cuyos vectores selváticos de hábitos arborícolas pertenecen al género Aedes. Este virus tiene un ciclo selvático similar al de la fiebre amarilla. Por otra parte, en Asia y África han ocurrido casos de transmisión urbana y suburbana asociados a Ae. aegypti y Ae. albopictus, con humanos como hospedadores amplificadores del virus (61,62).
Recientemente, el virus Chikungunya fue introdu-cido en Europa, con casos de transmisión autóctona asociada a Ae. albopictus (63,64), mientras que varios estudios han demostrado que una mutación y sustitución de aminoácidos en la posición 226 de la glucoproteína de envoltura E1 del virus Chikungunya es responsable de la mayor propensión de Ae. albopictus a este virus y de los brotes en la isla francesa de La Reunión (65-67). Por estos hallazgos, se teme la introducción en el continente americano del virus Chikungunya, sumado a la presencia de Ae. albopictus en Estados Unidos, así como en otros países del continente. Además, en Latinoamerica, Ae. aegypti se encuentra en grandes densidades y en algunos países también está presente Ae. albopictus.
Este tipo de cambio de vectores principales, como el ocurrido con el virus Chikungunya, podría presentarse con el virus Mayaro si, por alguna mutación en el virus o por cambios ecológicos, encuentran como vectores eficientes a Ae. aegypti o Ae. Albopictus; esto podría provocar brotes epidémicos urbanos o suburbanos, con consecuencias tan graves como las que tiene actualmente la transmisión del dengue. Por estas y otras características potenciales, Weaver y Reisen (62) proponen al virus Mayaro como uno de los seis arbovirus con riesgo de posible transmisión urbana.
Aedes aegypti,con alto grado de antropofilia y presente en grandes densidades en muchas ciudades de la región neotropical (68), posee potencial como vector del virus Mayaro y constituye un factor de riesgo importante, en un ciclo urbano del virus y una rápida propagación del agente causal entre humanos. Las pruebas de introducción del virus Mayaro en ciudades, como el caso de São Paulo (69) de tres personas positivas provenientes de zonas enzoóticas, son llamados de alerta. Sin embargo, no se ha registrado transmisión en localidades urbanas ni aislamientos del virus en Ae. aegypti. El aumento de la intervención y urbanización de zonas boscosas ha expandido su distribución, pudiéndose encontrar cada vez más en muestreos realizados en zonas peridomésticas y rurales, lo que se traduce en un mayor acercamiento de este eficiente vector a las zonas periselváticas en donde podría estar circulando el virus Mayaro (49,70).
El brote más reciente de virus Mayaro se presentó entre febrero y marzo de 2010, en la localidad de La Estación, Ospino, estado Portuguesa, Venezuela, con 72 casos humanos (71). No se han publicado datos que permitan inferir cuál o cuáles especies de mosquitos podrían estar involucradas en la transmisión del agente infeccioso en la localidad. El número tan elevado de afectados podría sugerir potencialmente la participación de Haemagogus en alta densidad o de otro u otros mosquitos más antropofílicos y de mayor abundancia relativa. En Santa Lucía, otra localidad del estado Portuguesa, ubicada aproximadamente a 56 km en línea recta de Ospino, en donde se reportaron casos de fiebre amarilla en humanos en 2005, se ha demostrado superposición del nicho entre mosquitos selváticos Haemagogus, Sabethes spp. y Ae. aegypti, en zonas de alta y baja influencia humana (49), lo cual sugiere que los casos de fiebre amarilla pudieron haber sido un brote selvático espurio (con características urbanas). Un caso similar al de Santa Lucía podría haberse presentado en Ospino, lo que sería de gran importancia epidemiológica. Es necesario llevar a cabo estudios entomológicos y epidemiológicos para identificar los posibles vectores que pudieron haber intervenido en el brote de Ospino, lo que permitiría formular nuevas hipótesis sobre el ciclo de transmisión del virus Mayaro. Debe considerarse que podría presentarse una exportación del virus fuera de las áreas enzoóticas debido a la creciente ocupación humana de áreas boscosas cercanas a zonas rurales-periurbanas, en las cuales coexisten en una misma localidad (junto a vertebrados reservorio) especies de mosquitos selváticas como Haemagogus, especies rurales-selváticas como Ae. serratus y especies urbanas como Ae. aegypti (49,53). El ciclo enzoótico más probable y los posibles ciclos alternos se muestran en la figura 3.
En el cuadro 1se muestra un resumen de los vectores que se han asociado como potencialmente involucrados en la transmisión del virus Mayaro.

Ciclo de transmisión del virus Mayaro, hospedadores vertebrados
El virus Mayaro infecta a un hospedador vertebrado cuando es introducido en su torrente sanguíneo, a partir de la picadura de un mosquito vector. En contraste con lo que ocurre en los invertebrados, en los cuales los alfavirus son muy selectivos a la hora de utilizarlos como hospedadores, en los vertebrados tienen gran adaptabilidad y pueden reproducirse de manera exitosa en organismos pertenecientes a diferentes clases (1,2) (figura 3). Este hecho parece obedecer a una estrategia evolutiva de los alfavirus, los cuales presentan mutaciones muy frecuentes, lo que les permite infectar una amplia variedad de vertebrados, compensando así los cortos períodos de gran viremia que originan en los mismos (1,2). Así, por ejemplo, el virus Mayaro se ha aislado en lagartos y primates en la zona tropical (33,40) y en un ave migratoria en Estados Unidos (33,72). Al mismo tiempo, se han detectado anticuerpos en los órdenes Primata, Xenarthra, Marsupialia, Rodentia y Carnívora, y, además, en aves (33,40,41). A diferencia de lo que ocurre en los insectos, la infección de los alfavirus en células de vertebrados dura pocos días (17).
Los alfavirus se mantienen en la naturaleza en un ciclo enzoótico que involucra mosquitos selváticos y animales silvestres, incluyendo en muchos casos roedores, aves o ambos (2). Los vertebrados que participan en el ciclo enzoótico son los principales amplificadores de los alfavirus en condiciones naturales; estos últimos, mediante un largo período de evolución, tienen la capacidad de alcanzar niveles de viremia lo suficientemente altos como para infectar a mosquitos que ingieran la sangre del vertebrado, sin que se presenten síntomas de la enfermedad (2,31). Estos vertebrados se denominan reservorios y, en el caso del virus Mayaro, existen varios datos, no muy claros aún, sobre los verterbrados que podrían participar como reservorios y mantenedores del ciclo enzoótico o como hospedadores multiplicadores y fuente de infección en epizootias (10-12,33,39-41).
Algunos de los hallazgos en campo tienen relación con zonas boscosas tropicales de Brasil, Panamá, Trinidad y Tobago, Colombia, Guayana Francesa, Honduras y Guatemala, donde se ha logrado detectar altos niveles de seroprevalencia en monos (11,12,33,39-41), incluso, en algunas regiones donde se ha reportado en localidades rurales aledañas casos por virus Mayaro; por ejemplo, en 1978 en Belterra, Brasil, se detectaron anticuerpos contra el virus Mayaro en el 27 % de monos Callithrix, mientras que sólo el 1 % de las aves examinadas presentaban anticuerpos (27,33).
En la Guayana Francesa, cerca de la localidad de Oyapock, donde en 1998 se reportó seroprevalencia de virus Mayaro en humanos, encontraron corre-lación entre la seroprevalencia para este virus y el hábito diurno y arbóreo (mayor densidad en el dosel de los árboles) de animales silvestres, lo que coincide espacial y temporalmente con los hábitos de los mosquitos Haemagogus (41). La mayor seroprevalencia se presentó en mamíferos pertenecientes al orden Primata, así: en 98 Alouatta seniculus (52 %), en 5 Pithecia pithecia (80 %), en 6 Saimiri sciureus (67 %) y en 42 Saguinus midas (19 %). Sin embargo, en aquellas especies en las que se observó una mayor prevalencia (primates) se presentaban títulos bajos de anticuerpos, mientras que en aquellas con menor seroprevalencia (puercoespines, marsu-piales y cuchicuchis o kankajoues), los títulos de anticuerpos fueron más altos. Este hecho fue explicado por los autores (41) como una respuesta del sistema inmunitario al contacto continuo del virus con los primates silvestres, mientras que aquellos grupos que usualmente no se infectan con el virus presentan respuestas inmunitarias más fuertes. Estos resultados permiten sugerir que los primates silvestres pueden jugar un importante papel como reservorios, mientras que otros vertebrados pueden desempeñarse como fuente de infección por sus altos títulos del virus Mayaro.
Se ha encontrado también importante seropreva-lencia en mamíferos del orden Xenarthra (perezas o perezosos), como Choloepus didactylus, Dasypus novemcinctus y Tamandua tetradactyla (41), en agutíes estrictamente diurnos (41) y en roedores Oryzomys, Proechimys y Nectomys (27). Experimentalmente, se ha determinado que los monos titíes Callithrix argentata y Callithrix humeralifer, por vía subcutánea, son capaces de desarrollar viremias suficientemente elevadas para lograr la infección en vectores vulnerables (27,33). Por otro lado, un primate del género Cebus (capuchino) inoculado por vía subcutánea, presentó leucopenia y viremia alta de cuatro a seis días, y posteriormente inmunidad, mientras que los primates Cynomolgus y Rhesus inoculados subcutáneamente también son capaces de desarrollar viremia (33). En futuras investiga-ciones se debe evaluar la posible participación de estos organismos como reservorios u hospedadores terminales en el ciclo de transmisión del virus, o determinar si su alta seroprevalencia es el resultado de la adaptabilidad alimentaria de los vectores.
Epidemiología molecular del virus Mayaro y modelos de nicho en vectores
Powers, et al. (10), encontraron dos “clados” (clades)filogenéticos (genotipos L y D) para el virus Mayaro utilizando 60 aislamientos del virus obtenidos en humanos, mosquitos Haemagogus y Coquillettidia, garrapatas (Ixodes) y primates silvestres, entre los años 1954 y 2003, mediante secuencias de nucleótidos de la región subgenómica que codifica para las glucoproteínas E2 y E1 (10). La divergencia genética entre las secuencias estuvo entre 15 y 19 %. El genotipo D está representado por cepas aisladas entre 1954 y 2003, en Trinidad y Tobago y la región norcentral de Suramérica, incluyendo Perú, Guayana Francesa, Surinam, Brasil y Bolivia; entre estas se encontró una divergencia de 0,05 a 5,9 %. El el genotipo L, está representado únicamente por seis aislamientos obtenidos todos en Brasil, con una divergencia de 0,1 a 0,3 %.
Los serotipos L y D coexisten en Belterra, Brasil, y probablemente lo han hecho durante varias décadas, al menos, cuatro. Sin embargo, no existen pruebas de que estos genotipos estén inter-cambiando material genético por recombinación, puesto que todos los aislamientos pertenecían al “clado” (clade) D o al L (no existe parafilia). Estos autores sugieren que ambos genotipos no comparten hospedadores (10). Debido a que el genotipo D tiene mayor extensión geográfica, se postula que el genotipo L se origina como consecuencia de la introducción del virus Mayaro en especies locales, entre las cuales el arbovirus se ha mantenido circulando. Por otro lado, el genotipo D constituye un grupo muy conservado genética-mente, no obstante su amplia distribución, lo que sugiere que las barreras y distancias geográficas no han impedido el flujo genético (10) (figura 3).
Los modelos de nicho ecológicos estimados para 14 especies de Haemagogus mediante algoritmos de máxima entropía (73), demuestran superposición y correlación con el patrón evolutivo de la introducción al continente americano por Brasil y dispersión del virus de fiebre amarilla calculado mediante reloj molecular y modelos bayesianos. Los patrones de modelo de nicho asocian a determinadas especies como responsables de la dispersión del genotipo I hacia el resto del continente, así como la evolución in situ del genotipoII del virus de fiebre amarilla. Los modelos de nicho para Haemagogus podrían explicar, igualmente, la distribución del genotipo D del virus Mayaro asociado a la transmisión por una mayor variedad especies, como Hg. capricornii, Hg. celeste y Hg. equinus; mientras que el genotipo L, hasta ahora restringido a Belterra (Pará, Brasil) y relacionado con una transmisión muy asociada a Hg. janthinomys, muestra la mayor probabilidad de nicho justo para el estado de Pará (73). Esta hipótesis apoyaría que la poca divergencia demostrada dentro de cada genotipo debe estar relacionada con una escasa diversidad de hospedadores vertebrados en una transmisión local (10).
Por lo general, los primates silvestres presentan rangos limitados de movilidad en comparación con las aves, las que son capaces de recorrer cientos de kilómetros sin tener mayores limitaciones por barreras geográficas (10,33). Un patrón similar al mostrado por el virus Mayaro se observa en Norteamérica en el virus de la encefalitis equina del este, donde se ha demostrado que las aves migratorias juegan un papel importante en la diseminación (10). La distribución del genotipo D podría sugerir que las aves pueden estar involucradas en la diseminación del virus Mayaro (10) (figura 4).
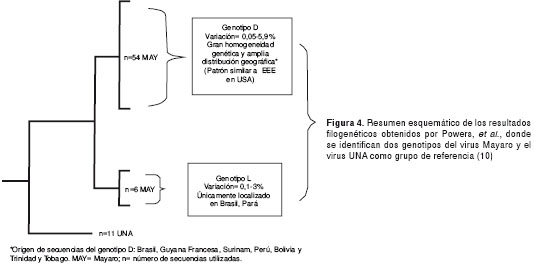
Calisher, et al., reportaron, en 1967 el único aislamiento de virus Mayaro en un ave, el cual se obtuvo de una oropéndola americana (Icterus spurius) en Louisiana, Estados Unidos, localidad que es un paso frecuente de aves migratorias (72). La especie Icterus spurius se caracteriza por ser aves que habitan principalmente en zonas semiabiertas con árboles caducifolios, localizadas al sureste de Estados Unidos. Estas aves migran en invierno al sur a través de Centroamérica, Colombia y el noroeste de Venezuela. Los autores descartaron que las aves participaran en el ciclo enzoótico del alfavirus y asumieron la infección accidental, debido a que un año después del aislamiento (1968) no se detectaron anticuerpos anti-Mayaro en un grupo de aves migratorias recolectadas en la misma localidad, entre las que se incluyeron 40 oropéndolas americanas y 126 aves de otras 27 especies.
Posteriormente, se han detectado niveles bajos a moderados de seroprevalencia en aves, con excepción de los organismos pertenecientes al género Columbigallina (33,40), en los cuales se ha reportado seroprevalencia de 29 % en Belterra (27).
Si bien, Powers, et al., sugieren la participación de aves, debido a la amplia distribución y poca divergencia del genotipo D, el patrón mostrado por los brotes de virus Mayaro registrados en Suramérica parecen estar más relacionados con un ciclo similar al de la fiebre amarilla, con focos localizados y distantes y brotes periódicos (10).
En el cuadro2 se resumen los principales aspectos discutidos con respecto a los potenciales hospedadores involucrados en la transmisión del virus Mayaro.

Brotes en humanos, sintomatología y diagnóstico
En humanos, el virus Mayaro es capaz de alcanzar niveles de viremia similares a los reportados en monos, los cuales son capaces de infectar con el virus a mosquitos vectores experimentalmente (11). La infección con virus Mayaro produce síntomas inespecíficos en forma similar a otros arbovirus en su fase inicial: fiebre, dolor de cabeza, mialgia, dolor retroocular, escalofríos, fuerte artralgia, mareos, náuseas, fotofobia, anorexia, erupción cutánea principalmente en el pecho, las piernas, la espalda, los brazos y con menor frecuencia en la cara, dolor abdominal, leucopenia y plaquetopenia; en algunos casos, se ha presentado diarrea, dolor de garganta, congestión nasal, tos y manifestaciones hemorrágicas (11,21,33,69,74,75).
En tres pacientes brasileños se reportó ictericia, mientras que en Bolivia algunos pacientes presen-taron poliuria (33). Todos los síntomas duran entre dos y cinco días, con excepción de la artralgia, la cual es la característica más prominente y diagnóstica de la enfermedad (33,75). La artralgia, que puede durar hasta dos meses y es capaz de generar incapacidad, afecta principalmente a las articulaciones y la unión de los tendones en las muñecas, tobillos, codos, rodillas y dedos (11,21,33,69,75,76). El mal de Mayaro se considera una enfermedad febril benigna y de resolución espontánea con síntomas subletales. Únicamente se ha reportado un caso mortal hasta la fecha, el cual se registró en México, en el 2001, en un paciente que presentó encefalopatía durante 30 días, luego de los cuales pereció (76). La viremia se presenta durante la fase aguda y dura de dos a tres días. Luego se producen los anticuerpos IgM (días 3 a 4), que es cuando puede detectarse una infección reciente en el suero (34).
Un diagnóstico clínico del mal de Mayaro con base en la sintomatología inicial, es confuso por la existencia de cuadros clínicos similares, incluso con otros grupos antigénicos como el dengue y Oropuche, por lo que es de gran importancia emplear métodos diagnósticos inmunológicos y moleculares eficientes (11,13). Los métodos de laboratorio utilizados son el aislamiento viral mediante la inoculación de cultivos celulares en ratones experimentales con posterior aplicación de pruebas serológicas, como ELISA, fijación de complemento, inhibición de hemaglutinación y reducción de placas por neutralización, con las cuales se detectan inmunoglobulinas M o G específicas, o bien con amplificación del material genético del virus mediante la técnica PCR (13,33,77,78). Entre los marcadores moleculares utilizados se encuentran secuencias parciales del gen nsP1, de la región no codificante 3´(RNC), E1, E2 y E3 (2,10-13).
Las pruebas serológicas presentan una limitación importante pues requieren que los pacientes se encuentren en la fase aguda (o tener sueros pareados) y, por lo general, son costosas y consumen mucho tiempo. Las técnicas moleculares, como la PCR, son rápidas y sensibles; sin embargo, el virus está presente únicamente durante los días 2 a 6 subsecuentes a la infección (13). Recientemente, Wang, et al. (13), usaron RT-PCR-ELISA, que combina la sensibilidad y la especificidad de las técnicas moleculares con la detección simplificada de la prueba ELISA, y permite diferenciar entre alfavirus estrechamente relacionados, como el Mayaro, el de la encefalitis equina del este, del oeste y venezolana, el Mucambo, el Tonate, el del Ross River, el SFV, el O´nyong-nyong, el Aura, el Highlands J, el Fort Morgan y el Whataroa, lo que convierte a esta prueba en un importante método de diagnóstico por su rapidez y gran efectividad.
El contacto reciente con zonas selváticas o boscosas tropicales húmedas se considera un factor de riesgo. La gran mayoría de los brotes epidémicos, luego del primero acaecido en 1955 en Brasil y Bolivia, se han registrado de manera esporádica y aislada en localidades rurales y semirurales de la Panamazonia (10-13,33,69,77,71). Históricamente, las zonas más afectadas por brotes esporádicos de virus Mayaro son las localidades que colindan con la selva amazónica, en especial, la parte norte de Brasil (10,11,33,69). En este sentido, el estado de Pará es donde se ha reportado la mayor cantidad de casos y de brotes; así, se tiene que en Belterra se han registrado dos epidemias importantes por virus Mayaro, una en 1955, en una comunidad de trabajadores mineros en las cercanías del río Guamá, y otra en 1977-1978, en una villa rural en plantaciones de caucho (8,10,69). Otros reportes de casos de esta enfermedad viral en Pára fueron registrados en Conceição do Araguaia, entre 1978 y 1981, en Benevides, entre 1981y 1991, (8,10,69) y en Pau D’Arco, en 2008 (39).
Otros estados norteños de Brasil que se han visto afectados, son Goiás, donde la seroprevalencia alcanzó un 16 % en 1973 (33), la localidad de Itaruma con un brote en 1987 y la localidad de Peixa en 1991 (8,10,69). En el estado de Mato Grosso se registraron casos en humanos en 1991 (69); entre 20 y 47 % de indígenas del Amazonas presentaron anticuerpos anti-Mayaro, mientras que en los indígenas xavante de Mato Grosso la seroprevalencia fue de 20 % (33,69). Por otro lado, en muchas localidades rurales de la parte norte de Brasil, la seroprevalencia varía entre 10 y 62 % (11,78). En Río Branco se reportó seroprevalencia contra el virus Mayaro en 2004 (79) y en el último brote en Brasil se registraron 33 casos en Manaos, en 2011 (80).
En localidades rurales cercanas a bosques húmedos y a la selva amazónica, de Perú, Bolivia, Surinam, Guayana Francesa, Guyana, Colombia, Brasil y Venezuela, el virus Mayaro ha ocasionado brotes de manera esporádica y los estudios serológicos revelan frecuente contacto de los pobladores con el virus (11,12,22,33,52,69,71,72,75,78,79,84,85). En Guyana, se ha reportado alta seroprevalencia en habitantes de la sabana Rupununi y en la región del río Mazaruni, mientras que en la zona de la costa del país la infección con el virus es prácticamente inexistente (33). Una situación similar se observa en la Guayana Francesa, donde existe, según estudios seroló-gicos, mayor riesgo de contagio con virus en Oyapock y Maroni, localidades que limitan con zonas selváticas, que en Cayenne, que es una ciudad costera donde los niveles de seroprevalencia son significativamente más bajos (12). En Surinam, en localidades boscosas, la seroprevalencia puede alcanzar niveles de 81 % en hombres y 51 % en mujeres (33). En 1998 se reportó el primer brote de la enfermedad en Perú, la mayoría de casos provenientes de las localidades amazónicas rurales del departamento de Loreto, cercanas a la frontera con Brasil (11), mientras que se ha registrado una alta seroprevalencia en la población indígena y mestiza del este de ese país (33).
El último brote de gran magnitud, en cuanto a número de personas afectadas, registrado hasta la fecha, ocurrió en el municipio Ospino del Estado Portuguesa, localizado en los llanos de Venezuela, entre febrero y marzo del 2010. El registro fue de 72 casos, de los cuales, el 49 % correspondía a personas con edades comprendidas entre los 25 y 54 años, 65 % mujeres y 35 % hombres, y más de 50 % eran amas de casa y obreros (71). Desde hace más de 30 años se reportó en dicho estado la presencia de Hg. celeste (38); la población La Estación, en donde se presentaron los casos de infección por virus Mayaro, se encuentra ubicada en las cercanías de un bosque tropófilo. Además, en la región se ha reportado la presencia de monos, como Cebus olivaceus (mono capuchino) y Aloutta seniculus (mono araguato o aullador) (81), los cuales están potencialmente involucrados en el ciclo de transmisión del virus (33,41). Esta epidemia representa el segundo registro de la infección de virus en humanos en Venezuela; el anterior se presentó en una población cercana a la costa norte del país, Panaquire, Estado Miranda (52).
Fuera de la Panamazonia se ha registrado alta seroprevalencia en habitantes de zonas rurales de Costa Rica, Panamá y Guatemala (33,69). En Trinidad, donde el virus se aisló por primera vez en 1954, se ha observado frecuente presencia de anticuerpos en pobladores de la zona boscosa del sureste de la isla (33). Dos pacientes fueron diagnosticados con virus Mayaro en dos puertos mexicanos: Tamaulipas y Veracruz sur (76). Estos datos hacen suponer que, posiblemente, aves y humanos podrían estar interviniendo en la diseminación del virus.
Los reportados en Estados Unidos (11), en la urbe de São Paulo (69), en Francia (82) y en Holanda (83), se consideraron casos especiales. Sin embargo, posteriormente, los dos casos de Estados Unidos se consideraron importados de la zona selvática de Perú, los tres de São Paulo y el de Francia, como importados de Brasil, y los dos de Holanda, como importados de Surinam. La presencia de una especie con una amplia competencia vectorial, como lo es Ae. albopictus en Europa, obliga a no descartar la posibiliuadrodad de una eventual transmisión local, como ha ocurrido recientemente con la fiebre Chikungunya en Francia (64). En el cuadro 3 se muestran algunas localidades donde se han reportado aislamientos, alta seroprevalencia y brotes del virus Mayaro.

Síntesis del ciclo de transmisión y perspectivas
El mal de Mayaro constituye una arbovirosis, causada por un alfavirus, que se mantiene en la naturaleza mediante un ciclo enzoótico en el que participan primates no humanos de vida silvestre (monos) como reservorios u hospedadores y, posiblemente, otros vertebrados arborícolas. Las aves podrían jugar un papel importante en la diseminación del virus. Por otro lado, dípteros de la familia Culicidae y del género Haemagogus son los principales vectores del agente causal en el ciclo enzoótico. Sin embargo, no debe descartarse la participación de especies como Ae. scapularis, Sabethes spp., Ae. albopictus y Ae. aegypti.
Existen suficientes datos para afirmar que los casos epizoóticos ocurren cuando los humanos ingresan en el nicho natural de los reservorios y vectores naturales, infectándose con el virus cuando son picados por insectos Haemagogus portadores. Es necesario evaluar la posible participación de otros mosquitos periselváticos y peridomésticos en la transmisión del agente causal.
Se ha determinado que el ser humano es capaz de presentar niveles de viremia similares al umbral de infección del virus para el vector. Además, mosquitos urbanos como Ae. aegypti y otros que presentan un franco crecimiento de su expansión y una gran capacidad adaptativa a ambientes alterados por el hombre, como Ae. albopictus y Ae. scapularis, se han reportado en la bibliografía científica como capaces de transmitir experimentalmente el virus Mayaro. Estos factores representan un riesgo epidemiológico importante, pues representan la posibilidad de trasmisión urbana del virus Mayaro. Por otro lado, el aumento del crecimiento de la población, la intervención y urbanización de áreas enzoóticas y la expansión del área de influencia de Ae. aegypti, Ae. albopictus y Ae. serratus, aumentan la probabilidad de contacto entre reservorio, vector silvestre, humano, vector urbano y periurbano, con lo que se incrementa la posibilidad de infección del hombre, fuera de los focos enzoóticos.
La investigación sobre los factores de riesgo asociados a la transmisión selvática y a una eventual transmisión urbana, debe tener un abordaje interdisciplinario e interinstitucional, incluyendo aspectos virológicos de evolución molecular, determinación de infección natural de vectores, reservorios vertebrados y estudios serológicos longitudinales y transversales. Estas variables incluidas en un sistema de información geográfico, proporcio-naría factores de riesgo en áreas localizadas y en regiones.
Agradecimientos
A Scott C. Weaver, por facilitar el original de la figura 2. A la Licenciada Rosa Hernández, por sus comentarios y discusiones sobre el tema tratado. A Fabiola Del Ventura por el diseño de la figura 3.
Conflicto de intereses
Los autores declaran no tener conflicto de interés.
Financiamiento
Misión Ciencia FONACIT 20080000911-4 (JCN)
Referencias
1. Weaver SC.Evolutionary influences in arboviral disease. Berlin, Heidelberg: Springer-Verlag; 2006.p. 285-314. [ Links ]
2. Strauss J, Strauss E. The Alphaviruses: gene expression, replication, and evolution. Microbiol Rev. 1994;58:491-562. [ Links ]
3. Organización Mundial de la Salud. Virosis transmitidas por artrópodos y roedores. Ginebra: OMS; 1985.p. 1-126. [ Links ]
4. Organización Mundial de la Salud. Lucha contra vectores y plagas urbanas. Ginebra; OMS; 1988. p. 1-88 [ Links ]
5. Kruse H, Kirkemo A, Handeland K.Wildlife as source of zoonotic infections. Emerg Infect Dis. 2004;10:2067-72. [ Links ]
6. Organización Mundial de la Salud. Lucha biológica contra los vectores de enfermedades. Ginebra: OMS; 1982. p. 1-68. [ Links ]
7. Organización Mundial de la Salud. Lucha antivectorial integrada. Ginebra: OMS; 1983. p. 1-84. [ Links ]
8. Vasconcelos P, Travassos A, Rodriguez S, Travassos E, Degallier N, Travassos J. Inadequate management of natural ecosystem in the Brazilian Amazon region results in the emergence and re-emergence of arboviruses. Cad Saúde Pública. 2001;17:155-64. [ Links ]
9. Ariza E, Lopez C, Martínez O, Arias S. Ecoepidemiología: el futuro posible de la epidemiología. Revista Facultad Nacional de Salud Pública. 2004;22:139-45. [ Links ]
10. Powers A, Aguilar P, Chandler L, Brault A, Meakins T, Watts D, et al. Genetic relationships among Mayaro and Una viruses suggest distinct patterns of transmission. Am J Trop Med Hyg. 2006;75:461-9. [ Links ]
11. TeshR, Watts D, Russell K, Damodaran C, Calampa C, Cabezas C, et al. Mayaro virus disease: an emerging mosquito-borne zoonosis in tropical South America. Clin Infect Dis. 1999;28:67-73. [ Links ]
12. Talarmin A, Chandler L, Kazanji M, De Thoisy B, Debon P, Lelarge J, et al. Mayaro virus fever in French Guiana: isolation, identification and seroprevalence. Am J Trop Med Hyg. 1998;59:452-6. [ Links ]
13 Wang E, Paessler S, Aguilar P, Carrara A, Ni H, Greene I, et al. Reverse transcription-PCR-enzyme-linked immunosorbent assay for rapid detection and differentiation of alphavirus infections. J Clin Microbiol. 2006;44:4000-8. [ Links ]
14. Lavergne A, Thoisy B, Lacoste V, Pascalis H, Pouliquen J. Mercier V, et al. Mayaro virus: complete nucleotide sequence and phylogenetic: Relationships with other alphaviruses. Virus Res. 2006;117:283-90. [ Links ]
15. Mandell G, Benett J, Dolin R. Enfermedades infecciosas principios y prácticas. Volumen 2. 5ta edición. Madrid: Editorial Médica Panamericana; 2002. p. 3500. [ Links ]
16. Shope R, Mackensie J. Artritis y erupción cutánea víricas transmitidas por artrópodos. En: Heymann D, editor .El control de enfermedades transmisibles. 18 edición. Washington D.C.; PAHO; 2005. p. 194-6. [ Links ]
17. Murray P, Rosenthal K, Pfaller M. Microbiología médica. Barcelona: Elservier; 2009. p. 915. [ Links ]
18. Talavera A, Sánchez H. Nuevos sistemas virales en terapia génica. Virología. 2004;10:1-16. [ Links ]
19. Henao L, Cortés F, Navas M. Semliki Forest Virus: un vector viral con múltiples aplicaciones. Revista Colombia Médica. 2007;38:159-69. [ Links ]
20. Ferreira M, Santo M, Rebello M.Weak bases affect late stages of Mayaro virus replication cycle in vertebrate cells. J Med Microbiol. 2000;49:313-8. [ Links ]
21. Ishimaru D, Marciano F, Rebello M. Inhibition of Mayaro virus replication by prostaglandin A1 and B2 in Vero cells. Braz J Med Biol Res. 1998;31:1119-23. [ Links ]
22. Forshey B, Guevara C, Laguna-Torres A, Céspedes M, Vargas J, Gianella A, et al. Arboviral etiologies of acute febrile illnesses in Western South America, 2000-2007. PLoS Negl Trop Dis. 2010;8:1-14. [ Links ]
23. Moraes L. Emergent arboviruses in Brazil. Rev Soc Bras Med Trop. 2007;40:224-9. [ Links ]
24. Machado-Allison CE. Ecología de los mosquitos (Culicidae) III. Adultos. Acta Biol Venez. 1982;11:133-237. [ Links ]
25. Wei H, Li X, Martcheva M. An epidemic model of a vector-borne disease with direct transmission and time delay. J Math Anal Appl. 2008;342:895-908. [ Links ]
26. Secundino N, Nacif-Pimenta R, Hajmova M, Volf P, Pimenta P. Midgut muscle network in Lutzomyia longipalpis and Phlebotomus duboscqi sand flies: spatial organization and structural modification after blood meal. Arth Struct Develop. 2005;34:167-78. [ Links ]
27. Acha P, Szyfres B. Zoonosis y enfermedades transmisibles comunes al hombre y a los animales: clamidiosis, rickettsiosis y virosis. Volumen II. 3era Edición. Washington D.C; Organización Panamericana de la Salud; 2003.p. 425. [ Links ]
28. Junt T, Heraud J, Lelarge J, Labeau B, Talarmin A. Determination of natural versus laboratory human infection. Epidemiol Infect. 1999;123:511-13. [ Links ]
29. Pascoa V, Oliveira P, Dansa-Petretskit M, Silva J, Alvarenga P, Jacobs-Lorena M, et al. Aedes aegypti peritrophic matriz and its interaction with heme during blood digestion. Insect Biochem Mol Biol. 2002;32:517-23. [ Links ]
30. Sudia W, Charberlain R. Collection and processing of medically important arthropods for arbovirus isolation. Atlanta, GA: Communicable Disease Center; 1967. p. 29. [ Links ]
31. Basáñez M, Rodríguez D. Dinámica de transmisión y modelos matemáticos en enfermedades transmitidas por vectores. Entomotropica.2004;3:113-34. [ Links ]
32. Schaub G. Parasitogenic alterations of vector behaviour. Int J Med Microbiol. 2006;1:37-40. [ Links ]
33. Pinheiro F, LeDuc J. Mayaro virus disease. In: Thomas P, Monath M, editor. The arboviruses epidemiology and ecology. Florida: CRC Press Inc; 1988. p. 137-50. [ Links ]
34. Tesh R. Arthritides caused by mosquito-borne viruses. Ann Rev Med.1982;33:31-40. [ Links ]
35. Barret A, Higgs S. Yellow fever: A disease that has yet to be conquered. Ann Rev Entomol. 2006;52:109-29. [ Links ]
36. Mondet B, Vasconcelos PF, Travassos da Rosa AP, Travassos da Rosa ES, Rodrigues SG, Travassos da Rosa JF, et al. Isolation of yellow fever virus from Nulliparous Haemagogus (Haemagogus) janthinomys in Eastern Amazonia. Vector Borne Zoonotic Dis. 2002;2:47-50. [ Links ]
37. Aragao N, Muller G, Queiroz B, Balbino V, Costa C, Lima R, et al. A list of mosquito species of the Brazilian State of Pernambuco, including the first report of Haemagogus janthinomys (Diptera: Culicidae), yellow fever vector and 14 other species (Diptera:Culicidae). Rev Soc Bras Med Trop. 2010;43:458-9. [ Links ]
38. Liria J, Navarro JC. Clave fotográfica para hembras de Haemagogus Williston 1896 (Diptera: Culicidae) de Venezuela, con nuevo registro para el país. Bol Malariol Salud Amb. 2009;49:283-92. [ Links ]
39. Azevedo R, Silva E, Carvalho V, Rodrigues S, Nunes-Neto J, Monteiro H, et al.Mayaro fever virus, Brazilian Amazon. Emerg Infect Dis. 2009;15:1830-2. [ Links ]
40. National Center of Infectious Diseases.Mayaro. Fecha de consulta: 23 de agosto 2011. Disponible en: http://wwwn.cdc.gov/arbocat/catalog-listing.asp?VirusID=293&SI=7 [ Links ]
41. Thoisy B, Gardon J, Salas R, Morva J, Kazanji M. Mayaro virus in wild mammals French Guiana. Emerg Infect Dis. 2003;9:1326-9. [ Links ]
42. Walter Reed Biosystematic Unit. Vector Identification Resources. Fecha de consulta: 7 de diciembre 2011. Disponible en: http://www.wrbu.org/index.html [ Links ]
43. Maestre R, Vergara C, Berrueco G, Bello B, Brochero H. Presencia de Haemagogus equinus Theobald, 1903 (Diptera: Culicidae) en los municipios de Soledad y Malambo en el Departamento del Atlántico, Colombia, 1998-2005. Biomédica. 2008;28:99-107. [ Links ]
44. Da Costa P. Febre Amarela. Rev Soc Bras Med Trop. 2003;36:275-93. [ Links ]
45. Lourenco R, Vazeille M, Bispo A, Failloux F. Large genetic differentiation and low variation in vector competence for dengue and yellow fever viruses of Aedes albopictus from Brazil, the United States, and the Cayman Islands. Am J Trop Med Hyg. 2003;60:105-14. [ Links ]
46. Valero N. A propósito de la fiebre amarilla en Venezuela. Invest Clin. 2003;44:269-71. [ Links ]
47. De Castro Gomes A, Nascimento M, Ferri L, Rocha F, Martins A. Encontro de Haemagogus (Conopostegus) leucocelaenus (Diptera: Culicidae), no Município de Porto Alegre Estado do Rio Grande do Sul. Rev Soc Bras Med Trop. 2007;4:487-8. [ Links ]
48. Suárez A. Fiebre amarilla repunta de nuevo en Venezuela. 2003. VITAE. Fecha de consulta: 5 de diciembre 2011. Disponible en: http://caibco.ucv.ve/caibco/vitae/VitaeDieciseis/FiebreAmarilla/ArchivosHTLM/fiebreamarilla.htm. [ Links ]
49. Muñoz-Rodríguez M, Arrivillaga J, Navarro JC.Casos de fiebre amarilla en Portuguesa, Venezuela: ¿un brote selvático espurio? Rev Biomed. 2010;21:163-77. [ Links ]
50. Pinheiro F, Travassos da Rosa AP. Arboviral zoonoses of Central and South America. In: Beran GW, editor. Handbook of zoonoses. 2nd ed. Florida: CRC Press; 1994. p. 201-25. [ Links ]
51. Navarro JC, Machado-Allison CE. Aspectos ecológicos de Sabethes chloropterus (Diptera: Culicidae) en un bosque húmedo del Edo. Miranda, Venezuela. Bol Entomol Venez. 1995;10:91-104. [ Links ]
52. Torres J, Russell K, Vásquez C, Barrera R, Tesh R, Salas R, et al. Family cluster of Mayaro fever, Venezuela. Emerg Infect Dis. 2004;10:1304-6. [ Links ]
53. Salas R, García C, Liria J, Barrera R, Navarro JC, Medina G, et al.Ecological studies of enzootic Venezuelan equine encephalitis in North-Central Venezuela, 1997-1998. Am J Trop Med Hyg. 2001;64:84-92. [ Links ]
54. Moore C, Mitchell C.Aedes albopictus in the United States: Ten-year presence and public health implications. Emerg Infect Dis. 1997;3:329-34. [ Links ]
55. DeCastro Gomez A, Forattini O, Kakitani I, Rita G, Azevedo C, Marucci D, et al. Microhabitats de Aedes albopictus (Skuse) na regiao do Vale do Paraíba, Estado de São Paulo, Brasil. Rev Saúde Públ. 1992;26:108-18. [ Links ]
56. Navarro JC, Zorrilla A, Moncada N. Primer registro de Aedes albopictus (Skuse) en Venezuela. Importancia como vector de dengue y acciones a desarrollar. Bol Malariol Salud Amb. 2009; 49:161-6. [ Links ]
57. Gratz N. Critical review of the vector status of Aedes albopictus. Med Vet Entomol. 2004;18:215-27. [ Links ]
58. Forattini O, De Castro A. Biting activity of Aedes scapularis (Rondani) and Haemagogus mosquitoes in Southern Brazil (Diptera: Culicidae). Rev. Saúde Públ.1988;22:84-93. [ Links ]
59. Sant´Ana A, Leuch A. Influencia do ciclo lunar na captura de Aedes scapularis (Diptera, Culicidae) na Mata Atlantica do Paraná. Ilheringia. Ser ZoolPorto Alegre. 2001;90:175-82. [ Links ]
60. Zorrilla A, Quintero L, Del Ventura F, Muñoz M, Moncada, N, Navarro JC.Aspectos ecológicos deAedes albopictus (Skuse, 1894) en Caracas, Venezuela. Bol Malariol Salud Amb. 2011;51:229-35. [ Links ]
61. Weaver SC, Klimstra WB, Ryman KD. Togaviruses: General features. En: Mahy BW, van Regenmortel MH, editors. Encyclopedia of virology. Oxford: Elsevier; 2008. p. 107-16. [ Links ]
62. Weaver SC, Reisen WK. Present and future arboviral threats. Antiviral Res. 2010;85:328-45. [ Links ]
63. Cavrini F, Gaibani P, Pierro AM, Rossini G, Landini MP, Sambri V. Chikungunya: An emerging and spreading arthropod-borne viral disease. J Infect Dev Ctries. 2009;3:744-72. [ Links ]
64. Grandadam M, Caro V, Plumet S, Thiberge J, Souarés Y, Failloux A, et al. Chikungunya Virus, Southeastern France. Emerg Infect Dis. 2011;17:910-3. [ Links ]
65. Vazeille M, Moutailler S, Coudrier D, Rousseaux C, Khun H, HuerreM, et al. Two chikungunya isolates from the outbreak of La Reunion (Indian Ocean) exhibit different patterns of infection in the mosquito, Aedes albopictus. PLoS ONE. 2007;2:e1168. [ Links ]
66. Tsetsarkin KA, McGee CE, Volk SM, Vanlandingham DL, WeaverSC, Higgs S. Epistatic roles of E2 glycoprotein mutations in adaption of chikungunya virus to Aedes albopictus and Ae. aegypti mosquitoes. PLoS ONE. 2009;4:e6835. [ Links ]
67. Thiboutot MM, Kannan S, Kawalekar OU, Shedlock DJ, Khan AS,et al. Chikungunya: A Potentially Emerging Epidemic? PLoS Negl Trop Dis. 2010;4:e623. [ Links ]
68. Aguilera L, González M, Marquetti M, Capín J, Fustes C. Incidencia de Aedes (S) aegypti y otros culícidos en el Municipio Playa, Ciudad de La Habana. Rev Cubana Med Trop. 2000;52:174-89. [ Links ]
69. Coimbra T, Santos C, Suzuki A, Petrella S, Bisord I, Nagamori A, et al. Mayaro virus: Imported cases of human infection in São Paulo State, Brazil. Rev Inst Med Trop São Paulo. 2007;49:221-4. [ Links ]
70. Troyes L, Villegas Z, Troyes M. Expansión del Aedes aegypti a localidades rurales de Cajamarca. Rev Peru Med Exp Salud Pub. 2006;23:163-7. [ Links ]
71. Red de Sociedades Científicas Médicas de Venezuela. Alerta epidemiológica Nº 132. Situación en Venezuela, América Latina y el Mundo. Brote epidémico de fiebre Mayaro. Una enfermedad viral emergente en Venezuela y una nueva censura de información epidemiológica. Fecha de consulta: 2 de diciembre 2011. Disponible en: http://www.ovsalud.org/doc/red132.pdf. [ Links ]
72. Calisher C, Gutiérrez E, Lord R, Maness K, Lord R. Isolation of Mayaro virus from a migrating bird captured in Louisiana in 1967. Bull Pan Am Health Organ.1974;8:148-54. [ Links ]
73. Liria J, Navarro J. Modelos de nicho ecológico en Haemagogus Williston (Diptera: Culicidae), vectores del virus de la fiebre amarilla. Rev Biomédica. 2010;21:149-61. [ Links ]
74. Pereira L, Marcicano F, Alcoforado M. Efeito da tunicamicina sobre a replicacao do vírus Mayaro em células de Aedes albopictus. Revista de Ciências Médicas e Biológicas. 2003;2:5-11. [ Links ]
75. Taylor S, Patel P, Herold T. Recurrent arthralgias in a patient with previous Mayaro fever infection. Southern Med J. 2005;98:484-5. [ Links ]
76. Navarrete-Espinosa J, Gómez-Dantés H. Arbovirus causales de fiebre hemorrágica en pacientes del Instituto Mexicano del Seguro Social. Rev Med Inst Mex Seguro Soc. 2006;44:347-53. [ Links ]
77. Calisher C, El-Kafrawi A, Mahmud M, Travassos A, Bartz C, Brummer-Korvenkontio S, et al.Complex-specific immunoglobulin M antibody patterns in humans infected with alphaviruses. J Clin Microbiol. 1986;23:155-9. [ Links ]
78. Moraes l, Ribeiro R, Baeta S, Schatzmayr H, Travassos A.Study of two different enzyme immunoassays for the detection of Mayaro virus antibodies. Mem Inst Oswaldo Cruz.1989;84:303-7. [ Links ]
79. Tavares-Neto J, Freitas-Carvalho J, Teixeira M, Rocha G, Guerreiro S, Damasceno E, et al. Pesquisa de anticorpos contra arbovírus e o virus vacinal da febre amárela em uma amostra da populacao de Rio Branco, antes e três meses após a vacina 17D. Rev Soc Bras Med Trop. 2004;37:1-6. [ Links ]
80. Torres J. Virus Mayaro, probable transmisión urbana-Brasil (Manaos). 2011. Promed Archive number: 20110222.0587. Fecha de consulta: 2 de diciembre 2011. Disponible en: http://www.promedmail.org/?p=2400:1001:8322781994137096::NO::F2400_P1001_BACK_PAGE,F2400_P1001_PUB_MAIL_ID:1060,87168. [ Links ]
81. Linares O. Mamíferos de Venezuela. Caracas: Sociedad Conservacionista Audubon de Venezuela; 1998. p. 691. [ Links ]
82. Receveur M, Grandadam M, Malvy D. Infection with Mayaro virus in a French traveler returning from the Amazon region, Brazil 2010. Euro Surveill. 2010;15:1-4. [ Links ]
83. Hassing R, Leparc-Goffart I, Blank S, Thevaravan S, Tolou H, Van Doornum G, et al. Imported Mayaro virus infection in the Netherlands. J Infect. 2010;61:343-5. [ Links ]
84. Mourão MP, Bastos MD, de Figueiredo RP, Gimaque JB, Dos Santos Galusso E, Kramer VM, et al. Mayaro fever in the City of Manaus, Brazil, 2007-2008. Vector Borne Zoonotic Dis. 2012;12:42-6. [ Links ]
85. Forshey BM, Guevara C, Laguna-Torres VA, Cespedes M, Vargas J, Gianella A, et al.Arboviral etiologies of acute febrile illnesses in Western South America, 2000-2007. PLoS Negl Trop Dis. 2010;4:e787. [ Links ]













