Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.14 no.3 Bogotá Sep./Dec. 2009
INDUCCIÓN DE RESISTENCIA SISTÉMICA CONTRA Fusarium oxysporum EN TOMATE POR Trichoderma koningiopsis Th003
Induced Systemic Resistance Against Fusarium oxysporum In Tomato By Trichoderma koningiopsis Th003
YEIRME YANETH JAIMES SUÁREZ1, M.Sc.; CARLOS ANDRÉS MORENO VELANDIA1, M.Sc.; ALBA MARINA COTES PRADO1, Ph. D.
1Corporación Colombiana de Investigación Agropecuaria - CORPOICA A.A. 240142, Las Palmas, Bogotá D.C., Colombia. amcotes@corpoica.org.co
Presentado 27 de junio de 2008, aceptado 10 de diciembre de 2008, correcciones 9 de octubre de 2009.
RESUMEN
Trichoderma koningiopsis Th003 ha mostrado alta eficacia en el control de diferentes fitopatógenos incluyendo Fusarium oxysporum, agente causal de la pudrición del cuello y la raíz del tomate (Solanum lycopersicum Mill.). Con el propósito de estudiar si este agente tiene la capacidad para inducir respuestas sistémicas de defensa, se utilizó como patosistema modelo Fusarium oxysporum -tomate, cuyas plantas se establecieron en cubos de enraizamiento con el sistema radical separado en dos porciones. Cuando Th003 se inoculó en una porción de la raíz 96 h antes de inocular en la otra porción F. oxysporum, se presentó un retraso de la colonización del fitopatógeno en el sistema vascular de la planta, en comparación con las plantas inoculadas solamente con el fitopatógeno. Este resultado sugiere que Th003 estimuló respuestas sistémicas de defensa en la planta, dado que el antagonista y el fitopatógeno permanecieron separados espacialmente. El microorganismo biocontrolador formulado como gránulos dispersables, se aplicó en un cultivo comercial de tomate bajo invernadero y redujo significativamente la incidencia de la pudrición del cuello y las raíces del tomate en 35%, en comparación con el testigo absoluto. El hongo T. koningiopsis Th003 demostró habilidad para controlar F. oxysporum f. sp. radicislycopersici mediante inducción de respuestas de defensa sistémica en las plantas de tomate.
Palabras clave: resistencia sistémica inducida, tomate, Fusarium oxysporum, Trichoderma koningiopsis.
ABSTRACT
Trichoderma koningiopsis Th003 has proved to be an efficient biocontrol agent of different plant pathogens including Fusarium oxysporum, causing agent of tomato crown and root rot. With the aim to studying whether Th003 has the ability to induce defense systemic responses to control Fusarium oxysporum infection, tomato plants (Solanumlycopersicum Mill.) were sown in pots using split root modified method. When Th003 was applied to one root portion 96 h before inoculating F. oxysporum in the other root portion, delayed colonization of the plant’s vascular system was observed as compared with plants inoculated only with the pathogen. Since the antagonist and the pathogen remained spatially separated in the host, the protection effect in plants was attributed to a systemic activity induced by Th003. In a commercial greenhouse the biopesticide based upon Th003 reduced significantly (P<0.05) by 35% the incidence of crown and root rot caused F. oxysporum f. sp. Lycopersici, compared with untreated control. T. koningiopsis Th003 showed ability to control F. oxysporum f. sp. radicis-lycopersici by inducing systemic defense responses in tomato plants.
Key words: Induced systemic resistance, tomato, Fusarium oxysporum, Trichoderma koningiopsis.
INTRODUCCIÓN
El control biológico de fitopatógenos con microorganismos antagonistas ha recibido gran interés en los últimos años debido a su potencial y a las aplicaciones exitosas en diferentes cultivos (Fravel, 2005). El éxito del control de estos organismos se atribuye a la actividad sinérgica de diferentes mecanismos de acción directos e indirectos (Harman et ál., 2004). La inducción de resistencia sistémica en el hospedero es uno de los mecanismos indirectos de mayor interés en la actualidad. Dentro de los agentes de control reportados como efectivos elicitores de este mecanismo se encuentran varias especies del género Trichoderma, principalmente para controlar fitopatógenos foliares (Howell, 2006; Harman et ál., 2004) sin embargo, son pocos los reportes contra patógenos del suelo. La inducción de resistencia sistémica por Trichoderma sp. involucra cambios celulares en el hospedero, tales como un aumento de depósitos de calosa en el interior de la pared celular y aumento en la actividad peroxidasa y quitinasa (Yedidia et ál., 1999). Otros procesos relacionados con la inducción sistémica contra patógenos del suelo, tal como F. oxysporum f. sp. lycopersici son el confinamiento, la inhibición del patógeno y los cambios histológicos en el hospedero (Benhamou et ál., 1998; Yedidia et ál., 1999). Estos últimos relacionados con la producción de reguladores de crecimiento y estimulación de la división, diferenciación y crecimiento celular en la planta por el agente elicitor (De Cal et ál., 2000).
El aislamiento Th003 de Trichoderma koningii (recientemente reidentificado como T. koningiopsis), ha mostrado ser eficaz en el control de patógenos foliares (Moreno y Cotes, 2007) y patógenos del suelo (Cotes et ál., 2001; Cotes et ál., 2007); este microorganismo constituye el principio activo de una formulación (WG) que también ha demostrado alta eficacia (Cotes et ál., 2007). En estudios previos Cotes et ál., 1996, y Clavijo y Cotes, 1998, encontraron que éste hongo estimuló la actividad de proteínas relacionadas con la patogénesis, del tipo β-1,3-endoglucanasas y endoquitinasas en plantas de fríjol y tomate respectivamente, sugiriendo un efecto inductor de respuestas de defensa. Así mismo, Castillo et ál., 2007, mediante la técnica de microarreglos, encontraron que plantas de tomate tratadas con Th003 expresaron 42 genes diferenciales, en contraste con plantas no tratadas. Dentro de los genes diferenciales se encontraron algunos relacionados con las categorías funcionales de transporte, de traducción de señales, de respuesta a hormonas y de señalización, entre otros. Por lo anterior, los objetivos de este trabajo fueron determinar la capacidad de T. koningiopsis Th003 para inducir resistencia sistémica en plantas de tomate y evaluar la eficacia en el control de F. oxysporum.
MATERIALES Y MÉTODOS
MICROORGANISMOS
Los aislamientos Fu040 de F. oxysporum f. sp. radicis-lycopersici, Fu041 de F. oxysporum f. sp. lycopersici y la cepa Th003 de T. koningiopsis fueron suministrados por el Banco de Germoplasma de Microorganismos del Laboratorio de Control Biológico de Corpoica. Los aislamientos de F. oxysporum se conservaron en medio de cultivo PDA inclinado y Th003 se conservó en suelo estéril. En todos los casos la temperatura de conservación fue de 4 °C. Previo a la producción de los inóculos, los hongos crecieron en medio de cultivo PDA durante siete días a 25 ºC.
PRODUCCIÓN DE INÓCULOS
Para la producción masiva de F. oxysporum se utilizó sustrato estéril salvado de trigo (100 g) suplementado con 100 mL de medio caseína hidrolizada (Dhingra y Sinclair, 1987) en bolsas de polietileno de alta densidad (Cotes et ál., 2001) al cual, se transfirieron cinco discos de 6 mm de diámetro provenientes de los cultivos en PDA y se incubó durante 15 días con luz constante a 25 °C. Para la obtención del inóculo de Th003 se preparó una suspensión de conidios a partir de un cultivo en PDA de siete días de edad y con la ayuda de una cámara de Neubauer se ajustaron las concentraciones 105, 106 y 107 conidios.mL-1.
MATERIAL VEGETAL
Se sembraron semillas de tomate híbrido Rocio® (Semillas Syngenta Ind.) en bandejas de 72 celdas con turba estéril bajo condiciones de invernadero. El material vegetal se mantuvo en semillero durante seis semanas hasta la aplicación de los tratamientos.
PRUEBA DE PATOGENICIDAD
Con el fin de evaluar la patogenicidad de los aislamientos Fu040 y Fu041, se transplantaron plántulas de tomate de seis semanas de edad cuya raíz se dividió longitudinalmente en dos porciones (Fuchs et ál., 1997; Duijff et ál., 1998). Cada porción de raíz se dispuso en un vaso de enraizamiento (6 x 6 x 12 cm) con vermiculita estéril. En una porción de la raíz se inoculó el fitopatógeno, para este fin el hongo crecido en el sustrato previamente descrito se mezcló en proporción de 5% p/p (103 UFC.g-1) con vermiculita estéril humedecida hasta capacidad de campo. La incidencia de la infección causada por los aislamientos Fu040 y Fu041 se evaluó mediante la indexación del tallo, según lo descrito por Rekah et ál., 2000, a los 15 y 28 días después de la inoculación. Para esto, el tallo se dividió en segmentos de 1 cm y se desinfectaron con hipoclorito de sodio al 1% durante 2 min con tres lavados posteriores en agua estéril. Los segmentos se colocaron en medio PDA y se incubaron a 25 °C durante siete días, tiempo después del cual se observó el crecimiento de F. oxysporum desde el tejido vegetal.
Se incluyó un testigo relativo (plantas con raíces dividas sin ningún inóculo) y un testigo absoluto (plantas sin ningún tratamiento). Se utilizó un diseño experimental completamente al azar con tres repeticiones. La unidad experimental consistió en diez plantas y la unidad de muestreo fue una planta.
BIOENSAYO DE INDUCCIÓN DE RESISTENCIA
Para determinar la capacidad de Th003 para inducir resistencia sistémica, se establecieron plantas de tomate de seis semanas con la raíz dividida. Una de las porciones del sistema radical se inoculó con 10 mL de suspensión de T. koningiopsis. Se evaluaron tres concentraciones, 105, 106 y 107 conidios.mL-1. Después de 96 h, la otra porción del sistema radical se inoculó con F. oxysporum siguiendo el procedimiento empleado en la prueba de patogenicidad. Se evaluó la incidencia de la infección causada por los aislamientos Fu040 y Fu041 mediante la indexación del tallo.
En el bioensayo se incluyó un testigo patógeno para cada aislamiento de F. oxysporum, un testigo relativo y un testigo absoluto. Se utilizó un diseño experimental completamente al azar con tres repeticiones por tratamiento. La unidad experimental consistió en diez plantas y la unidad de muestreo fue una planta.
EVALUACIÓN DE LA ACTIVIDAD BIOCONTROLADORA DE T. koningiopsis
El bioensayo se realizó en un invernadero de producción comercial de tomate (800 m2) en el municipio de Fusagasugá, Cundinamarca. El área experimental se seleccionó por presentar un historial de pérdidas importantes de tomate por pudrición del cuello y de la raíz de las plantas causadas por F. oxysporum f. sp. radicis-lycopersici Fu040.
El control biológico se implementó dentro de un esquema de manejo integrado de la enfermedad. Se utilizó la formulación WG a base de Th003, aplicada a las semillas de tomate mediante la técnica de pregerminación controlada en matriz sólida (Cotes et ál., 2001). Posteriormente las semillas se sembraron en bandejas de germinación de 127 celdas, utilizando como sustrato turba (Sunshine®). En el invernadero el suelo se solarizó después de la labranza, cubriéndolo con polietileno durante 20 días antes del transplante de las plántulas de cuatro semanas de edad. La formulación a base de Th003 se aplicó de forma directa en el fondo del sitio de transplante a razón de 0,5 g/planta; siete días después del transplante se realizó una segunda aplicación en drench de la formulación reconstituida en agua (50 cm3.planta-1) en dosis de 1g.L-1 (10 6 conidios.mL-1). Este último procedimiento se repitió una vez por semana durante tres semanas. Durante el periodo de evaluación se eliminaron las plantas muertas por F. oxysporum. Se incluyó un testigo agricultor, que consistió en el transplante de plántulas sin Th003 y en la aplicación en drench del fungicida Tolclofos metil (Rizolex® 75 WP) al suelo, en dosis de 2 g en 5 L/m2, dos días antes del transplante. También se incluyó un testigo absoluto, en el cual las plantas no recibieron ningún tipo de tratamiento para el control de la enfermedad tanto en semillero como en el invernadero. Las plántulas se transplantaron en surco doble, con distancias de 0,4 m entre surcos y 0,3 m entre plantas.
Se empleó un diseño experimental de bloques completos al azar con tres repeticiones. La unidad experimental consistió en cuatro camas de siembra de 13 m de longitud separadas entre si 0,5 m. Al finalizar el experimento se estimó la eficacia de control de la formulación mediante la fórmula (a-b/a)*100 donde a representa la incidencia de la enfermedad en el testigo y b representa la incidencia de la enfermedad en el tratamiento.
ANÁLISIS DE DATOS
Los resultados de los bioensayos de patogenicidad y de inducción de resistencia sistémica se sometieron a una prueba de Chi cuadrado. Los datos de la evaluación en campo se sometieron a un análisis de varianza (ANDEVA) y a una prueba de comparación de medias de tratamiento de Tukey (α=0,05).
RESULTADOS
PRUEBA DE PATOGENICIDAD
Los aislamientos Fu040 y Fu041 de F. oxysporum infectaron las plantas de tomate, ya que 15 días después de la inoculación se evidenció colonización del sistema vascular de la planta, desde el cuello hasta 3 cm por encima de éste (Fig. 1). La colonización del tallo no mostró diferencias significativas (p > 0,05) entre los dos aislamientos. Las plantas en los tratamientos testigo no presentaron infección. Se observó que ambos aislamientos colonizaron el 100% de la longitud del tallo de las plantas inoculadas 28 días después de la inoculación (datos no mostrados).
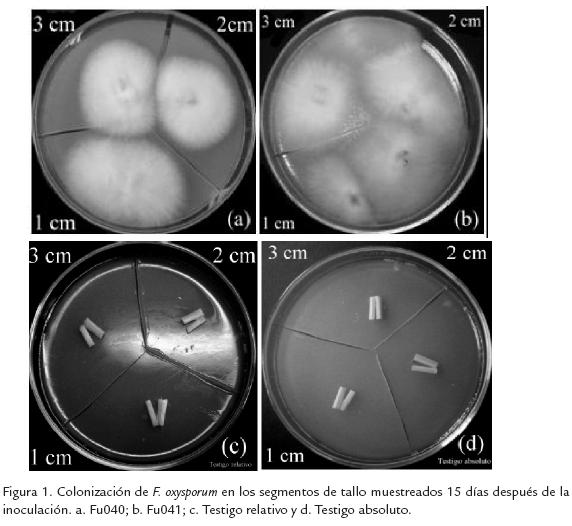
BIOENSAYO DE INDUCCIÓN DE RESISTENCIA
Los dos aislamientos de F. oxysporum infectaron las plantas de tomate y colonizaron los haces vasculares de forma similar. Después de 15 días de la inoculación de F. oxysporum en una porción de la raíz, se presentó un retraso significativo (p < 0,05) de la colonización del aislamiento Fu040 en los haces vasculares de las plantas tratadas con T. koningiopsis Th003, en comparación con las plantas inoculadas solamente con el fitopatógeno, en donde su ascenso ocurrió hasta 3 cm por encima del cuello del tallo en todas las plantas muestreadas. En las plantas tratadas con Th003 la colonización de los haces vasculares por los aislamientos Fu040 y Fu041 se vio limitada, ya que cuando se utilizaron las concentraciones de 106 y 107 conidios.mL-1 de Th003, el patógeno ascendió hasta 3 y 2 cm respectivamente, por encima del cuello en el 33% de las plantas muestreadas (Fig. 2). Aunque no se presentaron diferencias significativas entre las concentraciones de Th003 evaluadas, se observó que el mayor retraso se presentó cuando las plantas fueron tratadas con la concentración de 105 conidios.mL-1, en donde la colonización del xilema por los aislamientos Fu040 y Fu041 alcanzó sólo hasta 1 cm en el 33 y 67% de las plantas muestreadas respectivamente (Fig. 2).
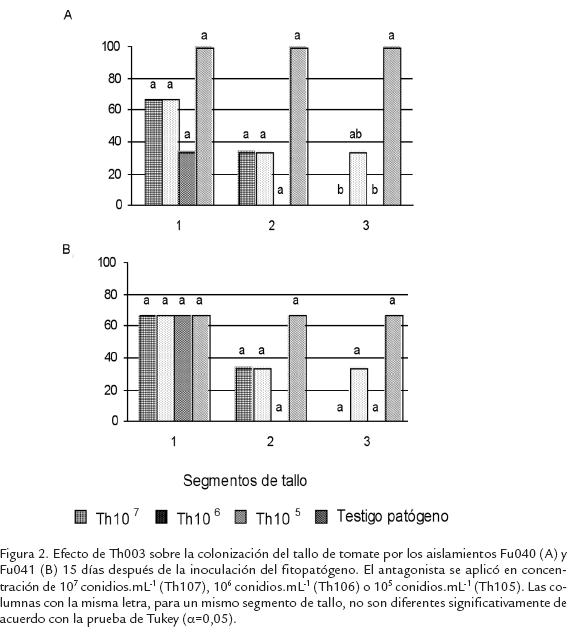
Aunque la concentración de 105 conidios.mL-1 de Th003, tuvo un mayor efecto de estimulación de respuestas de defensa en las plantas de tomate, éste efecto no fue de larga duración, ya que 28 días después de la inoculación del patógeno, este se encontró 12 cm por encima del cuello del tallo de las plantas en todos los tratamientos.
EFICACIA DEL PROTOTIPO GRANULADO A BASE DE T. koningiopsis SOBRE F. oxysporum EN INVERNADERO
Los primeros días después del transplante, las plantas de tomate afectadas por F. oxysporum mostraron síntomas de adelgazamiento del cuello, pudrición de la raíz y volcamiento. Durante 28 días posteriores al transplante, en los tres tratamientos evaluados la incidencia de la enfermedad tuvo un comportamiento similar, siendo inferior al 10% (Fig. 3). Sin embargo, después de este tiempo se presentó un incremento considerable de plantas que mostraron la sintomatología de la enfermedad, llegando a ser de 30 a 32% a los 37 días después del transplante, en las unidades experimentales tratadas con Tolclofos metil y las correspondientes al testigo no tratado respectivamente. En las unidades experimentales tratadas con la formulación a base de Th003 se observó un nivel de enfermedad significativamente inferior (p < 0,05) (Fig. 3) presentando una eficacia en la reducción de la enfermedad del 35% al 40% al finalizar la evaluación.
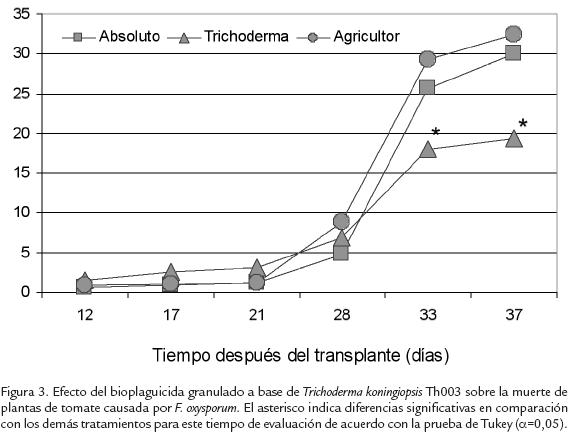
DISCUSIÓN
Dado que los aislamientos Fu040 y Fu041 fueron obtenidos de plantas de tomate con síntomas de marchitamiento vascular y de pudrición de corona y raíz respectivamente, cada uno constituye una forma especial f. sp. radicis-lycopersici y f. sp. lycopersici, respectivamente (Hibar et ál., 2007) por lo cual, se esperaba un comportamiento diferente de estos dos aislamientos de F. oxysporum. Sin embargo, en la prueba de patogenicidad no se encontraron diferencias en el ascenso del patógeno por el xilema de las plantas inoculadas. La presencia de Fu040 y Fu041 en los haces vasculares demostró que estos tienen la capacidad de penetrar las raíces y colonizar el xilema, en contraste con las cepas no patogénicas de F. oxysporum las cuales, se limitan a colonizar la corteza de las raíces y no alcanzan el sistema vascular de las plantas (Fravel et ál., 2003). Esto permitió confirmar la capacidad patogénica de los aislamientos Fu040 y Fu041 de F. oxysporum.
En el bioensayo de inducción de resistencia sistémica, las plantas de tomate tratadas en una porción de la raíz con T. koningiopsis Th003, presentaron un retraso considerable en la colonización del tallo por los aislamientos Fu040 y Fu041. A pesar de las diferencias numéricas entre los tratamientos, el ANDEVA no detectó significancia en la mayoría de los casos, debido posiblemente al alto coeficiente de variación, por lo cual se recomienda aumentar el tamaño de muestra en el experimento. En los segmentos de tallo indexados, no se observó crecimiento de Th003. Esto indicó que el antagonista y el patógeno permanecieron separados espacialmente en el hospedero, condición indispensable para la evaluación del efecto de inducción de resistencia sistémica en la planta y se puede afirmar que el sistema de división de raíces utilizado en este estudio permitió mantener esta condición de separación. Éste sistema ha sido utilizado por varios autores para evaluar el fenómeno de inducción de resistencia con agentes de biocontrol como Pencillium oxalicum (De Cal et ál., 2000), F. oxysporum Fo47 (Fuchs et ál., 1997; Duijff et ál., 1998) y Pythium oligandrum (Benhamou et ál., 1997) contra F. oxysporum en tomate. En el presente estudio se determinó la inducción de resistencia sistémica por T. koningiopsis contra este fitopatógeno sin cortar la raíz para su división, lo cual es deseable ya que las heridas pueden desencadenar respuestas de defensa en la planta (Reymond et ál., 2002) y estas podrían enmascarar el fenómeno de inducción de resistencia por el biocontrolador.
Aún no se conocen con exactitud todos los procesos involucrados en la inducción de respuestas de defensa en las plantas por T. koningiopsis Th003, otros estudios han sugerido previamente que Th003 es un agente inductor de este fenómeno en plantas de tomate. Clavijo y Cotes, 1998, informaron que semillas de tomate tratadas con Th003, presentaron un aumento de enzimas hidrolíticas con actividad β-1,3-glucanasa y endoquitinasa. También, Castillo et ál., 2007, mediante la técnica de microarreglos, encontraron que plantas de tomate híbrido Rocio® tratadas con T. koningiopsis Th003 expresaron 42 genes diferenciales, en contraste con plantas no tratadas. Dentro de estos genes, se encontraron algunos relacionados con las categorías funcionales de transporte, de traducción de señales, de respuesta a hormonas y de señalización.
La aplicación en campo de T. koningiopsis Th003 formulado como gránulos dispersables y dentro de un programa de manejo integrado de la pudrición del cuello y de la raíz del tomate, redujo significativamente la mortalidad de plantas en un 35%, resultado muy importante para los productores dada la dificultad para controlar la enfermedad con fungicidas. Adicionalmente, la implementación del manejo integrado contribuye en la reducción del uso de fungicidas químicos, y por ende la reducción de los efectos nocivos sobre el medio ambiente y el hombre.
El potencial que presenta Th003 en el control de un amplio rango de fitopatógenos (Cotes et ál., 2007; Moreno y Cotes, 2007), ha motivado estudiar los mecanismos de acción, teniendo en cuenta que el éxito de la aplicación del control biológico depende directamente del conocimiento del agente antagonista y sus interacciones con la planta hospedero, el fitopatógeno y el medio ambiente (Fravel, 2005), los avances obtenidos en este estudio contribuirán al diseño de estrategias para aumentar su eficacia y mantener la consistencia de su actividad biocontroladora.
AGRADECIMIENTOS
A COLCIENCIAS y a Corpoica entidades financiadoras del proyecto de investigación “Análisis de la expresión génica de plantas de tomate tratadas con Trichoderma koningiopsis Th003 en relación con parámetros de inducción de la resistencia y del crecimiento vegetal” en el cual se enmarcó el presente trabajo.
BIBLIOGRAFÍA
BENHAMOU N, REY P, CHÉRIF M, HOCKENHULL J, TIRILLY Y. Treatment with the mycoparasite Pythium oligandrum triggers induction of defense-related reactions in tomato roots when challenged with Fusarium oxysporum f. sp. radicis-lycopersici. Biochem Cell Biol. 1997;87:108-122.
[ Links ]BENHAMOU N, KLOEPPER J, TUZUN S. Induction of resistance against Fusarium wilt of tomato by combination of chitosan with an endophytic bacterial strain: ultrastructure and cytochemistry of the host response. Planta. 1998;204:153-168.
[ Links ]CASTILLO F, MORENO C, JAIMES Y, COTES A, RESTREPO S. Gene expression of tomato plants treated with Trichoderma koningii. CD-ROM de Memorias (Presentaciones orales) 6LABS; 2007.
[ Links ]CLAVIJO G, COTES AM. Evaluación de la actividad quitinasa en procesos de control biológico de Rhizoctonia solani y Fusarium oxysporum en tomate, mediante tratamientos de pregerminación controlada de semillas en presencia de Trichoderma koningii. Rev Colomb Biotecnol. 1998;1:58-66.
[ Links ]COTES AM, LEPOIVRE P, SEMAL J. Correlation between hydrolytic enzymes activities measured in bean seedlings after Trichoderma koningii combined with pregermination and the protective effect against Pythium splendens. Eur J Plant Pathol. 1996;102:487-506.
[ Links ]COTES AM, CÁRDENAS A, PINZON H. Effect of seed priming in the presence of Trichoderma koningii on seed and seedling disease induced in tomato by Rhizoctonia solani and Fusarium oxysporum f. sp. lycopersici. IOBC/WPRS Bull. 2001;24:259-263.
[ Links ]COTES AM, MORENO C, MOLANO L, VILLAMIZAR L, PIEDRAHITA W. Prospects for integrated management of Sclerotinia sclerotiorum in lettuce. IOBC/WPRS Bull. 2007;30:391-394.
[ Links ]DE CAL A, GARCIA-LEPE R, MELGAREJO P. Induced Resistance by Penicillium oxalicum against Fusarium oxysporum f. sp. lycopersici: histological studies of infected and induced tomato stem. Phytopathology. 2000;90:260-268.
[ Links ]DHINGRA O, SINCLAIR J. Basic plant pathology methods. Boca Raton: CRC Press; 1987.
[ Links ]DUIJFF B, POUHAIR D, OLIVIAN C, ALABOUVETTE C, LEMANCEAU P. Implication of systemic induced resistance in the suppression of Fusarium wilt of tomato by Pseudomonas fluorescens WCS417r and by nonpathogenic Fusarium oxysporum Fo47. Eur J Plant Pathol. 1998;104:903-910.
[ Links ]FRAVEL DR, OLIVIAN C, ALABOUVETTE C. Fusarium oxysporum and its biocontrol. New Phytologist. 2003;157:493-502.
[ Links ]FRAVEL DR. Commercialization and implementation of biocontrol. Annu Rev Phytopathol. 2005;43:1-23.
[ Links ]FUCHS J, MOËNNE-LOCCOZ Y, DÉFAGO G. Nonpathogenic Fusarium oxysporum strain Fo47 induces resistance to Fusarium wilt in tomato. Plant Dis. 1997;81:492-496.
[ Links ]HARMAN G, HOWELL C, VITERBO A, CHET I, LORITO M. Trichoderma species-opportunistic, avirulent plant symbionts. Nat Rev. 2004;2:43-56.
[ Links ]HIBAR K, EDEL-HERMAN V, STEINBERG CH, GAUTHERON N, DAAMI-REMADI M, ALABOUVETTE C, EL MAHJOUB M. Genetic diversity of Fusarium oxysporum populations isolated from tomato plants in Tunisia. J Phytopathol. 2007; 155: 136-142.
[ Links ]HOWELL C. Understanding the mechanisms employed by Trichoderma virens to effect biological control of cotton diseases. Phytopathology. 2006; 96:178-180.
[ Links ]MORENO C, COTES AM. Survival in the phylloplane of Trichoderma koningii and biocontrol activity against tomato foliar pathogens. IOBC/WPRS Bull. 2007;30:557-561.
[ Links ]REKAH Y, SHTIENBERG D, KATAN J. Disease development following infection of tomato and basil foliage by airborne conidia of the soilborne pathogens. Phytopathology. 2000;90:1322-1329.
[ Links ]REYMOND P, WEBER H, DAMOND M, FARMER EE. Differential gene expression in response to mechanical wounding and insect feeding in Arabidopsis. Plant Cell. 2002;12:707-719.
[ Links ]YEDIDIA I, BENHAMOU N, CHET I. Induction of defense responses in cucumber plants (Cucumis sativus L.) by the biocontrol agent Trichoderma harzianum. Appl Environ Microbiol. 1999;65:1061-1070.
[ Links ]













