Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.15 no.3 Bogotá Sept./Dec. 2010
SEGMENTACIÓN DE IMÁGENES DE RESONANCIA MAGNÉTICA EN CONTRASTE DE FASE PARA EL ESTUDIO DE LA DINÁMICA DEL LÍQUIDO CEFALORRAQUÍDEO PERIMEDULAR
Segmentation of Phase Contrast Magnetic Resonance Imaging to Study the Dynamic of Perimedullary Cerebrospinal Fluid
N. FLÓREZ1,2, Ph. D.; R. BOUZERAR3, Ph. D.; D. MORATAL4,5, Ph. D.; ME. MEYER3, Ph. D.; L. MARTÍ-BONMATÍ1, M.D., Ph, D.; O. BALÉDENT3, Ph. D.
1Servicio de Radiología, Hospital Quirón, Valencia, España. 2Grupo de investigación UNITEL, Universidad Santo Tomás, Bucaramanga, Colombia. 3Departamento de Procesamiento de Imagen y Medicina Nuclear, Hospital de Amiens, Francia. 4Centro de Biomateriales e Ingenieria Tisular, Universidad Politécnica de Valencia, España. 5Departmento de Ingeniería Electrónica, Universidad Politécnica de Valencia, España Correspondencia: Yudy Natalia Flórez. Facultad de Ingeniería de Telecomunicaciones, Universidad Santo Tomás, Bucaramanga, Colombia. nataliaf@mail.ustabuca.edu.co
Presentado 15 de marzo de 2010, aceptado 4 de junio de 2010, correcciones 22 de junio de 2010.
RESUMEN
La imagen de resonancia magnética en contraste de fase permite estudiar la dinámica del líquido cefalorraquídeo (LCR) perimedular de manera cuantitativa. Sin embargo la anatomía propia del espacio subaracnoideo dificulta la segmentación del LCR debido a la presencia de estructuras vasculares y nervios raquídeos. El objetivo de este trabajo es describir un método de segmentación semiautomático para el estudio de la dinámica del LCR perimedular. El proceso se inicializa con un punto semilla dentro de la región a analizar. El algoritmo crea un mapa de correlación, calcula un valor de umbral y clasifica píxeles de LCR combinando diversas características temporales del comportamiento del flujo como atributos de entrada a un algoritmo k-medias. Un observador llevó a cabo diez veces la segmentación en cinco sujetos sanos y se calculó el volumen por ciclo y el área en el espacio perimedular C2C3. Las variaciones de las medidas fueron evaluadas como una estimación de la reproducibilidad del método. Para esto se calculó el coeficiente de variación. La variabilidad de las medidas fue menor del 5%. El método facilita la cuantificación del LCR perimedular. En 16 sujetos sanos se cuantificó el volumen por ciclo de LCR y el área en el espacio C2C3 y cisterna prepontina.
Palabras clave: líquido cefalorraquídeo, resonancia magnética, segmentación, k-media.
ABSTRACT
Phase contrast magnetic resonance imaging allows studying quantitatively the perimedullary cerebrospinal fluid (CSF) dynamics. However, the anatomy of the subarachnoid space difficults the segmentation of CSF due to the presence of vascular structures and spinal nerves. The aim of this paper is to describe a semiautomatic segmentation method for the study of the perimedullary CSF dynamics. The process is started with a seed point within the region to analyze. The algorithm creates a correlation map, calculates a threshold value and classifies pixels of CSF combining different temporal characteristics of flow behavior as input attributes to a k-means algorithm. One observer carried out ten times the segmentation of the cervical images in 5 healthy subjects; stroke volume and area were calculated. The variability of the obtained measurements was evaluated as an estimation of the reproducibility of the method. For this the coefficient of variation was calculated. The variability of the measurements was less than 5%. The method facilitates the quantification of perimedullary CSF. Stroke volume and the area at C2C3 space and prepontine cistern were measured in 16 healthy subjects.
Key words: cerebrospinal fluid, magnetic resonance, segmentation, k-means.
INTRODUCCIÓN
Las alteraciones del flujo de líquido cefaloraquideo (LCR) son uno de los pilares fundamentales en el diagnóstico de diversos procesos neurológicos. Flujo hiperdinámico y un volumen alto por ciclo en el acueducto de Silvio se han considerado como indicadores de hidrocefalia normopresiva (HNP) y de una buena respuesta quirúrgica a la derivación de líquido cefalorraquídeo (LCR) (Bradley et al., 1996; Baledent et al., 2004). Sin embargo, hay casos con claros signos de HNP que tienen un flujo acueductal normal. Por tanto es necesario describir de manera cuantitativa la pulsatibilidad del LCR en otras regiones del sistema nervioso que permitan evaluar alteraciones en la dinámica del flujo.
La técnica de resonancia magnética (RM), específicamente las secuencias sensibles al flujo de líquidos como las de contraste de fase (RM-CF), ha permitido cuantificar el movimiento de flujo sanguíneo y de líquido cefaloraquideo (LCR) con alta precisión (Kim et al.,1999; Enzmann et al., 1993). Para obtener análisis cuantitativos fiables y reproducibles que sirvan de apoyo a la clínica, es necesario usar protocolos de adquisición adecuados y técnicas de posproceso que permitan delinear las áreas de interés (region of interest, ROI) independientemente del operador y sin influencia de volumen parcial y submuestreo (aliasing). El parametro de adquisición velocidad de codificación (Velocity encoding, Venc), debe ser mayor, pero estar próximo, a la velocidad máxima de flujo esperada en la región que se va a analizar para así evitar la presencia de submuestreo y obtener unas medidas más precisas de las variaciones temporales de la velocidad (Pelc, 1995; Wolf et al., 1993).
La anatomía propia del espacio subaracnoideo dificulta la segmentación del LCR debido a la presencia de estructuras vasculares y nervios raquídeos. Baledent et al., desarrollaron un método para segmentar el espacio cerebroespinal usando la transformada de Fourier (Baledent et al., 2001). Este método es altamente dependiente de la experiencia del usuario. La definición de la ROI es tediosa debido a la selección manual del valor de umbral. Otro grupo utilizó información tanto temporal como espacial para la segmentación del LCR (Alperin y Lee, 2003). Aunque este método fue debidamente validado mediante un fantomas con tubos circulares, un estudio reciente resalta que esta técnica no es suficiente para la determinación del flujo de LCR en regiones concentradas de flujo de alta velocidad (flow jet) (Marshall et al., 2008). El objetivo de este trabajo es proponer una aproximación para analizar la dinámica del flujo del LCR en regiones con anatómicas complejas: como el nivel cervical y cisterna prepontina modificando el método desarrollado por Alperin y Lee y teniendo en cuenta características del comportamiento temporal del LCR como atributos de entrada a un algoritmo de clasificación k-medias.
MATERIALES Y MÉTODOS
SEGMENTACIÓN DEL LCR
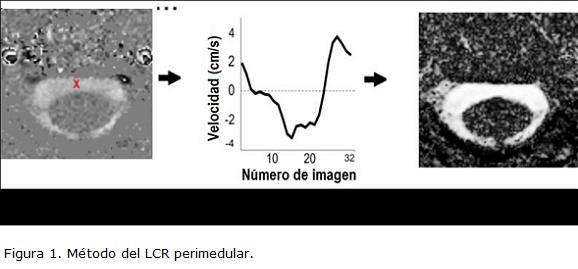
El proceso se inicializa con un punto semilla que el usuario selecciona dentro de la región a analizar (Fig. 1A). Al igual que en (Alperin y Lee, 2003), en un primer paso se crea un mapa de correlación (Fig. 1C), calculado como el coeficiente de correlación entre el perfil temporal de velocidad del punto semilla (Fig. 1B) y cada uno de los perfiles temporales de los píxeles que conforman la matriz. A continuación se calcula un valor de umbral de manera reproducible. Para calcular este valor de umbral se representan en una curva valores de umbrales desde 0,3 a 0,9 en pasos de 0,02 frente al número de píxeles segmentados por cada valor de umbral (Fig. 2A). Para escoger el valor de umbral se calcula la pendiente promedio entre puntos consecutivos de la curva siendo el valor de umbral el que coincide con la primera pendiente de la curva cuyo valor está por debajo de la pendiente promedio.
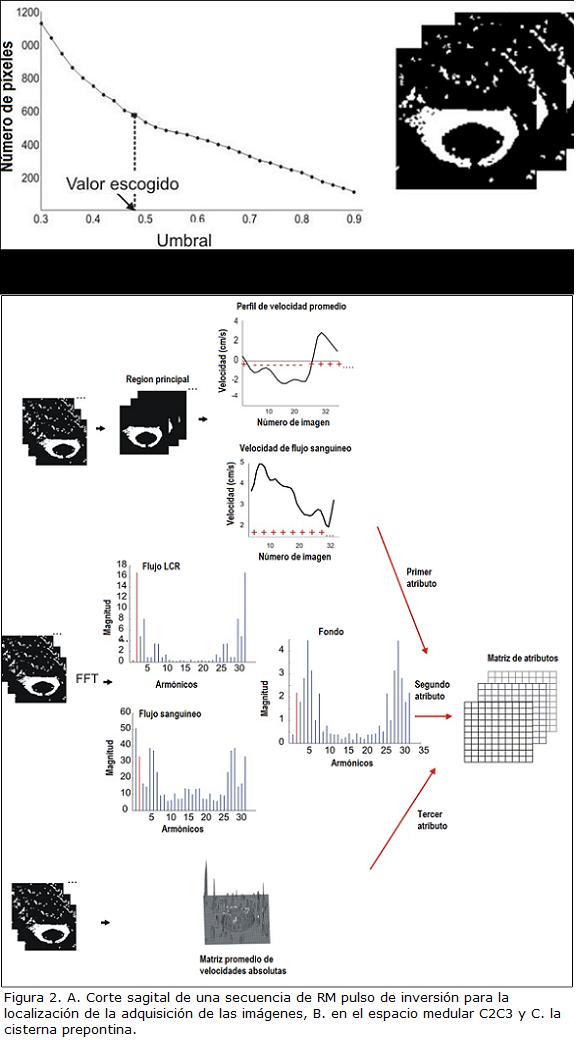
Después de umbralizar la secuencia de imágenes (Fig. 2B) se adicionó un método de clasificación de píxeles no supervisado k-medias. El cluster k-medias implementado define k=2 clases, escoge las posiciones de los iniciales de manera aleatoria y determina la distancia de cada elemento a los centroides por medio de la distancia euclidiana. La clasificación de los píxeles que forman la ROI esta basado sobre tres atributos por píxel. Se seleccionaron éstos atributos teniendo en cuenta el comportamiento de los flujos (Fig. 3).
Para calcular el primer atributo se define un perfil promedio de velocidad que caracteriza el flujo de LCR. Para esto se selecciona la región con el mayor número de píxeles. En este paso de la segmentación esta región contiene casi todos los píxeles con presencia de flujo LCR. Los perfiles de velocidad que conforman esta región son promediados. El perfil resultante contiene las velocidades promedio a lo largo de la secuencia de imágenes. El primer atributo se define entonces como el número de acuerdo entre la tendencia representada en signo del perfil promedio y cada uno de los perfiles de velocidad que conforman la matriz. Las amplitudes no son comparadas, siendo posible descartar flujo unidireccional (flujo sanguíneo).
El segundo atributo se obtiene de la descomposición espectral de la señal de velocidad obtenida durante un ciclo cardíaco en cada píxel mediante la transformada rápida de Fourier. La componente de la frecuencia fundamental, la cual corresponde a la frecuencia cardíaca del sujeto, permite excluir regiones no pulsátiles y ruido de fondo.
El último atributo se define como el promedio de la velocidad absoluta de cada píxel a lo largo de la secuencia de imágenes. De esta manera es posible diferenciar entre velocidades de LCR y velocidades altas (flujo sanguíneo) y velocidades bajas (parénquima).
Finalmente la máscara creada con la clase definida (Fig. 3A, ROI roja) es aplicada a toda la secuencia de imágenes para analizar temporalmente la dinámica del LCR. La segmentación no se realiza corte por corte sino de manera simultánea sobre la secuencia de imágenes completa.
SUJETOS Y ADQUISICIÓN DE LAS IMÁGENES
Se estudiaron 16 voluntarios sanos (diez mujeres y seis hombres), con una edad promedio de 29 ± 4 (media ± desviación estándar) años. Todos ellos fueron explorados usando un escáner de RM de 3 Teslas (Signa HDx General Electric Healthcare, WI, USA). La secuencia de imágenes de RM-CF se adquirió en sincronismo con el ciclo cardiáco empleando un dispositivo de pulso periférico. Se reconstruyeron 32 puntos temporales retrospectivamente por ciclo cardiáco.
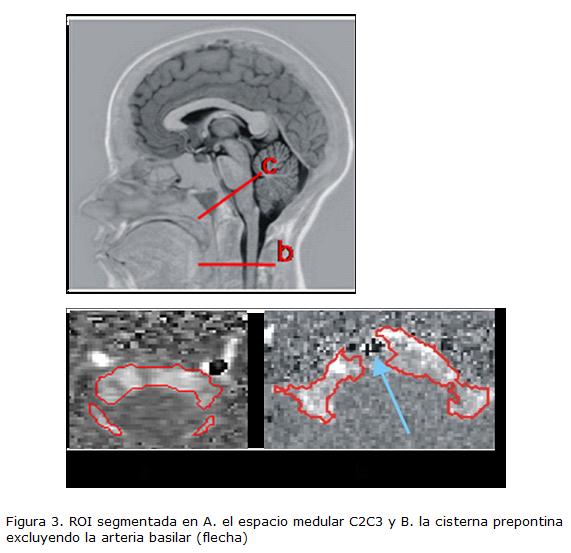
Para obtener las imágenes se utilizó un campo de visión de 140 mm, con un espesor de corte de 5 mm, y una matriz de 256 x 256 mm, ángulo de excitación de 30º, tiempo de repetición TR = 18 ms y el tiempo de eco TE = 8 ms. Para cada estudio de RM se realizaron dos adquisiciones perpendiculares a la dirección del flujo al nivel C2C3 y a cisterna prepontina con una velocidad de codificación (Velocity encoding, Venc) de 5 cm/s (Fig. 3B).
CÁLCULO DE PARÁMETROS Y REPRODUCIBILIDAD DEL MÉTODO
El volumen por ciclo (stroke volume) definido como el valor promedio del flujo en un período, independientemente del sentido, se calcula como la integral de la curva de flujo y se expresa en µl/ciclo. El área de la ROI en mm2 fue también calculada.
Un observador llevó a cabo diez veces la segmentación en cinco sujetos sanos. Se calculó el volumen por ciclo y el área en el espacio perimedular C2C3. Las variaciones de las medidas fueron evaluadas como una estimación de la reproducibilidad del método. Para esto se calculó el coeficiente de variación (CV), definido como la relación entre la desviación estándar y la media de las medidas.
RESULTADOS
La media y la desviación estándar del volumen por ciclo y área de la ROI se calcularon (datos no publicados). En la Figura 3C se pueden observar las ROIs segmentadas en el nivel C2C3 y cirterna prepontina de un sujeto sano.
El CV promedio para el volumen por ciclo obtenido en cinco sujetos sanos con diez mediciones realizadas marcando puntos semillas diferentes, demostró que la reproducibilidad del método desarrollado no se ve afectada por el punto inicial seleccionado. El CV promedio fue de 3% ± 1.5.
DISCUSIÓN
Las mediciones de flujo con RM-CF proporcionan una herramienta clínica de gran alcance para la evaluación no invasiva de la dinámica del LCR. No obstante se requiere de métodos de posproceso adecuados para delinear las regiones a analizar. El método descrito permite la cuantificación del flujo de LCR en regiones perimedulares de manera reproducible y rápida.
Dependiendo de la posición del corte, el área a analizar es divida por la presencia de los nervios raquídeos en compartimientos (posterior, anterior y lateral) (Fig. 3C). En cada uno de éstos el LCR presenta patrones de flujo pulsátiles complejos y heterogéneos (Henry-Feugeas et al., 2000) dificultando el proceso de segmentación. Para dar robustez al método se tienen en cuenta, como atributos de entrada al algoritmo de clasificación k-medias, ciertas características temporales del comportamiento del LCR. La eficacia del algoritmo del presente trabajo se atribuye principalmente al hecho de que atributos como valor absoluto de velocidad de flujo y la magnitud de la frecuencia fundamental permiten distinguir claramente las regiones de flujo pulsátil de tejidos de fondo y ruido. La pulsatibilidad del LCR a lo largo del eje craneoespinal desempeña un papel importante en la regulación de la presión intracraneal (Greitz et al., 1997). Caracterizar la dinámica de flujo en los diferentes espacios de LCR contribuirá a establecer marcadores biológicos de enfermedades neurológicas y cerebrovasculares.
La cisterna prepontina es un espacio considerable en la cara ventral de la protuberancia, conteniendo la arteria basilar. Debido a su anatomía compleja es difícil segmentar la región para extraer los diferentes parámetros. A nuestro conocimiento no existen valores publicados de flujo de LCR obtenidos en esta región. Utilizando el método presentado, fue posible delinear la cisterna pontina eliminando los píxeles de la arteria basilar y calcular el volumen por ciclo (Fig. 3C).
La principal ventaja del método desarrollado es la facilidad de cuantificar el LCR perimedular sirviendo como apoyo a la investigación de enfermedades neurológicas y cerebrovasculares. Una mejor comprensión global de la dinámica del LCR puede ayudar a entender mejor los disturbios de flujo de LCR que ocurren en patologías tales como la hidrocefalia normopresiva.
AGRADECIMIENTOS
Este trabajo ha sido financiado parcialmente por una beca de investigación de la Fundación del Colegio de Médicos de Valencia y por una beca de Formación de Personal Investigador de la Generalitat Valenciana (España).
La herramienta para el análisis cuantitativo de flujo usada en este trabajo está registrada en el Centro de Transferencia Tecnológica de la Universidad Politécnica de Valencia (España) con el número de registro CTT-0407804.
BIBLIOGRAFÍA
ALPERIN N, LEE SH. PUBS: Pulsatility-based segmentation of lumens conducting non-steady flow. Magn Reson Med 2003;49:934-944.
[ Links ]BALEDENT O, GONDRY-JOUET C, MEYER ME, DE MARCO G, LE GARS D, HENRY-FEUGEAS MC, et al. Relationship between cerebrospinal fluid and blood dynamics in healthy volunteers and patients with communicating hydrocephalus. Invest Radiol. 2004;39:45-55.
[ Links ]BALEDENT O, HENRY-FEUGEAS MC, IDY-PERETTI I. Cerebrospinal fluid dynamics and relation with blood flow. A magnetic resonance study with semiautomated cerebrospinal fluid segmentation. Invest Radiol. 2001;36:368-377.
[ Links ]BRADLEY WG, SCALZO D, QUERALT J, NITZ WN, ATKINSON DJ, WONG P. Normal-pressure hydrocephalus: evaluation with cerebrospinal fluid flow measurements at MR Imaging. Radiology. 1996;198:523-529.
[ Links ]ENZMANN DR, PELC NJ. Cerebrospinal fluid flow measured by phase-contrast cine MR. AJNR Am J Neuroradiol. 1993;14:1301-1307.
[ Links ]GREITZ D, GREITZ T, AND HINDMARSH T. A new view on the CSF-circulation with the potential for pharmacological treatment of childhood hydrocephalus. Acta Paediatr. 1997;86:125-132.
[ Links ]HENRY-FEUGEAS MC, IDY-PERETTI I, BALEDENT O, PONCELET-DIDON A, ZANNOLI G, BITTOUN J, et al. Origin of subarachnoid cerebrospinal fluid pulsations: a phase-contrast MR analysis. Magn Reson Imaging 2000;18:387-395
[ Links ]KIM DS, CHOI JU, HUH R, YUN PH, KIM DI. Quantitative assessment of cerebrospinal fluid hydrodynamics using a phasecontrast cine MR image in hydrocephalus. Childs Nervous System. 1999;15:461-467.
[ Links ]MARSHALL I, MACCORMICK I, SELLAR R, WHITTLE I. Assessment of factors affecting MRI measurement of intracranial volume changes and elastance index. Br. J. Neurosurg. 2008;22:389-397.
[ Links ]PELC NJ. Flow Quantification and Analysis Methods. MRI Clinics of North America. 1995;3:413-24.
[ Links ]WOLF RL, EHMAN RL, RIEDERER SJ, ROSSMAN PJ. Analysis of systematic and random error in MR volumetric flow measurements. Magn Reson. Med. 1993;30:82-91.
[ Links ]













