Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.19 no.3 Bogotá Sept./Dec. 2014
https://doi.org/10.15446/abc.v19n3.40909
Artículo de investigación
http://dx.doi.org/10.15446/abc.v19n3.40909
DISTRIBUCIÓN POTENCIAL DE Podocnemis lewyana (REPTILIA:PODOCNEMIDIDAE) Y SU POSIBLE FLUCTUACIÓN BAJO ESCENARIOS DE CAMBIO CLIMÁTICO GLOBAL
Potential Distribution of Podocnemis lewyana (Reptilia: Podocnemididae) and Its Possible Fluctuation Under Different Global Climate Change Scenarios
Carlos Ortíz-Yusty1, Biólogo; Adriana Restrepo1, Bióloga; Vivian P. Páez1, Ph. D.
1 Grupo Herpetológico de Antioquia, Instituto de Biología, Universidad de Antioquia. Calle 67 n.° 53 - 108, laboratorio 7-121. Medellín, Colombia. carlosyu1286@gmail.com; restrepoadriana78@gmail.com; vivianpaez1@gmail.com
Autor de correspondencia: Carlos Ortíz-Yusty, carlosyu1286@gmail.com
Recibido 19 de noviembre 2013, aceptado con modificaciones 29 de marzo 2014, fecha de reenvío 3 de junio 2014.
Citation / Citar este artículo como: ORTÍZ-YUSTY C, RESTREPO A, PÁEZ VP. Distribución potencial de Podocnemis lewyana (Reptilia: Podocnemididae) y su posible fluctuación bajo escenarios de cambio climático global. Acta biol. Colomb. 2014;19(3):471-481.
RESUMEN
En este estudio se implementó el modelaje de distribución de especies para establecer el rango de distribución potencial de Podocnemis lewyana, explorar los componentes del clima que pueden influenciar dicha distribución y evaluar posibles fluctuaciones de su distribución bajo escenarios de clima futuro. Los modelos obtenidos predicen una distribución continua de sur a norte por todo el río Magdalena, desde los municipios de Rivera y Palermo en el departamento de Huila, hasta los departamentos de Atlántico y Magdalena en el norte. La temperatura fue el elemento del clima que más influyó en la distribución de P. lewyana; esta especie tiende a estar presente en climas cálidos y con poca variabilidad en la temperatura. El modelo de distribución transferido a los escenarios de clima futuro predicen un aumento en el rango geográfico de P. lewyana. Sin embargo, teniendo en cuenta las preferencias de hábitat de esta especie y su fuerte asociación con los cuerpos de agua, este resultado debe tomarse con cautela, dado que el modelo solo tuvo en cuenta variables climáticas terrestres. Dadas las características de historia de vida de esta especie (presencia de determinación sexual dependiente de la temperatura, alta temperatura pivotal y un rango de transición de temperatura muy estrecho), y el efecto negativo de los cambios en los regímenes hidrológicos en la mortalidad embrionaria, la expansión del área potencial de P. lewyana en el futuro no significa que esta especie no vaya a verse afectada por el cambio climático global.
Palabras clave: Maxent, modelación de nicho, variables ambientales.
ABSTRACT
We implemented a species distribution modelling approach to establish the potential distribution of Podocnemis lewyana, to explore the climatic factors that may influence the species' distribution and to evaluate possible changes in distribution under future climate scenarios. The distribution models predicted a continuous distribution from south to north along the Magdalena River, from Rivera and Palermo in the department of Huila to the departments of Atlántico and Magdalena in the north. Temperature was the variable most influential in the distribution of P. lewyana; this species tends to be present in warm regions with low temperature variability. The distribution model predicted an increase in the geographic range of P. lewyana under climate change scenarios. However, taking into account the habitat preferences of this species and its strong association with water, this result should be treated with caution since the model considered only terrestrial climatic variables. Given the life history characteristics of this species (temperature-dependent sex determination, high pivotal temperature and a very narrow transition range) and the negative effect of changes in hydrological regimes on embryo survival, expansion of the potential distribution of P. lewyana in the future does not mean that the species will not be affected by global climate change.
Keywords: environmental variables, Maxent, niche modeling.
INTRODUCCIÓN
La distribución geográfica de una especie es una expresión compleja de su ecología e historia evolutiva (Brown et al., 1996) y está determinada por diversos factores que operan con diferentes intensidades a diferentes escalas (Pearson y Dawson, 2003). Dichos factores incluyen la relación de los organismos con su ambiente (e.g. condiciones climáticas y de hábitat) y las interacciones interespecíficas como la competencia, depredación y parasitismo (Chesson, 2000; Chave et al., 2002). Debido a esto, el conocimiento detallado de la distribución geográfica de las especies es fundamental para la investigación en ecología, biogeografía y biología de la conservación (Brown et al., 1996; Graham y Hijmans, 2006). Los tradicionales mapas de puntos (localidades de presencia de las especies documentadas en una región) representan las distribuciones de forma limitada, mientras que los mapas delineados por expertos en muchos casos sobreestiman o subestiman las distribuciones dependiendo del conocimiento que se tenga del grupo de estudio (Anderson et al., 2002; Graham y Hijmans, 2006). Con el fin de maximizar el conocimiento del rango geográfico de las especies, el uso de modelos de distribución de especies (SDM, por sus siglas en inglés) se ha incrementado en los últimos años (Soberon y Peterson, 2005; Elith et al., 2006; Peterson, 2006; Merow et al., 2013). Estos modelos se basan en las relaciones de la especie con variables ambientales y en sus requerimientos ecológicos para proyectar su distribución potencial (Guisan y Zimmermann, 2000; Elith et al., 2006) y permitir, por ejemplo, evaluar el efecto que podría tener algún cambio en el ambiente sobre dicha distribución (Pearson y Dawson, 2003; Franklin, 2009).
El rápido cambio climático predicho para el próximo siglo (Rogelj et al., 2012; Seneviratne et al,. 2012) ha suscitado numerosas preguntas sobre sus posibles efectos sobre los ecosistemas, y en particular sobre la potencial extinción o adaptación de las especies a los nuevos ambientes climáticos (Araújo et al., 2006; Bell y Collins, 2008). Se ha propuesto que cambios en el clima podrían ocasionar cambios en la fenología y abundancia de las especies, en sus patrones de distribución geográfica y en la composición de la comunidad o declives poblacionales (Araújo et al., 2006; Gibbon et al., 2008; Ihlow et al., 2012). Un gran número de trabajos han examinado la relación entre la distribución de las especies y el clima (e.g., Peterson y Vieglais, 2001; Escalante et al., 2007; Jones et al., 2012; Hosseini et al., 2013) y los posibles efectos del cambio climático global sobre la conformación de las áreas de distribución de las especies (e.g., Beaumont y Hughes, 2002; Araújo et al., 2006; Bystriakova et al., 2014; McDowell et al., 2014).
El efecto del cambio climático no será homogéneo en todos los taxa, ni en todas las zonas geográficas, y dependerá de la tolerancia fisiológica de los organismos (Beaumont y Hughes, 2002). Se ha sugerido que los animales poiquilotermos son particularmente sensibles al cambio climático (Araújo et al., 2006; Sinervo et al., 2010). Por ejemplo, las condiciones climáticas afectan ampliamente los patrones de actividad, el éxito de incubación y la determinación del sexo en muchas especies de reptiles (Neuwald y Valenzuela, 2011), haciéndolos particularmente vulnerables al cambio climático (Boone y Krohn, 2000; Ihlow et al., 2012). Existen evidencias de que las tortugas en particular, son uno de los grupos animales más susceptibles al cambio climático global (Corsini et al., 2011; Ihlow et al., 2012) debido a que presentan determinación sexual por temperatura (TSD) y una fuerte dependencia de la temperatura en el fitness de los individuos (Wyneken et al., 2007). Además, el efecto del clima en la distribución, diversidad y estructura de las comunidades de tortugas ha sido bien documentado (Bour 2008; Buhlmann et al., 2009; Stephens y Wiens, 2009; Ihlow et al., 2012).
Podocnemis lewyana Dumeril, 1852, es una tortuga dulceacuícola endémica de Colombia que se encuentra en los cauces principales de los ríos Magdalena, Sinú, San Jorge y bajo Cauca, así como en las ciénagas y caños asociados a éstos (Páez et al., 2012). Su distribución conocida se extiende desde el sur, en el municipio de María la Baja, departamento del Magdalena, hasta el norte en el municipio de Prado, departamento del Tolima; al este, sobre los ríos Cesar y Lebrija en el departamento del Cesar; y al oeste, sobre el rio Sinú en el departamento de Córdoba (Gallego 2004; Restrepo et al,. 2008; Páez et al., 2012). Actualmente se conocen al menos 44 localidades donde ha sido registrada esta especie; sin embargo, pocos estudios han tratado de determinar las abundancias o límites de su distribución (Gallego-García y Castaño-Mora, 2008; Restrepo et al., 2008; González-Zárate et al., 2011).
Los objetivos de este estudio comprendieron: estimar la distribución geográfica potencial de Podocnemis lewyana, establecer la importancia relativa de las variables climáticas en la conformación de dicha distribución y realizar transferencias en diferentes escenarios de clima futuro para evaluar el posible efecto del cambio climático en su distribución potencial.
MATERIALES Y MÉTODOS
Registros de ocurrencia y variables ambientales
Las 44 localidades de ocurrencia conocidas para P. lewyana fueron obtenidas de registros de literatura (Gallego 2004, Vargas-Ramírez, et al. 2007, Restrepo, et al. 2008, Correa-H, et al. 2010, Páez et al., 2012) e inspeccionadas visualmente en búsqueda de puntos geográficos potencialmente incorrectos. Se utilizó el mapa de ríos principales y cuerpos de agua de Colombia para ajustar las coordenadas obtenidas con la mayor precisión posible.
Las variables ambientales que describen el clima actual (19 variables bioclimáticas para el periodo 1950-2000 a una resolución de 30 arcs) fueron obtenidos de la base de datos WorldClim (http://www.worldclim.org/). Los datos sobre cambio climático del IPCC fueron descargados de la base de datos del Centro Internacional de Agricultura Tropical (http://www.ccafs-climate.org/). Las 19 variables climáticas utilizadas en este estudio como escenarios de cambio climático corresponden a las extrapoladas con el modelo CCSM-GCM para el año 2070, bajo los modelos de concentración de gases de efecto invernadero RCP26 y RCP85 que representan un escenario "optimista" (RCP26 = +2.6 W/m2) y otro escenario más "pesimista" (RCP85 = +8.5 W/ m2) (Weyant et al., 2009).
Previo a la construcción del modelo, la base de datos de clima actual fue reducida evaluando la variabilidad individual de cada variable en el área de estudio y mediante una matriz de correlaciones, con el fin de reducir la multicolinearidad entre las variables de entrada (Merow, et al. 2013). Para las variables que se encontraban altamente correlacionadas (r > 0,7) se escogió la variable que presentara mayor variación o la que representara mayor significado biológico para la especie. Al realizar este procedimiento, fueron retenidas siete variables climáticas (bio4, bio6, bio8, bio9, bio15, bio16, bio19). Estas variables representan variación (estacionalidad) y condiciones ambientales limitantes y constituyen a su vez dos de los factores que más influyen en la diversidad de un ecosistema, por disponibilidad de agua y energía en el ambiente (Hawkins et al., 2003).
MODELADO CON MAXENT
Se utilizó Maxent 3.3.3k (Phillips et al., 2006) para modelar el hábitat potencial para la tortuga P. lewyana y realizar transferencias a los dos escenarios de cambio climático. Maxent fue escogido debido a que actualmente es uno de los métodos más utilizados y eficaces para la modelación de distribución de especies con datos de presencia únicamente (Elith, et al. 2006, Elith, et al. 2011). La escogencia de: i) el área accesible (background o M); ii) el tipo de variables características que maxent construye (features): y iii) el tipo de salida del modelo (raw, cummulative, logistic), afectan las inferencias que se realicen del modelo, por lo que es necesario escogerlos a la luz de los conocimientos biológicos de la especie (Merow et al., 2013).
i) Área accesible o background: El área accesible tiene grandes efectos sobre la calibración, evaluación e interpretación de los modelos de distribución y por tanto debe ser definido a priori basado en las características de historia de vida de la especie de interés (Barve et al., 2011). El área de ajuste del modelo debe corresponder a las áreas del mundo que son accesibles por la especie y dependerán de las oportunidades y limitantes que tenga la especie para moverse o dispersarse (Barve et al., 2011; Merow et al., 2013). La estimación de esta área accesible es, sin embargo, una tarea desafiante en la práctica y existen varios enfoques para incluirla explícitamente en los análisis de modelamiento de nicho (Barve et al., 2011). Debido a que P. lewyana se ha detectado en las cuencas de los ríos Magdalena, Sinú y sus tributarios, a máximo 300 m s.n.m., para este estudio el área accesible se definió como toda la región transandina (occidente de la Cordillera Oriental) que estuviera por debajo de los 500 m s.n.m.
ii) Variables características o "features": Maxent construye las curvas de respuesta utilizando diferentes clases de variables (lineares, cuadráticas, producto, umbral y tipo "hinge") y dependiendo de las clases de variable que se definan el modelo resultante puede ser más o menos complejo (Merow, et al. 2013). Lo modelos más complejos pueden generar resultados más ajustados, sin embargo pueden ser más difíciles de interpretar, mientras que modelos más simples pueden generar suficiente ajuste para ser un buen resultado además de ser más fácilmente interpretables (Merow, et al. 2013). Con el fin de definir cuáles variables características son las más adecuadas para este caso de estudio, se realizaron modelos definiendo cada uno con un tipo de variable para luego ser comparados con el programa ENMTools 1.4.3 (Warren, et al. 2010).
Los cinco modelos entrenados con las siete variables climáticas definidas anteriormente y los 44 puntos de ocurrencia fueron comparados mediante el cálculo del coeficiente de información de Akaike estandarizado (AICc). De acuerdo con esta comparación, los modelos que mejor desempeño mostraron fueron los entrenados con las variables de tipo linear, cuadrático y umbral. Con el fin de interpretar los resultados de los modelos de forma más eficiente, se escogieron los modelos con variables tipo linear para determinar la influencia de las variables climáticas en la distribución de P. lewyana.
iii) Tipo de salida: para crear el mapa de rango geográfico de P. lewyana fue utilizado el formato de salida acumulativo (cummulative) y el máximo valor de sensibilidad en el entrenamiento más la especificidad como valor de corte (Maximum training sensitivity plus specificity), que ha sido considerado como uno métodos más robustos para generar mapa de distribución de los binario a partir del mapa contínuo de probabilidades (Liu, et al. 2005). Para el análisis de idoneidad de hábitat y la influencia de las variables climáticas en la distribución geográfica de la especie se utilizó el formato de salida crudo (raw) como recomiendan Merow et al., (2013).
IMPORTANCIA DE LAS VARIABLES AMBIENTALES
Con el fin de establecer la importancia relativa de los factores del clima sobre la conformación del área de distribución geográfica de P. lewyana, se realizaron análisis de Jackknife, en los que se ajustan los modelos con una sola variable a la vez y se mide el ajuste respecto al modelo completo (con todas las variables). Adicionalmente, se ajustan modelos excluyendo una variable cada vez y se comparan nuevamente con el modelo completo. Con este procedimiento se puede identificar las variables que más información aportan al modelo por sí solas y las variables que más información poseen y que no aparece en otras variables.
EVALUACIÓN DEL MODELO
Los modelos obtenidos con Maxent, fueron evaluados estadísticamente analizando el área bajo la curva (AUC: Area Under the Curve). El área bajo la curva (AUC) varía de 0 a 1, entre más cercano sea a 1 el valor de AUC quiere decir que el modelo tiene buen desempeño, mientras que valores cercanos o por debajo de 0,5 indican que el modelo no es más informativo que lo obtenido por azar. Cada análisis realizado (hábitat potencial en el presente y las transferencias a los dos escenarios de cambio climático) fue replicado diez veces con la opción de validación cruzada, usando diferentes subconjuntos de presencias para entrenar y validar el modelo. Los diez valores de idoneidad de hábitat, AUC, valores de corte e importancia de cada variable climática para cada análisis fueron promediados para obtener un valor único.
Adicionalmente, se realizó una evaluación empírica del modelo obtenido, visitando cinco localidades para determinar la presencia de P. lewyana en zonas donde no se han hecho reportes de su presencia o ausencia. Las localidades visitadas fueron seleccionadas dentro de la región Caribe basados en las facilidades logísticas e intereses de investigación particular de los autores. Dos de las localidades escogidas correspondían a zonas donde el modelo promedio predecía presencia de la especie, y para las otras tres predecía ausencia. Para determinar la presencia de la tortuga en estas localidades, se realizó búsqueda activa en los cuerpos de agua, posibles playas de anidamiento y lugares de asoleamiento, y se complementó con información secundaria obtenida de pescadores y habitantes de las diferentes zonas. Se asumió que, al ser una especie de consumo humano, si los pescadores de cada zona no reconocen la especie es porque esta no se ha distribuido históricamente en la localidad particular.
RESULTADOS
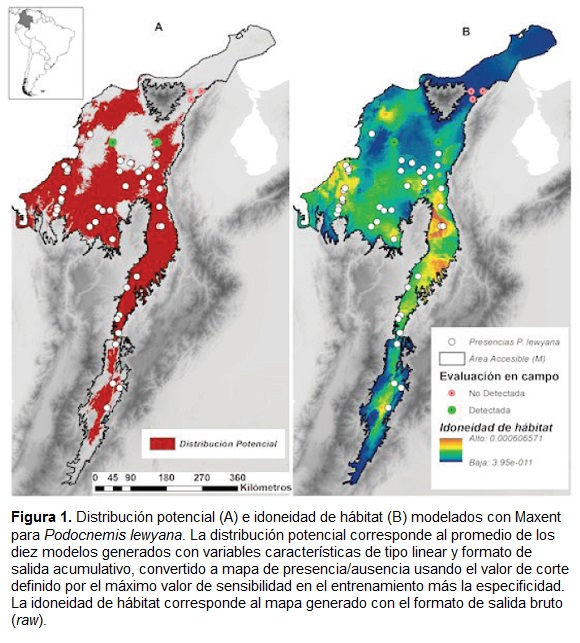
Los modelos de distribución para Podocnemis lewyana, entrenados con las variables de clima contemporáneo, obtuvieron en promedio un AUC de 0,74 (Rango: 0,726 - 0,749), indicando un buen desempeño con bajos niveles de errores de comisión e identificando correctamente todas las localidades donde ha sido reportada P. lewyana (Fig. 1). La evaluación empírica realizada permitió afirmar la utilidad y eficiencia del modelo para encontrar nuevos sitios de presencia de la especie. En las dos localidades visitadas donde el modelo predijo que la especie se distribuye, fue posible comprobar directamente la presencia de la especie al ser avistada en campo. Por otra parte las tres localidades visitadas donde el modelo predijo ausencia de la especie no se logró avistar y las personas que habitan las diferentes zonas no reconocen a P. lewyana como un elemento de sus actividades pesqueras, por lo que se asumió esto como una ausencia confirmada.
El modelo predice una distribución continua de P. lewyana, desde el sur hasta los departamentos de Magdalena y Atlántico, en el norte. Entre los departamentos de Bolívar y Magdalena, a la altura de la Serranía de San Jacinto al occidente y la Ciénaga de Zapayán al oriente, el modelo no predice la presencia de la especie. En esta zona, la temperatura es más baja que las observadas en los lugares donde se observó P. lewyana y donde fue predicha por el modelo. Sin embargo, es necesario verificar la presencia de P. lewyana en esta región. Igualmente, el modelo no predice la presencia de P. lewyana en la desembocadura del río Magdalena o en el piedemonte de la Sierra Nevada de Santa Marta; pero Páez et al., (2012) muestran tres registros en estas localidades, siendo la distribución más al norte del país, lo que puede indicar que la especie puede estar ocupando una zona límite de su distribución y que no es adecuada para su presencia.
La localidad más al noreste conocida para la especie era la ciénaga de Zapatosa (Bolívar). Al visitar el corregimiento de Santa Cecilia, municipio de Astrea (Cesar), se pudo comprobar la presencia de P. lewyana en el río Cesar, según la predicción del modelo. No encontramos evidencias de la presencia de P. lewyana más al norte subiendo por el mismo río. Hurtado (1973) reportó la extirpación de la especie del río Ranchería en La Guajira; sin embargo, el modelo no predijo su presencia en este cuerpo de agua, y al visitar la zona no se encontraron indicios de su presencia, ya que al mostrarle fotografías a las personas que habitaban a orillas del río en ningún caso dijeron conocerla (Fig. 1).
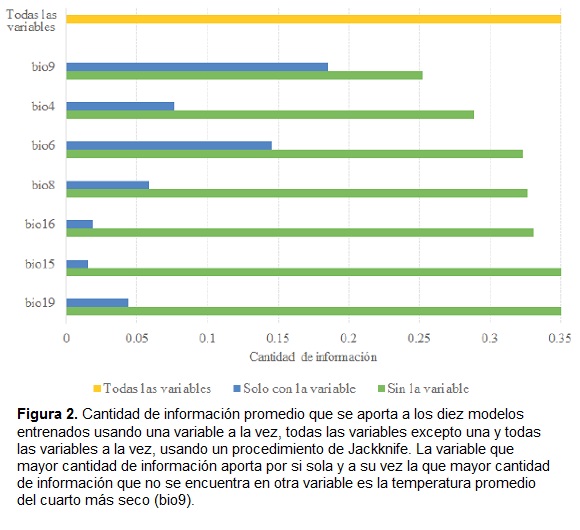
La temperatura promedio del cuarto más seco (bio9) fue la variable que aportó mayor información al modelo al usarse individualmente, y a su vez la que contiene mayor cantidad de información que no se encuentra en otra variable (Fig. 2). En general las variables que más aportan información a los modelos de distribución de P. lewyana son las que se encuentran relacionadas con la temperatura (bio4: estacionalidad en la temperatura; y bio6: temperatura mínima del mes más frio).
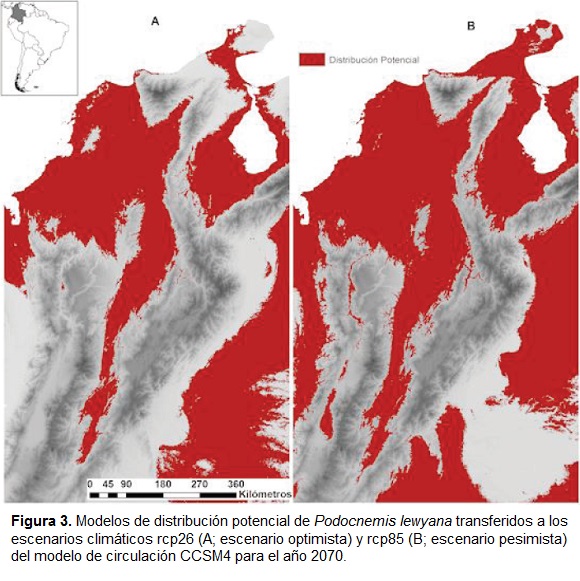
La transferencia del modelo entrenado con las variables de clima contemporáneo hacia los dos escenarios climáticos (rcp26 y rcp85) del modelo de circulación CCSM4 muestran un aumento en el área de distribución potencial de P. lewyana para el año 2070 (Fig. 3). Sin embargo, dado que la distribución de esta especie se encuentra limitada a los cuerpos de agua, este resultado debería interpretarse como que el cambio en los factores climáticos proyectados, no supondrán efectos negativos que limiten o disminuyan la distribución de P. lewyana.
DISCUSIÓN
La distribución de las especies de tortugas presentes en Colombia ha sido moldeada principalmente por el levantamiento de la cordillera de los Andes y el surgimiento del Istmo de Panamá (Galvis et al., 2012). En particular, la presencia de P. lewyana en el norte de Colombia, a diferencia de los demás representantes de la familia Podocnemididae, que se encuentran en las cuencas del Amazonas y Orinoco, estuvo determinada por el surgimiento de la Cordillera Oriental (Vargas-Ramírez et al., 2008). El levantamiento del Istmo de Panamá, que facilitó el arribo de tortugas Cryptodiras de Norte y Centroamérica, las cuales se adaptaron muy bien a las condiciones tropicales, jugó igualmente un importante papel en la restricción y distribución actual de los podocnemídidos (Cadena, 2012). La distribución conocida de P. lewyana se extiende a lo largo de las cuencas de los ríos Magdalena (incluyendo los ríos Cauca, San Jorge y Nechí), principal sistema fluvial de Colombia y uno de los complejos acuáticos más extensos de Sudamérica (Gallo y Díaz-Sarmiento, 2003) y el río Sinú, presentando una distribución simpátrica con Trachemys calliristris, Rhinoclemmys melanosterna y Cryptochelys leucostomum, todas tortugas Cryptodiras. En el río Magdalena, la localidad más al sur en la que ha sido registrada P. lewyana es en el municipio de Prado (Tolima) y a partir del modelo, el límite de la distribución potencial al sur se extiende hasta el norte del departamento del Huila en los límites de los municipios de Rivera y Palermo.
Al oriente, la distribución de la especie está restringida al río Magdalena y sus cuerpos de agua asociados. Pauler y Trebbau (1995), encontraron un individuo de P. lewyana proveniente del río Tarra, un tributario del río Catatumbo en Venezuela; sin embargo, este es el único registro de P. lewyana en ese país, por lo que se considera que fue producto de una introducción antrópica desde Colombia (Rivas et al., 2012). P. lewyana no se encuentra al occidente de la Cordillera Occidental, en el Chocó biogeográfico, y la distribución más al occidente se considera el río Sinú, donde se encuentra a lo largo de toda su extensión. Rueda Almonacid et al., (2007) registraron la presencia de la especie en el río Mulatos, en el Urabá antioqueño; pero este registro no cuenta con soportes en bases de datos o literatura a la que hayamos podido acceder. El límite de la distribución modelada de P. lewyana al occidente es el río San Juan en el Urabá Antioqueño, lo que podría indicar un muestreo pobre en esa zona o la existencia de barreras ecológicas o biogeográficas que no están siendo tenidas en cuenta en la modelación realizada en este estudio. Tradicionalmente se ha propuesto que los reptiles que habitan en climas templados se verán beneficiados por un incremento en la temperatura del ambiente (Kearney y Porter, 2009) y que por el contario, las especies de reptiles que habitan en tierras bajas o regiones tropicales se verían amenazadas por un incremento en la temperatura (Huey et al., 2009; Sinervo et al., 2010). Dado que la distribución de P. lewyana parece estar restringida principalmente por las temperaturas bajas, los diferentes escenarios de cambio climático no predicen la contracción de su rango de distribución. Por el contario, el modelo muestra nuevas áreas climáticamente disponibles para P. lewyana, por ejemplo las cuencas de los ríos San Juan y Mulatos en el Urabá Antioqueño, y el río Cesar hacia el norte. Sin embargo, es importante anotar que al modelar la distribución potencial solo se tiene en cuenta la relación con el clima, y no se consideran la presencia de barreras geográficas, interacciones ecológicas o requerimientos de hábitat que podrían determinar la distribución de una especie (Guisan y Zimmermann, 2000; Soberon y Peterson, 2005). Por ejemplo, Araújo et al., (2006) encontraron, al modelar el área de distribución de especies de reptiles bajo escenarios de cambio climático, que sus áreas potenciales de distribución podían expandirse, pero al restringir la capacidad de dispersión de los organismos, condición que se cumple para la mayoría de las especies de reptiles acuáticas, encontraron que los rangos de distribución podrían contraerse.
Además de considerar la capacidad de dispersión, es importante tener en cuenta otras características fisiológicas, comportamentales y de la historia de vida, para poder evaluar la respuesta de una especie ante un escenario de cambio climático (Moritz y Agudo, 2013). Por ejemplo, el efecto de la temperatura ambiental en las proporciones sexuales de las especies que presentan determinación sexual por temperatura (TSD por sus siglas en inglés) ha sido un aspecto considerado ampliamente. Teniendo en cuenta que la temperatura el aire está correlacionada fuertemente con la temperatura de los nidos (Janzen 1994, Fuentes, et al. 2010), se ha predicho que el aumento en la temperatura puede ocasionar feminización de las poblaciones de algunas especies, aumentando su probabilidad de extinción en el futuro (Nelson, et al. 2004, Hulin, et al. 2009, Fuentes, et al. 2010, Kallimanis 2010). P. lewyana presenta TSD y aunque su temperatura umbral es la más alta reportada para una especie de reptil, su rango transicional en las poblaciones del Magdalena es muy estrecho (Páez et al., 2009), lo que hace a estas poblaciones especialmente vulnerables, ya que las condiciones termales necesarias para producir neonatos de ambos sexos ya no se encontrarán disponibles. Hulin et al., (2009) propusieron que las especies con rangos transicionales estrechos y tiempos generacionales muy largos tienen cuatro alternativas para responder al cambio climático: modificar su rango geográfico, convertirse a determinación sexual genética, modificar su comportamiento de anidación, o extinguirse.
Hasta la fecha no se ha reportado ninguna especie de tortuga que pueda cambiar su mecanismo de determinación sexual bajo condiciones ambientales específicas, como si ocurre para ciertos lagartos (Mitchell y Janzen, 2010). Por el contrario, si se han encontrado evidencias de cambios en el comportamiento de anidación en respuesta a las condiciones climáticas, como cambios en las fechas de postura, profundidad del nido o del sitio de ovoposición (Morjan, 2003; Schwanz y Janzen, 2008; Refsnider et al., 2013). Se ha observado que por sí solos estos cambios en el comportamiento de las hembras, no podrán reversar la tendencia a la feminización de las poblaciones debido al aumento en la temperatura ambiental (Refsnider et al., 2013).
Sin embargo, las tortugas y cocodrilos, cuyo principal mecanismo de determinación sexual es el TSD, sufrieron bajas tasas de extinción durante los períodos de calentamiento que vivió el planeta en el Paleoceno-Eoceno y el Cretáceo-Paleógeno (Silber et al., 2011), lo que podría sugerir que estos grupos presentan mecanismos exitosos para responder al cambio climático. En Chelonia mydas, por ejemplo, se encontró que aunque las proporciones sexuales de los neonatos obtenidos en las playas podían ser de 0,95 hembras, las proporciones sexuales en grupos de adultos eran de 1,4 machos por cada hembra reproductiva (Wright et al., 2012). Este mismo resultado se ha observado en P. lewyana en el Magdalena Medio, donde las proporciones sexuales en adultos son de 1,29 machos por cada hembra, y esto teniendo en cuenta que la cosecha en este lugar ha estado sesgada históricamente hacia las hembras (Alzate, 2013). En este punto es importante tener en cuenta que aunque las proporciones sexuales de los adultos observados hoy corresponden a los neonatos obtenidos hace varias décadas atrás, el proceso de calentamiento global que estamos experimentando actualmente se inició hace aproximadamente 50 años (Fernández-Chacón et al., 2011). Si bien la respuesta de las especies al cambio climático global es incierta, existen características de la historia de vida que hacen más vulnerables a algunos grupos. P. lewyana, al ser una especie tropical, de tierras bajas, de agua dulce, longeva, endémica, presentar TSD y un estrecho rango transicional en algunas poblaciones, estar sujeta a la cosecha antrópica, y la transformación del hábitat (Páez et al., 2012), es una especie particularmente vulnerable al cambio climático. Aunque su rango de distribución no parece verse afectado por un incremento en la temperatura, es importante evaluar si esta especie presenta mecanismos para responder al acelerado incremento en la temperatura que se prevé en los próximos años.
Finalmente, con la aplicación de técnicas de modelaje de distribución de especies fue posible establecer que P. lewyana presenta un rango geográfico potencial continuó de sur a norte a lo largo del río Magdalena, siendo la temperatura la variable climática que mayor influencia presenta sobre la conformación de este. Las transferencias realizadas a los escenarios de clima futuros permitirían inferir que el área de distribución potencial P. lewyana aumentaría, sin embargo dichas predicciones deben ser tomadas con cautela teniendo en cuenta las preferencias de hábitat de la especie y las limitaciones propias de las metodologías de modelaje de distribución. Teniendo en cuenta que esta especie presenta determinación sexual dependiente de la temperatura, alta temperatura pivotal y un rango de transición de temperatura muy estrecho, sumado al efecto negativo de los cambios en los regímenes hidrológicos en la mortalidad embrionaria, la expansión del área potencial de P. lewyana en el futuro no significa que esta especie no vaya a verse afectada por el cambio climático global.
AGRADECIMIENTOS
Este trabajo fue realizado gracias al apoyo del programa de Jóvenes Investigadores e Innovadores de Colciencias, a la Universidad de Antioquia y al Grupo Herpetológico de Antioquia (GHA). Agradecemos a los dos evaluadores anónimos que contribuyeron de manera importante en la revisión de este trabajo.
REFERENCIAS
Alzate DA. Estructura poblacional de la tortuga de río Podocnemis lewyana (Testudines, Podocnemididae) en el Magdalena medio, Colombia. Trabajo de Grado, Universidad de Antioquia, Medellín, Colombia. 2003. 61 p. [ Links ]
Anderson RP, Peterson AT, Gómez-Laverde M. Using niche-based GIS modeling to test geographic predictions of competitive exclusion and competitive release in South American pocket mice. Oikos. 2002;98(1):3-16 [ Links ]
Araújo MB, Thuiller W, Pearson RG. Climate warming and the decline of amphibians and reptiles in Europe. J Biogeogr. 2006;33(10):1712-1728. [ Links ]
Barve N, Barve V, Jiménez-Valverde A, Lira-Noriega A, Maher SP, Peterson AT, et al. The crucial role of the accessible area in ecological niche modeling and species distribution modeling. Ecol Modell. 2011;222(11):1810-1819. [ Links ]
Beaumont LJ, Hughes L. Potential changes in the distributions of latitudinally restricted Australian butterfly species in response to climate change. Glob Chang Biol. 2002;8(10):954-971. [ Links ]
Beaumont LJ, Pitman A, Perkins S, Zimmermann NE, Yoccoz NG, Thuiller W. Impacts of climate change on the world´s most exceptional ecoregions. Proc Natl Acad Sci USA. 2011;108(6):2306-2311. [ Links ]
Bell G, Collins S. Adaptation, extinction and global change. Evol Appl. 2008;1(1):3-16. [ Links ]
Boone RB, Krohn WB. Partitioning sources of variation in vertebrate species richness. J Biogeogr. 2000;27(2):457-470. [ Links ]
Bour R. Global diversity of turtles (Chelonii; Reptilia) in freshwater. In: Lévêque C, Segers H, Martens K, editors. Freshwater animal diversity assessment (Vol. 198). Springer. Dordrecht, Netherlands; 2008. p. 593-598. [ Links ]
Brown JH, Stevens GC, Kaufman DM. The geographic range: size, shape, boundaries, and internal structure. Annu Rev Ecol Syst. 1996;27:597-623. [ Links ]
Buhlmann KA, Akre TSB, Iverson JB, Karapatakis D, Mittermeier RA, et al. A global analysis of tortoises and freshwater turtle distributions with identification of priority conservation areas. Chelonian Conserv Biol. 2009;8(2):116-149. [ Links ]
Busby JR. BIOCLIM: a bioclimate analysis and prediction system. In: Margules CR, Austin MP, editors. Nature Conservation: Cost Effective Biological Surveys and Data Analysis. CSIRO. Austin, Australia;1991. p.64-68. [ Links ]
Bystriakova N, Ansell SW, Russell SJ, Grundmann M, Vogel JC, Schneider H. Present, past and future of the European rock fern Asplenium fontanum: combining distribution modelling and population genetics to study the effect of climate change on geographic range and genetic diversity. Ann Bot. 2014;113(3): 453-465. [ Links ]
Cadena EA. Historia evolutiva y paleobiogeográfica de las tortugas de Colombia. In: Páez VP, Morales-Betancourt MA, Lasso CA, Castaño-Mora OV, Bock BC, editors. V. Biología y conservación de las tortugas continentales de Colombia. Serie Editorial Recursos Hidrobiológicos y Pesqueros Continentales de Colombia. Instituto de Investigación y Recursos Biológicos Alexander von Humboldt (IAvH). Bogotá D.C., Colombia; 2012. p.71-80. [ Links ]
Carpenter G, Gillison AN, Winter J. DOMAIN: A flexible modelling procedure for mapping potential distributions of plants and animals. Biodivers Conserv. 1993;2(6):667-680. [ Links ]
Chave J, Muller-Landau HC, Levin SA. Comparing Classical Community Models: Theoretical Consequences for Patterns of Diversity. Am Nat. 2002;159(1):1-23. [ Links ]
Chesson P. Mechanisms of maintenance of species diversity. Annu Rev Ecol Syst. 2000;31:343-366. [ Links ]
Correa-H JC, Cano-Castaño AM, Páez VP, Restrepo A. Reproductive ecology of the Magdalena River turtle (Podocnemis lewyana) in the Mompos Depression, Colombia. Chelonian Conserv Bi. 2010; 9(1):70-78. [ Links ]
Corsini JA, Smith TR, Leite MB. Turtle decline in the early oligocene of Western Nebraska. J Herpetol. 2011;45(2):238-243. [ Links ]
Elith J, Graham CH, Anderson RP, Dudík M, Ferrier S, Guisan A, et al. Novel methods improve prediction of species' distributions from occurrence data. Ecography. 2006;29(2):129-151. [ Links ]
Elith J, Phillips SJ, Hastie T, Dudík M, Chee YE, Yates CJ. A statistical explanation of MaxEnt for ecologists. Divers distrib. 2011;17(1):43-57. [ Links ]
Escalante T, Sánchez-Cordero V, Morrone JJ, Linaje M. Areas of endemism of Mexican terrestrial mammals: A case study using species' ecological niche modeling, Parsimony Analysis of Endemicity and Goloboff fit. Interciencia. 2007;32(3):151-154. [ Links ]
Fernámdez-Chacón A, Bertolero A, Amengual A, Tavecchia G, Homar V, Oro D. Spatial heterogeneity in the effects of climate change on the population dynamics of a Mediterranean tortoise. Glob Chang Biol. 2011;17(10):3075-3088. [ Links ]
Fielding AH, Bell JF. A review of methods for the assessment of prediction errors in conservation presence/absence models. Environ Conserv. 1997;24(1):38-49. [ Links ]
Franklin J. Mapping species distributions: spatial inference and prediction. Cambridge University Press, Cambridge; 2009. 319 p. [ Links ]
Fuentes MMPB, Hamann M, Limpus CJ. Past, current and future thermal profiles of green turtle nesting grounds: Implications from climate change. J Exp Mar Bio Ecol. 2010;383(1):56-64. [ Links ]
Gallego N. Anotaciones sobre la historia natural de la tortuga de río Podocnemis lewyana (Testudinata: Podocnemididae) en el río Sinú, Córdoba, Colombia. Tesis de grado, Universidad Militar Nueva Granada, Bogotá, Colombia; 2004. 83 p. [ Links ]
Gallego-García N, Castaño-Mora OV. Ecology and status of the Magdalena River turtle, Podocnemis lewyana, a Colombian endemic. Chelonian Conserv Biol. 2008;7(1):37-44. [ Links ]
Gallo H, Díaz-Sarmiento J. Variabilidad genética del bagre rayado Pseudoplatystoma fasciatum, (Pises: Pimelodidae) en el río Magdalena (Colombia). Rev. Acad Colomb Cienc. 2003:27(105):599-605. [ Links ]
Galvis G, Mesa LM, Lasso CA. Biogeografía continental colombiana: un enfoque desde la hidrografía. In: Páez VP, Morales-Betancourt MA, Lasso CA, Castaño-Mora OV, Bock BC, editors. V. Biología y conservación de las tortugas continentales de Colombia. Serie Editorial Recursos Hidrobiológicos y Pesqueros Continentales de Colombia. Instituto de Investigación y Recursos Biológicos Alexander von Humboldt (IAvH). Bogotá D.C.; 2012. p. 81-90. [ Links ]
Gibbon JW, David ES, Travis JR, Kurt AB, Tracey DT, Brian SM, et al. The global decline of reptiles, déjà vu amphibians. BioScience. 2000;50(8):653-666. [ Links ]
González-Z A, Montenegro OL, Castaño-Mora OV. Caracterización del hábitat de la tortuga de río Podocnemis lewyana, en el río Prado, aguas abajo del embalse de Hidroprado, Tolima, Colombia. Caldasia. 2011;33(2):471-493. [ Links ]
Graham CH, Hijmans RJ. A comparison of methods for mapping species ranges and species richness. Glob Ecol Biogeogr. 2006;15(6):578-587. [ Links ]
Guisan A, Zimmermann NE. Predictive habitat distribution models in ecology. Ecol Modell. 2000;135(2):147-186. [ Links ]
Hawkins BA, Field R, Cornell HV, Currie DJ, Guégan JF, Kaufman DM, et al. Energy, water, and broad-scale geographic patterns of species richness. Ecology. 2003;84(12):3105-3117. [ Links ]
Hijmans RJ, Cameron SE, Parra JL, Jones PG, Jarvis A. WorldClim. Available at: www.worldclim.org. [ Links ]
Hosseini S, Kappas M, Zare Chahouki M, Gerold G, Erasmi S, Rafiei Emam A. Modelling potential habitats for Artemisia sieberi and Artemisia aucheri in Poshtkouh area, central Iran using the maximum entropy model and geostatistics. Ecol Inform. 2013;(18): 61-68. [ Links ]
Huey RB, Deutsch CA, Tewksbury JJ, Vitt LJ, Hertz PE, Pérez HJA, et al. Why tropical forest lizards are vulnerable to climate warming. Proc R Soc Lond B Biol Sci. 2009;276:1939-1948. [ Links ]
Hulin V, Delmas V, Girondot M, Godfrey M, Guillon JM. Temperature-dependent sex determination and global change: are some species at greater risk? Oecologia. 2009;160(3):493-506. [ Links ]
Hurtado SN. Algunos aspectos bioecológicos de Podocnemis lewyana (Dumeril, 1984) (Testudinata: Pleurodira: Pelomedusidae 1830). Biol 1. Centro de Investigaciones Biológicas Pesqueras del Río Magdalena. Caldas, Colombia; 1973. 34 p. [ Links ]
Ihlow F, Dambach J, Engler JO, Flecks M, Hartmann T, Nekum S, et al. On the brink of extinction? How climate change may affect global chelonian species richness and distribution. Glob Chang Biol. 2012;18(5):1520-1530. [ Links ]
Janzen FJ. Climate change and temperature-dependent sex determination in reptiles. Proc Natl Acad Sci. 1994;91(16):7487-7490. [ Links ]
Jones MC, SR Dye, Pinnegar JK, Warren R, Cheung WW. Modelling commercial fish distributions: Prediction and assessment using different approaches. Ecol Model. 2012;225:133-145. [ Links ]
Kallimanis AS. Temperature dependent sex determination and climate change. Oikos. 2010;119(1):197-200. [ Links ]
Kearney M, Porter WP. Mapping the fundamental niche: physiology, climate, and the distribution of a nocturnal lizard. Ecology. 2004;85(11):3119-3131. [ Links ]
Kearney M, Porter WP. Mechanistic niche modelling: combining physiological and spatial data to predict species' ranges. Ecol Lett. 2009;12:334-350. [ Links ]
Liu C, Berry PM, Dawson TP, Pearson RG. Selecting thresholds of occurrence in the prediction of species distributions. Ecography. 2005;28(3):385-393. [ Links ]
Luoto M, Kuussaari M, Toivonen T. Modelling butterfly distribution based on remote sensing data. J Biogeogr. 2002;29(8):1027-1037. [ Links ]
Mcdowell W, Benson A, Byers J. Climate controls the distribution of a widespread invasive species: implications for future range expansion. Freshwater Biol. 2014;59 (4):847-857 [ Links ]
Merow C, Smith MJ, Silander JA. A practical guide to MaxEnt for modeling species' distributions: what it does, and why inputs and settings matter. Ecography. 2013;36(10): 1058-1069. [ Links ]
Miller RI, Stuart SN, Howell KN. A methodology for analyzing rare species distribution patterns utilizing GIS technology: The rare birds of Tanzania. J Landscape Ecol. 1989;2(3):173-189. [ Links ]
Mitchell NJ, Janzen FJ. Temperature-dependent sex determination and contemporary climate change. Sex Dev. 2010;4(1-2):129-140. [ Links ]
Moritz C, Agudo R. The Future of Species Under Climate Change: Resilience or Decline?. Science. 2013;341:504-508. [ Links ]
Morjan CL. How rapidly can maternal behavior affecting primary sex ratio evolve in a reptile with environmental sex determination? Am Nat. 2003;162(2):205-219. [ Links ]
Nelson NJ, Thompson MB, Pledger S, Keall SN, Daugherty CH. Do TSD, sex ratios, and nest characteristics influence the vulnerability of tuatara to global warming?. Int Congr Ser. 2004;1275:250-257. [ Links ]
Neuwald JL, Valenzuela N. The lesser known challenge of climate change: termal variance and sex-reversal in vertebrates with temperature-dependent sex determination. PLoS One. 2011;6(3):e18117. [ Links ]
Nix HA. A biogeographic analysis of Australian elapid snakes. Aust Flora Fauna Series. 1986;8:4-15. [ Links ]
Páez VP, Correa-Hurtado JC, Cano AM. A comparison of maternal and temperature effects on sex, size and growth of hatchlings of the Magdalena River turtle (Podocnemis lewyana) incubated under field and laboratory conditions. Copeia. 2009;4:698-704. [ Links ]
Páez VP, Restrepo A, Vargas-Ramírez M, Bock BC, Gallego-García N. Podocnemis lewyana. In: Páez VP, Morales-Betancourt MA, Lasso CA, Castaño-Mora OV, Bock BC, editors. V. Biología y conservación de las tortugas continentales de Colombia. Serie Editorial Recursos Hidrobiológicos y Pesqueros Continentales de Colombia. Instituto de Investigación y Recursos Biológicos Alexander von Humboldt (IAvH). Bogotá DC, Colombia; 2012. [ Links ]
Pauler I, Trebbau P. Erstnachweis von Podocnemis lewyana Duméril, 1852 (Testudines) in Venezuela. Salamandra. 1995;31:181-186. [ Links ]
Pearson RG, Dawson TP. Predicting the impacts of climate change on the distribution of species: are bioclimate envelope models useful? Glob Ecol Biogeogr. 2003;12(5):361-371. [ Links ]
Pearson RG, Dawson TP. Predicting the impacts of climate change on the distribution of species: are bioclimate envelope models useful?. Global Ecol Biogeogr. 2003;12: 361-371. [ Links ]
Peterson AT, Vieglais DA. Predicting species invasions using ecological niche modeling: new approaches from bioinformatics attack a pressing problem. BioScience. 2001;51(5):363-371. [ Links ]
Peterson AT. Uses and requirements of ecological niche models and related distributional models. Biodiversity Informatics. 2006;3:59-72. [ Links ]
Phillips SJ, Anderson RP, Schapire RE. Maximum entropy modeling of species geographic distributions. Ecol Modell. 2006;190(3):231-259. [ Links ]
Raxworthy CJ, Martínez-Meyer E, Horning N, Nussbaum RA, Schneider GE, Ortega-Huerta MA, et al. Predicting distributions of known and unknown reptile species in Madagascar. Nature. 2003;426(6968):837-841. [ Links ]
Refsnider JM, Bodensteiner BL, Reneker JL, Janzen FJ. Nest depth may not compensate for sex ratio skews caused by climate change in turtles. Anim Conserv. 2013;16(5):481-490. [ Links ]
Restrepo A, Páez VP, López C, Bock BC. Distribution and status of Podocnemis lewyana in the Magdalena River drainage of Colombia. Chelonian Conserv Biol. 2008;7(1):45-51. [ Links ]
Restrepo A, Bock BC, Páez VP. Genetic variability in the Magdalena river turtle, Podocnemis lewyana (Duméril, 1852), in the Mompos depression, Colombia. Actu Biol. 2008;30(89):151-159. [ Links ]
Restrepo A, Páez VP, López C, Bock BC. Distribution and status of Podocnemis lewyana in the Magdalena River drainage of Colombia. Chelonian Conserv Biol. 2008;7(1): 45-51. [ Links ]
Rivas GA, Molina CR, Ugueto GN, Barros TR, Barrio-Amoros CL, Kok PJ. Reptiles of Venezuela: an updated and commented checklist. Zootaxa. 2012;3211:1-64. [ Links ]
Rogelj J, Meinshausen M, Knutti R. Global warming under old and new scenarios using IPCC climate sensitivity range estimates. Nature Clim Change. 2012;2:248-253. DOI:10.1038/nclimate1385. [ Links ]
Rueda-Almonacid JV, Carr JL, Mittermejer RA, Rodríguez-Maecha JV, Mast RB, Vogt RC, et al. Las Tortugas y los Cocodrilianos de los países andinos del trópico. Serie de guías tropicales de campo N° 6. Conservación Internacional. Editorial Panamericana. Bogotá, Colombia; 2007. p. 412-423. [ Links ]
Schall JJ, Pianka ER. Geographical trends in numbers of species. Science. 1978;201(4357):679-686. [ Links ]
Schwanz LE, Janzen FJ. Climate change and Temperature-Dependent Sex Determination: Can individual plasticity in nesting phenology prevent extreme sex ratios?. Physiol Biochem Zool. 2008;81(6):826-834. [ Links ]
Seneviratne S, Nicholls N, Easterling D, Goodess C, Kanae S, Kossin J, et al. Changes in climate extremes and their impacts on the natural physical environment: An overview of the IPCC SREX report. In: Intergovernmental Panel on Climate Change Special Report on Managing the Risks of Extreme Events and Disasters to Advance Climate Change Adaptation. Cambridge University Press, Cambridge, United Kingdom and New York, NY, USA; 2012. [ Links ]
Silber S, Geisler JH, Bolortsetseg M. Unexpected resilience of species with temperature-dependent sex determination at the Cretaceous-Palaeogene boundary. Biol Lett. 2011;7(2):295-298. [ Links ]
Sinervo B, Méndez-De-La-Cruz F, Miles DB, Heulin B, Bastiaans E, Villagrán-Santa Cruz M, et al. Erosion of lizard diversity by climate change and altered thermal niches. Science 2010;328(5980):894-899. [ Links ]
Soberon J, Peterson AT. Interpretation of models of fundamental ecological niches and species' distributional areas. Biodiv Informatics 2005;2:1-10. [ Links ]
Stephens PR, Wiens JJ. Bridging the gap between community ecology and historical biogeography: niche conservatism and community structure in emydid turtles. Mol Ecol. 2009;18(22):4664-4679. [ Links ]
Vargas-Ramírez M, Castaño-Mora OV, Fritz U. Molecular phylogeny and divergence times of the ancient South American and Malagasy river turtles (Testudines: Pleurodira: Podocnemididae). Org Divers Evol. 2008;8(5):388-398. [ Links ]
Vargas-Ramírez M, Chiari Y, Castaño-Mora OV, Menken SB. Low genetic variability in the endangered Colombian endemic freshwater turtle Podocnemis lewyana (Testudines, Podocnemididae). Contrib Zool. 2007;76(1):1-7. [ Links ]
Walker PA, Cocks KD. HABITAT: A procedure for modelling a disjoint environmental envelope for a plant or animal species. Global Ecol Biogeog Lett. 1991;1(4):108-18. [ Links ]
Warren DL, Glor RE, Turelli M. ENMTools: a toolbox for comparative studies of environmental niche models. Ecography. 2010;(33):607-611. [ Links ]
Weyant J, Azar C, Kainuma M, Kejun J, Nakicenovic N, Shukla P, et al. Report of 2.6 versus 2.9 Watts/m2 RCPP evaluation panel. Integrated Assessment Modeling Consortium. 2009. [ Links ]
Wright LI, Stokes KL, Fuller WJ, Godley BJ, Mcgowan A, Snape R, et al. Turtle mating patterns buffer against disruptive effects of climate change. Proc R Soc Lond B Biol Sci. 2012;279(1736):2122-2127. [ Links ]
Wyneken J, Godfrey MH, Bels V. Biology of Turtles. CRC press, Boca Raton, FL, USA; 2010, p. 279-300. [ Links ]