Introducción
El término amiloidosis hace referencia a un grupo de enfermedades caracterizadas por el depósito de proteínas en la matriz extracelular de distintos órganos. Existen varios tipos de amiloidosis: la amiloidosis por cadenas ligeras (AL), en la cual se depositan fragmentos o cadenas ligeras intactas de inmunoglobulina monoclonal, asociados a discrasias de células plasmáticas; la amiloidosis A (AA), en la cual se deposita el extremo N-terminal del reactante de fase aguda proteína amiloide A sérica y que se asocia a estados inflamatorios crónicos; y la amiloidosis asociada a transtirretina (ATTR), en la cual la transtirretina, (TTR, previamente conocida como prealbúmina), proteína sintetizada en el hígado y encargada de transportar la tiroxina y la proteína unida al retinol, presenta anomalías que llevan a alteraciones en el plegado de la proteína en hojas beta. Esta alteración hace que la proteína sea insoluble y no solo infiltre la matriz extracelular, sino que, además, active el receptor de productos finales de glicación avanzada (RAGE, por su sigla en inglés) lo cual genera citotoxicidad. Debido a los bajos niveles de catalasa y glutatión en el tejido cardíaco, este es particularmente sensible a la citotoxicidad inducida por la ATTR1.
Existen dos tipos de ATTR: una variante hereditaria (ATTRv) y una variante adquirida (ATTRwt). El desarrollo de tafamidis, una molécula capaz de estabilizar los tetrámeros de TTR, permitió, por primera vez, ofrecer a los pacientes con miocardiopatía asociada a ATTR (CM-ATTR) un tratamiento específico para su enfermedad. Recientemente, el uso de tafamidis ha logrado demostrar tener un impacto significativo en la morbilidad y la mortalidad asociada a ATTR, lo cual ha llevado a su aprobación por parte de los entes reguladores de varios países, incluido Colombia. No obstante, su alto costo mundial ha generado controversia sobre su costo-efectividad y sobre la importancia de la adecuada selección de los pacientes. En esta revisión sistemática, se evalúa el impacto de tafamidis en parámetros clínicos y paraclínicos, así como su costo-efectividad.
Métodos
Se realizó una búsqueda en Embase, PubMed y Cochrane usando los términos “tafamidis AND (cardiac OR heart OR myocardial) AND amyloid”, sin restricción de idioma. Las listas de referencias de los artículos seleccionados fueron revisadas manualmente para buscar estudios adicionales. Se incluyeron estudios clínicos relevantes al tratamiento con tafamidis en pacientes mayores de 18 años con CM-ATTR (tanto ATTRv como ATTRwt) en los que se haya evaluado el impacto (tanto clínico como paraclínico), el seguimiento imagenológico y la costo-efectividad del medicamento. Se excluyeron estudios sin grupo de control, artículos de revisión, reportes de casos, resúmenes de congreso, cartas al editor y artículos en los cuales no se evaluó el impacto del medicamento en CM-ATTR. Los resultados duplicados fueron eliminados utilizando un programa editor de referencias bibliográficas (Endnote v. 20.6). Todos los artículos fueron tamizados y la calidad de los estudios incluidos fue evaluada por tres investigadores de manera independiente (JCD, JMA, OB). En el caso de los estudios observacionales, esta se realizó utilizando la lista de chequeo propuesta por Downs et al.2. Para la presente revisión sistemática, un puntaje de 23-26 se consideró excelente, 20-22 puntos bueno, 17-19 puntos aceptable y menos de 17 puntos, deficiente. En el caso de estudios aleatorizados, la calidad fue evaluada mediante Risk of Bias Tool (ROB 2, Cochrane Collaboration). Las diferencias se resolvieron por consenso.
La presente revisión sistemática está acorde con la directriz PRISMA del 20203 y se realizó buscando resolver las siguientes preguntas:
– ¿Cuál es el impacto del tratamiento con tafamidis sobre la mortalidad total y la hospitalización por falla cardíaca en pacientes con CM-ATTR?
– ¿Cuál es el impacto de tafamidis en la calidad de vida y la capacidad funcional en pacientes con CM-ATTR?
– ¿Cuál es el impacto de tafamidis en la progresión del compromiso cardíaco?
– ¿Cuál es la costo-efectividad del tamizaje y el tratamiento con tafamidis en pacientes con CM-ATTR?
Resultados
La búsqueda se realizó el 16 de enero de 2024 y arrojó en total 1342 estudios: 979 en EMBASE, 293 en PubMed y 70 en Cochrane (Fig. 1). Se excluyeron inicialmente 330 registros duplicados, y durante la evaluación secuencial se excluyeron un total de 1326 estudios. Se incluyeron en total dieciséis artículos: cuatro artículos que evaluaron el impacto de tafamidis en desenlaces clínicos, dos artículos que evaluaron el impacto de tafamidis sobre medidas de calidad de vida y capacidad funcional, siete artículos que evaluaron el seguimiento de la respuesta al tafamidis y tres artículos que evaluaron la costo-efectividad del tamizaje y manejo con tafamidis.
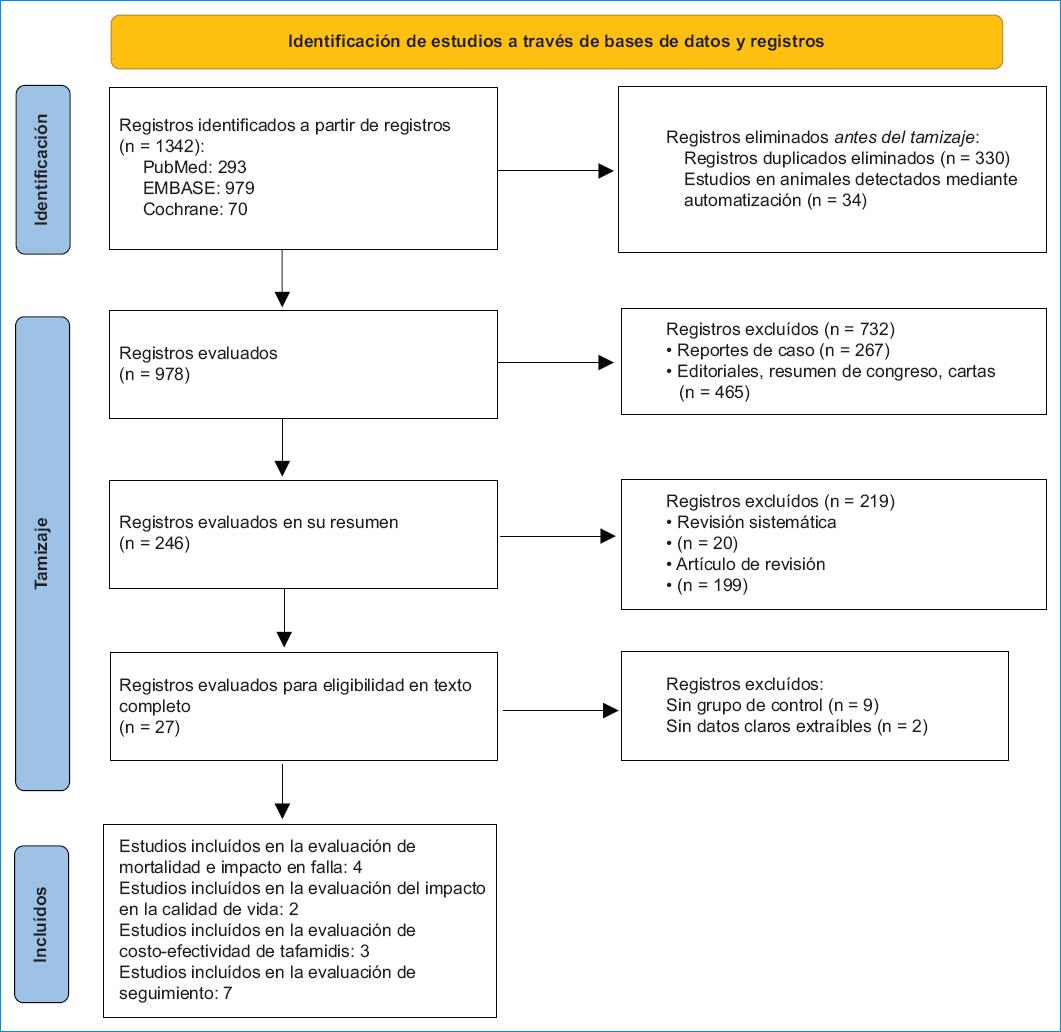
Figura 1 Flujograma para la evaluación y selección de los estudios clínicos incluidos en esta revisión sistemática.
1. ¿Cuál es el impacto del tratamiento con tafamidis sobre la mortalidad total y la hospitalización por falla cardíaca en pacientes con CM-ATTR?
En total, se incluyeron cuatro artículos que evaluaron el impacto de tafamidis sobre mortalidad y hospitalización: un estudio aleatorizado (ATTR-ACT, NCT01994889) y tres estudios observacionales (Tabla 1). Los estudios de Bezard et al. y Sultan et al.4,5 no fueron incluidos ya que no había suficiente información en el artículo escrito para responder la pregunta de investigación. El estudio ATTR-ACT se consideró de buena calidad, con bajo riesgo de sesgo de acuerdo con la herramienta ROB 2 (Fig. 2). El estudio de Ochi et al.6 se clasificó como de buena calidad, el de Takashio et al.7 de calidad aceptable y el de Ghoneem et al.8 de calidad deficiente debido a la presencia de confusores residuales (Tabla 2).
Tabla 1 Estudios que evalúan desenlaces clínicos (hospitalización por falla cardíaca y mortalidad) en pacientes tratados con tafamidis vs. grupo de control
| Autor, año | n | Tipo | Impacto en falla cardíaca (Tafamidis vs. control) | Impacto en mortalidad (Tafamidis vs. control) |
|---|---|---|---|---|
| Maurer et al., 20189 | 441 (Tafamidis, placebo 177) | RCT | Hospitalización por causas cardiovasculares: 0.48 vs. 0.7 por año, riesgo relativo | 44.9 vs. 62.7%; HR: 0.59; IC 95%: 0.44-0.79; p < 0.001 |
| Ochi et al., 20226 | 82 (Tafamidis: 38; control 44) | Retrospectivo | Hospitalización por falla cardíaca a 16 meses: 16 vs. 59%; p < 0.001 | Mortalidad por todas las causas: 8% vs. 34%; p = 0.003 |
| Ghoneem et al., 20238 | 1362 (Tafamidis: 553; control 809; PPP: 421 por grupo) | Base, PPP | Análisis PPP Eventos de falla cardíaca: 9 vs. 13.8%; OR: 0.62; IC 95%: 0.40-0.95; p = 0.030 | Análisis PPP Mortalidad por todas las causas: 10.7 vs. 16.4%; OR: 0.61; IC 95%: 0.40-0.91; p = 0.016 |
| Takashio et al., 20237 | 180 (Tafamidis 125; control 55; PPP: 33 por grupo) | Retrospectivo | Análisis PPP Hospitalización por falla cardíaca: 30 vs. 67%, HR: 0.48; IC 95%: 0.22-1.01; p = 0.054 | Análisis PPP Mortalidad por todas las causas: 18 vs. 67%; HR: 0.37; IC 95%: 0.15-0.92; p = 0.03 |
RCT: ensayo clínico aleatorizado (su sigla en inglés por randomized clinical trial); Base: datos obtenidos de bases de datos comercialmente disponibles; Retro: retrospectivo; PPP: pareado por puntaje de propensión; ND: no disponible.
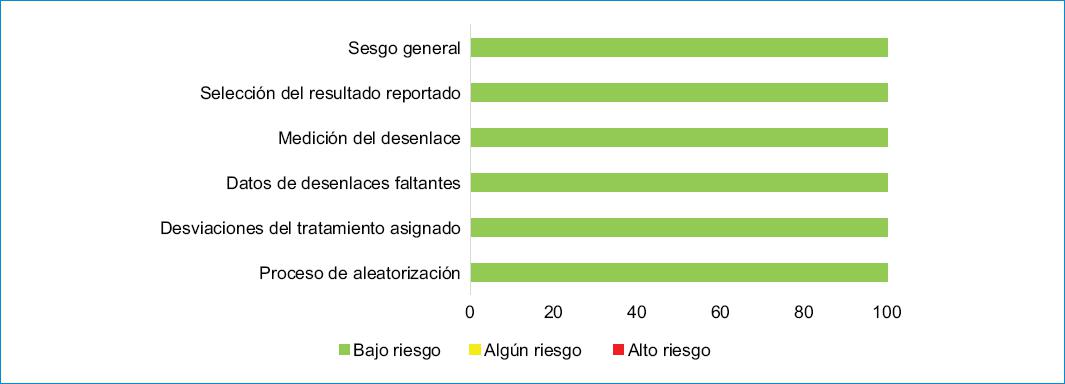
Figura 2 Evaluación del riesgo de sesgo (intención a tratar) del estudio de Maurer et al.9 usando la herramienta ROB2 (Cochrane collaboration).
Tabla 2 Evaluación de la calidad de los estudios observacionales que evalúan el impacto de tafamidis en mortalidad por todas las causas y hospitalización por falla cardíaca utilizando la lista de chequeo de propuesta por Downs et al.2
| Pregunta | Ochi et al.6 | Ghoneem et al.8 | Takashio et al.7 |
|---|---|---|---|
| ¿Está claramente descrita la hipótesis/objetivo del estudio? | No | Sí | No |
| ¿Está claramente descrito el desenlace primario en la introducción o en el método? | No | Sí | No |
| ¿Están claramente descritas las características de los pacientes incluidos en el estudio? | Sí | No | Sí |
| ¿Están claramente descritas las intervenciones de interés? | Sí | Sí | Sí |
| ¿Están claramente descritas las distribuciones de los principales confusores? | Sí | No | Sí |
| ¿Están claramente descritos los resultados principales del estudio? | Sí | Sí | Sí |
| ¿Provee el estudio estimados de variabilidad aleatoria para los resultados principales? | Sí | Sí | Sí |
| ¿Se reportaron todos los eventos adversos que pudieron haber sido consecuencia de la intervención? | Sí | Sí | Sí |
| ¿Se describieron las características de los pacientes perdidos durante el seguimiento? | Sí | Sí | Sí |
| ¿Se describieron los valores exactos de probabilidad para el desenlace principal? | Sí | Sí | Sí |
| ¿Son los pacientes tamizados representativos de la población a partir de la cual fueron reclutados? | Sí | Sí | Sí |
| ¿Son los pacientes incluidos representativos de la población a partir de la cual fueron reclutados? | Sí | Sí | Sí |
| ¿Son el personal tratante y las instalaciones representativas del tratamiento que la mayoría de los pacientes recibió? | Sí | Sí | Sí |
| ¿Se hizo un intento por cegar a los pacientes con relación a la intervención recibida? | No | No | No |
| ¿Se hizo un intento por cegar a los que evaluaron los resultados con relación a la intervención recibida? | No | No | No |
| ¿Si alguno de los resultados del estudio se basó en «dragado de datos», esto fue explicado claramente? | Sí | Sí | Sí |
| En los estudios de cohorte y aleatorizados, ¿los análisis se ajustan para las diferentes duraciones de seguimiento? Y en los estudios de casos y controles ¿el periodo entre la intervención y el desenlace es el mismo para los casos y los controles? | Sí | No | Sí |
| ¿Son apropiadas las pruebas estadísticas utilizadas? | Sí | Sí | Sí |
| ¿Es confiable la adherencia a las intervenciones? | Sí | No | Sí |
| ¿Fueron adecuados los desenlaces evaluados (válidos y confiables)? | Sí | Sí | Sí |
| ¿Fueron los pacientes de estudio en las diferentes intervenciones (en estudios clínicos y estudios de cohorte, o los casos y controles (en estudios de casos y controles) reclutados de la misma población? | Sí | Sí | No |
| ¿Fueron los pacientes de estudio en las diferentes intervenciones (en estudios clínicos y estudios de cohorte, o los casos y controles (en estudios de casos y controles) reclutados en el mismo periodo? | Sí | No | No |
| ¿Fueron aleatorizados los sujetos a los grupos de intervención? | No | No | No |
| ¿Fue ocultado el resultado de la aleatorización tanto a los pacientes como al personal tratante? | No | No | No |
| ¿Se hizo un ajuste adecuado de los confusores en el análisis del cual se extrajeron los resultados? | Sí | No | Sí |
| ¿Se tuvieron en cuenta las pérdidas de pacientes? | Sí | No | Sí |
El ATTR-ACT incluyó pacientes con CM-ATTR, tanto ATTRv como ATTRwt, que tuvieran evidencia de falla cardíaca, definida como al menos una hospitalización previa o documentación de sobrecarga de volumen o presiones intracardíacas elevadas e hipertrofia septal, definida como un grosor septal mayor a 12 mm por ecocardiografía9. Se excluyeron pacientes con compromiso grave de la capacidad física, definidos mediante una prueba de caminata de 6 minutos menor a 100 m, clase funcional NYHA IV, evidencia de mal estado constitucional, definido como el producto del índice de masa corporal contra la albúmina sérica menor a 600 o disfunción renal con depuración de creatinina menor al 25 ml/min/1.73 m2. Los pacientes fueron aleatorizados a tratamiento con tafamidis 80 mg, 20 mg o placebo en una relación 2:1:2. Durante el seguimiento a treinta meses, el uso de tafamidis se asoció a una reducción significativa en la mortalidad por todas las causas (29.5 vs. 42.9%, Hazard ratio [HR] 0.7, intervalo de confianza [IC] 95% 0.51-0.96; p < 0.001); la mayoría de estas muertes (73% en el grupo de tafamidis y 69% en el grupo de placebo) fueron por causas cardiovasculares10. No hubo diferencias entre los tipos de ATTR (reducción en el riesgo de muerte con tafamidis en pacientes con ATTRwt 29.4% (HR: 0.706; IC 95%: 0.474-1.052; p = 0.0875); reducción en el riesgo de muerte con tafamidis en pacientes con ATTRv 31.0% (HR: 0.690; IC 95%: 0.408-1.16; p = 0.1667); sin embargo, el tamaño de la muestra no fue suficiente para detectar diferencias entre tafamidis y placebo en la evaluación de estos subgrupos11.
En el programa de seguimiento extendido a 58.5 meses, el uso de tafamidis se asoció a una menor probabilidad de muerte (44.9 vs. 62.7%) (HR: 0.59; IC 95%: 0.44-0.79; p < 0.001)12, y al prolongar el seguimiento se observó también un beneficio en la mortalidad en pacientes con clase funcional NYHA III (HR: 0.64; IC 95%: 0.41-0.99; p = 0.046). La presencia de ATTRwt, una distancia de caminata de 6 minutos (6MWT, por su sigla en inglés) mayor a 351 metros, una fracción de eyección del ventrículo izquierdo (FEVI) mayor a 48.9%, un nitrógeno ureico menor a 26 mg/dl y un NT-proBNP menor a 3011 pg/ml fueron factores asociados a un mejor pronóstico; a mayor número de estos factores, mejor pronóstico de sobrevida13.
Adicionalmente, el uso de tafamidis tiene un impacto estadísticamente significativo (0.48 vs. 0.7 hospitalizaciones por año (RR: 0.68; IC 95%: 0.56-0.81)9 en pacientes con clase funcional NYHA I-II, sin encontrar impacto estadísticamente significativo en pacientes en clase funcional NYHA III14. Esto se traduce en una reducción significativa de 2.62 días de hospitalización por paciente por cada año de tratamiento, la cual aumenta a 3.96 días por paciente por cada año de tratamiento recibido en pacientes en clase funcional NYHA I-II15. En pacientes octogenarios, no hubo diferencia ni en las hospitalizaciones (60.8 vs. 56.8%, p = 0.572) ni en la mortalidad (62.7 vs. 83.8%, p = 0.1526) entre el grupo de tafamidis y el grupo de control, respectivamente16.
Ghoneem et al.8, en un estudio con pareado por puntaje de propensión que utilizó una base de datos comercial, reportaron una reducción en los eventos de falla cardíaca a doce meses, definidos como edema pulmonar o necesidad de terapia diurética intravenosa (9 vs. 13.8%; OR: 0.62; IC 95%; 0.40-0.95, p = 0.03) en los pacientes tratados con tafamidis, lo cual implica una reducción del 4.8% en el riesgo de este desenlace, sin que hubiese diferencia en la hospitalización por todas las causas (OR: 0.824; IC 95%: 0.613-1.108; p = 0.20). Adicionalmente, los pacientes tratados con tafamidis demostraron una reducción significativa de la mortalidad (10.7 vs. 16.4%; OR: 0.61; IC 95%: 0.40-0.91; p = 0.016)8. En el estudio de Ochi et al.6, en el cual se evaluaron 88 pacientes con CM-ATTR, el uso de tafamidis se asoció a una reducción significativa en la mortalidad por todas las causas (8 vs. 34%; p = 0.003) y la hospitalización por falla cardíaca (16 vs. 59%; p < 0.001). En el estudio de Takashio et al.7, en el cual se evaluaron de manera retrospectiva 180 pacientes con CM-ATTR, el uso de tafamidis se asoció a una reducción significativa en la mortalidad por todas las causas (18 vs. 67%; HR: 0.37; IC 95%: 0.15-0.92; p = 0.03) y la hospitalización por falla cardíaca (30 vs. 67%; HR: 0.48; IC 95%: 0.22-1.01; p = 0.054) en el análisis pareado por puntaje de propensión.
2. ¿Cuál es el impacto de tafamidis en la calidad de vida y la capacidad funcional en pacientes con CM-ATTR?
En el ATTR-ACT, los pacientes del grupo tafamidis mostraron una menor reducción en la prueba de caminata de 6 minutos (6MWD, por su sigla en inglés) que los pacientes del grupo placebo (diferencia en la reducción de la distancia caminada, 75.68 m, error estándar ± 9.24; p < 0.001) y en el deterioro de la calidad de vida de acuerdo con el KCCQ-OS (diferencia en la reducción 13.65, error estándar ± 2.13; p < 0.001) a los 30 meses9. Ambas diferencias fueron evidentes a partir de la evaluación de los seis meses y se observan tanto en pacientes con ATTRv, como en aquellos con ATTRwt11. En pacientes octogenarios, García-Pavia et al.16 reportaron una atenuación de la progresión en el grupo que usó tafamidis, con menor reducción en la 6MWD (regresión de mínimos cuadrados parciales: –71 vs. –155 metros; p = 0.0098), menor aumento en el NT-proBNP respecto al basal (incremento de 1.18 veces vs. 1.96 veces el basal; p = 0.0011) y menor progresión en los síntomas de falla de acuerdo con el cuestionario de miocardiopatía de Kansas (–13.2 vs. –26.8; p = 0.0251) en comparación con el grupo de placebo. Un subanálisis del ATTR-ACT no fue tenido en cuenta para la presente revisión, ya que los autores no describen la realización de pruebas de significancia estadística para la mayoría de los resultados presentados17. En un estudio observacional, Rettl et al.18 reportaron que los pacientes tratados con tafamidis en dosis de 61 mg, no mostraron cambios en la 6MWD (397 m vs. 406 m; p = 0.456) mientras que los aquellos que no recibieron tratamiento tuvieron un deterioro (404; vs. 350 m; p = 0.009), siendo significativa la diferencia entre ambos grupos (p = 0.005).
3. ¿Cuál es el impacto de tafamidis en la progresión del compromiso cardíaco?
Las guías actuales recomiendan la evaluación de la progresión de la enfermedad con base en tres dominios: clínico/funcional, biomarcadores e imagenología/electrocardiografía19. En total, siete estudios evaluaron la progresión del compromiso cardíaco más allá del dominio clínico/funcional (ya descrito).
Desde el punto de vista electrocardiográfico, Girvin et al.20 reportaron menor incidencia de fibrilación auricular en pacientes tratados con tafamidis vs. aquellos que no recibieron tratamiento (42 vs. 53%; p = 0.003) durante un periodo de seguimiento de 3.4 ± 2.4 años. En el ámbito imagenológico, Odouard et al.21 reportaron una reducción de 11 ± 7% en la captación cardíaca de Tc99m en pacientes que habían recibido tafamidis durante al menos un año. De manera similar, Papathanasiou et al.22 evaluaron la captación de Tc99m en 14 pacientes que habían recibido tafamidis por un promedio de 44 ± 14 meses, encontrando mejoría en la escala de Perugini en cinco de ellos. La presencia de regresión en imágenes con Tc99m se relacionó con mejoría en los parámetros de función ventricular derecha izquierda; sin embargo, no todos los pacientes tuvieron dicha regresión23. A través de resonancia magnética cardíaca, Chamling et al.24 demostraron que los pacientes tratados con tafamidis demuestran estabilización del compromiso cardíaco, mientras que en el grupo de control se observó un aumento en el volumen extracelular, el espesor de las paredes y el volumen ventricular izquierdo. Rettl et al.18, reportaron resultados similares, demostrando, además, que los pacientes que obtuvieron más beneficios fueron los que recibieron la dosis de 80 mg de tafamidis sin diferencias entre el grupo de tafamidis 20 mg y el grupo de control.
A nivel ecocardiográfico, algunos estudios también han confirmado que el uso de tafamidis se asocia a menor progresión de la enfermedad, sin demostrarse regresión. Giblin et al.25 demostraron menor deterioro en el strain longitudinal (0.3 vs. 1.1%; p = 0.02) sin diferencias en la FEVI, en el strain radial o circunferencial o en las velocidades del Doppler tisular a un año de seguimiento. Hallazgos similares fueron reportados por Rettl et al.26, con un menor deterioro en el strain longitudinal tanto del ventrículo izquierdo como del ventrículo derecho en el grupo manejado con tafamidis. Estos resultados concuerdan con los de un subanálisis del ATTR-ACT, en el que el uso de tafamidis se asoció a menor deterioro del strain longitudinal global (-1.02; IC 95%: -1.73 a -0.31; p = 0.005), el volumen ventricular izquierdo (diferencia de mínimos cuadrados parciales 7.02 ml, IC 95%: 2.55-11.49; p = 0.002) y en las mediciones del Doppler tisular27.
4. ¿Cuál es la costo-efectividad del tamizaje y tratamiento con tafamidis en pacientes con CM-ATTR?
En total, tres estudios evaluaron la costo-efectividad del tamizaje y posterior tratamiento con tafamidis en pacientes con CM-ATTR (Tabla 3). Con base en los costos y riesgos de la biopsia endomiocárdica como método diagnóstico, Ge et al.28 estudiaron si la evaluación de pacientes mayores de 65 años con hipertrofia septal mayor o igual a 12 mm mediante estudios imagenológicos no invasivos (ecocardiografía, resonancia, gammagrafía con Tc99m), en quienes previamente se ha descartado AL mediante electroforesis de fijación en orina y cadenas ligeras en sangre, sería costo-efectiva en comparación con una estrategia guiada por biopsia endomiocárdica. Para realizar el análisis, los autores asumieron una reducción en el costo anual del tratamiento de tafamidis de > 90%. Entre los estudios imagenológicos, el uso de gammagrafía con Tc99m como único método imagenológico sería la estrategia más costo-efectiva (relación de costo-efectividad incremental [ICER, por su sigla en inglés]: USD $100,000/años de vida ajustados por calidad [QALY, por su sigla en inglés]) por encima del uso inicial o secuencial de resonancia magnética cardíaca (ICER: USD $120,000/QALY y USD $130,000/QALY, respectivamente). Con el escenario de precios actuales, los autores estiman que el uso de gammagrafía exclusivamente como método diagnóstico tendría un ICER de USD $1,200,000/QALY.
Tabla 3 Estudios que evalúan la costo-efectividad del diagnóstico y tratamiento de la amiloidosis con tafamidis
| Autor, año | Parámetro evaluado | Resultado | Costo-efectividad |
|---|---|---|---|
| Kazi et al., 202030 | Costo-efectividad del tratamiento con tafamidis | ICER: USD 880 000/QALY | No |
| Ge et al., 202228 | Costo-efectividad de las diferentes estrategias diagnósticas | Asumiendo una reducción en el precio de tafamidis: ICER para gammagrafia Tc99m: $100,000/QALY ICER para resonancia inicial: $120,000/QALY ICER para gammagrafia Tc99m seguida por resonancia: $130,000/QALY ICER para biopsia endomiocárdica: $200,000/QALY Con el precio actual: ICER para gammagrafía Tc99m: $1,200,000/QALY |
Siempre y cuando el costo de tafamidis se reduzca en > 90% |
| Lau et al., 202441 | Costo-efectividad tamizaje universal vs. selectivo | ICER para tamizaje universal: USD 919 509/QALY | No |
ICER: relación de costo-efectividad incremental (su sigla en inglés por incremental cost-effectiveness ratio); USD: dólares americanos; QALY: años de vida ajustados por calidad (su sigla en inglés por quality-adjusted life years).
Lau et al.29 evaluaron la costo-efectividad de una estrategia universal de tamizaje, usando gammagrafía ósea con Tc99 pirofosfato y cadenas ligeras en suero o electroforesis de inmunofijación, en aquellos pacientes con falla cardíaca con FEVI preservada e hipertrofia ventricular, comparada con una estrategia en la cual se evaluó solamente a aquellos pacientes con falla cardíaca con FEVI preservada y sospecha clínica de amiloidosis (definida como hipertrofia ventricular izquierda asociada a manifestaciones clínicas sugestivas de amiloidosis como polineuropatía, síndrome de túnel carpiano o bloqueo auriculoventricular). Comparado con una estrategia selectiva, el tamizaje universal llevó a un aumento significativo en los costos, con ICER de USD $919 293 por QALY, dado principalmente por los elevados costos del tratamiento con tafamidis29. Para alcanzar la costo-efectividad de dicha estrategia de tamizaje, los autores calculan que el costo de tafamidis debe reducirse en un 84%.
En ese sentido, un análisis de costo-efectividad encontró que, con los precios actuales, el uso de tafamidis supera ampliamente los estándares de costo-efectividad en EE.UU., con un ICER de USD $880 00030. Los autores afirman que en 0% de las 10.000 simulaciones probabilísticas, el tratamiento de la ATTR con tafamidis fue costo-efectivo, y estiman que es necesaria una reducción del 92.6% en el precio del medicamento para que la estrategia de manejo de la amiloidosis sea costo-efectiva.
Discusión
Debido al reciente desarrollo de medicamentos para el tratamiento de la ATTR, se ha generado en el mundo un marcado interés, tanto por parte de la industria farmacéutica como por parte de la comunidad médica, en el diagnóstico y tratamiento de pacientes con ATTR. Hasta hace poco, este se basaba en el manejo sintomático de las manifestaciones clínicas, incluyendo el uso de medicamentos para falla cardíaca, antiarrítmicos, o ambos, mas no de la causa subyacente; con la introducción de tafamidis, se logró, por primera vez, modificar el curso de la enfermedad al disminuir el depósito tisular. Sin embargo, el alto costo de este medicamento limita de manera significativa su uso generalizado haciendo que el criterio clínico y el uso racional cobren particular importancia. A continuación, los principales resultados de esta revisión sistemática:
– En pacientes con CM-ATTR, el uso de tafamidis se asocia con una reducción significativa de la mortalidad por todas las causas.
– En pacientes con CM-ATTR, el uso de tafamidis se asocia con una reducción estadísticamente significativa en el riesgo de hospitalización.
– El uso de tafamidis disminuye la velocidad de progresión de la enfermedad de acuerdo con pruebas imagenológicas, sin lograr detenerla por completo o revertir el daño cardíaco previo.
– Dado el alto costo del medicamento, ni el tamizaje ni el tratamiento de la CM-ATTR con tafamidis son costo-efectivos.
El uso de tafamidis para el tratamiento de la CM-ATTR ha sido aprobado en el mundo con base en los resultados del ATTR-ACT, en el cual se encontró una reducción significativa de la mortalidad y la sobrevida libre de hospitalización por falla cardíaca en pacientes tratados con dicho medicamento. Adicionalmente, varios subanálisis del ATTR-ACT han demostrado mejoría en la calidad de vida y la capacidad funcional. No obstante, la evidencia que avala el uso de tafamidis es limitada, ya que, infortunadamente, los estudios observacionales tienen un claro sesgo de selección: debido al alto costo del medicamento, solo se inicia tratamiento a los pacientes más sanos, lo que podría explicar por qué algunos estudios observacionales han reportado un beneficio superior al observado en el estudio aleatorizado. En el caso de algunos subanálisis del ATTR-ACT, la ausencia de información crítica para la interpretación de los resultados también ha sido resaltada en varias cartas al editor31,32. Incluso, algunos de los estudios publicados muestran un claro sesgo con presencia de confusores residuales33 o reportan como positivos resultados que estadísticamente no lo son14,34, haciendo aún más difícil la lectura crítica de los resultados. Es por ello que la revisión de la literatura es fundamental para tomar una decisión adecuada al momento de seleccionar los pacientes indicados para recibir tratamiento con tafamidis.
En esta revisión sistemática, se evidencia que el uso de tafamidis se asocia con una reducción significativa en la mortalidad, con lo que se espera una ganancia de 1.29-3.29 QALYS30,35, un número atractivo en comparación con el alcanzado por otras terapias para falla cardíaca con FEVI preservada36-38. Esta reducción de la mortalidad se traduce en que el uso de tafamidis se asocia a un aumento de sobrevida de ≈44 meses en comparación con placebo12, el cual se observa después de 18 meses de tratamiento y únicamente en pacientes con clase funcional NYHA I-II durante el estudio inicial y no en pacientes en clase funcional NYHA III, en quienes solo se encontró beneficio durante el seguimiento extendido, lo que apoya el concepto de que el beneficio se observa únicamente en pacientes con condiciones basales adecuadas, en quienes se espera una sobrevida significativa11,12. Tampoco se observó beneficio alguno en pacientes por encima de los 80 años. Estos beneficios no solo se aprecian en el ATTR-ACT, sino en varios estudios observacionales, algunos de los cuales tienen claros sesgos, como se evidencia en la separación temprana de las curvas de supervivencia libre de los dos desenlaces: se separan antes de un mes para mortalidad y en menos de diez días para el desenlace de falla, lo cual indica la presencia de confusores residuales a pesar del análisis pareado8.
Además de la disminución en la mortalidad y en el riesgo de hospitalización, el uso de tafamidis parece asociarse a una reducción en la progresión de la enfermedad, demostrado como menor deterioro de la calidad de vida y capacidad física, al igual que disminución en la progresión en la evaluación imagenológica. Es importante resaltar que el uso de tafamidis disminuye (sin detener por completo) la progresión de la enfermedad, sin lograr reversión de la cardiopatía existente, resaltando que su uso en pacientes con enfermedad avanzada no tendrá impacto significativo. Estos beneficios se evidenciaron tanto en el ATTR-ACT, como en estudios observacionales. Al interpretar los resultados de dichos estudios, es importante tener en cuenta que son propensos a un sesgo de supervivencia, mediante el cual los pacientes más enfermos no recibieron imagen de control (ya sea por enfermedad avanzada que les impide realizar el examen, o por muerte)21. Además, en varios estudios observacionales hubo diferencias significativas entre el grupo tratado y el grupo de control, ya que los pacientes del grupo de control por lo general eran de mayor edad, con mayor compromiso cardíaco y extracardíaco, y menor clase funcional.
A pesar de estos beneficios, la presente revisión sistemática encontró que ni el tamizaje ni el tratamiento de la CM-ATTR con tafamidis fuesen costo-efectivos, debido al alto costo del medicamento. Estos costos han sido catalogados como insostenibles aún en países desarrollados, ya que se estimó que tratar a todos los pacientes elegibles con ATTR en los Estados Unidos con tafamidis (n = 120,000), aumentaría el gasto anual en salud por $32.3 billones, y se considera que se requiere de una reducción de más del 90% en el costo del medicamento para alcanzar la costo-efectividad30. Adicionalmente, aunque la disminución en el riesgo de hospitalización es estadísticamente significativa, el impacto de esta reducción en los costos de atención en salud es mínimo: al tratar un paciente por un año, se reduce en tan solo 2.6 días la duración de hospitalización asociada a falla15. El momento del inicio de la terapia también podría tener un impacto significativo en los costos del manejo con tafamidis: aunque frecuentemente se utiliza en pacientes con falla cardíaca establecida, la sobrevida de estos pacientes es de apenas 2.5-3.5 años39 en comparación del 82% a 5 años en pacientes sin falla cardíaca40. No obstante, al iniciar tafamidis de manera temprana, los costos para el sistema de salud aumentan y superan hasta en casi seis veces un estándar de «willingness to pay» fijado en 200 000 dólares por QALY29. Infortunadamente, los análisis de costo-efectividad son dependientes de los costos en atención en salud de cada país, y en Colombia no encontramos ningún estudio que evalúe la costo-efectividad del tratamiento con tafamidis. La evaluación juiciosa de la evidencia que avala el uso de tafamidis en los pacientes con amiloidosis es particularmente importante teniendo en cuenta el alto costo del medicamento, el cual puede llevar a sobrecostos exagerados en el gasto en salud.
Conclusión
El uso de tafamidis tiene un impacto significativo en la mortalidad asociada a CM-ATTR, y un impacto estadísticamente significativo, pero clínicamente irrelevante, en el riesgo de hospitalización por falla cardíaca de pacientes con clase funcional NYHA I-II menores de 80 años. Adicionalmente, el uso de tafamidis retrasa, mas no revierte, la progresión de las alteraciones estructurales cardíacas en pacientes con CM-ATTR. Los altos costos del medicamento hacen que las estrategias para la tamización y selección de los pacientes cobren particular importancia, ya que con los costos actuales ni el tamizaje ni el manejo son costo-efectivos. Se requieren estudios clínicos adicionales con adecuado diseño metodológico, incluyendo estudios de costo-efectividad en Colombia.














