Introducción
SGB se describe clásicamente como una polineuropatía desmielinizante, ascendente, simétrica y progresiva. Puede acompañarse de arreflexia y síntomas disautonómicos(1). Las presentaciones atípicas incluyen debilidad y síntomas sensitivos asimétricos, de predominio distal o proximal, dolor difuso o compromiso aislado de pares craneales previo al inicio de los síntomas, irritabilidad, meningismo y marcha inestable, entre otros(2). La debilidad asimétrica se describe en el 23% de los pacientes pediátricos con SGB(3). La alteración en pares craneales puede ocurrir en el 45 - 75% de los pacientes, la perturbación en el XII par craneal es poco frecuente(4). El objetivo de este trabajo es describir la presentación atípica de SGB en un paciente pediátrico dada por debilidad asimétrica, marcha atáxica y compromiso de XII par craneal. Se cuenta con el consentimiento informado del representante legal del paciente y aval del comité de ética institucional.
Descripción del caso
Paciente masculino de 15 años procedente de la costa pacífica colombiana, afrodescendiente, quien consulta por sus propios medios al servicio de urgencias de un hospital de III nivel de complejidad por cuadro clínico de aproximadamente tres meses de evolución de alteración progresiva de la marcha, con lateralización izquierda, debilidad distal de predominio en hemicuerpo izquierdo, disartria y disfagia. Inicialmente consultó a su centro primario, fue diagnosticado con síndrome vertiginoso y recibió tratamiento sintomático, sin mejoría, no se dispone de registros clínicos de dicha atención. En la revisión por sistemas se encontró que aproximadamente tres semanas previas al inicio de los síntomas neurológicos tuvo rinorrea, tos, disgeusia, anosmia y diarrea, no buscó atención médica.
Examen neurológico: alerta, orientado, euproséxico, marcha con apoyo y aumento de la base de sustentación, fuerza muscular (Escala de Daniels) miembro superior derecho 5/5, miembro superior izquierdo 4/5, miembro inferior derecho 4/5, miembro inferior izquierdo 3/5. En miembros superiores reflejos bicipitales presentes, tricipitales y estiloradiales ausentes, en miembros inferiores reflejos rotulianos y aquilianos ausentes. Disártrico, mímica facial simétrica, no alteración de la percepción olfatoria, isocórico normorreactivo bilateral, fondo de ojo normal, movimientos oculares conservados, sin alteración de la agudeza visual, Weber izquierdo negativo, Rinne izquierdo negativo, incapacidad para la lateralización izquierda y la elevación de la lengua, sin presencia de alteración sensitiva aparente, no signos irritativos meníngeos.
La tomografía de cráneo no reporta hallazgos patológicos. Punción lumbar con presión de apertura normal, estudio citoquímico: disociación albumino citológica, estudio de bandas oligoclonales en líquido cefalorraquídeo negativo.
La resonancia magnética de columna contrastada evidenció “engrosamiento e hipercaptación del medio de contraste en las raíces nerviosas, que conforman la cauda equina, comprometiendo desde T12 hasta la región sacra” Figura 1.
Neuroconducción en miembros inferiores: respuestas ausentes en neuroconducciones motoras de los nervios peroneo y tibial bilateral, respuestas ausentes en las neuroconducciones sensitivas del nervio sural bilateral. Respuestas tardías: reflejo H ausentes bilateral, onda F del nervio tibial bilateral ausentes, signos de inestabilidad de membrana al reposo y a la actividad voluntaria con reclutamiento disminuido, hallazgos consistentes con polineuropatía de tipo axonal en miembros inferiores de carácter grave, compromiso axonal parcial grave en fase aguda.
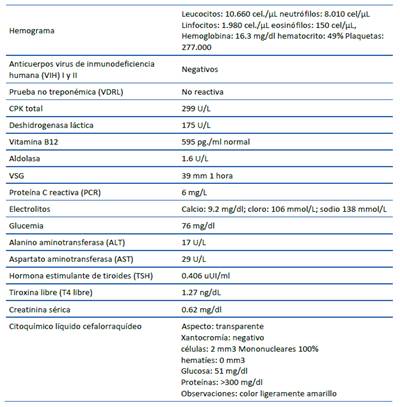
La Tabla 1 describe los análisis de química sanguínea. No se realizó medición de IgG o IgM para SARS-CoV-2.
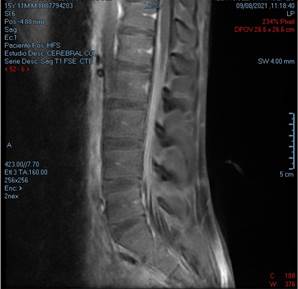
Figura 1 Columna toracolumbar en T1 que evidencia engrosamiento e hipercaptación del medio de contraste en las raíces nerviosas, que conforman la cauda equina, comprometiendo desde T12 hasta la región sacra.
Considerando la debilidad ascendente progresiva, de distribución asimétrica, la afección del nervio hipogloso, asociados a disociación albumino citológica, hipercaptación de contraste en raíces nerviosas de cauda equina en la resonancia y la alteración en estudio de neuroconducción se diagnosticó SGB con presentación atípica. Por tiempo de evolución y ausencia de compromiso respiratorio o síntomas disautonómicos, EGRIS (Erasmus GBS Respiratory Insufficiency Score) con baja probabilidad de necesidad de soporte ventilatorio fue iniciado plan de rehabilitación con adecuada respuesta clínica.
Discusión
Se describe un paciente pediátrico con SGB de presentación atípica dada por la asimetría en la progresión de la debilidad distal, marcha atáxica y afectación de XII par craneal.
La literatura reporta incidencia anual de 0.89 - 1.89 casos por cada 100.000 personas año, aumenta aproximadamente un 20% por cada década de vida y afecta predominantemente a los hombres (5). En Latinoamérica se estima que la incidencia es de 0.46 a 1.37 por 100.000 habitantes (6).
El SGB típicamente es precedido por infección o estimulación inmune que induce una respuesta inmunológica aberrante que afecta los nervios periféricos y las raíces nerviosas (7). Está descrito un incremento en la incidencia posterior a infecciones por Campilobacter jejuny, citomegalovirus, influenza A y B, VIH, Zika, Chikunguña, virus Epstein Barr, SARS-CoV- 2, entre otros (8-10. En el presente caso, el paciente reportó síntomas compatibles con infección por SARS-CoV-2, sin pruebas virológicas para confirmar COVID 19.
La presentación clásica de SGB incluye debilidad simétrica en miembros inferiores, ascendente y rápidamente progresiva. Incluye varios fenotipos: polineuropatía desmielinizante inflamatoria aguda (PDIA), neuropatía axonal motora aguda (NAMA), neuropatía axonal motora sensitiva aguda (NAMSA), síndrome de Miller Fisher, encefalitis de Bickerstaff, polineuritis craneal, debilidad faríngea cervical braquial, entre otras variantes (9). La progresión asimétrica de la debilidad es rara en adultos (10) y en niños. Yosha - Orpaz estudió una cohorte de 39 niños entre 2009 y 2015, encontró hallazgos atípicos al ingreso como debilidad asimétrica (23%), debilidad no ascendente (30%) y reflejos osteotendinosos profundos normales (28%). Entre aquellos pacientes con debilidad asimétrica, tres cumplían criterios de PDIA y uno con NAMA 3.
Se considera que la ataxia aguda o subaguda, signo de Romberg negativo, ausencia de oftalmoplejía y neuropatía desmielinizante aguda es una variante atáxica de SGB. La ataxia como debut de SGB pediátrico es muy rara y su incidencia es desconocida. Deliceo describe una paciente femenina de 7.5 años con SGB con alteración de la marcha y del equilibrio, reflejos tendinosos profundos conservados en miembros superiores y disminuidos en miembros inferiores, alteración del test dedo nariz bilateral, temblor en extremidades superiores, dismetría, marcha inestable con aumento de la base de sustentación y anticuerpos antiGM-2 positivos (11). El presente reporte de caso comparte características clínicas con dicha paciente, sin embargo, en el país no se realizan de rutina estudios de anticuerpos anti-gangliósidos.
El compromiso de los pares craneales ocurre en el 45 - 75% de los pacientes con SGB. La parálisis facial, usualmente bilateral, se puede encontrar en al menos el 50% de los casos (12). Hay variables del SGB poco frecuentes en con afección de pares craneales tales como el Síndrome de Miller Fisher caracterizado por oftalmoplejía (afección de III, IV y IV pares), ataxia y arreflexia (13) y la variante faringocervicobraquial en la cual hay la debilidad orofaríngea (daño de IX y XII pares), cervical y de extremidades superiores (14). El paciente descrito en este estudio presentó incapacidad para la lateralización izquierda y la elevación de la lengua, compatible con compromiso del XII par craneal de manera aislada, síntoma poco usual 4.
Los criterios diagnósticos del SGB propuestos por Asbury y Cornblath aún están vigentes (15), por su parte los criterios Brighton establecen niveles de certeza diagnóstica, Roodbol et al (16) en 2017 y Korinthenberg et al (17) en 2020 los validaron en población pediátrica y encontraron relación con el nivel de certeza y la probabilidad de padecer esta enfermedad y concluyeron que los criterios de Brighton son útiles para orientar el diagnóstico. La presentación atípica de SBG constituye un reto diagnóstico, en este caso la progresión asimétrica de la debilidad hizo necesarios estudios complementarios. La disociación albumino citológica, los hallazgos en resonancia magnética y los estudios de neuroconducción fueron decisivos para confirmar SGB.
La opción terapéutica tanto en formas típicas como atípicas depende del tiempo de evolución, compromiso respiratorio, presencia de síntomas disautonómicos, experiencia del grupo tratante y recursos disponibles 18. Dado el tiempo de inicio de los síntomas, el paciente descrito recibió rehabilitación, sin necesidad de uso de inmunoglobulina o plasmaféresis, con adecuada respuesta clínica.
Este trabajo presenta limitaciones por cuanto se trata de un reporte de caso y un estudio retrospectivo. Son necesarios estudios más amplios que permitan el conocimiento del curso clínico de las presentaciones atípicas del SGB en pediatría.
En conclusión, las presentaciones atípicas del SGB constituyen un reto diagnóstico, la debilidad asimétrica y el compromiso de XII par craneal obligan a descartar otras patologías. La historia clínica y el examen físico apoyados en estudios complementarios de líquido cefalorraquídeo, neuroimagen y neuroconducción son útiles para confirmar SGB. El conocimiento de las variables atípicas de SGB en la población pediátrica es indispensable para la identificación oportuna y tratamiento precoz.