Introducción
La epilepsia constituye una de las enfermedades neurológicas más frecuentes. Los pacientes con este diagnóstico presentan cambios en el estilo de vida, destacándose las limitaciones en las actividades durante el tiempo libre y restricciones para la actividad física. A través de los años, se ha evidenciado el efecto beneficioso de la actividad física en la función cognitiva 1-2, una reducción de la actividad epileptiforme en el electroencefalograma (EEG), un aumento del umbral de crisis y una disminución del estrés, considerado este último como uno de los principales factores desencadenantes de crisis epilépticas 3-5.
En los últimos años, se discute el rol específico de la actividad física para un mejor control de crisis epilépticas, para lo cual se han diseñado varios estudios en los cuales se evalúan diferentes tipos de actividades: las de baja intensidad, como relajación, yoga y ejercicio aeróbico con combinaciones de ejercicio cardiovascular y fuerza muscular 6-7; y las de intensidad moderada-alta, que incluyen la cinta o bicicleta ergométrica y danza en protocolos que, en su mayoría, llevan al paciente hasta el agotamiento 8-9. Los resultados han sido variables, sin embargo, la evidencia más reciente se inclina a favor de una reducción del número de crisis, así como una mejoría significativa en las escalas de calidad de vida, estado de ánimo y variables fisiológicas 10-12.
Por otra parte, se ha analizado la relación existente entre la actividad física y las descargas epileptifor-mes interictales (DEI), entendidas operacionalmente como los grafoelementos en el EEG que se observan fuera de las crisis epilépticas clínicas y sin constituir patrones ictales, pero que cumplen criterios de epileptogenicidad, definidos por Gloor y recientemente actualizados 13-14. En tanto que los estudios en animales mostraron una reducción significativa de las descargas, los resultados en humanos han sido variables 15-17.
En el presente estudio se propuso evaluar la eventual modulación de descargas epileptiformes interictales en pacientes con epilepsia de cualquier tipo, durante diferentes tipos de actividad física habitual (ejercicio aeróbico no extenuante y técnicas de relajación). Este análisis permitiría generar recomendaciones relacionadas al ejercicio físico.
Materiales y métodos
Es un estudio cuasiexperimental con medidas repetidas. Se compararon los resultados de la medición basal de DEI antes de la intervención (actividad física) con la medición durante la actividad física y luego en el período inmediatamente posterior a esta, donde cada paciente fue su propio control. Asimismo, se incluyeron dos tipos de actividad física que fueron presentados en forma de bloques secuenciales de 15 minutos de duración y en orden fijo: actividad física aeróbica (prueba de Ruffier Dickson) y ejercicios de relajación activa, que incluyeron la prueba de Jacob-son y un ejercicio de biofeedback (figura 1).

Fuente: elaboración propia.
Figura 1 Protocolo de actividad física bajo EEG, donde cada etapa tiene una duración de 15 minutos
Criterios de inclusión
Diagnóstico de epilepsia activa 18, edades entre 18 y 45 años, y capacidad de realizar las pruebas correctamente.
Criterios de exclusión
Presencia de comorbilidades cardiovasculares, historia previa demostrada de crisis epilépticas desencadenadas por ejercicio físico, discapacidad intelectual severa que impida el seguimiento del plan de ejercicios establecidos, discapacidad motriz severa que impida la realización de la intervención y embarazo en curso.
La inclusión de los casos se realizó mediante un muestreo por conveniencia durante el período de octubre 2020 hasta julio 2022, que incluyó a todos los pacientes coordinados para video-EEG en el programa de cirugía de epilepsia y a los pacientes valorados en la policlínica de epilepsia del Hospital de Clínicas, previa firma del consentimiento informado. El estudio fue aprobado por el Comité de Ética del Hospital de Clínicas.
Se realizó una entrevista clínica inicial por el equipo neurológico, con un cuestionario preestablecido que incluía variables clínicas, de la epilepsia y demográficas. El equipo de medicina del deporte valoró el nivel de actividad física previa de cada individuo mediante el cuestionario IPAQ (siglas en inglés para el cuestionario de aptitud de actividad física). En función de la respuesta de cada paciente a siete preguntas que exploraron el tiempo que han estado sentados, caminando, realizando actividad física moderada o intensa, durante los últimos siete días, estos son clasificados en inactivos, con actividad física de nivel moderado o de nivel alto 19. Este es un cuestionario ampliamente utilizado y validado en su versión en español. En esta instancia se realizó una valoración inicial y una explicación de las diferentes actividades incluidas en el protocolo de investigación.
La fase cuasiexperimental se realizó en la Unidad de Monitoreo de Video-EEG Prolongado, tanto para los pacientes en monitoreo para evaluación prequirúrgica como para los pacientes ambulatorios. Esto permitió contar con un mayor espacio físico y cables extensores que facilitaron el desplazamiento del paciente durante el protocolo de estudio, minimizando la pérdida de calidad del registro. Asimismo, la actividad física propuesta se adaptó no solo a las restricciones técnicas vinculadas a minimizar artefactos del registro EEG, sino a las condiciones de la sala de registro para minimizar el riesgo de caídas durante el mismo, en caso de presentar una crisis epiléptica.
Así, se sustituyó la opción de aplicar steps al trabajo en plano, con exigencias equivalentes y, en conjunto con el equipo de medicina del deporte, se diseñó con este fin una modificación del test de Ruffier-Dick-son, prueba utilizada para evaluar la capacidad de recuperación cardíaca y la condición física de forma segura, considerada especialmente en personas con alguna limitación física, la cual consiste en la realización de 30 sentadillas en 45 segundos, flexionando las rodillas a 90 grados mientras se mantiene la espalda recta y los brazos extendidos hacia adelante. Previo y posterior al ejercicio, el paciente se recupera en decúbito y durante toda la prueba se registra la frecuencia cardíaca y su variación, medida como intervalos entre latidos 20.
En esta adaptación, que denominamos Test de Ruffier-Dickson modificado, la fase posterior a las sentadillas fue de recuperación activa con una caminata de 2 minutos y 15 segundos; además, el moni-toreo de la frecuencia cardíaca se realizó a través del equipo de video-EEG, bajo la supervisión del personal de medicina del deporte. La secuencia de actividades físicas se detalla en la figura 1.
Intervención
Protocolo de EEG con actividad física y técnicas de relajación activa (figura 1): se realizó un registro de video-EEG, con 21 electrodos de superfície colocados de acuerdo con el sistema internacional 10-20. Se utilizó un equipo Nihon-Kohden de 32 canales, donde uno de los canales se destinó a registro de EKG simultáneo.
Etapa 1: registro EEG basal. Sentado con ojos abiertos durante 15 minutos.
Etapa 2: ejercicio aeróbico (EA). Registro EEG en actividad física aeróbica de 15 minutos de duración, que incluyó un período de entrada en calor (caminata de seis minutos) seguida de tres ciclos del test de Ruffier-Dickson modificado (sentadillas realizadas con el máximo esfuerzo durante 45 segundos y recuperación con caminata durante 2 minutos y 15 segundos), totalizando nueve minutos de actividad física 20.
Etapa 3: posejercicio aeróbico (PEA). Registro de EEG posejercicio, sentado con ojos abiertos durante 15 minutos.
Etapa 4: relajación activa (RA). Registro de EEG de 15 minutos durante las técnicas de relajación activa, guiadas por profesionales del equipo de psicología del deporte. Se incluyó: A) un proceso de relajación muscular progresiva (RMP con protocolo de Jacob-son) consistente en contraer y relajar en forma secuencial y guiada por audio, 16 grupos musculares, los cuales se distribuyeron en sentido cefalocaudal. Se aplicó durante 12 minutos 21-22; y B) protocolo de biofeedback con el software EmWave: duración de 3 minutos 23.
Etapa 5: posrelajación activa (PRA). Registro EEG posterior a toda la actividad, sentado con ojos abiertos, durante 15 minutos.
Medición de variables relacionadas al procedimiento
Los datos de cada paciente se cargaron en una base de datos digital anonimizada, incluyendo datos clínicos precodificados y el resultado del registro EEG.
A) Medición de parámetros de intensidad del ejercicio durante la etapa de EA
Medida de frecuencia cardíaca (FC) basal y al final de cada ciclo de ejercicio, con base en el registro EEG-EKG 21. Se realizó el cálculo de la FC máxima esperada según el American College of Sports Medicine (ACSM) (210-0,5 x edad). Se identificó la FC máxima registrada efectivamente durante el ejercicio, para luego realizar el cálculo del porcentaje de FC máxima esperada que se alcanzó, ajustada según la valoración de percepción del esfuerzo físico realizada por cada paciente, mediante la escala de Borg, al final de cada ciclo del circuito.
B) Medición de parámetros de eficiencia de biofeedback el rendimiento en esta prueba se evaluó mediante la coherencia cardíaca, que se obtuvo con el software EmWave.
C) Medición de la variable dependiente: descargas epileptiformes (DEI) en el EEG de superficie.
Se consideraron las DEI y los patrones ictales. En relación con el conteo de descargas, se incluyeron solo aquellas que cumplían con los criterios de Gloor en su operacionalización revisada 13-14, incluyendo espigas, puntas, polipuntas, complejos espiga-onda lenta, punta-onda lenta y polipunta-onda lenta. En caso de salvas o brotes de DEI, se contabilizaron cada una de las puntas o espigas, replicando la metodología publicada para la comparación de frecuencias de DEI entre períodos de exposición y ajustando por la variabilidad basal individual, se realizó la cuantificación del número de DEI en períodos ventana de tres minutos dentro de cada una de las diferentes etapas del estudio. La frecuencia basal de DEI se calculó como la media y su respectivo intervalo de confianza (IC) del 95 % para las cinco ventanas de tiempo consecutivas de tres minutos de duración durante las condiciones basales 24-25.
Evaluación del outcome primario
Se definió que la activación o inhibición significativa de las DEI en una determinada condición estaba presente cuando el número de DEI durante ese período de 15 minutos estaba por encima o por debajo del IC del 95 % individual para los DEI de referencia, respectivamente 24-25. Las crisis epilépticas y los patrones ictales subclínicos que surgieran durante la actividad física, también se consideraron como activación. Para cada paciente se exploraron las diferencias significativas de las DEI entre las condiciones mediante Anova y se analizaron las diferencias entre el período de reposo basal y cada condición, así como entre las condiciones consecutivas, mediante la prueba T de Student y el IC del 95 % de la diferencia. El análisis estadístico se realizó con el paquete estadístico para ciencias sociales (SPSS, versión 21.0).
Análisis en relación con parámetros cardiovasculares
Se estimó la variabilidad de la frecuencia cardíaca comparando la misma al final de cada período de actividad física aeróbica, con el reposo, definiéndose operacionalmente como significativo un aumento del 25 %. Se evaluó la existencia de asociación del parámetro de coherencia cardíaca (clasificado por el software EmWave en categorías ordinales: insuficiente, principiante, bueno y muy bueno), con la variación de la frecuencia cardíaca del ejercicio aeróbico predefinida operacionalmente como adecuada o insuficiente, mediante la prueba U de Mann-Whitney (α= 0,05).
Resultados
Se incluyeron a 20 pacientes, 9 de sexo femenino y 11 de sexo masculino, con una edad promedio de 30 + 7,7 años (18- 45 años).
En cuanto al tipo de epilepsia, 18 casos fueron epilepsias focales, 1 fue de tipo generalizada y 1 de tipo indeterminada. La duración promedio de la epilepsia fue de 15 ± 13 años (1-44 años) y la frecuencia mensual promedio de crisis fue de 20 por mes (1120 por mes), predominando las crisis focales con compromiso de conciencia (15 pacientes). 11 pacientes resultaron ser farmacorresistentes (55 %) y en cuanto al uso de fármacos anticrisis epilépticas, 2 estaban en monoterapia, 10 en biterapia y 8 consumían tres o más fármacos.
En cuanto a la valoración por el IPAQ (para medir el índice de actividad física habitual) se encontraron: seis pacientes sedentarios, seis con índices leves y ocho con índices moderados.
Del análisis de los registros de EEG, 13 pacientes presentaron DEI y, de estos, en ocho casos se encontró modulación de las descargas en forma significativa. Del análisis de estos se destaca que, comparados con el reposo (tabla 1), cinco pacientes mostraron modulación: tres tuvieron inhibición significativa durante el EA y uno de ellos durante el período PRA; además, tres pacientes mostraron una activación significativa, uno durante la RA y dos en la PRA.
En la comparación intraindividual entre condiciones consecutivas (EA-PEA / RA-PRA) se verificó la modulación en seis casos (tabla 2) y se observó que en cinco pacientes se activaron las DEI de forma significativa en PEA comparado con EA, en tanto que en dos pacientes se inhibieron las descargas durante la Para, comparado con la RA. De estos últimos, es de destacar que en el caso #7 se observó una modulación variable en las dos actividades (figura 2). Adicionalmente, un paciente (caso #9), bajo descenso de medicación que no realizó el ejercicio activo, presentó crisis durante el período PRA.
Tabla 1 Análisis de datos de DEI en cada condición (frecuencia promedio) comparados con el reposo en pacientes con modulación significativa (IC 95 % de la diferencia)
| # Caso | Descargas epileptiformes interictales (DEI) | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Basal | EA | IC 95% | P * | Post-EA | IC 95 % | P* | RA | IC 95 % | P* | Post RA | IC 95 % | P* | |
| Caso 2 | 39 | 15 | 13.5 a 34.5 | 0.003* | 29.5 | -1.7 a +20 | 0.085 | 27.8 | -1.4 a +23.8 | 0.076 | 27 | -1.4 a +26 | 0.073 |
| Caso 4 | 7.8 | 2.4 | -2.2 a +13 | 0.137 | 6.8 | -9 a +11 | 0.83 | 19.6 | -21 a -1.6 | 0.0.28 | 1.6 | -1.2 a +13.7 | 0.088 |
| Caso 7 | 19.2 | 11.2 | -1.6 a +17 | 0.093 | 22.6 | -12 a +5 | 0.334 | 25.4 | -16 a +3 | 0.168 | 15.9 | -5 a +12 | 0.433 |
| Caso 9 | 0 | 7.20 | -19 a +5 | 0.192 | 4.4 | -13 a +4 CRISIS | 0.242 | ||||||
| Caso 11 | 7.6 | 0 | 2 a 13 | 0.02* | 16.2 | -20 a +3 | 0.133 | 12,2 | -21 a +12 | 0.511 | 24.6 | -26 a -8 | 0.003* |
| Caso 13 | 18.6 | 7.4 | 2.1 a 20.3 | 0.023* | 11.8 | -4.8 a +18 | 0.202 | 11.5 | -5 a +29 | 0.32 | 6 | 2.8 a 22 | 0.021* |
Nota: DEI: número (#) de descargas epileptiformes; EA: ejercicio aeróbico; RA: relajación activa; PEA: posejercicio aeróbico.; PRA: posrelajación activa; (*P estadísticamente significativa ≤0,05); : activación de DEI;: inhibición de DEI.
Fuente: elaboración propia.
Tabla 2 Análisis de datos de DEI en las comparaciones de condiciones consecutivas en pacientes con modulación significativa
| Descargas epileptiformes interictales (DEI) | ||||||||
|---|---|---|---|---|---|---|---|---|
| # Caso | EA | Post-EA | IC 95% | P* | RA | Post-RA | IC 95 % | P* |
| Caso 2 | 15 | 29.4 | -22.6 a -6.15 | 0.008* | 26.8 | 27.8 | -12 a +14 | 0.87 |
| Caso 4 | 2.4 | 4.68 | -14 a +5 | 0.33 | 19.6 | 1.6 | 8.6 a 27.3 | 0.004* |
| Caso 5 | 1.4 | 5.67 a 9 | 0.018* | 4.2 | 6.8 | -7,0 a +1.8 | 0.208 | |
| Caso 7 | 11.2 | 22.6 | -18 a -4 | 0.007* | 25.4 | 15.8 | 4 a 17.8 | 0.027* |
| Caso 11 | 0.00 | 16.2 | -28 a -3 | 0.022* | 12.2 | 24.6 | -29 a +4.6 | 0.125 |
| Caso 19 | 3.4 | 7.2-7.5 a -0.05 | 0.048 | 4.6 | 7.2 | -9.4 a +4.2 | 0.37 | |
Nota: DEI: frecuencia promedio del número (#) de descargas epileptiformes; EA: ejercicio aeróbico; RA: relajación activa; PEA: posejercicio aeróbico.; PRA: posrelajación activa; (* p ≤0,05); activación de DEI; inhibición de DEI.
Fuente: elaboración propia.
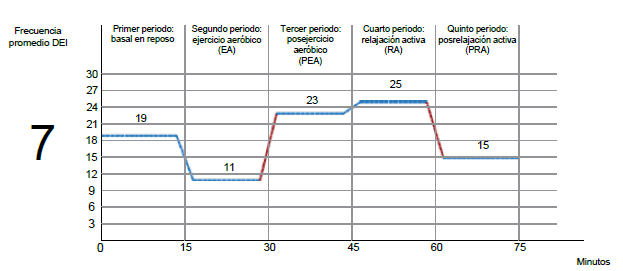
Fuente: elaboración propia.
Figura 2 Modulación de descargas epileptiformes interictales (DEI) en el caso # 7 en condiciones consecutivas
Con relación a la distribución de los factores clínicos en estos pacientes, si bien no hubo asociaciones significativas, se destaca que los tres casos con inhibición de descargas epileptiformes interictales durante el ejercicio (EA) no eran farmacorresistentes. Por otra parte, los dos casos con activación de su actividad epileptiforme interictal al final del protocolo, posrelajación activa (PRA), eran sedentarios.
En relación con los parámetros cardiovasculares, se analizaron las variaciones de frecuencia cardíaca en el EA con métodos no estandarizados (medición de FC con equipo de video-EEG). La FC máxima promedio fue de 122/min. El porcentaje de la FC máxima alcanzado promedialmente en el grupo de pacientes fue del 68 % (tabla 3) y la variación de la FC durante el ejercicio fue menor del 25 % en 7 de los 19 pacientes que realizaron la tarea de EA: 2 con epilepsia focal multilobar, 4 con epilepsia focal unilobar (2 frontales y 2 temporales) y 1 paciente con epilepsia generalizada idiopática. No se encontró una relación de la variación de la FC con las variables demográficas ni con las modulaciones de las DEI. En la RMP no se encontraron grandes variaciones de FC, siendo en la mayoría similar al estado de reposo.
Tabla 3 Registro de FC en las diferentes condiciones durante la actividad física aeróbica y las técnicas de relajación
| Paciente | FC promedio (latidos por minuto) | |||||
|---|---|---|---|---|---|---|
| FC reposo | FC máxima | FC MÁX (ACSM) | FC RMP1 | FC RMP2 | Biofeedback | |
| Caso 1 | 66 | 108 | 187 | 66 | 66 | 66 |
| Caso 2 | 102 | 150 | 169 | 96 | 84 | 92 |
| Caso3 | 60 | 145 | 190 | 66 | 66 | 70 |
| Caso 4 | 66 | 96 | 187 | 66 | 72 | 66 |
| Caso 5 | 66 | 108 | 187 | 84 | 89 | 89 |
| Caso 6 | 66 | 114 | 187 | 72 | 66 | 66 |
| Caso 7 | 84 | 126 | 178 | 90 | 96 | 84 |
| Caso 8 | 84 | 114 | 178 | 78 | 84 | 84 |
| Caso 9 | 102 | 70 | 66 | |||
| Caso 10 | 65 | 102 | 187 | 79 | ||
| Caso 11 | 102 | 138 | 169 | 84 | 84 | 81 |
| Caso 12 | 90 | 150 | 175 | 84 | 80 | 79 |
| Caso 13 | 96 | 132 | 172 | 78 | 75 | |
| Caso 14 | 84 | 114 | 178 | 84 | 84 | 81 |
| Caso 15 | 54 | 120 | 193 | 60 | 66 | 63 |
| Caso 16 | 72 | 184 | 78 | 62 | 79 | |
| Caso 17 | 96 | 114 | 172 | 78 | 78 | 74 |
| Caso 18 | 72 | 114 | 184 | 90 | 90 | 87 |
| Caso 19 | 72 | 162 | 184 | 90 | 80 | 81 |
| Caso 20 | 96 | 108 | 172 | 88 | 72 | 83 |
Nota: ACSM: American College of Sports Medicine; FC: frecuencia cardíaca; RMP: relajación muscular progresiva.
Fuente: elaboración propia.
En cuanto a la percepción del ejercicio con la escala de Borg, la media fue de 5 ± 1,7 (Mdn 5), lo cual permitió corroborar la realización de un ejercicio no extenuante. No se encontró tampoco una relación significativa entre el IPAQ y la percepción del ejercicio a través del Borg.
Del análisis de la relación entre el IPAQ y la variación de la frecuencia cardíaca durante el test de ejercicio de Ruffier-Dickson, se evidenció una relación directa: a mayor IPAQ, mayor variabilidad de la FC (tabla 4).
En cuanto a la coherencia cardíaca en los pacientes que realizaron el biofeedback (tabla 5), se destaca que la mayoría obtuvo un rendimiento en nivel principiante (55 %), donde un 30 % de los pacientes alcanzaron un nivel de bueno a muy bueno de coherencia cardíaca y solo un 15 % mostró un nivel insuficiente.
Además, se analizó la relación entre una variabilidad de FC menor al 25 % en el ejercicio, con la coherencia cardíaca en la técnica de biofeedback, la edad, el sexo y la politerapia. Los tres pacientes que tuvieron una insuficiente coherencia cardíaca también tuvieron una variabilidad menor al 25 % en el ejercicio (prueba U de Mann-Whitney, p = 0,010) (casos #7, #8 y #17, tablas 5 y 6), y no se encontró una relación significativa con la edad, el sexo y la politerapia. En cuanto a los pacientes con rendimiento de principiante en la técnica de biofeedback, los mismos no presentaron una relación significativa con la variabilidad de la FC en el ejercicio (tabla 6).
Tabla 4 Actividad física habitual según el IPAQ y la variabilidad estimada de la FC con el ejercicio
| Número de pacientes (#) | IPAQ | Variabilidad de FC |
|---|---|---|
| 5 | Sedentarios | 21,7 % ±13 % |
| 6 | Leve | 25,3 % ± 21 % |
| 8 | Moderado | 48,4 % ± 25,8 % |
Fuente: elaboración propia.
Tabla 5 Resultados de datos de coherencia cardíaca en técnicas de biofeedback
| Coherencia cardíaca | ||
|---|---|---|
| Paciente | Puntaje | Nivel |
| Caso 13 | 2,0 | Muy bueno |
| Caso 1 | 1,0 | Bueno |
| Caso 3 | 1,1 | Bueno |
| Caso 10 | 1,9 | Bueno |
| Caso 16 | 1,9 | Bueno |
| Caso 19 | 1,7 | Bueno |
| Caso 2 | 0,9 | Principiante |
| Caso 4 | 0,9 | Principiante |
| Caso 6 | 0.9 | Principiante |
| Caso 5 | 0,8 | Principiante |
| Caso 9 | 0,9 | Principiante |
| Caso 11 | 0,5 | Principiante |
| Caso 12 | 0,7 | Principiante |
| Caso 14 | 0.9 | Principiante |
| Caso 15 | 0,7 | Principiante |
| Caso 18 | 0,7 | Principiante |
| Caso 20 | 0,6 | Principiante |
| Caso 7 | 0,1 | Insuficiente |
| Caso 8 | 0,1 | Insuficiente |
| Caso 17 | 0,4 | Insuficiente |
Nota: 0,5-0,9 básico principiante; 1,0-1,9 bueno; 2,0-2,9 muy bueno y 3,0 excelente.
Fuente: elaboración propia.
Discusión
En este estudio se encontró una modulación de las DEI durante la realización de actividad física, destacando el hallazgo de una disminución en las DEI durante el EA no extenuante en aproximadamente el 20 % de los casos, y sin evidencia de su aumento durante la actividad física, es decir, en ningún caso se observó, lo cual es concordante con los resultados de estudios previos 15-17. Hay que mencionar que estos estudios se realizaron en una población heterogénea de pacientes con diferentes tipos y etiologías de epilepsia, por ejemplo, en niños con epilepsia refractaria 15, pacientes con epilepsia del lóbulo temporal 16 y epilepsia mioclónica juvenil 17.
Los mecanismos fisiológicos que relacionan la disminución de DEI durante la actividad física no han sido dilucidados, siendo una de las teorías postuladas el aumento de endorfinas y cambios en el pH sanguíneo 4.
Otro hallazgo fue el aumento de DEI en PEA comparado con EA, que se observó en cinco pacientes; esto también ha sido descrito en otro estudio 15, donde 4/26 pacientes presentaron un aumento en las DEI mayor al 30 % posterior a un EA. Los autores de dicho estudio plantearon hipótesis tales como: bajos niveles de valor de pH, aumento de catecolaminas, hipertermia e hiperventilación como inductores posibles de un aumento de las DEI.
Además de lo descrito en actividad física, se analizó la variación en las DEI durante técnicas de RA, que incluyeron una prueba de RMP y una técnica de biofeedback. De la revisión de la literatura, en un ensayo clínico controlado aleatorizado describieron una reducción de crisis epilépticas con técnicas de RMP durante 12 semanas 22. En cuanto al biofeedback validado con el software EmWave, no hubo reportes en la literatura en valoración de frecuencia de crisis o modulación de DEI.
En este estudio se encontraron resultados variables, con aumento (3/20 pacientes) o inhibición (3/20 pacientes) de DEI en PRA y en RA, comparados con reposo y actividades consecutivas.
En otro estudio 25 se describió la presencia de inhibición de DEI frente a ciertas tareas cognitivas en algunos pacientes con epilepsia mioclónica juvenil, postulándose un rol de la atención en este fenómeno inhibitorio, el cual podría compararse con los hallazgos del presente estudio, debido a que la RMP constituye una actividad de seguimiento de órdenes y concentración en la contracción-relajación de movimientos corporales en sentido cefalocaudal y el biofeedback es una actividad de concentración y atención en un paisaje. Por otra parte, el aumento en las DEI en esta condición en algunos pacientes podría equipararse a lo observado posrealización de tareas cognitivas en estudios previos 24-25.
Los datos de FC durante el test de EA y la realización de la escala de Borg (escala de percepción subjetiva de ejercicio) ayudaron a confirmar que los pacientes realizaron un ejercicio no extenuante. En ese sentido, la presente investigación no es comparable con otros trabajos, ya que en la mayoría de los estudios descritos 8 se buscó alcanzar el agotamiento, en tanto que en esta oportunidad se buscó priorizar la posible aplicación de los hallazgos a actividades que pudieran realizarse luego de forma ecológica. De todas formas, constatamos que el efecto sobre las descargas interictales de la actividad física no extenuante es similar al referido en la literatura para el ejercicio extenuante.
Se ha descrito una disminución en la variabilidad de la FC en personas con epilepsia, particularmente farmacorresistentes del lóbulo temporal y postulándose un rol en la muerte súbita inesperada en epilepsia o SUDEP (siglas en inglés para sudden unexpected death in epilepsy)23.
El estudio de variabilidad de FC se realiza usualmente a través de dispositivos de registro continuo durante actividad basal, pero en esta investigación se realizó una estimación basada en promedios de FC alcanzada en diferentes tipos de actividad física, sin contar con valores de referencia con esta metodología ni durante el ejercicio físico, para establecer comparaciones válidas. Al tener en cuenta estas limitaciones, se encontraron elementos sugestivos de una reducción en la variabilidad de la FC, a través de una estimación operacional, en 7 de 19 pacientes, sin relación significativa con el tipo o la topografía de origen de la epilepsia, ni con el IPAQ previo, y se presentó en un grupo heterogéneo de pacientes. Se destaca que los métodos no estandarizados utilizados para medir la FC y la coherencia cardíaca durante el ejercicio y el biofeedback pudieron limitar la validez de estos datos y su interpretación. La profundización del análisis de estas variables requerirá de estudios específicamente diseñados para este objetivo central, con mayor tamaño muestral y con un grupo control de individuos sin epilepsia, para fortalecer los hallazgos.
A través de la aplicación de técnicas de biofeedback, se obtuvieron datos de coherencia cardíaca y se encontró, como hallazgo significativo, que 3/20 pacientes que presentaban baja variabilidad de FC (cambio con el ejercicio menor a un 25 %), tenían menor rendimiento en el biofeedback, con puntajes menores a 0,5 en coherencia cardíaca. Estos datos abren la puerta para considerar la variación de la FC y la coherencia cardíaca como potenciales biomarcadores de riesgo de SUDEP 23.
Este estudio presenta limitaciones como son: un bajo número de pacientes, el sesgo de selección de la muestra por un lado, y también la heterogeneidad de ésta, lo que contribuye a limitar la generalización de los resultados. De todas formas, se trata de un primer estudio, con el objetivo de validar la metodología y se piensa que puede constituir el primer paso para estudios en cohortes de pacientes mayores y con diferentes subgrupos clínicos o demográficos. No se incluyó un grupo de control, que tendría sentido si el diseño comparara la respuesta diferencial en distintos tipos de epilepsia, pero que no era el objetivo del presente estudio.
Por otra parte, la comparación de la variabilidad de las DEI en diferentes pacientes sometidos o no a intervención de ejercicio físico presentaría la mayor dificultad sobre la extensa variabilidad interindividual en la frecuencia de DEI y en sus oscilaciones.
También se reconocen las limitaciones técnicas en la lectura del EEG durante el ejercicio aeróbico; donde para minimizar este factor, se realizó una prueba piloto para verificar la calidad del registro con diferentes patrones de ejercicio físico. En consecuencia, se modificó el test de Ruffier- Dickson para adaptarlo al registro EEG y disminuir así los artefactos que permitieran una mejor lectura. Los datos de la escala de Borg y la modificación de la FC muestran que el protocolo de ejercicio fue eficaz para alcanzar el efecto deseado. Finalmente, se asume que la realización de las diferentes actividades bajo un diseño secuencial y sucesivo puede haber influido en los resultados, particularmente en los últimos períodos del protocolo, sin embargo, esto permitió realizar la comparación entre períodos consecutivos, así como homogeneizó el período basal de referencia.
Si bien el mayor impacto de esta línea de investigación estaría en la potencialidad de incluir el ejercicio físico o ciertos tipos de actividad física en los protocolos terapéuticos en pacientes con epilepsia como medida complementaria para mejorar la frecuencia de crisis, esto requeriría de estudios con mayor número de pacientes y en exposiciones a protocolos más prolongados en el tiempo, idealmente ecológicos, con limitaciones reconocidas en el reclutamiento, la financiación y la adherencia. De los hallazgos significativos, se enfatiza que los pacientes que inhibieron las DEI durante el ejercicio aeróbico no tenían epilepsia farmacorresistente; por lo que se postula que, con las limitaciones metodológicas antedichas, este hallazgo puede sustentar un mayor rol de la actividad física como medida complementaria eficaz en el control de las crisis epilépticas en pacientes con epilepsia activa, pero no severa, que constituyen hasta el 70-80 % de las personas con epilepsia, en tanto que no sería una intervención suficiente para un cambio drástico en el subgrupo de pacientes con farmacorresistencia, naturalmente más complejos y con mayor epileptogenicidad.
Si bien el número de pacientes incluidos es muy bajo para emitir conclusiones, estos resultados no permiten identificar características clínicas que se asocien a una potencial respuesta inhibitoria del ejercicio en las descargas epilépticas o crisis, especialmente en pacientes con farmacorresistencia.
Conclusión
Diferentes tipos de actividad en pacientes con epilepsia pueden causar modulación de las descargas epileptiformes interictales. En este protocolo de ejercicio físico no extenuante hubo inhibición de las descargas epileptiformes, con rápido retorno al basal, en un 20 % de los casos. Las técnicas de RA raramente asociaron cambios y la relajación al finalizar el protocolo se asoció a modulación frecuente y variable.
En tanto que el presente estudio aporta un marco metodológico para el estudio de la respuesta electroencefalográfica a la actividad física en pacientes con epilepsia, se requieren estudios adicionales en poblaciones mayores o subpoblaciones específicas para definir el significado de estos hallazgos, así como su potencial influencia, contribuyendo al manejo no farmacológico en los pacientes con epilepsia.















