Introducción
El cartílago es un tejido conectivo especializado que se divide en tres tipos: fibroso, elástico y hialino. Este último es el más abundante en el cuerpo humano, situándose en las articulaciones móviles. Estructuralmente, tiene un alto contenido de matriz extracelular (MEC) compuesta por colágeno tipo II, proteoglicanos y ácido hialurónico. Una de las particularidades del cartílago hialino es la ausencia de irrigación e inervación, pero con la presencia de una alta lubricación producto de los sinoviocitos ubicados en la membrana sinovial1. Estas características permiten la amortiguación de cargas mecánicas (ej. comprensión y cizallamiento) y la disminución del coeficiente de fricción entre las superficies óseas, sin la presencia de dolor2.
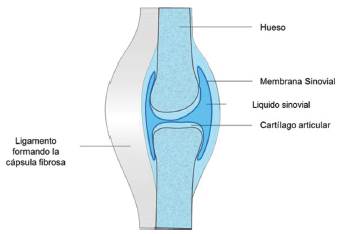
Fuente: Parte de las imágenes de los kits de herramientas de dibujo de Motifolio (Motifolio, Inc.) se usaron en la preparación de la figura3.
Figura 1: Esquema anatómico de un articulación
Cuando el cartílago sufre una lesión se genera una liberación de citocinas, principalmente de interleucina-1 (IL-1), que a su vez induce a la liberación de agrecanasas y metaloproteinasas que degradan la matriz extracelular. A partir de este momento, se perturba la homeostasis de la articulación, lo cual estimula la producción y secreción de componentes de MEC que no son característicos del cartílago hialino (ej. colágeno tipo I), lo que induce la formación de fibrocartílago4,5. Este proceso de reparación patológica genera un cambio estructural en el cartílago hialino que induce un aumento en el coeficiente de fricción entre las superficies óseas, lo cual es característico de una degeneración del cartílago articular. A este proceso patológico se le denominada artrosis u osteoartrosis (OA)6. Los signos más característicos de esta enfermedad son la presencia de dolor, crepitaciones y disminución del rango articular. Estas manifestaciones clínicas se asocian al hecho de que el tejido óseo que se encuentra debajo del cartílago (i.e. hueso subcondral) es altamente irrigado e inervado. Por otro lado, la OA afecta cualquier articulación, pero es más frecuente en los segmentos anatómicos de cadera y rodilla7, los cuales son utilizados en la mayoría de patrones de movimiento fundamentales involucrados en las actividades de la vida diaria8.
La OA es la enfermedad articular más común y su prevalencia e incidencia tienen una tendencia al aumento9. Esto se debe a que la esperanza de vida ha incrementado, así como el número de personas que sufren de sobrepeso y obesidad, pues la edad avanzada y la obesidad constituyen factores de riesgos asociados a esta enfermedad. En los países desarrollados se reportan prevalencias promedio de alrededor de 240 personas afectadas por cada 100.000 habitantes, lo que se calcula representa un costo económico que oscila entre el 0,25% y el 0,50% del producto interno bruto10. En Estados Unidos, por ejemplo, en el año 2014 se estimó que alrededor de 26 millones de personas padecían de algún tipo de artrosis11. Existen otros factores de riesgo asociados al desarrollo de la enfermedad como lo son el sexo femenino, las alteraciones posturales y los estilos de vida (i.e, ocupación laboral)12,13. Sin embargo, la OA también puede iniciarse posterior a un traumatismo directo en la articulación, como los ocurridos en ciertas caídas, accidentes de tránsito, heridas de guerra y lesiones deportivas. Estos mecanismos de lesión producen un ambiente inflamatorio en la articulación que altera su homeostasis y promueve la cicatrización del cartílago14.
Por lo descrito hasta el momento, urge la necesidad de entender el funcionamiento del cartílago ante las respuestas mecánicas, para entender sus límites y capacidades frente a las cargas durante la prescripción del ejercicio, en el contexto de una patología que hoy en día no tiene un gold estándar de tratamiento15.
Materiales y métodos
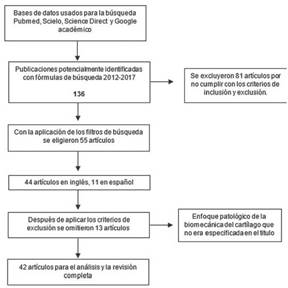
La recolección de la información, el análisis de esta y la construcción del artículo tomó un tiempo aproximado de seis meses. Se realizó una búsqueda en las bases de datos Pubmed, Scielo, Science Direct y Google académico de artículos publicados entre los años 2012 y 2017, con los términos: "Cartilage Biomechanic", "Cartilage Fisiology", y "Cartilage Histology". Se encontraron 136 artículos, de los cuales fueron seleccionados solamente 55 al aplicar los criterios de inclusión y exclusión, fueron 44 en inglés y 11 en español. Adicionalmente, se excluyeron 13 artículos al identificar que en el resumen se realizaba un análisis biomecánico en situaciones patológicas del cartílago articular. Por lo anterior, se usaron 42 artículos para el análisis y la revisión completa. Las referencias restantes hacen parte de capítulos de libros, los cuales contenían información relevante a cerca de la biomecánica del cartílago articular. Las referencias del 2011 y años atrás fueron utilizadas en la presente revisión para precisar conceptos básicos del cartílago en cuanto a su morfología, histología, funcionamiento básico y en aquellos casos en donde la literatura era escasa, como por ejemplo en los conceptos de anisotropía e histéresis del cartílago y condrocito.
Los criterios de inclusión fueron: artículos encontrados con los términos MeSH y DeCS, artículos realizados solamente en idioma español e inglés, artículos enfocados en el comportamiento y estructura del cartílago hialino. Como criterios de exclusión se tuvieron en cuenta: artículos que no se encontraban dentro del rango cronológico de búsqueda, a menos que incluyeran temas específicos que no se encontraban en las referencias dentro de dicho rango, artículos de revisión o estudios donde su enfoque era la descripción del cartílago o condrocito en situaciones patológicas.
La información recopilada fue organizada con el fin de proporcionar elementos claros para cada uno de los aspectos biomecánicos que se describen a continuación.
Desarrollo del tema
Cartílago articular
El cartílago articular está divido en cuatros zonas: superficial, transicional, radial y zona de cartílago calcificado (en donde el cartílago se relaciona directamente con el hueso), las cuales se caracterizan principalmente por una organización variada de redes colágeno (tipo II) y también por diferencias en las cantidades de agua y tipos de proteoglicanos15-17.
El cartílago posee un alto contenido de colágeno tipo II distribuido de manera dishomogénea. En la zona superficial se encuentra en fibras ubicadas aleatoriamente y entrelazadas en planos paralelos a la superficie, en la zona media las fibras de colágeno están más espaciadas en relación a su orientación aleatoria y dispersa, mientras que la zona profunda se agrupan de manera radial en forma de raíz anclando el cartílago al hueso adyacente18-20.
El colágeno que predomina en la matriz extracelular cartilaginosa es el colágeno tipo ll, que se divide en dos tipos: tipo 2A y 2B, siendo el primero sintetizado por células mesenquimatosas y células epiteliales de tejidos precartilaginosos, mientras el tipo 2B es sintetizado sólo por los condrocitos, por lo tanto durante la diferenciación en tejidos en procesos de condrogénesis, no se expresan los genes para el procolágenos 2A pero si los de tipo 2B21. Adicionalmente, debido a la estructura en forma de vara de las fibras de colágeno, mecánicamente las hace rígidas y fuertes en tensión, pero débiles y deformables en compresión22,23.
En lo que respecta a los proteoglicanos, se trata de moléculas compuestas de proteínas básicas unidas a uno o más glucosaminoglicanos (GAG), los cuales debido a su carga negativa en los brazos laterales, atraen cationes de sodio y por ende a las moléculas de agua, hidratando la matriz del cartílago hasta un 80%, por esta razón cuando actúan las fuerza de compresión, la presión interna del cartílago aumenta y dispersa el agua, acomodándose nuevamente por sus cargas negativas actuando como una almohada de colchón15,16.
Los proteoglicanos pueden ser de varios tipos y tamaños, encontrando desde moléculas pequeñas como biglicano y decorina que conforman apenas el 10 % de estas estructuras, hasta moléculas grandes como el agrecan que representa el 90% de los proteoglicanos y brinda una función de estabilización del cartílago articular, restringiendo así la salida de los componentes de proteoglicano del mismo24-26.
Concretamente, el agrecan está compuesto por alrededor de 100 moléculas de condroitín sulfato y 30 moléculas de keratán sulfato unidas a una proteína central de más de 3000 aminoácidos, que a su vez se une mediante proteínas de anclaje al ácido hialurónico (glicosaminoglicano producido en los condrocitos y sinoviocitos constituyente del eje central de varios proteoglicanos necesarios para la funcionalidad del cartílago)18 para formar agregados de proteoglicanos.
La función principal del agrecan es atrapar y mantener el agua hasta 500 veces su peso dándole la resistencia al cartílago articular19. Adicionalmente, el gran tamaño de los proteoglicanos permite su permanencia dentro de las fibras colágenas, y gracias a su carga negativa, atraen moléculas de agua creando una presión osmótica elevada lo cual garantiza la hidratación del cartílago16,20,21. Otro componente fundamental, y de hecho él más abundante, es el agua (con alto contenido de Na+, K+ y Ca+), que permite el movimiento de los gases, nutrientes y productos de desecho entre los condrocitos y el líquido sinovial26. Sin embargo, su contenido disminuye desde un 80 % en la zona superficial hasta el 65% en la zona profunda, diferente a la concentración de proteoglicanos la cual es baja en la zona superficial mientras que en la zona media es mayor27-31.
La interacción entre el colágeno, los proteoglicanos y el agua se da a través de la presión osmótica de Donnan, mediante la cual se regula la organización estructural de matriz extracelular y sus propiedades de tumefacción; además, el agua es capaz de desplazarse de manera libre cuando se aplican cargas al tejido cumpliendo con un rol controlador de la mecánica y lubricación articular26.
Lubricación del cartílago
La lubricación del cartílago está dada a partir de dos mecanismos: el primero por una lubricación de barrera, mediante la cual la lubricina, una glicoproteína, se absorbe como una monocapa macromolecular para cada superficie articular. Este tipo de lubricación es independiente de las propiedades físicas del lubricante, en este caso la viscosidad y también del material de la superficie de la carga que es rígido18,32.
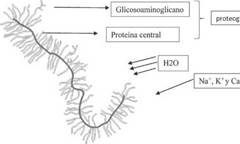
Fuente: Parte de las imágenes de los kits de herramientas de dibujo de Motifolio (Motifolio, Inc.) se usaron en la preparación de la figura3.
Figura 3: Proteoglicano
El segundo mecanismo es la lubricación película-fluido, la cual permite una mayor separación de las superficies articulares y soporta la carga por la misma presión que se produce en tal película, que a su vez puede ser de dos tipos: lubricación hidrodinámica, en donde las superficies de soporte de carga se deslizan entre sí formando una cuña de conversión del fluido generando la separación de las superficies; y una lubricación película-prensa, que se produce cuando las superficies articulares se mueven perpendicularmente entre sí33-35, generando una resistencia viscosa del fluido que actúa para impedir su escape del espacio, soportando altas cargas durante corta duración18,36,37.
Adicionalmente, se habla de una lubricación mixta, que no es más que la función conjunta que cumplen los dos mecanismos antes mencionados, de tal manera que en zonas de bajo contacto la lubricación se da a partir de la película-fluido, mientras que en zonas de mayor fricción la de barrera será el protector principal18.
El cartílago como modelo bifásico
El cartílago se ha considerado como modelo bifásico, teniendo en cuenta las fuerzas de arrastre producidas por el flujo del fluido intersticial a través de poros en la matriz extracelular que separan las superficies articulares, brindando carga hidrostática y facilitando la lubricación del cartílago con mínima fricción38.
Las características específicas del cartílago articular, basadas en su modelo bifásico, contemplan también una fase sólida proporcionada por la matriz extracelular que está compuesta por fibras colágenas que brindan resistencia a la tracción del tejido por su estructura organizada por: proteoglicanos, que son macromoléculas con propiedades hidrofílicas ubicadas de manera intercalada con las fibras de colágeno, generando una presión de hinchazón en el cartílago para cumplir la función de rigidez ante las cargas de compresión; y glicoproteínas no colágenas como la proteína oligomérica de matriz de cartílago (COMP, por sus siglas en inglés), que tiene función estructural en la osificación endocondral y estabilización de la matriz extracelular por su interacción con el colágeno, matrilinas y agrecano39-41.
Lopez et al., mencionan una tercera fase en el cartílago, relacionada con un modelo electroquímico en donde se incluye la influencia de la concentración de iones, permitiendo la representación del comportamiento de la inflamación del cartílago articular42, teniendo en cuenta también que la presencia de los grupos aniónicos carboxilo y sulfato en los glucosaminoglicanos le dan a la matriz una composición iónica y osmótica diferencial, pues la alta densidad de cargas negativas de los proteoglicanos atrae cationes de Na+, K+ y Ca2+ y repele aniones como el Cl y HCO243.
Adicionalmente, en procesos de carga articular se producen cambios físicoquímicos que modifican la composición iónica y osmótica de la matriz del cartílago, alterando a su vez la composición intracelular de los iones y su pH, con un aumento en la presión hidrostática y a su vez (efecto Donnan) en la concentración local de cationes y la osmolaridad del tejido mencionada anteriormente43.
Mecanotransducción
Uno de los papeles más importantes del cartílago es la capacidad de disipar fuerzas y disminuir los índices de fricción, por ende, es un tejido adaptado hacia la mecanotransducción, entendiéndose esta como la conversión de fuerzas físicas en respuestas bioquímicas, fundamentalmente para el mantenimiento y desarrollo fisiológico en el cuerpo humano, como por ejemplo la diferenciación, crecimiento, organización, liberación de factores de quimiotaxis, transmisión de información, entre otros44.
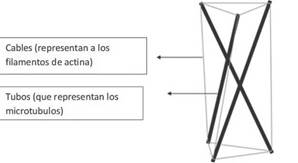
Dicha transmisión de fuerzas puede ser de célula a célula o de matriz a célula, debido a que tiene una base de tensegridad por las uniones focales compuestas por integrinas que conectan uniones citoesqueléticas con la matriz extracelular, reforzada con vinculina y talina que se conectan con los filamentos de actina que resisten a la fuerzas de tensión (representados con cables), mientras que los microtúbulos resisten a las fuerzas de compresión (representados con tubos)45.
Lo anterior genera una estabilidad arquitectónica a la estructura mediante la integración de fuerzas de tensión y de compresión que como resultado final suman 0 (cero), generando la integridad de fuerzas, de ahí el nombre de tensegridad. Los filamentos de actina, al mantenerse pre-tensados, pasan las fuerzas vibratorias que vienen de la matriz extracelular hasta el núcleo para generar cambios en el ADN para la producción de distintas proteínas dependiendo de las necesidades46.
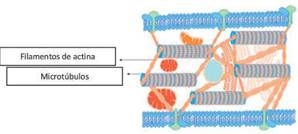
Figura 5: Esquema de tensegridad en un modelo celular Fuente: Parte de las imágenes de los kits de herramientas de dibujo de Motifolio (Motifolio, Inc.) se usaron en la preparación de la figura3.
El soporte y distribución de cargas realizada por el cartílago requiere del eficiente funcionamiento del condrocito, entendiéndose este como la célula mecano-sensible responsable de la mecanotransducción, a partir de la cual se llevarán a cabo la producción y mantenimiento de la matriz extracelular, colágeno tipo II y proteoglicanos; por lo tanto, funciona de manera biosintética dependiente de los estímulos mecánicos impuestos sobre él47.
También pueden inducir la liberación y activación de factores de crecimiento transformante como el beta (TGF- β)48, dichos estímulos mecánicos como los de compresión dinámica o estática generan respuestas bioquímicas reflejadas en la estimulación de la producción de matriz o la inhibición en la síntesis de proteoglicanos y proteínas respectivamente47.
El condrocito está rodeado de una matriz pericelular con propiedades estructurales compuestas de colágeno tipo IV y el proteoglicano perlecan, que modula la señalización de factores de crecimiento a través de sus cadenas de heparán sulfato, favoreciendo además la organización estructural y estabilización de esta matriz, cuya función principal es la regulación del microambiente biomecánico del condrocito, protegiéndolo durante estímulos de carga compresiva49.
La mecanotransducción del cartílago varía dependiendo de la capa por donde está pasando el estímulo mecánico. La zona superficial es la más próxima a la articulación, la más delgada y la más sensible a los estímulos mecánicos, debido a que maneja un estado pretensión mayor que en las otras zonas, implicando una durotaxis desde la zona superficial a la zona media y que, junto con la lubrina se horizontalizan las fuerzas de manera que compactan paralelamente a la superficie del cartílago, pasando la fuerza hacia todo el intersticio50.
En la capa media hay mayores distancias entre las fibras, y junto con el líquido intersticial, puede funcionar como un amplificador del estímulo mecánico para extenderlo a la capa más profunda, en donde las fibras se agrupan formando haces de longitud mayor, orientándose radialmente, pero con menos liquido intersticial: por ende, es importante de la amplificación del estímulo mecánico de la capa media para poder estimular la capa profunda18,51,52.
A nivel de la matriz extracelular, la mecanotransducción también libera factores que involucran cambios en el intersticio, como por ejemplo la proteína de matriz oligomérica (COMP), que hace parte de las trombospondinas de tipo 5 y tiene un papel muy importante en la determinación del fenotipo celular y la matriz que rodea53. Esta molécula tiene la capacidad de formar anclajes y organizar el colágeno tipo I y II, como sintetizar procolágeno tipo I y II para la formación de dicho colágeno adicionalmente se conoce que la COMP promueve la fibrogénesis de colágeno tipo I y II40.
Ahora bien, la mecánica del cartílago articular comprende sus propiedades viscoelásticas, que a su vez implican características como fluencia, relajación de la tensión e histéresis54, además de su falta de homogeneidad dependiente de la profundidad y la relación no lineal entre tensión-compresión47.
Anisotropía
La falta de homogeneidad del cartílago es determinada por la anisotropía, la cual se ve reflejada por la orientación y distribución de las diferentes fibras en sus zonas, recordando que, en la zona superficial, la orientación paralela de las fibras colágenas a la superficie articular brinda alta resistencia a la tensión en dicha dirección y baja resistencia en direcciones perpendiculares; mientras que en la zona profunda la orientación es principalmente perpendicular a la superficie articular, brindando resistencia ante compresión55-57.
La anisotropía a nivel celular se ve afectada por variables en el condroblasto, como por ejemplo el hecho de encontrarse dentro de su matriz y convertirse en condrocito, con lo cual se produce limitación en su desplazamiento. De esta manera, dependiendo de la matriz de su entorno puede desplazarse en distancias muy cortas según ésta lo permita, y se desplazará de acuerdo con la dirección de donde provenga la fuerza y en un gradiente de mayor a menor resistencia, lo que en este sentido se denomina como la durotaxis del condrocito58.
En cuanto al condroblasto se observa que al no tener una laguna de matriz que lo rodea, posee un mayor grado de desplazamiento. Por tanto, la tendencia del condroblasto o el condrocito en la dirección que se desplazan depende netamente de la fuerza aplicada y la respuesta que se origina, lo que se denomina plitotaxis del condroblasto o condrocito58.
Respuesta viscoelástica
Por otro lado, la respuesta viscoelástica se da a partir de la capacidad que tiene el cartílago de someterse a una carga constante dependiente del tiempo, respondiendo con una deformación inicial rápida que con el transcurso del tiempo pasa a ser lenta y progresiva, todo esto es posible gracias al flujo de fluido intersticial y la resistencia friccional asociada al mismo flujo; lo que significa que al principio de la aplicación de la fuerza el cartílago actúa más como un líquido, y posterior al equilibrio de las fuerzas interiores, se comporta más como un sólido59-61. Tal respuesta se ha justificado a partir de la teoría bifásica lineal, en donde la viscoelasticidad del cartílago implica parámetros como el módulo de equilibrio agregado, permeabilidad hidráulica y el radio de Poisson62.
El módulo de equilibrio agregado ha sido estudiado a partir de ensayos en donde se expone al cartílago bajo compresión confinada, hasta que la deformación llega a un equilibrio dado a partir de la carga desarrollada dentro de la matriz extracelular y la resistencia friccional generada por el fluido intersticial63.
El flujo de fluido intersticial está asociado directamente a la permeabilidad hidráulica del cartílago articular, la cual está determinada por la tasa de volumen del fluido con relación al volumen total del componente poroso, que depende de la interconexión de los poros y de la facilidad con la cual el fluido puede desplazarse a través del cartílago, siendo además inversamente proporcional a la resistencia friccional ejecutada por el fluido que se desplaza a través del mismo26.
Por otro lado, el radio de Poisson contempla la relación entre dos deformaciones a las que se somete el cartílago: al aplicar fuerzas compresivas uniaxiales, las dimensiones del cartílago disminuyen en dirección a dichas fuerzas y aumentan en dirección transversa; mientras que, al aplicar cargas tensiles, sus dimensiones disminuyen en dirección transversal y aumentan en dirección longitudinal64.
No obstante, es importante agregar un cuarto parámetro: el módulo elástico o de Young, entendiéndose como la fuerza de inercia que se opone un tejido para dejarse deformar, ya que, de acuerdo con este, la capacidad viscoelástica en el cartílago depende de la profundidad y de la cantidad de carga proporcionada al mismo65.
Acorde a lo anterior, en la zona superficial se puede encontrar un módulo de Young menor por las características viscosas de la zona, motivo por el cual el tejido soportará mayor deformación, mientras que en las zonas más profundas el cartílago se comporta como un material rígido, con un módulo de Young alto, representando fragilidad del cartílago y mayor riesgo al colapso65.
Fluencia
Se ha determinado que esta depende de la profundidad del tejido y del tiempo en el que se suministra la carga, de tal manera que en la zona superficial la amplitud de la fluencia es mayor, ya que el fluido intersticial del cartílago responde con cambios en su gradiente de presión, disipándose hasta el momento en que requiere de la regulación brindada por la matriz extracelular para disminuir la deformación31. De hecho, se ha evidenciado que las deformaciones rápidas sufridas por los condrocitos y la matriz extracelular son producidas en menos de un segundo, pero a medida que el tiempo transcurre, los cambios en volumen son insignificantes, permitiendo a estas estructuras la obtención de una homeostasis que garantice el soporte de cargas, que por lo general son cíclicas54.
Respuesta del cartílago ante las cargas
Ahora bien, el cartílago articular es sometido a cargas compresivas, de tensión y de cizalla, en las cuales responde de la siguiente manera:
El cartílago resiste cargas compresivas mediante tensión en su fase sólida y por la presión generada por la exudación del fluido, siendo esta última de inicio rápido, generando una deformación progresiva del cartílago que provoca el aumento inmediato en la presión del fluido, tendiendo a exprimir el líquido de la matriz extracelular, causando su deformación y también alteraciones en la presión hidrostática, composición iónica, osmótica y en el fluido intersticial, seguida de un cese de la misma exudación hasta un punto de equilibrio; igualmente se disminuye la distancia entre los proteoglicanos que tienen cargas negativas las cuales se repelen entre ellas, aumentando aún más la resistencia ante las cargas de compresión66.
El cese de la exudación es debido a la inhibición de la exudación del líquido producida por la matriz extracelular a raíz de su baja permeabilidad, además de la impermeabilidad del hueso subcondral circundante y del cartílago adyacente, que confinan al mismo cartílago en un marco de superficie de contacto que limita la deformación mecánica66.
En relación con la respuesta en tensión, cuando el cartílago es sometido a una carga constante, la deformación se produce de manera lineal en tres estadios: en el inicial la tensión causa realineación de las fibras colágenas en dirección de la carga aplicada; a continuación el mantenimiento de la carga produce como respuesta un aumento en la rigidez del cartílago, que seguirá acorde a la exposición ante tensión; llegando a la última etapa en donde el tejido finalmente colapsa26.
Por último, la respuesta del cartílago ante fuerzas de cizalla, a diferencia de las cargas mencionadas anteriormente, no produce ningún cambio en el gradiente de presión ni volumétrico del tejido, por tanto tampoco se llevará a cabo flujo de fluido intersticial26. De esta manera, ante dicho tipo de carga, la respuesta del cartílago será rígida, dependiente de la interacción entre el colágeno y proteoglicanos.
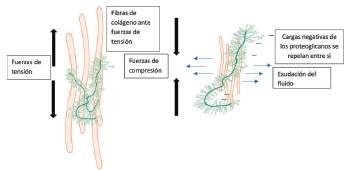
Fuente: Parte de las imágenes de los kits de herramientas de dibujo de Motifolio (Motifolio, Inc.) se usaron en la preparación de la figura3.
Figura 6: Respuesta de la matriz extracelular ante las fuerzas de compresión y tensión.
Histéresis
Un factor fundamental para tener en cuenta en el cartílago como material viscoelástico y avascular es el aumento de temperatura local, producto de la disipación de energía después de una carga cíclica, lo cual afecta el metabolismo celular incrementando la síntesis de proteoglicanos y la liberación de los mismos por los condrocitos, además del aumento en la síntesis de ácido hialurónico y glucosaminoglicanos, elementos constituyentes del líquido sinovial67.
De hecho, estudios han evidenciado que la temperatura local puede variar de 33 °C en reposo a 37 °C después de una hora de marcha, favoreciendo tales procesos metabólicos en cartílagos sanos, mientras que en procesos artrósicos la disipación de temperatura disminuye considerablemente, lo que se asocia con la perdida de proteoglicanos, proceso observado en dicha patología67. Tal disipación de energía comprende una característica común en los tejidos conectivos denominada histéresis, proceso mediante el cual se produce pérdida de energía debido a la fricción y a una alteración estructural que ocurre cuando en este caso el cartílago es sometido a determinada carga y a continuación es liberado de la misma68.
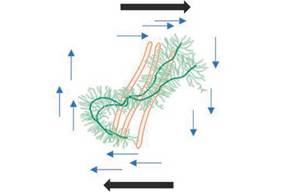
Fuente: Parte de las imágenes de los kits de herramientas de dibujo de Motifolio (Motifolio, Inc.) se usaron en la preparación de la figura3.
Figura 7: Respuesta de la matriz ante las fuerzas de cizalla, no hay cambios volumétricos y gradientes de presión.
Tal proceso se ve influenciado entonces por los aumentos en los niveles de carga. En estudios como el de Walter et al., en donde se ha utilizado la energía disipada como un método para caracterizar el daño de cartílago articular estudiado in vitro, se ha evidenciado que el aumento de los niveles de carga aumentan la energía disipada, justificando esta respuesta a partir del aumento en la presión del cartílago por aumento de los niveles de carga llevándolo hasta los límites de su lubricación69.
En otros estudios se ha demostrado que al exponer cartílago in vitro a 0,1 Hz la histéresis aumenta, mientras que a 40 HZ disminuye. Por lo tanto, el trabajo cíclico de alta velocidad disminuye la histéresis promoviendo un mayor retroceso elástico y mejoría en la aplicación de fuerza inversamente a la unidad de tiempo70.
Conclusiones
El cartílago articular es un tejido conectivo especializado y complejo que permite el soporte y transmisión de cargas gracias a los procesos de mecanotransducción inmersos en su funcionamiento. En este artículo de revisión fueron incluidos y abordados temas con escasa información en la literatura, como lo son la descripción de una estructura desde un modelo matemático como la tensegridad y por ende su función de transmisión de fuerzas por medio de la mecanotransducción; se analiza la anisotropía del cartílago, el cual produce diferentes respuestas dependiendo del estímulo mecánico y en la zona que se realizó dicho estímulo, debido a la no uniformidad en su estructura. Adicionalmente, otro componente de análisis en el artículo fue la fluencia, que varía dependiendo de la zona del cartílago a la cual se le aplica el estrés mecánico, y de la velocidad del estímulo mecánico, la cual produce un aumento de la secreción de componentes estructurales del intersticio del cartílago hialino.
La histéresis es otro concepto mecánico poco abordado en el cartílago; sin embargo, los estudios demuestran cómo el aumento de calor por la disipación de energía durante las cargas cíclicas modifica la síntesis de componentes de la matriz extracelular. No obstante, aún existen vacíos en el conocimiento para la descripción de cartílago y condrocito desde la tensegridad, histéresis y fluencia, además de los procesos químicos que se generan ante las fuerzas mecánicas. Por lo anterior, se debe profundizar en investigaciones de señalización celular a partir de las fuerzas aplicadas, y explicar, mediante comportamientos físicos, cómo se promueve la homeostasis del cartílago y sus alteraciones.