Introducción
La mucormicosis es una infección aguda causada por hongos del orden de los mucorales, rápidamente progresiva y de curso generalmente fatal, que se suele presentar en pacientes inmunodeprimidos con factores predisponentes como malignidad hematológica (linfoma de Hodgkin), uso de corticoesteroides sistémicos, insuficiencia renal o hepática, trasplante de órganos sólidos, VIH/ SIDA y enfermedad autoinmune, especialmente en diabéticos descompensados especialmente en estados de cetoacidosis1,2.
Es una patología de escasa ocurrencia y aunque en los últimos años se ha aumentado el número de casos reportados, es una enfermedad que poco se sospecha a nivel clínico, por lo tanto, su diagnóstico es usualmente tardío realizándose durante la autopsia3. En Colombia no se poseen datos epidemiológicos exactos dado que es una enfermedad que no requiere notificación obligatoria4, sin embargo, se estima una mortalidad global entre en un 20-60 %5,6, y a nivel del continente americano se estima una mortalidad de 40 y 80 % según Valdez et al7 teniendo en cuenta países como Brasil, Chile, los Estados Unidos , Honduras, México, Paraguay, Uruguay.
Su espectro clínico comprende seis formas de presentación: rinocerebral (MROC), pulmonar, cutánea, gastrointestinal (MGI), diseminada y miscelánea8. La principal vía de ingreso al organismo humano de este patógeno es la vía aérea, seguida por la vía directa relacionada con la contaminación de tejidos lesionados por traumatismos profundos que sobrepasan de manera extensa la barrera mucocutánea y, en tercer lugar, por la ingestión de alimentos colonizados9-11.
La mucormicosis pulmonar es la más prevalente, y alcanza una tasa de mortalidad de hasta el 76 % de casos la cual aumenta con la gravedad del estado de inmunosupresión12-14. La MROC las esporangiosporas inhaladas alcanzan los senos paranasales diseminándose luego a las órbitas, seno cavernoso y cavidad craneal15-17. El cuadro inicialmente semeja en un principio una sinusitis o una celulitis periorbitaria y se suele presentar en pacientes diabéticos en estados de cetoacidosis3,18. En cuanto a la mucormicosis cutánea es infrecuente, pero se suele presentar en pacientes con traumatismos severos de tejidos blandos, se cataloga como localizada cuando afecta piel o el tejido subcutáneo y extensión profunda cuando invade músculos, tendones o huesos y diseminada cuando compromete órganos no contiguos19. La MGI es la forma más difícil de diagnosticar debido a su ubicación anatómica y la inespecificidad de sus síntomas, curso generalmente fatal con una mortalidad de hasta el 85 %, casi siempre secundaria a perforación intestinal o a hemorragia del tracto gastrointestinal superior20,21. La diseminada es la forma menos frecuente del padecimiento y en la mayoría de los pacientes se inicia en pulmón y se disemina por vía hematógena; el diagnóstico clínico es inusual y por lo general se establece mediante la autopsia14. Aunque el cerebro es el sitio más común de diseminación, las lesiones también pueden alcanzar hígado, bazo, corazón y otros órganos5. Por último, la forma miscelánea hace referencia a las presentaciones menos comunes de mucormicosis incluyen endocarditis, osteomielitis, peritonitis y pielonefritis22.
El diagnóstico de mucormicosis constituye un gran reto para el médico, ya que rara vez se sospecha, y se realiza de manera ante mórtem solo en el 25-50 % de los casos23, dado que, sólo a partir de la sospecha clínica se realizan las pruebas específicas para la identificación del patógeno responsable de la enfermedad, de las cuales el examen microscópico directo, el cultivo y la histopatología continúan siendo las más utilizadas24. El tropismo vascular es el sello distintivo de la mucormicosis dado el hongo puede adherirse a las proteínas de la matriz subendotelial para luego ser fagocitadas lo que induce trombosis, infarto y necrosis de los tejidos circundantes25. Es la tercera micosis invasiva tras la candidiasis y la aspergilosis, donde su diagnóstico diferencial más común es aspergilosis por su similitud histológica, pues esta se comprende de hifas septadas dicotómicas hialinas que se ramifican en un ángulo de 45°, y también presenta la invasión vascular y la oclusión características de la mucormicosis26.
Dada la baja prevalencia de la enfermedad, se presenta el caso de un joven con antecedente de inmunosupresión con síntomas iniciales leves rápidamente progresivos hasta su fallecimiento sin un claro diagnóstico etiológico.
Caso clínico
Se trata de un varón de 39 años, con clínica de fiebre, tos, astenia y adinamia de 8 días de evolución quien consulta a primer nivel en zona rural de Santander, donde es atendido y remitido a tercer nivel por no control de la fiebre, aparente neumonía, que cuenta con antecedente de VIH sin adherencia farmacológica, y sin posibilidad de conteo de CD4 a tercer nivel, ni paraclínicos por lo que se remite a centro de tercer nivel. Entre otros antecedentes relevantes se encuentran quirúrgicos como toracotomía,biopsia pulmonar e historia con reporte de inflamación crónica granulomatosa con tinciones de ZN y PAS negativas para bacilos ácido alcohol resistentes y para hongos, sin embargo, para la fecha de esa hospitalización recibió 33 dosis de tratamiento empírico antituberculoso supervisado, luego de egreso hospitalario abandonó tratamiento. Al ingreso en tercer nivel se encuentra paciente caquéxico, con signos vitales dentro de rango de normalidad, consciente, orientado, quien a la auscultación se encuentra roncus en hemitórax izquierdo, sin signos meníngeos, ni otros hallazgos patológicos. Se realiza hemograma que reporta hemoglobina de 5,9 gr/dl; hematocrito 17 %, leucocitos 829 x mm3 con 82 % de neutrófilos, por lo que se diagnóstica neutropenia febril asociada a SIDA. Teniendo en cuenta la pobre adherencia farmacológica, se inicia tratamiento con lamivudina, abacavir, trimetoprim/ sulfametoxazol y azitromicina. Por el compromiso pancitopenico se le realiza biopsia de médula ósea que reporta celularidad inferior al 5 %, sin granulomas ni neoplasia. Por el abandono de manejo anti-TB se reinicia este teniendo en cuenta foco a nivel pulmonar. En hemograma de control se informa hemoglobina 4,5 gr/dl; hematocrito 14,5 %; leucocitos 1500 x mm3 con 81 % de neutrófilos, demostrando una progresión desfavorable y sin respuesta al tratamiento. Por el empeoramiento paraclínico y sistémico se adicionó empíricamente anfotericina B el día 11 de hospitalización, sin respuesta favorable, falleciendo dos días más tarde al día 13 de ingreso hospitalario. Por no tener claridad sobre causa de muerte, se solicita autopsia médico-científica.
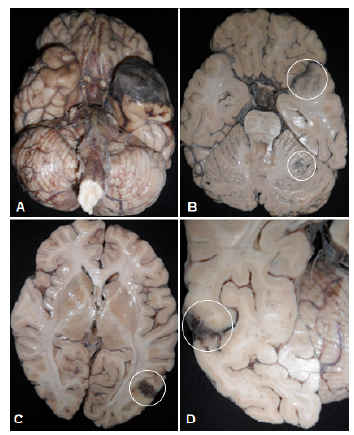
Los hallazgos de la autopsia fueron: edema cerebral severo, lóbulo temporal izquierdo de tonalidad negruzca, al corte se encuentra necrosis en lóbulo polo temporal izquierdo, en la periferia del lóbulo occipital izquierdo, en el límite parieto occipital derecho y en el centro del hemisferio cerebeloso izquierdo (ver Imagen 1). El estudio microscópico de estas lesiones muestra extensa necrosis del tejido nervioso asociado a trombosis de vasos arteriales, reconociéndose al interior de los trombos y en el tejido necrótico adyacente estructuras micóticas representadas por hifas grandes de pared gruesa y contorno irregular que se bifurcan en ángulo recto (ver Imagen 2).
Fuente: autores.
Imagen 1: A. Aspecto externo del polo temporal con necrosis y hemorragia B. Infarto hemorrágico en polo temporal y en hemisferio cerebeloso izquierdo. C. Infarto hemorrágico en lóbulo occipital. D. Infarto hemorrágico en el límite parieto occipital derecho.
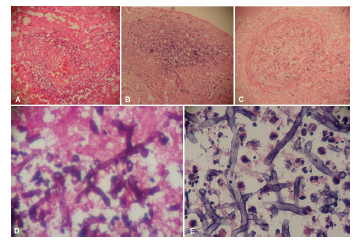
Fuente: autores.
Imagen 2: A-B-C Tejido nervioso con angioinvasión, trombosis y necrosis tisular. D-E. Aspecto microscópico de las hifas de mucor con hematoxilina/eosina y tinción P.A.S.
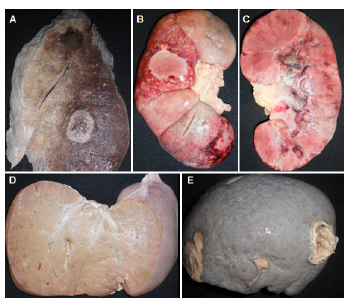
El pulmón derecho muestra su lóbulo inferior consolidado y al corte se observa aspecto congestivo con zonas de tonalidad pardo-rojiza en su lóbulo inferior. El pulmón izquierdo muestra al corte dos lesiones negruzcas de forma ovalada, la mayor de 3,5 cm de diámetro, al estudio microscópico del pulmón derecho se permite reconocer zonas de inflamación granulomatosa con células gigantes multinucleadas en relación con estructuras micóticas similares a las descritas en los cortes del tejido nervioso. En los cortes del pulmón izquierdo hay trombosis reciente de vasos venosos y arteriales en cuyo interior se identifican las estructuras micóticas grandes, de pared gruesa e irregular ya descritas cuya morfología se caracteriza mucho mejor con la tinción de PAS. Los riñones, el bazo y el hígado muestran amplias zonas de necrosis y el examen microscópico extensa necrosis tisular en medio de la cual se identifican las hifas ya mencionadas (ver Imagen 3).
Discusión
Se trata de un paciente con hallazgos patológicos que sumado a su sintomatología clínica resultan un caso compatible de mucormicosis diseminada, con inicio primario en pulmón, facilitado por su estado de inmunosupresión secundaria a antecedentes de VIH en estadio SIDA. Aguad et al comenta si bien la presentación de mucormicosis no es habitual, ya que ocurre generalmente en pacientes con muy bajo recuento de linfocitos T CD4, generalmente <100 cel/ mm3, junto con otros factores predisponentes como la neutropenia27, la cual también encontramos en nuestro caso.
Las características morfológicas que permiten el diagnóstico microscópico de la mucormicosis incluyen la identificación de hifas grandes no septadas, plegadas, de contorno irregular con tamaño variable entre 5-25 micras que se ramifican formando un ángulo de 90°22-24. En el caso presentado se estableció este hallazgo en más de dos órganos, categorizandolo como una forma diseminada, y fueron los síntomas respiratorios los primeros en presentarse muy probablemente al ser el pulmón el primero órgano en ser afectado como lo señala la literatura en este tipo de mucormicosis28, si bien en casos como los presentados por Salazar et al se describen síntomas agudos como fiebre, tos, expectoración variable y un rápido deterioro en nuestro medio se enfoca a descartar otras patologías más frecuentes que la mucormicosis. Sin embargo, en estos casos se debe mantener un alto índice de sospecha debido a su elevada mortalidad del 96 % aún con diagnóstico pre-mortem29.
Ante la sospecha de mucormicosis se recomienda el uso de imágenes diagnósticas (CT con contraste o resonancia magnética) para documentar el compromiso de la infección, y en caso de ser necesario desbridamiento quirúrgico urgente y junto a estudios histopatológicos y microbiológicos e iniciar concomitantemente el tratamiento médico de primera línea con anfotericina B liposomal30,31a dosis de 5-10 mg/kg/día, sin embargo, en caso de existir disfunción renal evitar uso con anfotericina e iniciar con medicamentos de segunda línea como lo son el isavuconazol intravenoso 3 dosis por 200 mg el primer y segundo día y luego reducir a 200 mg desde el día tres o Posaconazol intravenosos o en comprimidos de liberación prolongada 2 por 300 mg el primer día y posteriormente a 300 mg día32.
A pesar de los grandes avances y la profilaxis, el diagnóstico temprano es la principal dificultad en el abordaje de este tipo de infecciones33,34. Sin el tratamiento oportuno, la infección progresa rápidamente y causa invasión vascular e infartos con amplia necrosis35. La estrategia ideal para el manejo incluye terapia antifúngica específica, control de los factores desencadenantes y el tratamiento complementario necesario para evitar el desenlace fatal 32, 36,37.
Conclusiones
La mucormicosis se desarrolla en la mayoría de los casos como una enfermedad de curso agudo, angioinvasiva generando extensa necrosis no supurativa en personas inmunodeprimidas y en pacientes con factores predisponentes. La revisión de este caso constituye una invitación para la práctica clínica considerar la mucormicosis como posibilidad diagnóstica ante un paciente con patología infecciosa que no reacciona de manera favorable al tratamiento instalado y que cuenta con factores predisponentes mencionados. Al incluir a esta enfermedad dentro de un posible diagnóstico diferencial se le brindaría al paciente la oportunidad de modificar la rápida y agresiva evolución de la mucormicosis, disminuyendo el desenlace fatal gracias al manejo médico antifúngico y quirúrgico en caso de requerirse en las primeras instancias.