Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.20 no.3 Medellín July/Sept. 2007
Accidente bothrópico en Colombia: estudio multicéntrico de la eficacia seguridad de Antivipmyn-Tri®, un antiveneno polivalente producido en México
Bothrops bites in Colombia: a multicenter study on the efficacy and safety of Antivipmyn-tri®, a polyvalent antivenom produced in Mexico
RAFAEL OTERO-PATIÑO1, JUAN JOSÉ SILVA-HAAD2, MARÍA JACQUELINE BARONA ACEVEDO1,3 , MARÍA FABIOLA TORO CASTAÑO1, JUAN CARLOS QUINTANA CASTILLO1, ABEL DÍAZ CADAVID1, ISABEL CRISTINA VÁSQUEZ VÉLEZ1, VERÓNICA RODRÍGUEZ RIVERA1, CARLOS IVÁN DELGADO FIGUEROA2, MANUEL FERNÁNDEZ CEBALLOS2, SHIRLEY AYALA AUDIBER4, NECTTY LORENA CONRADO CHAVERRA4, CARLOS ARTURO MARÍN RESTREPO4, CORIOLANO EUGENIO RAMÍREZ GIRALDO5, ANA BERTA ARRIETA VIDES5, ELKIN AICARDO CÓRDOBA JULIO5, TANIA ISABEL ABEL RUIZ ZABALETA6, MARÍA VIALÓ GARCÍA CASTAÑEDA6, ADRIANA DEL SOCORRO AGUIRRE AGUDELO6, JOHN JAIRO LONDOÑO GUERRA7, NATALIA OSPINA BEDOYA7, DIANA MARÍA MACÍAS PRADA7, OSCAR FERNANDO JARARAMILLO DELGADO8, HERNÁN DARÍO PELÁEZ AGUDELO8, MARÍA EUGENIA ESPINAL SALDARRIAGA8, JUAN MANUEL CAMARGO BALLESTAS9
- Programa de Ofidismo / Escorpionismo, Facultad de Medicina y Corporación Académica para el Estudio de las Patologías Tropicales, Universidad de Antioquia, Medellín, Colombia.
- Hospital San Rafael, Leticia, Amazonas, Colombia.
- Escuela de Microbiología y Bioanálisis, Universidad de Antioquia, Medellín, Colombia.
- Hospital San Francisco de Asís, Quibdo, Chocó, Colombia.
- Hospital César Uribe Piedrahíta, Caucasia, Antioquia, Colombia.
- Hospital La Cruz, Puerto Berrío, Antioquia, Colombia.
- Hospital San Camilo de Lelis, Vegachí, Antioquia, Colombia.
- Hospital Antonio Roldán Betancur, Apartadó, Antioquia, Colombia.
- Hospital San Antonio, Tarazá, Antioquia, Colombia.
Responsable de la correspondencia: R Rafael afael Otero, Programa de Ofidismo / Escorpionismo, Facultad de Medicina, Universidad de Antioquia, AA 1226, Medellín, Colombia. Telefax: (574) 2631914.
Direcciones electrónicas: rafaotero@une.net.co
Recibido: abril 30 de 2007
Aceptado: junio 04 de 2007
RESUMEN
Introducción: Colombia es un país con dos productores de antivenenos de IgG, pero hay un mercado insatisfecho por diferentes razones técnicas.
Objetivos: evaluar la eficacia y la seguridad de un antiveneno F(ab´)2 polivalente (Antivipmyn-Tri®) producido en México, y un nuevo esquema de dosis en accidente bothrópico en Colombia.
Métodos: se realizaron durante 9 meses un ensayo clínico-terapéutico y cuantificaciones de veneno y antiveneno sérico (ELISA) en 53 pacientes.
Resultados: cuarenta y cuatro pacientes fueron mordidos por Bothrops asper en Antioquia y Chocó y 9 por B. atrox en Amazonas; todos tenían sangre incoagulable al ingreso, 30 (56,6%) con sangrado local y 24 (45,3%) con sangrado sistémico. El grado final de envenenamiento fue leve en 13 (24,5%), moderado en 30 (56,6%) y grave en 10 pacientes (18,9%). A las dosis recomendadas de 5 frascos para los casos leves o moderados y 10 para los graves, Antivipmyn-Tri® fue 100% eficaz para disminuir significativamente las concentraciones séricas de veneno en la primera hora de tratamiento y para detener el sangrado en las primeras 6-12 horas, 96,2% eficaz para normalizar la coagulación en 24 horas y 100% en 48 horas. Hubo 2 casos (3,8%) de recurrencia de coagulopatía sin sangrado y 12 recurrencias de antigenemia sin implicaciones clínicas. Diez pacientes (18,9%) presentaron reacciones tempranas adversas (leves) a la faboterapia. No hubo muertes, y cuatro pacientes (7,5%) tuvieron secuelas.
Conclusión: a las dosis utilizadas en este estudio, Antivipmyn-Tri® fue eficaz y seguro para el tratamiento del envenenamiento bothrópico en Colombia.
PALABRAS CLAVE
BOTHROPS ASPER
BOTHROPS ATROX
COLOMBIA
ENVENENAMIENTO BOTHRÓPICO
FABOTERAPIA
SUMMARY
Introduction: Colombia is a country with two whole IgG antivenom producers, but the expectancy of all the market are not fulfilled by different technical reasons.
Objectives: To evaluate the efficacy and safety of a F(ab´)2 polyvalent antivenom produced in Mexico and of a new dosage regimen for Bothrops bites in Colombia.
Methods: A clinical trial, including serum venom and antivenom measurements (ELISA), was performed during 9 months in 53 patients.
Results: forty four patients were bitten by Bothrops asper in Antioquia and Chocó and 9 by B. atrox in Amazonas; on admission, all of them had nonclottable blood, 30 (56.6%) presented local and 24 (45.3%) systemic bleeding. The final envenoming grade was mild in 13 (24.5%), moderate in 30 (56.6%) and severe in 10 patients (18.9%). At the antivenom doses used in this study (5 vials for mild / moderate and 10 for severe envenoming), Antivipmyn Tri ® was 100% efficient to decrease significantly serum venom concentrations within the first treatment hour, and to stop local and systemic bleeding within 6-12 hours, 96.2% efficient to restore blood coagulation within 24 hours and 100% within 48 hours. Two patients (3.8%) had recurrence of coagulopathy without bleeding, and there were 12 recurrences of antigenaemia without clinical relevance. Ten (18.9%) patients suffered early mild adverse reactions to fabotherapy. There were no deaths and four patients (7.5%) presented sequelae.
Conclusion: at the doses used in this study, Antivipmyn Tri® was efficient and safe for the treatment of Bothrops bites in Colombia.
KEY WORDS
BOTHROPS ATROX
BOTHROPIC ENVENOMING
BOTHROPS ASPER
COLOMBIA
FABOTHERAPY
INTRODUCCIÓN
El accidente ofídico es un serio problema de salud pública en un país tropical como Colombia. A pesar del subregistro que resulta de los pacientes tratados por la medicina tradicional, en la década de 1990 a 1999 se informaron en promedio cada año 2.675 mordeduras por serpientes (Registro SIS-12, Ministerio de Salud de Colombia, 1990-1998). El 90-95% son producidas por serpientes de los géneros Bothrops, Porthidium, Bothriopsis, Bothriechis y Bothrocophias, principalmente en Antioquia, Chocó y Amazonas, donde se registran anualmente cerca de 800 casos (120 de ellos en Amazonas), con una mortalidad del 3-8,9% y secuelas en el 6-9,9%, según estudios recientes.1-4 Bothrops asper, especie ampliamente distribuida hasta 1.200 msnm, es responsable del 50-70% de estos accidentes en Antioquia y Chocó; B. atrox es a su vez la especie causante del 95% de las mordeduras en el territorio amazónico.5 Sus venenos inducen intensos efectos locales (edema, hemorragia, formación de bulas, dermonecrosis y mionecrosis) y graves efectos sistémicos que ponen en peligro la vida (desfibrinación, trombocitopenia, hemorragias en otros órganos, nefrotoxicidad).1,4,6-9
Transcurridos más de 100 años desde el descubrimiento de la seroterapia antivenenosa, los antivenenos no han podido resolver todos los problemas originados por los venenos de víboras, especialmente los efectos locales que son de rápida instalación (4-15 minutos) y que causan secuelas por necrosis, con pérdida de masa muscular, desfiguraciones y amputaciones, así como tampoco las reacciones adversas inducidas por aquellos.10-14 Los antivenenos de tercera [F(ab´)2] y cuarta (Fab) generaciones (faboterápicos), con partículas de menor tamaño y mayor volumen de distribución en los tejidos, producen neutralización parcial de estos efectos, de la misma manera que los de IgG total, mejor cuando todos se administran muy pronto por vía intravenosa (IV).15-19
En Colombia hay dos productores de antivenenos de IgG, pero hay un mercado insatisfecho por diferentes razones técnicas.3,9,19,20 El Instituto Bioclón de México produce un antiveneno polivalente antibothrópico, anticrotálico y antilachésico (Antivipmyn-Tri®) digerido con pepsina (Fab2), a partir del plasma hiperinmune de caballos inmunizados con una mezcla de los venenos de B. asper de México, Crotalus durissus de Suramérica y Lachesis muta de Centroamérica. Este antiveneno tiene menor concentración de proteínas e impurezas (albúmina, agregados de proteínas) que los productos colombianos, y buena eficacia neutralizante de los diferentes efectos inducidos in vitro y en ratones por los venenos de B. asper y P. nasutum de Colombia.19,20
Este proyecto de investigación se realizó con el objetivo de evaluar la eficacia y seguridad de Antivipmyn-Tri® en mordeduras por B. asper y B. atrox en tres departamentos de Colombia (Antioquia, Chocó y Amazonas). Así mismo, para establecer la eficacia de un nuevo esquema de tratamiento utilizando dosis de antiveneno polivalente mayores que las administradas en estudios previos efectuados en el país.
PACIENTES ACIENTES Y MÉTODOS
Antiveneno
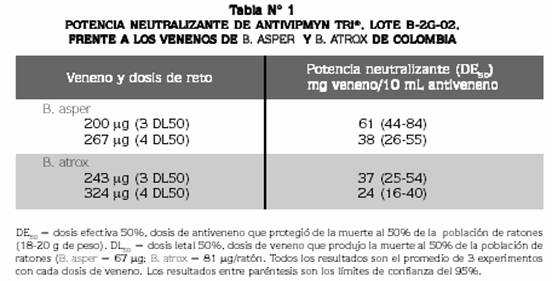
Se utilizó un antiveneno polivalente liofilizado antibothrópico, anticrotálico y antilachésico (Antivipmyn-Tri®) digerido con pepsina [F(ab’)2], lote B-2G-02, con fecha de expiración 02 de julio de 2007, producido por el Instituto Bioclón de México a partir del plasma hiperinmune de caballos inmunizados con los venenos de B. asper de México, C. durissus de Suramérica y L. muta de Centroamérica. El producto final, que era estéril y estaba libre de pirógenos y de albúmina, tenía una concentración de proteínas21 de 1,86 g/dL. La dosis efectiva 50% (DE50) neutralizante del efecto letal de los venenos de B. asper de Antioquia / Chocó y de B. atrox del Meta (especie que habita en la Amazonia y en la Orinoquia) en ratones Swiss Webster (18-20 g), se determinó siguiendo el método de Spearman-Karber22,23 (Tabla Nº 1).
Antes de la iniciación del estudio, el proyecto fue aprobado por los comités de ética médica de la Universidad de Antioquia y de los hospitales participantes. Así mismo, el proyecto y la importación del antiveneno requerido fueron aprobados por la Comisión Revisora de Medicamentos del Invima, acta 25 de agosto 28 de 2002.
Datos clínicos y epidemiológicos
El estudio se diseñó para una muestra de 60 pacientes durante 9 meses. Los pacientes (niños y adultos) ingresaron al estudio si llenaban los siguientes criterios:
1) Haber sufrido una mordedura por B. asper (mapaná, equis) o por B. atrox (cuatronarices, jergón, jararaca), confirmada por examen de la serpiente viva o muerta, efectuado por el paciente, por sus familiares o por el médico (Figuras Nº 1A y 1B).
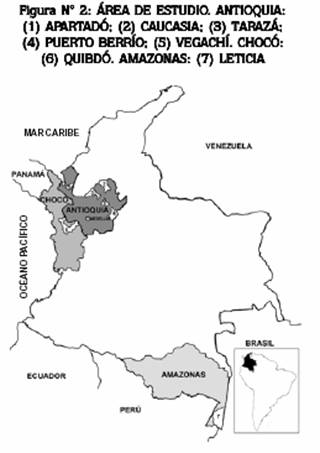
2) Consultar a los hospitales de Quibdó (Chocó), Apartadó, Caucasia, Tarazá, Puerto Berrío, Vegachí (Antioquia) y Leticia (Amazonas), con menos de 48 horas de evolución de la mordedura (Figura Nº 2).
3) Presentar alteraciones de la coagulación sanguínea al ingreso, con o sin sangrado local o sistémico.
4) No haber recibido antiveneno antes de ingresar al hospital.
Se obtuvo el consentimiento informado de todos los pacientes o de sus familiares. En el formulario se registraron los siguientes datos: edad, sitio de la mordedura y tiempo transcurrido entre ésta, el ingreso y el comienzo de la seroterapia; atención por la medicina tradicional; tamaño y especie de la serpiente; signos de envenenamiento local y sistémico; resultados de los exámenes hematológicos, bacteriológicos, de química clínica e imágenes diagnósticas; pruebas de coagulación y determinación de la concentración de fibrinógeno en el plasma 24 (normal por encima de 150 mg/dL) al ingreso y a las 6, 12, 24, 48, 72 y 96 horas después de la faboterapia; dosis del antiveneno; reacciones tempranas adversas (RTA);7-10,22 tratamientos complementarios (antibióticos, cirugías, etc.); complicaciones y evolución final. Además, se programaron para cada paciente una o varias citas de revisión después del alta, para detectar las reacciones tardías de hipersensibilidad (RTH o enfermedad del suero)19,22,25 que aparecen 5-24 días después de aplicado el antiveneno, y para determinar la evolución y las secuelas.
Grado de envenenamiento y tratamiento
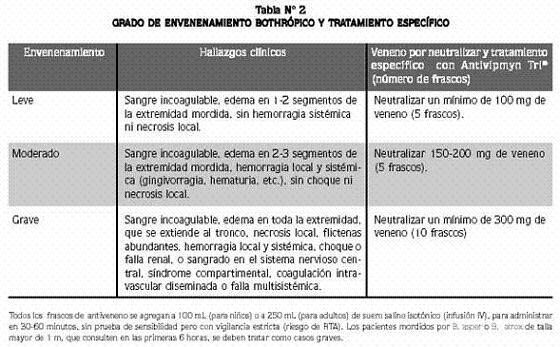
Se dividió a los pacientes en 3 grupos (envenenamiento leve, moderado y grave) siguiendo criterios ya descritos (Tabla Nº 2).4,9 Basados en estudios previos, solo los pacientes con envenenamiento grave tienen riesgo de muerte y de secuelas.1,2,7-9
Los pacientes que presentaron envenenamiento leve o moderado recibieron una dosis inicial de 5 frascos de antiveneno; quienes tenían envenenamiento grave y los mordidos por una serpiente de más de 1 metro (independientemente del grado del envenenamiento al ingreso, si éste fue en las primeras 6 horas), recibieron una dosis inicial de 10 frascos del antiveneno (tabla Nº 2), por la frecuente asociación con envenenamiento grave.1,2,6-9 No se hicieron premedicación con antihistamínicos o esteroides ni pruebas de sensibilidad porque no tienen valor predictivo.10,19,26 En consecuencia, se vigiló estrictamente a todos los pacientes durante 24 horas por considerarlos potencialmente reactivos a la seroterapia. Las reacciones tempranas adversas (RTA) o eventos adversos a la seroterapia, definidas por la OMS22 como las que se presentan durante las primeras 24 horas después de aplicado el antiveneno, fueron clasificadas como leves (cutáneas, gastrointestinales, fiebre, escalofríos), moderadas (leve hipotensión, edema angioneurótico facial) y graves (edema angioneurótico de la vía aérea, broncoespasmo, choque, paro cardíaco). Cuando ocurrieron, se hicieron los tratamientos convencionales.9,25 Brevemente, se detuvo la infusión de antiveneno y se administró adrenalina subcutánea (SC) o IV según la gravedad de la reacción (0,2-0,5 mg en adultos; 0,01 mg/kg en niños), un corticoide IV equivalente a 100-200 mg de hidrocortisona cada 6 horas por 24 horas y un antihistamínico IV. Cuando los síntomas desaparecieron, se reanudó cuidadosamente la infusión.
Se consideraron como criterios de eficacia de la dosis inicial de antiveneno el cese de las hemorragias local y sistémica (diferentes de la hematuria) en las primeras 12 horas de tratamiento y la normalización de la coagulación sanguínea (pruebas de coagulación o fibrinógeno) durante las primeras 24 horas de la seroterapia.7-9 Si no se lograban esos criterios, se administraba una dosis adicional de 3 frascos de antiveneno a las 12 (por sangrado persistente) o a las 24 horas (por coagulopatía persistente).
Test de coagulación del todo o nada en 20 minutos (20 min WB WBCT)
Este método, sencillo y rápido, se efectuó al ingreso y a las 6, 12, 24, 48, 72 y 96 horas después de administrado el antiveneno: se dejó en reposo 20 minutos a temperatura ambiente un tubo de ensayo de vidrio, limpio y seco, con 3 mL de sangre, y luego se lo inclinó suavemente para observar si había o no formación de coágulo total y firme.27-29
Concentraciones séricas de veneno y antiveneno
Estas concentraciones se determinaron por medio de un inmunoensayo (ELISA), siguiendo la técnica descrita por Theakston et al. 30,31 con pequeñas modificaciones.7,27,32 Se recolectaron las muestras de sangre (3 mL) en tubos de ensayo limpios y secos al ingreso y a las 1, 6, 12, 24, 48, 72 y 96 horas después del comienzo de la seroterapia. Se congeló el suero obtenido a -20 ºC hasta el momento de usarlo. Los resultados se expresaron en µL de antiveneno/mL de suero con referencia a una curva estándar preparada con concentraciones conocidas del antiveneno F(ab’)2, desde 0,8 hasta 50 µL de antiveneno/mL de suero, utilizando como diluyente suero humano (dilución 1:1.000) proveniente de 63 donantes sanos de la región de estudio y del mismo grupo socioeconómico. Se utilizaron las muestras tomadas al ingreso como controles negativos individuales para el inmunoensayo de cuantificación de las concentraciones de antiveneno. Se determinó la línea basal para el inmunoensayo de las concentraciones de veneno cuantificando las absorbancias en las 63 muestras de suero de los donantes sanos, e interpolando los resultados en una curva de concentraciones conocidas de veneno. Las absorbancias a 492 nm fueron 0,055 ± 0,025 (media ± DE). Usando 0,105 como punto de corte negativo (media + 2 DE), dos de los 63 sueros de donantes sanos fueron positivos. La especificidad fue 96,8%, y el límite más bajo para la detección de veneno fue 8,4 ng/mL.
Análisis estadístico
Se construyó una base de datos con la información de los pacientes y se la analizó utilizando el software estadístico STATISTICA 98 (Statsoft Inc., Tulsa, OK, USA). Los promedios de las concentraciones iniciales de veneno y antiveneno se compararon, para los grupos de pacientes según el grado de envenenamiento, mediante análisis de varianza unifactorial. Luego, se utilizó el análisis de varianza multivariado en la comparación de las mediciones repetidas en el tiempo. La asociación entre variables cualitativas se estableció mediante la prueba exacta de Freeman y Halton en el software StatXact 6.2 (Cytel Software Corporation, Cambridge, MA, USA), y entre variables cuantitativas por la prueba t de Student. Se consideraron significativas las diferencias cuando p era menor de 0,05.
RESULTADOS
Aspectos clínicos y epidemiológicos
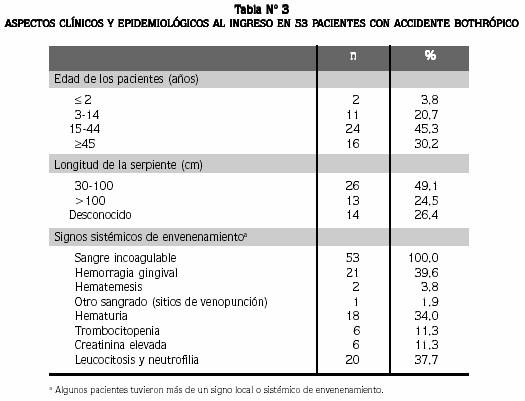
En 2003, entre marzo y noviembre, 53 pacientes llenaron los criterios para su inclusión en el estudio; 44 de ellos fueron mordidos por B. asper (22 en Chocó y 22 en Antioquia), y nueve lo fueron por B. atrox en Leticia (Amazonas). Trece pacientes (24,5%) eran menores y 40 (75,5%) mayores de 15 años, muchos de estos adultos eran agricultores (Tabla Nº 3).
El accidente fue significativamente más frecuente en hombres (37 casos = 69,8%; p = 0,004), en áreas rurales (49 accidentes = 92,5%; p < 0,001) y en las extremidades inferiores (38 = 71,7%; p = 0,002), principalmente en los pies (47,2%). Quince de las víctimas (28,3%) fueron mordidas en las manos.
Trece mordeduras (24,5%) fueron de animales adultos (mayores de 1 m) y en seis de ellas ocurrió necrosis local. Veintitrés pacientes (43,4%) fueron atendidos inicialmente por curanderos en sus veredas, donde recibieron remedios tradicionales; 39 del total (73,6%) consultaron a los hospitales en las primeras seis horas después del accidente, seis de 53 (11,3%) en la primera hora, y nueve (17,0%) en la segunda hora; otros nueve (17,0%) acudieron al hospital entre las 6 y 12 horas y cinco más (9,4%) consultaron después de las 12 horas. Cincuenta y dos pacientes (98,1%) tuvieron signos locales de envenenamiento, principalmente edema, hemorragia activa/equimosis (56,6%), flictenas (9,4%) y necrosis (11,3%). Los 53 pacientes presentaban sangre incoagulable al ingreso, 24 (45,3%) tenían sangrado sistémico con o sin hematuria, especialmente gingivorragia (tabla Nº 3). El grado final de envenenamiento fue leve en 13 pacientes (24,5%), moderado en 30 (56,6%) y grave en 10 (18,9%).
Respuesta terapéutica
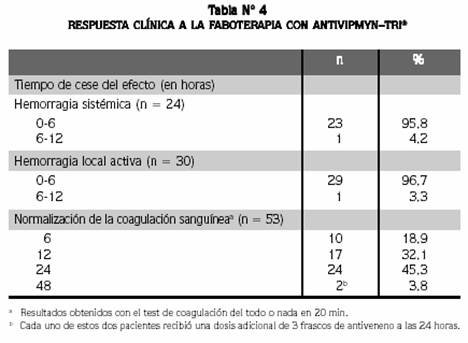
Cuarenta y ocho pacientes (90,6%) recibieron una dosis inicial de 5 frascos de antiveneno y los cinco restantes, 10 frascos. Cinco pacientes que llegaron a tener finalmente envenenamiento grave fueron inicialmente asignados a una categoría inferior de envenenamiento por no tener disponible el resultado de la creatinina al ingreso o porque consultaron en las primeras 2-6 horas después de la mordedura, cuando el cuadro clínico no estaba totalmente instalado, lo cual explica que no hayan recibido 10 frascos como se planteó en los métodos para los casos de envenenamiento grave. Veintitrés (95,8%) de los 24 pacientes que tuvieron hemorragia sistémica diferente de la hematuria dejaron de sangrar en las primeras 6 horas después de iniciada la faboterapia, y el otro, en las 6 horas siguientes. El cese de la hemorragia local tuvo un comportamiento similar (Tabla Nº 4).
La hematuria cesó en 12 horas en seis pacientes (33,3%), en 24 horas en 15 (83,3%) y en 48 horas en 17 (94,4%). La coagulación se normalizó (20 min WBCT) en 6 horas en 10 casos (18,9%) y en 12 horas en otros 27 (50,9%). A las 24 horas ya era normal en 51 (96,2%) pacientes (tabla Nº 4). Las excepciones fueron dos casos de hipoprotrombinemia persistente (TP de 16 y 23 segundos a las 24 horas, con control de 11,7 segundos, coágulo incompleto y fibrinógeno normal), que se corrigieron en las siguientes 24 horas con dosis adicionales de 3 frascos de antiveneno. Además, hubo dos recurrencias de la coagulopatía (20 min WBCT alterado, fibrinógeno 100 y 110 mg/dL, respectivamente) a las 24 horas (un caso leve) y a las 48 horas (un caso moderado) que previamente habían normalizado la coagulación a las 12 y 24 horas, respectivamente, recurrencia que se corrigió en ambos casos en las siguientes 12 horas, también con la aplicación de una dosis adicional de tres frascos de antiveneno. A las 72 horas la coagulación se había normalizado en todos los pacientes.
En 18 pacientes (34%) no progresó el edema después de aplicado el antiveneno. Por consiguiente, el cese de su progresión se consideró solo en 35 casos: en 32 de ellos (91,4%) cesó en las primeras 24 horas y lo mismo ocurrió durante el segundo y tercer días en los tres casos restantes.
Dieciséis pacientes (30,2%) recibieron dosis adicionales de antiveneno (3 frascos). Diez de ellos por fuera del protocolo establecido, así: dos por persistencia del sangrado a las 6 horas y 8 por sangre incoagulable: dos de éstos a las 6 horas y seis a las 12 horas. Otros dos las recibieron por tener sangre incoagulable a las 24 horas; dos más por recurrencia de la coagulopatía (24 y 48 horas) y dos para ajustar a las 6 horas la dosis recomendada en mordeduras por B. asper mayor de 1 m y envenenamiento grave. No hubo asociación estadísticamente significativa (p > 0,05) entre la dosis inicial de antiveneno (5 ó 10 frascos) y el tiempo requerido para que se normalizara la coagulación (6, 12 ó 24 horas). Tampoco la hubo entre la restauración de la coagulación en las primeras 12 ó 24 horas y la aplicación de dosis adicionales de antiveneno a las 6 ó 12 horas. Sin embargo, los dos casos de recurrencia de la coagulopatía habían recibido la dosis inicial más baja de antiveneno (5 frascos).
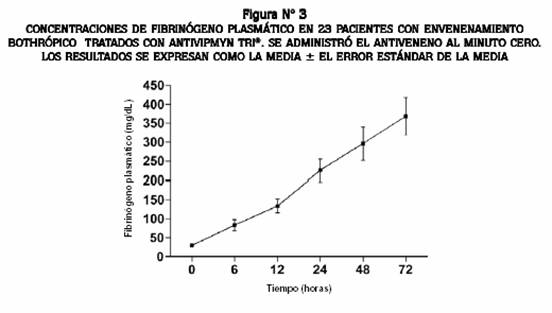
El fibrinógeno plasmático solo se pudo cuantificar en 23 pacientes, cuya concentración al ingreso era de 22,7 ± 7,4 mg/dL (media ± error estándar de la media). En la figura Nº 3 se puede ver que la concentración de fibrinógeno aumentaba significativamente (p < 0,001) desde las 6 (79,2 ± 15,7 mg/dL) y 12 horas (155,7 ± 18,6 mg/dL) hasta su normalización en la mayoría de los pacientes en el transcurso de 12-24 horas en concordancia con la restauración del test de coagulación.
Concentraciones séricas de veneno y antiveneno
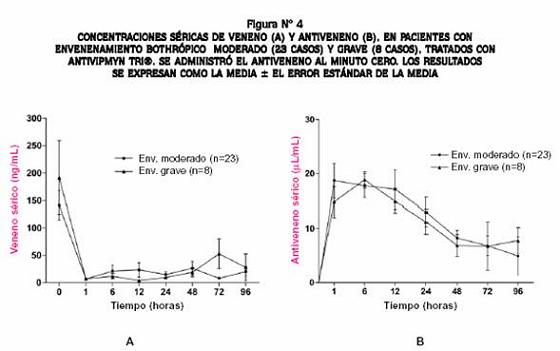
Se cuantificaron en 36 pacientes: 5 leves, 23 moderados y 8 graves. Antes de administrar el antiveneno, las concentraciones séricas de veneno eran significativamente más altas (p = 0,02) en los casos moderados (141,8 ± 27,7 ng/mL) y graves (191,5 ± 67,5 ng/mL) que en los leves (15,4 ± 2,3 ng/mL) (media ± error estándar de la media), pero no había diferencia entre las concentraciones de veneno al ingreso de los grupos de casos moderados y graves (p = 0,63). Al final de la infusión del antiveneno (1 hora), las concentraciones séricas de veneno disminuían significativamente y en los intervalos posteriores permanecían por debajo del punto de corte en la mayoría de los 36 pacientes (Figura Nº 4A).
Sin embargo, 12 de los 36 pacientes (33,3%), 8 de ellos casos moderados y 4 graves, presentaron recurrencia de la antigenemia (10-70 ng/mL) entre las 6 y 96 horas después de iniciada la faboterapia, aunque tuvo significado clínico en solo uno de ellos que presentó coagulopatía persistente, sin sangrado, hasta las 48 horas.
No hubo asociación estadísticamente significativa (p = 0,14) entre recurrencia de la antigenemia sin significado clínico y envenenamiento moderado/grave; tampoco la hubo (p = 0,82) con la dosis inicial de antiveneno administrada. Las concentraciones séricas de antiveneno aumentaron significativamente al final de la infusión de Antivipmyn Tri® (1 hora), y permanecieron detectables con una curva de descenso progresivo, durante las 96 horas en que se hizo el ensayo (Figura Nº 4B).
Reacciones tempranas adversas al antiveneno (RTA)
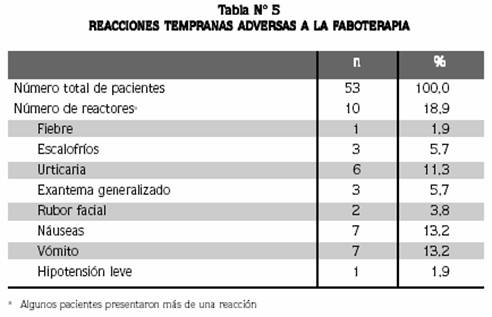
Diez pacientes (18,9%) presentaron eventos adversos, que en nueve fueron considerados leves (reacciones cutáneas, febriles, gastrointestinales) (Tabla Nº 5).
Un paciente de 73 años presentó una reacción moderada (hipotensión de 80/60). Todos los eventos adversos ocurrieron durante la infusión del antiveneno o en las dos horas siguientes. En dos de los pacientes se presentaron con la administración de la dosis adicional del faboterápico. Todos los pacientes con RTA respondieron pronto (1-2 horas) al tratamiento convencional.
Reacciones tardías de hipersensibilidad al antiveneno (RTH)
Como la mayoría de los pacientes provenían de áreas rurales, solo cuatro regresaron a control clínico después de haber sido dados de alta. Uno de ellos presentó una RTH (urticaria) cinco días después de la administración del faboterápico, la cual respondió en 24 horas con la administración de un corticoide intramuscular (IM) y un antihistamínico oral (hidroxicina).
Complicaciones y evolución final
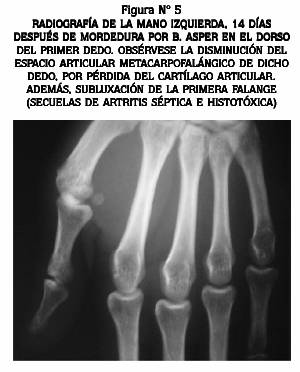
Seis pacientes (11,3%) tuvieron insuficiencia renal aguda y respondieron al tratamiento de soporte sin requerir diálisis. En 16 pacientes (30,2%) se presentaron infecciones de tejidos blandos, a saber: celulitis sin absceso en 10 casos y abscesos que fueron drenados quirúrgicamente en seis, uno de ellos con artritis séptica de la articulación metacarpofalángica del dedo pulgar (Figura Nº 5).
Dados los escasos recursos para estudios microbiológicos en los hospitales del estudio, solo en uno de los pacientes se logró aislar un bacilo gramnegativo que no fue identificado, sensible a ciprofloxacina y gentamicina.
No hubo muertes. Cuatro pacientes (7,5%) quedaron con secuelas, que en dos fueron pérdidas de masa muscular por necrosis; además de ellos una niña de cuatro años presentó síndrome compartimental y necrosis del dedo índice, por lo que requirió fasciotomía en el dorso de la mano y luego amputación del dedo. El cuarto de estos pacientes tuvo subluxación metacarpofalángica del dedo pulgar con pérdida del cartílago articular, secundarias a artritis séptica y lesión intrarticular ocasionada por el veneno (Figura Nº 5).
DISCUSIÓN
Desde la reunión efectuada en Zúrich (1979) por el Comité de Expertos de la OMS, se han recomendado los ensayos clínicos controlados como la mejor forma de evaluar la eficacia, dosificación y seguridad de un antiveneno, y se ha promovido la producción mundial de antivenenos de mayor pureza (Fab2 y Fab) para disminuir la incidencia de RTA.22,33
La desfibrinación se presenta en el 60-80% de los pacientes y facilita el sangrado tanto local como en órganos distantes del sitio de la mordedura, cuando hay daño en la microvasculatura inducido por las hemorraginas o en presencia de trombocitopenia; dicho sangrado puede poner en peligro la vida.1,7-9,34-38 Por tal motivo, en diversos estudios de accidentes ocasionados por B. asper y por otras especies de víboras, llevados a cabo en América y en otros continentes, se ha concluido que una de las metas del tratamiento con antivenenos es detener en las primeras 6-12 horas los sangrados local y sistémico y normalizar la coagulación sanguínea.27,29
Los resultados del presente trabajo son similares a los de tres estudios controlados hechos previamente en Colombia con antivenenos F(ab’)2 producidos en Brasil (Instituto Butantán), y de IgG total producidos en Costa Rica (Instituto Clodomiro Picado, ICP) y Colombia (Instituto Nacional de Salud, INS), puesto que en todos los pacientes se detuvieron los sangrados local y sistémico en las primeras 6-12 horas, y se normalizó la coagulación en las primeras 24 horas en el 96,2-100% de los pacientes (Tabla Nº 4).7-9 Estos criterios son simples y están al alcance de todos los clínicos en todos los lugares, para valorar la eficacia de un antiveneno en accidente bothrópico. Los cuatro estudios concuerdan también en que, independientemente de la dosis inicial de antiveneno administrada, es bajo el número de pacientes mordidos por B. asper y B. atrox que normalizan la coagulación en 6 horas (11-30%).
En este estudio, 16 pacientes (30,2%) recibieron dosis adicionales de antiveneno. La administración de una dosis adicional de este preparado a las 6 ó 12 horas no afectó el resultado del test de coagulación en las primeras 24 horas. Así, parece innecesaria la recomendación de administrar dosis adicionales de antiveneno a las 6 ó 12 horas, si no se ha normalizado la coagulación sanguínea en ese tiempo, cuando se han administrado dosis iniciales adecuadas como las aquí utilizadas. Por otra parte, en algunos individuos pueden ser inconvenientes las dosis adicionales, por representar un exceso de antiveneno e incrementar el riesgo de RTA, tal como sucedió en dos pacientes de este estudio. Lo anterior permite también sugerir que las dosis adicionales estarían recomendadas solo en las siguientes circunstancias: si a las 12 horas persiste un sangrado diferente a la hematuria, si a las 24 horas persiste la coagulopatía, si a las 48 horas continúa progresando el edema, o en casos de recurrencia de cualquiera de estas tres situaciones clínicas.7-9,19
El fenómeno de recurrencia de los signos locales de envenenamiento (edema, hemorragia), de la coagulopatía (hipofibrinogenemia), de la trombocitopenia y de la elevación del nivel sérico de veneno, se ha descrito en el tratamiento del envenenamiento grave por crotálidos, utilizando cualquiera de los 3 tipos de antivenenos. Sin embargo, la recurrencia de la coagulopatía es más frecuente con el uso de antivenenos de fragmentos Fab (53%) y F(ab´)2 (5-17%).8,9,27,39-44 El otro factor que se relaciona con la recurrencia de la antigenemia y la coagulopatía es la administración inicial de subdosis de antivenenos.8,9,45 En el presente estudio, llevado a cabo con un antiveneno F(ab´)2, dos pacientes (3,8%), uno con envenenamiento leve y otro con un cuadro moderado, cada uno de ellos tratado con una dosis inicial de cinco frascos del faboterápico, tuvieron recurrencia de la coagulopatía (24 y 48 horas) sin sangrado adicional.
Hay otras explicaciones posibles para el fenómeno de la recurrencia, que es más frecuente en las primeras 72-96 horas de tratamiento, cuando se utilizan antivenenos de IgG y F(ab´)2: 1) la disparidad en la cinética y dinámica del veneno y del antiveneno; 2) el antiveneno falla en neutralizar inicialmente todo el veneno; 3) el veneno no neutralizado en los depósitos tisulares (tercer espacio) se puede difundir hacia el torrente circulatorio de tal manera que finalmente la concentración sérica de antiveneno es insuficiente para neutralizarlo; 4) la más rápida eliminación de los fragmentos F(ab´)2 o Fab no unidos a los antígenos, en comparación con la eliminación de los componentes del veneno; 5) la separación de los complejos veneno/antiveneno después de su unión inicial eficaz; 6) en algunos casos, un exceso de antiveneno no parece prevenir la recurrencia de la antigenemia, porque una fracción del antiveneno no es funcional, debido a su poca avidez por los antígenos o a que forma agregados.19,27,43,45 Tal como está descrito, la monitorización estricta de la coagulación en los intervalos aquí recomendados es indispensable para detectar oportunamente las recurrencias. La administración de una dosis adicional de 3 frascos de antiveneno es suficiente en estos casos para restaurar la coagulación en 12-24 horas.27,43,46
Un hallazgo interesante fue la persistencia de hipoprotrombinemia leve y coágulo incompleto en dos pacientes mordidos por B. asper, con concentraciones normales de fibrinógeno, 24 horas después de iniciado el tratamiento Esto ha sido descrito en otros continentes (Australia), y en Brasil en mordeduras por B. jararaca, especialmente con el uso de antivenenos de baja potencia neutralizante de la fracción activadora de la protrombina, en comparación con su alta actividad frente a otros componentes del veneno.28,43,47,48 Adicionalmente, debe recordarse que los venenos de B. asper y B. atrox tienen toxinas procoagulantes activadoras de la protrombina (factor II) y del factor X, y toxinas desfibrinantes similares a la trombina, que activan el fibrinógeno.34,49,50 Así, en algunos pacientes puede observarse disparidad en la cinética de recuperación de los factores de coagulación que estaban alterados, de modo que puede ser más rápida la recuperación del fibrinógeno que la de la protrombina (observación personal). Otra situación que puede presentarse es la persistencia a las 24 horas de alteraciones de la coagulación, por activación del sistema fibrinolítico o por la presencia de un factor antiagregante plaquetario.28
Una dosis suficiente de antiveneno en pacientes con accidentes bothrópicos logra que cese el progreso del edema en 12 horas en el 80% de los casos y en 24 horas en el 95%.7-9 En este estudio, la progresión del edema se detuvo en el 91,4% de los casos en 24 horas y en el 97,1% en 48 horas. Tal como se recomendó en los estudios previos, el progreso del edema hasta el segundo día no se debe tomar como criterio para administrar dosis adicionales de antiveneno, puesto que el edema es un fenómeno autofarmacológico (liberación de sustancias endógenas) que desencadena el veneno.7-9,51 Por consiguiente, el cese de su progresión y su desaparición posterior están relacionados con otros factores homeostáticos que no necesariamente dependen de la neutralización del veneno por el antiveneno. Si el edema sigue progresando después de 48 horas de iniciado el tratamiento, se debe pensar en la posibilidad de infección sobreagregada y correlacionar el cuadro clínico con los resultados de exámenes paraclínicos (observación personal).
A pesar de las innovaciones tecnológicas introducidas en la producción de los tres tipos de antivenenos, no se ha logrado eliminar las reacciones tempranas adversas (RTA). Se presentan en el 5-87% de los pacientes tratados con antivenenos de IgG total o F(ab’)2 y pueden ser anafilácticas (por IgE), anafilactoides (por activación del complemento), pirógenas (por endotoxinas), idiosincrásicas o tóxicas (por ejemplo, por el fenol, preservante utilizado en la producción de antivenenos y que puede provocar hipotensión).7-9,19,26,52-62 Entre los factores involucrados en la generación de dichas reacciones adversas se encuentran: 1) a mayor concentración de proteínas, incluyendo la albúmina, y de sus agregados, mayor es la incidencia de RTA, situación que depende de los pasos seguidos en la purificación de la IgG (el ácido caprílico permite obtener un antiveneno más rico en IgG, libre de albúmina y con menor concentración de agregados de proteínas, que el sulfato de amonio; los antivenenos F(ab’)2 tienen menor concentración de proteínas que los antivenenos de IgG total);8,19,63 2) la activación del complemento según el tipo de antiveneno: los de IgG total lo activan por la vía clásica por la porción Fc de su molécula, en tanto que los digeridos con pepsina [F(ab’)2] lo activan por la vía alterna;17 la actividad anticomplementaria es mayor en los de IgG total fraccionada con sulfato de amonio;17,64 3) la administración por vía IV tiene mayor riesgo de RTA; 4) la naturaleza de la población expuesta.22 Los antivenenos Fab, que no activan el complemento, son los que menos RTA inducen (1-14%), pero su elevado costo limita su uso en países en vía de desarrollo.41,60,65
Antivipmyn-Tri® indujo en este trabajo eventos adversos (RTA) en 10 de 53 pacientes (18,9%), frecuencia similar a la observada en un estudio reciente (18,4-19,4%) llevado a cabo en la Amazonía brasileña (estado Pará) con antivenenos F(ab’)2 producidos en dos institutos de Brasil,61 pero menor que la observada en Colombia y Ecuador (19-81,8%) con antivenenos producidos en estos dos países y en el ICP de Costa Rica entre 1994 y 1998, compuestos de IgG fraccionada con sulfato de amonio.7-9,38,66 Ninguna de estas reacciones puso en peligro la vida de los pacientes, y desaparecieron en pocas horas con el tratamiento convencional.
En conclusión, Antivipmyn-Tri® demostró ser un faboterápico eficaz y seguro para el tratamiento del envenenamiento bothrópico en Colombia. Las dosis utilizadas fueron eficaces para revertir las alteraciones clínicas y de laboratorio más relevantes de este envenenamiento.
AGRADECIMIENTOS
Al personal de los hospitales en que se realizó el estudio. A Colciencias, a la Universidad de Antioquia y al Instituto Bioclón S. A. de C. V. (capital variable) de México, por el apoyo financiero para la investigación. A Janeth Lucía García por las labores de secretaría durante el desarrollo del proyecto y por la digitación del manuscrito.
REFERENCIAS BIBLIOGRÁFICAS
1. Otero R, Tobón GS, Gómez LF, Osorio R, Valderrama R, Hoyos D, et al. Accidente ofídico en Antioquia y Chocó. Aspectos clínicos y epidemiológicos (marzo de 1989-febrero de 1990). Acta Med Colomb 1992; 17: 229-249. [ Links ]
2. Otero R, Gutiérrez J, Rodríguez O, Cárdenas SJ, Rodríguez L, Caro E, et al. Aspectos actuales de las mordeduras de serpientes en Colombia. Propuesta de intervención para un problema grave de salud en Antioquia y Chocó. Rev Epidemiol Antioquia 2001; 26: 43-48. [ Links ]
3. Otero R, Callejas ME, Gutiérrez J, Lotero GJ, Rodríguez O, Villa NH, et al. Necesidades reales de antivenenos en Colombia. Características de los productos y del mercado. Rev Epidemiol Antioquia 2001; 26: 49-59. [ Links ]
4. Silva- Haad JJ. Las serpientes del género Bothrops en la Amazonía colombiana. Acta Med Colomb 1989; 14: 148-165. [ Links ]
5. Campbell JA, Lamar WW. The Venomous Reptiles of the Western Hemisphere. Ithaca (NY): Cornell University Press; 2004. [ Links ]
6. Otero R, Valderrama R, Osorio RG, Posada LE. Programa de atención primaria del accidente ofídico. Una propuesta para Colombia. Iatreia 1992; 5: 96-102. [ Links ]
7. Otero R, Gutiérrez JM, Núñez V, Robles A, Estrada R, Segura E, et al. A randomized double-blind clinical trial of two antivenoms in patients bitten by Bothrops atrox in Colombia. Trans R Soc Trop Med Hyg 1996; 90: 696 -700. [ Links ]
8. Otero R, Gutiérrez JM, Rojas G, Núñez V, Díaz A, Miranda E, et al. A randomized blind clinical trial of two antivenoms prepared by caprylic acid or ammonium sulphate fractionation of IgG, in Bothrops and Porthidium snake bites in Colombia. Correlation between safety and biochemical characteristics of antivenoms. Toxicon 1999; 37: 895-908. [ Links ]
9. Otero-Patiño R, Cardoso JLC, Higashi HG, Núñez V, Díaz A, Toro MF, et al. A randomized, blinded, comparative trial of one pepsin-digested and two whole IgG antivenoms for Bothrops snake bites in Urabá, Colombia. Am J Trop Med Hyg 1998; 58: 183-189. [ Links ]
10. Ayres JA, Barraviera B. Evaluation of the intradermal sensitivity test in patients submitted to heterologous serotheraphy. J Venom Anim Toxins 1999; 5: 142-152. [ Links ]
11. Bon C. The serum-therapy was discovered 100 years ago. Toxicon 1996; 34: 142-143. [ Links ]
12. Gowda TV. Interaction of snake venom phospholipases A2 with plant isolates. In: Kini RM, ed. Venom phospholipase A2 enzymes, 1st ed. Chichester: John Wiley & Sons; 1997. p. 205-221. [ Links ]
13. Melo PA, Ownby CL. Ability of wedelolactone, heparin, and para-bromophenacyl bromide to antagonize the myotoxic effects of two crotaline venoms and their PLA2 myotoxins. Toxicon 1999; 37: 199-215. [ Links ]
14. Lomonte B, Lundgren J, Johansson B, Bagge U. The dynamics of local tissue damage induced by Bothrops asper snake venom and myotoxin II on the mouse cremaster muscle: an intravital and electron miocroscopic study. Toxicon 1994; 32: 41-55. [ Links ]
15. Gutiérrez JM, León G, Rojas G, Lomonte B, Rucavado A, Chaves F. Neutralization of local tissue damage induced by Bothrops asper (terciopelo) snake venom. Toxicon 1998; 36: 1529-1538. [ Links ]
16. León G, Valverde Jm, Rojas G, Lomonte B, Gutiérrez JM. Comparative study on the ability of IgG and Fab sheep antivenoms to neutralize local hemorrhage, edema and myonecrosis induced by Bothrops asper (terciopelo) snake venom. Toxicon 2000; 38: 233-244. [ Links ]
17. León G, Mongue M, Rojas E, Lomonte B, Gutiérrez JM. Comparison between IgG and F(ab’)2 polyvalent antivenoms: neutralization of systemic effects induced by Bothrops asper venom in mice, extravasation to muscle tissue, and potential for induction of adverse reactions. Toxicon 2001; 39: 793-801. [ Links ]
18. Chippaux JP, Goyffon M. Venoms, antivenoms and immunotherapy. Toxicon 1998; 36: 823-846. [ Links ]
19. Otero R. Seroterapia antivenenosa. Ventajas del uso de antivenenos del tipo IgG, F(ab´)2 o Fab en picaduras de escorpiones y mordeduras de serpientes. Pediatría 2002; 37: 8-16. [ Links ]
20. Otero R, Núñez V, Barona J, Díaz A, Saldarriaga M. Características bioquímicas y capacidad neutralizante de cuatro antivenenos polivalentes frente a los efectos farmacológicos y enzimáticos del veneno de Bothrops asper y Porthidium nasutum de Antioquia y Chocó. Iatreia 2002; 15: 5 -15. [ Links ]
21. Lowry OH, Rosebrough NJ, Farr AL, Randall RJ. Protein measurement with the folin phenol reagent. J Biol Chem 1951; 193: 265-275. [ Links ]
22. WORLD HEALTH ORGANIZATION. Progress in the Characterization of Venoms and Standardization of Antivenoms. WHO Offset Publication 1981; 58: 1- 44. [ Links ]
23. Robles A, Gene JA. Determinación de la dosis letal 50% por el método de Spearman-Karber. Toxicalc. San José: Publicación Offset, Instituto Clodomiro Picado, 1ª ed. Universidad de Costa Rica; 1990. [ Links ]
24. Ratnoff OD, Menzie C. A new method for the determination of fibrinogen in small samples of plasma. J Lab Clin Med 1951; 37: 316-320. [ Links ]
25. Fan HW, França FOS. Soroterapia. In: Schvartsman S, ed. Plantas Venenosas e Animais Peçonhentos, 1ª ed. São Paulo: Sarvier; 1992. p. 176-181. [ Links ]
26. Malasit P, Warrell DA, Chantavanich P, Viravan C, Mongkilsapaya J, Singhthong B, et al. Prediction, prevention and mechanism of early (anaphylactic) antivenom reactions in victims of snake bites. Br Med J 1986; 292: 17-20. [ Links ]
27. Ho M, Warrell Da, Looareesuwan S, Phillips RE, Chanthavanich P, Karbwang J, et al. Clinical significance of venom antigen levels in patients envenomed by the Malayan pit viper (Calloselasma rhodostoma). Am J Trop Med Hyg 1986; 35: 579 -587. [ Links ]
28. Sano-Martins IS, Fan HW, Castro SCB, Tomy SC, França FOS, Jorge MT, et al. Reliability of the simple 20 minute whole blood clotting test (WBCT20) as an indicator of low plasma fibrinogen concentration in patients envenomed by Bothrops snakes. Toxicon 1994; 32: 1045-1050. [ Links ]
29. Warrell DA. Clinical toxicology of snakebite in Asia. In: Meier J, White J, eds. Handbook of Clinical Toxicology of Animal, Venoms and Poisons, 1st ed. Boca Ratón: CRC Press; 1995. p. 493-594. [ Links ]
30. Theakston RDG, Lloyd-Jones MJ, Reid HA. Micro-ELISA for detecting and assaying snake venom and venom antibody. Lancet 1977; 2: 639-641. [ Links ]
31. Theakston RDG, Fan HW, Warrell DA, Dias DA Silva WD, Ward SA, Higashi HG, et al. Use of enzyme immunoassays to compare the effect and assess the dosage regimens of three Brazilian Bothrops antivenoms. Am J Trop Med Hyg 1992; 47: 593-604. [ Links ]
32. Barraviera B, Sartori A, Pereira DA Silva MF, Kaneo R, Peracolli MTS. Use of an Elisa assay to evaluate venom, antivenom, IgG and IgM human antibody levels in serum and cerebrospinal fluid from patients bitten by Crotalus durissus terrificus in Brazil. J Venom Anim Toxins 1996; 2: 14-27. [ Links ]
33. Theakston RDG, Warrell DA, Griffiths E. Report of a WHO workshop on the standardization and control of antivenoms. Toxicon 2003; 41: 541- 557. [ Links ]
34. Kamiguti AS, Cardoso JLC. Haemostatic changes caused by venoms of South American snakes. Toxicon 1989; 27: 955-963. [ Links ]
35. Kamiguti AS, Hay CRM, Theakston RDG, Zuzel M. Insights into the mechanism of haemorrhage caused by snake venom metalloproteinases. Toxicon 1996; 34: 627-642. [ Links ]
36. Escalante T, Núñez J, Moura DA Silva AM, Rucavado A, Theakston RDG, Gutiérrez JM. Pulmonary hemorrhage induced by jararhagin, a metalloproteinase from Bothrops jararaca snake venom. Toxicol Appl Pharmacol 2003; 193: 17-28. [ Links ]
37. Escalante T, Rucavado A, Kamiguti AS, Theakston RDG, Gutiérrez JM. Bothrops asper metalloproteinase BaP1 is inhibited by alfa 2-macroglobulin and mouse serum and does not induce systemic hemorrhage or coagulopathy. Toxicon 2004; 43: 213-217. [ Links ]
38. Otero R, Gutiérrez J, Mesa MB, Duque E, Rodríguez O, Arango JL, et al. Complications of Bothrops, Porthidium and Bothriechis snakebites in Colombia. A clinical and epidemiological study of 39 cases attended in an university hospital. Toxicon 2002; 40: 1107-1114. [ Links ]
39. Warrell DA, Looareesuwan S, Theakston RDG, Phillips RE, Chanthavanich P, Viravan C, et al. Comparative trial of three monospecific antivenoms for bites by the Malayan Pit viper (Calloselasma rhodostoma) in Southern Thailand; clinical and laboratory correlations. Am J Trop Med Hyg 1986; 35: 1235- 1247. [ Links ]
40. Chippaux JP, Lang J, Eddinc SA, Fagot P, Rage V, Peyrieux JC, et al. Clinical safety of a polyvalent F(ab´)2 equine antivenom in 223 African snake envenomations: a field trial in Cameroon. VAO (Venin Afrique de l´Ouest) Investigators. Trans R Soc Trop Med Hyg 1998; 92: 657-662. [ Links ]
41. Dart RC, Macnally J. Efficacy, safety, and use of snake antivenoms in the United States. Ann Emerg Med 2001; 37: 181-188. [ Links ]
42. Seifert SA, Boyer LV. Recurrence phenomena after immunoglobulin therapy for snake envenomations: Part 1. Pharmacokinetics and pharmacodynamics of immunoglobulin antivenoms and related antibodies. Ann Emerg Med 2001; 37: 189-195. [ Links ]
43. Boyer LV, Seifert SA, Cain JS. Recurrence phenomena after immunoglobulin therapy for snake envenomations: Part 2. Guidelines for clinical management with crotaline Fab antivenom. Ann Emerg Med 2001; 37: 196-201. [ Links ]
44. Ho M, Silamut K, White NJ, Karbwang J, Looareesuwan S, Phillips RE, et al. Pharmacokinetics of three commercial antivenoms in patients envenomed by the Malayan pit viper, Calloselasma rhodostoma, in Thailand. Am J Trop Med Hyg 1990; 42: 260-266. [ Links ]
45. Lalloo DG, Theakston RDG. Snake antivenoms. J Toxicol Clin Toxicol 2003; 41: 277-290. [ Links ]
46. Otero R, Mesa MB. Mordeduras graves por serpientes. In: Quevedo A, Martínez Y, Duque JI, Mejía JA, eds. El niño en estado crítico, 1ª ed. Medellín: CIB; 2001. p. 571-578. [ Links ]
47. Henderson A, Baldwin LN, May C. Fatal brown snake (Pseudonaja textilis) envenomation despite the use of antivenom. Med J Aust 1993; 158: 709-710. [ Links ]
48. Masci PP, Mirtschin PJ, Nias TN, Turnbull RK, Kuchel TR, Whitaker AN. Brown snakes (Pseudonaja genus): venom yields, prothrombin activator neutralization and implications affecting antivenom usage. Anaesth Intensive Care 1998; 26: 276-281. [ Links ]
49. Markland FS. Snake venoms and the hemostatic system. Toxicon 1998; 36: 1749-1800. [ Links ]
50. Sano-Martins IS, Santoro ML. Distúrbios hemostáticos em envenenamentos por animais peçonhentos no Brasil. In: Cardoso JLC, França FOS, Fan HW, Málaque CMSA, Haddad Jr V, eds. Animais Peçonhentos no Brasil. Biología, Clínica e Terapêutica dos Accidentes, 1ª ed. São Paulo: Sarvier; 2003. p. 289-309. [ Links ]
51. Gutiérrez JM, Lomonte B. Efectos locales en el envenenamiento ofídico en América Latina. In: Cardoso JLC, França FOS, Fan HW, Málaque CMSA, Haddad Jr V, editors. Animais Peçonhentos no Brasil. Biología, Clínica e Terapêutica dos Accidentes, 1ª ed. São Paulo: Sarvier; 2003. p. 310-323. [ Links ]
52. García M, Monge M, León G, Lizano S, Segura E, Solano G, et al. Effect of preservatives on IgG aggregation, complement-activating effect and hypotensive activity of horse polyvalent antivenom used in snakebite envenomation. Biologicals 2002; 30: 143-151. [ Links ]
53. Jurkovich GJ, Luterman A, Mccullar K, Ramenofsky ML, Curreri PW. Complications of Crotalidae antivenin therapy. J Trauma 1988; 28: 1032-1037. [ Links ]
54. Cupo P, Azevedo-Marques MM, De Menezes JB, Hering SE. Reaçoes de hipersensibilidade imediatas apos uso intravenoso de soros antivenenos: valor prognistico dos testes de sensibilidade intradermicos. Rev Inst Med Trop São Paulo 1991; 33: 115-122. [ Links ]
55. Cardoso JLC, Fan HW, França FOS, Jorge MT, Leite SA, Nishioka SA, et al. Randomized comparative trial of three antivenoms in the treatment of envenoming by lance-headed vipers (Bothrops jararaca) in São Paulo, Brazil. Q J Med 1993; 56: 315-325. [ Links ]
56. Teixeira-Caiaffa W, Vlahov D, Figueiredo-Antunes CM, Ramos De Oliveira H, Diniz CR. Snake bite and antivenom complications in Belo Horizonte, Brazil. Trans R Soc Trop Med Hyg 1994; 88: 81-85. [ Links ]
57. Smith DC, Reddi KR, Laing G, Theakston RDG, Landon J. An affinity purified ovine antivenom for the treatment of Vipera berus envenoming. Toxicon 1992; 30: 865-871. [ Links ]
58. Sutherland SK. Antivenom use in Australia. Premedication, adverse reactions and the use of venom detection kits. Med J Aust 1992; 157: 734 –739. [ Links ]
59. Karlson-Stiber C, Persson H. Antivenom treatment in Vipera berus envenoming: report of 30 cases. J Intern Med 1994; 235: 57-61. [ Links ]
60. Kirkpatrick CH. Allergic histories and reactions of patients treated with digoxin immune Fab (ovine) antibody. Am J Emerg Med 1991; 9 (Suppl. 1): 7-10. [ Links ]
61. Pardal PPO, Souza SM, Monteiro MRCC, Fan HW, Cardoso JLC, França FOS, et al. Clinical trial of two antivenoms for the treatment of Bothrops and Lachesis bites in the north eastern Amazon region of Brazil. Trans R Soc Trop Med Hyg 2004; 98: 28-42. [ Links ]
62. Rawat S, Laing G, Smith DC, Theakston RDG, Landon J. A new antivenom to treat Eastern Coral snake (Micrurus fulvius fulvius) envenoming. Toxicon 1994; 32: 185-190. [ Links ]
63. Rojas G, Jiménez JM, Gutiérrez JM. Caprylic acid fractionation of hyperimmune horse plasma. Description of a simple procedure for antivenom production. Toxicon 1994; 32: 351-363. [ Links ]
64. Morais JF, De Freitas MCW, Yamaguchi IK, Dos Santos MC, Dias Da Silva WD. Snake antivenoms from hyperimmunized horses: comparison of the antivenom activity and biological properties of their whole IgG and F(ab´)2 fragments. Toxicon 1994; 32: 725-734 [ Links ]
65. Chippaux JP. The development and use of immunotherapy in Africa. Toxicon 1998; 36: 1503-1506. [ Links ]
66. Smalligan R, Cole J, Brito N, Laing GD, Mertz BL, Manock S, et al. Crotaline snake bite in the Ecuadorian Amazon: randomized double blind comparative trial of three South American polyspecific antivenoms. Br Med J 2004; 329: 1129-1135. [ Links ]