Introducción
La dipirona, es un medicamento antinflamatorio no esteroideo (AINES) de la familia de la pirazolona también llamado metamizol, analgésico, antipirético, antiespasmódico, aunque con pobre actividad antiinflamatoria1, de amplio uso en Latinoamérica y Colombia debido a su demostrada eficacia en el manejo del dolor agudo y por la ventaja que ofrece con su efecto analgésico y antiinflamatorio que no lo tienen otros medicamentos como el tramadol y los opioides2. En cuanto a sus características farmacodinámicas y farmacocinéticas, la fracción activa 4-metil-amino-antipirina (MAA) de la dipirona después de su administración intravenosa, presenta 85% de biodisponibilidad y alcanza su concentración máxima sérica (tmax) en 1,2 a 2 horas y su efecto analgésico alcanza su pico entre 20 a 45 minutos. Su unión a proteínas en menor del 60%, no pasa barreras con facilidad, tiene poca acumulación en tejidos y se elimina a través de glucurónidos en un 60%1.
La dipirona, incluso en dosis única, es efectiva para el dolor posquirúrgico, sola o acompañada con opioides, y en algunos casos, permite reducir o eliminar el uso de opioides en postoperatorio posterior a la artroscopia, cirugía abdominal y pélvica, hernia inguinal, histerectomía, artroplastia de cadera y rodilla, y apendicectomía laparoscópica3. En Colombia existen las presentaciones de dipirona sódica ampolla de l g/2ml y 2g/5ml, dipirona magnésica ampolla de 2,5 g/5ml, dipirona tabletas de 500 y 324 mg, solución oral 50 mg/ml y jarabe 50 mg/ml4, siendo la presentación intravenosa utilizada intrahospitalariamente. Sin embargo, su uso ha sido controversial debido la alta incidencia de trastornos hematológicos en los años 60 con el Estudio Internacional de Agranulocitosis y Anemia Aplásica (IAAAS) que reportó una incidencia global de 6,2 casos por millón y una tasa de mortalidad de 0,5 por millón5, lo cual llevo al retiro de este medicamento en varios países como Canadá en l963, Estados Unidos en l973 y otros 30 países europeos6,7. Aunque, el estudio Incidencia de anemia aplásica y agranulocitosis en Latinoamérica, the LATIN study8, reporta que existe una variabilidad considerable entre las regiones de los diferentes países, por lo cual son necesarios más estudios.
Por otra parte, el tramadol es un opioide sintético con efecto analgésico mediado por su acción agonista central en receptores de opioides endógenos9, muy utilizado a nivel mundial sin restricciones, como tratamiento para dolor agudo o crónico de moderado a grave, incluyendo dolor postoperatorio10. Las concentraciones máximas del metabolito activo del tramadol (Ml) se obtienen a las 3 horas después de una dosis oral, aunque el fármaco nativo es detectable a los 15-45 minutos y alcanza su máximo a las 2 horas, tiene unión a proteínas del 20% y su metabolismo es hepático9. Es de destacar que el tramadol es análogo sintético de la codeína y una menor afinidad por los receptores opioides, por lo cual tiene un potencial mucho menor que otros opiáceos para inducir depresión respiratoria y dependencia. En cuanto a sus efectos adversos, se han reportado constipación, vértigo, cefalea, prurito, somnolencia, ansiedad, agitación, entre otros11.
La dipirona y el tramadol intravenoso son medicamentos esenciales para el manejo del dolor en el servicio de hospitalización de ortopedia12. La literatura existente sobre dipirona es escasa por lo cual existe una brecha en la generación de conocimiento a nivel de Latinoamérica y no hay unanimidad frente a la seguridad y riesgo/beneficio del uso de dipirona frente al tramadol por vía intravenosa2. El efecto adverso, según la Organización Mundial de la Salud (OMS), también denominado reacción o evento adverso, es "La reacción nociva y no deseada que se presenta tras la administración de un medicamento, a dosis utilizadas habitualmente en la especie humana, para prevenir, diagnosticar o tratar una enfermedad, o para modificar cualquier función biológica". Siendo los eventos adversos un factor importante para determinar la seguridad de los medicamentos13, en Colombia el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA), mediante la Resolución 3100 del 201914, Sistema Único de Habilitación, obliga a realizar acciones de farmacovigilancia. Por tanto, el objetivo del presente estudio fue establecer la prevalencia y los factores asociados a eventos adversos por dipirona y tramadol intravenoso en pacientes hospitalizados en el servicio de ortopedia de un hospital en Medellín durante los años 2010 a 2020.
Metodología
Tipo de estudio, población y muestra
Se trató de un estudio transversal analítico de fuente secundaria. Se incluyeron todos los registros de los pacientes mayores de l8 años hospitalizados en área de ortopedia del Hospital Alma Máter de Antioquia, que recibieron dipirona y tramadol intravenoso entre el año 2010 y 2020. Se excluyeron pacientes con vía de administración del tramadol y dipirona diferente a intravenoso, con eventos adversos a otros medicamentos y aquellos en los que no se haya definido cuál de los dos medicamentos generó la reacción. El Hospital Alma Máter de Antioquia, es de alto nivel de complejidad, se encuentra ubicado en la ciudad de Medellín y atiende población del régimen contributivo y subsidiado de la ciudad y alrededores con 20.987 egresos para el año 2022.
Para el periodo de estudio se registraron en el servicio de ortopedia, l8.522 atenciones que recibieron tramadol y 18.049 que recibieron dipirona, de los cuales 9.256 recibieron los dos medicamentos. Posterior a la aplicación de los criterios de inclusión/exclusión quedaron 9.l55 registros, de los cuales se obtuvo una muestra representativa de 973 registros, 720 registros sin reacción adversa y 253 registros con reacción adversa (Figura 1).
Para el cálculo del tamaño de la muestra se tuvo en cuenta un nivel de confianza del 95% y margen de error del 5%, y una prevalencia esperada del l,87%, más el l0% por posibles pérdidas, utilizando Epidat 3.1.
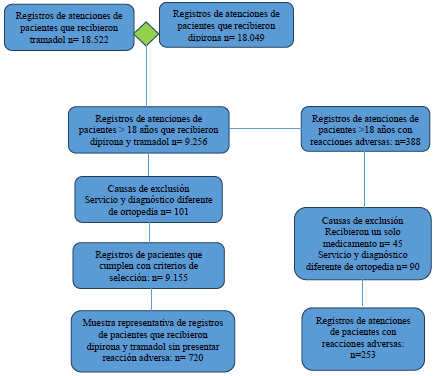
Figura 1 Identificación de los registros de pacientes que recibieron dipirona y tramadol del servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
Fuentes de datos y medición
La información fue obtenida a partir de los registros de la base de datos de egresos de pacientes del servicio de ortopedia que recibieron dipirona y tramadol intravenoso y la base de datos problemas relacionados con medicamentos 2010 a 2020 filtrada por reacciones a dipirona y tramadol intravenoso en el mismo servicio, las cuales se unificaron con el código de atención del paciente.
La variable desenlace fue reacción adversa (si-no), mientras que las variables independientes se agruparon en factores sociodemográficos (edad en años cumplidos y sexo) y clínicos. Las variables clínicas fueron: diagnóstico principal de acuerdo a la clasificación CIE-10, medicamento implicado en la reacción (no reacción; reacción adversa a dipirona; reacción adversa a tramadol), evento adverso especifico a cualquiera de los medicamentos (anafilaxia; eosinofilia; nauseas/vómito; neutropenia; rash; pruritootros; toxicidad medular; agranulocitosis; no reacción), dosis de tramadol al día (50 miligramos; otra dosis), dosis de dipirona al día (1 y 3 gramos), frecuencia de uso de tramadol (cada 6 horas; cada 8 horas; cada 12 horas; cada 24 horas), frecuencia de uso de dipirona (cada 6 horas; cada 8 horas; cada 12 horas; cada 24 horas), duración de uso de la dipirona (0-3 días; 4-6 días; mayor a 7 días), duración de uso del tramadol (0-3 días; 4-6 días; mayor a 7 días), estancia hospitalaria de pacientes (número de días de hospitalización) de acuerdo a lineamientos de Grupo de Farmacovigilancia Seccional de Antioquia15, días de uso para la aparición de reacción adversa (número de días al momento de aparición de reacción) y clasificación de evento adverso - reacción adversa de acuerdo con el mecanismo de la reacción (tipo A; tipo B), clasificación de evento adverso - reacción adversa de acuerdo con la gravedad (serio; no serio), clasificación de evento adverso - reacción adversa de acuerdo con la causalidad (definitivo; probable; posible), clasificación de evento adverso - reacción adversa de acuerdo con la evitabilidad (evitable; no evitable)16,17, según el algoritmo de la OMS18.
La calidad de los datos obtenidos se garantiza por la implementación de historias clínicas electrónicas con campos estandarizados; además de ser considerado un documento legal, se hace todo lo posible para garantizar que esté completado correctamente. Por otra parte, la institución cuenta con un grupo de farmacovigilancia conformado por toxicólogos clínicos, químicos farmacéuticos y regentes que realizan farmacovigilancia activa diaria, así como la recolección de notificaciones pasivas y se encargan de la búsqueda, análisis y tabulación de la base de datos de los problemas relacionados con medicamentos. Se realizó un control de calidad para eliminar registros incompletos (sin registro de edad, que recibieron un solo medicamento y sin diagnóstico ortopédico) y que no cumplieran los criterios imputación (se eliminó la variable pertenencia étnica por registro incompleto en más del 66% de la información). Los registros seleccionados para el estudio recibieron tanto dipirona como tramadol intravenoso para evitar el sesgo de diagnóstico.
Análisis estadístico
Para las variables cuantitativas se calcularon estadísticos de tendencia central (media o mediana) con sus respectivos estadísticos de dispersión. Para las variables cualitativas se obtuvieron distribuciones de frecuencias absolutas y relativas. Esta descripción se realizó por grupo analgésico. Se estimó la proporción de eventos adversos en cada analgésico con su respectivo IC95% y la misma estimación por gravedad, mecanismo de acción, evitabilidad y causalidad. Se llevó a cabo una prueba de hipótesis de comparación de proporciones con IC95%.
Para la asociación entre dosis y aparición de eventos adversos se realizaron pruebas de Chi cuadrado. Adicionalmente se calcularon las medidas de asociación respectivas. Para la asociación entre duración y aparición de eventos adversos se procedió con el mismo análisis anterior. Finalmente, para establecer los factores de riesgo asociados con la aparición de eventos adversos en el modelo multivariado, las variables se seleccionaron teniendo en cuenta los resultados del análisis bivariado y la relevancia clínica, por lo que se incluyeron dosis y duración, edad, sexo, diagnóstico, días de estancia, y días de uso para la aparición de reacción adversa. Para la estimación del modelo se utilizó el método de Máxima Verosimilitud que permite estimar los coeficientes del modelo optimizando la probabilidad de observar los datos dados los valores de las covariables. Las pruebas se consideraron significativas con p ≤ 0,05. Los datos fueron procesados con el software SPSS 29.
Resultados
De los 973 registros incluidos en el estudio, 253 registros presentaron reacciones adversas (l70 por dipirona y 83 por tramadol) y 720 no presentaron reacción adversa. En relación a las características sociodemográficas de los registros incluidos, se observa que el sexo masculino predomina en los tres grupos de análisis (Tabla 1). La media de edad fue similar para todos los grupos, 56,1 ± 21,8 años para el grupo de reacción a tramadol, 52,1 ± 19,4 años para el grupo reacción a dipirona y 54,3 ± 20,4 años para el grupo sin reacción adversa. Por otra parte, de acuerdo a la distribución por años, el 2010 fue el año donde se registraron más reacciones adversas para el tramadol (l8,07%) y dipirona (26,47%), mientras que para el grupo sin reacción adversa fue el año 20l9 (13,75%).
Tabla 1 Características sociodemográficas de los registros incluidos en el estudio, del servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
| Variables sociodemográficas | Total | Sin reacción | Reacción a dipirona | Reacción a tramadol |
|---|---|---|---|---|
| 973 (100) | 720(74) | 170(17,5) | 83 (8,5) | |
| Edad - años (X̄ ± ds) | 54,10 20,70 | 54,34 20,88 | 52,10 19,40 | 56 21,80 |
| Sexo - n (%) | ||||
| Femenino | 452 (46,45) | 339 (47,08) | 79 (46,47) | 34 (40.96) |
| Masculino | 521 (53,55) | 381 (52,92) | 91 (53,53) | 49 (59,04) |
| Distribución de reacciones adversas por año - | ||||
| 2010 | 111 (11,40 | 51 (7,08) | 45 (26,47) | 15 (18,07) |
| 2011 | 76 (7,81) | 50 (6,94) | 21 (12,35) | 5 (6,02) |
| 2012 | 67 (6,88) | 4l (5,69) | l5 (8,82) | ll (13,25) |
| 2013 | 81 (8,32) | 48 (6,66) | 27 (15,88) | 6 (7,22) |
| 2014 | 81 (8,23) | 57 (7,91) | 18 (10,58) | 6 (7,22) |
| 2015 | 105 (10,79) | 82 (11,38) | 9 (5,29) | l4 (l6,86) |
| 2016 | 78 (8,01) | 67 (9,30) | 6 (3,52) | 5 (6,02) |
| 2017 | 94 (9,66) | 82 (11,38) | 8 (4,70) | 4 (4,8l) |
| 2018 | 111 (11,40) | 93 (12,91) | 10 (5,88) | 8 (9,63) |
| 2019 | 109 (11,20) | 99 (13,75) | 8 (4,70) | 2 (2,04) |
| 2020 | 60 (6,16) | 50 (6,94) | 3 (1,76) | 7 (8,43) |
Abreviaturas: X̄:media; ds: desviación estandar; %: porcentaje
En relación a las variables clínicas (Tabla 2), los diagnósticos más frecuentemente registrados fueron fracturas, seguido por, las infecciones en el grupo del tramadol y otros diagnósticos (heridas múltiples en extremidades, contusiones, artrosis, entre otros) en los grupos de dipirona y sin reacción adversa. En cuanto al tipo de evento adverso, los eventos fueron principalmente rash o erupción cutánea para el tramadol (40.96%) y la dipirona (62,94%).
Tabla 2 Características clínicas de los registros incluidos del servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
| Variables clínicas | Total | Sin reacción | Reacción a dipirona | Reacción a tramadol |
|---|---|---|---|---|
| 973 (100) | 720 (74) | 170 (17,47) | 83 (8,53) | |
| Diagnósticos CIE10 - n (%) | ||||
| Infecciones | 106 (10,89) | 59 (8,19) | 25 (14,70) | 22 (26,50) |
| Fracturas | 481 (49,43) | 386 (53,61) | 69 (40,58) | 26 (31,32) |
| Luxaciones | 44 (4,52) | 39 (5,41) | 4 (2,35) | 1 (1,20) |
| Complicaciones de diabetes | 38 (3,90) | 22 (3,05) | 9 (5,29) | 7 (8,43) |
| Radiculopatías | 71 (7,29) | 45 (6,25) | 17 (10,0) | 9 (10,84) |
| Traumatismos | 39 (4,00) | 20 (2,77) | 14 (8,23) | 5 (6,02) |
| Otros | 194 (19,93) | 149 (20,69) | 32 (18,82) | 13 (15,66) |
| Evento adverso - n (%) | ||||
| Rash | 141 (14,49) | - | 107 (62,94) | 34 (40.96) |
| Prurito | 20 (2,05) | - | 16 (9,41) | 4 (4,82) |
| Eosinofilia | 13 (1,33) | - | 12 (7,06) | 1 (1,20) |
| Nauseas /Vómito | 7 (0,71) | - | 1 (0,59) | 6 (7,23) |
| Neutropenia | 9 (0,92) | - | 5 (2,94) | 4 (4,82) |
| Anafilaxia | 8 (0,82) | - | 5 (2,94) | 3 (3,61) |
| Toxicidad Medular | 2 (0,20) | - | 2 (1,18) | - |
| Otros | 53 (5,44) | - | 22 (12,94) | 31 (37,35) |
| Dosis dipirona - n (%) | ||||
| 1gramo día | 893 (91,77) | 655 (90.97) | 158 (92,95) | 80 (96,38) |
| 3gramos día | 80 (8,23) | 65 (9,03) | 12 (7,05) | 3 (3,62) |
| Dosis tramadol - n (%) | ||||
| 50 mg día | 779 (80,06) | 598 (83,05) | 118 (69,41) | 63 (75,90) |
| Otras dosis | 194 (l9,93) | 122 (16,95) | 52 (30,59) | 20 (24,10) |
| Frecuencia tramadol - n (%) | ||||
| Cada 6 horas | 272 (27,95) | 196 (27,22) | 48 (28,24) | 28 (33,73) |
| Cada 8 horas | 622 (63,92) | 457 (63,47) | 112 (65,88) | 53 (63,86) |
| Cada 12 horas | 28 (2,87) | 21 (2,92) | 5 (2,94) | 2 (2,41) |
| Cada 24 horas | 51 (5.26) | 46 (6,39) | 5 (2,94) | - |
| Frecuencia dipirona - n (%) | ||||
| Cada 6 horas | 535 (54,98) | 366 (50,8) | 121 (71,2) | 48 (57,8) |
| Cada 8 horas | 353 (36,28) | 280 (38,9) | 46 (27,l) | 27 (32,5) |
| Cada 12 horas | 23 (2,36) | 19 (2,6) | 2 (1,2) | 2 (2,4) |
| Cada 24 horas | 62 (6,37) | 55 (7,6) | 1 (0,6) | 6 (7,2) |
| Duración tramadol - n (%) | ||||
| 0 - 3 días | 454 (46,66) | 393 (54,6) | 42 (24,7) | 19 (22,9) |
| 4 - 6 días | 228 (23,43) | 174 (24,2) | 38 (22,4) | 16 (19,3) |
| ≥7 días | 291 (29.91) | 153 (21,2) | 90 (52,9) | 48 (57,8) |
| Duración dipirona - n (%) | ||||
| 0 - 3 días | 467 (48,00) | 389 (54,0) | 56 (32,9) | 22 (26,5) |
| 4 - 6 días | 225 (23,12) | 169 (23,5) | 38 (22,4) | l8 (2l,7) |
| ≥7 días | 281 (28,88) | 162 (22,5) | 76 (44,7) | 43 (5l,8) |
| Reacción adversa según mecanismo de reacción - n (%) | ||||
| Tipo A | 23 (9,09) | - | 9 (5,29) | 14 (16,87) |
| Tipo B | 230 (90,91) | - | 161 (94,71) | 69 (83,13) |
| Reacción adversa según gravedad - n (%) | ||||
| Serias | 8 (0,82) | - | 6 (3,53) | 2 (2,41) |
| No serias | 245 (25,18) | - | 164 (96,47) | 81 (97,59) |
| Reacción adversa según causalidad - n (%) | ||||
| Definitiva | 18 (1,85) | - | 16 (9,41) | 2 (2,41) |
| Probable Posible | 131 (13,46) 104 (10,69) | - | 90 (52,94) 64 (37,65) | 41 (49,40) 40 (48,19) |
| Reacción adversa de acuerdo con la evitabilidad - n (%) | ||||
| Evitable | 7 (0,72) | - | 5 (2,94) | 2 (2,41) |
| No evitable | 246 (25,28) | - | 165 (97,06) | 81 (97,59) |
| Estancia hospitalaria - Me (RIC) | 5 (2-12) | 3,0 (1-7) | 13 (8-28) | 21 (10-35) |
| Días al uso de aparición de reacción adversa - Me (RIC) | 7 (4,0-13,0) | - | 6 (3,75-12,0) | 8 (4,0-14,0) |
Abreviaturas: Me: mediana; RIC: rangos intercuartílicos Q1-Q3; %: porcentaje
La dosis de uso del analgésico fue con mayor frecuencia de 1 gramo para dipirona y 50 mg para tramadol, siendo similar la frecuencia de uso de los medicamentos, para el tramadol de cada 8 horas y para la dipirona cada 6 horas. En los grupos con reacciones adversas, se observa alto porcentaje de registros con una duración de uso mayor a 7 días, 52,91% para el grupo de reacción adversa a dipirona y 57,81% para el grupo de reacción adversa a tramadol.
En cuanto a la clasificación de las reacciones adversas, estas se distribuyeron en: a) Mecanismo de acción, la clasificación tipo B fue la más frecuente en los grupos con reacción adversa; b) Gravedad, donde se observaron reacciones serias para el grupo de dipirona en un 3,53% de los casos y 2,41% para el grupo de tramadol; c) Causalidad de acuerdo con la clasificación de la OMS, siendo la más frecuente la clasificación probable para ambos medicamentos; y d) Evitabilidad, que se encontró menos del 3% para los dos grupos de medicamentos.
Finalmente, para estancia hospitalaria, la mediana de duración de la hospitalización fue de 21 días (RIC Q1-Q3: 10-35) para el grupo de eventos adversos a tramadol y 13 días (RIC Q1-Q3: 8-28) para el grupo de reacción adversa a dipirona, y los días de aparición de la reacción adversa fue de 8 días (RIC Q1-Q3: 4-14) para el grupo de tramadol y 6 días (RIC Q1-Q3: 3,75-12) para el grupo de reacción adversa a dipirona.
Prevalencia de eventos adversos según dosis y duración de uso
Se observa una prevalencia de eventos adversos a dipirona de 0,175 (IC95%: 0,15-0,20) y una prevalencia de eventos adversos por tramadol de 0,085 (IC95%: 0,067-0,103). En la tabla 3 se presentan las proporciones de cada uno de los analgésicos según la clasificación de las reacciones adversas.
Tabla 3 Clasificación de eventos adversos por dipirona y tramadol intravenoso en el servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
| Clasificación de reacción adversa | Dipirona (170) n (%; IC95%) | Tramadol (83) n (%; IC95%) |
|---|---|---|
| Según mecanismo de reacción | ||
| Tipo A | 9 (0,05; 0,01-0,08) | 14 (0,16; 0,88-0,24) |
| Tipo B | 161 (0,94; 0,91-0,98) | 69 (0,83; 0,75-0,91) |
| Según gravedad | ||
| Serio | 6 (0,03; 0,007-0,06) | 2 (0,02; -0,008-0,05) |
| No serio | 164 (0,96; 0,93-0,99) | 81 (0,97; 0,94-1,00) |
| Según causalidad | ||
| Definitivo | 16 (0,09; 0,05-0,13) | 2 (0,024; -0,008-0,05) |
| Probable | 90 (0,52; 0,45-0,60) | 41 (0,49; 0,38-0,60) |
| Posible | 64 (0,37; 0,30-0,44) | 40 (0,48; 0,37-0,58) |
| Según evitabilidad | ||
| Evitable | 5 (0,002; 0,004-0,005) | 2 (0,002; -0,008-0,05) |
| No evitable | 165 (0,97; 0,94-0,99) | 81 (0,97; 0,94-1,00) |
Abreviaturas: IC: intervalo de confianza; %: porcentaje; Tipo A: reacción adversa relacionada con el medicamento; Tipo B: reacción adversa impredecible
Al comparar las prevalencias de los efectos adversos de los dos grupos de medicamentos, la diferencia fue significativa con valor p <0,001 (IC95%: 0,059-0,120), por lo cual la proporción de pacientes con reacciones adversas por dipirona fue 5,9% y 12% más que la proporción de pacientes con reacciones adversas por tramadol.
Al evaluar la dosis empleada y duración de uso del analgésico respecto a la aparición de reacciones adversas, se observaron diferencias significativas con valor p <0,001, en relación a la dosis de tramadol y la duración del uso de dipirona y tramadol (Tabla 4).
Tabla 4 Dosis empleada y la duración de la terapia con respecto a la aparición de eventos adversos por dipirona y tramadol en el servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
| Medicamento Dosis/Duración | Si | No | X2 | Valor p |
|---|---|---|---|---|
| Dosis dipirona | 2,38 | 0,123 | ||
| 1 gr | 238 | 655 | ||
| 3 gr | 15 | 65 | ||
| Dosis tramadol | 15,54 | < 0,001 | ||
| Otra dosis | 72 | 122 | ||
| 50 mg | 181 | 598 | ||
| Duración dipirona | 60,16 | < 0,001 | ||
| 0-3 días | 78 | 389 | ||
| 4-6 días | 56 | l69 | ||
| >7 días | 119 | l62 | ||
| Duración tramadol | 107,29 | < 0,001 | ||
| 0-3 días | 61 | 393 | ||
| 4-6 días | 54 | 174 | ||
| ≥7 días | 138 | 153 |
Abreviaturas: X2: chi cuadrado; gr: gramos; mg: miligramos
Factores asociados a eventos adversos por dipirona y tramadol
Se realizó un modelo de regresión logística multivariado exploratorio, para identificar factores asociados con las reacciones adversas a dipirona y tramadol, para lo cual se incluyeron las variables edad, sexo, diagnósticos, duración de uso de tramadol, duración de uso de dipirona, dosis de dipirona, dosis de tramadol, frecuencia de uso de tramadol y frecuencia de uso de dipirona. En este modelo, resultaron significativas las variables duración de uso de tramadol y el diagnóstico de infección, radiculopatía y traumatismo, destacando la duración del uso del tramadol por más de 7 días con OR=5,7 (IC95%:3,96 -8,24), y el diagnóstico de traumatismo con OR=3,43 (IC95%:1,64-7,19). La duración del uso de tramadol demuestra que a mayores días de uso aumenta la probabilidad de presentar reacción adversa. Por otra parte, la duración y frecuencia de uso de dipirona no resultó significativa en este modelo (Tabla 5).
Finalmente, para evaluar que tanto este modelo se ajusta a los datos, se realizó una prueba de bondad de ajuste y se obtuvo un valor p 0,36 en la prueba de Hosmer-Lemeshow, indicando que el modelo se ajustó bien.
Tabla 5 Factores asociados a eventos adversos por dipirona y tramadol el servicio de ortopedia, Hospital Alma Mater de Antioquia, 2010-2020
| Variables | OR (IC 95%) | Valor p |
|---|---|---|
| Duración Tramadol | ||
| 0-3 días | Ref | |
| 4 a 6 días | 2,05 (1,36-3,12) | < 0,001 |
| > de 7 días | 5,71 (3,96-8,24) | < 0,001 |
| Diagnostico CIE-l0 | ||
| Infecciones | 1,96 (1,15-3,15) | 0,012 |
| Fracturas | 0,79 (0,54-1,16) | 0,237 |
| Radiculopatias | 2,l6 (1,19-3,92) | 0,011 |
| Traumatismos | 3,43 (1,64-7,l9) | 0,001 |
Abreviaturas: OR: odds ratio; IC: intervalo de confianza al 95%; CIE-10: clasificación internacional de enfermedades décima revisión
Discusión
La dipirona o metamizol, continúa generando controversia por asociarse a reacciones adversas graves como agranulocitosis20, especialmente en Europa21, sin embargo, en países como Colombia, se usa frecuentemente para manejar el dolor. Así mismo, el tramadol es otro analgésico de uso frecuente para tratar el dolor, pues, aunque se asocia con reacciones adversas parece ser más seguro que otros medicamentos 9. En nuestro estudio se identificaron entre 5,90% y 12,00% más reacciones adversas por dipirona en comparación al tramadol, siendo mayor el porcentaje de reacciones adversas serias (3,53%) pero también la evitabilidad de estos eventos (2,94%) en este grupo de medicamentos. Adicionalmente, este estudio permitió identificar como factores asociados a reacciones adversas, la duración de uso de tramadol más de 7 días (OR=5,71; IC95%: 3,96-8,24) y los diagnósticos de infección (OR=1.96; IC95%:1,15-3,15), radiculopatía (OR=2,16; IC95%:1,19-3,92) y traumatismo (OR=3,43; IC95%:1,64-7,19).
En contraste con estudio de Lobo et al22, en el cual se reportó una prevalencia de 0,007 para dipirona y 0,004 para tramadol, en nuestro estudio la prevalencia de las reacciones adversas a dipirona fue 0,175 (IC95%: 0,15-0,20) y para tramadol 0,085 (IC95%: 0,067- 0,103), lo cual puede ser explicado porque el hospital donde se realizó el estudio cuenta con un programa de farmacovigilancia activa que analiza la totalidad de pacientes expuestos y se notifica las diferentes reacciones y a que los registros incluidos, fueron del servicio de ortopedia donde la frecuencia de uso de estos analgésicos es alta. En relación a las reacciones adversas específicas reportadas tanto para dipirona como para tramadol, el más frecuente fue rash cutáneo, mayor al 40%, difiriendo de los resultados de Moreno de Santacruz et al23, para la dipirona y Dhagudu et al24 para tramadol, donde registraron proporciones bajas de esta reacción adversa para ambos medicamentos, aunque este último estudio se realizó en pacientes en un servicio de salud mental.
En cuanto a la distribución por sexo, en su mayoría fueron hombres con una proporción mayor de reacciones adversas, presentando similitud con el estudio de Machado-Alba et al7, realizado en 2019, donde el 55,5% pertenecían al sexo masculino. Se observa además que, los registros de pacientes que presentaron reacciones adversas por tramadol tenían mayor edad (56 años), que las personas que presentaron reacciones por dipirona (52 años). Por otro lado, en nuestro estudio, las fracturas fueron los diagnósticos más frecuentes en pacientes con reacciones adversas tanto con dipirona como tramadol, parcialmente consistente con lo descrito por Montoya et al25, quienes reportan los politraumatismos con o sin fractura como los más frecuentes. El segundo diagnóstico más frecuente fue infecciones para el grupo con efectos adversos al tramadol, y para dipirona, otros diagnósticos, incluidas heridas múltiples en extremidades, contusiones, artrosis, entre otros; difiriendo en algunos casos de los diagnósticos reportados en el estudio Montoya et al 25, debido probablemente a que en nuestro estudio solo incluimos pacientes hospitalizados en ortopedia.
De acuerdo a la clasificación de las reacciones adversas, el mecanismo de reacción más frecuente fue la de tipo B, en contraste a lo reportado por Zazzara et al26, debido probablemente a que nuestro estudio se realizó con registros de pacientes hospitalizados y no en población general, por lo cual la dosificación de los medicamentos se realiza bajo vigilancia del equipo médico y por ello las principales reacciones son de tipo idiosincráticas o inmunológicas en lugar de aquellas relacionadas con la dosis. El hospital en donde se realizó el estudio cuenta con dosis máximas protocolizadas y sistematizadas para cada medicamento, evitando reacciones adversas dosis-dependiente. Para gravedad, el 3,16% de las reacciones adversas fueron serias, muy por debajo de lo reportado por Lobo et al22, que fue de 15,8%; específicamente por dipirona se encontró 3,53% de reacciones adversas serias, muy inferior al l0,2% descrito por Machado-Alba et al7. En el estudio realizado por Montoya et al25, quienes realizaron una comparación entre los dos analgésicos, encontraron 6,8% de reacciones adversas serias relacionadas con dipirona y 7,9% por tramadol; sin embargo, en nuestro estudio, estas fueron más bajas tanto para dipirona (3,5%) presentándose principalmente anafilaxia y toxicidad medular (un caso de neutropenia sin agranulocitosis), y para tramadol (2,41%) anafilaxia, consistente con Machado-Alba et al7, en el cual se reportaron iguales reacciones adversas serias para la dipirona.
De acuerdo a la causalidad según el algoritmo de la OMS18, se observó que para la dipirona las reacciones clasificadas como probables presentaron mayor frecuencia (52,94%), seguida de las reacciones posibles (37,65%) y por último, las definitivas (9,41%); en contraste con Machado-Alba et al7, en el cual el 66,l% fueron clasificadas como posibles, 32,2% probables y 1,7% definitivas, sin embargo, se debe aclarar que este último autor, no utilizó los criterios de la OMS, lo cual puede limitar las comparaciones con este estudio. Por otra parte, el hospital en el cual se realizó el estudio clasifica las reacciones adversas15, por lo cual es factible que esto se relacione con los resultados obtenidos, dado que los pacientes se evalúan y se clasifican solo hasta que se descartan otras causas. Por último, en cuanto a la evitabilidad, en el hospital donde se realizó el estudio hay una alerta que bloquea el medicamento al cual el paciente es alérgico o intolerante, lo cual evita la reexposición y disminuye el riesgo de evitabilidad, y la administración está protocolizada para evitar la ocurrencia de reacciones adversas. En nuestro estudio, la evitabilidad frente a las reacciones adversas por el uso de dipirona fue de 2,94% en contraste con el estudio de Machado-Alba et al7, donde reportan en el 28,8% de los pacientes que usaron dipirona y tenían un antecedente de reacción adversa a este medicamento.
Según la dosificación y frecuencia de los esquemas terapéuticos utilizados, en nuestro estudio predominó el esquema de 1 gramo cada 6 horas para el grupo con reacción adversa a la dipirona, lo cual difiere de lo reportado por Montoya et al25, donde las reacciones más frecuentes fueron por la administración de 2,5 gramos cada 6 horas. Para el grupo con reacciones adversas al tramadol, los resultados fueron similares entre nuestro estudio y la investigación de Montoya et al, indicando que 50 miligramos cada 8 horas produjeron más de dos terceras partes de las reacciones adversas, pudiendo ser esto debido a la no evitabilidad de la mayoría de las reacciones adversas, por el uso de dosis protocolizadas. Por otra parte, la mediana de estancia hospitalaria fue de 13 días para el grupo con reacción adversa a dipirona y 2l días para tramadol, opuesto a lo indicado por Montoya et al25, quienes describen una estancia hospitalaria de 12,44±9,07 días para pacientes con efectos secundarios a la dipirona y 9,28±7,32 días para el tramadol, lo que sugiere que estancias aproximadas a 10 días en el servicio de ortopedia se han relacionado con aparición de reacciones adversas. Frente a esto, los resultados de Sánchez Muñoz-Torrero et al27, afirman que un tiempo mayor a 12 días de hospitalización, es un factor de riesgo para presentar reacción adversa a medicamentos y se relaciona con reacciones de hipersensibilidad grado IV de la clasificación de Gell y Coombs28, siendo mayores a mayor tiempo de exposición. Dentro de este tipo de reacciones se encuentra el rash y, teniendo presente que el 62,9% y 4l% de los pacientes presentaron rash como efecto adverso por dipirona y tramadol respectivamente, esto podría explicar porque las duraciones de uso de dipirona y tramadol presentaron una diferencia significativa; a más días de uso, mayor es la probabilidad de presentar reacción adversa.
En cuanto a la asociación entre la dosis empleada y la duración de la terapia con la aparición de reacción adversa, Sánchez Muñoz-Torrero et al27 observaron de manera similar a nuestro estudio que, a mayor número de días de hospitalización y duración de uso de los medicamentos, aumenta el riesgo para presentar reacciones adversas; sin embargo, dicho estudio incluyó pacientes de medicina interna con diferentes diagnósticos y uso de medicamentos. La dosis de tramadol de 50 miligramos fue la más frecuente entre los pacientes con reacciones adversas, siendo esta una dosis usual, las reacciones adversas puede ser debido a que esta es la dosis más frecuentemente prescrita. En esta línea, Ferner y Aronson29 demuestran como con el uso repetido de un medicamento, se acumula y puede generar un efecto de hipersensibilidad a mayor tiempo de uso, lo cual podría explicar que la dosis repetida de 50 miligramos y la duración de uso de tramadol por más de 7 días, se vincule con aparición de reacciones adversas. Lobo et al22, también indican en su estudio la mayor presencia de reacciones adversas en los pacientes de ortopedia que usaron más de 6 días medicamentos analgésicos. Estos resultados, fueron confirmados por el modelo de regresión logística, el cual permitió establecer como factores asociados a la ocurrencia de los efectos adversos la duración de uso del tramadol más de 7 días y los diagnósticos de infecciones, radiculopatías y traumatismos. Sin embargo, también se podría plantear que estos resultados pueden estar relacionados a la presencia de interacciones farmacológicas o el uso de otros medicamentos que sensibilizaran a los pacientes para la aparición de reacciones adversas como lo indica Hernández et al30, ya que en el actual estudio esto no fue evaluado.
Este estudio cuenta con varias limitaciones. La principal, está relacionada con el diseño metodológico, pues por ser de corte trasversal de fuente secundaria tiene la limitante de no ser indicado para establecer causalidad y la medición de la prevalencia se puede verse afectada por el periodo definido para la realizar la investigación y el tipo de pacientes y patologías incluidas, y el completo diligenciamiento de los registros. Sin embargo, se destaca que este estudio contó con un importante número de registros en las bases de datos y que el sistema de farmacovigilancia del hospital de donde se tomaron los datos, asegura la calidad de los mismos. Otra limitante, la constituye la escasa literatura para discutir los resultados, dado el retiro de la dipirona en Estados Unidos y varios países de Europa.
Conclusiones
A pesar de las limitaciones, este estudio permitió establecer las prevalencias de las reacciones adversas asociados al uso de dipirona y tramadol intravenoso mayores que lo reportado en la literatura, y el tiempo de uso del medicamento podría estar relacionado con la aparición de eventos adversos. Adicionalmente, las reacciones adversas serias y evitables se presentaron en baja frecuencia y no se encontró ningún caso de agranulocitosis; destaca que la proporción de pacientes con reacciones adversas a dipirona fue 5,90% y 12,00% más que los pacientes con tramadol. Por tanto, se considera necesario mantener un uso prudente y protocolizado de dipirona para minimizar el riesgo reacciones adversas. Es necesario reforzar la farmacovigilancia activa que permita identificar eventos adversos y factores de riesgo asociados. Se recomienda diseñar protocolos y guías de práctica clínica para el uso de dipirona y tramadol intravenoso en los servicios intrahospitalarios de ortopedia.















