Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Vitae
Print version ISSN 0121-4004
Vitae vol.13 no.1 Medellín Jan./Jun. 2006
COMPUESTOS DE HIERRO PARA SUPLEMENTACIÓN ORAL: PRINCIPIOS Y AVANCES -REVISIÓN SISTEMATICA -
Lina J. PEREZ M1*. y Gloria TOBÓN1
1 Departamento de Farmacia. Facultad de Química Farmacéutica. Universidad de Antioquia. A.A 1226. Medellín - Colombia.
* Autora a quien se debe dirigir la correspondencia: linjohnna@yahoo.com
Recibido: Abril 07 de 2005 Aceptado: Febrero 28 de 2006
RESUMEN
Se presenta una revisión que abarca los principales aspectos sobre la absorción oral del hierro (fuentes y captación) y sus funciones en el organismo, centrándose en la tendencia actual de utilizar complejos o quelatos de este metal con ligandos orgánicos para el tratamiento oral por deficiencia del mismo (monosacáridos, aminoácidos y ácidos carboxílicos de bajo peso molecular), ya que estos compuestos aumentan la biodisponibilidad del hierro y disminuyen los efectos adversos que presentan sus sales inorgánicas a nivel gastrointestinal. Se describen los hallazgos más relevantes para la síntesis y caracterización de estos compuestos para uso farmacéutico, como suplemento nutricional. Por último se explican algunas de las principales interacciones del hierro con otros componentes de la dieta.
Palabras clave: Hierro (II), ligandos orgánicos, quelatos nutricionalmente funcionales, síntesis y caracterización
IRON COMPOUNDS FOR ORAL SUPPLEMENTATION :PRINCIPLES AND ADVANCES -SYSTEMATIC REVIEW-
ABSTRACT
A summary is presented of the main features about oral iron absorption (iron sources and pickup), and its functions in the body, focusing in the present tendency to use iron complexes formed mainly with ligands such as saccharides, amino acids and carboxylic acids of low molecular weight, for oral therapy in patients with iron deficiencies. These complexes or quelates increase the iron bio availability and reduce the adverse effects of inorganic salts in the gastrointestinal system. Also, this article describes, the more relevant findings about synthesis and characterization of this kind of compounds useful as s food supplement. Finally, some interactions between iron and other compounds of the daily diet are explained.
Keywords: Iron (II), organic ligands, nutritionally functional quelates, synthesis and characterization.
INTRODUCCIÓN
El hierro es un oligoelemento esencial para la vida, cuya deficiencia puede producir eritropoyesis defectuosa y anemia. Según se estima, más de 500 millones de personas en el mundo, sufren de anemia por deficiencia de este mineral en la dieta. En Indonesia, por ejemplo, 50 a 70 millones de personas (25–30% de la población) la padecen (1). Entre las medidas adoptadas está la que obliga a los empleadores a proporcionar suplementos de hierro a sus trabajadoras (2).
Pero este no es sólo un problema de los países conocidos como tercermundistas; en países como Suiza se han detectado deficiencias de micronutrientes en las mujeres, recomendándose la suplementación y la fortificación de los alimentos como posibles soluciones al problema (3).
Las deficiencias de hierro se pueden incrementar por el uso prolongado de anticonceptivos orales, aspirina, antiácidos, antiinflamatorios, anticoagulantes y esteroides. Adicionalmente, enfermedades del tracto gastrointestinal (TGI) o ginecológicas, tales como la fibrosis, aumentan el riesgo debido a la incapacidad de absorberlo eficientemente o simplemente incrementan las necesidades del organismo (4).
El hierro y sus sales deben ser administrados sólo para el tratamiento o profilaxis de anemias por deficiencia de hierro. La ruta de administración preferida es la oral, usualmente como sales ferrosas solubles que son mejor absorbidas que las sales férricas. La acción astringente de las preparaciones inorgánicas hasta ahora más usadas, como el sulfato ferroso, generalmente producen irritación gastrointestinal y dolor abdominal acompañados de náuseas y vómito, debido a que este tipo de sales se hidrolizan en el lumen, permitiendo el contacto del hierro con la mucosa, lo que genera radicales libres con acción irritante y deletérea para el tejido (5). Estos síntomas pueden ocasionar el abandono de la terapia.
¿Por qué es tan importante el hierro?
El hierro es un componente esencial de las proteínas involucradas en el transporte de oxígeno, además es necesario para la regulación del crecimiento y la diferenciación celular. Su deficiencia reduce la cantidad de oxígeno liberada a las células, lo que produce fatiga, reduce el desempeño y disminuye la inmunidad. Sin embargo, su exceso puede producir toxicidad (6).
El cuerpo de un hombre adulto contiene cerca de 50 mg Fe/kg de peso, mientras que el de una mujer 35 mg Fe/kg. Más de dos tercios se encuentran en la hemoglobina (hierro hemo, ver Figura 1), y un 3% hace parte de la mioglobina en el músculo. El hierro funcional restante se ubica en enzimas específicas de las células para la respiración celular (4).
El comportamiento único del hierro viene de la extrema variabilidad de su potencial redox Fe2+/Fe3+, que puede ser finamente ajustado por los ligandos apropiados, de forma que el hierro puede abarcar casi todo el rango de potenciales redox, biológicamente significativo, que va desde -0.5 V a +0.6 V (7).
¿Qué factores afectan la absorción de hierro?
Hay dos fuentes mayores de hierro: el hierro hemo, que deriva de la hemoglobina y por tanto se encuentra en carnes y pescados, y el hierro no hemo que se encuentra también en productos animales y vegetales. Es importante considerar que estos últimos, por poseer un alto contenido de fosfatos o fitatos, pueden disminuir su absorción (5).
El hierro hemo es altamente biodisponible (de un 20 a un 30%), ya que se absorbe como metaloporfirina intacta a través de receptores hemo específicos, de alta afinidad, en la mucosa intestinal de borde de cepillo. Sin embargo, como molécula aislada es pobremente absorbido, probablemente porque tiende a formar polímeros macromoleculares entre sí. En cambio, como parte de la proteína hemoglobina, es bien absorbido ya que esta lo mantiene en su estado monomérico. Debe tenerse en cuenta que la biodisponibilidad del hierro puede verse disminuída cuando los alimentos que lo contienen son sometidos a tiempos de cocción prolongados (1).
El hierro no hemo está sujeto a factores intraluminares que pueden promover o inhibir su absorción; entre los principales promotores del hierro no hemo encontramos la carne, los ácidos orgánicos como el ácido ascórbico y los aniones el malato, citrato, lactato y tartrato. Como inhibidores del hierro no hemo se cuentan los polifenoles y fitatos presentes en el té, vegetales, legumbres y condimentos, además del calcio y el fósforo, que se cree forman con él complejos no biodisponibles. Pero la biodisponibilidad de hierro en la dieta se ve influenciada no solo por la presencia de inhibidores y promotores de la absorción, sino también por el pH intraluminar y la motilidad gástrica (1), en tal forma que sólo entre el 5 y 15% del hierro ingerido en los alimentos es absorbido bajo condiciones normales (6).
Hay que tener en cuenta que la absorción y almacenamiento de hierro en el organismo mantienen una relación recíproca. Cuando disminuye el hierro almacenado la absorción aumenta, de tal manera que ciertas condiciones fisiológicas que aumentan la actividad eritropoyética y utilizan las reservas del mineral, se relacionan con un aumento en su absorción, siempre y cuando haya fuentes que lo proporcionen en la dieta (1).
¿Cómo es captado el hierro a nivel gastrointestinal ?
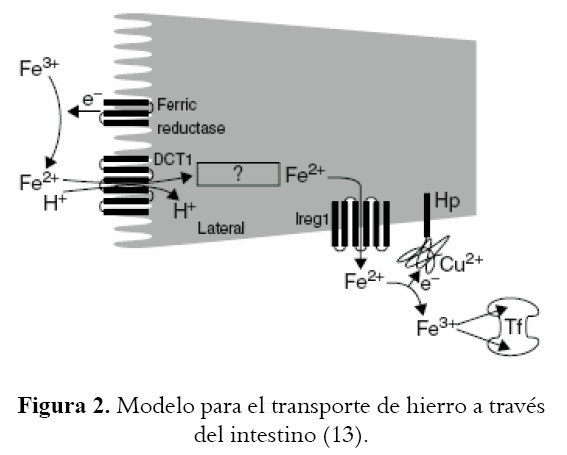
El hierro no hemo es captado después de su reducción por una enzima ferrirreductasa apical unida a la membrana del intestino y subsecuentemente transportado como Fe2+ por una proteína transportadora conocida como DCT1 o Nramp2 como se muestra en la figura 2.
La proteína DCT1 también se ha asociado con la captación rápida de hierro II de la mucosa intestinal, transportando no sólo este, sino otros metales divalentes. Esto genera que algunos metales compitan o saturen los sitios de unión, lo que sumado al control ejercido por la cantidad de hierro almacenado, las condiciones fisiológicas del individuo y la dieta, hace aún más variable la absorción de hierro por vía oral, conduciendo finalmente a la búsqueda de formas alternativas que mejoren o aseguren su absorción (1).
¿Cómo se sintetizan quelatos metálicos con ligandos orgánicos?
Consideraciones básicas:
En la formación de compuestos entre metales y moléculas orgánicas existen tres categorías:
• Complejos Metálicos
• Compuestos Quelato o Metal quelado
• Compuestos Organometálicos
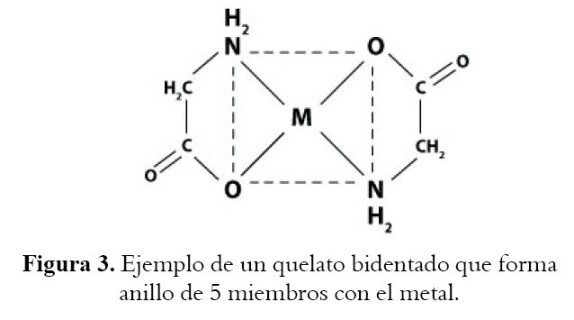
Cuando un ión metálico se combina con un donador de electrones, la sustancia resultante es un complejo o compuesto de coordinación; si el donador o agente complejante tiene dos o más grupos donadores, de manera que se forman uno o más anillos entre este y el metal, se forma un quelato (este puede ser bidentado, tridentado, etc. (Véase figura 3). De acuerdo con esto, casi todos los metales pueden formar complejos y quelatos, pero los agentes complejantes y quelantes se restringen a moléculas con elementos no metálicos de los grupos V y VI, comúnmente Nitrógeno, Oxígeno y Azufre.
Los compuestos organometálicos son sólo aquellos que involucran un enlace covalente entre el metal y el Carbono; tienen propiedades muy distintas a las de los complejos y quelatos metálicos y no se utilizan para suplementación oral de minerales; por tanto quedan fuera de la pertinencia y alcance de este artículo (9).
Formación y biodisponibilidad de los quelatos de hierro
Estudios con 14 preparaciones orales de hierro di- y trivalente, realizadas desde 1977, muestran una biodisponibilidad del 46 al 100% para las preparaciones divalentes y del 6 a 29% para las trivalentes. Considerando finalmente que las últimas deberían ser excluídas de cualquier terapia oral de hierro (10), esta revisión se centra en las preparaciones con Fe II. Estudios realizados en el 2001 reportan que ciertos ligandos orgánicos proporcionan enlaces con hierro lo suficientemente fuertes como para producir complejos o quelatos que resistan el rompimiento por la digestión, o los ataques de los inhibidores de su absorción y que, además, puedan ser captados por la mucosa, permitiendo la posterior utilización del metal (1).
Según el concepto HSAB (Hard-Soft Acid-Base) de R. G. Pearson, los ácidos y bases de Lewis se pueden categorizar como duros o suaves, de manera que una reacción procede generalmente en la dirección que pueda unir el ácido más duro con la base más dura y viceversa. Los iones metálicos se consideran ácidos duros si tienen alta densidad de carga, un pequeño radio iónico y electrones externos no fácilmente oxidables; lo contrario aplica para bases duras. El hierro en su estado de oxidación III, con una densidad de carga mayor a 200 Cmm-3, es considerado un ácido duro, mientras que en su estado de oxidación II, con una densidad de carga de aproximadamente 100 Cmm-3, se categoriza como intermedio, de manera que reacciona más favorablemente con bases suaves o intermedias (11, 12) La mayoría de los quelatos forman anillos de 5 ó 6 miembros; en general el anillo de 5 es más estable cuando está completamente saturado, pero el de 6 se favorece al haber uno o más dobles enlaces, como se muestra en la figura 3 (13).
En estos casos el número de coordinación más frecuentemente encontrado para el hierro II y el hierro III es de 6, originando una estereoquímica octahédrica para estos complejos (ver figura 1), aunque también se puede presentar una coordinación de 4 (tetrahédrica) y muy particularmente de 5 (trigonal bipiramidal o cuadrado piramidal) (11).
Rutas de síntesis
En solución, la hidrólisis de una sal metálica produce un primer complejo entre el metal y las moléculas de agua, estas forman la primera esfera de solvatación del metal. Durante la síntesis de un nuevo complejo o quelato las posiciones de las moléculas de agua serán desplazadas por los ligandos de interés. Por lo tanto, las principales rutas de síntesis de compuestos de coordinación son las reacciones de reemplazo de ligando, oxidación-reducción y reacciones de descomposición parcial (17). Sin embargo, la química de estos compuestos no es sencilla, dado que las reacciones que los generan están dirigidas por la entropía y no por la entalpía del sistema, lo que provoca que la distribución de los productos obtenidos sea función de la naturaleza del ligando, la estequiometría de los reactivos, el pH y el tiempo de la reacción (14), como lo demuestran estudios de especiación que profundizan en el tema (15).
En el caso del hierro II, es necesario mantener una atmósfera inerte sobre los reactivos durante la preparación de sus complejos para evitar la oxidación a hierro III, lo que puede lograrse empleando una cámara inerte con atmósfera de nitrógeno (16).
Constantes de estabilidad
Se ha llegado a la conclusión de que la constante de estabilidad del quelato debe ser lo suficientemente alta para permitirle atravesar el TGI con mínima hidrólisis, y lo suficientemente baja para que los ligandos citoplasmáticos puedan remover el hierro del quelato absorbido. El valor de esta constante para quelatos metal-aminoácido debe estar entre 4 y 6, lo cual garantiza la funcionalidad del quelato (4).
La fuerza de una constante está determinada por el número de miembros en los anillos del quelato, el número de anillos formados con el catión, la fuerza básica del enlace del ligando, el tamaño y carga del ligando, la naturaleza del metal, el efecto de resonancia del anillo y sus orientaciones estéricas. Algunos valores muestran que con un mismo ligando, la constante es mayor para los compuestos de hierro III que para los de hierro II, y que aumenta al aumentar la proporción metal:ligando (17).
Sacáridos como ligandos del hierro
Los sacáridos son considerados ligandos potenciales no sólo por su abundancia a nivel biológico, baja toxicidad y alta solubilidad, sino también por su funcionalidad multi-hidroxi y su ya bien definida estereoquímica para la coordinación con metales (18). Burger y Nagy han reportado la formación de complejos oligo-polinucleares de hierro con sacáridos simples y derivados (19).
De los monosacáridos, solamente la D-glucosa y la D-galactosa son absorbidos activamente en el intestino delgado. La D-fructosa no se absorbe activamente, pero tiene una velocidad de difusión mayor que la esperada para una difusión pasiva. Estos tres monosacáridos constituyen las mayores fuentes de energía de gran parte de las células de los mamíferos y los hace candidatos a agentes quelantes metálicos (20).
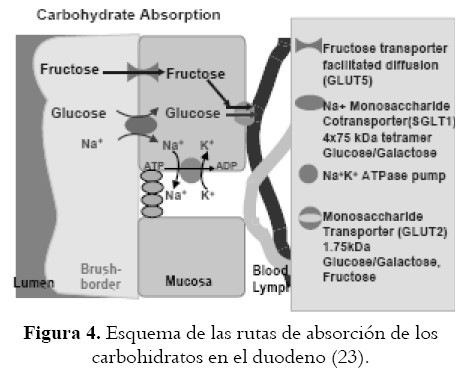
Los dos tipos de transportadores involucrados en la captación de carbohidratos a través de membranas son: los cotransportadores Na+/glucosa dependientes de sodio (SGLT) y los transportadores independientes de Sodio (GLUT) (21), siendo el transportador de glucosa SGLT1 el responsable del transporte activo de glucosa y galactosa junto con una cantidad equimolar de Sodio y contra un gradiente de concentración dentro del citoplasma del enterocito (ver figura 4) (22).
Los complejos de coordinación se forman en solución acuosa por el desplazamiento de las moléculas de agua de la esfera de solvatación que realizan los grupos –OH de los polioles, al parecer, por ser los sitios donadores más fuertes de los sacáridos. Para estos complejos se requieren al menos 3 grupos –OH en un ordenamiento estérico favorable, como el de una secuencia axial-ecuatorial-axial en un anillo de 6 miembros en conformación de silla (piranosa) o 3 átomos de oxígeno en 3 átomos de carbono consecutivos (cis-cis-cis) en un anillo de 5 miembros (furanosa) esta forma se obtienen complejos 1:1 entre ciclitoles y azúcares con cationes metálicos, en solventes polares. El tamaño y carga del catión parecen jugar roles vitales en la formación de complejos (24). Los alditioles y carbohidratos de cadena abierta con ordenamientos threo-threo de los grupos hidroxi, forman complejos más estables que los de ordenamientos eritro; la estabilidad relativamente baja de estos últimos refleja su poca capacidad donadora.
La carga del metal interviene en la estructura y estabilidad de este tipo de complejos especialmente en solventes polares, en los cuales los átomos de oxígeno donadores del carbohidrato tienen más dificultad para desplazar la esfera de solvatación de iones trivalentes que divalentes (24).
Los complejos de hierro con ligandos tipo azúcares ácidos son moléculas potenciales para uso farmacéutico, ya que su estabilidad es lo suficientemente alta para prevenir la hidrólisis del ión metálico en los sistemas biológicos. Cabe agregar que una de las funciones de los sacáridos a nivel fisiológico, es el transporte de iones metálicos a través de las membranas celulares. Por ejemplo, los polisacáridos extracelulares exhiben una extraordinaria habilidad complejante de cationes (25).
El ácido D-galactopiranosidurónico y el malato son algunos de los ligandos más promisorios en la terapia oral de hierro, pero la estabilidad relativa de los complejos con Fe III es mayor con el ácido D-Glucónico (25). Se ha reportado, además, que el gluconato ferroso causa mucho menos irritación gástrica que otras sales ferrosas inorgánicas comúnmente usadas, como el sulfato ferroso (8).
Resultados recientes sobre la composición y estructura de complejos Fe III con carbohidratos (aldosas, cetosas, polialcoholes, azucares ácidos, di y trisacáridos) indican que la naturaleza del ligando orgánico, el tipo de anión de la sal de hierro usada para la reacción (aunque no haga parte de la esfera de coordinación), incrementos en la proporción de los reactivos (ligando:hierro) y el pH, influencian la cantidad de especies de hierro que reaccionan, y pueden favorecer o no, la formación de centros aislados de hierro. Este comportamiento se puede explicar por el cambio en la actividad del agua en respuesta al cambio de anión de las soluciones concentradas (25).
Aminoácidos como ligandos del hierro
En estudios de Novell-Benjamin, (26) donde se compararon el sulfato, el bisglicinato y el trisglicinato ferroso, se encontró una mayor absorción con los dos últimos.
La absorción del hierro como quelato de aminoácido es mayor que su absorción como sal inorgánica, al parecer debido a que los aminoácidos lo protegen de reacciones químicas que pueden interferir con su absorción, reducen el potencial de irritabilidad gástrica al evitar que entre en contacto con la mucosa y aumentan su biodisponibilidad al utilizar rutas alternas de absorción, proporcionando un suministro rápido y seguro, lo que permite el uso de menores dosis para lograr resultados fisiológicos. Una vez absorbido en la mucosa, el quelato es hidrolizado y la liberación del hierro en el plasma y al resto de los tejidos es regulada como para cualquier otra fuente de hierro (4).
Los aminoácidos, con o sin ligar, son captados por un sistema de múltiples transportadores, entre los que se destacan los sistemas heterodiméricos HAT, y el sistema cotransportador,PAT, ubicados en las células epiteliales del borde de cepillo (21). El estudio de Amidon y cols. (27) sugiere que los derivados de glicina pueden ser absorbidos por mecanismos como la difusión pasiva, sin gasto de energía.
La producción de un quelato metal-aminoácido resulta de la reacción de una sal soluble de un ión metálico con un aminoácido, en una relación molar de un mol de metal con una a tres moles de aminoácido para formar enlaces covalentes coordinados (28). La estructura real del quelato dependerá de la relación molar metal:ligando y es generalmente de 1:2. En la reacción, el grupo carboxilo (COOH) forma un enlace iónico con el catión, mientras que el grupo a-amino (NH2) dona un par de electrones a un orbital d vacío del ión metálico, formando así el enlace covalente coordinado (29). Para producir un anillo estable de 5 miembros, cada ligando aminoácido forma dos enlaces con el hierro (30) siempre y cuando la reacción se dé a un pH por encima del punto isoeléctrico del aminoácido. Estos compuestos son suficientemente estables cuando se formulan apropiadamente y pueden ser absorbidos intactos en el intestino delgado de todos los mamíferos (31).
De acuerdo con la AAFCO (Association of American Feed Control Officials) el peso promedio del aminoácido hidrolizado debe ser aproximadamente 150 y el peso molecular del quelato no debe exceder 800 (32). Adicionalmente, para ser nutricionalmente funcional, el quelato debe tener una constante de estabilidad adecuada, presentar neutralidad eléctrica y su ligando debe ser fácilmente metabolizable por el organismo. El glicinato ferroso cumple todos estos requerimientos (33).
Algunos compuestos de metales y aminoácidos exhiben las siguientes propiedades especiales: Ausencia de reacciones químicas normales para los iones metálicos que contienen, diferencias en las propiedades de las formas a(alfa), ß y g(gamma), baja conductancia eléctrica, color característico; además, ha sido posible el aislamiento de ciertas sales internas del complejo (34).
Christensen y colaboradores (35) reportan los mayores efectos en la absorción de hierro con asparagina y glicina. Las constantes de estabilidad de estos complejos, aunque altas son apropiadas, en contraste con lo que ocurre con constantes de estabilidad extremadamente altas como la del complejo Fe-EDTA que, además de proteger al hierro de precipitar con fosfatos, impiden su absorción.
Los quelatos de glicina con cationes como hierro, zinc y cobre han sido ampliamente estudiados (36) y han demostrado disminuir la competencia entre los metales por el sitio de absorción, que se presenta cuando estos están en su forma inorgánica (37).
Ácidos carboxílicos de bajo peso molecular como ligandos de hierro
Los complejos puros metal-ácido pueden prepararse por precipitación de los hidróxidos o carbonatos del metal, lavando el precipitado de sales solubles, y disolviéndolo con las cantidades estequiométricas del ácido respectivo (7).
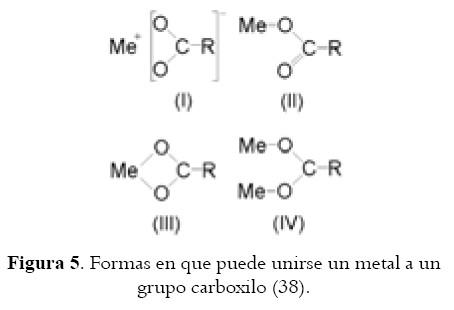
Se han establecido cuatro patrones de comportamiento para el ligando carboxilato, con base a determinaciones estructurales reales: iónico (I), bidentado (III) y bidentado puenteado (IV), que muestran cierta semejanza en el espectro infrarrojo (IR), y unidentado (II) que exhibe una marcada diferencia en el mismo espectro (ver figura 5) (38).
Ácidos como el cítrico, ascórbico, fumárico, láctico, succínico y málico, se han empleado para formar complejos monoméricos y solubles con hierro, previniendo su polimerización y por lo tanto promoviendo su absorción (39, 40).
El hierro III forma un complejo bidentado mononuclear con el ácido cítrico, y el hierro II forma con este un complejo tridentado, confirmado por estudios de RMN, según lo reportado por Francis y Dodge (41).
El ácido cítrico tiene tres protones fácilmente disociables de sus tres grupos carboxilato, y bajo ciertas condiciones también puede ser disociado el protón alcohólico. En medio ácido se pueden formar complejos entre el metal y los grupos carboxilo, mientras que en medio neutro o alcalino puede interaccionar tanto con los carboxilos como con los hidroxilos (42).
El ácido fumárico puede formar una sal de fumarato ferroso con el hierro. La literatura reporta su uso desde hace ya varias décadas, indicando que es muy estable a la oxidación o hidratación, terapéuticamente equivalente al gluconato ferroso y al sulfato ferroso como hematínico y bien tolerado por los pacientes (7).
¿Cómo se pueden caracterizar los complejos metal-ligando?
Métodos comunes:
La caracterización cuantitativa de complejos metálicos con ligando tipo azúcar es difícil cuando se presentan en solución, dada la baja estabilidad de los complejos en medio ácido o neutro, la presencia de equilibrio anomérico y conformacional y las diferentes interacciones de los isómeros con el metal (25).
La formación de quelatos entre iones metálicos con la forma ácida de los ligandos, resulta en una disminución del pH, la cual es mayor a medida que aumenta la unión entre ellos, de tal forma que la medición del pH en solución acuosa constituye un método para determinar las constantes de estabilidad de los complejos formados (13).
Entre los métodos de caracterización de complejos metal-ligando, se encuentran:
- Constantes de equilibrio: pH-métricos, espectrofotométricos y electro-químicos
- Estructurales: NMR, FTIR, EPR, Mössbauer, Difracción de Rayos X y EXAFS
- Susceptibilidad magnética
A continuación se explican brevemente los principios de algunas de estas técnicas.
Susceptibilidad Magnética
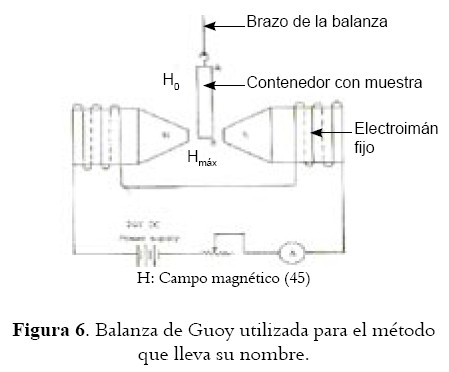
La susceptibilidad magnética es un fenómeno que se produce cuando se induce un momento magnético en un objeto al aplicarle un campo magnético no homogéneo; se determina por el método de Guoy, que consiste en empacar la muestra en un cilindro de vidrio y suspenderla del brazo de una balanza, de forma que su extremo inferior quede entre los polos de un electroimán (ver figura 6). El tubo con la muestra y la cadena que lo soporta se pesan en ausencia del campo magnético y luego bajo la influencia de este. Al ser el campo, máximo en la parte inferior y mínimo en la parte superior (campo no homogéneo), se produce una fuerza descendente, que se mide como el peso requerido para restablecer el equilibrio. El efecto físico del paramagnetismo es una atracción hacia la fuente del magnetismo. Se emplean patrones de comparación como el FeSO4(NH4)2 (43).
El paramagnetismo puede deberse a dos causas: una es el campo magnético asociado con el spin del electrón y la otra es el campo asociado con el movimiento del electrón en su orbital; ambos se suman para cada electrón desapareado; por tanto, toda especie paramagnética tiene un momento magnético asociado; en cambio, los átomos que tienen todos sus electrones apareados, tienen un momento magnético nulo (43). Esta técnica puede ser usada en la caracterización de los compuestos a los que hace referencia este artículo, ya que el grado de paramagnetismo de la sustancia depende no sólo del tipo de metal, sino también de su estado de oxidación, su estereoquímica y la naturaleza del ligando. Un ejemplo de su aplicabilidad puede apreciarse en el trabajo de Raman y cols. con complejos de cobre, niquel, manganeso y zinc (44).
EXAFS (Extended X-Ray Absorption Fine Structure)
Mediante esta técnica pueden ser determinados el número y especies de los átomos vecinos, su distancia del átomo seleccionado y el desorden térmico o estructural de sus posiciones. El análisis puede ser aplicado a materiales cristalinos, nanoestructurales o amorfos, líquidos y gases moleculares. EXAFS es en general, la única forma de estudiar el ordenamiento de átomos en materiales sin un gran ordenamiento, donde las técnicas de difracción tradicional no pueden ser usadas (46).
La absorción de Rayos X puede medirse por la atenuación del paso de los rayos X a través del material. Cuando la energía fotónica de los rayos es sintonizada con la energía de enlace de algún nivel nuclear de un átomo en el material, se da un incremento abrupto en el coeficiente de absorción conocido como el límite de absorción. Para átomos en una molécula o en una fase condensada, la variación de este coeficiente en energías por encima del límite de absorción muestra una estructura fina conocida como EXAFS. Con esta técnica se obtiene la función de distribución radial centrada en el absorbente, que involucra sólo pares de átomos formados por él y los otros átomos, proporcionando información estructural local muy específica sin importar la organización del material (cristalina, amorfa o en solución) (24). Un ejemplo lo constituyen los estudios de K. Geetha y colaboradores donde, mediante caracterización por EXAFS sugieren la formación de complejos metal-sacárido bidentados a través de los grupos OH (47).
Espectroscopia Mössbauer
Esta técnica mide la absorción de rayos gamma por los átomos de un sólido como función de la energía de la radiación (por cambios en la velocidad de la fuente). A velocidades correspondientes a los niveles de energía resonante de la muestra, algunos rayos son absorbidos, dando como resultados una caída de la intensidad medida. El espectro provee información sobre el ambiente químico del núcleo absorbente y puede usarse para caracterizar la muestra.
Los rayos gamma deben ser de la energía apropiada para que se den las transiciones nucleares; además, la energía de la radiación debe ser relativamente baja, o si no el sistema tendrá una baja fracción de retroceso, que tiene como resultado una señal pobre. Sólo existen unos pocos isótopos elementales para los cuales se cumple este criterio, por lo cual la espectroscopia Mossbauer sólo puede ser aplicada a un grupo relativamente pequeño de átomos, incluyendo: 57Co, 57Fe (el más comúnmente usado), 129I, 119Sn, 121Sb (48).
Para biomoléculas que contienen hierro, esta técnica provee un poderoso medio para identificar el estado del spin, estado de oxidación, sitio de simetría del sitio del Fe, número de coordinación y tipo de ligando, a través de la medición de las interacciones hiperfinas del núcleo 57Fe y los electrones de su entorno (49). Nagy y Burger (1.986), en un estudio con complejos metal-sacárido, muestran la interacción antiferromagnética entre los centros de hierro III, por lo que sugieren la presencia de estructuras diméricas u oligoméricas, gracias a la espectroscopia Mossbauer (50). El conocimiento de los estados químicos del hierro es de gran importancia para determinar su efecto y/o toxicidad en compuestos farmacéuticos como suplementos dietarios y multivitamínicos (51).
EPR (Electrón Spin Resonance Spectroscopy)
Cuando un átomo o molécula con un electrón desapareado se ubica en un campo magnético, el spin del electrón desapareado puede alinearse en la misma dirección o en la dirección opuesta al campo impuesto. EPR mide la absorción de la radiación de microondas por un electrón desapareado, cuando este es colocado en un fuerte campo magnético.
Además de un magnetismo conferido por su spin intrínseco, un electrón puede adquirir magnetismo del movimiento orbital. Adicionalmente hay un magnetismo que proviene de los protones del núcleo, estos tienen el mismo momento angular de spin que el electrón, pero debido a que la masa del núcleo; es mucho mayor, su momento magnético es mucho menor y esto no permite el estudio del paramagnetismo por NMR. El fenómeno de resonancia para electrones ocurre a frecuencias miles de veces mayores que las usadas en NMR, debido a que la masa de un electrón es miles de veces menor que la del núcleo. El ancho y estructura de las curvas de absorción de resonancia en EPR, se deben al ambiente atómico del electrón y pueden ser usadas para estudiar la naturaleza del centro involucrado.
Entre las especies con electrón desapareado están los radicales libres, complejos de metales de transición, iones lantánidos, moléculas con electrones impares y moléculas en estado triplete (52). Se han reportado estudios de complejos metal-sacárido en los cuales esta técnica ha permitido identificar la presencia de centros aislados o especies polinucleares interactuantes de hierro, complementando el análisis de estas estructuras (53).
¿Que interacciones presenta el hierro con otros componentes de la dieta?
Antagonismo
Hierro y cobre: Normalmente el hierro iónico y el cobre iónico antagonizan en el intestino delgado, donde un alto nivel dietario de alguno de los dos, reduce la absorción del otro (54-59). Este antagonismo se manifiesta en una disminución en los valores de hemoglobina (60).
Un estudio doble ciego con 30 adultos voluntarios sanos, concluyó que cuando el hierro y el cobre se ingieren a la vez, en la forma de quelatos de aminoácido, no hay cambios significativos en los niveles de hemoglobina, es decir que no hay competencia antagonista entre ellos durante su absorción intestinal. Este mismo estudio mostró que la absorción neta promedio de hierro dentro de la mucosa es 4.7 a 7.2 veces mayor para el quelato de aminoácido que para las sales inorgánicas del metal (4).
Hierro y zinc: La deficiencia de zinc está asociada con disminución del crecimiento, pérdida de apetito, lesiones en la piel, hipogonadismo, maduración sexual lenta y curación de heridas y respuesta inmune deteriorada (61). Las formas altamente biodisponibles de hierro y zinc provienen de fuentes animales, pero la competencia por la absorción entre ellos en las paredes celulares de la mucosa puede producir la inhibición de la captación de uno y otro (61-63). En un estudio realizado por Christian y colaboradores (64), no se halla evidencia de antagonismo cuando se consumen dosis de hierro:zinc en relación de 2:1; Solomons reporta que en una proporción Fe:Zn mayor de 2:1 el hierro inhibe la captación de zinc, mientras que un alto consumo de zinc puede llevar a una pobre absorción de hierro (65, 66). Otros estudios reportan que una cantidad de hierro total superior a 25 mg puede afectar la absorción de zinc, por lo que se recomienda no ingerir suplementos de este mineral con las comidas (61).
Hay que tener en cuenta que estudios recientes muestran que alimentos fortificados con hierro en los niveles normales, no tienen efectos adversos a nivel gástrico sobre la absorción de zinc (31).
Agonismo
Ácido fólico: El metabolismo de estos nutrientes está íntimamente conectado. Una deficiencia de folato causa replicación celular anormal, particularmente en el sistema eritropoyético y produce anemia megaloblástica. Primero hay disminución de la concentración de folato en suero, luego disminuye la concentración de folato en el eritrocito y aumenta la de homocisteína, (67) debido a que el folato no puede cumplir su función de metilación para convertir la homocisteína en metionina, entonces baja la concentración de S-adenosilmetionina, el principal donador de metilos para el DNA. La hipometilación del DNA puede cambiar la expresión genética e incrementar el número de rompimientos de las cadenas de DNA. El folato también interviene de la misma manera en la formación de timidilato, su deficiencia cambia el balance de precursores de DNA y puede generar una incorporación de uridina en vez de timidina en el DNA, es entonces cuando, por repetidos intentos de reparar enzimas para sacar el uracilo, puede desestabilizarse el DNA rompiéndose las cadenas y generando aberraciones cromosómicas y transformaciones malignas.
Se reporta la asociación inversa del uso de suplementación de hierro y folato en el embarazo con el riesgo de leucemia linfoblástica aguda, cáncer más común entre los niños de países más desarrollados (68).
Un estudio reciente en México, para comparar el efecto de la suplementación oral con hierro solamente y de hierro con folato en casos de anemia por deficiencia de hierro, con más de 300 mujeres gestantes entre la 14 y 27ª semana de embarazo, mostró que la terapia combinada de hierro y folato aumentaba los niveles de hemoglobina, independientemente de los niveles basales de hierro en sangre, ferritina y folato en suero, y fue más evidente en mujeres con anemia más severa; por esto se recomienda su uso concomitante (69).
Recomendaciones para la investigación
Es de gran relevancia que para la síntesis de compuestos tipo metal quelato, se tengan en cuenta los requisitos citados para que sean nutricionalmente funcionales. Además, es necesaria la medición de su constante de estabilidad como un requisito de calidad, ya que esta proporciona el rango de pH en el que el complejo es estable. Al respecto faltan aún estudios concluyentes.
Esta revisión muestra cómo los ligandos orgánicos pueden ser usados no solo para quelar hierro, sino que son aptos para quelar otro tipo de metales.
Otro aspecto que se debe tener en cuenta es la necesidad en nuestro medio de la adquisición de nuevas tecnologías para la caracterización y el estudio de los complejos y quelatos metálicos, dado el enorme potencial que poseen y la convivencia permanente del hombre con la necesidad de minerales, pues en la vida moderna se requiere en muchos casos de su suplementación para prevenir o curar enfermedades causadas por su déficit.
Recomendaciones para la salud pública
Los complejos y quelatos de hierro con ligandos orgánicos como aminoácidos, sacáridos y ácidos carboxílicos de bajo peso molecular, son una excelente alternativa para formular suplementos alimenticios o terapias en pro de reestablecer los niveles normales de este metal en el organismo, ya que permiten su administración concomitante con otros metales, reduciendo la competencia por el sitio de absorción y la quelación por parte de otros componentes presentes en la dieta. Además, es una alternativa segura y eficaz, ya que reduce de manera notoria los efectos adversos que producen sus sales inorgánicas a nivel gástrico, lo que favorece el cumplimiento de la terapia.
Se recomienda que la suplementación oral de hierro esté acompañada asimismo de suplementación en ácido fólico, especialmente durante el embarazo.
REFERENCIAS BIBLIOGRAFICAS
1. Crichton, Robert. (2001) Inorganic biochemistry of iron metabolism: from molecular mechanisms to clinical consecuences 2 (Ed) Jhon Whiley & Sons Ltd. England [ Links ]
2. Benny Kodyat, Soewarta Kosen and Saskia de Pee. (1998) Iron deficiency in Indonesia: Current situation and intervention. Nutrition Research. 18 (12) : 1953-1963[ [ Links ]STANDARDIZEDENDPARAG]
3. Eichholzer, Monika. (2003) Micronutrient deficiencies in Switzerland: causes and consecuences. J. of Food Engineering (56) : 171-179. [ Links ]
4. H. DeWayne Ashmead. (2001) The absorption and metabolism of iron amino acid chelate. Albion Laboratories, Inc. Clearfield, Utah U.S.A. ALAN 51 supl. 1 (1) : 13-21. [ Links ]
5. Martindale : The complete drug reference. (1999) 32. ed. The Pharmaceutical Press, USA. p 1346-1347 [ Links ]
6. http://ods.od.nih.gov/factsheets/iron.asp Abril de 2.005
7. Roger, Charles. (1961) Inorganic Pharmaceutical chemistry 7th Ed. Lea & Febige. Filadelfia. USA. [ Links ]
8. http://www.chemguide.co.uk/inorganic/complexions/shapes.html#top Abril de 2.005
9. Martell, Arthur. (1956) Chemistry of the Metal Chelate compounds. Prentice Hall, Inc. N. J.. p. 1. [ Links ]
10. Dietzfelbinger H. (1987) Bioavailability of bi- and trivalent oral iron preparations. Investigations of iron absorption by postabsorption serum iron concentrations curves. Arzneimittelforschung. Jan., 37 (1A) : 107-12. [ Links ]
11. Rayner-Canham, Geoff; Overton, Tina. (2003) Descriptive Inorganic Chemistry. Third edition. W. H. Freeman and Company. USA. [ Links ]
12. JEPPSEN, Robert. (2001) Toxicology and safety of Ferrochel and other iron amino acid chelates. ALAN. Mar., 51 (1 Suppl 1) : 26-34. [ Links ]
13. Martell, A; Calvin, M. (1952) Química de los compuestos metálicos quelatos. (Ed) Prentice Hall. New York. [ Links ]
14. Steinborn, Dirk and Junicke, Henrik. (2000) Carbohydrate complexes of Platimum group Metals. Chem. Rev. (100) : 4283-4317. [ Links ]
15. Yaman, M; Kaya, G. (2005) Speciation of iron (II) and (III) by using solvent extraction and flame atomic absorption spectrometry. Analytica Chimica Acta. (540) : 77-81[ [ Links ]STANDARDIZEDENDPARAG]
16. Pérez M., L. J. (2005) Quelatos orgánicos de hierro para administración oral: Síntesis, identificación y análisis de imagen de partículas. Trabajo de Maestría. Fac. de Química Farmacéutica. U. de A. Medellín, Colombia. [ Links ]
17. Chaberek S & AE Martell. (1959) Organic Sequestering Agents. NY, John Wiley & Sons. [ Links ]
18. Rao, C. et al. (2000) Transition metal saccharide chemistry and biology: syntheses, characterization, solution stability and putative bio-relevant studies of iron saccharide complexes. Inorganica Chimica Acta. (297) : 373-382. [ Links ]
19. Burger, K et al. (1983) A novel polynuclear iron (III) mixed ligand complex for use in parenteral iron therapy. Inorg. Chim. Acta (80) : 231-235[ [ Links ]STANDARDIZEDENDPARAG]
20. http://www.fao.org/docrep/w8079e/w8079e0k.htm Marzo de 2005.
21. Steffansen, Bente el al. (2004) Intestinal solute carriers: an overview of trends and strategies for improving oral drug absorption. European Journal of Pharmaceutical Sciences (21) : 3-16 [ Links ]
22. http://www.fao.org/docrep/w8079e/w8079e0k.htm Marzo de 2005. (ver referencia 29)
23. Devlin, T. (1997) Textbook of Biochemistry With Clinical Correlations, Fourth Edition. Ed. Wiley-Liss Inc. Section 26. [ Links ]
24. Nagy, L; Szorcsik, A. (2002) Equilibrium and structural studies on metal complexes of carbohydrates and their derivatives. J. of Inorganic Biochemistry (89) : 1-12[ [ Links ]STANDARDIZEDENDPARAG]
25. Gyurcsik, B; Nagy, L. Carbohydrates as ligands: coordination equilibria and structure of the metal complexes. Coordination chemistry reviews 203 (2000) 81-149[ [ Links ]STANDARDIZEDENDPARAG]
26. Nove11-Benjamin, AC, FE Viteri & LH Al1en. (2000) Iron absorption from ferrous bisg1ycinate and ferric trisg1ycinate in whole maize is regu1ated by iron status. Amer J C1in Nutr. (71) : 1563-1569. [ Links ]
27. Amidon, L et al. (1982) Intestinal Absorption of Amino Acid Derivatives: Importance of the Free a-Amino Group. J. of Pharm. Sci. 10 (71) : 1138-1141. [ Links ]
28. www.zinpro.com Noviembre 2004.
29. Bailar JC, et al. (1984). Chemistry. Orlando, FL, Acadernic Press, p. 223. [ Links ]
30. Bell CF. (1977) Principles and Application of Metal Chelation. Oxford, Clarendon Press, p 17-18. [ Links ]
31. Davidsson, L. et al. (1995) Br. J. Nutr. Zinc absorption in adult humans: the effect of iron fortification.; 74 pp 417-25. [ Links ]
32. US PATENT 6,518,240 Feb. 11, 2.003
33. Ashmead, Stephen D. (2001) The chemistry of ferrous bis-glycinate chelate. ALAN 51 (1 supl 1) : 7-12[ [ Links ]STANDARDIZEDENDPARAG]
34. Martell, A; Calvin, M. (1952) Química de los compuestos metálicos quelatos. Prentice Hall. New York. [ Links ]
35 CHRISTENSEN, J et al. (1984) Effects of Divalent Amino Acids on Iron Absorption. J. of Pharm. Sci. 73 ( 9) : 1245-1248[ [ Links ]STANDARDIZEDENDPARAG]
36. Ashmead HD, DJ Graff & HH Ashmead. (1985) Intestinal Absorption of Metal Ions and Che1ates. Springfie1d, IL, Charles C Thomas. [ Links ]
37. Solomons, N. W. and Jacobs, R. (1981) Studies on the bioavailability of zinc in humans: effects of heme and nonheme iron on the absorption of zinc. AJCN (34) : 475-487. [ Links ]
38. Palacios, E. G. (2004) Infrared spectroscopy of metal carboxylates II. Analysis of Fe III, Ni and Zn carboxylate solutions . Hydrometallurgy (72) : 139-148. [ Links ]
39. A. K. Nikumbh, M. M. Phadke and A. A. Latkar. (1994) Mössbauer spectroscopic and direct current electrical conductivity study of some iron (II) dicarboxylates. Journal of Magnetism and Magnetic Materials 131 (1-2) : 189-198[ [ Links ]STANDARDIZEDENDPARAG]
40. Harmon B. Abrahamson, Ahmad B. Rezvani1 and J. George Brushmiller. (1994) Photochemical and spectroscopic studies of complexes, of iron(III) with citric acid and other carboxylic acids. Inorganica Chimica Acta. 226, (1-2): 117-127[ [ Links ]STANDARDIZEDENDPARAG]
41. Francis, A. J. And Dodge, C. J. (1993) Influence of complex structure on the biodegradation of iron-citrate complexes. Applied and environmental microbiology 1 (59): 109-113. [ Links ]
42. Konigsberger, Lan-Chi et al. (2000) Complexation of iron (III) and iron (II) by citrate. Implications for iron speciation in blood plasma. J. of Inorg. Biochem. (78) : 175-184[ [ Links ]STANDARDIZEDENDPARAG]
43. Larsen, Edwin. (1972) Elementos de transición. Reverté S.A. Barcelona p 22-23[ [ Links ]STANDARDIZEDENDPARAG]
44. Raman, N et al. (2001) Synthesis and characterization of Cu, Ni, Mn, Zn and VO Schiff base complexes derived from o-phenylenediamine and acetoacetanilide. Proc. Indian Acad. Sci (Chem. Sci.), 113 (3): 183-189. [ Links ]
45. http://physics.iitm.ernet.in/courses/gplab03_odd/Guoy.htm Octubre de 2.005
46. http://www.p-ng.si/~arcon/xas/exafs/exafs.htm Octubre de 2.005
47. K. Geetha, (1995) Transition-Metal saccharide chemistry: Síntesis, spectroscopy, electrochemistry and magnetic susceptibility studies of iron (III) compounds. Carbohydr. Res. (271) : 163-175. [ Links ]
48. http://encyclopedia.laborlawtalk.com/Mossbauer_spectroscopy Octubre de 2.005
49. http://www.uga.edu/cms/Moss.html Febrero 2005.
50. Nagy L, Burger K. (1986) Iron III complexes of sugar-type ligands. Inorg. Chimica Acta. 1 (124) : 55-59. [ Links ]
51. Oschtrakh M.L., Milder O.B., Semionkin V.A. (2004) Analysis of the iron containing vitamins and dietary supplements by Mossbauer spectroscopy. Analytica Chimica Acta (506) : 155-160. [ Links ]
52. www.chemistry.adelaide.edu.au/external/soc-rel/content/epr.htm Diciembre de 2.004
53. Nagy, L; Szorcsik, A. (2002) Equilibrium and structural studies on metal complexes of carbohydrates and their derivatives. J. of Inorganic Biochemistry, 89. (ver referencia 33) [ Links ]
54. Cuser WO & A Resurrecion. (1982) Influence of copper, zinc, and protein on biological response to dietary iron. Nutritional Bioavailability of Iron. Washington, DC, American Chemical Society , p 97. [ Links ]
55. Greger JL, ML Storey, JL Stahl, ME Cook, SE Gentry-Roberts & JC Lynds. (1988) Zinc, iron and copper interactions in humans, rats, and chicks. En: Trace Elements in Man and Animals. LS Hurley, CL Keen, B Lonnerdal & RB Rucker. (Eds.) NY, Plenum Press, , p 231-232. [ Links ]
56. Howell JM & JM Gaiothoma. (1987) Copper in Animals and Man. Boca Raton, FL, (Ed) CRC Press, Vol. VI, p 90. [ Links ]
57. O'Dell, B. Copper and zinc in poultry nutrition. (1979) Copper and Zinc in Poultry, Swine and Ruminant Nutrition. (Ed) Miller & WJ Mil. West Des Moines IA NFIA p 5. [ Links ]
58. Bezkorovainy, A. (1980). Biochemistry of Nonheme Iron. Ed Plenum. N.Y. p 5. [ Links ]
59. El-Shobaki FA & W Rummel. (1979) Binding of copper to mucosal transferrin and inhibition of intestinal iron absorption in rats. Res Exp Med (174) : 187-195. [ Links ]
60. Grassman E & M Kirchgessner. (1981) On the metabolic availability of absorbed copper and iron. En: Trace Element Metabolism in Man and Animals. Canberra City, Australia Academy of Science p. 593. [ Links ]
61. Solomons, N.W. (1986) Competitive interaction of iron and zinc in the diet: consecuences for human nutrition. J. Nutr. (116) : 927-35[ [ Links ]STANDARDIZEDENDPARAG]
62. Solomons N.W. RUZ M. (1997) Zinc and iron interaction: concepts and perspectives in the developing word. Nutr. Res. (17) : 177-85. [ Links ]
63. Whitaker P. (1998) Iron and zinc interactions in humans. Am. J. Clin. Nutr. (68) : 442S-446S[ [ Links ]STANDARDIZEDENDPARAG]
64. Christian, P et al. (2001) Iron and zinc interactions among pregnant Nepali women. Nutrition research (21) : 141-148. [ Links ]
65. Crofton, R. W. et al. (1989) Inorganic zinc and the intestinal absorption of ferrous iron. Am. J. Clin. Nutr. (5) : 141-144. [ Links ]
66. Rossander-Hulten L et al. (1991) Competitive inhibition of iron absorption by manganese and zinc in humans. Am. J. Clin. Nutr. (54) : 152-156. [ Links ]
67. Lukaski, Henry. (2004) Vitamin and mineral status : effects on physical performance. Nutrition (20) : 632-644. [ Links ]
68. Thompson, Judith ; Fitz Patrick ; Willoughby Michael and Armstrong Bruce. (2001) Maternal folate supplementation in pregnancy and protection against acute lymphoblastic leukaemia in childhood : a case-control study. Lancet (358) : 1935-1940. [ Links ]
69. Juarez, J. Bonizzonni E., Scotti, A. (2002) Iron plus folate is more effective than iron alone in the treatment of iron deficiency anaemia in pregnancy : a randomised, double blind clinical trial. BJOG : An intern. J. Of Obstetrics an gynaecology. 9 ( 109) : 1009-1014. [ Links ]