Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Med
Print version ISSN 0121-5256On-line version ISSN 1909-7700
rev.fac.med vol.16 no.1 Bogotá Jan./June 2008
PRÁCTICA CLÍNICA
NEUMONIA CRIPTOGÉNICA ORGANIZADA CAVITADA Y ANORMALIDADES DE LOS GANGLIOS BASALES: PRESENTACION DE UN CASO
CAVITARY CRYPTOGENIC ORGANIZED PNEUMONIA AND ABNORMALITIES OF THE BASAL GANGLIA: CASE REPORT
NEUMONIA CRIPTOGÉNICA ORGANIZADA CAVITADA E ANORMALIDADES DOS GÂNGLIOS BASAIS. PRESENTACION DE UM CASO
SERGIO MORAa, c*, ENRIQUE PRIETOa Y JULLY MARIANA SÁNCHEZb
a Hospital de la Samaritana, Bogotá, D.C., Colombia.
b Servicio de Medicina Interna, Hospital de San Ignacio, Pontificia Universidad Javeriana, Bogotá, D.C., Colombia.
c Servicio de Reumatología, Hospital Militar Central, Bogotá, D.C., Colombia.
* Correspondencia: sergiomora3@yahoo.com. Dirección postal: Servicio de Reumatología, Hospital Militar Central. Tr. 3 N° 49-00. Bogotá, D.C., Colombia.
Recibido: Octubre 1 de 2007. Aceptado: Octubre 31 de 2007.
Resumen
La neumonía criptogénica organizada (NCO) es una enfermedad pulmonar con un amplio espectro de características radiológicas. Se presenta el caso de una paciente de 16 años con aparición en una TAC de múltiples nódulos cavitados en ambos pulmones, que respondió con completa resolución luego de terapia con corticosteroides. La paciente también presentó anormalidades en los ganglios basales, como resultado de encefalopatía hipóxico isquémica asociada a la presentación aguda de la entidad. Se justifica la inclusión de NCO en el diagnóstico diferencial de múltiples nódulos cavitados y se discuten los diagnósticos diferenciales de las anormalidades a nivel de los ganglios basales.
Palabras clave: Neumonía, ganglios basales.
Abstract
Cryptogenic Organizing Pneumonia (COP) is a pulmonary disorder with a wide spectrum of radiological features. A case of a young patient, 16 years old is shown with a CAT appearance of multiple cavitary nodules in both lungs that responded with a complete resolution after corticosteroid therapy. This patient also reveals abnormalities of the basal ganglia as the result of hypoxic ischemic encephalopathy associated with the acute presentation of this disorder.
Key words: Pneumonia, basal ganglia.
Resumo
A pneumonia criptogénica organizada (NCO) é uma doença pulmonar com um amplo espectro de características radiológicas. Apresenta-se o caso de uma paciente de 16 anos com aparição em TAC de múltiplas nódulos cavitados em ambos pulmões, que respondeu com completa resolução depois de terapia com corticosteroides. A paciente também apresentou anormalidades nos gânglios da base, como resultado de encefalopatia hipóxico isquémica associada à apresentação aguda da entidade. Justifica-se a inclusão de NCO no diagnóstico diferencial de múltiplos nódulos cavitados e se discutem os diagnósticos diferenciais das anormalidades no nível dos gânglios da base.
Palavras-chave: Pneumonia, gânglios da base.
Presentación del caso
Paciente femenina de 16 años de edad, natural y procedente de Cota (Cundinamarca), estudiante de bachillerato y remitida de la unidad de cuidados intensivos del Hospital de Zipaquirá. Consultó inicialmente por un cuadro de dos días de evolución de astenia, adinamia, hipertermia subjetiva no cuantificada, dolor torácico generalizado tipo opresivo, sin irradiación y en ocasiones exacerbado con la inspiración y sin disautonomías asociadas. Al segundo día refiere, con el cuadro inicial, tos hemoptoica en dos oportunidades. No hay asociación a consumo de medicamentos, no se observan lesiones en piel, no se presentan síntomas intestinales, la diuresis y deposición son normales, ausencia de síntomas respiratorios superiores y tampoco hay exposiciones o contactos con agentes determinados. Ingresa al hospital local con SDR severo, en falla ventilatoria y con hipoxemia, requiriendo IOT, sedación y relajación. Por el tubo orotraqueal se evidencia secreción hemoptoica, de las cuales se toman muestras, requiere de soporte inotrópico, se le realiza paso de catéter central y se remite al centro de tercer nivel de atención.
Antecedentes: Desarrollo psicomotor adecuado; escolaridad y curso adecuados; antecedentes patológicos negativos; neonatales negativos; familiares negativos; farmacológicos negativos, toxicoalérgicos negativos; ambientales negativos; ginecobstétricos: G0A0V0.FUR: 5/junio/2006, Ciclos: 30x 5días, regulares; vida sexual aún no iniciada y contactos negativos.
Revisión por sistemas: Clase funcional previa I/IV, no pérdida de peso, no síntomas B, no alteraciones en hábito urinario y/o intestinal, niega previa tos, ortopnea o disnea paroxística nocturna.
Examen físico: Ingresa en malas condiciones generales, con soporte ventilatorio, soporte inotrópico y con sonda vesical. FC: 90 x FR: 14x, T/A: 150/100 mmHg, T: 37 ºC. C/C: Conjuntivas pálidas, mucosas semisecas, no IY a 45 grados, sin tinte ictérico escleral, sin lesiones en cavidad oral y sin lesiones faciales. C/P: ruidos cardiacos rítmicos, no soplos, no reforzamientos, no desdoblamientos, ruidos respiratorios: estertores gruesos en 2/3 de ambos campos pulmonares, con disminución de murmullo vesicular comparativamente campo derecho, gran enfisema subcutáneo en cuello y hemitórax derecho, no tirajes. Abdomen blando, sin irritación peritoneal ni visceromegalias. Las extremidades sin edema, no hipocratismo digital, llenado capilar dos segundos. Bajo efectos de la sedación, pupilas isocóricas normorreactivas a la luz y acomodación, sin desviación de comisura labial, corneano (+), oculocefalógiros (+), nauseoso (+), no Hoffman, respuesta plantar flexora bilateral, Sin rigidez nucal, sin signos meníngeos y sin movimientos anormales. En las tablas 1 y 2 se pueden observar los valores del cuadro hemático y de los paraclínicos desde su ingreso. El parcial de orina reportó 100 mg/dl de proteinas y 200 eritrocitos/ul sangre y el sedimento urinario de 14-16 cilindros granulosos y más de 100 hematíes.
Gases arteriales del sitio de remisión: Ph: 7,40; PCO2: 36,2; HCO3:3:21; PO2: 46 Sat: 81%. Gases arteriales de ingreso a la institución: Ph: 7, 26; PO1: 52,4; PCO2: 48; HCO3: 23,3; Sat: 82%
Rx de tórax portátil del (22/06/06): silueta cardiaca de tamaño, forma y configuración habitual; se observan múltiples infiltrados de predominio alveolar localizados hacia las bases y hacia el segmento apical del campo pulmonar derecho. Ángulos costofrénicos libres y cámara de neumotórax en el ápice pulmonar derecho del 10%.
Se la consideró como paciente joven con falla respiratoria hipoxémica de origen agudo, con Rx de tórax inicial sugestiva de síndrome de dificultad respiratoria aguda (SDRA), imagen de neumomediastino asociado a paso de catéter central. No se descartó proceso infeccioso asociado, por lo que se inició cubrimiento antibiótico de amplio espectro y se planteó la posibilidad de Síndrome Riñón-Pulmón, por lo que se iniciaron esteroides IV. Se valoró por el grupo de neumología (30/06/06), quienes encontraron un paciente anémico, con adecuada función l, parcial de orina con hematuria y proteinuria. Se solicitó TAC de tórax que evidenció múltiples nódulos, masas cavitadas, difusas bilaterales y mejoría de extensas zonas iniciales de consolidación (Figura 1). Se consideró neumotórax de causa iatrogénica, manejado con toracostomía cerrada, planteándose como posibles diagnósticos:
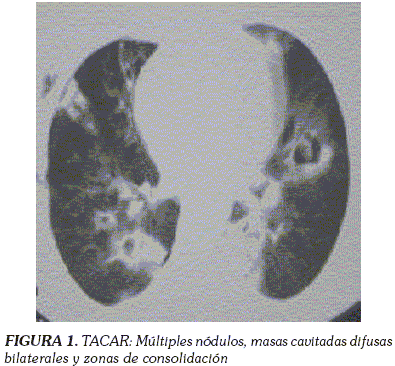
1. Insuficiencia respiratoria aguda; 2. Síndrome Pulmón-Riñón; 3. Granulomatosis de Wegener; 4. Síndrome Goodpasture; 5. Síndrome de Churg-Strauss; 6. Conectivopatía (LES ¿???); 7. SDRA.
La paciente presentó durante su hospitalización (30/06/06) en UCI una marcada disminución de la fuerza muscular de manera simétrica en miembros superiores e inferiores, con hallazgos positivos: disartria marcada, bradipsiquia, alucinaciones visuales, Babinsky bilateral de predominio derecho, fuerza 4/5 simétrica miembros superiores e inferiores. Se consideró síndrome piramidal de predominio derecho (¿parálisis flácida por relajantes musculares?) y delirium mixto. Se solicitó IRM, se suspendieron los relajantes musculares, se realizó punción lumbar (18/07/2006) con Gram negativo y Cryptococcus negativo, glucosa de 62 mg/dl; proteínas de 15 mg/dl; leucocitos de 5 x mm3; hematíes de 0-2 x mm3; cultivo bacteriológico negativo y Dipstick: negativo para H. influenzae, S. pneumoniae, N.meningitidis. En la IRM cerebral simple (14/07/2006) se observó un aumento simétrico de la intensidad de señal del putamen y globus pallidus, con compromiso de las cabezas de los núcleos caudado y región subependimaria de los ventrículos laterales en su aspecto externo, visualizadas en las secuencias FLAIR, T2 y Spin ECO (Figura 2). El diagnóstico podría corresponder a Enfermedad de Leigh (encefalomielopatía subaguda necrotizante) vs. Enfermedad de Wilson.
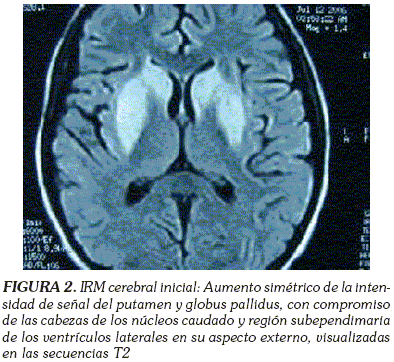
La electromiografía fue normal y el perfil Inmunológico mostró ANAS (-), Anti ADN (-), C3 y C4 normales, ACA IgG 1,3 (-), ACA IgM 7,4 (-), SM 3,5 (normal), Ro 2,4 (normal), La 3.1 (normal) RNP 7,3 (normal), ANCAS (-), ceruloplasmina 0,363 g/L (0,204-0,407). El ELISA para VIH (-), el perfil hepático normal, los hemocultivos seriados (-), HCV (-) y los Ags de superficie APRA hepatitis B (-).
En la IRM cerebral de control (28/07/2006) se observó aumento en la intensidad de señal en las secuencias potenciadas en T1, T2 y FLAIR de las regiones gangliobasales con compromiso de las cabezas de los núcleos caudados y globus pallidus, en forma simétrica con extensión hacia la sustancia subependimaria de los ventrículos laterales (Figura 3). Dichas lesiones eran simétricas, sin efecto de masa y tampoco había imágenes sugestivas de edema; no hubo realce con la administración de medio de contraste paramagnético; el sistema ventricular de amplitud y configuración normal, el mesencéfalo y el tallo de aspecto usual; los globos oculares y las regiones parasinusales, así como el mastoides de aspecto usual y las leptomeninges también normales. Estos hallazgos, dados los antecedentes y la edad del paciente, sugirieron cambios de encefalopatía mitocondrial vs. acidosis láctica, o aciduria glutárica, o ambas.
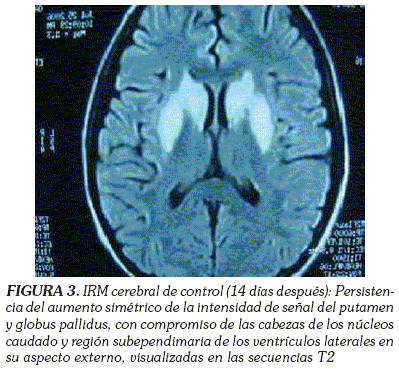
La fibrinoscopia (07/07/06) mostró una laringe, cuerdas vocales y mucosa normales; en la tráquea y carina principal abundante secreción serosa, mucosa normal, sin úlceras y sin obstrucción del flujo. Árbol bronquial: bronquio fuente derecho (BFD) normal y bronquio fuente izquierdo (BFI), desde su entrada y en toda su extensión endoscópica con lesiones de aspecto petequial difuso, diseminadas y en cantidad importante; presentó tendencia a desaturación. La citología de lavado bronquial (08/07/2006) reportó células bronquiales de características benignas, algunas con metaplasia escamosa y sin reconocimiento de células malignas en el material examinado. El Gram, el ZN, el KOH y los cultivos, todos negativos.
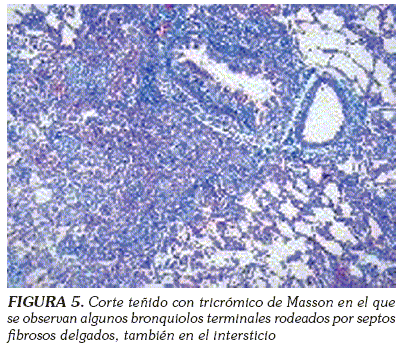
Se realizó biopsia pulmonar cielo abierto (31/VII/06), cuyos cortes mostraron un pulmón con áreas de colapso y de sobredistensión, secundaria a lesión bronquiolocéntrica residual y caracterizada por obstrucción de su luz, por pólipos fibroblásticos en algunos y por secreción en otros, concomitante con hiperplasia del epitelio e inflamación crónica de la pared, evidenciándose a nivel alveolar algunos pólipos fibroblásticos residuales, e histiocitos espumosos (NLE), cambios estos que se confirmaron con la tinción de TM. Las tinciones de Gomori, PAS y Rojo Congo fueron todas negativas. La pleura engrosada por fibrosis con neovascularización, inflamación aguda y crónica e hiperplasia mesotelial activa. El reporte de la biopsia fue de bronquitis obliterante con neumonía organizada (BOOP) parcialmente resuelta y pleuritis aguda y crónica (Figuras 4 y 5).
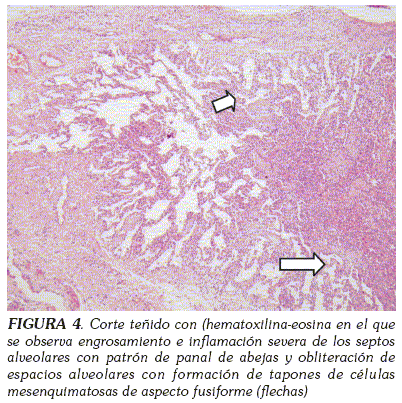
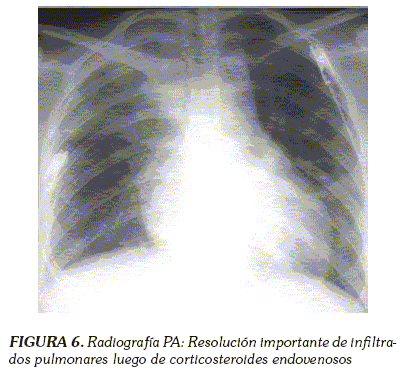
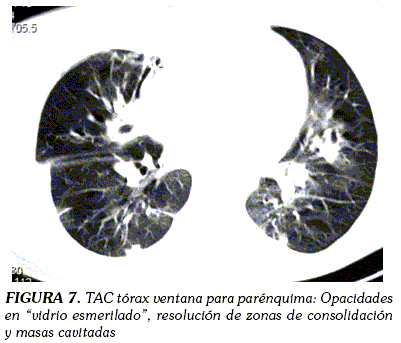
Se discutieron los hallazgos sucesivos de IRM en junta médica de neurorradiología, entre el Hospital Universitario de la Samaritana y el Instituto Nacional de Cancerología y se consideró (por clínica de aparición, por edad y por hallazgos paraclínicos) que las lesiones en ganglios basales correspondían a lesiones por encefalopatía hipóxico-isquémica. La paciente evolucionó adecuadamente desde el punto de vista neurológico, con mejoría de la fuerza generalizada y con autolimitación de alteración de su estado de conciencia. En cuanto al aspecto neumológico y ante persistencia de dificultad respiratoria, a pesar de mejoría radiológica de infiltrados (Figura 6), se sospechó de tromboembolismo pulmonar (TEP) desarrollado durante su hospitalización. Se solicitó un ANGIOTAC de tórax que descartó un TEP, mostrándose en ventana para pulmón, opacidades en "vidrio esmerilado" y resolución importante de los nódulos y de las masas cavitadas (Figura 7) que se observaron en el TAC inicial (Figura 1).
Con los hallazgos de la biopsia y con los parciales de orina de control, todos normales, se descartaron las posibilidades diagnósticas planteadas sobre Síndrome Riñón-Pulmón.
La paciente evolucionó adecuadamente, se resolvieron los infiltrados pulmonares y se le dio salida con esteroides orales y con controles ambulatorios.
Discusión
El diagnóstico de NCO se sugiere usualmente por los hallazgos en la radiografía de tórax y se confirma por biopsia transbronquial, o por biopsia de pulmón a cielo abierto. Los hallazgos en la TACAR se clasifican en diferentes patrones a saber: patrón nodular, patrón broncocéntrico, patrón linear y en banda, patrón perilobular, fibrótico progresivo y patrón con lesiones focales (1).
En un estudio realizado por Cordier et al., la NCO se clasificó dentro de tres patrones, siendo el de "lesiones focales" uno de ellos (2). La localización habitual de las lesiones en ese estudio fue en lóbulos superiores y la cavitación ocasional sugiere la posibilidad de evaluar si son estériles post- infecciosas, o si son abscesos estériles post-infarto. El patrón focal también se puede presentar como múltiples opacidades que semejan masas (3-5), el cual fue el hallazgo más frecuente en otro estudio en el que la mayoría de lesiones se ubicaban en la periferia (6). En la serie de Akira et al., en la que la NCO se manifestaba como múltiples nódulos alargados o masas, la característica más prominente fue la de márgenes espiculados e irregulares (7). El patrón cavitado de la NCO se puede encontrar tanto en su expresión idiopática, como en la inducida por bleomicina, la cual se puede presentar con nódulos pseudometastásicos y con cavitación ocasional (8). También se reconocen las asociaciones de NCO con crioglobulinemia esencial mixta (12) y con linfoma (13).
El estudio de Epler et al. describen las primeras lesiones cavitadas en el contexto de NCO, en dos de sus 50 pacientes (9). Desde el año de su publicación, las series más grandes de casos con hallazgos, ya sea como nódulos solitarios, o como múltiples cavitados, incluyen las ya descritas por Akira et al. y por Cordier et al. En razón a sus series de casos, Cordier sugiere, en una editorial de 1995, la inclusión de la NCO como causa de cavitaciones pulmonares (11).
Los principales diagnósticos diferenciales de infiltrados cavitarios incluyen abscesos piógenos por una gran variedad de organismos bacterianos, tuberculosis pulmonar y enfermedades parasitarias del pulmón. Además de las patologías infecciosas, las cavitaciones pulmonares también se han documentado en pacientes con patologías malignas (primarias o secundarias), en enfermedades del colágeno, en la granulomatosis de Wegener y menos frecuentemente en otras vasculitis. Raramente en linfoma, en sarcoidosis y en quistes 10).
Las presentaciones clínicas de la NCO pueden expresar todas las características manifestadas por la paciente del caso que se reporta. Tos, disnea, fiebre y leucocitosis son hallazgos en un 50 % de los pacientes durante la fase aguda, mientras el dolor pleurítico ocurre solamente en uno de cada cuatro pacientes (14). De acuerdo con la experiencia del grupo tratante, la presentación en niños y en adolescentes de esta patología es extremadamente rara, existiendo algunos reportes en la literatura (15). Este es, hasta el momento, el único caso reportado de NCO aguda idiopática, en edad adolescente y con manifestación de múltiples masas cavitadas.
Es importante resaltar que como manifestación inicial radiológica y clínica, la paciente de este caso cursó con la posibilidad diagnóstica de daño pulmonar agudo (APA) /Síndrome de Dificultad Respiratoria Aguda en el Adulto (SDRA). Como bien lo manifiestan Marvin et al. , la bronquiolitis obliterante con neumonía organizada (BOOP), es mejor reconocida como un síndrome subagudo (16), produciendo síntomas durante varios meses y con frecuencia precedidos de una infección del tracto respiratorio superior (9). Menos común, BOOP cursa como un cuadro agudo, fulminante, que resulta en falla respiratoria y que requiere de ventilación mecánica (17-21). Las formas agudas son idiopáticas, o asociadas a enfermedades del tejido conectivo, o a toxicidad por drogas (22-25). Los estudios imaginológicos demuestran infiltrados en parches, con áreas de consolidación inespecíficas. A pesar de que en la literatura se describen solamente alrededor de veinte casos, los tratamientos del BOOP idiopático agudo parecen ser inferiores a los de la presentación subaguda y es menos probable realizar el retiro de corticosteroides, como sucede en el caso de la forma subaguda de BOOP (16). En el contexto de IPA/SDRA, el papel del lavado broncoalveolar indica un predominio de neutrófilos y un menor porcentaje de linfocitos y de eosinófilos (26). El BOOP agudo, a causa de las bajas tasas de reporte, los resultados de tratamiento son poco claros. La mortalidad puede ser alta, hasta de un 70%, sobre todo cuando se acompaña de enfermedad del tejido conectivo (19, 23). En un reporte de Schwarz et al., tres de cinco pacientes con BOOP agudo idiopático sobrevivieron después de haber recibido corticosteroides dentro de la primera semana posterior a la biopsia pulmonar, tratamiento que fue diferido hasta dos semanas en los no sobrevivientes (23). Otros estudios confirman que el diagnóstico temprano y el inicio concomitante de corticosteroides, mejora la sobrevida (20, 21). En el paciente de este caso, el inicio temprano de corticosteroides dio evidencia de una resolución clínica y radiológica completa, en concordancia con los hallazgos de la literatura.
Respecto de los hallazgos neurológicos de la paciente, se debe destacar que durante la infancia y a causa de los altos requerimentos energéticos, que demandan una irrigación aumentada y altas concentraciones de elementos traza (hierro, cobre, manganeso), los ganglios basales son susceptibles de daño y sus lesiones se traducen en incremento en la irritabilidad, letargia, distonía, convulsiones y cambios conductuales. Por su edad (16 años), los diagnósticos diferenciales se enmarcaron en las patologías de instauración aguda, dentro del grupo etáreo de adolescentes-adultos. En las tablas 3, 4 y 5, se resumen las posibilidades de acuerdo a su instauración:


En la paciente de este caso se reconocen las posibilidades de anoxia anóxica por un bajo contenido sanguíneo de O2, o de anoxia isquémica por el estado de "bajo flujo" que llevó a la necesidad inicial de soporte inotrópico, como las causales de las lesiones en ganglios de la base. En este caso particular, la simetría de las lesiones y su instauración aguda limitó los diagnósticos a una serie de entidades bien definidas. Es importante resaltar que en las IRM cerebrales de pacientes adultos con posterior encefalopatía hipóxico- isquémica, se encuentran múltiples lesiones hiperintensas parieto-occipitales bilaterales, que indican necrosis laminar cortical progresiva y que incluso llegan, en la fase crónica, a un patrón de hiperintensidad de la sustancia blanca bilateral (28). En comparación, los hallazgos de encefalopatía hipóxico-isquémica en los pacientes de edad adolescente- adulta pueden ser similares a los de los adultos, pero en ellos se debe evaluar el compromiso ganglio- basal, mucho mayor en esta población y que hace pensar, como en esta paciente, en una amplia gama de diagnósticos, que de no enmarcarse en el contexto y en el grupo etáreo, pueden conllevar a diagnósticos erróneos y a estudios innecesarios.
En conclusión, la NCO es una entidad con diversas manifestaciones clínicas y radiológicas, con bajas tasas de reporte en su presentación aguda, así como en la forma cavitada. Por la revisión de la literatura y por el caso que se expone, se considera que en el diagnóstico diferencial de enfermedad cavitada pulmonar, se debe incluir la NCO. En cuanto a las anormalidades de los ganglios de la base, los pacientes que las sufren se deben enmarcar en un tiempo de evolución y en un grupo etáreo específico, para dar una adecuada aproximación diagnóstica.
Referencias
1. Anastasia O, David M. H. Organizing pneumonia: the many morphological faces .Eur Radiol. 2002;12:1486–1496. [ Links ]
2. Cordier JF, Loire R, Brune J. Idiopathic bronchiolitis obliterans organizing pneumonia. Definition of characteristic clinical profiles in a series of 16 patients. Chest. 1989;96:999-1004. [ Links ]
3. Haro M, Vizcaya M, Texido A, Aguilar X, Arevalo M. Idiopathic bronchiolitis obliterans organizing pneumonia with multiple cavitary lung nodules. Eur Respir J. 1995;8:1975–1977. [ Links ]
4 . Froudarakis M, Bouros D, Loire R, Valasiadou K, Tsiftsis D, Siafakas NM. BOOP presenting with haemoptysis and multiple cavitary nodules. Eur Respir J. 1995;8:1972–1974. [ Links ]
5. Cordier JF. Cavitary bronchiolitis obliterans organizing pneumonia. Eur Respir J. 1995;8:1822–1823. [ Links ]
6. Bouchardy LM, Kuhlman JE, Ball WC Jr, Hruban RH, Askin FB, Siegelman SS. CT findings in bronchiolitis obliterans organizing pneumonia (BOOP) with radiographic, clinical, and histologic correlation. J Comput Assist Tomogr. 1993;17:352–357. [ Links ]
7. Akira M, Yamamoto S, Sakatani M. Bronchiolitis obliterans organizing pneumonia manifesting as multiple large nodules or masses. Am J Roentgenol. 1998;170:291–295. [ Links ]
8. Cohen MB, Austin JH, Smith-Vaniz A, Lutzky J, Grimes MM. Nodular bleomycin toxicity. Am J Clin Pathol. 1989;92:101–10. [ Links ]
9. Epler GR, Colby TV, McLoud TC, Carrington CB, Gaensler EA. Bronchiolitis obliterans organizing pneumonia. N Engl J Med. 1985;312:152–158. [ Links ]
10. Swartz MN. Approach to the patient with pulmonary infections. En: Fishman AP, editor. Pulmonary diseases and disorders. New York: McGraw-Hill; 1998. p. 1915–1916. [ Links ]
11. Cordier JF. Cavitary bronchiolitis obliterans organizing pneumonia [editorial[. Eur Respir J. 1995;8:1822–1823. [ Links ]
12. Zackrison LH, Katz P. Bronchiolitis obliterans organizing pneumonia associated with essential mixed cryoglobulinemia. Arthritis Rheum. 1993;36:1627–1630. [ Links ]
13. Safadi R, Berkman N, Haviv Y. Primary non-Hodgkins lymphoma of the lung presenting as bronchiolitis obliterans organizing pneumonia. Leuk Lymphoma. 1997;28:209–213. [ Links ]
14. Cordier. JF. Rare interstitial lung diseases. Cryptogenic organizing pneumonia. Eur Respir J. 2006;28:422–446. [ Links ]
15. Inoue T, Toyoshima K, Kikui M. Idiopathic bronchiolitis obliterans organizing pneumonia (idiopathic BOOP) in childhood. Pediatr Pulmonol. 1996;22:67–72. [ Links ]
16. Schwarz M, Albert R. "Imitators" of the ARDS: implications for Diagnosis and Treatment. Chest. 2004;125:1530–1535. [ Links ]
17. Schwarz MI. Diffuse pulmonary infiltrates and respiratory failure following 2 weeks of dyspnea in a 45-year-old woman. Chest. 1993;104:927–929. [ Links ]
18. Cohen AJ, King TE, Downey GP. Rapidly progressive bronchiolitis obliterans with organizing pneumonia. Am J Respir Crit Care Med. 1994;149:1670–1675. [ Links ]
19. Llano LA, Soilan JL, Garcia Pais M. Idiopathic bronchiolitis obliterans with organizing pneumonia presenting with the adult respiratory distress syndrome. Respir Med. 1998;92:884–886. [ Links ]
20. Nizami IY, Kissner DG, Visscher DW. Idiopathic bronchiolitis obliterans with organizing pneumonia: an acute and life-threatening syndrome. Chest. 1995;108:271–277. [ Links ]
21. Waxman AB, Shepard JO, Mark EJ. Case 14–2003: a 73-year old woman with pneumonia and progressive respiratory failure. N Engl J Med. 2003; 348:1902–1912. [ Links ]
22. Schwarz MI. The lung in polymyositis. Clin Chest Med. 1998;19:701–712. [ Links ]
23. Schwarz MI, Matthey RA, Sahn S. Interstitial lung disease in polymyositis and dermatomyositis: analysis of six cases and review of the literature. Medicine. 1976;55:89–104. [ Links ]
24. Fata F, Rathore R, Schiff C. Bronchiolitis obliterans organizing pneumonia as the first manifestation of polymyositis. South Med J. 1997;90:227–230. [ Links ]
25. Cazzato S, Zompatori G, Baruzzi G. Bronchiolitis obliterans-organizing pneumonia: an Italian experience. Respir Med. 2000;94:702–708. [ Links ]
26. Vourlekis VS, Brown KK, Schwarz MI. Acute interstitial pneumonitis: current understanding regarding diagnosis, pathogenesis and natural history. Semin Respir Crit Care Med. 2001;22:399–408. [ Links ]
27. Brami-Zylberberg F, Méary E, Abnormalities of the basal ganglia and thalami in adults. J Radiol. 2005;86:281-93. [ Links ]
28. Maisee K. Hypoxic Ischemic encephalopathy. 1 st ed. Boston: Arbor Press; 2001. [ Links ]














