INTRODUCCIÓN
Las garrapatas son artrópodos hematófagos distribuidos en todo el mundo, parasitan diferentes especies de mamíferos (incluido el hombre), aves, anfibios y reptiles. A esta capacidad parasitaria, se les suma a algunas especies la propiedad de ser vectores transmisores de enfermedades causadas por bacterias, virus y protozoarios de gran importancia en salud pública 1,2. Adicionalmente, producen reacciones de hipersensibilidad en el sitio de fijación e incluso puede presentarse reacciones anafilácticas, parálisis neurotóxica y traumatismo local a nivel de piel y tejido celular subcutáneo, al introducir agentes potencialmente patógenos a través de la saliva, durante el proceso de alimentación; lo que favorece una sobreinfección piógena 1. En ciertas ocasiones las infestaciones elevadas de garrapatas en animales causan anemia severa e incluso la muerte 3, de tal forma que se consideran de los vectores de mayor importancia en la transmisión de patógenos a los humanos y a los animales silvestres, de compañía y de producción. Estos ectoparásitos pertenecen al orden Parasitiformes, suborden Ixodida, y se subdividen en tres familias: Ixodidae, también llamadas "garrapatas de cuerpo duro", Argasidae o "garrapatas de cuerpo blando" y Nuttalliellidae representada por solo una especie que no se encuentra presente en América y que no transmite patógenos a los seres humanos 4 (Figura 1).
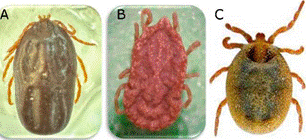
Figura 1. Clasificación de las garrapatas. 1A) Familia Ixodidae (Rhipicephalus sanguineus sensu lato) y 1b) Familia Argasidae (Ornithodorus spp.) - Imágenes proporcionadas por el Dr. Francisco Martínez-Ibañez. 1C) Familia Nuttalliellidae (Nuttalliella namaqua)5.
En México, existen alrededor de 100 especies de garrapatas que parasitan a los animales domésticos y silvestres 6,7. Los géneros pertenecientes a la familia Ixodidae y Argasidae que usualmente actúan como vectores transmisores de patógenos a los humanos son Ixodes spp., Dermacentor spp., Amblyomma spp., Haemaphysalis spp., Hyalomma spp., Rhipicephalus spp. y Ornithodoros spp. 1,3 (Figura 2).

Figura 2. Garrapatas transmisoras de patógenos a los humanos. 2A) Macho y hembra de Ixodes scapularis. 2B) Macho y hembra de Dermacentor variabilis. 2C) Macho y hembra de Amblyomma americanum. Imágenes proporcionadas por el Dr. Francisco Martínez-Ibañez.
Actualmente, las garrapatas se han convertido en uno de los principales vectores de enfermedades más importantes en el mundo, siendo el segundo lugar después de los mosquitos 8. Durante el ciclo de vida, las garrapatas pueden durar entre 1 y 3 años dependiendo la especie y las condiciones ambientales, pasan por tres estadios o fases: larva, ninfa y adulto. Los seres humanos generalmente actúan como un hospedador accidental dentro del ciclo de vida de las garrapatas. Sin embargo, al ser infestados por cualquiera de las fases de desarrollo pueden contraer alguna de las enfermedades que son capaces de transmitir. Por ejemplo, Ixodes ricinus (transmisora de la enfermedad de Lyme) parasita al humano en la fase de ninfa, mientras que Dermacentor marginatus (transmisora de la enfermedad Debonel) lo hace en fase adulta 9. Por otro lado, las garrapatas blandas son vectores de la fiebre recurrente endémica, una infección provocada por diferentes especies de bacterias del género Borrelia spp., donde la garrapata transmisora es Ornithodoros erraticus10.
La incidencia y prevalencia de las enfermedades transmitidas por garrapatas se correlaciona con su distribución geográfica y ecología, siendo fundamental la presencia de factores ambientales como temperatura, humedad, altitud, vegetación y presencia de hospedadores. En México, durante los últimos tres años se ha presentado un incremento del 69% de casos por año de enfermedades transmitidas por garrapatas 11. En el 2023, de acuerdo con los reportes del sistema de vigilancia epidemiológica, se notificaron 480 casos de enfermedades bacterianas por rickettsias distribuidos en el 53% de los estados del país, siendo cinco estados los de mayor incidencia (Sonora - 116, Chihuahua - 103, Baja California - 102, Nuevo León - 94 y Coahuila - 37) 11. Así mismo, se ha observado un incremento de la distribución de las garrapatas y de las enfermedades que transmiten entre animales de compañía y humanos; esto puede deberse tanto a la intensificación de la actividad humana como a la caza de animales. Actividades como: camping, viajes intercontinentales, urbanización no controlada, cambios en el uso de suelo (agricultura y ganadería), situaciones socioeconómicas, transporte de animales de abasto, son algunas causas del aumento de los casos. Además, las garrapatas pueden expandirse y colonizar fácilmente nuevas regiones a través del movimiento de hospedadores, ya sea durante el transporte de animales domésticos, a través de la migración de las aves o a través del contacto de animales domésticos con silvestres 2,12.
La población humana en general puede llegar a infectarse con enfermedades que transmiten las garrapatas. Sin embargo, las personas que trabajan en actividades relacionadas al campo, propietarios de animales de compañía que no realizan buen manejo en el control de ectoparásitos, así como aquellas viviendas que se encuentran cerca de propiedades agropecuarias o zonas con mucha vegetación, presentan mayor riesgo de adquirirlas 13,14,15. Actualmente, la incidencia va en aumento en muchos países, por lo que se consideran enfermedades emergentes y/o reemergentes que representan desafíos importantes para la salud pública. En este sentido, es fundamental contribuir en la educación de la población y de los profesionales de la salud (principalmente de zonas rurales) para capacitarse en los temas relacionados al conocimiento de las especies de garrapatas y las enfermedades que transmiten; ya que normalmente se desconoce el riesgo potencial que llegan a tener como vectores de agentes infecciosos 12. Por lo cual, el objetivo de este artículo es realizar una revisión actualizada de las principales enfermedades transmitidas por garrapatas a los humanos con la finalidad de establecer medidas preventivas y estrategias de control oportunas para evitar su propagación.
Enfermedades causadas por agentes virales transmitidos por garrapatas
Los virus transmitidos por garrapatas pertenecen a las familias Flaviviridae, Bunyaviridae, Reoviridae, Asfarviridae y Orthomyxoviridae; son agentes causales de diferentes enfermedades en humanos y animales 16. En muchas ocasiones los roedores actúan como hospedadores naturales y la zoonosis ocurre por el contacto entre roedores y humanos debido a que presentan una interacción inespecífica, compartiendo prácticamente todos los ecosistemas donde habitan 16. De la familia Reoviridae, entre los Coltivirus se destaca el virus de la fiebre por garrapatas del Colorado (Colorado tick fever virus: CTFV, por sus siglas en inglés), también llamado fiebre por garrapatas de las montañas, fiebre de las montañas americanas o fiebre de montaña. La CTFV se ha asociado principalmente con la garrapata Dermacentor andersoni en Norteamérica (Estados Unidos y Canadá). Un total de 75 casos fueron confirmados en Estados Unidos y un estudio realizado con garrapatas colectadas en dos parques durante el 2010 demostró que el 99% eran D. andersoni y el 21% de estas estaban infectadas con el virus causante de esta enfermedad. Este padecimiento presenta un periodo de incubación entre 3-5 días y cursa con un cuadro febril, dolor de cabeza, dolor retroocular, dolores musculares, náuseas, vómito, sudoración, leucopenia, fotofobia y debilidad generalizada 17,18. El diagnóstico se realiza mediante la prueba de Fijación de
Complemento, titulación de anticuerpos por Inmunofluorescencia (IFI) y técnicas moleculares como la Reacción en Cadena de la Polimerasa (PCR). A la fecha no se ha desarrollado ninguna vacuna contra esta enfermedad por lo cual el tratamiento está basado en medidas de soporte vital. La ribavirina y los análogos de nucleósidos han demostrado tener un efecto inhibitorio de manera eficaz 19 cuando son administrados en etapas tempranas de la enfermedad.
La encefalitis transmitida por garrapatas es otra enfermedad común en humanos y es causada por un flavivirus; este virus se transmite en Europa por garrapatas I. ricinus y en Rusia por Ixodes persulcatus (20,21). Esta enfermedad se considera endémica de Europa y Asia. El virus tiene la capacidad de subsistir en las garrapatas durante toda su vida, lo que permite la transmisión de la enfermedad durante ciclos que pueden durar años; además, muchas especies de animales pueden llegan a ser reservorios del virus que ocasiona la enfermedad 21,22. La vigilancia epidemiológica en Europa se encuentra bien establecida y en constante alerta para evitar la transmisión de la enfermedad, sin embargo, se han reportado hasta 10,000 casos al año. Como medida preventiva se utiliza la aplicación de una vacuna que es muy útil para minimizar los síntomas de la enfermedad. No obstante, la incidencia de la encefalitis está en aumento y la cobertura de la vacunación está siendo insuficiente en muchos sectores de la población europea 23.
En cuanto a virus transmitidos por garrapatas en la región Neotropical no existe suficiente investigación que afecte a los humanos. Sin embargo, la diversidad que existe entre las garrapatas establecidas en la región Neotropical con las otras zonas geográficas es muy diferente, por lo tanto, no se descarta que sean vectores de virus previamente descritos o virus desconocidos 23. En Sudamérica existe evidencia de virus reportados en garrapatas como el virus Mogiana en Rhipicephalus microplus, el virus Huacho en Ornithodoros amblus, el virus Cacipacoré en Amblyomma sculptum y el virus Matucare en Ornithodoros kohlsi. Sin embargo, se desconoce el potencial patogénico de cada uno de ellos, así como su ecología 24. Finalmente, existen diversos factores que pueden influir en la introducción de virus transmitidos por garrapatas a regiones donde previamente no existían; como la fauna silvestre, las aves migratorias, el cambio climático, el transporte de animales domésticos, etc. Esto demuestra que los virus en garrapatas presentan una adaptación evolutiva importante, lo que implica algún impacto en la salud animal y la salud pública.
Enfermedades causadas por agentes bacterianos transmitidos por garrapatas
Las infecciones por bacterias transmitidas por garrapatas representan un riesgo importante para la salud pública, debido a su fácil expansión, transmisión y adaptación a nuevos hospedadores 21. En ese sentido, se han identificado diversas bacterias que pueden ser transmitidas por garrapatas a los humanos como las pertenecientes a los géneros Borrelia spp., Ehrlichia spp., Rickettsia spp. y Anaplasma spp.
La Enfermedad de Lyme, conocida comúnmente como Borreliosis, es una infección bacteriana y multisistémica de pequeños y grandes mamíferos, ocasionada por la bacteria Borrelia burgdorferi sensu lato y transmitida por garrapatas del género Ixodes (I. scapularis (Figura 3A) e I. ricinus) Amblyomma spp. y Dermacentor spp.; siendo hospedadores naturales perros y roedores (25,26). Esta enfermedad es reconocida como endémica en Europa y Estados Unidos. En el caso de México, la Borreliosis que causa fiebre recurrente se transmite principalmente por garrapatas blandas del género Ornithodoros spp. y el piojo Pediculus humanus. Sin embargo, las garrapatas de los géneros Ixodes spp., Amblyomma spp. y Rhipicephalus spp. también se han implicado como vectores potenciales. Varios factores promueven su propagación, como la biodiversidad de artrópodos y vertebrados, el clima, la cercanía geográfica con Estados Unidos y la afluencia de turistas, migrantes y refugiados provenientes de Europa, Norteamérica y Latinoamérica 26. Esta enfermedad es compleja, presenta manifestaciones cutáneas, articulares, neurológicas, cardiacas y sistémicas. La lesión más específica desde el punto de vista de diagnóstico es el eritema crónico migratorio (mancha rojiza que suele hacerse cada vez de mayor tamaño y frecuentemente se vuelve más pálida en el centro) (Figura 3B). Los síntomas que pueden cursar las personas infectadas son: fiebre, somnolencia, dolor muscular, dolor de cabeza, dolor de articulaciones, comezón, fatiga, visión borrosa, inflamación de las articulaciones y los nódulos linfáticos, palpitaciones, eritema migrante, entre otros. Un 15% de las personas con enfermedad de Lyme padecerá una enfermedad neurológica, que suele comenzar de una a cinco semanas después de la interacción con la garrapata. Para confirmar el diagnóstico lo más recomendable es la cuantificación de anticuerpos mediante el ensayo de inmunoabsorción ligado a enzimas (ELISA) 27. En caso de positividad o sospecha es recomendable realizar un estudio más sensible y específico mediante la prueba de inmunotransferencia para la detección de anticuerpos contra varias proteínas de la bacteria B. burgdorferi. Estas pruebas determinarán si el paciente ha desarrollado anticuerpos contra la bacteria. En caso de ser positivo se realizará el tratamiento mediante medicamentos como doxiciclina (solo adultos) en etapa temprana de la enfermedad y bencilpenicilina o cefalosporinas (ceftriaxona) en la etapa aguda o de manifestación de la enfermedad 26,27.
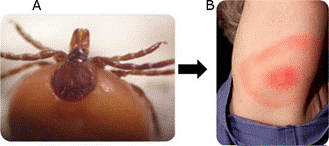
Figura 3 Enfermedad de Lyme. 3A) Garrapata Ixodes scapularis (Imagen proporcionada por el Dr. Francisco Martínez-Ibañez). 3B) Eritema crónico migratorio (Imagen proporcionada por el Dr. Luis Tinoco García).
Otra enfermedad bacteriana de interés es la llamada fiebre Q, la cual es causada por la bacteria Coxiella burnetti y puede ser transmitida por garrapatas Amblyomma spp., aunque la fuente habitual de contagio son los aerosoles generados a partir de los productos del parto de las vacas y de otros animales. El hospedador natural son principalmente pequeños mamíferos como ovejas, cabras, pájaros, perros y gatos 28. En los animales, la enfermedad se conoce como coxielosis y ocurre sin signos perceptibles. Sin embargo, en rumiantes se asocia con infertilidad, aborto espontáneo, mortalidad neonatal y parto prematuro. En el caso de perros y gatos se asocia con mortalidad perinatal, descendencia débil y aborto tardío. En los humanos la enfermedad puede estar acompañada por un síndrome febril agudo con escalofríos, sudores nocturnos, dolor de cabeza, fatiga, dolores en el pecho acompañado de neumonitis y hepatitis. En algunas ocasiones es posible observar cuadros de neumonía y endocarditis 29. El diagnóstico se realiza por serología y como tratamiento se puede administrar doxiciclina o tetraciclinas. Sin embargo, cuando hay presencia de endocarditis es difícil tratar y su pronóstico es reservado 30.
En el caso de la tularemia, conocida comúnmente como Fiebre de los conejos, es causada por la bacteria Francisella tularensis y es transmitida por ectoparásitos como garrapatas del género Dermacentor spp., Amblyomma americanum, pulgas y moscas. Otras formas comunes de contagio humano incluyen beber agua contaminada, inhalar polvo de suelo contaminado o manipular pieles o garras de animales contaminados. Los hospedadores naturales son los conejos y roedores. Esta enfermedad en los humanos se presenta con fiebre súbita, escalofrío, dolor de cabeza, dolor muscular, diarrea, tos seca y debilidad progresiva. El diagnóstico se realiza por medio de serología y PCR de una muestra de úlcera y hemocultivos, y como tratamiento se pueden administrar quinolonas o cefalosporinas 31.
Anaplasmosis y Ehrlichiosis
La anaplasmosis y la ehrlichiosis humana son enfermedades de distribución mundial, transmitidas por garrapatas y ocasionadas por especies de los géneros Anaplasma spp. y Ehrlichia spp., las cuales pertenecen al orden rickettsiales, sin embargo, a diferencia de las rickettsias estas se replican en vacuolas derivadas de la membrana celular de las células que infectan (leucocitos y plaquetas). Presentan la característica de ser gramnegativas, pleomórficas y de crecimiento intracelular obligado 7,32.
La anaplasmosis granulocítica se ha reportado en Europa, Norteamérica y norte de África, guarda cierto paralelismo con la enfermedad de Lyme en cuanto a vectores y reservorios. El vector transmisor es I. ricinus y el agente patógeno es Anaplasma phagocytophilum. Esta enfermedad se manifiesta en forma inespecífica, los pacientes presentan fiebre, malestar general, cefalea, mialgias y artralgias. Adicionalmente, la infección se puede presentar con otro cuadro clínico como meningitis, vomito, diarrea, dolor abdominal y problemas respiratorios. En cuanto al diagnóstico, este se realiza principalmente por medio de una extensión sanguínea teñida con Giemsa, serología (IFI) o detección molecular (PCR). El tratamiento se basa en la administración de doxiciclina y rifampicina 32,33.
La Ehrlichiosis humana es causada principalmente por Ehrlichia chaffeensis y en perros por Ehrlichia canis. Esta enfermedad se transmite por garrapatas del género Amblyomma spp., Rhipicephalus spp., e Ixodes spp, y los hospedadores naturales pueden ser: perros, venados y roedores 34. Los signos informados en perros incluyen fiebre de forma aguda y crónica, letargo, pérdida de apetito, mialgia, esplenomegalia y linfadenopatía. En el caso de los humanos, los síntomas incluyen fiebre, comezón, dolor de cabeza, dolor muscular, vómito, diarrea y tos. La enfermedad se diagnostica mediante tinción con Giemsa de una extensión de sangre periférica y la titulación de anticuerpos mediante IFI. El tratamiento de elección es la doxiciclina o las tetraciclinas 32.
Rickettsias
Las infecciones rickettsiales son afecciones de distribución mundial provocadas por diferentes especies de Rickettsia principalmente. Son transmitidas por artrópodos y se consideran infecciones emergentes y reemergentes. Su epidemiología ha estado siempre ligada a un círculo formado por la interacción reservorio - artrópodo -humano y en los últimos años el número de especies de Rickettsias que han sido implicadas en patología humana se ha incrementado, principalmente por las que son transmitidas por garrapatas duras 35. Estas enfermedades se caracterizan por presentar fiebre (bifásica), síntomas sistémicos de infección y a menudo erupción dérmica papular. Las infecciones rickettsiales deben ser tratadas oportunamente con antibióticos justo después de la sospecha clínica, con la finalidad de obtener un resultado satisfactorio ya que se ha documentado que un retraso en el diagnóstico y tratamiento resultan en mortalidad de los pacientes. Por ejemplo, en el estado de Chiapas se encontró un rango de 73 garrapatas infectadas con rickettsias por cada 1000 especímenes analizados, lo cual podría ocasionar severos problemas de salud entre la población 36.
La enfermedad llamada Fiebre botonosa, tiene como agente causal a Rickettsia conorii y como vector involucrado de su transmisión a Rhipicephalus spp. El hospedador natural es el perro y los roedores. Esta enfermedad en los humanos se caracteriza por presentar fiebre por arriba de 39°C, escalofríos, mancha negra (úlcera o costra oscura) y artromialgias. El diagnóstico se realiza mediante título de anticuerpos por fijación de complemento o IFI y para el tratamiento se utiliza la doxiciclina 37.
Una de las principales enfermedades ocasionadas por rickettsias es la Fiebre Manchada, conocida también como Fiebre Maculosa de las Montañas Rocosas, Fiebre Amarilla de las Montañas Rocallosas o Fiebre manchada de las Montañas Rocosas 38. Se le considera la más grave de las rickettsiosis, siendo el agente causal Rickettsia rickettsii, el cual se transmite por Amblyomma imitator y A. americanum, Haemaphysalis leporispalustris, Dermacentor venustur, D. andersoni y D. variabilis. En el caso de México, las garrapatas implicadas en la transmisión son R. sanguineus y A. mixtum (Figura 4A y 4B). Clínicamente, la rickettsia presenta un periodo de incubación de 2 a 14 días después de la mordedura de la garrapata. Los síntomas más comunes de la enfermedad son; escalofríos, fiebre, dolor de cabeza intenso, dolor muscular, anorexia, vómito, dolor abdominal, confusión mental y exantema (erupción cutánea) 14 (Figura 4C). El exantema suele comenzar pocos días después del inicio de la fiebre, apareciendo primero en las muñecas y en los tobillos como manchas de 1 a 5 mm de diámetro; posteriormente, se propaga a la mayor parte del cuerpo. El diagnóstico se lleva a cabo mediante título de anticuerpos por fijación de complemento o IFI, inmunotransferencia, pruebas moleculares, pruebas de la función renal, conteo de plaquetas, tiempo parcial de tromboplastina (TPT), Tiempo de protrombina (TP) y Conteo de glóbulos. Se toma una biopsia de la erupción en piel para verificar la presencia de R. ricketsii y análisis de orina para verificar la presencia de sangre o proteínas en la orina 15.
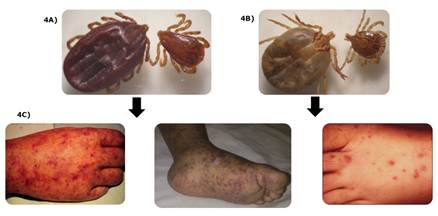
Figura 4. Enfermedad Fiebre manchada de las Montañas Rocosas. 4A) Macho y hembra de R. sanguineus y 4B) Macho y hembra de A. mixtum (Imágenes proporcionadas por el Dr. Francisco Martínez-Ibañez). 4C) Exantema eritematoso y macular en humanos (Imágenes proporcionadas por el Dr. Luis Tinoco García y Dr. Gerardo Álvarez-Hernández).
En los exámenes de laboratorio se puede apreciar leucocitosis o leucopenia con desviación a la izquierda, trombocitopenia, hiponatremia, hipoalbuminemia, aumento de las transaminasas y creatininemia, y ocasionalmente albuminuria. El tratamiento de elección consiste en doxiciclina o tetraciclina para casos sospechosos como casos confirmados. La bacteria R. rickettsii se considera la especie más patógena del género con tasas de letalidad que van del 23 al 85% en la era preantibiótica y del 5% con tratamientos adecuados 36. Se han documentado casos humanos de R. rickettsii en países como Brasil, México, Panamá, Costa Rica, Colombia y Argentina. Muchos de estos casos se han producido como brotes familiares o en zonas geográficas cercanas, siendo los perros quienes actuan como hospedador natural al igual que los conejos 14. En el caso de los perros llegan a presentar signos similares a los humanos, sin embargo, en animales silvestres no se ha observado signología aparente.
Protozoarios
Las enfermedades como la babesiosis (piroplasmosis) tiene gran relevancia por ser un protozoario transmitido por garrapatas y por el interés sobre su epidemiología, distribución geográfica, incidencia y patogenicidad. Para algunos protozoarios transmitidos por vectores, la temperatura es un factor crítico del que depende tanto la densidad como la capacidad vectorial. La babesiosis tiene sinonimias como Fiebre de Texas, Fiebre de Garrapata y Aguas Rojas; es una enfermedad febril con presencia de anemia, afecta a animales domésticos, silvestres y ocasionalmente a humanos. En los animales el agente causal comprende especies como Babesia bovis, B. bigemina y B. vogeli; como agente transmisor Rhipicephalus microplus, R. sanguineus, Ixodes spp. y Dermacentor spp. 39,40.
La babesiosis en humanos se considera una infección de distribución mundial, siendo los casos reportados en Europa y Norteamérica los de mayor importancia 41. En el caso de Norteamérica, la enfermedad se presenta por mordedura de garrapatas del género Ixodes spp. que parasitan a varias especies de ratones del género Peromyscus spp. y ha sido catalogada como emergente en humanos. En ocasiones la infección también se debe a transfusiones de sangre o infecciones transplacentarias. En el 2018 se reportó la detección de casos clínicos de babesiosis en niños, encontrando como agente causal a Babesia microti en el estado de Yucatán, México 42. La infección cursa con un cuadro de debilitamiento o agotamiento, dolor de músculos y coyunturas, fiebre y escalofríos, pérdida de apetito, náuseas, vómito, dolor abdominal y orina oscura. En cuanto al diagnóstico se realiza extensión de sangre periférica teñida con Giemsa o serología por técnica de ELISA. El tratamiento se basa en la administración de azitromicina o clindamicina y cloroquinina 43.
Enfermedades causadas por otros agentes no infecciosos transmitidas por garrapatas
La parálisis flácida producida por garrapatas es un trastorno poco frecuente en pediatría. Diversas garrapatas se han asociado con la transmisión de esta enfermedad debido a las neurotoxinas que producen por la mordedura y el proceso de alimentación. Se menciona que existen 43 especies descritas en el mundo con la capacidad de transmitir esta enfermedad y se relaciona a la garrapata D. andersoni y D. variabilis como las más frecuentes en Norteamérica. Se caracteriza por ser ascendente y flácida, en general se llega a encontrar a la garrapata cerca del cuero cabelludo y la columna vertebral 44.
Una de las características de esta enfermedad, es la presentación de pápula eritematosa indolora y otras veces dolor y úlcera necrótica. Posteriormente, aparece irritabilidad y 2448 horas más tarde comienza la debilidad de extremidades inferiores con hipotonía, que puede afectar tanto a la musculatura del tronco como a la respiratoria. La mayor cantidad de toxinas se producen entre el quinto y séptimo día post-fijación, sin embargo, la gravedad va a estar dada dependiendo del tiempo de fijación y del número de ejemplares encontrados. El diagnóstico normalmente es clínico y se puede diferenciar con el síndrome de Guillain-Barré por un LCR (líquido cefaloraquideo) normal. En el tratamiento se recomienda extraer a las garrapatas y utilizar analgésicos evitando los relajantes musculares 45.
La mayoría de los casos de parálisis por mordedura de garrapatas se producen entre los meses de abril y junio cuando la fase adulta de las garrapatas emerge de su hibernación y buscan activamente hospedadores. En Australia, este padecimiento es causado por la garrapata Ixodes holocyclus, implicada en la transmisión de la parálisis principalmente en perros, pero también en otras especies, como gatos, rumiantes, cerdos y caballos. Recientemente, se llevaron a cabo estudios de predicción de distribución espacial de esta garrapata para el 2050, indicando un aumento moderado en zonas con condiciones climáticas favorables para su desarrollo 46,47.
Prevención
Las garrapatas y las enfermedades que transmiten representan una amenaza latente para la salud pública y la salud animal. Actualmente, existe suficiente evidencia científica que confirma la importancia de implementar medidas preventivas para reducir el riesgo de contacto y la mordedura por garrapatas 48. Algunas recomendaciones son: 1) Evitar visitar áreas boscosas o con vegetación muy densa, pastos altos, arbustos, montes, etc. En caso de hacerlo, utilizar ropa adecuada (pantalones largos, camisa de manga larga), preferentemente de color claro para poder visualizar a las garrapatas que llegan a subirse al cuerpo y poder removerlas. Usar zapatos que cubran por completo el pie y con calcetines largos y gruesos. Usar sombrero con la finalidad de evitar que las garrapatas lleguen al cuero cabelludo. 2) Utilizar repelentes de insectos sobre la ropa y en las partes del cuerpo que quedan expuestas. Se pueden utilizar repelentes a base de permetrinas (principio activo - DEET). 3) Al finalizar la actividad en campo, se recomienda inspeccionar la ropa utilizada y bañarse examinando cuidadosamente zonas del cuerpo donde se pudieran localizar garrapatas (12,48) (Figura 5).
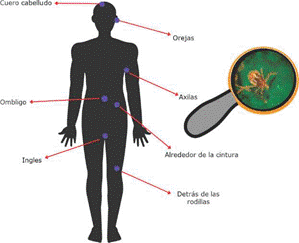
Figura 5. Zonas del cuerpo humano donde es frecuente la localización de garrapatas. (Imagen elaborada por el Dr. Rodolfo Lagunes-Quintanilla y la Mtra. Nancy Mendoza-Martínez).
Cuando se llegan a encontrar garrapatas en el cuerpo, se deben retirar a la brevedad, evitando dejar el aparato bucal incrustado. Este proceso se realiza mediante pinzas de punta fina, tomándola lo más cercano al aparato bucal y levantando en posición vertical tirando de ésta. Actualmente, en el mercado se venden pinzas especiales para la extracción de garrapatas que pueden utilizarse en humanos y en animales de compañía (Figura 6). Una vez retirada la garrapata es conveniente resguardarla en un recipiente o frasco con la finalidad de que, si la persona presenta sintomatología en los días posteriores, el ejemplar pueda utilizarse para identificación taxonómica y para realizar un diagnóstico definitivo, ayudando a prescribir un tratamiento oportuno y certero 12,49.
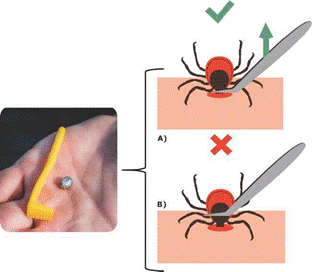
Figura 6. Pinzas removedoras de garrapatas. A) Forma correcta de retirar a las garrapatas tomándolas desde la base del aparato bucal. B) Forma incorrecta de retirar a las garrapatas dejando el aparato bucal fijado en la piel. (Imagen elaborada por el Dr. Rodolfo Lagunes-Quintanilla y la Mtra. Nancy Mendoza-Martínez).
Finalmente, el manejo de garrapatas debe implementarse de manera regular en zonas de alta incidencia y debe estar supervisado por un Médico Veterinario Zootecnista. Es importante realizar un control periódico de ectoparásitos tanto en animales de producción como en animales de compañía, haciendo uso responsable de los ixodicidas para evitar la contaminación ambiental y la selección de garrapatas resistentes 50. También, es importante inspeccionar a los animales de compañía frecuentemente cuando han pasado tiempo al aire libre (parques, campo, jardines), buscando garrapatas en zonas del cuerpo como: orejas, cola, parpados, axilas, ingles, espacios interdigitales y debajo del collar 51.
En conclusión, el estudio biológico - médico -veterinario de las garrapatas ha tomado gran relevancia en todo el mundo ya que no sólo ocasionan daños directos a sus hospedadores por medio de reacciones de hipersensibilidad en el sitio de la mordedura, reacciones anafilácticas, inoculación de toxinas y traumatismo en la piel, sino que también son vectores de diversas enfermedades de gran importancia en salud pública que si no son tratadas a tiempo pueden llegar a causar la muerte de las personas. Por lo cual, es trascendental realizar estudios epidemiológicos y de control de poblaciones de garrapatas, guías médicas para el abordaje de enfermedades (tanto en humanos y animales), implementación de brigadas de educación para la salud (zonas de alta incidencia de enfermedades) y utilización de métodos de control para evitar su expansión. Actualmente, se ha propuesto diseñar y aplicar programas integrados de control para reducir las poblaciones de garrapatas de forma eficaz. Esta estrategia consiste en la aplicación de dos o más métodos como pueden ser el control cultural (manejo de pastos), control biológico (utilización de organismos vivos), control inmunológico (vacunas) y control natural (extractos de plantas y aceites esenciales). Finalmente, se pretende concientizar a la población de la existencia de enfermedades emergentes y reemergentes transmitidas por garrapatas con el fin de implementar estrategias de control adecuadas y tratamientos oportunos en las personas que se encuentran en zonas de riesgo y que conviven con animales de compañía















