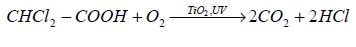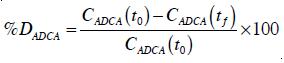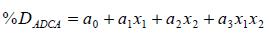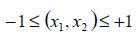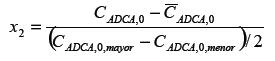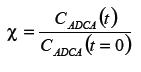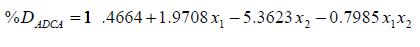Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ingeniería y Desarrollo
Print version ISSN 0122-3461On-line version ISSN 2145-9371
Ing. Desarro. no.24 Barranquilla July/Dec. 2008
Degradación fotocatalítica de ácido dicloroacético al aplicar un campo de radiación de baja energía
Photocatalytic degradation of dichloroacetic acid using a radiation field of low energy
Miguel Ángel Mueses*, José Colina-Márquez **, Fiderman Machuca-Martínez***
* Ingeniero Químico, M. Sc., Grupo de Investigación en Tecnologías Avanzadas de Oxidación GAOX, Escuela de Ingeniería Química, Universidad del Valle, Cali (Colombia). mgmueses@univalle.edu.co
**Ingeniero Químico, candidato a Doctor en Ingeniería, Grupo de Investigación en Tecnologías Avanzadas de Oxidación GAOX, Escuela de Ingeniería Química, Universidad del Valle, Cali (Colombia). jocolina@univalle.edu.co
***Ingeniero Químico, M. Sc., Ph. D., profesor de la Escuela de Ingeniería Química, Grupo de Investigación en Tecnologías Avanzadas de Oxidación GAOX, Universidad del Valle, Cali (Colombia). fiderman@univalle.edu.co
Subvenciones y apoyo: Colciencias y Universidad del Valle (Código interno 2520). Proyecto "Modelamiento y simulación de la cinética intrínseca de reacciones fotocatalíticas heterogéneas".
Fecha de recepción: 11 de julio de 2008
Fecha de aceptación: 29 de agosto de 2008
Resumen
Los efectos de geometría del reactor y concentración inicial de sustrato para una reacción de fotodegradación de ácido dicloroacético (ADCA) con TiO2 - P25 como catalizador al aplicar un campo radiante de baja energía fueron evaluados en tres reactores con diferente geometría y área de absorción. La concentración de catalizador fue constante y la concentración de oxígeno es cercana a saturación a temperatura ambiente.
El desempeño del proceso y la significancia de los efectos fueron evaluados a través del porcentaje de fotodegradación de ADCA y de un modelo de ajuste lineal. La fotodegradación se favoreció en reactores con colectores de radiación difusa, alta superficie de absorción y baja concentración inicial de ADCA. El factor geométrico fue el más influyente en el desempeño del proceso. El modelo obtuvo alta capacidad predictiva con un error global asociado menor al 3.5% y un coeficiente de correlación de 0.98.
Palabras claves: fotocatálisis, reactores fotocatalíticos, ácido dicloroacético, radiación monocromática.
Abstract
The geometry effects in the reactor and the initial concentration of substratum for a reaction of dichloroacetic acid (DCA) photodegradation with TiO2 - P25 as catalyst using a low-energy radiant field, were evaluated in three lab-scale reactors with different geometry and absorption area. The catalyst concentration was constant and oxygen concentration was near the saturation level at room temperature. The process performance and the effect significance were evaluated through the DCA photodegradation percentage and a lineal model. The photodegradation was improved with diffuse-radiation collectors, wide absorption area, and initial low concentration of DCA. The geometric factor had the highest influence in the process performance. The model obtained a high predictive capacity with a global associated error less than 3.5% and a correlation coefficient of 0.98.
Key words: Photocatalysis, Photocatalytic Reactors, Dichloroacetic acid, Monochromatic radiation.index.
INTRODUCCIÓN
La fotodegradación del ácido dicloroacético (ADCA) ha sido implementada recientemente para estudios cinéticos de sistemas fotocatalíticos heterogéneos con dióxido de titanio ( TiO2 ), debido a la simplicidad de la ecuación de estequiometria y fácil seguimiento experimental [1-2].
Este compuesto se ha propuesto como una sustancia patrón en actinometría heterogénea, dado que cumple con propiedades físicas y químicas que permiten considerarlo como un actinómetro químico válido para reacciones de fotodegradación heterogénea con partículas sólidas suspendidas [3].
El ADCA tiene un pKa = 1.29, que ante pH>2 existe en forma iónica. La reacción de fotodegradación es una oxidación isotérmica simple que genera dióxido de carbono ( O2 ) y ácido clorhídrico [1,4]. La ecuación de estequiometría neta para la reacción es:
La oxidación no presenta reacciones competitivas ni de fotolisis directa, fundamentalmente por la longitud de onda de absorción del ADCA nm ADCA λ < 270 [1], la cual es mucho menor a 785 nm, condición límite para absorción de energía por sustancias actinométricas [5].
La degradación del ADCA se basa en el ataque directo del ion dicloroacetato (CCl2 -COO-) por los huecos (h+) fotogenerados por la excitación del catalizador. El oxígeno por su parte es el aceptor de electrones (e-) fotogenerados, que mejora el proceso de fotodegradación por la formación de radicales súperóxido O.2 , además de controlar la etapa de oxidación fotocatalítica y de reducir la probabilidad de recombinación e-/h+ [2].
De otra parte, la fotodegradación de ADCA, al igual que todos los procesos fotocatalíticos heterogéneos, depende no solo del catalizador, sino tambien de variables de proceso como el pH, el flujo luminoso, la concentración del sistema y la geometría del reactor [6].
Las soluciones diluidas de ADCA presentan pH ácidos entre 3.2 y 6.5, dependiendo de la concentración lo cual es beneficioso para el proceso [4]. El flujo luminoso y la geometría del reactor van asociados al desempeño de la fotodegradación. Una buena configuración geométrica y disposición espacial de campo de radiación implican mayor energía absorbida y por tanto, mayores eficiencias de fotodegradación para un flujo luminoso constante [7]. La concentración del sustrato puede afectar las velocidades de recombinación y la actividad del catalizador por efectos de turbidez o neutralización de superficie activa [8].
Con relación a la geometría y concentración inicial del sustrato, investigaciones previas reportadas en la literatura [6, 7] indican que se obtienen mejores rendimientos globales de fotodegradación en reactores irradiados con radiación policromática directa y difusa a concentraciones bajas de sustrato. Se han encontrado pocos trabajos con evidencia experimental comparativa directa que diferencie la significancia de estos dos efectos para con un mismo sistema de reacción en diferentes configuraciones experimentales [7, 9, 10].
En este trabajo se presenta la evaluación comparativa para los efectos de geometría y concentración inicial de ADCA sobre el comportamiento de la fotodegradación, utilizando un campo radiante de baja energía. Para evaluar la significancia de los dos efectos, se implementó un análisis estadístico basado en un modelo de regresión lineal de dos parámetros.
METODOLOGÍA
2.1. Materiales y equipos
Se utilizó ácido dicloroacético (CHCl2COOH) grado analítico Merck® CAS 79-43-6 en el sistema de reacción, dióxido de titanio (TiO2) AEROXIDE® Degussa P-25 como catalizador. Se midieron las concentraciones de iones cloruro por medida de voltaje con un electro do selectivo ORION® modelo 9417BN acoplado a un potenciómetro estándar y a un electrodo de plata / cloruro de plata (Ag / AgCl). El oxígeno (O2 ) se suministró al sistema por burbujeo de aire atmosférico. La concentración de O2 se midió con un oxímetro ORION® - 330 WT-W.
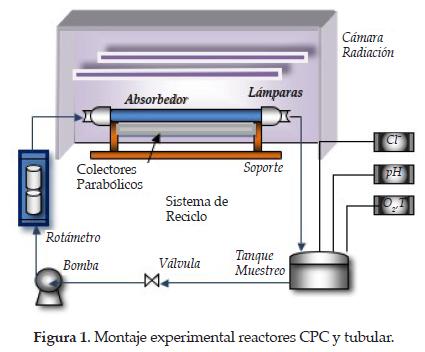
Se evaluaron tres geometrías de reacción: un reactor de colectores parabólicos compacto (CPC) y un reactor tubular, ambos con radiación radial, igual tamaño y sistema de reciclo, y uno con radiación axial. Los reactores CPC y tubular constan de un absorbedor cilíndrico en vidrio PYREX® de 300 mm de longitud, 38 mm de diámetro interno y espesor de 2 mm, ubicado a una distancia de 50 mm debajo de la fuente de radiación y acoplado a un sistema de reciclo. El flujo volumétrico de operación fue de 30 L·min-1 y un volumen total de 7 L( VR /VT= 1). El reactor CPC posee dos colectores de radiación parabólicos (en aluminio), ubicados a 10 mm en la parte inferior axial del tubo absorbedor (véase figura 1).
El reactor axial es un cilindro con agitación magnética hecho de vidrio PYREX® iluminado axialmente y aislado lumínicamente con recubrimiento de aluminio en la superficie periférica radial y la cara inferior. La altura del reactor es de 80 mm, un diámetro interno de 79.6 mm y un volumen de reacción de 400 cm3 ( VR /VT=1 ).
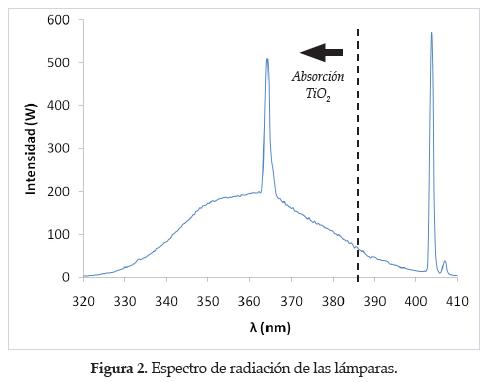
El sistema emisor constó de 6 lámparas negras Opalux T8-FLUBLB de 20 W, con radiación UV superficial actínica y una longitud de onda de operación de 365 nm. El espectro de radiación se presenta en la figura2.
2.2. Diseño experimental
Se implementó un diseño experimental de tipo factorial 3f. Los factores fueron la geometría del reactor (CPC, tubular y axial) y la concentración inicial de ADCA (120, 60 y 30 ppm). Se utilizó una concentración de catalizador de 1 g·L-1. El pH inicial del sistema se ubicó entre 3.2 y 5.6 dependiendo de la concentración inicial de ADCA. La temperatura se estableció en 26ºC ± 1ºC y la concentración de O2 se mantuvo en un 80% de saturación con respecto a la temperatura de operación.
La variable de respuesta fue el porcentaje de fotodegradación de ADCA (D%ADCA ) para una hora de operación. Estas condiciones fueron establecidas a partir de un estudio cinético de fotodegradación de ADCA realizado por Zalazar y colaboradores [1].
2.3. Procedimiento experimental
Los experimentos se iniciaron con la puesta en marcha del sistema de reciclo y burbujeo de oxígeno, para garantizar turbulencia, mezcla perfecta y saturación de O2.
Posteriormente, se realizó una primera medición de las variables del proceso para establecer el punto de referencia inicial: voltaje (para determinar los electrolitos en el agua), pH, oxígeno disuelto y temperatura. Se adicionó el catalizador al tanque y se dejó el sistema por 5 minutos, tiempo en el cual se midieron de nuevo las variables evaluadas en el proceso de fotodegradación.
A continuación se adicionó el ADCA, se dejó por 10 minutos y se midieron las variables del proceso. Inmediatamente después se encendieron las lámparas de radiación. El registro de variables en este instante correspondió al tiempo cero de fotodegradación. Después se registraron datos de las variables con el cambio de voltaje de la solución durante 1 hora de iluminación. Las concentraciones de ADCA fueron obtenidas a través del balance estequiométrico de la ecuación (1).
2.4. Modelo estadístico lineal de dos parámetros
Para evaluar los efectos de geometría y concentración inicial de ADCA se estableció el porcentaje de fotodegradación como variable de respuesta, calculado por la ecuación (2):
Donde %DADCA es el porcentaje de fotodegradación de ADCA,C(tf) y CADCA (to) son las concentraciones de ADCA al final del proceso y en el tiempo cero de fotodegradación, respectivamente.
Se consideró un modelo estadístico multilineal de dos parámetros (ecuación 3) para evaluar la significancia de los efectos establecidos sobre el porcentaje de fotodegradación de ADCA [11]:
Donde a0,a1,a2 son coeficientes de significancia del modelo, los cuales indican qué factor favorece positiva o negativamente al proceso. Las variables x1 y x2 corresponden, respectivamente, a los factores no dimensionales del modelo: x1( geometría) y x2 (concentración inicial de ADCA), con la siguiente restricción:
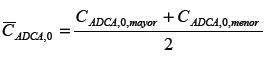
La geometría es un factor cualitativo por lo cual los valores para x1 fueron asignados así: X1,cpc=+1, X1,tubular=0 y X1,axial=-1.La variable x2 se define a través de la ecuación (5):
Los subíndices, "mayor y 0,menor", corresponden a concentración inicial mayor y menor de ADCA, respectivamente.
RESULTADOS, ANÁLISIS Y DISCUSIÓN
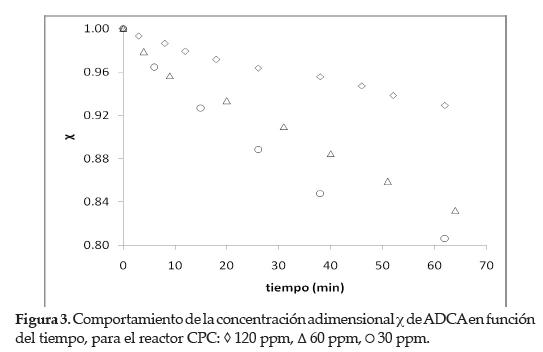
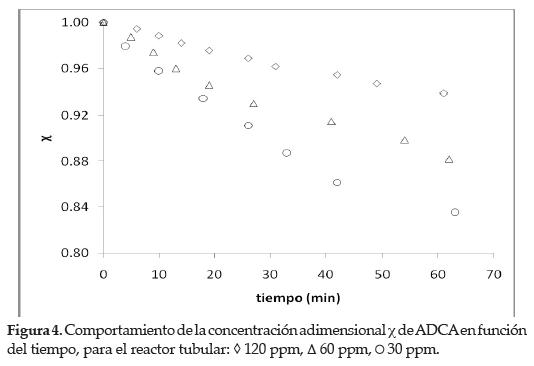
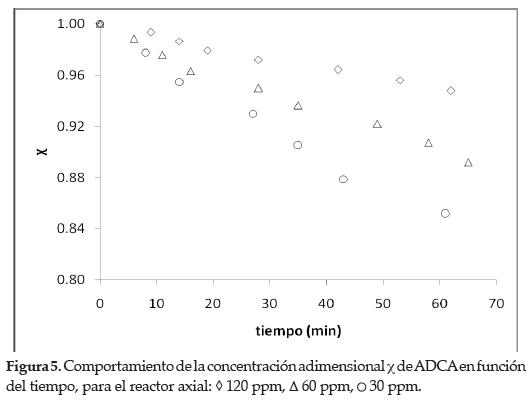
En las figuras 3 a 5 se presenta el comportamiento de la fotodegradación de ADCA en términos de la concentración no dimensional X en función del tiempo, expresada por la ecuación (7):
Donde C ADCA(t) y CADCA (t = 0) ADCA corresponden a la concentración de ADCA en cualquier tiempo y al tiempo cero de operación, respectivamente.
Una primera observación muestra que el proceso de fotodegradación tiene un comportamiento análogo para todas las geometrías evaluadas. Respecto a una misma configuración, la fotodegradación es mayor para la concentración inicial más baja de ADCA establecida y recíprocamente, la fotodegradación es lenta por lo que la concentración inicial es más alta.
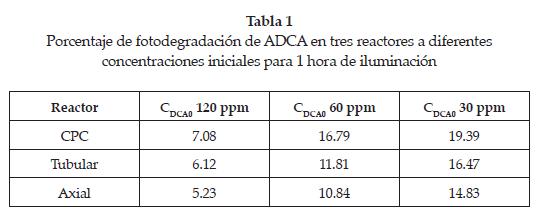
Para visualizar y diferenciar el desempeño de cada geometría evaluada con relación a una misma concentración inicial de ADCA, se determinó el porcentaje de fotodegradación de ADCA (%DADCA) utilizando la ecuación (2). Los resultados se muestran en la tabla 1.
Los resultados muestran que el desempeño del reactor CPC es mayor al tubular y axial cuando se trabaja a una misma concentración inicial de ADCA; es decir, los mayores porcentajes de fotodegradación para una misma concentración se obtienen en el reactor CPC y menores, para el reactor axial.
Estos dos resultados generales pueden atribuirse al efecto que tiene la eficiencia de los huecos fotogenerados a baja concentración [8] y a la forma como entra y se distribuye la radiación en el reactor [7].
De otra parte, para evaluar la significancia de los efectos analizados y el posible sinergismo de estos sobre la fotodegradación de ADCA, se implementó el modelo estadístico de dos variables (dado por las ecuaciones 3 a 6) acoplado a un método de regresión por mínimos cuadrados de múltiples parámetros [3] y por medio del cual se obtiene la ecuación (8):
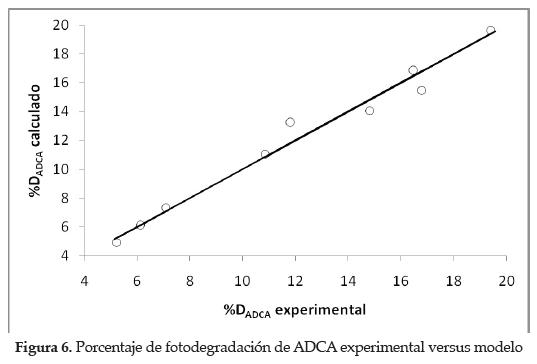
El modelo evaluado tiene una alta capacidad predictiva tal como se muestra en la figura 6, donde se han comparado los valores experimentales con los calculados por el modelo de la ecuación (8). El error global relativo asociado es menor al 3.5% con un coeficiente de correlación de 0.98.
3.1. Campo de energía radiante y absorción de radiación del catalizador
El sistema de emisión disponible puede considerarse de naturaleza monocromática con potencia fotoquímica alta y fotones incidentes de baja energía. El espectro de radiación (véase figura 2), tiene dos picos significativos en 365 nm (cerca del límite superior del UV) y 403 nm (fuera del rango UV). Las magnitudes energéticas de las otras longitudes de onda no son relevantes en el sistema [12]. Esta característica del campo radiante va asociada a las propiedades ópticas del TiO2 dado que la absorción de energía es significativa por debajo de 385 nm [13].
Para que un proceso fotocatalítico sea físicamente posible, la energía de banda prohibida gap + gap E , debe ser menor que la energía irradiada sobre la partícula de catalizador hv > Eg+ap ; de esta forma, se garantiza una alta eficiencia en la generación de duplas electrón-hueco, e-/h+ [14].
El TiO2 DegussaP- tiene un ancho de banda E+gap =3.2 eV (5.1267x10-19 J) y los valores de energía para las longitudes de onda de 365 y 403 nm son, respectivamente, 5.44232x10-19 J y 4.92915x10-19 J. Por tanto, se concluye que para 365 nm gap hν365nm > E+gap y para (403 nm) hν403nm < E+gap.
El resultado anterior indica que la activación del semiconductor es promovida a 365 nm siendo una radiación monocromática de baja energía por la cercanía de hν365nm y E+gap. Esta observación es relevante puesto que no se tendrán fluctuaciones del flujo luminoso y efectos de radiación policromática sobre la fotodegradación de ADCA, donde son explícitos únicamente los efectos antes establecidos (geometría y concentración inicial de ADCA).
3.2. Efecto geométrico
Para una misma concentración inicial de ADCA en las tres geometrías eva- luadas (véanse figuras 3 a 5) la fotodegradación es favorecida en el reactor CPC y presenta menores porcentajes en el tubular y axial, respectivamente (véase tabla 1). Lo anterior puede ser atribuido a la concentración de energía difusa en el sistema y a la configuración de entrada de radiación.
El reactor CPC cuenta con colectores de radiación que concentran la componente difusa del campo de energía radiante [7], la direccionan hacia el absorbedor (tubo de reacción) y la distribuyen con uniformidad en la superficie de absorción no iluminada directamente [15].
Aunque el flujo de radiación fue constante, los colectores del CPC generan un campo radiante con la misma energía, pero distribuido completamente en el área de absorción de reacción. Esta característica lo beneficia en comparación con el reactor tubular. Para lograr similares porcentajes de fotodegradación será necesario utilizar un reactor tubular de mayor área superficial de absorción [7, 16].
De otra parte, la configuración de entrada de radiación es otro elemento rele- vante para la fotodegradación. Los reactores CPC y tubular tienen mayores áreas de absorción de radiación (754 cm2) para bajos cocientes volumétricos ( 05.0/ =RR VV ) en comparación con el reactor axial (50 cm2) con coeficiente volumétrico unitario; por lo tanto, la cantidad de energía incidente sobre las partículas de catalizador será mayor a pesar de su naturaleza fotoquímica de baja energía [16]. Lo anterior implicaría que la cantidad absorbida de energía también es superior, promoviendo mayor cantidad de partículas de catalizador activadas y, por tanto, beneficiando la formación de duplas reactivas electrón – hueco y, finalmente, la fotodegradación [17].
Entonces, el efecto geométrico beneficia la fotodegradación con la presencia de concentradores de radiación difusa y mayores áreas de absorción, lo que resulta consistente con reportes de la literatura [7, 9, 10, 17].
3.3. Efecto de concentración inicial
Para una misma geometría, la fotodegradación se favorece de concentra- ciones iniciales más bajas de ADCA (véanse figuras 3 a 5). Esto se atribuye a la efectividad del ataque de los huecos (h+) libres fotogenerados [8].
La fotodegradación de ADCA, como se mencionó precedentemente, es una oxidación inducida por el ataque de los h+ [1]. Para la misma cantidad de energía absorbida (una misma geometría, flujo luminoso constante y concen- tración de catalizador), la excitación del semiconductor será posiblemente la misma y, por ende, los h+ generados [8]; afunción explícita de las concentraciones.
Para concentraciones más altas de ADCA hay mayor presencia de aniones dicloroacetato y, posiblemente, mayor adsorción de moléculas en la superficie del semiconductor. Esto afecta las propiedades catalíticas del sólido, por efecto de adsorción de moléculas del sustrato, el tipo de enlaces superficiales formados y el potencial redox [4].
El efecto se ve reflejado en los valores ácidos de pH obtenidos: 3.2 para 120 ppm; 3.6 para 60 ppm y 5.6 para 30 ppm; no obstante ser menores al valor del punto cero de carga superficial del catalizador [4]. Este hecho es una limitante para el proceso de fotodegra- dación puesto que las reacciones fotoinducidas consideran el ataque de los h+ a las moléculas adyacentes contenidas en el plano superficial de la partícula y no las moléculas adsorbidas [8,13, 18].
Recíprocamente, a concentraciones bajas de ADCA, aunque la velocidad de recombinación de especies fotogeneradas (e- / h+) es mayor, el ataque de los h+ es más efectivo por la baja presencia local de moléculas en el plano superficial de la partícula, reflejándose en una mayor velocidad global de fotodegradación [8, 18].
3.4. Significancia estadística del efecto geometría-concentración inicial
El análisis precedente permite establecer que la fotodegradación de ADCA es favorecida en reactores con colectores de radiación difusa para una misma concentración inicial más baja de ADCA. La significancia estadística de los dos efectos puede ser evaluada recurriendo a un análisis del modelo propuesto para ecuación (7).
Los parámetros obtenidos para el efecto de geometría y concentración inicial de ADCA son, respectivamente, +1.9708 y −5.3623, lo que indica que el actor más influyente es la geometría del sistema. Los coeficientes positivos indican que la fotodegradación es favorecida a través de los valores altos de la respectiva variable, mientras que los negativos indican un favorecimiento desde los valores bajos [18].
El efecto geométrico está asociado a la configuración de entrada de radia- ción y, por tanto, a la cantidad de energía absorbida por las partículas del semiconductor, que genera mayor actividad catalítica proporcionalmente a la cantidad de radiación absorbida [19]. Si la actividad catalítica es baja, es decir, si la cantidad de energía absorbida no es capaz de generar activación, no habrá un buen desempeño de la fotodegradación incluso a concentraciones bajas de sustrato.
El coeficiente negativo correspondiente a la concentración inicial corrobora las observaciones anteriormente analizadas (véase sección 3.3). En presencia de un flujo luminoso constante y una misma cantidad de energía absorbida (geometría), la fotodegradación se favorece de los valores bajos de la vari- able (concentración inicial de ADCA).
De otra parte, el efecto combinado geometría-concentración inicial mostró un coeficiente de significancia negativo entre -1 y 0 (-0.7985). En la tabla 1 se aprecia que el porcentaje de fotodegradación es mayor cuando se tiene un efecto combinado de las dos variables (≈ 20%), que de los efectos de las variables individuales (<20%). El sinergismo de los efectos permite entonces corroborar el resultado general para la fotodegradación de ADCA, la cual se ve favorecida para reactores con colectores de radiación difusa y altas eficiencias de absorción de radiación y concentración inicial más baja del sustrato.
4. CONCLUSIONES
La fotodegradación de ácido dicloroacético puede ser evaluada con un campo de radiación monocromática de baja energía favoreciendo sola- mente la significancia de los efectos de geometría y concentración inicial de sustrato.
El proceso fue más efectivo en reactores con colectores de radiación difusa y altas superficies absorbentes para una misma concentración inicial. La inter- acción entre las variables (geometría – concentración inicial) permite obtener un efecto de sinergia en la fotodegradación del ácido dicloroacético.
El factor geométrico fue el más influyente en el desempeño de la fotode- gradación. El modelo implementado obtuvo alta capacidad predictiva con un error global asociado menor al 3.5% y un coeficiente de correlación de 0.98.
AGRADECIMIENTOS
Los autores agradecen a la Universidad del Valle, por la financiación. Al grupo de investigación en Óptica Cuántica de esa misma universidad, por la medición del espectro de radiación de las lámparas, y también al programa de apoyo a doctorados nacionales de COLCIENCIAS.
REFERENCIAS
[1] C. ZALAZAR, R. ROMERO, C. MARTIN and A. CASSANO, "Photocatalytic Intrinsic Reaction Kinetics I: Mineralization of Dichloroacetic Acid", Chem. Eng. Sci., 60 (2005), 5240-5254. [ Links ]
[2] C. ZALAZAR, C. MARTIN and A. CASSANO, "Photocatalytic Intrinsic Reaction Kinet- ics II: Effects of Oxigen Concentration on the Kinetics of the Photocatalytic Degradation of Dichloroacetic Acid", Chem. Eng. Sci., 60 (2005), 4311-4322. [ Links ]
[3] F. MACHUCA, J. COLINA-MÁRQUEZ and M. MUESES, "Determination of Quantum Yield in a Heterogeneous Photocatalytic System Using a Fitting-Parameters Model", J. Adv. Oxid. Technol., 11, n.o 1, (2008), 42-48. [ Links ]
[4] D. BAHNEMANN, S. KHOLUISKAYA, R. DILLERT, A. KULAK and A. KOKORIN, "Photo- destruction of Dichloroacetic Acid Catalyzed by Nano-Zised TiO2 Particles", Appl. Catal. B: Env., 36 (2002), 161-169. [ Links ]
[5] H. KUHN, S. BRASLAVSKY and R. SCHMIDT, "Chemical Actinometry", P. Appl. Chem., 76, n.o 12 (2004), 2105-2146. [ Links ]
[6] J. BLANCO, S. MALATO, C. ESTRADA, J. PERAL, B. SÁNCHES and I. CARDONA, "Purificación de aguas por fotocatálisis heterogénea: Estado del Arte", en CYTED Eliminación de Contaminantes por Fotocatálisis Heterogénea Ed. Miguel A. Blesa, La Plata-Argentina (2001), 51 - 76. ISBN 987-43-3809-1. [ Links ]
[7] J. BLANCO, S. MALATO, C. ESTRADA, E. BANDALA, S. GELOVER and T. LEAL, "Diseño de reactores para fotocatálisis: Evaluación comparativa de las distintas opciones", en Eliminación de contaminantes por fotocatálisis heterogénea, Ed. Miguel A. Blesa, La Plata-Argentina (2001), 243 - 266. ISBN 987-43-3809-1. [ Links ]
[8] G. ROTHENBERGER, J. MOSER, M. GRÄTZEL, N. SERPONE and D. SHARMA, "Charge Carrier Trapping and Recombination Dynamics in Small Semiconductor Particles", J. Am. Chem. Soc., 17, n.o 26 (1985), 8054 - 8059. [ Links ]
[9] E. BANDALA, C. ARANCIBIA-BULNES, S. OROZCO and C. ESTRADA, "Solar Photoreactors Comparison Based on Oxalic Acid Photocatalytic Degradation", Solar Energy, 77 (2004), 503 - 512. [ Links ]
[10] M. DIJKSTRA, E. KOERTS, A. BEENACKERS and J. WESSELINGH, "Performance of Inmobilized Photocatalytic Reactors in Continuous Mode", AIChE J., 49, n.o 3 (2003), 734-744. [ Links ]
[11] D. MONTGOMERY, Design and Analysis of Experiments, Wiley, Nebraska (2000), 696, ISBN 0-471-31649-0. [ Links ]
[12] E. SOLARTE, Comunicación personal, Grupo de Investigación de Óptica Cuántica, Universidad del Valle, Cali, Colombia, dic. 14 (2008). [ Links ]
[13] A. WOLD, "Photocatalytic Properties of TiO2", Chem. Mater., 5 (1993), 280- 283. [ Links ]
[14] N. SERPONE, "Relative Photonic Efficiencies and Quantum Yields in Hetero- geneous Photocatalysis", J. Photochem. and Photobio. A: Chem., 104 (1997), 1-12. [ Links ]
[15] J. COLINA-MÁRQUEZ, A. LÓPEZ-VÁSQUEZ and F. MACHUCA-MARTÍNEZ, "Modeling of Solar Direct Radiation in a Compound Parabolic Collector (CPC)" in 13th International Symposium in Solar Energy, Thermoelectric Energy and Chemical Energy, SOLAR-PACES 2006, Seville (Spain), 20-23 Jun. (2006). [ Links ]
[16] A. CASSANO, C. MARTÍN, R. BRANDI and O. ALFANO, "Photoreactor Analysis and Design: Fundamentals and Applications", Ind. Eng. Chem. Res., 34 (1995), 2155-2201. [ Links ]
[17] A. CASSANO and O. ALFANO, "Reaction Engineering of Suspended Solid Heterogeneous Photocatalytic Reactors", Catal. Today, 58 (2000), 167-197. [ Links ]
[18] M. MUESES, Modelo de rendimiento cuántico y campo de radiación efectiva para la determinación de cinética de reacciones fotocatalíticas heterogéneas, Tesis de Maestría en Ingeniería, Escuela de Ingeniería Química, Universidad del Valle, Cali, Colombia (2008). [ Links ]
[19] M. CABRERA, O. ALFANO and A. CASSANO, "Absorption and Scattering Coefficients of Titanium Dioxide Particulate Suspensions in Water", J. Phys. Chem., 100 (1996), 20043-20050. [ Links ]