Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Medicina Veterinaria
Print version ISSN 0122-9354On-line version ISSN 2389-8526
Rev. Med. Vet. no.19 Bogotá Jan./June 2010
El Lipopolisacárido1
Lipopolysaccharide
Stefany Romero Hurtado * / Carlos Arturo Iregui **
1 Grupo de Patobiología Veterinaria Universidad Nacional de Colombia.
* Médica veterinaria de la Universidad de La Salle. M.Sc. (C) en Fisiopatología Veterinaria de la Universidad Nacional de Colombia. Correo electrónico: csromeroh@unal.edu.co
** Médico veterinario de la Universidad Nacional de Colombia. DMV Escuela Superior de Medicina Veterinaria de Hannover, Alemania. Correo electrónico: caireguic@unal.edu.co
Fecha de recepción: julio 26 de 2009.
Fecha de aprobación: febrero 26 de 2010.
Resumen
El lipopolisacárido (LPS) o endotoxina es el mayor componente de la membrana externa de las bacterias Gram negativas, desempeñan una importante función en la activación del sistema inmune al constituir el antígeno superficial más importante de este tipo de bacterias. El LPS está compuesto por una región lípidica y una glicosídica con funciones separadas y/o sinérgicas lo que hace de esta molécula uno de los factores de virulencia más complejos de comprender, esta revisión pretende hacer un acercamiento para dimensionar la universalidad y diversidad de efectos del principal responsable del shock endotóxico inducido por bacterias Gram negativas.
Palabras clave: endotoxina, lipopolisacárido, membrana externa.
Abstract
The lipopolysaccharide (LPS) or endotoxin is the major component of the outer membrane in Gram negative bacterial pathogens; it plays an important role in the activation of the immune system to be the most important surface antigen of Gram negative bacteria. The LPS consist of a lipophilic component and a polysaccharide portion with different function that makes this molecule one of the virulence factors more complex to understand, this review make an approach to measure the diversity effects and universality of LPS.
Keywords: endotoxin, lipopolysaccharide, Gram negative bacteria, outer membrane.
Introducción
La aparición de una molécula capaz de inducir fiebre y enfermedad como consecuencia de una pobre higiene llamó la atención en el siglo XVIII, nombrada en ese entonces como material pirógeno o toxina, cobraría gran importancia en 1872 cuando un bacteriólogo alemán atribuiría la gran mayoría de las muertes en las guerras no a los ataques de tropas contrarias sino a una partícula proveniente de microorganismos a la que llamó Microsporon septicum. En 1874 el patólogo danés Panum, quien extraía sustancias de materia orgánica en descomposición, reportó una sustancia resistente al calor, no volátil, soluble en agua y capaz de inducir fiebre; años más tarde Robert Koch con el desarrollo de las primeras técnicas de cultivo bacteriano, demostró que las bacterias que crecían en éstos, eran capaces de generar sepsis en animales a los que se les inoculaba dichas bacterias; en 1892 Richard Pfeiffer trabajando en el laboratorio de Koch, identificó una molécula resistente al calor proveniente de lisados de Vibrio cholerae causante de shock tóxico en animales, este hecho llamó su atención pues la aparición del shock no se relacionaba con la presencia de bacterias vivas, desde entonces los productos tóxicos secretadas por bacterias vivas se conocieron como toxinas y sus materiales tóxicos constitutivos como endotoxina, (Rietschel & Cavaillon, 2002). Entre 1930 y 1940, gracias al avance en técnicas bacteriológicas, fue posible discernir las primeras características químicas de la molécula, lográndose identificar una porción lipídica y una glicosídica, motivo por el cual recibe el nombre de Lipopolisacárido (LPS). Años más tarde se establecería que el LPS hace parte de la segunda membrana de las bacterias Gram negativas [G(-)] y que no se encuentra en Gram positivas (Rietschel et ál., 1999).
Estructura química
El LPS es una molécula glicolípidica anclada a la membrana externa y considerada como el antígeno de superficie más importante de las bacterias G(-), se estima que una bacteria G(-) posee unas 3,5 * 106 moléculas de LPS que ocupan un área de 4,9 µm2, si la superficie aproximada de una bacteria oscila entre 6-9 µm2 el LPS correspondería a las ¾ partes de la superficie bacteriana, siendo así el mayor componente de la membrana externa en este tipo de microorganismos (Mayeux, 1997; Raetz & Whitfield, 2002).
La molécula se compone de dos regiones principalmente, un glucolípido llamado lípido A y un heteropolisacárido conocido como el núcleo o core unidos entre sí por el azúcar ácido 2-keto-3-deoxioctanato (KDO). El lípido A se le reconoce como la fracción biológicamente activa de la molécula, se trata de un disacárido (glucosamina) unido a ácidos grasos que por lo general son ácido caproíco, laúrico, mirístico, palmítico y esteárico los cuales están insertos en la membrana externa de la bacteria.
El core se subdivide en core externo (formado por hexosas) y en core interno (formado por heptosas). En algunos microorganismos el LPS presenta una región sacárida adicional conocida como antígeno O el cual es un polímero de unidades repetidas que consta de 1 a 8 residuos glicosídicos altamente variable entre especias bacterianas (Mandrell & Apicella, 1993). Dada esta variabilidad se designa a un LPS como lipopolisacárido (LPS) cuando presenta las fracciones lipídicas, core y antígeno O, y como lipooligosacárido (LOS) cuando presenta únicamente las fracciones lipídicas y core, al LPS además se le conoce con el nombre de LPS liso porque al sembrar en agar gel bacterias con este tipo de LPS sus colonias crecen con bordes lisos y al LOS con el nombre de LPS rugoso porque sus colonias crecen con bordes irregulares de apariencia rugosa (Mandrell & Apicella, 1993; Rietschel et ál, 1994) (figura 1).
Propiedades biológicas
Desde su descubrimiento, el LPS y el LOS fueron reconocidos como moléculas con una potente acción endotóxica hasta ser identificadas como los principales responsable del shock inducido por bacterias G(-); en la actualidad, se les atribuyen otras funciones entre las que se incluyen, mantenimiento y organización de la membrana externa, mimetismo molecular, inhibición de anticuerpos, variaciones antigénicas, activador del sistema inmune y mediación en la adherencia a las células y tejidos hospederos, entre otras (Jaques, 1996; Harvill et ál., 2000; Raetz & Whitfield, 2002). A continuación nos centraremos en la función endotóxica y en la función adherente que desempeña esta molécula.
Acción endotóxica
Cuando el LPS es liberado de la membrana de la bacteria como consecuencia de la multiplicación o lisis, entra en contacto con varias proteínas del hospedero, dentro de las que se destacan la proteína de unión al LPS (LBP) y los receptores CD14, TLR4 y MD-2 (Brandtzaeg, 1996; Rietschel et ál., 1996; Backhed et ál., 2003; Lu et ál., 2008). La proteína LBP es la encargada de capturar al LPS y formar el complejo LPS-LBP facilitando, de esta manera, la asociación del LPS con el receptor CD14, el CD14 es un glicoproteina que se encuentra en forma soluble o anclada a la superficie celular de monocitos, macrófagos, polimorfonucleares y células endoteliales que no posee dominio intracitoplasmático y que tiene como función principal transferir el LPS al complejo encargado de su reconocimiento (TLR4/MD-2) (Heumann et ál., 1998; Malhotra et ál.,1998). La MD-2 es una proteína soluble que se asocia con el receptor TLR4 (receptor toll o receptor de proteína transmembrana) para llevar a cabo la transducción del LPS (Haziot, et ál., 1988; O'Neill L, 2000; Akira, 2000; Backhed et ál., 2003). Nuevas investigaciones sugieren que ésta proteína es capaz de unirse al LPS en ausencia del receptor TLR4 originando en menor proporción los efectos del LPS sobre las células del hospedero, por lo que parece que la presencia del TLR4 es esencial tanto para el reconocimiento como para la magnitud de la respuesta generada por el LPS (Shimazu et ál., 1999).
Una vez se ha formado el complejo LPS-TLR4/MD-2, el TLR4 sufre una oligomerización luego de la cual se inicia una reacción que comienza con la interacción con proteínas celulares que poseen dominios TIR (Receptores Toll de Interleuquina 1), las cuales son las encargadas de mediar la relación entre el TLR4 y las proteínas celulares de transducción del LPS; existen cinco proteínas celulares utilizadas por el TLR4 que contienen dominios TIR (MyD88: proteína de diferenciación mieloide; TIRAP: proteína adaptadora del dominio TIR; TRIF: proteína adaptadora asociada al dominio TIR inductora de interferon |3; TRAM: molécula adaptadora relacionada con el TRIF y SARM: proteína inhibidora de la señal del TRIF).
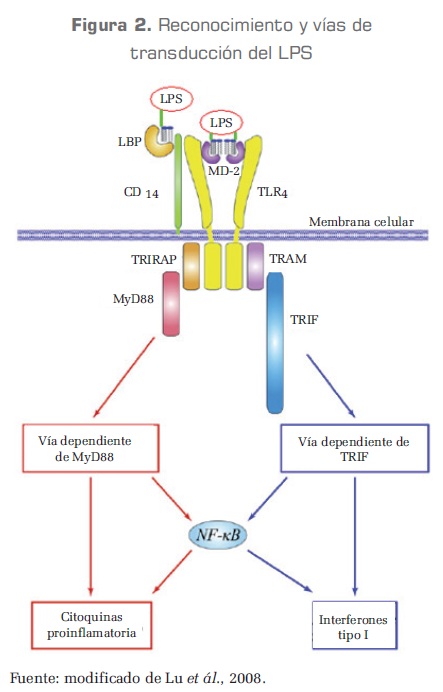
Debido a la utilización de las proteínas con dominios TIR y sus productos finales (citoquinas proinflamatorias o interferones tipo I), la señal de transducción del LPS a través del TLR4 ha sido dividida en dos rutas, la vía dependiente de la proteína MyD88 y la vía dependiente de la proteína TRIF, cada una genera reacciones diferentes que concuerdan en un punto donde activan el factor de transcripción nuclear NF-kB, en condiciones normales (ausencia del LPS) este factor se encuentra en forma inactiva en el citoplasma unido al inhibidor del factor KB (INF-kB), pero tras la señal enviada por las proteínas MyD88 o TRIF se activan quinasas del INF-kB que lo separan del NF-kB y lo activan, una vez activo se transloca al núcleo donde se une a la región promotora de los genes de respuesta inflamatoria generando como respuesta final la trascripción de interferones tipo I (a, pía y (31b) si fue activado por la vía del TRIF y de citoquinas proinflamatorias (IL-1, IL6 y TNF ∞) si ocurrió por la vía de la proteína MyD88 (Cannon et ál., 1990; Pinsky et ál., 1993; Pedreira et ál., 2006; Lu et ál., 2008) (figura 2).
La estimulación del receptor TLR4, la producción de interferones tipo 1 y de citoquinas proinflamatorias inducen varios tipos de respuestas en el organismo tales como, aumento en la permeabilidad vascular, aumento en la expresión de moléculas de adhesión en leucocitos y células endoteliales (Cohen, 2002), estimulación de la producción de nuevas citocinas y quimiocinas, extravasación de neutrófilos para que migren a través del endotelio a los epitelios, activación del factor XII de la coagulación, la fibrinólisis y la vía clásica del complemento. Por ende deben existir vías de inhibición de la señal de transducción del LPS que tiene como fin proteger al hospedero del daño inducido por el LPS (Kobayashi et ál., 2002).
El bloqueo de la señal emitida por el TLR4 puede ocurrir a través de proteínas de superficie celular o por proteínas a nivel citoplasmático; a nivel citoplasmático se encuentran las proteínas TIRAF1 - TIRAF4 (factor 1/4 asociado al receptor de TNF) e IRAK-M (Kinasa 4 asociada al receptor de IL-1) que inhiben al NF-kB y a la proteína MyD88 respectivamente; las proteínas RP105 (radioprotector 105), ST2L (análogo del receptor de IL-1) y la SIGIRR (molécula relacionada con la inmunoglobulina 1) se expresan en la superficie de las células e inhiben directamente al receptor TLR4, a la proteína MyD88 y al TIRAP respectivamente (Liew et ál., 2005). Cuando los mecanismos inhibitorios se agotan y prevalecen las respuestas inducidas por el LPS, los eventos mencionados pueden terminar en shock endotóxico, falla multiorgánica y muerte del hospedero (Suffredini et ál., 1989; Pixley et ál., 1993; Raetz et ál., 2002).
Acción adherente
El papel del LPS en la adhesión a los epitelios ha comenzado a llamar la atención en cuanto a que no sólo actuaría como un potente inmunógeno sino que participaría activamente en el proceso de colonización y establecimiento de la infección en el hospedero al ser la molécula que se encuentra en mayor proporción en la superficie bacteriana. La adherencia de los microorganismos a la superficie epitelial es un paso clave en la patogénesis de las infecciones bacterianas, la actividad del LPS/LOS en la mediación de la adhesión a las células y tejidos fue reconocida por primera vez en bacterias de plantas (Matthysee et ál., 1978; Wolpert and Albersheim, 1971), en 1973 Ma-roudas, sugirió un papel similar en microorganismos que afectan a animales y desde entonces comenzó la investigación para discernir el papel del LPS/LOS en la adhesión bacteriana (tabla 1); sin embargo, los mecanismos por los cuales ocurre esta acción aún no son claros, varios trabajos indican que en ausencia del LPS se inhibe la adhesión de las bacterias (Cohen et ál., 1985; Gupta et ál., 1994; McSweegan & Walker, 1986; Pier et ál., 1996; Valkonen et ál., 1994), otras investigaciones donde se modifican los niveles de expresión y la estructura del LPS señalan una disminución o inhibición de la adherencia en diferentes tipos bacterianos (Francki & Chang, 1994; Mroczenki-Wildey et ál., 1989; Tang et ál., 1996), lo anterior sugiere que esta acción podría ser mediada por alguna de las regiones del LPS/LOS bien sea el lípido A, el núcleo o la cadena o específica.
El proceso de adhesión bacteriana requiere de la expresión, exposición y acoplamiento de ligandos por parte de los microorganismos y de receptores de superficie sobre las células hospederas, los niveles de expresión de las mismos derivan en el estímulo o inhibición de la adhesión de los microorganismos a los epitelios, para los LPS/LOS se sugiere que su papel en la adhesión bacteriana probablemente ocurre a través de interacciones físico-químicas más que a presencia de receptores sobre la superficie de las células del hospedero, las hipótesis sugieren que la atracción entre los LPS/LOS y las células sería mediada por moléculas de agua (H20) o por proteínas presentes en las superficies epiteliales (líquido periciliar).
A través del agua, el mecanismo sugerido es que la porción hidrófoba de los LPS/LOS es decir el lípido A (fracción cargada negativamente) por afinidad química tenderá a entrar en contacto con las moléculas hidrófobas del líquido periciliar (proteínas) esto con el fin de minimizar el número de interacción con el H20 presente en el líquido, esa atracción haría que las proteínas se desplazaran de su ubicación original hasta hacer contacto con el lípido A permitiendo así la exposición de la superficie celular y el contacto bacteria-célula (Butrus & Klotz, 1990; Dazzo et ál., 1976; Klotz et ál., 1989; Maroudas, 1973).
Además, se propone que la estructura del LPS/LOS sería la responsable de la acción adhesiva, así en un LPS liso al ser más largo el medio que lo rodea tiene tres regiones en las que puede fijarse; sin embargo, se cree que la región más llamativa sería el antígeno O haciendo menos evidente al núcleo y al lípido A de la molécula. Por lo general, los azúcares que hacen parte del antígeno O son de tipo neutro tales como arabinosa, galactosa, manosa, etc.; al no tener carga estos azúcares, las interacciones con el medio son débiles o no se dan siendo incapaz este LPS de formar uniones con moléculas que lo rodean. Es decir, que aunque es llamativo para el medio es menos atractivo para la formación de nuevas interacción, por ejemplo, con proteínas del líquido periciliar; mientras que en un LOS lo más llamativo es el núcleo y el lípido A los cuales poseen cargas positivas y negativas siendo estos atractivos para la formación de puentes de H+ con átomos de 02 o de N+ de las proteínas del medio e igualmente la hipótesis de las interacciones fisicoquímicas arriba descritas con la formación de los nuevos enlaces las proteínas del líquido periciliar se desplazarían de su ubicación original y se expondría la superficie epitelial lo que daría lugar a la adhesión bacteriana y un posible establecimiento de la infección (Atabek & Camesano, 2007).
No obstante, se han descrito algunos receptores tipo lectina para los LPS/LOS principalmente en leucocitos, se conoce por ejemplo que la región polisacárida es capaz de unirse a receptores de manosa y que el núcleo puede unirse a receptores KDO en macrófagos (Morrison & Ryan, 1992). Por su parte, Parent (1990) identificó unos receptores similares a lectinas para el núcleo de los LPS/LOS en la membrana citoplasmática de hepatocitos de ratas; sin embargo, aún no se conocen en detalle receptores en membranas de células epiteliales y mucosas que pudieran estar jugando un papel fundamental en el inicio y establecimiento de las infecciones bacterianas (Jaques, 1996).
Conclusiones
El LPS/LOS es una molécula compleja de funciones alternantes dentro de las que se destacan su propiedad estimulatoria del sistema inmune y su capacidad de mediar la adhesión de las bacterias a los epitelios; el reconocimiento de las rutas de transducción del LPS/LOS así como las de regulación y control son determinantes para el entendimiento de los efectos potencialmente malignos que puede tener esta molécula una vez es liberada de la membrana externa de los microorganismos G(-).
Nuevas investigaciones apuntan hacia el establecimiento del papel que desempeña el LPS/LOS en diferentes especies de bacterias G(-) en la adherencia a las células epiteliales, se propone que está molécula no sólo se comportaría como endotoxina sino que además podría actuar como una adhesina facilitando la unión de las bacterias a las células permitiendo que la infección se establezca o acreciente, de tal manera que los tratamientos contra infecciones por bacterias G(-) no solamente deberían incluir a las bacterias sino además al LPS como posible inductor y potenciador de este tipo de infecciones.
BlBLIOGRAFIA
Akira, S. "Toll-like receptors: lessons from knockout mice". Biochem Soc. Trans. 28. (2000): 551-556. [ Links ]
Atabek, A. & Camesano, T. A. "Atomic Force Microscopy Study of the Effect of Lipopolysaccharides and Extracellular Polymers on Adhesion of Pseudomonas aeruginosa". J. Bacteriol. 189. (2007): 8503-8509. [ Links ]
Backhed, F; Normark, S.; Schweda, E.; Oscarson, S. & Richter-Dahlfors, A. "Structural requirements for TLR4-mediated LPS signalling: a biological role for LPS modifications". Microbes Infect. 5. (2003):1057-1063. [ Links ]
Brandtzaeg, P. "Significance and pathogenesis of septic shock". Curr Top Microbiol Immunol. 216. (1996): 16-37. [ Links ]
Butrus, S.I. y Klotz, S. "Contact lens surface deposits increase the adhesion of Pseudomonas aeruginosa". Curr Eye Res. 9. (1990): 717-724. [ Links ]
Cannon, J.G, Tompkins, R.G.; Gelfand, J.A; Michie, H.R. & Standford, G.G. "Circulating interleukin-1 and tumor necrosis factor in septic shock and experimental endotoxin fever". J Infect Dis .161. (1990): 79-84. [ Links ]
Cohen, P.S.; Arruda, J.C.; Williams, T. & Laux, D. "Adhesion of a human fecal E.coli strain to mouse colonic mucus". Infect Immun. 48. (1985): 139-145. [ Links ]
Cohen, J. "The inmmunopathogenesis of sepsis". Nature 420. (2002): 885-891. [ Links ]
Dazzo, F. B.; Napoli, C. A.; Hubbell, D. H. "Adsorption of bacteria to roots as related to host specificity in the Rhizobium-clover symbiosis". Appl Environ Microbiol 32. (1976): 166-171. [ Links ]
Fletcher, E.L.; Fleiszig, S.M.J. and Brennan, N.A. Invest. Ophthalmol. Vis. Sci. 34. (1993): 1930-1936. [ Links ]
Francki, K. T. & Chang, B.J. "Variable expression of O-antigen and the role of lipopolysaccharide as an adhesin in Aeromonas sobria". Microbiol Lett. 122. (1994): 97-102. [ Links ]
Gupta, S.K.; Berk, R. S.; Masinck, S. & Hazlett, L, D. "Pili and lipopolysaccharide of Pseudomonas aeruginosa bind to the glycolipid asialo GM1". Infect. Immun. 62. (1994): 4572-4579. [ Links ]
Harvill, E.; Preston, A.; Cotter, P.; Allen, A.; Maskell, D.; & Miller, J. "Multiple roles for Bordetella lipopolysaccharide molecules during respiratory tract infection". Infect iInmmun. 68. (2000): 6720-6728. [ Links ]
Haziot, A.; Chen, S. & Ferrero, E. "The monocyte differentiation antigen, CD14, is anchored to the cell membrane by a phosphatidylinositol linkage". J Immunol 141. (1988): 547-552. [ Links ]
Heumann, D.; Glauser, M.P. & Calandra, T. "Molecular basis of host-pathogen interaction in septic shock". Curr Opin Microbiol. 1. (1998): 49-55. [ Links ]
Izhar, M.; Nuchamowitz, Y. and Mirelman, D. "Adherence of Shigella flexneri to guinea pig intestinal cells is mediated by a mucosal adhesion". Infect. Immun. 35. (1982): 1110-1118. [ Links ]
Jaques, M. "Role of lipo-oligosaccharides and lipopolysacharides in bacterial adherence". Trends and microbiology.; 4. (1996): 408-410. [ Links ]
Kobayashi, K.; Hernandez, L.D.; Galan, J.E.; Janeway, J.R, Medzhitov, R. & Flavell, RA. "IRAK-M is a negative regulator of Toll-like receptor signaling". Cell. 110. (2002): 191-202. [ Links ]
Klotz, S. A.; Butrus, S. I.; Misra, R. P. & Osato, M.; S. "The contribution of bacterial surface hydrophobicity to the process of adherence of Pseudomonas aeniginosa. to hydrophilic contact lenses". Cmr Eye Res. 8. (1989): 195-202. [ Links ]
Morrison, D.C. & Ryan, J.L. "Bacterial Endotoxic Lipopolysaccharide". Molecular Biochemistry and Cellular Biology. (1992): 253-267. [ Links ]
Liew, F.Y.; Xu, D.; Brint, E.K. & O'Neill, LA. "Negative regulation of Tolllike receptor-mediated immune responses". Nat Rev Immunol. 5. (2005): 446-458. [ Links ]
Lu, Y.C.; Yeh, W.C. & Ohashi, S,P "LPS/TLR4 signal transduction pathway". Cytokine 42. (2008): 145-151. [ Links ]
Malhotra, R.; Priest, R.; Foster, M.R. & Bird MI. "P-selectin binds to bacterial lipopolysaccharide". Eur J Immunol. 28. (1998): 983-988. [ Links ]
Mandrell, R.E. and Apicella, M.A. "Lipo-oligosaccharides (LOS) of mucosal pathoegns: molecular mimicry and host-modification of LOS". Immunobiology. 187. (1993): 382-402. [ Links ]
Maroudas, N.G. "Chemical and mechanical requirements for fibroblast adhesion". Nature (London). 254. (1993): 695-696. [ Links ]
Matthysse, A. G.; Wyman, P. M. & Holmes, K. V. "Plasmid-dependent attachment of Agrobacterium tumefaciens to plant tissue culture cells". Infect Immun. 22. (1978): 516-522. [ Links ]
Mayeux, R. P. "Pathobiology of lipopolysaccharide". J Tox Environm Health. 51. (1997): 415-435. [ Links ]
McSweegan, E. & Walker, R.; I. "Identification and characterization of two Campylobacter jejuni adhesins for cellular and mucous substrates". Infect Immun. 53. (1986): 141-148. [ Links ]
Mroczenski-Wildey, M.J.; Di Fabio, J.L. and Cabello. EC. "Invasion and lysis of HeLa cell monolayers by Salmonella typhi: the role of lipopolysaccharide Microb". Pathog. 6. (1989): 143-152. [ Links ]
O'Neill L. "The Toll/interleukin-I receptor domain: a molecular switch for inflammation and host defence". Biochem Soc Trans. 28. (2000): 557-563. [ Links ]
Palomar, J.; Leranoz, A.M. & Vinas, M. "Serratia marcescens adherence: the effect of O-antigen presence". Microbios. 81. (1995): 107-113. [ Links ]
Paradis, S. E,. Dubreuil, D.; Rioux, D.; Gottschalk, M. & Jacques M. (1994). "High-molecular-mass lipopolysaccharides are involved in Actinobacillus pleuropneumoniae adherence to porcine respiratory tract cells". Infect Immu. 62. (1994): 3311-3319. [ Links ]
Parent, J.B. Biol. Chem. 265. (1990): 3455-346. [ Links ]
Pedreira, PR.; Garcia, E.P; Albaiceta, CM. & Taboada, F "Puesta al dia en medicina intensiva: sindrome de distres respiratorio agudo". Med Intensiva. 30. (2006): 149-150. [ Links ]
Pier, G. B.; Grout, M.; Tanweer, S.; Zaidi, Olsen, J.; Johnson, G.; Yankaskas, R. J. & Goldberg, B. J. "Role of Mutant CFTR in Hypersusceptibility of Cystic Fibrosis Patients to Lung Infections". Science. 271. (1996): 5264-5267. [ Links ]
Pinsky, M. R.; Vincent, J. L.; Deviere, J.; Alegre, M.; Kahn, R. J. & Dupont, E. "Serum cytokine levels in human septic shock Relation to multiple-system organ failure and mortality". Chest. 103. (1993): 565-575. [ Links ]
Pixley, R.A.; De la Cadena R.; Page, J.D.; Kaufman, N.; Wynshock, E.G. & Chang. "The contact system contributes to hypotension but not disseminated intravascular coagulation in lethal bacteremia. In vivo use of a monoclonal anti-factor XII antibody to block contact activation in baboons". J Clin Invest. 91. (1993): 6-8. [ Links ]
Raetz, C. & Whitfield, C. "Lipopolysaccharide endotoxins". Annu. Rev. Biochem. 71. (2002): 635-700. [ Links ]
Rietschel, E. T; Kirikae, T; Shade, Fu.; Mamat, U.; Schmidt, G.; Lappnow, H.; Ulmer, A.J.; Zahringer, U.; Seydel, U. & Di Padova, EE. "Bacterial endotoxin: molecular relationships of structure to activity and function". FASEB. 8. (1994): 217-225. [ Links ]
Rietschel, E.T,; Brade, H.; Hoist, O.; Brade, L.; Muller-Loennies, S. & Mamat, U. "Bacterial endotoxin: Chemical constitution, biological recognition, host response, and immunological detoxification". Curr Top Microbiol Immunol. 216. (1996): 39-81. [ Links ]
Rietschel, E. T; Westphal, O.; Brade, H.; Opal, S. M.; Vogel, S. N.; Morrison. & Marcel, D. C. "History of Endotoxins". Endotoxins in Health and Disease. (1999):1-30. [ Links ]
Rietschel, E. T. & Cavaillon, J.M. "The endotoxina". J Endotoxin 14. 2. 8 (2002) : / 1-12. [ Links ]
Shimazu, R.; Akashi, S.; Nagafuku, M.; Ogata, M.; Nagai, Y.; Fukudome, K.; Miyake, K. & Kimoto, M. "MD-2 a molecule that confers lipololysaccharide responsiveness on Toll- Like receptor 4". J. Exp Med. 189. (1999): 1777-1782. [ Links ]
Suffredini, A.E; Fromm, R.E.; Parker, M.M.; Brenner, M.; Kovacs, J.A.; Wesley, RA. & Parrillo, J. "The cardiovascular response of normal humans to the administration of endotoxin". N Engl J Med. 321. (1989): 280-287. [ Links ]
Tang, H. B.; DiMango, E.; Bryan, R.; Gambello, M.; Iglewski, B.H.; Goldberg, J. B. & Prince, A. "Contribution of specific Pseudomonas aeruginosa virulence factors to pathogenesis of pneumonia in a neonatal mouse model of infection". Infect. Immun. 64. (1996): 37-43. [ Links ]
Valkonen, K. H; Wadström. T. & Moran, A. P "Interaction of lipopolysaccharides of Helicobacter pylori with basement membrane protein laminin". Infect and Immun. 9. (1994): 3640-3648. [ Links ]
Wolpert, J. S. & Albersheim, P. "Host-symbiont interactions. I. The lectins of legumes interact with the O-antigen-containing lipopolysaccharides of their symbiont Rhizobia". Biochem Biophys Res Commun. 70. (1976): 729-737. [ Links ]