Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Investigaciones Marinas y Costeras - INVEMAR
Print version ISSN 0122-9761
Bol. Invest. Mar. Cost. vol.28 no.1 Santa Marta Jan./Dec. 1999
ESTUDIO EPIZOOTIOLÓGICO DE PENAEUS VANNAMEI EN TRES FINCAS CAMARONERAS DEL CARIBE COLOMBIANO
EPIZOOTIOLOGICAL STUDY THE PENAEUS VANNAMEI IN TREE FARMS OF THE COLOMBIAN CARIBBEAN.
Adriana Vallejo Isaza1 y Federico Newmark U2.
1. Universidad de Córdoba Sede Lorica, Facultad de medicina Veterinaria y Zootécnia, Departamento de Acuicultura. Lorica, Córdoba. E-mail: ucdacuic@ns.unicordoba.edu.co (A.V.I.).
2. Instituto de Investigaciones Marinas y Costeras (INVEMAR), A.A. 1016 Santa Marta, Colombia. E-mail: fnewmark@invemar.org.co (F.N.U)
RESUMEN
Con el fin de determinar la presencia de las enfermedades que afectan los cultivos semi-intensivo de camarones marinos Penaeus vannamei, un estudio epizootiológico fue realizado entre junio de 1994 y agosto de 1995, en tres fincas localizadas a lo largo de la Costa Caribe colombiana. Mediante el examen externo de muestras poblacionales se determinó la presencia de signos clínicos, con el subsecuente análisis de laboratorio empleando técnicas histológicas; la prevalencia de agentes infecciosos tales como bacterias, hongos, protozoos, cuerpos de inclusión viral y algunas alteraciones histopatológicas fueron estudiadas con el fín de establecer su posible relación con las manifestacines clínicas observadas. La presencia de algunos virus como Baculovirus penaei, IHHNV, TSV y LOVV fue determinada mediante la observación del efecto citopático característico de cada uno de estos agentes en los tejidos. Se realizó un análisis de regresión logística con el cual se relacionaron algunos signos clínicos con la presencia de los agentes infecciosos y el factor de riesgo de cada enfermedad; así, camarones con tumores y deformidades registraron un riesgo casi dos veces mayor de presentar cuerpos de inclusión Cowdry tipo A (CAI’s), que aquellos sin deformidades. De manera análoga, el factor de riego de presentar alteraciones en el órgano linfoide (O.L) fue mayor en camarones sobrevivientes expuestos a la infección del TSV, que aquellos que no lo estuvieron. Infecciones bacterianas e infestaciones por protozoos también fueron analizadas. Algunas diferencias relacionadas con la presencia prevalencia de algunas enfermedades dependiendo de la localización geográfica de las fincas y sus diferentes condiciones climáticas en las cuales los cultivos fueron iniciados, son discutidas.
PALABRAS CLAVE: Camaronicultura, patologia, Penaeus vannamei, Caribe colombiano.
ABSTRACT
An epizootiological study of the mayor deseases affecting the penaeid shrimp Penaeus vannamei was performed from june 1994 throuh august, 1995 in tree farms located on the colombian Carebbean coast. The presence and prevalence of infectious agents such as bacteria, protozoa, viral inclusions bodies and changes histopatologicals was determinated by means of gross examination and histological analysis.. The relationship between these infection agents and specific disease was also studies. The presence of some viruses such a Baculovirus penaei, IHHNV, TSV and LOVV, were determinated by demostration of the cytopathical effects characteristic of these agent. Additionaly, a logistic regression analysis was used to determine the relationship between some clinical signs and the presence of the infectious agent; the risk factor of having the disease, was also determinated; thus, shrimp with tumors and deformities presented a risk almost two times higher having IHHNV disease, as determined by the presence of inclusion bodies Cowdry A (CAI’s) than those whitout deformities; in an analogous way, the risk factor of presenting alterations in the lymphoid organ (L.O) was higher in organisms that have exposed to the TSV desease, than in those were not. Bacterial infections an infestations by protozoa were also analyzed. Some differences concerning the presence and prevalence of some of the diseases according to the geographical location of the farms and the different climatic conditions in such the cultivation started, wer observed. Some physical-chemical variables such as salinity, where related to the presence and prevalence of some clinical signs.
KEY WORDS: Shrimp aqyuaculture, pathology, Penaeus vannamei, Caribbean colombian.
INTRODUCCION
El cultivo del camarón marino es una de las actividades actuales más importantes en el sector agroindustrial colombiano. Se inició en la costa Caribe colombiana hace ya cerca de tres décadas en sistemas semi-intensivos con Penaeus schmitti, especie nativa de la costa Atlántica, pero remplazada luego por la especie del Pacífico P. vannamei (y en menor escala P. stylirostris), por su buen crecimiento en altas densidades y resistencia a cambios en la salinidad, constituyéndose como la de mayor importancia en esta área (Weinder, 1992).
Con el creciente desarrollo de esta actividad, la importación de semilla y el deterioro ambiental de los ecosistemas acuáticos costeros, continuamente se presenta en este tipo de actividad el establecimiento de diversos agentes patógenos tales como virus, bacterias, hongos, protozoos y algunos metazoos, afectando de manera significativa la producción (Vallejo, 1996).
De acuerdo con Brock (1995), hasta el momento se han reportado cerca de 17 virus causantes de enfermedad en camarones penaeidos; entre éstos, Baculovirus penaei, Baculovirus tipo monodon (BMV), virus de la necrosis infecciosa hipodermal y hematopoyética (IHHNV), Parvovirus hepatopancreático (HPV), virus de la vacuolización del órgano linfoide (LOVV), Reo III, y el virus tipo síndrome de Taura (TSV), han sido registrados en los cultivos de camarones de Suramérica. El último de estos virus es considerado en la actualidad, como uno de los agentes infecciosos de mayor relevancia, responsable de la disminución de 60% a 85 % en promedio de la sobrevivencia de los camarones. En la costa Caribe colombiana, TSV fue reportado por primera vez en noviembre de 1994 (Brock, 1995) en fincas camaroneras localizadas en la franja costera continental del litoral Caribe en la Bahía de Cispatá, Departamento de Córdoba, y posteriormente fue detectado en otras fincas ubicadas hacia la costa noreste del país (CENIACUA, 1996). Aunque se han presentado registros sobre enfermedades donde se menciona además el efecto del TSV sobre la producción del área del Caribe colombiano (CENIACUA, 1996), este es el primer estudio de tipo epizootiológico de camarones en Colombia que establece la prevalencia de diversos signos clínicos y su relación con agentes infecciosos, incluyendo el TSV.
A través de un estudio epizootiológico e histopatológico se pretendió determinar el estado sanitario en tres fincas camaroneras que cultivan P. vannamei, haciendo especial referencia a las infecciones producidas por virus. De otro lado, mediante un análisis de regresión logística se busca establecer la relación entre los signos clínicos observados y los resultados histopatológicos a fin de obtener finalmente un factor que ayude a determinar el riesgo de presentar un agente infeccioso o ciertas alteraciones citológicas.
AREA DE ESTUDIO
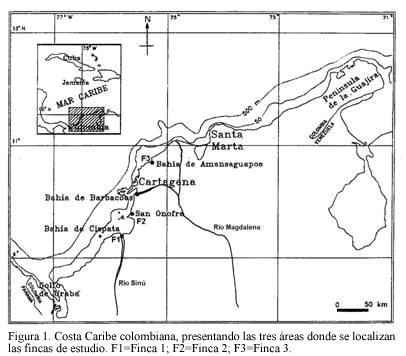
El presente estudio se realizó en tres fincas camaroneras localizadas en la franja costera continental del litoral Caribe colombiano entre los 75o y 76o longitud oeste, y 9o y 11o latitud norte, entre la Bahía de Cispatá en el Departamento de Córdoba y la Bahía de Amanzaguapos en el Departamento de Bolívar (Figura 1). Climatológicamente, el área de estudio presenta un período lluvioso de mayo a noviembre con una precipitación promedio anual de 500 a 1200 mm y una temperatura media de 27o a 29oC. El período seco entre diciembre y abril presenta temperatura media entre 29oC y 31oC (COLCIENCIAS-BID, 1989).
La finca camaronera ubicada en la Bahía de Cispatá (F1), presenta gran influencia del Río Sinú, el cual se desborda en épocas de lluvias creando un permanente flujo y reflujo de aguas de variable salinidad y transportando una alta carga de sedimentos con una alta concentración de nutrientes, elevando el de pH a valores superiores a 7.0 (Patiño y Flórez, 1993). En la actualidad, el incremento en el uso de fertilizantes y agroquímicos transportados a la Bahía por las redes de riego de los cultivos de algodón, sorgo y arroz, constituyes una fuente adicional de contaminación para el ecosistema (CORPES, 1992).
La finca de cultivo ubicada en la zona de la Bahía de Barbacoas (F2), presenta una influencia directa de las descargas del Río Magdalena. Esta zona posee características de estuario debido a la presencia del Canal del Dique y es allí donde se encuentran concentradas la mayoría de fincas camaroneras, con aproximadamente 600 ha en producción (Weidner, 1992).
Por su parte la zona de la Bahía de Amanzaguapos en cercanías al municipio de Santa Catalina (Dpto. Bolívar), se caracteriza por la presencia de bosque seco a semiseco. La finca de estudio en esta zona (F3), se abastece del agua proveniente de la Ciénaga La Redonda la cual se comunica a través de unas compuertas con la Ciénaga del Totumo, caracterizada por ser de agua dulce. Estas compuertas sólo son abiertas en épocas de invierno para controlar las inundaciones.
MATERIALES Y METODOS
Con una frecuencia mensual, en cada finca se estudió una piscina durante tres ciclos de producción consecutivos (110 a 120 días por ciclo), en el período comprendido entre junio de 1994 y agosto de 1995. El primer ciclo (C1) comprendió entre junio y octubre de 1994; el segundo ciclo (C2) entre noviembre y febrero de 1995 y el tercer ciclo (C3), entre abril a julio (agosto para la F1) de 1995.
Toma de muestras
Para proporcionar un 95 % de probabilidad de que los especímenes afectados estén incluidos en la muestra, se realizó un muestreo aleatorio de la población (tipo cohorte) de aproximadamente 100 individuos (Brock, 1995). En el primer mes de muestreo, las post-larvas se recolectaron de los tanques de aclimatación antes de ser inoculadas a las piscinas. Estas post-larvas fueron de diferente procedencia, dependiendo del proveedor de cada finca.
La muestra recolectada fue examinada en su totalidad, manteniendo a los camarones vivos en baldes con recambio constante de agua utilizando una bomba sumergible. En cada uno de ellos, se registró información sobre la especie, el sexo, la longitud estándar (desde la base del ojo hasta el extremo del telson) y la textura del exoesqueleto. Se examinaron externamente, tomando como criterios de signo clínico de enfermedad los parámetros propuestos por D.V.Lightner (com. pers., 1993): coloración anormal en cualquiera de sus partes corporales, señales y áreas melanizadas, deformidades abdominales, rostro deforme, textura de la cutícula, talla pequeña, coloración y/o decoloración anormal de las branquias, etc. Los camarones que presentaron signos clínicos aparentes o evidentes de enfermedad y al menos uno aparentemente sano, fueron fijados por inyección e inmersión en una solución FAA de Davidson previamente preparada y luego de 24 a 72 horas se preservaron en etanol al 70% para su posterior análisis histopatológico (Bell y Lightner, 1988). Las observaciones fueron registradas en un formato anamésico y transferidas a una base de datos para el análisis de la información.
Diagnóstico histopatológico
De los camarones fijados, se escogieron entre cinco (5) y siete (7) ejemplares con signos de enfermedad, disectando todo el cefalotórax en un corte longitudinal medio, para observar órganos internos; una sección longitudinal-sagital para observación de branquias y cortes transversales de los segmentos abdominales I, III y VI. Las muestras de camarón fueron procesadas, seccionadas (5 mm de grosor) y teñidas con hematoxilina & eosina-floxina (H&E), según Bell y Lightner (1988). Los cortes histológicos fueron examinados con un microscopio óptico a 10, 40 y 100X aumentos, analizando todos los tejidos visibles en el corte y registrando agentes infecciosos o alteraciones tisulares presentes. Las observaciones fueron consignadas en un formato en términos de presencia (1) y ausencia(0).
Análisis epidemiológico
Se determinó la prevalencia (Pr) de los signos clínicos a partir de la muestra de la población, de acuerdo con la ecuación propuesta por Daniel (1980):
Pr = número de casos con signo clínico de enfermedad x 100
número total de individuos examinados
En este análisis se estableció la relación particular de cada signo clínico y la relación generalizada de todos los signos clínicos por finca y por ciclo de cultivo.
Grado de severidad
Para algunas variables se obtuvo el grado de severidad de infección o infestación de manera semicuantitativa teniendo en cuenta la cantidad de tejidos afectado por superficie examinada. De acuerdo con Brock (1995), se asignaron categorías de 4 a 0, así: el grado-4 para los tejidos severamente afectados (un cubrimiento total); el grado-3 para aquellos muy afectados (un cubrimiento del 50 al 75 % de la superficie); grado-2 para los relativamente afectados (del 25 al 50% de la superficie) y grado-1 para aquellos levemente afectados (hallazgos a partir de una partícula extraña hasta un 25% de la superficie afectada); la categoría cero (0) fue asignada cuando no se observó agente o daño alguno. Cada una de estas categorías se registró independientemente de manera dicotómica (1) presencia ó (0) ausencia.
Análisis del riesgo
Mediante modelos de regresión logística, se relacionó la variable dicotómica “diagnóstico histológico o análisis histológico” (Yi), con un conjunto de “signos clínicos” (K variables X1 ...Xk), basado en la función de probabilidad, donde,
P (Y=1| X) = pi (X)
Así, pi (X) en términos epidemiológicos, se define como el Riesgo individual de adquirir una enfermedad dados determinados valores de las variables explicativas (Kleinbaum, 1994).
RESULTADOS
Estudio epizootiológico
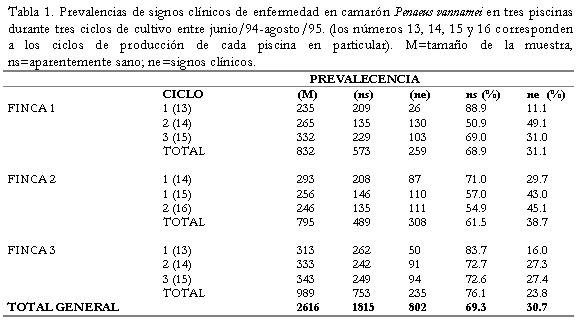
Prevalencia de los signos clínicos. Se examinaron un total de 2616 camarones durante un período de doce (12) meses correspondientes a tres ciclos de cultivo (Tabla 1). Se estableció que el 30.7 % de los camarones examinados presentaron al menos un signo clínico aparente o evidente de enfermedad. La mayor prevalencia de signos clínicos se presentó en la Finca 2 con un 38.7 %, mientras que la menor se observó en la F3 con el 23.8 %. Por su parte, en los ciclos 2 y 3 se presentaron los más altos índices de signos clínicos registrados en el presente estudio, con un máximo de 49.1 % correspondiente al ciclo 2 de la Finca 1.
En el examen in vivo de los ejemplares, se encontraron diversos signos aparentes de enfermedad, tales como: cambios en el color del individuo, textura blanda, manchas, laceraciones y ulceraciones cuticulares, deformidades corporales; enanismo (tamaño pequeño con relación al promedio general), etc. La (Tabla 2) presenta la prevalencia de los principales signos clínicos presentes en el estudio. Apéndices y branquias ennegecidas constituyeron el índice más alto de los signos clínicos (5.3%), seguido de la prevalencia de tumores y/o deformidades corporales (principalmente en el tercer segmento abdominal) con 5.2%. Esta última condición junto con los individuos enanos 2.6% (n=2616), se presentaron en forma variable en las tres fincas, siendo la F3 aquella con los más altos índices (21.1 y 8.7% respectivamente); en contraste, las otras dos fincas se observaron prevalencias para estas características de 4 y 2 % respectivamente. En la finca F3, el ciclo de cultivo de mayor prevalencia de deformidades fue el Ciclo 2 (noviembre/94-febrero/95) con un máximo de 16.8 %. De otro lado, la prevalencia de organismos con rostro deforme fue característico de la F2, en la cual se presentó un elevado índice de camarones con esta condición en el Ciclo 3 (11.4 %), en contraste con la F3 en la que la prevalencia fue menor del 1% . Los totales integrados para la prevalencia de necrosis cuticular focal fue de 3.9 % y la presencia de camarones con músculo opaco de 3.2 %.
Determinación de agentes patógenos
Durante todo el estudio se analizaron histológicamente un total de 232 camarones. Las alteraciones citopatológicas para cada órgano y tejido se reportan en la (Tabla 3). Los virus encontrados y las alteraciones acompañantes se describen a continuación:
Baculovirus penaei (BP). Únicamente en los estadíos post-larvales antes de ser inoculados a las piscinas fueron observados cuerpos de inclusión polihédricos (CIP) en el tejido hepatopancreático y en células del epitelio intestinal, con una prevalencia integrada del 6.0% (n=232), detectándose únicamente en un 8.5% de la muestra en la F1 (n=82) y 9.3 % (n= 75) en la F3. Se observó además en algunos casos, tejido hepatopancreático con núcleos eosinofílicos hipertrofiados y necrosis celular. Sin embargo, la infección con BP en ningún caso superó el grado de severidad g-3. En la (Figura 2a). se presenta una sección histológica del hepatopáncreas con CIP de Baculovirus penaei.
Virus de la necrosis infecciosa hipodermal y hematopoyética (IHHNV).Se detectó la presencia de cuerpos de inclusión Cowdry Tipo A (CAI´s), indicando infección por el virus IHHNV, en células de diferentes tejidos tales como epitelio cuticular, cardíaco, nervioso y glándula antenal, con prevalencias que variaron entre el 1.2 y 15.9 % (n=232) (Tabla 3). En algunos casos se observaron células con núcleos pignóticos y focos con necrosis celular acompañaron la presencia de los CAI’s. En la mayoría de los casos el grado de severidad de infección fue leve (g-1 y g-2); solo en casos aislados se presentó un grado de infección severo (g-4). En la (Figura 2b) se presenta una sección de tejido nervioso con cuerpo de inclusión intranuclear CAI’s, con núcleo hipertrofiado, cromatina marginada y núcleo eosinofílico.
Virus de la vacuolización del órgano linfoide (LOVV). Los dos primeros casos de esta infección se dieron durante el ciclo C1 de cultivo (junio-octubre/94), en camarones provenientes de la finca F2, en cuyo órgano linfoide se observaron alteraciones tales como la presencia de cuerpos de inclusión intracitoplasmáticos, tejido hiperplásico, vacuolización y focos necróticos características de la infección con LOVV (Flegel et al, 1992), registrando una prevalencia de 6.5 % (n=31). En la (Figura 2c) se presenta en una sección de tejido linfoidal con hipertrofia, inclusiones intracitoplasmáticas (ic.), esferoides (s) y vacuolización (v).
Virus tipo síndrome de taura (TSV). Debido a que al momento de realizar los muestreos la etapa aguda de la infección por TSV ya había ocurrido, la prevalencia de los signos en los juveniles con esta condición en la finca F1 (n=832) fue la siguiente: coloración rosado difuso fue 3.6%, urópodo rojo 5.4% y cutícula con textura blanda 2.4% (Tabla 2). Histológicamente, zonas con necrosis multifocal del epitelio cuticular (NMEC) con cuerpos de inclusión basofílicos (ci), confirmaron la presencia de TSV en fase aguda (Figura 2d), con una prevalencia de 1.2%, n=82 (Tabla 3). Por su parte, camarones con signos clínicos que caracterizan la fase de transición y crónica de la infección por TSV, presentaron necrosis cuticular focal con una prevalencia de 4.2%, en la cual las alteraciones del órgano linfoide en las muestras analizadas, presentaron prevalencias de 12.2% (necrosis O.L), 25.6% (vacuolización O.L), 23.2% (cuerpos intracitoplasmáticos) y 17.4% (hiperplasia nodular), con un grado de severidad g-3 (muy afectado). Este tipo de alteraciones histológicas correspondieron exactamente a las mismas observadas por la infección por LOVV (Figura 2b): hiperplasia, vacuolización (v), cuerpos de inclusión intracitoplasmáticos (ci) de tamaño variable eosinofílicos y en ocasiones grisáceos (en tinciones con H&E).
La finca F2 reportó por primera vez TSV a partir del ciclo 3 de el presente estudio (marzo de 1995) y en la Finca F3 hasta la fecha de culminación de éste no se habían reportado casos de esta enfermedad (Vallejo, 1996).
Análisis de regresión logística
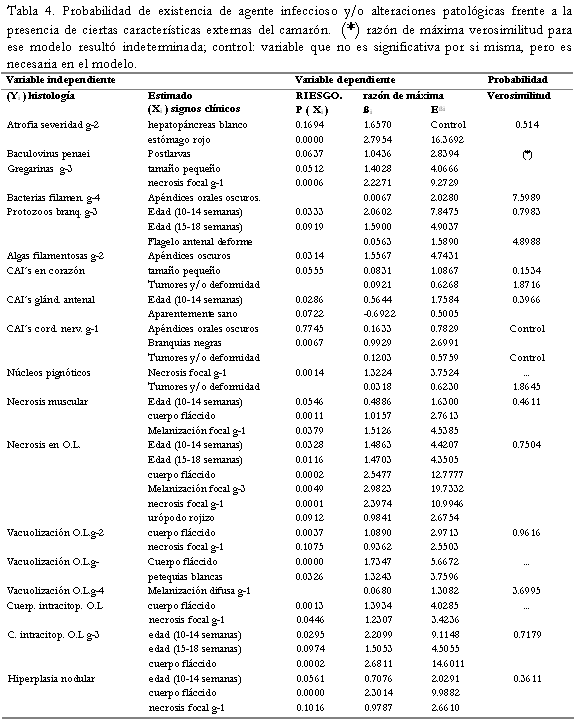
La (Tabla 4) resume el análisis de la regresión logística; en ésta, la expresión ebi representa en términos epidemiológicos la variación en la razón de probabilidad de Riesgo de presentar un determinado agente infeccioso o patología Yi, ante la ocurrencia de un signo clínico Xi. La razón de máxima verosimilitud evalúa el ajuste del modelo de regresión logística y representa la contribución de cada una de las variables explicativas Xi a la probabilidad de ocurrencia de Yi; De acuerdo con el modelo, este valor se considera aceptable a partir del 20%, con un nivel de significancia mayor del 85% para cada variable explicativa (p<0.15).
En relación con la infección por BP, las postlarvas presentaron un riesgo 2.8 veces mayor de presentar este virus, que aquellos camarones de mayor edad (solo se detectaron en el primer mes de muestreo de los ciclos). La presencia de CAI´s y núcleos picnóticos estuvieron asociados con camarones de tamaño pequeño y tumores-deformidades (rostro principalmente), con un nivel de riesgo dos veces mayor en relación con aquellos que no la presentaron.
Así mismo, los camarones de edades superiores a 10 semanas (meses 3 y 4 del cultivo) con signos clínicos como necrosis cuticular focal, petequias blancas, melanización difusa y urópodo rojizo presentaron alto riesgo de presentar alteraciones en el O.L. como necrosis en el O.L, vacuolización del O.L, cuerpos intracitoplasmáticos (ci) e hiperplasia nodular (Tabla 4). Otras manifestaciones clínicas como la condición de cuerpo fláccido presentando un riesgo 2.7 veces de presentar necrosis muscular, que en aquellos que no presentaron este cuadro clínico.
La condición de estómago vacío estuvo asociado con el grado de vacuolización del hepatopáncreas; tanto el grado g-1 como g-2 presentaron un riesgo 3 veces mayor ante la presencia de dicha condición. Los camarones con estómago rojo tuvieron un riesgo 16 veces mayor de presentar atrofia g-2 en el hepatopáncreas que aquellos que no presentaron ese signo clínico. En este modelo la variable hepatopáncreas blanco contribuyó como una variable control (P<0.15). De manera análoga, se encontró que camarones de talla pequeña y necrosis cuticular focal presentaron 4 y 9 veces, respectivamente, mayor riesgo de presentar infestación en un grado de severidad g-3 por gregarinas que en otras condiciones.
La presencia de branquias negras tuvo un riesgo 2.4 veces más elevado de presentar detritus que en otras condiciones, mientras que el ennegrecimiento de apéndices estuvo mas asociado a la infestación por bacterias filamentosas en todos los grados de infestación, con un nivel de riesgo entre 4.7 y 7.6.
Finalmente, las diferencias entre la prevalencia de algunas enfermedades infecciosas y no infecciosas, estuvieron relacionados en algunos casos con la distribución geográfica que, a su vez, está afectado por la influencia de las descargas de los Ríos Sinú y Magdalena. La zona de mayor influencia de descargas de agua dulce fue la F1, que además presentó los niveles más bajos de salinidad durante el período de muestreo.
Por su parte, en la F2 la prevalencia de branquias y apéndices ennegrecidos y por ende la carga de material detrítico dentro de las branquias y los brotes de bacterias filamentosas y diatomeas epibiontes, están asociados con la calidad del suelo y del agua. La alta carga de materia orgánica y nutrientes provenientes del Río Magdalena transportados a través del canal del Dique, llegan a las pisicinas donde parte de estos materiales se sedimentan al no alcanzar a ser remineralizadas por las bacterias aeróbicas. Esta situación pudo evidenciarse indirectamente por la permanente transparencia del agua de esa piscina y la presencia de bacterias anaeróbicas y sulfitorreductoras como Clostridium sp y Salmonella spp. en el medio durante el período de muestreo (Vallejo, 1996).
La finca F3 ubicada en la zona de Galerazamba, mantuvo los niveles más altos de salinidad durante la mayor parte del período anual analizado, observándose diferencias significativas en relación con las demás fincas (P<0.05); registró, además, cambios bruscos en la salinidad ocacionado por la influencia de aguas de origen continental en la época de lluvias (ciclo 2: octubre-diciembre/94), presentándose una disminución drástica en los niveles de salinidad. Esta condición coincidió con la presencia de los más altos índices de deformidades, sobre todo en este ciclo mencionado.
DISCUSION
La enfermedad ha sido reconocida como uno de los factores biológicos que limitan y reducen la producción en el cultivo de camarón, con el incremento de esta actividad, la aparición de nuevas enfermedades han afectado la producción de manera sustancial. La información disponible sobre el tema es muy limitada y se ha desarrollado más por estudios retrospectivos que mediante estudios experimentales diseñados específicamente para el entendimiento de aspectos particulares (Brock, 1995). En general se argumenta que las pérdidas causadas por enfermedades se calculan entre un 10 y un 20 % del valor total de la producción (Prieto y Silveira, 1995).
En este sentido, los tensores ambientales están involucrados en el desarrollo y tasa de incidencia en un buen número de enfermedades infecciosas y no infecciosas que afectan a los camarones peneidos (Sindermann, 1990). El estrés derivado de los contaminantes es uno de los factores más importantes que favorecen el desarrollo de muchas de las enfermedades en organismos marinos. Su efecto incluye cambios directos producto del daño en los compuestos químicos sobre las membranas y tejidos, modificación de la fisiología y de las reacciones bioquímicas, incremento de la infección debido a la presión de patógenos microbianos facultativos y reducción de la resistencia a la infección.
En términos epidemiológicos la prevalencia de enfermedad, representa la proporción de la población afectada por algún agente infeccioso o no infeccioso que de alguna manera está incrementando las tasas de morbilidad o mortalidad dentro de la población (Daniel, 1980).
De los virus registrados hasta ahora, solo algunos fueron encontrados en la zona de estudio afectando la salud de los camarones. A excepción de la enfermedad causada por el TSV, los demás virus registrados representaron infecciones subclínicas por su baja prevalencia dentro de la población y porque aunque algunos mantuvieron una amplia distribución espacial y temporal, el grado de infección no causó efectos graves sobre su salud (Vallejo, 1996).
La presencia de cuerpos de inclusión polihédricos de BP en camarones procedentes de las fincas estudiadas, estuvo restringida a los estadíos post-larvales, con un nivel de prevalencia bajo, en comparación con otros agentes. Resultado similar fue obtenido por CENIACUA (1996) y Saavedra (1993) donde la prevalencia de BP fue de 6.3% y de 5.3 %, respectivamente; así mismo, el grado de severidad de infección fue menor o igual a g-3, en el presente estudio lo mismo que en Saavedra (1993). La presencia del BP en los piscinas de engorda fue muy leve y a medida que transcurrió el ciclo de cultivo, el grado de infección en los individuos y la prevalencia dentro de la población se hizo menor. Esta situación concuerda con los resultados obtenidos por Leblanc y Overstreet (1990). Según estos autores, las partículas polihédricas de BP son eliminadas al medio a través del intestino; sin embargo la infectividad de BP es cada vez menos efectiva a medida que el camarón crece en el estanque (Lightner et al., 1992). En el transcurso de los ciclos se evidenció la presencia de células hepatopancreáticas presentando núcleos hipertrofiados y eosinofílicos aunque no se encontraron cuerpos de inclusión polihédricos en ejemplares examinados. En cuanto a la distribución geográfica, la incidencia de BP en los estanques de cultivo dependió del lugar de procedencia de las larvas lo que significa que éstas ya venían infectadas antes de la inoculación en las piscinas (Vallejo, 1996).
Según Lightner (1996), la principal evidencia este virus IHHN es la presencia de cuerpos de inclusión eosinofílicos Cowdry tipo A (CAI´s) en tejido de origen mesodermal y ectodermal (glándula antenal, tejido muscular, epidermis cuticular y cordón nervioso) y la presencia (en algunos casos) de células con núcleos pignóticos como el paso preliminar a la necrosis celular, como respuesta degenerativa de la célula; sin embargo, con el grado de severidad observado en este estudio, puede argüirse que el nivel de infección en la mayoría de los casos fue subclínico, con grado de severidad por debajo de g-3 y solo en casos aislados llegó a presentarse infección g-4. Los principales signos asociados con esta infección en el área de estudio son los mismos reportados por otros autores (Lightner et al., 1992; Lightner y Redman, 1992; Brock, 1995), en donde la necrosis cuticular, la enfermedad de las branquias negras y el cuerpo fláccido, fueron los signos más correlacionados. De acuerdo con estos mismos autores, las deformidades y las tallas pequeñas presentaron un riesgo dos veces mayor de presentar IHHNV que en otras condiciones.
Sin embargo, en la finca F3 se presentó la mayor prevalencia de camarones con deformidades abdominales, pero la prevalencia de los CAI´s fue baja. Esto podría indicar que este signo no es exclusivo de la infección por IHHNV. El estrés causado por los cambios bruscos de salinidad durante el ciclo de cultivo, podría ser un factor desencadenante de esta condición, mas que la presencia del virus (Sindermann, 1990).
Para el área de estudio, las evidencias que se tuvieron del estado agudo de la infección por TSV, fueron dadas por las características morfológicas y las altas mortalidades registradas en camarones entre los 20 a 40 días postsiembra (Brock, com.pers.). Las demás evidencias se basaron en la infección crónica demostrada por los signos clínicos característicos (Chamberlain, 1994; Brock, 1995; Brock et al., 1995; Lightner et al., 1995) y por la presencia de alteraciones en el órgano linfoide (O.L); éstas son muy similares a las ocasionadas por el virus LOVV e igualmente reconocidas para la infección por TSV (Brock, com pers.). En reportes de CENIACUA, (1996) la prevalencia de hiperplasia del O.L. alcanzó 12.5% en camarones del Caribe colombiano, porcentaje similar al reportado para el presente estudio en la F1.
Dado que en toda la zona de estudio se presentaron alteraciones en el órgano linfoide, no fue posible por el método de diagnóstico usado en el presente estudio, identificar si estas alteraciones corresponden al agente infeccioso LOVV o TSV. El primero, es un virus que se presenta en camarones sin manifestaciones externas reconocibles (Flegel et al., 1992) y hasta antes de la aparición del TSV, su prevalencia y grado de severidad se mantuvo en niveles bajos (menor a g-3). Con el registro del nuevo virus TSV, además de incrementar la tasa de mortalidad, la prevalencia y grado de severidad de las alteraciones en el organo linfoide en los sobrevivientes, se incrementaron notablemente. Otros signos clínicos y agentes infecciosos incrementaron su prevalencia ante el nivel de estrés generado por la infección producida por el TSV (Vallejo, 1996).
Según Brock (1995), los camarones que han superado la fase aguda de la infección por TSV y pasan a un estado crónico y de recuperación siguen portando el virus en forma latente, con la posibilidad de reinfección. Según el mismo autor, la principal función reconocida hasta ahora del órgano linfoide, es la de captura y procesamiento de antígenos. Por lo tanto se podría argumentar que posiblemente el virus TSV permanece en este tejido en etapa no infectiva, causando las alteraciones ya descritas. El TSV, como virus de cadena RNA, podría ser también responsable de la presencia de los cuerpos de inclusión intracitoplasmáticos.
Aparentemente la prevalencia del TSV, estuvo asociada a esas condiciones de baja salinidad, pero de acuerdo con Brock et al. (1995), brotes de TSV también se han reportado en zonas con alta salinidad, lo que significa que ésta no es un factor condicionante de la infección. Sin embargo se argumenta, que el factor de estrés ocasionado por el cambio brusco en la salinidad, influyó en el desarrollo de esta condición en los camarones de esta finca. De otro lado, este autor sostiene que las deformidades en el cuerpo de los camarones están asociadas generalmente con patógenos como el virus IHHNV; en los análisis histológicos y posteriormente en el análisis de regresión logística esta correlación se dió pero fue menor de la esperada..
AGRADECIMIENTOS
Este trabajo constituye parte de la tesis de M.Sc. de La Universidad Nacional de Colombia-INVEMAR de la primera autora, co-dirigida por Néstor H. Campos Dr. rer.nat. Los autores agradecen a COLCIENCIAS por el apoyo financiero a través del proyecto “Desarrollo y optimización del cultivo de camarones marinos (Penaeus vannamei y P. stylirostris) en el Caribe colombiano”, código 2105-09-030-93, al INVEMAR por el apoyo logístico y a CENIACUA por su cooperación con el desarrollo del proyecto. Al Dr. Jorge Cuéllar A. en los aspectos histopatológicos y al Profesor Hernando Hurtado de la Universidad del Quindío por su asesoría en los análisis estadísticos.
BIBLIOGRAFIA
1. Bell, T.A. y D.V. Lightner. 1988. A handbook of normal penaeid shrimp histology. World Aquaculture Society, Baton Rouge, USA, 75 p. [ Links ]
2. Brock, J.A. 1995. Shrimp health management short course. Training course notes. CENIACUA, Cartagena, 156 p. [ Links ]
3. _________ ; R. Gose; D.V. Lightner y K. Hasson. 1995. An overview on Taura syndrome, an important disease of farmed Penaeus vannamei. Swimming through troubled water, Procceding of the special session on shrimp farming. Aquaculture'95. World Aquaculture Society, C.L. Browdy y J.S. Hopkins (Eds.). Baton Rouge, U.S.A., 84-94. [ Links ]
4. CENIACUA. 1996. Noti-Proyectos. Acuicarta, Santafé de Bogotá, D.C., 1: 3-6 [ Links ]
5. COLCIENCIAS-BID. 1989. Perfil Ambiental de Colombia. Escala, Bogotá, 348 p. [ Links ]
6. CORPES. 1992. El Caribe colombiano. Consejo Regional de Planificación, Santa Marta, 210 p. [ Links ]
7. Chamberlain, G.W. 1994. Taura syndrome and China collapse caused by new shrimps viruses. World Aquaculture, 25(3): 22-25. [ Links ]
8. Daniel, W.W. 1980. Bioestadística. Base para el análisis de las ciencias de la salud. Limusa, México, 485 p. [ Links ]
9. Flegel, T.W.; D.F. Fegan; S. Kongsom; S. Vuthikomudomkit; S. Sriurairatana; S.; Boonyaratpalin; C.; Chantanachookhin; J. Vickers y O. Macdonald. 1992. Occurrence, diagnosis and treatment of shrimp diseases in Thailand. Disease of cultured penaeid shrimp in Asia and the United States. Fulks, W. y K.L. Main (Eds.). The Oceanic Institute, Hawaii, U.S.A., 57-112. [ Links ]
10. Kleinbaum, D.G. 1994. Logistic Regression. Springer-Verlag, New York, 120-145. [ Links ]
11.Leblanc, B. y R.M. Overstreet. 1990. Prevalence of Baculovirus penaei in experimentally infected white shrimp relative to age. Aquaculture, 87(3/4): 237-242. [ Links ]
12. Lightner, D.V. 1996. A handbook of pathology and procedures for diseases of penaeid shrimp. World Aquaculture Society, Baton Rouge, U.S.A., paginación varía. [ Links ]
13. __________ y R.M. Redman. 1992. Geographic distribution, host and diagnostic procedures for the penaeid virus diseases of concern to shrimp culturists in the Americas. en: A.W. Fast y L.J. Lester (Eds.). Culture of Marine Shrimp: Principles and Practices . Elsevier, 354 p. [ Links ]
14. __________ ; T.A. Bell; R.M. Redman; L.L Mohney; J.M. Natividad; A. Rukyani y A. Poernomo. 1992. A review of some major diseases of economic significance in penaeid prawns/shrimps of the Americas and Indo Pacific. Proc. Symp. Dis. Asian Aqua. M. Shariff, R. Subasinghe y J.R. Arthur (Eds.). Fish Health Section, asian isheries Society, Manila, 57 p. [ Links ]
15. __________ ; R.M. Redman; K.W. Hasson y C.R. Pantoja. 1995. Taura syndrome in Penaeus vannamei (Crustacea: Decapoda): gross signs, histopathology and ultrastructure. Dis. Aquat. Org., 21: 53-59. [ Links ]
16. Prieto, A. y R. Silveira. 1995. Prevención y control de enfermedades en organismos acuáticos. Manual. Centro de Investigaciones Pesqueras, Ciudad Habana, Cuba, 96 p. [ Links ]
17. Saavedra B., M. 1993. Analisis de la incidencia del protozoo gregarina (Esporozoa), en estanques para el cultivo de camarones peneidos. Tesis Biol. Mar., Universidad Jorge Tadeo Lozano. Bogotá, 143 p. [ Links ]
18. Sindermann, C.J. 1990. Principal diseases of marine fish and shellfish. Academic Press, Inc, San Diego, California, Vol.2. 516 p. [ Links ]
19. Vallejo, A.. 1996. Estatus de sanidad de camarones Penaeus vannamei cultivados en tres fincas productoras del Caribe colombiano, con énfasis en las enfermedades causadas por agentes virales. Tesis M.Sc. Biol. Mar., Univ. Nacional de Colombia, Santafé de Bogotá, 115 p. [ Links ]
20. Weidner, D. 1992. Colombian shrimp culture industry (final draft). Department of Commerce of United States, 28 p. [ Links ]
FECHA DE RECEPCION: 06/02/1997 FECHA DE ACEPTACION: 03/03/1999