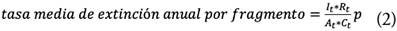Introducción
Los primates tienen funciones claves en los ecosistemas (Sengupta et al., 2015), entre ellas la regulación de las poblaciones de sus insectos presa (en el caso de que los consuman) y de las comunidades vegetales favoreciendo la dispersión de semillas, la polinización, la renovación de los brotes de hojas, la fertilización del suelo, entre otros (Chapman et al., 2013). Son particularmente importantes sus funciones en el Neotrópico por la falta de redundancia ecológica con otros grupos taxonómicos, siendo clave para la persistencia de los ecosistemas evitar su extinción (Stevenson y Aldana, 2008; Cerullo y Edwards, 2019; Chapman y Peres, 2021).
Dada la importancia ecológica de los primates se han implementado diferentes aproximaciones para su conservación: a nivel ex situ, la cría en cautiverio y su reintroducción (Ferrie, 2017); a nivel in situ los esfuerzos han estado orientados a la protección del hábitat natural (creación y monitoreo de áreas protegidas) (Condro et al., 2021); regulaciones para detener la deforestación (Krause et al., 2019); la promoción de sistemas de producción sostenibles, entre otros (Estrada et al., 2012, 2020; Strona et al., 2018); el monitoreo poblacional (Bezanson y McNamara, 2019); así como la educación, sensibilización (Bezanson et al., 2022) y monitoreo ciudadano con las comunidades presentes en el territorio donde habitan los primates (Battisti y Cerfolli, 2021).
De las estrategias anteriormente mencionadas, las in situ han mostrado ser más efectivas a largo plazo, pero en ellas es necesario priorizar las acciones de conservación para hacer un mejor uso de los limitados recursos disponibles (Rylands et al., 2020). En los procesos de priorización, usualmente se construyen escenarios para analizar el riesgo a la extinción de las especies de primates de interés y la influencia que las acciones de conservación tienen para evitarlo (Strona et al., 2018).
Estos escenarios pueden construirse por consenso entre expertos, consulta a los pobladores del territorio, análisis de la dinámica poblacional, y con la distribución de sus registros en los paisajes, cuando se dispone de dicha información (Estrada et al., 2020). En la conservación de primates no se ha utilizado ampliamente la modelación matemática para crear dichos escenarios, mientras que en otros grupos biológicos (plantas maderables y los animales que interactúan con ellas) esta aproximación ha complementado de manera exitosa las estrategias de gestión de especies silvestres (Agarwal y Pathak, 2015; Pathak, 2018; Qureshi y Yusuf, 2019).
Por otra parte, el mono Zocay [Plecturocebus ornatus, Gray (1866)] es una especie endémica de Colombia (Figura 1), clasificada en la categoría de Vulnerable (VU) según las amenazas para su supervivencia por la Unión Internacional para la Conservación de la Naturaleza (IUCN), debido a la disminución de su área de distribución, sus poblaciones altamente fragmentadas y la continua disminución de sus subpoblaciones (Carretero-Pinzón et al., 2020; Henao-Díaz et al., 2020). Esta clasificación se conserva a nivel nacional (MinAmbiente, 2024).
P. ornatus es un primate pequeño que pesa alrededor de 1.000 g y se diferencia de otras especies del género por presentar una banda blanca sobre los ojos, con pies y manos de color blanco y antebrazos rojizos (Defler, 2010). Es una especie endémica que se distribuye al norte del río Guayabero desde la Cordillera Oriental hasta el río Ariari y por el piedemonte se extiende hasta el río Upía (Carretero-Pinzón et al., 2020). Habita bosques húmedos de tierras bajas, bosques de galería y morichales, siendo capaces de sobrevivir en zonas de bosques secundarios (Carretero-Pinzón y Defler, 2016). P. ornatus es una especie principalmente frugívora, con áreas vitales por individuo de 3-15 ha (Defler, 2010). Vive en grupos familiares de tres a cinco individuos compuestos de una pareja y sus crías de diferentes edades (Carretero-Pinzón et al., 2017).
Las densidades reportadas para esta especie son influidas por la cantidad de área de hábitat disponible, con valores más altos en fragmentos de 1-50 ha cuando el paisaje es altamente fragmentado y mayores en fragmentos de >100 ha cuando el paisaje es más conservado y conectado (Carretero-Pinzón y Defler, 2016). A su vez, P. ornatus es más detectable en los bordes de los fragmentos, ya que suele usarlos para obtener recursos alimenticios que son abundantes en ellos (Carretero-Pinzón y Defler, 2016; Eppley et al., 2022).
A su vez, la presencia y abundancia de esta especie son influenciadas por variables a la escala de sitio y paisaje en un radio de 1.000 m, siendo el área disponible medida como el porcentaje de bosque alrededor del fragmento focal más importante para la presencia de esta especie en paisajes ganaderos (Carretero-Pinzón et al., 2017). En el caso de paisajes periurbanos, la abundancia de la especie es influenciada por variables a escala de paisaje como la conectividad de los parches de bosque, y a escala del parche como el tamaño del fragmento (Ortiz-Moreno et al., 2022).
En este contexto, el objetivo de este trabajo fue construir un modelo matemático como una propuesta para el análisis de la dinámica de la proporción de fragmentos de bosque ocupados por P. ornatus dentro de un paisaje agropecuario en diferentes escenarios de conservación. Específicamente, el modelo matemático permitió construir escenarios variando parámetros asociados al paisaje para analizar de forma cualitativa la presencia de la especie en el paisaje, a través de la dinámica temporal de la proporción de fragmentos de bosque que ocupa P. ornatus. A partir de las predicciones del modelo se espera contribuir al desarrollo de posibles recomendaciones para la conservación de esta especie y la de su hábitat.
Metodología
Área de estudio
En la presente investigación se seleccionó al municipio de San Martín, departamento del Meta (Colombia), como área de estudio, ya que el Proyecto Zocay (Proyecto de investigación independiente liderado por la Dra. Xyomara Carretero-Pinzón) ha venido monitoreando desde hace más de 12 años la presencia y abundancia de P. ornatus en predios privados, siendo el conjunto de datos más completo disponible para la especie. En la presente investigación solo se accedió a los datos de presencia facilitados por su autora.
El municipio de San Martín (Figura 2), tiene un clima tropical con temperatura promedio de 27oC, la precipitación anual varía entre 2.000-3.000 mm, con una temporada de lluvias de abril a noviembre, y una temporada seca de diciembre a marzo (García-Restrepo y Gómez-Sánchez, 2021). Tiene un paisaje geomorfológico de planicie sedimentaria, formada por procesos coluvio-aluviales asociados a la dinámica de la red de drenaje de los ríos Humadea y Guamal (Chicangana-Montón et al., 2022). Los suelos del municipio son principalmente ultisol y entisol (Malagón, 2003) y sus características ecológicas determinan la distribución de comunidades vegetales como bosques de galería y sabanas, cuya estructura está relacionada con el papel ecológico de los dispersores de semillas, y con los procesos de transformación del uso y cobertura del suelo (Stevenson y Aldana, 2008) (Anexo 1).
Desde el punto de vista del histórico de ocupación y uso del suelo, el municipio de San Martín se ha caracterizado por la deforestación asociada a las actividades agropecuarias, principalmente ganadera, que se remontan desde el siglo XVII con el proceso de colonización española (Rausch, 2007) (Anexo 1). De acuerdo con Carretero-Pinzón (2017), en el paisaje del municipio los remanentes de cobertura boscosa se ubican principalmente en rondas o retiros hídricos, reservas privadas y pequeños fragmentos dispersos dentro de las pasturas para la cría extensiva de ganado (Figura 2).

Nota. Las versiones corresponden a la coincidencia de los puntos de georreferenciación (simbolizados como estrellas y diamantes) para la presencia de los grupos familiares o individuos de P. ornatus (simbolizados como puntos negros) en los fragmentos analizados (F1, F2, F3, MG y CH) en el periodo de 2013 a 2019. En este caso, se presenta solo el 2013 para facilitar su visualización (escala 1:5 km). Sistema de proyección UTM Datum WGS84. El panel inferior derecho muestra la ubicación de los fragmentos dentro del municipio de San Martín, su área urbana y el área protegida más próxima (escala 1:20 km).
Fuentes cartográficas: IDEAM (2017) y RUNAP (2020).
Figura 2 Ubicación de los fragmentos de bosque estudiados con presencia de P. ornatus registrados por el Proyecto Zocay (Proyecto de investigación independiente liderado por la Dra. Xyomara Carretero-Pinzón) en San Martín (Meta, Colombia).
Presencia de P. ornatus
De la base de datos de presencia de P. ornatus del Proyecto Zocay con mayor número de años muestreados (Anexo 2) se seleccionaron dos fragmentos claramente georreferenciados para el presente estudio, que corresponden a la agrupación de los fragmentos MG y CH que se podrían evidenciar conectados en algún momento (Figura 5), a la escala de análisis de esta investigación que es municipal (1:25.000); y el fragmento F3 (Figura 2 y Figura 5). Los registros de P. ornatus fueron obtenidos en transectos de 1 km, con un esfuerzo de muestreo de 90,25 km, durante los años 2013 a 2019, en dos fragmentos de bosque de propiedades privadas ubicadas en el centro oriente de San Martín (Meta, Colombia) (Figura 2).
Análisis de cobertura boscosa
En la digitalización de los fragmentos donde se registraba la presencia de P. ornatusse emplearon imágenes satelitales georreferenciadas y preprocesadas obtenidas de la NASA USGS Earth explorer Landsat 8, con nubosidad inferior al 3,5% y resolución pancromática de 15x15 m y termal reflectiva de 30x30 m; empleando las órbitas 0757 y 0758, de los años presentados en el Anexo 2. Las imágenes fueron digitalizadas manualmente con escala 1:25.000 en ArcGIS 10.8, empleando como base la banda con mejor contraste de la cobertura boscosa (B4 para los años 2014, 2016, 2017 y 2019; B8 para 2013) (Mairota et al., 2013). Toda la información cartográfica de la investigación fue establecida en el sistema de referencia UTM WGS84, EPSG: 32618.
Para el análisis de la estructura del paisaje se empleó la extensión V-LATE 2.0 en ArcGIS 10.8 donde se determinaron las métricas de área (Area_m2) y perímetro, relación perímetro/área (Paratio), índice de forma (Shape index), dimensión fractal (Frac_Dim), distancia al vecino más próximo (NNDist), área del vecino más próximo (NN_Area) de los fragmentos (Lausch et al., 2015) y proximidad en un buffer de 500 m (PxFg_500) (Carretero-Pinzón et al., 2017), con un efecto de borde estimado de 30 m (Bueno y Llambí, 2015) para la estimación del área nuclear de cada fragmento; y un área vital mínima estimada de 1 ha del mono Zocay (P. ornatus), característica de un paisaje fragmentado (Carretero-Pinzón et al., 2017). A partir de los resultados obtenidos y los referentes de literatura se seleccionaron las variables a ser incluidas dentro del modelo.
Modelación matemática
El proceso de modelación matemática inició con un análisis de información sobre la biología de P. ornatus y modelos matemáticos usados en el estudio de poblaciones de primates (Schreier et al., 2022). Con la información analizada y datos disponibles, se establecieron supuestos biológicos para la construcción del modelo matemático (Lata et al., 2018). Teniendo en cuenta que P. ornatus presenta bajas tasas de dispersión y asumiendo que la persistencia de este primate en un paisaje fragmentado puede estar definida por procesos de colonización y extinción local de sus subpoblaciones en los fragmentos de bosque, se formuló un modelo matemático con enfoque metapoblacional (Hanski, 1999) para la dinámica de la presencia de P. ornatus en este tipo de paisaje.
En este sentido, la variable de estado del modelo es la proporción de fragmentos de bosque ocupados por P. ornatus. Además, se asume que las tasas de colonización y extinción local dependen de algunas características del paisaje (Carretero-Pinzón et al., 2017). Por tanto, el modelo incluye los siguientes parámetros asociados a los fragmentos de bosque: área del fragmento, índice de forma, distancia al vecino más próximo y dimensión fractal, los cuales han sido usados en estudios previos para explicar la presencia y abundancia de esta especie en Villavicencio (Meta, Colombia) en el periodo 1986-2019 (Ortiz-Moreno et al., 2022). La construcción del modelo se realizó desde el enfoque de la Dinámica de Sistemas (Forrester, 1994) con la simulación computacional de diferentes escenarios en el software Vensim PLE (Ventana Systems Inc., 2019). Finalmente, los resultados obtenidos se analizaron para dar una explicación aproximada a la dinámica de la presencia de P. ornatus en un paisaje fragmentado agropecuario.
Simulaciones numéricas
Se simularon cuatro escenarios: escenario base o “business as usual”, es decir, continúa con la tendencia actual; escenario de alta deforestación; escenario intermedio (conservación local, que involucra incrementos puntuales del área de cobertura forestal) y escenario pro-conservación (donde se aumenta la cantidad, calidad y conectividad del hábitat para la especie).
En el escenario base se usaron los datos promedio anuales de los parámetros de los fragmentos de bosque de San Martín (Meta) de los años 2013, 2014, 2016, 2017 y 2019 (Tabla 4). Debido a la falta de esos datos para 2015 y 2018, se asignó a cada parámetro el promedio entre los valores del respectivo parámetro del año inmediatamente anterior y el posterior (Anexo 5). En el escenario de alta deforestación, se redujeron la dimensión fractal media y el área media total en un 50%, y se aumentó en un 50% la distancia media al fragmento más próximo y el índice de forma (Bogaert et al., 2002; Carretero-Pinzón et al., 2017). Para el escenario intermedio, se disminuyó el índice de forma en un 25% y se aumentó el área media total en un 25% (Bogaert et al., 2002; Carretero-Pinzón et al., 2017). Finalmente, en el escenario de pro-conservación, se aumentaron la dimensión fractal y el área media total en un 50%, y se redujeron la distancia media al fragmento más próximo y el índice de forma en un 50% (Bogaert et al., 2002; Ortiz-Moreno et al., 2022). Dichos escenarios fueron propuestos con base en los trabajos de Carretero-Pinzón et al. (2017), Galán‐Acedo et al. (2019) y Cudney-Valenzuela et al. (2022).
Resultados
Valores de referencia del modelo matemático
La caracterización de los parches observados en el paisaje y el comportamiento medio de las variables de las métricas se presentan en los anexos 4 y 5. En general, se observa que el área en 2016 estuvo por encima de 27’644.516 m2 (media total en el tiempo de estudio), como lo evidencian la tabla del Anexo 4 y las figuras de los anexos 3 y 7; situación contraria se observa en 2017 y 2019 donde la cantidad de hábitat disminuyó, aspecto que se evidencia en el decrecimiento de la tasa de variación de 2017 en un 67,3% (Tabla 5) y para 2019 baja un 2,2%, respecto al periodo observado inmediatamente anterior.
El comportamiento de la dimensión fractal tiende al promedio total (Figura 6). En la tabla 4 (anexo) se muestra que desde 2014 este índice ha incrementado, y está por encima de la media total (1,42) en 2017 y 2019. Además, al evaluar las tasas de variación en la tabla 5 (anexo), desde 2017 presenta un leve incremento cercano al 2,5% y en 2019 no hay variación con respecto al año anterior (Figura 6).
La distancia al vecino más próximo presentó un comportamiento variable. En 2016 se observó su menor valor, por debajo de la media total (6.939,1 m), en los años siguientes incrementó, aunque en 2019 presentó una tasa de variación por debajo del periodo anterior del 18,9% (Tabla 5); entonces, aunque hubo un leve aumento respecto a 2018, hay una tendencia a menor conectividad entre los fragmentos estudiados, lo cual puede afectar la tasa de dispersión de la especie.
En los anexos 4, 5, 6 y 7 (Tabla 3, 4 y 5, Figura 6) se evidencia que entre 2013 y 2019 hay una baja calidad del hábitat, dado que el promedio anual observado para el índice de forma (Shape_Idx) fue mayor a tres, indicando linearización o irregularidad en la forma de los fragmentos. Además, sus tasas de variación fueron altas (Tabla 5), en 2016 esta aumentó (39,1%) respecto a 2014, en 2017 disminuyó en 44,6%, y para 2019 presentó un leve incremento. A su vez, en el presente análisis el área nuclear solo incrementó en 2016 respecto a 2014 (Figura 6).
Modelo matemático
El modelo matemático propuesto para la dinámica de la presencia de P. ornatusen un paisaje fragmentado, desde un enfoque metapoblacional (Hanski, 1999), se fundamenta en los siguientes supuestos:
El paisaje que habita P. ornatus está conformado por fragmentos de bosque donde la especie establece subpoblaciones y su dinámica puede estar definida por procesos de colonización y extinción de esas subpoblaciones (Carretero-Pinzón et al., 2020). Por tanto, se asume una dinámica metapoblacional para P. ornatus en este paisaje fragmentado (Carretero-Pinzón et al., 2017). En consecuencia, la persistencia de la especie en el paisaje fragmentado depende del riesgo de extinción y la probabilidad de colonización (Gilpin y Hanski, 1991; Hanski, 1999; Escobedo-Morales y Mandujano, 2007; Qureshi y Yusuf, 2019).
La presencia de P. ornatus en el paisaje se determina a partir de la proporción de fragmentos de bosque que ocupa (p), la cual es la variable de estado del modelo. Por tanto, se considera que la proporción de fragmentos ocupados por P. ornatus depende de la relación entre las tasas de colonización y extinción por fragmento (Figura 3) (Carretero-Pinzón et al., 2017). Además, se asume que estas tasas locales de colonización y extinción varían anualmente con el tamaño, la calidad y el aislamiento entre los fragmentos.
El aumento de la conectividad del paisaje permite que la tasa de dispersión de primates se incremente (Escobedo-Morales y Mandujano, 2007; Pathak, 2018). Por ende, se asume que la tasa de colonización de un fragmento de bosque depende de la capacidad de dispersión de la especie, la cual aumenta con la conectividad del paisaje y la dimensión fractal de los fragmentos (Figura 3) (Swart y Lawes, 1996; Schreier et al., 2022). En este sentido, se planteó una tasa media local de colonización que varía anualmente en función de los valores promedio por año de la distancia al fragmento más próximo (o aislamiento) Dty la dimensión fractal Ft, así como de la proporción de fragmentos ocupados p y no ocupados por la especie (1-p), dada por la ecuación 1:
El área y la calidad de los fragmentos de bosque tienen un efecto positivo en la presencia de primates en un paisaje fragmentado (Hanski, 1999; Escobedo-Morales y Mandujano, 2007). Desde esta perspectiva, se asume que la tasa de extinción por fragmento disminuye con el incremento de la calidad y el tamaño del fragmento (Hames et al., 2001; Fahrig, 2003). En este sentido, se considera que la calidad del fragmento aumenta con el área total A y el área nuclear C del mismo; y disminuye con su índice de forma I y su relación perímetro-área R (R=perímetro/área) (Figura 3). Por tanto, se planteó una tasa media local de extinción, que varía anualmente, en función de los valores promedio por año de esos parámetros (A t , C t , I t y R t ) y la proporción de fragmentos ocupados, dada por la ecuación 2:
A partir de los supuestos anteriores, se propone un modelo matemático para la dinámica de la proporción de fragmentos ocupados por P. ornatus en el paisaje, dado por la ecuación diferencial 3, que describe la tasa neta anual de cambio de la proporción de fragmentos ocupados por las subpoblaciones de la especie (dp/dt):
donde c, β, δ, μ, α y e son constantes de proporcionalidad positivas. Todos los parámetros en el modelo se consideran positivos, con el fin de que tengan sentido biológico. La Tabla 1 indica las definiciones y unidades de los parámetros del modelo.
El modelo matemático tiene dos estados de equilibrio: p 1*=0 y p 2*=1-(eμδI t R t D t /cαβA t C t F t ). Al analizar la estabilidad local de los equilibrios, se identifican dos casos: 1) Si cαβA t C t F t < eμδI t R t D t , el único equilibrio del modelo con sentido biológico es p1*=0 y es asintóticamente estable; y 2) Si cαβAtCtFt > eμδItRtDt entonces el equilibrio p1* es inestable, el equilibrio p2* es positivo (tiene sentido biológico) y es asintóticamente estable.

Fuente: las autoras, Vensim PLE.
Figura 3 Diagrama causal de la dinámica de la proporción de fragmentos de bosque ocupados por P. ornatus.
Tabla 1 Definición y unidades de los parámetros del modelo.
| Parámetro | Definición | Unidad |
|---|---|---|
| A t | Área media total por fragmento en el año t | Km 2 |
| C t | Área nuclear media de los fragmentos en el año t | Km 2 |
| D t | Distancia media al fragmento vecino más próximo en el año t (aislamiento) | Km |
| F t | Dimensión fractal media de los fragmentos en el año t | Adimensional |
| I t | Índice de forma promedio de los fragmentos en el año t | Adimensional |
| R t | Relación perímetro-área media de los fragmentos en el año t | Km -1 |
| ( | Proporción de Ft | Adimensional |
| ( | Proporción de Dt | Adimensional |
| ( | Proporción de It | Adimensional |
| ( | Proporción de At | Adimensional |
| c | Constante de proporcionalidad | Km/año |
| e | Constante de proporcionalidad | Km 4 /año |
Fuente: las autoras.
Simulaciones numéricas
La Figura 4 muestra los resultados de las simulaciones que constituyen las predicciones del modelo matemático en cuatro escenarios diferentes: base, intermedio, alta deforestación y pro-conservación. Teniendo en cuenta que los valores medios anuales de los parámetros de los fragmentos de bosque (dimensión fractal, distancia al vecino más próximo, índice de forma, área total y área nuclear) de San Martín (Meta) utilizados en el modelo para los años 2015 y 2018 no son datos obtenidos de mediciones directas (Tabla 3) y que los valores de las constantes de proporcionalidad son hipotéticos, entonces los resultados de las simulaciones de los escenarios se deben considerar de forma cualitativa más que cuantitativa en la interpretación de las predicciones biológicas del modelo, esto para dar una explicación aproximada sobre la dinámica de la proporción de fragmentos de bosque ocupados por P. ornatus en el área de este municipio.

Nota. El escenario base (línea amarilla) corresponde a la predicción del modelo usando los valores medios por año, desde 2013 a 2019, de los parámetros de los fragmentos de bosque: dimensión fractal, distancia al fragmento vecino más próximo, índice de forma, área total y área nuclear. Para simular el escenario intermedio o de conservación local (línea gris) se redujo en un 25% el valor medio del índice de forma y se aumentó en un 25% el valor medio del área total de los fragmentos. En el escenario de alta deforestación (línea naranja) se redujeron en un 50% los valores medios de la dimensión fractal y el área total, mientras que se aumentaron en un 50% los valores medios de la distancia al fragmento vecino más próximo y el índice de forma. Para el escenario de pro-conservación (línea azul) se aumentaron en un 50% los valores medios de la dimensión fractal y el área total, y se redujeron en un 50% los valores medios de la distancia al fragmento vecino más próximo y el índice de forma.
Fuente: las autoras.
Figura 4 Predicciones del modelo de la proporción de fragmentos de bosque ocupados por P. ornatus en San Martín (Meta).
Discusión de resultados
Características del modelo y novedad con respecto a otros abordajes
El modelo matemático propuesto involucra los efectos positivos del aumento de la dimensión fractal y la conectividad de los fragmentos sobre la capacidad de dispersión del mono Zocay y la tasa de colonización por fragmento (Galán-Acedo et al., 2019), en tanto que considera los efectos negativos de la deforestación sobre el índice de forma y el aumento de la relación perímetro/área, acorde a las consideraciones de Carretero-Pinzón et al. (2017) y Arasa-Gisbert et al. (2021) sobre el impacto de la fragmentación sobre la biodiversidad y específicamente en P. ornatus. Además, en el modelo propuesto, las tasas de colonización y extinción local no son constantes, esto es, varían anualmente con los valores medios de los parámetros asociados a las características del paisaje. En este sentido, el modelo asume que el paisaje fragmentado es dinámico.
Cavada et al. (2019) también identifican un efecto negativo de la antropización en la densidad metapoblacional a escala del paisaje en primates africanos como Colobus angolensis palliatus, Procolobus gordonorum y Cercopithecus mitis monoides. En cuanto a la modelación estadística, Aliaga‐Samanez et al. (2020) desarrollan un análisis para modelar la distribución de primates limitada por barreras geográficas y destacan el rol de los ríos para limitar la dispersión de los primates.
Por otra parte, Schreier et al. (2022) con su modelo matemático sugieren que las características del borde de los fragmentos influyen en el comportamiento de los primates, donde la limitación de los recursos disponibles aumenta la territorialidad y el desarrollo de vocalizaciones para su defensa. En tanto que Rooker y Gavrilets (2020), al modelar matemáticamente la influencia del fitness reproductivo de las hembras de primates y su respuesta al infanticidio, identifican la evolución de caracteres que afectan la dinámica poblacional. Además, Colchero et al. (2021) sugieren que aspectos relacionados con el fitness individual como la expectativa de vida y la fecundidad, también influyen en el éxito poblacional de los taxa de primates. Siendo importante considerar la competencia ínter e intraespecífica para comprender los factores que explican la presencia de P. ornatus, lo cual debería ser incluido en futuros estudios.
En Sudáfrica, Swart y Lawes (1996) emplearon modelos metapoblacionales temporales para evaluar el impacto de la conectividad en bosques altamente fragmentados sobre la supervivencia en los monos Samango (Cercopithecus mitis), analizando de manera independientemente la zona de borde y el interior de los parches (área nuclear). Posteriormente, Lawes et al. (2000) aplicaron el modelo metapoblacional isla-continente para describir el patrón de fragmentación de los parches.
En México, Palacios-Silva y Mandujano (2008) estudiaron la conservación del mono araña (Ateles geoffroyi) y el mono aullador (Alouatta palliata) en la región de Los Tuxtlas, mediante un enfoque metapoblacional para modelar la ocupación de parches. Estimaron las tasas de colonización, asumiendo un patrón espacial estacionario y empleando la distancia entre los fragmentos como una medida de conectividad. Escobedo-Morales y Mandujano (2007) y Mandujano y Escobedo-Morales (2008), bajo un enfoque similar, evaluaron la probabilidad de extinción del mono aullador, el número de poblaciones remanentes y el número total de individuos. Por su parte, Mandujano et al. (2008) aplicaron un modelo poblacional estocástico para simular escenarios en poblaciones aisladas y metapoblacionales, destacando la importancia de implementar estrategias de conservación que incrementen el área y la conectividad de los fragmentos de hábitat.
Análisis de cobertura boscosa y dinámica de los fragmentos estudiados entre 2013 y 2019
Los fragmentos de bosque base (F3 y MG+CH) para la modelación matemática muestran una clara tendencia al cambio influenciado por la deforestación local (Stevenson y Aldana, 2008) (Tabla 2 y Figura 5), lo cual explica cómo su área se transforma año a año (Figura 5, Tabla 3 y 5) (Stevenson y Aldana, 2008). Este tipo de deforestación selectiva no se asocia directamente a la extracción de madera sino a cubrir las necesidades de leñateo para las actividades rurales, además de aperturas de caminos para la mecanización y la ganadería (Anexo 1), generando discontinuidades en el paisaje con diferente grado de resistencia para las especies dependientes de las coberturas arbóreas como los primates (Cerullo y Edwards, 2019; Ortiz-Moreno et al., 2022; Yanai et al., 2022). En el análisis de la estructura del paisaje, 2016 fue el año con mayor cantidad de hábitat disponible que favorece la presencia del P. ornatus (Carretero-Pinzón, 2017) (Figura 5).
Efecto de la fragmentación
En cuanto a la influencia de la transformación del paisaje sobre la biodiversidad, la reducción del hábitat para P. ornatus se hace más acentuada en el oeste del municipio donde se aprecia la reducción de las rondas hídricas que actúan como corredores ecológicos (Figura 2), así como el número y área de los fragmentos de bosque (Tabla 3), acompañadas por una baja heterogeneidad de coberturas, lo que reduce la diversidad de recursos para las especies silvestres (Fahrig et al., 2011; Sengupta et al., 2015; Arasa-Gisbert et al., 2021).
En cuanto al índice de forma, la literatura indica que entre mayor sea su valor el efecto de borde será más intenso en los fragmentos, por tanto, valores mayores a 3 tendrán baja calidad (Bogaert et al., 2002; Fahrig, 2003; Asquith y Mejía-Chang, 2005), tal y como los encontrados en la presente investigación (Tabla 3).
De acuerdo con Li et al. (2023), el contexto del paisaje influye sobre los patrones de biodiversidad local, siendo particularmente afectadas las especies que tienen requerimientos ecológicos particulares que les limitan usar grandes áreas para sus actividades vitales y que emplean una gama estrecha de recursos alimenticios. Además, la cantidad de hábitat disponible para las especies especialistas o que prefieren bosques continuos aumenta con el área nuclear (De Gabriel et al., 2022), siendo estas especies particularmente afectadas por la deforestación selectiva, tanto como la total, ya que se introducen las consecuencias del efecto de borde más allá de los límites del fragmento.
Análisis de los resultados del modelo matemático
El modelo matemático tiene dos estados de equilibrio, p 1*=0 y p 2*=1-(eμδI t R t D t /cαβA t C t F t ). Desde el punto de vista biológico, el equilibrio p 1* significa que existe la posibilidad de que la especie P. ornatus desaparezca del paisaje fragmentado; mientras que el equilibrio p 2*representa la posibilidad de que la especie persista en tal paisaje siempre que cαβAtCtFt > eμδItRtDt. La persistencia o la extinción de la especie en el paisaje depende de la relación entre los parámetros asociados a las características del paisaje. En efecto, si cαβAtCtFt < eμδItRtDt, el modelo predice que el equilibrio p 1* es asintóticamente estable; mientras que si cαβAtCtFt > eμδItRtDt, la predicción es que el equilibrio p 2* es asintóticamente estable. Estas predicciones del modelo significan que la especie persistirá en el paisaje fragmentado siempre y cuando los parámetros del paisaje que favorecen el proceso de colonización local (dimensión fractal) y aquellos que disminuyen la probabilidad de extinción local (área total y área nuclear) sean más intensos que los factores que aumentan la probabilidad de extinción (índice de forma y relación perímetro-área) y el que limita el proceso de colonización local (distancia al fragmento vecino más próximo) (Bogaert et al., 2002; Cudney-Valenzuela et al., 2022).
En otras palabras, si la conectividad del paisaje, su patrón de agregación (índice fractal) y la calidad de los fragmentos de bosque declinan entonces aumenta la probabilidad de que las subpoblaciones locales de la especie desaparezcan del paisaje. Por tanto, actividades que reduzcan la calidad y conectividad del paisaje son perjudiciales para la persistencia de la especie (Carretero-Pinzón et al., 2020), ya que pueden producir una disminución en la proporción de fragmentos de bosque que ella ocupa, lo cual implicaría una reducción en los tamaños promedios de las poblaciones locales (Rockwood, 2015).
De los datos del paisaje de San Martín (Meta) se tiene que el área total y el área nuclear de los fragmentos disminuyeron en la mayoría de los años, a excepción de 2015 y 2016, lo cual genera un aumento en la tasa media de extinción anual por fragmento, según el modelo. Alternativamente, en 2015 y 2016 la conectividad aumentó, haciendo que la tasa media de colonización anual por fragmento se haya incrementado para esos años. Sin embargo, la tasa media de extinción anual por fragmento supera la tasa media de colonización anual por fragmento en la mayoría de los años, menos en 2015 y 2016 (anexos 4 y 5). En consecuencia, la tendencia en el escenario base es hacia la disminución de la proporción de fragmentos ocupados por la especie (Figura 4), especialmente desde 2016 donde el modelo predice que no es posible una persistencia estable de la especie en el paisaje.
Los demás escenarios simulados predicen lo que podría suceder con la dinámica de la ocupación de fragmentos por parte de la especie al modificar las características del paisaje de San Martín en los mismos años. Las predicciones del modelo en el escenario intermedio, en el que se hicieron incrementos puntuales del área de cobertura, siguen la misma tendencia del escenario base (Figura 4). En el escenario de alta deforestación (Figura 4) se evidencia cómo al disminuir la conectividad del paisaje y la calidad de los fragmentos de bosque, la proporción de parches ocupados por la especie tiende a cero, lo cual predice que la especie desaparecería del paisaje agropecuario bajo estas condiciones. En contraste, el escenario pro-conservación muestra que el incremento de la conectividad, el área de cobertura y la calidad de los fragmentos aumenta en más de un 90% la proporción de fragmentos ocupados por la especie en la mayoría de años (Figura 4).
Implicaciones para la conservación de P. ornatus
La conservación in situ de primates requiere la ampliación del área y recursos del hábitat para las especies, dado que se ha evidenciado la importancia de la disponibilidad de alimento, así como del paisaje contexto con recursos complementarios, refugio y elementos que favorezcan la dispersión de los individuos (Carretero-Pinzón et al., 2017; Galán-Acedo et al., 2019; Arroyo-Rodríguez et al., 2020, 2023). Además, se ha identificado que es necesaria la conexión de los ecosistemas antropizados con las áreas protegidas para permitir el flujo de genes e individuos en el paisaje, ralentizando la formación de subpoblaciones en áreas afectadas por la fragmentación (Ruiz-Garcia y Shostell, 2016; Linero et al., 2020; Arasa-Gisbert et al., 2021; Chapman y Peres, 2021).
En el modelo propuesto en la presente investigación se evidencia la importancia de la conectividad y la dimensión fractal del paisaje, junto con el incremento en el área nuclear de los fragmentos para favorecer la conservación de P. ornatus, como se observa en el escenario de pro-conservación. Por tanto, se resalta la importancia de la restauración de la conexión entre los fragmentos a través de la siembra de especies nativas frugíferas aprovechables por P. ornatus (Carretero-Pinzón y Defler, 2016; Arroyo-Rodríguez et al., 2020). Además de aumentar la heterogeneidad de las coberturas en el paisaje para incrementar la permeabilidad de la matriz de pastos para los primates, así como la disponibilidad de recursos alimenticios para las especies (Arroyo-Rodríguez et al., 2020; Cudney-Valenzuela et al., 2022).
Conclusión
El modelo matemático propuesto para la presencia de P. ornatus en un paisaje agropecuario, muestra que la especie tenderá a desaparecer si la transformación de la cobertura boscosa en áreas de explotación agropecuaria se mantiene. Por tanto, es urgente aumentar la conectividad y la cantidad de hábitat disponible con el fin de que P. ornatus pueda sobrevivir en el entorno antropizado, siendo una especie endémica de gran importancia ecológica.