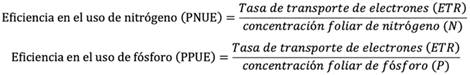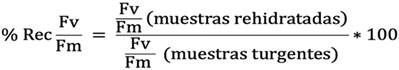Introducción
Una especie endémica es aquella cuya distribución se limita a una región geográfica específica y caracteriza a un ecosistema en particular (Noguera, 2017). El páramo es considerado un centro de endemismos y constituye uno de los ecosistemas de mayor importancia biológica por su historia ecológica y evolutiva ligada a la formación de los Andes y alberga una gran diversidad con más de 500 géneros y 3.500 especies de plantas vasculares nativas, de las cuales hasta un 60% pueden ser endémicas (Cabrera y Ramírez, 2014; Madriñán et al., 2013; Rangel, 1999). Posiblemente el alto porcentaje de endemismo se debe a varios factores. En primer lugar, se plantea una radiación adaptativa, ya que las tasas de diversificación de las plantas aumentan debido a la necesidad de adaptarse a las condiciones locales extremas, como la radiación ultravioleta (Madriñán et al., 2013). Sin embargo, Zachos et al., (2008) y Luebert y Weigend (2014) mencionan que el enfriamiento por la formación de la cadena montañosa de los Andes es otro factor que pudo haber disparado la diversificación de plantas en el páramo.
La hipótesis de endemismo que se puede aplicar a las condiciones del páramo puede ser la “especialista” basada en Meyer (1986), que plantea que las especies endémicas resultan de cambios fenotípicos oportunos en respuesta a la heterogeneidad ambiental, es decir que tienen una menor amplitud ecológica y una mayor competitividad, con base a un balance entre el grado de especialización y la amplitud ecológica. Por el contrario, las especies generalistas de amplia distribución ocupan un mayor rango ambiental debido a su mayor plasticidad, pero con una menor competitividad en determinados ambientes (Galmes et al., 2010). La asociación que existe entre los parámetros ambientales y los rasgos funcionales puede indicar que las especies endémicas son raras debido a la especialización adaptativa y a la selección a favor de ciertos rasgos funcionales, es decir, a su convergencia evolutiva (Behroozian et al., 2020). De acuerdo con esta hipótesis debería ser posible entender las características de plantas endémicas y no endémicas simpátricas a través del estudio de rasgos funcionales fisiológicos y los contextos del ambiente del páramo como una medida para su conservación.
Gran parte de las investigaciones ecofisiológicas en plantas endémicas de páramo se han orientado al estudio de adaptaciones a factores ambientales específicos, como temperatura o radiación. Se destacan en este sentido los trabajos en especies de los géneros Espeletia y Puya, que han demostrado que estas plantas han generado adaptaciones que favorecen el mantenimiento de la temperatura, y del equilibrio hídrico en las condiciones severas del entorno paramuno, con mecanismos de prevención tales como el sobreenfriamiento, el aislamiento por la retención de necromasa, la secreción de fluidos mucilaginosos y pubescencia densa en las hojas (Molina-Montenegro y Cavieres, 2010; Muraoka et al., 1998; Rada et al., 2019). Sin embargo, aún no es claro cómo difieren estas características entre especies endémicas y las no endémicas que coexisten en el ecosistema de páramo, por otra parte, es necesario entender otros rasgos ligados a las condiciones del páramo como la tolerancia a la desecación, el uso eficiente de nitrógeno y fósforo teniendo en cuenta que este ecosistema tiene limitaciones en nutrición y son regiones complejas topográfica y climáticamente, con algunos de los gradientes más amplios de precipitación y temperatura (Killeen et al., 2007; Young et al., 2011).
Investigaciones en otros ecosistemas han determinado que las plantas endémicas difieren significativamente de las no endémicas en varios parámetros, en particular en la capacidad fotosintética (Am), contenido foliar de nitrógeno y área foliar específica (SLA) que, por ejemplo, presentan valores menores en las especies endémicas mediterráneas que en las no endémicas. Estas diferencias pueden implicar que una mayor proporción de la biomasa foliar está constituida de compuestos y estructuras no fotosintéticas en las endémicas y que la disminución de la capacidad competitiva de estas especies podría ser consecuencia de dedicar grandes cantidades de recursos a la síntesis de compuestos defensivos, dada la evolución bajo alta presión por herbivoría en estas islas (Bover y Alcover, 2000; Gulías et al., 2003).
En ambientes insulares mediterráneos, las especies endémicas y no endémicas no presentan diferencias en rasgos como SLA ni en contenido de nitrógeno, pero sí difieren significativamente en cuanto a fotosíntesis por área y uso eficiente del nitrógeno, donde las especies endémicas presentaron valores menores, con posibles efectos en la capacidad de asimilación de CO2 y el crecimiento (Gulías et al., 2003). Diferencias similares se encontraron en el sistema insular de Hawaii con alto porcentaje de endemismos donde las especies nativas presentan baja Am, SLA y tasa relativa de crecimiento en comparación con especies invasivas. Este hecho se ha relacionado con la capacidad competitiva e invasiva de estas especies, las cuales dedicarían más recursos al crecimiento y la reproducción que a los mecanismos de defensa promoviendo tasas de crecimiento más rápidas (Baruch y Goldstein, 1999; Durand y Goldstein, 2001; Pattison et al., 1998). Por otra parte, se ha encontrado que las especies endémicas o especialistas podrían ser incapaces de tolerar la variación en las condiciones microambientales que sí toleran las especies generalistas y, por tanto, esto puede limitar la distribución de las especies (Maliakal, 2003).
Teniendo en cuenta lo anterior, esta investigación pretende comparar rasgos fisiológicos de las especies endémicas y generalistas del ecosistema de páramo, ya que este tema es de gran relevancia para determinar las estrategias que presentan estas especies para sobrevivir y distribuirse en un ecosistema con condiciones ambientales extremas. De igual manera, generar información importante para la toma de decisiones y acciones de conservación, establecimiento de vulnerabilidad y planes de manejo tanto de las especies como del ecosistema bajo escenarios futuros de cambio climático.
Materiales y métodos
Área de estudio
La investigación se llevó a cabo en el Páramo Las Ovejas (Nariño, Colombia), a una elevación entre 3.000 y 4.100 msnm (00°55”N - 77°23”O). Tiene un clima frío y húmedo con una precipitación media anual de 1.050,5 mm, presentando un comportamiento bimodal, con períodos lluviosos entre marzo-mayo y octubre-diciembre. La temperatura media anual es de 9°C con pocas variaciones estacionales (± 1°C durante todo el año), la temperatura máxima promedio es de 14°C y la mínima de 5°C; para el período de muestreo, la precipitación fue de 997,6 mm, inferior a la precipitación media de los últimos 10 años (1.114,5 mm) (Solarte et al., 2015; CORPONARIÑO - Universidad de Nariño, 2009).
Los análisis de suelo en el sitio de muestreo indicaron que el Páramo Las Ovejas tiene un suelo orgánico, con una densidad aparente de 0,51 g/cc, un pH de 4,73 y una capacidad de intercambio catiónico de 65,8 (meq/100 g). Ecológicamente el área de muestreo se caracteriza por formaciones vegetales de tipo frailejonal-pajonal, con dominancia de Espeletia pycnophylla, Calamagrostis effusa, Carex xenophyllum, Rhynchospora macrochaeta y helechos y arbustos de los géneros Blechnum, Weinmannia, Miconia, Diplostephium (Solarte et al., 2015).Selección y muestreo de especies
Se eligieron 14 especies de hoja perenne (Tabla 1) y se clasificaron como endémicas o no endémicas siguiendo el concepto de endemismo biogeográfico. En este sentido, todas las especies con una distribución restringida al ecosistema del páramo (rango altitudinal entre 3.000 y 4.100 msnm) se consideraron endémicas y aquellas que muestran un área de distribución más amplia se clasificaron como no endémicos. El área de distribución de cada especie se determinó mediante revisión bibliográfica de Bernal et al., (2015), Fernández-Alonso (2002), Miranda-Esquivel et al. (2002), Rangel (1999), Rangel et al. (1992) y Solarte et al., (2015).
Tabla 1 Lista de especies de plantas endémicas y no endémicas muestreadas en el Páramo Las Ovejas.
| Especie | Familia | Historia evolutiva | Forma de vida | Rango de distribución |
|---|---|---|---|---|
| Loricaria thuyoides | Asteraceae | E | Subarbusto | 3.000-4.500 |
| Espeletia pycnophylla | Asteraceae | E | Roseta caulescente | 3.000-4.250 |
| Pentacalia vaccinioides | Asteraceae | E | Subarbusto | 3.000-3.990 |
| Diplostephium tabanense | Asteraceae | E | Arbusto | 3.000-3.900 |
| Gynoxys sancti-antonii | Asteraceae | E | Arbusto | 3.150-4.200 |
| Geranium rhomboidale | Geraniaceae | E | Hierba | 3.000-3.600 |
| Weinmannia brachystachya | Cunoniaceae | NE | Arbusto | 2.790-3.700 |
| Clusia multiflora | Clusiaceae | NE | Árbol | 80-3.500 |
| Hypericum mexicanum | Hypericaceae | NE | Subarbusto | 1.700-4.200 |
| Diplostephium floribundum | Asteraceae | NE | Arbusto | 2.380-3.860 |
| Vaccinium floribundum | Ericaceae | NE | Subarbusto | 1.600-4.600 |
| Pernettya prostrata | Ericaceae | NE | Subarbusto | 2.000-4.525 |
| Miconia chlorocarpa | Melastomataceae | NE | Arbusto | 2.500-3.750 |
| Themistoclesia epiphytica | Ericaceae | NE | Subarbusto | 2.400-4.000 |
Nota. Historia evolutiva: E: endémica, NE: no endémica. Forma de vida (Arzac et al., 2011). Rango de distribución (Bernal et al., 2015).
Fuente: los autores.
Las especies elegidas se muestrearon de octubre a diciembre de 2017; la altura mínima de colecta fue 3.337 msnm y la máxima 3.508 msnm. Los individuos muestreados se seleccionaron de acuerdo con los siguientes criterios de inclusión: sanos, con rastro de reproducción y separados por un mínimo de 10 metros para garantizar que no sean clones. El muestreo se realizó de conformidad con la Resolución N° 126 del 19 de febrero de 2015 emitida por la Corporación Autónoma Regional de Nariño (Corponariño) a través de la cual se otorga un permiso marco para la recolección de especímenes silvestres de diversidad biológica para fines de investigación científica no comercial.
Rasgos funcionales de la hoja
Área foliar específica (SLA): se calculó como la relación entre el área foliar y el peso seco de la hoja. Los datos fueron tomados de 10 individuos de cada especie y 5 hojas por individuo.
Capacidad fotosintética: se estimó a partir de curvas de inducción con un pulso de luz saturante (alrededor de 15 segundos a 1.500 μmol m-2 s-1), en hojas previamente adaptadas a oscuridad por mínimo 30 minutos, utilizando un fluorómetro JUNIOR PAM (Walz, Alemania). A partir de las curvas de inducción, se obtuvieron los parámetros de eficiencia cuántica máxima del fotosistema II (Fv/Fm), Quenching no fotoquímico (NPQ) (Maxwell y Johnson, 2000) y la tasa de transporte de electrones (ETR) que se calculó mediante la fórmula: ETR= φPSII * PPFD * 0,5 * 0,84 (Baker, 2008), donde φPSII corresponde al rendimiento cuántico actual del PSII, estimado como (Fm’-Ft /Fm’) (Maxwell y Johnson, 2000); PPFD representa la densidad de flujo fotónico fotosintético; el 0,5 asume una distribución equitativa de los fotones absorbidos entre el PSI y el PSII y 0,84 corresponde a la fracción de luz absorbida por la hoja. Los datos fueron tomados de 10 individuos de cada especie y 5 hojas por individuo.
Nutrientes foliares: se evaluó el contenido foliar de nitrógeno (N) con el método de Kjeldahl, mientras que el contenido foliar de fósforo (P) con el método de azul de molibdeno; se analizaron 42 muestras en total, tres repeticiones para cada especie; las muestras fueron procesadas en los Laboratorios Especializados de la Universidad de Nariño.
Tomando los datos de capacidad fotosintética y nutrientes foliares, se calculó la eficiencia en el uso del nitrógeno (PNUE-μmol electrones.mg N-1.S-1) y la eficiencia en el uso de fósforo PPUE (μmol electrones.mg P-1.S-1), con las fórmulas que se indican a continuación:
Resistencia a la desecación del tejido fotosintético: se evaluó de acuerdo con el protocolo de Wood (2007), se tomaron 100 mg de tejido fotosintético, se hidrataron a 100 * 100 de contenido hídrico relativo CHR (turgencia) y se midió Fv/Fm, posteriormente se establecieron tres condiciones en las que las muestras se desecaron (75%, 30% y <10% de humedad relativa), luego se evalúo Fv/Fm, posteriormente se rehidrataron las muestras durante 24 h y se midió Fv/Fm. La resistencia a la desecación se determinó con el porcentaje de recuperación de Fv/Fm, de acuerdo con la siguiente fórmula:
En cuanto al análisis estadístico, se promediaron los datos obtenidos para cada rasgo, se imputaron los valores atípicos y se aplicaron pruebas de normalidad (prueba de Kolmogorov-Smirnov con la corrección de Lilliefors), se realizaron pruebas de t-Student para determinar si las especies endémicas difieren significativamente de las no endémicas en cuanto a los rasgos foliares evaluados; adicionalmente, se realizaron correlaciones de Pearson para evaluar las relaciones funcionales entre los rasgos medidos en especies endémicas y no endémicas. Para todas las pruebas se estableció un α = 0,05. Los análisis estadísticos se realizaron en R-Studio.
Resultados
Las especies endémicas difieren significativamente de las no endémicas en cuanto a SLA, N, P, ETR y resistencia a la desecación, además, se resalta que las especies endémicas en todos los rasgos presentan valores significativamente mayores que las especies no endémicas (Tabla 2 y Figura 1). Para tener una visión un poco más amplia del estado fotosintético de las especies evaluadas, además de ETR, se midió el rendimiento cuántico máximo del fotosistema II (Fv/Fm) encontrando que las especies endémicas tienen un promedio de 0,801, mientras que las no endémicas 0,786, no habiendo diferencias estadísticamente significativas (p=0,18). También, se midió el Quenching no fotoquímico (NPQ) y se encontró que las especies endémicas presentan un valor de 2,24 significativamente menor que el registrado en las no endémicas que fue 2,86 (p <0,001).
Tabla 2 Rasgos funcionales de las hojas de especies endémicas y no endémicas presentes en el Páramo Las Ovejas (Nariño, Colombia).
| Rasgo foliar | Unidades | Promedio especies endémicas | Promedio especies no endémicas | Prueba comparación de medias |
|---|---|---|---|---|
| Área foliar específica (SLA) | cm2/g | 84,46 | 70,12 | t-Student (p<0,001)* |
| Contenido foliar de nitrógeno (N) | % | 1,31 | 1,14 | t-Student (p=0,041)* |
| Contenido foliar de fósforo (P) | ppm | 830,06 | 630,42 | t-Student (p=0,01)* |
| Tasa de transporte de electrones (ETR) | μmol electrones.m-2.s-1 | 89,49 | 71,46 | t-Student (p<0,001)* |
| Resistencia a la desecación | % recuperación Fv/Fm | 57,08 | 34,28 | t-Student (p<0,001)* |
* Resultados estadísticamente significativos.
Fuente: los autores.
Adicionalmente, se calculó la eficiencia en el uso del nitrógeno (PNUE) y la eficiencia en el uso del fósforo (PPUE). Respecto a PNUE se presentan diferencias estadísticamente significativas y las especies endémicas tienen valores mayores a 0,009 μmol electrones.mg N-1.S-1 respecto a las no endémicas 0,006 μmol electrones.mg N-1.S-1. En cuanto al PPUE, se encontraron diferencias estadísticamente significativas. Las especies endémicas muestran un mayor promedio 0,15 μmol electrones.mg P-1.S-1 respecto a las no endémicas 0,12 μmol electrones.mg P-1.S-1.
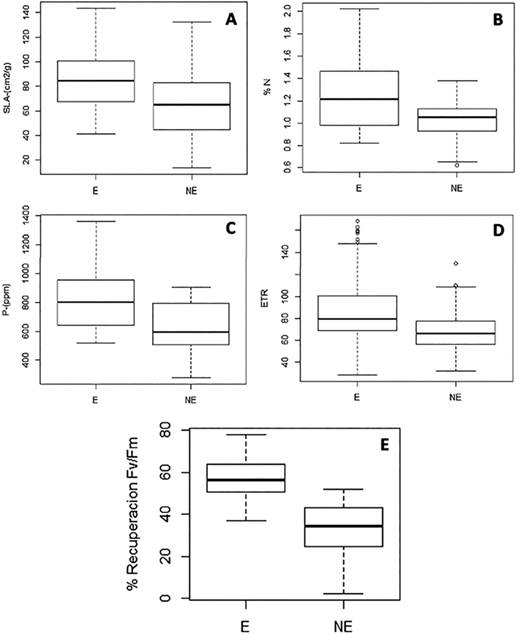
Fuente: los autores.
Figura 1 Comparación de medias de rasgos foliares en especies endémicas y no endémicas evaluadas en el Páramo Las Ovejas (Nariño, Colombia). A. Área foliar específica. B. Contenido foliar de nitrógeno. C. Contenido foliar de fósforo. D. Tasa de transporte de electrones. E. Resistencia a la desecación.
Para evaluar las respuestas funcionales de las especies evaluadas se realizó un análisis de correlación de Pearson (Figura 2); para las dos categorías fue significativo en el caso de N-P con un valor p<0,01, para las especies endémicas la correlación tuvo un valor de 0,89 mientras que para las no endémicas fue 0,86 indicando que a medida que incrementa la concentración foliar de nitrógeno la de fósforo también lo hace. Por otra parte, solo para las especies endémicas se encontró significancia en la correlación positiva entre el SLA-ETR y una asociación negativa entre ETR-% Rec Fv/Fm mostrando que a medida que el ETR aumenta el % Rec Fv/Fm disminuye.
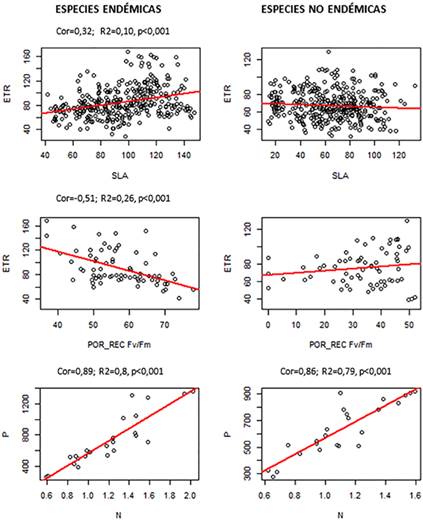
Fuente: los autores.
Figura 2 Correlaciones de Pearson rasgos funcionales como área foliar específica (SLA), tasa de transporte de electrones (ETR), resistencia a la desecación (% Rec Fv/Fm), concentración foliar de nitrógeno (N) y concentración foliar de fósforo (P) en especies endémicas y no endémicas evaluadas en el Páramo Las Ovejas (Nariño, Colombia).
Discusión
Los resultados muestran que las especies endémicas presentan valores elevados de SLA, lo cual indica que tienen hojas más delgadas y con menor densidad o grosor en comparación con las no endémicas. Esto sugiere que podrían tener mayores tasas potenciales de crecimiento relativo y un mejor aprovechamiento de los recursos. Un mayor SLA puede aumentar la capacidad de la planta para asimilar CO2 porque se producen más hojas para una determinada masa de carbono invertida en tejidos fotosintéticos (Lambers y Poorter, 1992). Las especies no endémicas presentaron valores de SLA que están asociados con una mayor densidad o grosor tisular, por lo tanto, una mayor asignación de biomasa a componentes estructurales en lugar de metabólicos. Estas características llevarían a aumentar la longevidad foliar, pero también da lugar a una mayor sombra interna y posiblemente a problemas difusionales para la asimilación fotosintética (Reich et al., 1999; Wright et al., 2004).
Los datos indican la existencia de dos estrategias contrastantes. Por un lado, las especies endémicas pueden catalogarse como adquisitivas, ya que presentan valores elevados de SLA y altos contenidos de nutrientes foliares (N y P). Esta combinación favorece elevadas tasas de transporte de electrones y eficiencia fotosintética, pero conlleva baja inversión estructural en mecanismos de defensa física contra la herbivoría (Poorter y Bongers, 2006; Wright et al., 2004). Como resultado, estas especies desarrollan hojas nutricionalmente atractivas, lo cual las hace más susceptibles a tasas más altas de herbivoría (Zandt, 2007) y descomposición (Pérez-Harguindeguy et al., 2000). Por otro lado, las especies no endémicas pueden clasificarse como conservativas, ya que presentan valores bajos de SLA y menores concentraciones de nutrientes foliares. Esto sugiere una mayor inversión de carbono en estructuras más resistentes, lo que reduce la herbivoría e incrementa la longevidad foliar (Reich et al., 2009; Stamp, 2003; Züst y Agrawal, 2017).
En especies endémicas se presentaron mayores valores de SLA y ETR en comparación con las no endémicas. Esto podría explicarse puesto que las hojas con mayor SLA son hojas más delgadas que facilitan la llegada de CO2 al sitio de carboxilación y también puede influir en la conductancia del mesófilo al CO2 (Flexas et al., 2008). Además, al tener una alta relación área/masa habrá mayor captación de luz haciendo más eficiente el proceso fotosintético, lo cual podría considerarse una ventaja ecológica que responde a la hipótesis “especialista” de plantas endémicas, dado que hay una mayor captación de recursos confiriendo a la planta mayor capacidad competitiva (Reich et al., 1999). Según Wright et al., (2004), una combinación de mayor SLA, mayor capacidad fotosintética y mayor contenido de nitrógeno generaría mayor metabolismo indicando que son especies de retorno rápido con altas tasas de crecimiento relativo aunque con menor longevidad foliar y más propensas a la herbivoría. Las especies no endémicas tuvieron bajos valores tanto de SLA como de ETR, probablemente hay un desacople de esta relación ya que al ser especies generalistas en un ambiente con condiciones poco favorables como el páramo deben desarrollar otras estrategias para poder establecerse y sobrevivir.
En especies endémicas, la ETR es más alta comparada con las no endémicas al igual que Fv/Fm indicando que tienen una alta capacidad fotosintética y quizá son especies mejor adaptadas a las condiciones adversas del páramo como baja temperatura y alta radiación, factores que afectan directamente el rendimiento fotosintético; esto, además de verse reflejado en los valores del rasgo evaluado, también se ve en su alta presencia relativa en la zona de muestreo, como lo indica el trabajo realizado por Solarte et al., (2015) en la misma zona de muestreo donde una de las especies con mayor frecuencia relativa es Espeletia pycnophylla (endémica) y las especies no endémicas evaluadas presentan bajas frecuencias relativas.
Las especies no endémicas, además de presentar valores bajos de ETR, mostraron un incremento significativo de NPQ en comparación con las especies endémicas. Este aumento podría estar relacionado con mecanismos de fotoprotección que reducen la formación de especies reactivas de oxígeno, como el ciclo de las xantofilas; en este sentido, se sugiere que las especies no endémicas podrían presentar una mayor formación de zeaxantina, posiblemente como respuesta al incremento en el rango altitudinal en el que suelen establecerse (Adams III et al., 2008).
En este estudio, se observó que las especies endémicas exhiben un porcentaje promedio de recuperación de Fv/Fm del 57% cuando su contenido hídrico relativo desciende por debajo del 30%, lo que sugiere una tolerancia moderada a la desecación, esta capacidad podría estar asociada a mecanismos como el ajuste osmótico, la elasticidad celular y la activación de proteínas específicas, tales como las proteínas abundantes de embriogénesis tardía (LEA), que protegen proteínas y membranas del daño causado por la deshidratación (Hoekstra et al., 2001; Laloi et al., 2004).
Es llamativo que, en un ambiente tan húmedo, las especies endémicas presenten una alta resistencia a la desecación. Esto podría explicarse por el hecho de que, a pesar de la abundante disponibilidad de agua, factores como los fuertes vientos, las bajas temperaturas, el encharcamiento y la alta radiación pueden generar episodios puntuales de desecación (Leuschner, 2000). Como respuesta a estas condiciones, estas plantas desarrollan características xeromórficas que les permiten tolerar el estrés hídrico (Alpert, 2000; Moreno, 2009), este es el caso de Espeletia pycnophylla que presenta estomas encriptados, característicos de especies adaptadas al estrés hídrico, cuya función principal es reducir la transpiración, maximizar la eficiencia en el uso del agua (Hassiotou et al., 2009; Roth-Nebelsick et al., 2009).
Por otro lado, las especies no endémicas tienen un bajo porcentaje de recuperación de Fv/Fm (en promedio un 34%), por lo cual podrían clasificarse como sensibles a la desecación, ya que no pueden recuperar su funcionalidad después de que su contenido hídrico descendió por debajo del 30%. Esto podría deberse a que estas especies provienen de zonas de menor altitud y, al establecerse en el páramo, se enfrentan a un mayor déficit hídrico, ya que las bajas temperaturas limitan la absorción de agua tanto atmosférica como por parte de las raíces; si bien cuentan con mecanismos generales de respuesta al estrés hídrico, estos pueden no ser suficientemente eficientes o especializados para enfrentar las condiciones particulares del páramo, lo cual reduce su capacidad de tolerar la desecación en comparación con las especies endémicas de este ecosistema (Gaff y Oliver, 2013).
Se encontró una tendencia de asociación negativa entre ETR y porcentaje de recuperación de Fv/Fm en especies endémicas, la cual indica que cuando la ETR sube una unidad el porcentaje recuperación de Fv/Fm disminuye 0,26%. Se sabe que la tolerancia a la desecación se relaciona en parte con diversos mecanismos que le ayudan a la planta a sobrevivir después de periodos de desecación; cabe destacar que el aumento evolutivo observado en la capacidad fotosintética es de alguna manera paralelo a la disminución en la frecuencia de la tolerancia a la desecación (Alpert, 2000; Oliver et al., 2000). La existencia de un equilibrio entre capacidad fotosintética y resistencia a la desecación se ha propuesto ya que surge la tendencia del aumento de la capacidad fotosintética desde las plantas tempranas hacia las más modernas, y este aumento de la capacidad fotosintética fue relacionado en primera instancia con la aparición de estomas, seguido de un aumento gradual de su complejidad morfológica y regulación (Franks y Farquhar, 2007), pero el aumento evolutivo observado en la capacidad fotosintética de alguna manera es paralelo a la disminución en la frecuencia de tolerancia a la desecación. Alpert (2000) sugiere que para taxones más evolucionados la tolerancia a la desecación se puede interpretar como un regreso en la evolución que se puede adaptar para algunos entornos específicos, dado que la capacidad de tolerar la desecación conlleva costos que limitan la productividad.
Por otra parte, los resultados obtenidos respecto al contenido foliar de nutrientes indican que, a pesar de la baja concentración de P (3,63 ppm) y N (0,79 %) disponible en el suelo, así como de la extrema acidez que puede dificultar su absorción, las especies endémicas presentan un contenido foliar de P (830,06 ppm) y N (1,31 %) significativamente mayor que las especies no endémicas, las cuales alcanzan valores de P (630,42 ppm) y N (1,1 %). Esta diferencia también se refleja en las eficiencias, dado que las especies endémicas muestran una mayor eficiencia en el uso de nitrógeno (PNUE) y fósforo (PPUE) en comparación con las no endémicas. Probablemente, esto se deba a que las especies no endémicas, al extender su límite altitudinal de distribución, podrían ver restringida la absorción de N y P, sobreviviendo con menores eficiencias en el uso de nutrientes. En consecuencia, esto podría limitar su crecimiento, particularmente en lo que respecta al desarrollo del área foliar y a la tasa fotosintética (Huang et al., 2017; Marschner y Clarkson, 1995).
Respecto a PPUE, es mayor en las especies endémicas ya que se está concentrando mayor cantidad de P a las células del mesófilo que puede permitir una mejor reabsorción y asignación de P, aumentando la capacidad fotosintética (Reich et al., 2009). En relación con PNUE, los resultados reflejan que un menor SLA a baja disponibilidad de N y P causa la reducción de PNUE, como se observa en las especies no endémicas, las hojas de menor SLA tienen un PNUE reducido porque se invierte una mayor proporción de N foliar en las paredes celulares y compuestos no involucrados en la fijación de C (como estructuras y metabolitos de defensa) y hay una mayor resistencia a la difusión de CO2. En consecuencia, la asignación de N para las enzimas fotosintéticas se reduce, lo que resulta en una reducción de la tasa fotosintética (Onoda et al., 2004; Takashima et al., 2004).
Los resultados encontrados en esta investigación difieren de lo reportado para otras especies endémicas (Baruch y Goldstein, 1999; Durand y Goldstein, 2001; Gulías et al., 2003; Pattison et al., 1998) dado que las especies endémicas de páramo tienen mayor SLA, ETR, concentración de N, P y resistencia a la desecación, lo que indica que estas especies responden de diferente manera a las de zonas bajas. Posiblemente esto se deba a que el páramo se podría considerar una isla biogeográfica que ha generado endemicidad adaptada al clima, por lo tanto, los endemismos son dominantes y presentan mejor desempeño fisiológico en comparación con las especies no endémicas. Tal vez esto se deba a que estas especies están colonizando el páramo hace poco tiempo; Dulhoste (2010) y Llambí (2015) han enfatizado en aspectos como los cambios en la composición y estructura de la vegetación en el gradiente altitudinal, indicando que se ha generado una ampliación de nicho y rango de establecimiento hacia las zonas altas. Por lo tanto, se podría decir que las especies no endémicas, al ser relativamente nuevas en páramo en comparación con las endémicas, están en proceso de adaptación a las nuevas condiciones climáticas y esto se ve reflejado en su bajo desempeño fisiológico.
Conclusiones
Este estudio permitió determinar que las especies endémicas difieren significativamente de las no endémicas, presentando valores más altos de SLA, ETR, N, P y porcentaje de recuperación de Fv/Fm, pero menores de NPQ, indicando mayor desempeño fisiológico. Asimismo, se evidencia que las plantas endémicas y no endémicas responden de manera diferencial a las presiones ambientales del páramo, esto se refleja en los valores y asociaciones entre los rasgos evaluados. En general, las especies endémicas exhiben mejores características adaptativas, lo cual se traduce en una mayor tasa de crecimiento, una mayor capacidad fotosintética y un uso más eficiente de los recursos.