Introducción
La alteración del hábitat y la intensificación del uso de la tierra con fines de desarrollo, probablemente son los factores que más influyen en la pérdida de diversidad biológica (Sala et al., 2000), además, representan un riesgo en el aumento de la prevalencia de enfermedades infecciosas que son transmitidas por vectores a hospederos vertebrados (Hatcher et al., 2012; Hooper et al., 2012; Lafferty et al., 2008). La prevalencia de hemosporidios en aves se ha relacionado con diferentes características del hábitat, como cambios en el microclima, cobertura vegetal, cercanía a cuerpos de agua y temperatura ambiental, debido a que se asocian con la dinámica poblacional de los vectores y, por lo tanto, con la transmisión de patógenos (Harvell et al., 2002; LaPointe et al., 2012; Myers et al., 2013; Renner et al., 2016). Así mismo, la prevalencia se ha relacionado con aspectos biológicos y ecológicos de los hospederos, como estrato de alimentación, sexo, tipo de nido, migración, grupo filogenético y masa corporal (De Angeli, 2024; Fecchio et al., 2011; González et al., 2014; Jones et al., 2024; Pulgarín-R. et al., 2018). Los hemosporidios que infectan aves son parásitos protozoarios del orden Haemosporida y phylum Apicomplexa, que a su vez se clasifican en cuatro géneros: Haemoproteus, Plasmodium, Leucocytozoon y Fallisia, y cada uno de los géneros está asociado a un grupo de vectores dípteros, donde llevan a cabo su etapa de reproducción sexual, permitiéndoles completar su ciclo de vida (Guillén-Rodríguez et al., 2024; Santiago-Alarcón y Marzal, 2020; Valkiūnas, 2005).
La infección por hemosporidios suele prolongarse durante muchos años, incluso de por vida, con eventuales recaídas que facilitan la transferencia de parásitos a nuevos hospederos (Valkiūnas, 2005). Aunque los efectos causados por la infección de hemosporidios generalmente no son letales, se ha descrito que pueden alterar la biología y ecología de los hospederos debido a que pueden provocar anemia (Santiago-Alarcón et al., 2012), reducir el consumo de alimentos, retrasar la reproducción y disminuir la cantidad de huevos en las posturas (Marzal et al., 2005; Schoepf et al., 2022). Sin embargo, también se han reportado casos de letalidad, particularmente en hospederos que no habían estado expuestos al parásito anteriormente, como en las aves nativas de Hawai o en el caso de parásitos especialistas, cuando infectan hospederos que se encuentran filogenéticamente más lejanos de sus hospederos habituales (Atkinson et al., 2000; Galen et al., 2022; Van Riper et al., 1986).
Las investigaciones que analizan la frecuencia de infección y diversidad de parásitos con los rasgos del hospedero y a su vez con las características del hábitat, permiten comprender cómo se dan las interacciones entre hospedero-vector-parásito, particularmente en ambientes modificados antropogénicamente, pues son de mucha utilidad para analizar los efectos del cambio en el uso del suelo sobre las infecciones patógenas (Civitello et al., 2015; Reinoso-Pérez et al., 2016; Vittor et al., 2006). Aunque aún no existe un consenso general sobre la respuesta de la infección a la transformación del hábitat, debido a que algunos autores reportan cambios negativos (Ferreira-Junior et al., 2018; Neumann et al., 2024), otros positivos (Chasar et al., 2009; Laurance et al., 2013) y otros no reportan ningún efecto (Hoesel et al., 2020), sugiriendo que se requieren más investigaciones que ayuden a interpretar estas relaciones.
En Colombia se han realizado diversos estudios sobre hemosporidios en aves, asociados a varios ecosistemas (Álvarez-Londoño et al., 2022; Basto et al., 2006; González, 2013; González et al., 2015; Hernández-Ospina et al., 2024; Lotta et al., 2016; Mantilla et al., 2013; Matta et al., 2004; Rodríguez et al., 2009; Tamayo-Quintero et al., 2023), que han permitido describir nuevas especies de hemoparásitos aviares, así como nuevas interacciones entre parásitos, linajes moleculares y hospederos (González et al., 2015; Lotta et al., 2015, 2019; Mantilla et al., 2013; Matta et al., 2014a; Walther et al., 2014). Sin embargo, la mayoría de estas investigaciones se concentran en el centro y nororiente del país, especialmente en las cordilleras Oriental y Central, mientras que son menos los estudios reportados en el suroccidente colombiano (Bennett y Borrero, 1976; Lotta et al., 2015; Lotta-Arévalo et al., 2023; Valkiūnas et al., 2003).
A pesar de la notable diversidad de aves y ecosistemas en Colombia, y particularmente en el departamento del Cauca, el conocimiento sobre la presencia y distribución de hemosporidios en esta región sigue siendo limitado. En este contexto, es necesario explorar la presencia de hemoparásitos en aves del suroccidente del país, considerando además los cambios en la cobertura vegetal como un posible factor asociado a la dinámica hospedero-parásito. Por tanto, el objetivo de este estudio fue determinar la frecuencia de infección de hemosporidios en aves de la Bota Caucana y evaluar su posible asociación con la altitud y tipo de cobertura vegetal.
Materiales y métodos
Área de estudio
El estudio se llevó a cabo en el municipio de Santa Rosa, departamento del Cauca, ubicado en el ramal centro-oriental de los Andes colombianos, en la denominada Bota Caucana, donde convergen el Macizo Colombiano y el piedemonte andino-amazónico. Santa Rosa se encuentra en un gradiente altitudinal que va desde los 1.100 hasta 4.350 m, con una precipitación promedio anual de 2.170 mm en la cabecera municipal, y presenta un régimen pluviométrico de tipo bimodal, con un periodo lluvioso entre abril-agosto y un periodo de menor intensidad de lluvias entre septiembre y finales de marzo (Paredes-Leguizamón, 2018).
El ecosistema predominante en la zona de estudio corresponde a bosque subandino (Cuatrecasas, 1958). Los muestreos se realizaron en tres sectores distintos, La Cocha, El Placer y la zona de amortiguamiento del área protegida Serranía la Vieja, los cuales estuvieron representados por tres tipos de cobertura vegetal: bosque denso, bosque fragmentado y pastos arbolados, seleccionados en campo mediante observación directa y con base en la clasificación de coberturas del IDEAM (Cruz, 2012) (Figura 1). La altitud de los puntos de muestreo varió entre 1.642 y 2.107 m (Tabla 1).
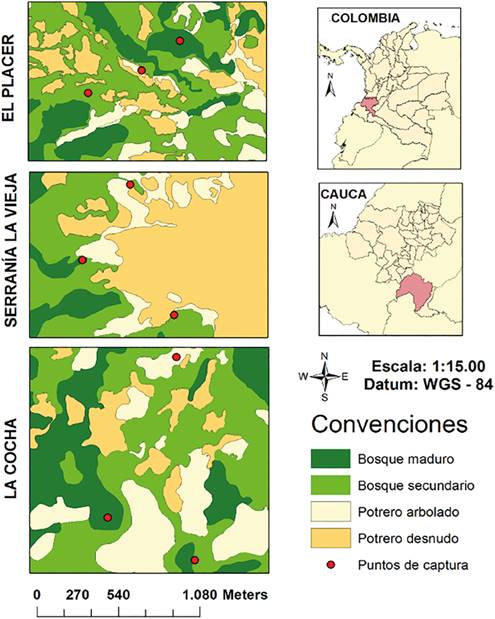
Fuente: Betancourt-Hernández R. del P.
Figura 1 Mapa de coberturas para la zona de estudio con base en la clasificación del IDEAM (2012), municipio de Santa Rosa, Cauca, suroccidente de Colombia.
Tabla 1 Puntos de muestreo, tipos de cobertura vegetal, valores de riqueza específica de aves, frecuencia de infección general por género de hemosporidios y clasificación de parasitemia en aves del suroccidente de Colombia.
| Sector | Cobertura vegetal | Coordenadas (DD) | Elevación m | N° individuos / N° especies | N° individuos positivos / Frecuencia general de infección (%) | Frecuencia de infección por género % | Clasificación de parasitemia (N° individuos) |
|---|---|---|---|---|---|---|---|
| Bosque denso | 1.7041667 N-76.586389 W | 1975 | 28 / 13 | 6 / 21,43 | H (14,2); P (7,14); L (7,14) | Alta (1); Media (3); Baja (4) | |
| Serranía la Vieja | Bosque fragmentado | 1.700833 N -76.58111 W | 1779 | 41 / 12 | 4 / 9,75 | P (9,75); L (2,43) | Alta (1); Media (3); Baja (1) |
| Pastos arbolados | 1.708611 N -76.583611 W | 1893 | 22 / 13 | 3 / 13,63 | H (9,09); P (4,54) | Alta (1); Media (1); Baja (1) | |
| Bosque denso | 1.7336111 N- 76.6075 W | 1900 | 51 / 24 | 9 / 17,64 | H (3,92); P (7,84); L (5,88) | Alta (3); Media (2); Baja (4) | |
| El Placer | Bosque fragmentado | 1.7305556 N-76.612777 W | 2107 | 33 / 23 | 10 / 30,30 | H (15,15); P (9,09); L (18,18) | Alta (2); Media (10); Baja (2) |
| Pastos arbolados | 1.7319444 N-76.609722 W | 1974 | 48 / 19 | 24 / 50 | H (20,83); P (8,33); L (33,33) | Alta (1); Media (21); Baja (8) | |
| Bosque denso | 1.6686111 N -76.571388 W | 1830 | 19 / 11 | 2 / 10,52 | L (10,52) | Media (1); Baja (1) | |
| La Cocha | Bosque fragmentado | 1.6661111 N-76.566111 W | 1719 | 20 / 14 | 2 / 10 | H (5); P (5) | Alta (1); Baja (1) |
| Pastos arbolados | 1.6783333 N-76.567222 W | 1642 | 12 / 9 | 1 / 8,33 | P (8,33) | Baja (1) |
Nota. H: Haemoproteus, P: Plasmodium, L: Leucocytozoon.
Fuente: autores.
Las coberturas seleccionadas se caracterizaron por distintos niveles de densidad y estructura de la vegetación. El bosque denso se caracterizó por una comunidad vegetal dominada por árboles de más de 10 metros de altura, con un dosel cerrado y una cobertura arbórea superior al 70% del área total, con alta densidad de epífitas y correspondía a áreas sin intervención antrópica. El bosque fragmentado estuvo compuesto por árboles de más de 10 metros de altura, pero con un dosel más abierto, donde la cobertura arbórea osciló entre el 30% y el 70% del área, y correspondían a bosques sometidos ocasionalmente a entresacas de especies forestales. Finalmente, los pastos arbolados correspondían a áreas dominadas por gramíneas, con presencia dispersa de árboles de más de cinco metros de altura, cuya cobertura arbórea osciló entre el 30% y el 50% del área total, y en las que se llevaban a cabo actividades de pastoreo para ganado (Figura 2).

Fuente: Betancourt-Hernández R. del P.
Figura 2 Coberturas vegetales seleccionadas en este estudio. a) Bosque denso; b) Bosque fragmentado; c) Pastos arbolados. Departamento del Cauca, suroccidente de Colombia.
Se realizaron tres salidas de campo entre los años 2019 y 2020: a) agosto-septiembre, b) noviembre y c) enero-febrero de 2020. Cada uno de los puntos seleccionados fue muestreado un día por salida para un total de nueve puntos de muestreo y días efectivos de trabajo en campo.
Trabajo de campo
Para el muestreo de las aves se emplearon 20 redes de niebla de 12 m x 2,5 m y ojo de malla de 16 mm, que se mantuvieron activas entre las 06:00 y 11:00 h en cada punto de muestreo, en cada una de las coberturas vegetales. Las aves capturadas fueron anilladas (anillos de material Darvic con un código numérico único) e identificadas hasta especie usando la guía de campo de la avifauna colombiana (Ayerbe-Quiñones, 2018). A cada individuo se le tomó una muestra de sangre entre 5 y 30 μl, mediante punción de la vena braquial o yugular (en el caso de los colibríes), con una aguja hipodérmica estéril (#27) y un tubo capilar heparinizado (Gallina y López, 2015), y se realizó de uno a tres extendidos de sangre que se secaron al aire libre. Después de tomar la muestra de sangre, los individuos fueron liberados lo más rápido posible, en el lugar de la captura.
Trabajo de laboratorio
Los extendidos de sangre se fijaron con metanol absoluto por cinco minutos y se tiñeron con Giemsa al 10% durante 20 minutos; pasado este tiempo, se retiró el exceso de colorante y se secaron a temperatura ambiente en el laboratorio. Una vez realizada la tinción, se procedió a examinar con un microscopio de luz, Nikon Eclipse E100, primero con un objetivo de bajo aumento (10x) por todo el extendido, con el fin de observar si la muestra presentaba infección por Leucocytozoon u otro tipo de parásitos de mayor tamaño como microfilaria o Trypanosoma, y luego se realizó una revisión con un objetivo de mayor aumento (100x) con aceite de inmersión, cubriendo la totalidad del extendido donde las células formaron una sola capa. La determinación taxonómica de los parásitos sanguíneos se realizó hasta género, subgénero o grupo de especies cuando fue posible, siguiendo las claves de Valkiūnas (2005) y Valkiūnas e Iezhova (2018, 2022) y la confirmación de la doctora Angie Daniela González de la Universidad Nacional de Colombia.
Análisis de datos
La frecuencia de infección se estimó como el número de individuos muestreados que están infectados por el hemoparásito y se calculó a partir de la siguiente fórmula: Prevalencia = (número de hospederos infectados / número total de hospederos) x 100 (Gallina y López, 2015). La parasitemia se cuantificó para cada extendido de sangre basándose en 100 campos aleatorios en aumento total de 1.000x, donde las células formaron una sola capa de aproximadamente 100 eritrocitos/campo = 10.000 eritrocitos totales, en los que se registró el número de células infectadas. La parasitemia se clasificó como baja, media o alta de acuerdo con Hauptmanová (2006); en el caso de infección por Haemoproteus y Plasmodium se clasificó como baja < 0,1% de las células infectadas; media = 0,1 - 0,5% y alta > 0,5%, mientras que la infección por Leucocytozoon y Trypanosoma se clasificó como baja < 0,02%, media = 0,02 - 0,1% y alta > 0,1%. La parasitemia por microfilaria se clasificó teniendo en cuenta el número total de microfilarias en el extendido, así: baja (1-10 microfilarias por placa), media (11-20 microfilarias por placa) y alta (> 20 microfilarias por placa) (Haas et al., 2011).
Para evaluar el efecto del tipo de cobertura, altitud y familia taxonómica de las aves (variables independientes) sobre la frecuencia de infección y la parasitemia (variables respuesta), se ajustaron Modelos Lineales Generalizados (GLM) con distribución binomial. En primer lugar, se construyó un modelo general para cada variable respuesta, y posteriormente se desarrollaron modelos específicos para cada uno de los géneros de parásitos. Para los modelos generales y los específicos, se plantearon seis combinaciones diferentes, que incluyeron efectos aditivos e interacciones entre las variables independientes. La ausencia de sobredispersión fue evaluada y confirmada en todos los modelos, y la selección de modelos se basó en el Criterio de Información de Akaike (AIC), el Criterio de Información Bayesiano (BIC) y la razón de verosimilitud. Posteriormente se aplicó la prueba post Anova de Tukey con corrección por tasa de falsos descubrimientos (FDR, siglas en inglés). Para los análisis se utilizaron los paquetes “lme4”, “MASS”, “car”, “DHARMa” en RStudio (R Core Team, 2008).
Resultados
Frecuencia de infección por hemoparásitos
Se logró obtener muestra sanguínea de 274 individuos, de los cuales se identificaron hemoparásitos en 64 individuos. Las infecciones por hemosporidios se registraron en 61 individuos, distribuidos en 19 especies de aves, y la frecuencia general de infección fue del 22,2%. El género de parásito con mayor prevalencia fue Leucocytozoon (10,9%), seguido de Haemoproteus (8,7%) y Plasmodium (6,9%). Además, se encontraron otros parásitos diferentes a Haemosporida como microfilarias 1,09% (3 ind.) (Figura 3z, aa) y Trypanosoma de 0,3% (1 ind.) (Figura 3ab). Las aves infectadas por microfilaria y Trypanosoma no presentaron coinfección por otros hemoparásitos.
No se encontraron hemosporidios en los órdenes Apodiformes, Coraciiformes, Cuculiformes, Piciformes y Trogoniformes. Sin embargo, sí se encontraron microfilarias en dos especies que pertenecen a los órdenes Piciformes (Aulacorhynchus albivitta) y Cuculiformes (Momotus aequatorialis).
Se detectó coinfección en 10 individuos, de los cuales siete presentaron coinfección por Haemoproteus/Leucocytozoon, un individuo presentó coinfección por Plasmodium/Leucocytozoon y dos individuos presentaron coinfección de los tres géneros (Tabla 2).
Las familias de aves con mayor frecuencia de infección general fueron Thraupidae 71,1% (36/52 ind.), seguido de Turdidae 34,7% (8/23 ind.), y las que presentaron menor frecuencia de infección fueron Cotingidae 33,3% (2/6 ind.), Fringillidae 11,7% (2/17 ind.) y Tyrannidae 2,5% (2/78 ind.). Además, la distribución de hemosporidios entre las familias se dio de manera diferencial, donde Thraupidae, Passerellidae y Parulidae presentaron infección por Leucocytozoon, Plasmodium y Haemoproteus; Turdidae presentó infección para Leucocytozoon y Plasmodium; Fringillidae presentó infección por Leucocytozoon y Haemoproteus, mientras que Cotingidae, Tyrannidae y Vireonidae presentaron infección únicamente por uno de los géneros (Figura 4).
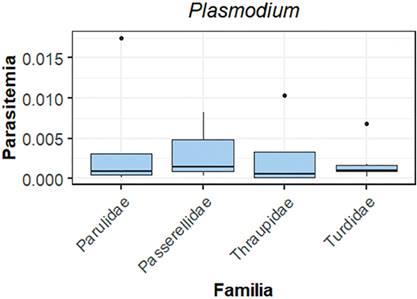
La mayoría de los individuos que presentaron infección por hemosporidios, tuvieron parasitemias medias y bajas (Tabla 2). Las especies de aves que presentaron las parasitemias más altas para Haemoproteus fueron Diglossa cyanea (3 ind.), Diglossa albilatera (1 ind.), Tangara xanthocephala (1 ind.) y Tangara nigroviridis (1 ind.), mientras que las aves que presentaron parasitemias altas para Plasmodium fueron Myadestes ralloides (1 ind.), Basileuterus tristriatus (1 ind.), Anisognathus somptuosus (1 ind.) y Arremon brunneinucha (1 ind.). Finalmente, para el género Leucocytozoon ningún individuo presentó parasitemias altas.
La poca representatividad de algunos estadios de desarrollo tempranos en los extendidos dificultó la identificación precisa de los hemoparásitos a nivel de especie. No obstante, con base en similitudes morfológicas descritas en la literatura, se considera que el grupo de especies descrito como Haemoproteus coatneyi podría estar infectando individuos de Anisognathus somptuosus, Tangara nigroviridis, Tangara labradorides, Tangara xanthocephala, Tangara parzudakii, Diglossa albilatera y Diglossa cyanea. Los gametocitos jóvenes se observaron adheridos al núcleo de los eritrocitos, creciendo en dirección a la membrana celular y, en muchos casos, desplazando el núcleo de la célula hospedera. El núcleo del parásito se ubicó con frecuencia en posición subterminal, y se observaron gametocitos con morfología característica en forma de mancuerna, lo cual coincide con descripciones previas del complejo H. coatneyi (Figura 3a-i).
Por otro lado, se identificaron hemoparásitos Plasmodium del subgénero Novyellaen individuos de Myadestes ralloides, Basileuterus tristriatus, Arremon brunneinucha y Anisognathus somptuosus, en los que se observó que los gametocitos presentaban forma elongada con pigmentos grandes, de forma ovalada y en su mayoría infectaron eritrocitos maduros; además, los trofozoítos usualmente presentaron formas redondeadas u ovaladas, sin excrecencias largas claramente definidas, ni glóbulos refractivos y se ubicaron en posición polar, sin tener contacto con el núcleo del eritrocito infectado y contenía un único gránulo de pigmento de forma circular. En el caso de los merozoitos, estos no superaron el tamaño del núcleo del eritrocitario y generalmente contenían entre 4 y 6 merontes (Figura 3j-p).
Finalmente, Leucocytozoon majoris podría estar infectando individuos de Anisognathus somptuosus, Tangara xanthocephala, Tangara vassorii, Tangara nigroviridis, Tangara parzudakii, Arremon brunneinucha y Myioborus miniatus, ya que los gametocitos observados se desarrollaron en células hospederas redondeadas, en las que el núcleo se encontraba desplazado hacia la periferia en forma de banda, la cual generalmente era del mismo ancho en toda su longitud y se extendía alrededor del gametocito abarcando más de la mitad de la circunferencia (Figura 3q-s). Asimismo, Leucocytozoon fringillinarum podría estar infectando individuos de las especies Tangara vassorii, Tangara nigroviridis, Tangara xanthocephala, Diglossa cyanea y Anisognathus somptuosus. Los gametocitos observados también se desarrollaron en células hospederas redondeadas, pero el núcleo de las células hospederas, desplazado por el gametocito, adoptó forma de capuchón y ocasionalmente se extendió hasta la mitad de la circunferencia del gametocito, a diferencia de L. majoris (Figura 3q-y).
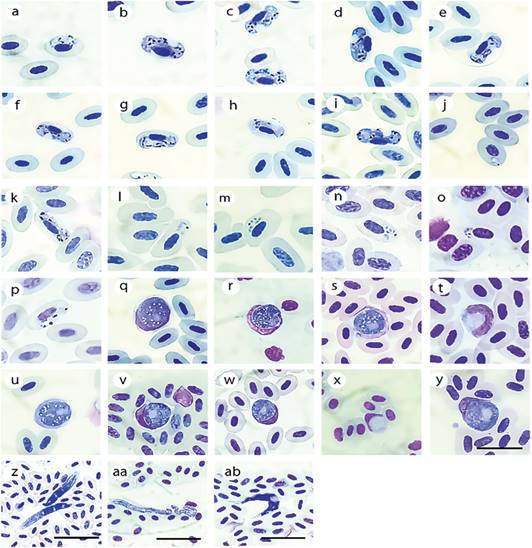
Fuente: Betancourt-Hernández R. del P.
Figura 3 Fotografías de hemoparásitos encontrados en aves del suroccidente de Colombia. a-i. Microgametocitos y macrogametocitos de Haemoproteus subgénero Para Haemoproteus, posiblemente del grupo de especies de Haemoproteus coatneyien diferentes hospederos (a-c Tangara nigroviridis; d: Tangara parzudakii; e-h: Anisognathus somptuosus; i: Tangara labradorides; j-p Plasmodium, subgénero Novyella en j-k: Arremon brunneinucha (trofozoíto y gametocito); l-m Anisognathus somptuosus (merozoítos); n-o Basileuterus tristriatus (merozoítos); p: Myadestes ralloides (gametocito): q-u gametocitos de Leucocytozoon, posiblemente Leucocytozoon majorois en q: Myioborus miniatus, r-t Anisognathus somptuosus; u: Tangara xanthocephala posiblemente Leucocytozoon fringillinarum en v: Tangara xanthocephala; w-x: Diglossa cyanea, y: Tangara vassorii; microfilaria (z-aa) en z: Aulacorhynchus albivitta y aa: Momotus aequatorialis, ab: Trypanosoma sp. en Pogonotriccus poecilotis. Línea horizontal: barra de escala para hemosporidios corresponde a 10 μm y para microfilaria y Trypanosoma corresponde a 20 μm.
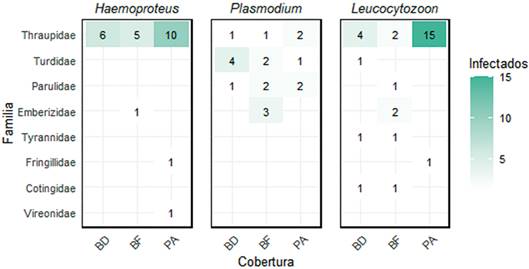
Fuente: autores.
Figura 4 Frecuencia de infección por hemosporidios según cobertura vegetal en cada una de las familias taxonómicas de aves del suroccidente de Colombia.
Tabla 2 Frecuencia de infección por hemoparásitos encontrados en aves del Cauca, suroccidente de Colombia. Orden filogenético propuesto por el Comité de Clasificación Suramericano de Ornitología (Remsen et al., 2024).
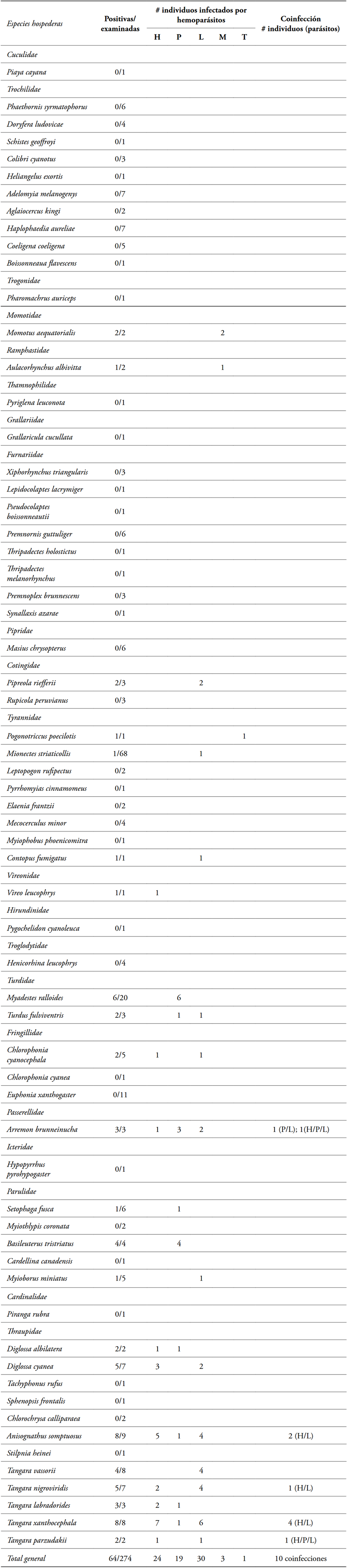
Nota. H: Haemoproteus, P: Plasmodium, L: Leucocytozoon, M: microfilaria, T: Trypanosoma.
Fuente: autores.
Frecuencia de infección y parasitemia según tipo de cobertura, altitud y familia
La altitud y el tipo de cobertura no mostraron un efecto significativo para la frecuencia de infección a nivel general, sin embargo, la familia sí tuvo un efecto significativo entre Fringillidae y Thraupidae (Media = 11,76 vs 71,15, respectivamente; Tukey test = -2.905; Z = -3,539; SE = 0,82; p = 0,030) y entre Parulidae y Tyrannidae (Media = 33,33 vs 2,56, respectivamente; Tukey test = 9,908; Z = 3,279; SE = 0,89; p = 0,049). La frecuencia de infección evaluada para cada uno de los géneros mostró que en Haemoproteus y Plasmodium la familia influye sobre la frecuencia de infección, pero en el caso de Leucocytozoon tanto la familia como la altitud tuvieron un efecto significativo en la frecuencia de infección (Tabla 3 y Figura 5). Para la parasitemia, la cobertura vegetal, la altitud y la familia tuvieron efectos significativos en Haemoproteus y Leucocytozoon (Tabla 3 y Figura 6). Este último presentó un efecto interactivo entre las variables altitud y cobertura (Figura 7). La parasitemia con Plasmodium se relacionó de manera significativa con la familia de ave (Figura 8).
Tabla 3 Resultados del Análisis de Varianza-ANOVA de los modelos GLM para evaluación de la frecuencia de infección y parasitemia de hemosporidios en aves, suroccidente de Colombia.
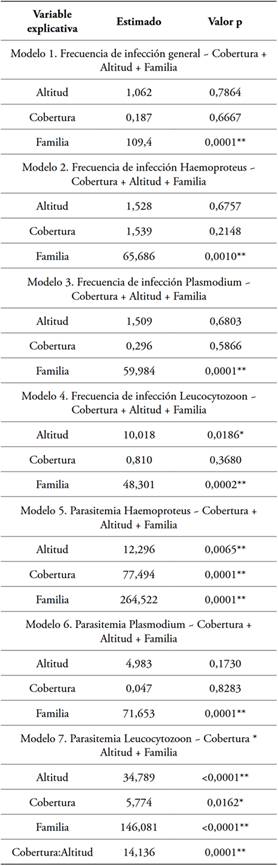
Nota. Valores de significancia: 0 ‘***’ 0.001 ‘**’ 0.01 ‘*’.
Fuente: autores.
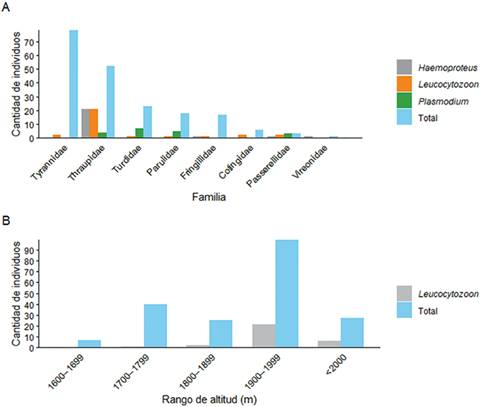
Fuente: autores.
Figura 5 Frecuencia de infección por Haemoproteus, Plasmodium y Leucocytozoon en relación con la familia taxonómica del hospedero (A) y la altitud (B), en el suroccidente de Colombia.
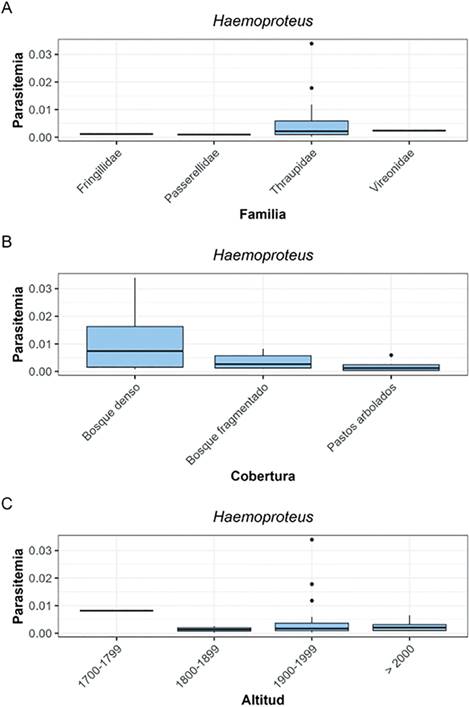
Fuente: autores.
Figura 6 Parasitemia de Haemoproteus según el tipo de cobertura vegetal, familia taxonómica del hospedero y altitud, en el suroccidente de Colombia.
Fuente: autores.
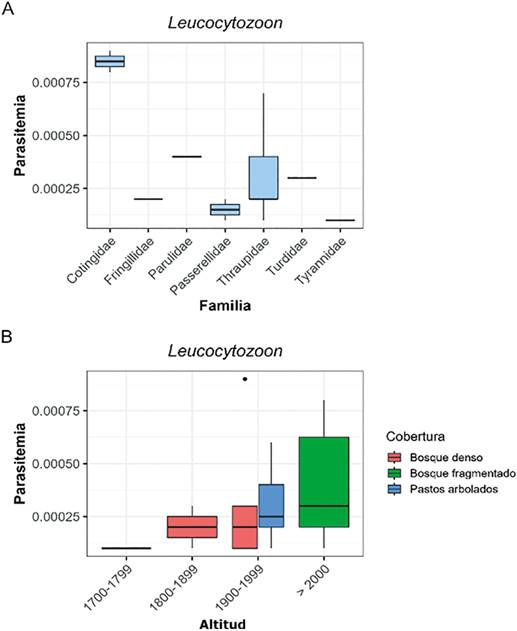
Figura 7 Parasitemia de Leucocytozoon según el tipo de cobertura vegetal, familia taxonómica del hospedero y altitud, en el suroccidente de Colombia. Parasitemia entre 1.700-1.799 m, corresponde al bosque fragmentado.
Discusión
La región andina neotropical es uno de los principales lugares de diversidad de aves en el mundo, albergando numerosas especies con distribución restringida o en categorías de amenaza preocupantes (Vélez et al., 2021). A pesar del incremento de investigaciones ornitológicas en las últimas décadas, la distribución y dinámica de los hemosporidios en aves de esta región continúan siendo escasamente conocidas. En este contexto, el presente estudio representa la primera aproximación al análisis de hemosporidios en aves silvestres del municipio de Santa Rosa, Cauca, una de las zonas de mayor diversidad avifaunística de Colombia (Ayerbe-Quiñones et al., 2008).
La frecuencia general de infección encontrada para la zona de estudio (22,2%) es similar a la reportada por otras investigaciones realizadas en el país, pero en ecosistemas de mayor altitud, por ejemplo, en el PNN Chingaza, en ecosistemas de bosque altoandino y páramo a elevaciones superiores a 2.900 m (Lotta et al., 2015; Rodríguez et al., 2009); donde la frecuencia de infección general fue de 27,9% de 136 hospederos (Rodríguez et al., 2009). Sin embargo, se resalta la alta prevalencia encontrada para Leucocytozoon (10,9%) a elevaciones inferiores a 2.000 m como lo reportado en otras investigaciones realizadas en ecosistemas de alta montaña (González et al., 2015; Lotta et al., 2015).
Por otra parte, se encontró infección por microfilaria en dos especies de aves, para las cuales existen reportes previos en sus respectivas familias taxonómicas, Ramphastidae (Pteroglossus castanotis) y Momotidae (Momotus aequatorialis) en Villavicencio, Meta (Renjifo et al., 1952; Valkiūnas et al., 2003). La mayoría de estos parásitos se consideran no patógenos, debido a que causan poco daño al hospedero (Campbell y Ellis, 2007), mientras que Pogonotriccus poecilotis fue la única especie (con un individuo) que presentó infección por Trypanosoma (0,3%). En Colombia, la infección con Trypanosoma y microfilarias se ha relacionado negativamente con la elevación (González et al., 2015); posiblemente, esto se deba a la distribución de los vectores que transmiten estos hemoparásitos, dentro de los que se han descrito mosquitos de las familias Simuliidae, Culicidae y Ceratopogonidae; los mismos vectores de Leucocytozoon, Plasmodium y Haemoproteus (Atkinson et al., 2008),por lo que se requieren estudios enfocados en los vectores de estos parásitos (Matta y Rodríguez, 2001).
En la presente investigación, no se reporta la presencia de hemoparásitos en colibríes, lo cual podría estar relacionado con el tipo de técnica empleada para su detección, teniendo en cuenta que las pruebas moleculares son más sensibles que la microscopía de luz (Valkiūnas et al., 2014), como lo reportan Moens et al. (2016) y Harrigan et al. (2014) en Ecuador, quienes utilizando simultáneamente microscopía de luz y técnicas moleculares evidenciaron altas frecuencias de infección por Haemoproteus en algunas especies de colibríes; sin embargo, en Colombia, González et al. (2014) reportan infecciones de 3% (9/289) en colibríes, así mismo, se describió la especie Leucocytozoon quynzae que infectó a cuatro individuos de diferentes especies de colibrí (Heliangelus amethysticollis, Coeligena helianthea, Opisthoprora euryptera y Metallura tyrianthina), muestreados en la zona de amortiguamiento del PNN Chingaza (Matta et al., 2014b).
La prevalencia de hemosporidios se ha relacionado positivamente con la abundancia de los vectores (Bukauskaitė et al., 2019; Fecchio et al., 2017) y posiblemente esto explique las diferencias encontradas, de manera que probablemente hay más vectores de la familia Simuliidae y Ceratopoginidae, transmisores de Leucocytozoon y Haemoproteus, que mosquitos de la familia Culicidae, vectores de Plasmodium. Además, las infecciones por Haemoproteus y Leucocytozoon también se han asociado con aspectos filogenéticos y ecológicos de las aves, como el agrupamiento en bandadas mixtas, debido a que al estar agrupados intensifican las emisiones de CO2 facilitando la localización por parte de los vectores (De Angeli et al., 2023; Fecchio et al., 2013; González et al., 2014). Así mismo, otros factores como la edad del hospedero, el tipo de nido en forma de taza, y la altura en la que se encuentra el nido, se han relacionado con una mayor prevalencia de hemosporidios (Fecchio et al., 2022; Gao et al., 2024), debido a una mayor exposición de las aves a la picadura de los vectores, que además son más abundantes en el sotobosque y el dosel (Barrow et al., 2019; Fecchio et al., 2011). Lo anterior concuerda con los resultados obtenidos, ya que las especies de aves que presentaron infección por Plasmodium y Haemoproteus construyen nidos en forma de taza y, en el caso de Thraupidae, tienden a formar agrupaciones en bandadas mixtas con el fin de optimizar la búsqueda de alimento y disminuir el riesgo de depredación (Powell, 1985).
Las diferencias significativas que se presentaron en la prevalencia de Leucocytozoon en los pastos arbolados en comparación con las otras dos coberturas, se debe a la cantidad de individuos de la familia Thraupidae capturados en este tipo de cobertura, ya que esto se relacionó con la alta oferta de recurso alimenticio durante la época de muestreo, donde se detectó mayor abundancia de especies como Anisognathus somptuosus, Tangara nigroviridis, Tangara vassorii, Tangara xanthocephala y Diglossa cyanea. Esta situación se considera un factor que puede sesgar las conclusiones, es decir, que no se puede afirmar categóricamente que existe una diferencia real entre la prevalencia y parasitemia originada por el tipo de cobertura. Además, el parásito Leucocytozoon no fue exclusivo de pastos arbolados, lo que indica que el tipo de cobertura no es factor limitante para la transmisión de este hemoparásito. De acuerdo con algunos investigadores, las características ecológicas y filogenéticas de la especie hospedera se asocian más con la prevalencia de hemosporidios que con las condiciones del hábitat, ya que la prevalencia de hemosporidios varía entre especies de aves que comparten el mismo hábitat (De Angeli, 2024; Sebaio et al., 2010), sin embargo, cambios en las frecuencias de infección también se han relacionado con la calidad del hábitat, por ejemplo, Ferreira et al. (2017) reportaron frecuencias de infección mayores en aves asociadas a pastizal en comparación con aves de estados sucesionales tempranos y tardíos en un bosque tropical de Brasil.
Teniendo en cuenta que la mayoría de las parasitemias encontradas en las aves infectadas fueron medias y bajas, se considera que las infecciones son crónicas, ya que los parásitos pueden permanecer en el torrente sanguíneo y en los órganos infectados mucho tiempo después de la fase inicial aguda, incluso de por vida (Hammers et al., 2016; Valkiūnas, 2005), no obstante, cambios fisiológicos asociados a actividades físicas exigentes como la migración y reproducción, pueden dar lugar a que se presenten aumentos en las parasitemias, debido a que estas actividades tienen un impacto negativo en la respuesta inmunitaria del hospedero (Dunn et al., 2011; Pulgarín-R. et al., 2018).
Finalmente, los resultados sugieren que la infección por hemosporidios depende más de las características de la especie hospedera que del tipo de cobertura vegetal. Esto podría explicarse por la alta conectividad entre los relictos de bosque en la zona de estudio, la cual facilita la movilidad de vectores y hospederos entre diferentes tipos de cobertura. Esta dinámica se refleja en la distribución relativamente homogénea de los hemosporidios en los tipos de cobertura evaluados, con excepción de la familia Thraupidae, cuya alta frecuencia de infección influyó notablemente en las diferencias observadas.
No obstante, es importante considerar que este estudio no evaluó la relación con otros factores clave en la transmisión de hemoparásitos, como la identidad de los vectores implicados o la proximidad a cuerpos de agua, los cuales desempeñan un papel fundamental en las interacciones parásito-vector-hospedero. Sin embargo, se cuenta con muestras de sangre en líquido, para desarrollar futuras investigaciones que integren herramientas moleculares en la identificación precisa de los hemosporidios detectados. Por último, se enfatiza en la necesidad de realizar más estudios sobre hemosporidios en regiones con alta diversidad ecosistémica y ornitológica, como Santa Rosa, Cauca, con el fin de profundizar en el conocimiento sobre hospederos potenciales, dinámicas de transmisión y redes de interacción ecológica.