Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.12 no.2 Bogotá Apr./June 2008
1 Grupo de Micología Médica Experimental, Corporación para Investigaciones Biológicas (CIB), Medellín, Colombia.
2 Escuela de Ciencias de la Salud, Maestría en Ciencias Médicas, programa de Microbiología, niversidad Pontificia Bolivariana (UPB), Medellín, Colombia.
3 Grupo de Microbiología Molecular, Escuela de Microbiología, Universidad de Antioquia, Medellín, Colombia.
Fecha recibido: 27/01/2008; fecha aceptación: 06/06/2008
Resumen
La melanina es uno de los pigmentos más comunes y de mayor distribución en la naturaleza. Es responsable de la coloración de plantas y animales; se encuentra en los ojos, el cabello, la piel, el plumaje, la cáscara de los huevos, la cutícula de los insectos, la tinta de los cefalópodos y en la pared y el citoplasma de muchos microorganismos. En los humanos este pigmento se ha encontrado también fuera de la piel, en las neuronas de la sustancia nigra y en los hepatocitos.Entre los microorganismos que se han reportado como productores de melanina tenemos Vibrio cholerae, Mycobacterium leprae, Bacillus thurigiensis, Pseudomonas aeruginosa, Schistosoma mansoni, Fasciola gigantita Trichuris suis, Alternaria alternata, Aspergillus niger, Blastomyces dermatitidis, Candida albicans, Cladosporium carionii, Coccidioides immitis, Cryptococcus neoformans, Exophiala (Wangiella) dermatitidis, Fonsecaea pedrosoi, Histoplasma capsulatum, Paracoccidioides brasiliensis, Penicillium marneffei, Pneumocystis carinii (jirovecii), Scedosporium prolificans, Scytalidium dimidiatum y Sporothrix schenckii; esto sin tener en cuenta los hongos dematiáceos, entre muchos otros.
Esta revisión pretende hacer un compendio de las más recientes publicaciones sobre melanina relacionadas principalmente con su función, su importante contribución a la supervivencia en el ambiente y durante la infección, como factor de virulencia en diversos microorganismos, principalmente en hongos patógenos, y su papel como agente inmunomodulador, así como la reducida susceptibilidad que confiere contra muchos de los antimicóticos usados en la actualidad.
Palabras clave: melanina, factor de virulencia, respuesta inmune, complemento, fagocitosis, estrés oxidativo, apoptosis, citocinas, anticuerpos, antimicrobianos.
Abstract Melanin is one of the common pigments in nature; it is responsible for pigmentation in plants and animals. It is found in skin, eyes, feathers, egg shell, hair, insect cuticle, cuttlefish ink and wall and/or cytoplasm from many microorganisms. Melanin in humans is also present in substantia nigra and hepatocytes.
Some microorganisms that have been reported producing melanin are: Vibrio cholerae, Mycobacterium leprae, Bacillus thurigiensis, Pseudomonas aeruginosa, Schistosoma mansoni, Fasciola gigantita, Trichuris suis, Alternaria alternata, Aspergillus niger, Blastomyces dermatitidis, Candida albicans, Cladosporium carionii, Coccidioides immitis, Cryptococcus neoformans, Exophiala (Wangiella) dermatitidis, Fonsecaea pedrosoi, Histoplasma capsulatum, Paracoccidioides brasiliensis, Penicillium marneffei, Pneumocystis carinii (jirovecii), Scedosporium prolificans, Scytalidium dimidiatum, Sporothrix schenckii, and most of the dematiaceous fungi.
This review is focused on recent international publications concerning melanin analysing its capacity to survive in nature and during infection inside the host and its evasion of the immune response. Melanin acts as an inmunomodulador particle and it is known that its presence in many of microorganisms could protect them from microbicidal agents presently used.
Key words: melanin, virulence factors, immune response, complement, phagocitoses, oxidative stress, apoptosis, cytokines, antibodies,antifungals.
Introducción
Hasta el momento han sido muchas las características que se le ha conferido a la melanina. Se sabe que protege las bacterias como Vibrio cholerae el choque térmico hiperosmolar en los estuarios, generando así bacterias resistentes estos cambios ambientales (1-3). En otras especies, la producción de este pigmento es usado en la taxonomía del género, como es el caso de Streptomyces(4), Entre los parásitos más estudiados para melanina y las enzimas que la sintetizan, encontramos Fasciola gigantita (5), Isoparorchis hypselobagri (6), Trichuris suis (7) y Trichuris muris (8). En relación con los hongos, se han estudiado tanto en aquellos patógenos de importancia para el humano, como en otros de tipo ambiental y de interés biotecnológico, en los cuales se ha encontrado que las melaninas son importantes para la supervivencia y la longevidad de las propágulas micóticas (9-11).
La melanina también funciona como sistema de evasión de los mecanismos inmunológicos del huésped. Se sabe que la melanina de la uva tiene propiedades inmunomoduladoras, principalmente en la disminución de las citocinas de tipo proinflamatorias (12,13).Otras observaciones sugieren que la melanina contribuye a la virulencia de los agentes micóticos, protegiéndolos de la respuesta de defensa del huésped, pueden activar la cascada del complemento (14), protegerlos frente a agentes oxidantes (15-17), reducir la fagocitosis o la inducción de la muerte celular (15,18-20), inducir una fuerte respuesta de anticuerpos (21,22)y generar disminución en la absorción de ciertos medicamentos en los tejidos del huésped, representada por la resistencia o la disminución de la sensibilidad a los compuestos antimicrobianos, como son la anfotericina B y la caspofungina (23-25).
El estudio de estas propiedades de la melanina no sólo se ha llevado a cabo in vitro o con cepas mutantes, sino también con modelos animales en ratones;así,se sabe que los ratones son susceptibles a un amplio rango de infecciones microbianas como los humanos. Esto ha hecho de ellos un buen modelo para generar infecciones que simulen lo que ocurre en los humanos (26); a pesar de las muchas diferencias entre ambos (27), el sistema inmune del ratón y el del humano son muy similares y ambos están formados por los componentes: la respuesta innata, la cual actúan mediatamente contra los microorganismos, y la respuesta adaptativa, a cual genera memoria inmunológica (28).
Definición de melanina
La melanina no es una sustancia única: se la considera como un amplio grupo de sustancias (pigmentos)que tienen propiedades similares (29,30). La melanina es un pigmento ubicuo distribuido en todos los reinos biológicos. En general, se ha descrito como un pigmento oscuro, negro o café; sin embargo, puede presentar otros colores. Son moléculas con alto peso molecular, muy estables, amorfas, cargadas negativamente, resistentes a la degradación con ácidos pero susceptibles a la degradación con bases fuertes, hidrofóbicas, insolubles en agua o solventes orgánicos, las cuales son formadas por la polimerización oxidativa de compuesto fenólicos o indólicos. Las melaninas derivadas de levodopa (3,4-dihidroxi-L-fenilalanina) (L-DOPA) son llamadas feumelaninas y característicamente son negras o café; las melaninas amarillas o rojizas son llamadas feomelaninas e incorporan cisteína on L-DOPA; las iomelaninas son tras melaninas de color café, están formadas por compuestos del ácido homogentísico a partir de tirosinasas; y las melaninas de dihidroxinaftaleno (alomelanina) son pigmentos derivados a partir de acetatos por la vía de la polikétido sintasa y, generalmente, on de color negro o café (11,31-33) (figura 1).
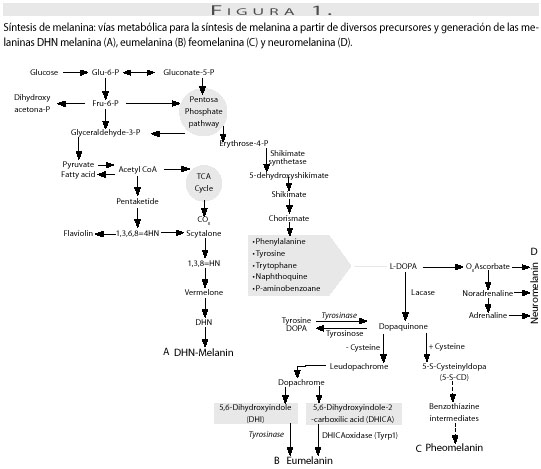
Hasta el momento no hay métodos que permitan establecer una identificación confiable de las unidades monoméricas o del polímero total de la melanina. Aunque la estructura de las melaninas es desconocida por la incapacidad que existe de estudiarlas por cristalografía, existen algunos métodos, como la resonancia electrónica que ofrece características que establecen si un compuesto tiene electrones no pareados, lo que generalmente significa que puede ser un radical libre lo cual implica una molécula orgánica o, por el contrario, que tiene iones metálicos de transición, los que reconocerían una molécula inorgánica compleja (34); o como la identificación de algunos intermediarios con el uso de la cromatografía líquida de alta presión (HPLC) (31,35,36).
Así mismo, el uso de anticuerpos monoclonales es también un mecanismo por el cual puede reconocerse, de modo indirecto y preliminar, la existencia de melanina en una determinada muestra, debido a que este compuesto posee una estructura y posibles factores determinantes antigénicos bastante conservados, por lo cual se presentan reacciones cruzadas entre los anticuerpos monoclonales contra melaninas de diferentes microorganismos (37-39).
Importancia de las melaninas en la naturaleza
La melanización es un proceso encontrado en casi todos los dominios de la naturaleza (arquea, bacteria y eucaria) (40, 41), aunque los reportes hasta el presente se han centrado en los dominios bacteria y eucaria; en este último es donde encontramos los hongos, los animales y las plantas.
En las plantas la melanina es de tipo DNH-melanina y hace parte de los metabolitos secundarios; una gran variedad de funciones se han asociado con la melanina; puede servir como transmisora de energía, unir medicamentos y químicos, y afectar la integridad celular (42). Las melaninas también son usadas como camuflaje y para manifestaciones sexuales. La tinta de Sepia officinalis es una suspensión de partículas de melanina que ha mostrado tener actividad antiviral in vitro, contra el virus de la inmunodeficiencia humana (43) y puede inhibir la formación de sincitios o efectos citopáticos producidos por los virus (44). Los insectos generan una respuesta inmune contra la melanina expresada por los microorganismos invasores (45). En general, la melanina ha sido involucrada en muchos procesos fisiológicos, fisiopatológicos y patogénicos (11,30). En la actualidad se ha reportado la producción de melanina por muchos microorganismos, tanto ambientales como patógenos para plantas y animales.
En los mamíferos, la melanina es producida por los melanocitos y se localiza en vacuolas especializadas denominadas melanosomas; los melanocitos producen principalmente DOPA-melaninas (eumelanina y feomelanina) (46). La coloración del cabello y la melanina en la piel brindan protección contra la luz solar y en cierto grado de resistencia a melanomas en radiaciones terapéuticas (47); sin embargo, el papel de la melanina sigue siendo desconocido en otros casos, por ejemplo, en la sustancia nigra del cerebro humano (48,49) (figura 1).
Melanina en plantas
Los pigmentos de origen vegetal, desde rojos y cafés hasta negros, generalmente se producen por sustancias no nitrogenadas. Estas sustancias en las plantas se denominan alomelaninas o melaninas DHN, por su precursor el dihidroxinaftaleno. Hasta la fecha, las melaninas de las plantas no han sido ampliamente estudiadas. Sin embargo, se conoce que Sarothamnus scoparius (retama) es una de las plantas con mayor contenido de melanógenos; de las legumbres y frutas es posible aislar tirosina, DOPA, tiramina, dopamina y epinefrina (N-metildopamina), el color ennegrecido de los tubérculos (papas), las frutas (manzanas, etc.) y en plantas como Vicia faba (habas)se encuentra alta gran cantidad de DOPA, siendo éste un proceso de melanogénesis de tirosinasa o DOPA. En todas las plantas las polifenoloxidasas son muy comunes, pero no siempre terminan en la formación de melanina; por ejemplo, el proceso de maduración del banano está relacionado con la dopamina. Aunque la melanina se localiza en un solo tejido de la planta, las enzimas que participan en su síntesis están distribuidas en varias partes de la planta (50, 51).
Las melaninas extraídas de semillas y hojas, así como los flavonoides extraídos de pétalos y semillas de plantas (50) o los pigmentos purificados de plantas comerciales, presentan actividad anti-tumoral en sistemas in vitro 52).
Las melaninas son pigmentos oscuros que protegen los organismos contra el estrés ambiental; así mismo, algunos fitopatógenos requieren de la melanización en los apresorios para invadir los tejidos del huésped. En muchos hongos, fitopatógenos como Gaeumannomyces graminis var. tritici, el agente etiológico de la enfermedad devastadora de las raíces de los cereales (devastating root disease of cereals), requieren de la producción de melanina para causar enfermedad (53). Muchos de estos estudios muestran que la melanina puede jugar un papel crucial en la virulencia de los patógenos para las plantas, en la penetración (54, 55).
Melanina en mamíferos
La melanina está presente en todos los animales y varía en sus colores desde el amarillo hasta el negro. En contraste con los microorganismos, en los animales la melanina está localizada en vacuolas especializadas denominadas melanosomas. En los mamíferos y las aves está localizada o emigra a los pelos y a las plumas, y en los anfibios y reptiles se localiza en los melanóforos de las células de la piel en la parte superior de la dermis. Sin embargo, hay algunos pigmentos que los animales no pueden sintetizar y los toman directamente de su alimentación de plantas, como son los carotenoides y las xantinas, los cuales son acumulados en los lipóforos. Gracias a todos estos pigmentos los animales pueden camuflarse, mimetizarse, usarlos para las manifestaciones sexuales y apareamiento. También ocurren cambios de color con la edad; en general, cuando los animales son más viejos presentan colores más oscuros o, incluso, llegan a perder el color, como es el caso del encanecimiento en los humanos.
En humanos, la melanina se encuentra en la piel, el cabello, el recubrimiento de la retina, la médula y la zona reticular de la suprarrenal, el oído interno, la substantia nigra y la mancha azul del cerebro o locus ceruleus; esta última se denomina neuromelanina y también se ha encontrado en primates y carnívoros, como los gatos y perros (56). La neuromelanina se produce químicamente por oxidación de las catecolaminas dopamina y norepinefrina (figura 1). Los cambios en el metabolismo o la acumulación de la melanina (57)pueden llevar al origen de enfermedades, como en el caso de la pérdida de color en el núcleo del cerebro que se observa en ciertas enfermedades neurodegenerativas, como en el mal de Parkinson, en el cual existe una disminución de neuromelanina en la substantia nigra, como consecuencia de una disminución específica de neuronas dopaminérgicas (58-60).
El albinismo ocurre en los animales que carecen de melanina y se debe a una mutación genética en la cual está bloqueada la ruta metabólica de la fenilalanina en su paso de DOPA hacia melanina (61); las personas o animales con esta deficiencia suelen tener poca visión. La conexión entre el albinismo y la sordera ha sido siempre conocida, pero poco comprendida, aunque desde 1859 en el "Tratado del origen de las especies", escrito por Charles Darwin, se apunta que "los gatos que son blancos y tienen ojos azules, generalmente, son sordos"(62).
Así mismo, la melanina de muchos animales se usa de diversas formas; tal es el caso de la tinta de Sepia officinalis, de tono rojizo-marrón que, una vez preparada, es usada por dibujantes y pintores artísticos, aunque su uso se reduce a artistas especializados. El ámbar gris es extraído de sepias, pulpos y calamares, y su principal uso comercial ha sido la elaboración de perfumes, aunque también se ha usado como saborizante y en medicina homeopática. No obstante, la melanina ha mostrado tener actividad antiviral in vitro, contra el virus de la inmunodeficiencia humana (43), y puede inhibir la formación de sincitios o efectos citopáticos producidos por los virus (44). También se conoce que los insectos generan una respuesta inmune contra la melanina generada por los microorganismos invasores (45).
Síntesis de melanina en microorganismos
Síntesis de melanina en bacterias
Entre las bacterias, la producción de melanina se ha descrito en muchos géneros, incluyendo Aeromonas (63-65), Alteromonas sp.(66), Bacillus (67), Legionella (68), Mycobacterium (66 70), Proteus (71,72), Pseudomonas (73-77), Streptomyces (78-80) y Vibrio (1, 81) (tabla 1).
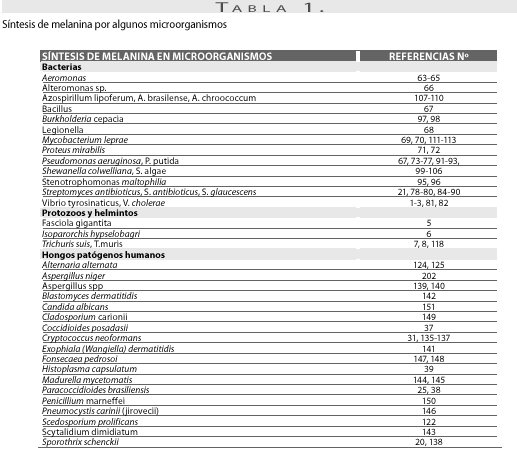
En los Vibrios, la producción de melanina ha sido descrita en Vibrio tyrosinaticus y Vibrio cholerae (1), en los que colonias hipertoxigénicas producían copiosa cantidad de un pigmento oscuro difusible mientras que colonias nativas no producían dicho pigmento (81). La producción de melanina es inducida en respuesta al estrés, particularmente al cambio hiperosmótico y a elevadas temperatura, y se asocia a su capacidad de sobrevivir en estuarios durante el verano (1-3, 82); la producción de feomelanina en mutantes de Vibrio las hace sustancialmente más virulentas que las cepas parentales no melánicas (3, 83).
Diversas especies de Streptomyces producen melanina y la producción de este pigmento es usado en la taxonomía del género (4), en particular, la producción de melanina está comprobada para Streptomyces antibioticus (21,84-86) y Streptomyces glaucescens (87,88); la producción de la casa por Streptomyces galbus es inducida a 42 C°, lo cual sugiere que la formación de melanina es una respuesta a las condiciones adversas del medio ambiente (89,90).
Pseudomonas aeruginosa produce un pigmento café descrito en 1897 como una melanina (piomelanina) sintetizada a partir de la tirosina (75, 91). Asimismo, ya ha sido bien caracterizada la estructura primaria de la enzima responsable de la síntesis de melanina en P. aeruginosa, la cual es una 4-di- hidroxifenilpiruvato dehidrogenasa (92). La melanización de P. aeruginosa es de relevancia clínica, como lo demuestra un estudio de 712 aislamientos clínicos, de los cuales, 16 de ellos eran melanogénicos (93); en otros estudios se ha encontrado que cepas melanogénicas de P. aeruginosa tienen gran actividad de lecitinasa y neuroaminidasa,lo cual aumenta su patogenicidad al invadir los tejidos del huésped con mayor facilidad (94). Además, P. aeruginosa y especies relacionadas como P. putida parecen tener lacasas, una de las principales enzimas en la vía metabólica de la melanina (67).
En otras especies patógenas para los humanos, como Stenotrophomonas maltophilia, la melanina es sintetizada intracelularmente en forma constitutiva por tirosinasas (95, 96).
Proteus mirabilis (71) Burkholderia cepacia (97,98), bacterias de importancia clínica, producen melanina. En P. mirabilis (71) actúa eliminando radicales libres (scavenger) y en Burkholderia cepacia protege el microorganismo del anión superóxido (98); asi mismo, ha sido propuesta como factor de colonización y transmisión, de ahí su importancia (98).
Shewanella colwelliana cataliza la piomelanina utilizando ácido homogentísico (99-103). Las melaninas han sido caracterizadas como compuestos capaces de captar o aceptar electrones (104), como en el caso de la bacteria marina Shewanella algae, microorganismo en el cual la melanina es usada como bomba para electrones solubles de hierro y, también, como aceptor de electrones terminales (105, 106).
Azospirillum lipoferum, una bacteria asociada con las raíces de los pastos, aumenta su actividad de la casa durante el crecimiento a extremas bajas concentraciones de oxígeno; la activación de la la casa ocurre por una vía de dos pasos (107) y es posible que las quinonas intermediarias producidas antes de la formación de la melanina sean el medio de A. lipoferum para respirar en condiciones anaerobias (108). Azospirillum brasilense produce un pigmento café tipo melanina durante el enquistamiento (109) y Azospirillum chroococcum sintetiza melanina a partir de catecolaminas (110).
Se ha reportado la identificación de lacasas bacterianas en 14 especies diferentes mediante una búsqueda en bancos de proteínas y usando como blanco una lacasa micótica previamente identificada y clasificada (67). Entre las bacterias identificadas se encontraron muchos patógenos humanos como Escherichia coli, Pseudomonas spp., Yersinia pestis, Campylobacter jejuni, Bordetella pertussis y Mycobacterium spp. (67).
Dicha búsqueda no identificó Mycobacterium leprae entre las posibles bacterias que pudieran tener lacasa; sin embargo, ésta ha sido la única micobacteria a la cual se le ha atribuido la capacidad de oxidar una variedad de difenoles en quinonas (70, 111) y también en DOPA, lo cual ha facilitado la identificación rápida de estos organismos en el laboratorio (112). Por otro lado, se sabe que M. leprae tiene una tirosinasa (O-difenoloxidasa) y que esta enzima puede ser inhibida directamente, lo que se refleja en la supresión de la multiplicación bacteriana en modelos experimentales (ratón), lo cual indica que la producción de esta enzima es la llave en una vía metabólica para el crecimiento de la micobacteria; además, derivados de DOPA o la misma DOPA son metabolizados efectivamente in vitro por la micobacteria, lo cual sugiere que este factor, sumado a otros, podría generar gérmenes más capaces de sobrevivir en el hospedero y esta DOPA así metabolizada podría ser esencial para la proliferación de la micobacteria (113).
En la ultima década se ha intensificado el interés por el estudio de las lacasas bacterianas como potenciales elementos en la explotación biotecnológica (114, 115), ya que éstas sirven en la decoloración de los efluentes resultantes del proceso de tintura; principalmente en la industria de papel y textil, se ha usado la enzima purificada o el microorganismo completo, debido a que la producción y purificación de estas lacasas resulta ser un proceso mucho más económico que la purificación de lacasas provenientes de organismos eucarióticos (116).
Síntesis de melanina en protozoos y helmintos
La actividad de las enzimas lacasa y tirosinasa también se ha descrito en muchos parásitos patógenos. Fasciola gigantita tiene una tirosinasa unida a su membrana como una lacasa en forma soluble; la inhibición de estas enzimas por cloruro de mercurio o yoduro de potasio indica la presencia de grupos tiol y tirosil (5). En Isoparorchis hypselobagri se encontró actividad de polifenol oxidasas, la cual parece estar asociada con la formación de los huevos del parásito (6). En Trichuris, la presencia de la enzima fenol oxidasa tiene la capacidad de convertir la DOPA en dopacromo, tanto en Trichuris suis (7) como en Trichuris muris (8, 118) (tabla 1).
Síntesis de la melanina en hongos
Las melaninas han sido consideradas como el escudo de los hongos (32) por su capacidad de proteger el microorganismo contra un amplio rango de agresiones tóxicas, tanto de tipo ambiental como producto de la respuesta inmune del huésped durante la infección. Por tal motivo, se ha considerado que las melaninas tienen un papel importante en la virulencia de muchos microorganismos (36).
La mayoría de los hongos contienen melanina y la producción de este pigmento puede proteger el organismo de diversas agresiones ambientales. La importancia de la melanina en los hongos como un producto metabólico es señalada por el hecho de que los hongos melánicos ofrecen una gran cantidad de este producto (119). Por ejemplo, la melanina aporta, aproximadamente, 30% del peso seco de las esporas de Agaricus bisporus (120, 121); si este componente representa una parte considerable del hongo, así como las fuentes de energía que debe haber usado para sintetizarla, podría suponerse que las melaninas en los hongos tienen una función predominante (120).
La mayoría de hongos patógenos para humanos son organismos ambientales y pueden incluir hongos melánicos que actualmente incrementan su importancia clínica (122, 123).
La melanina se ha estudiado tanto en aquellos patógenos de importancia para el humano como un otros de tipo melánicos que actualmente incrementan su importancia clínica (122,123).
La melanina se ha estudiado tanto en aquellos patógenos de importancia para el humano como en otros de tipo ambiental y de interés biotecnológico, como son: Alternaria alternata (124,125), Trametes versicolor (126-128), Podospora anserine (129), Rhizoctonia solani (130), Agaricus bisporus (131), Pleurotus ostreatus (132) y Gauemannomyces graminis var. tritici (133, 134). Entre los hongos patogénos en los cuales se ha reportado la presencia de melanina, encontramos Cryptococcus neoformans (31,135-137), Histoplasma capsulatum (39), Sporothrix schenckii (20, 138), Aspergillus spp. (139, 140), Paracoccidioides brasiliensis (22 38), Exophiala (Wangiella) dermatitidis (141), Blastomyces dermatitidis (142), Scedosporium prolificans (122), Scytalidium dimidiatum (143), Coccidioides posadasii 37), Madurella mycetomatis (144,145), Pneumocystis carinii (jirovecii) (146), Fonsecaea pedrosoi (147, 148), Cladosporium carrionii (149), Penicillium marneffei (150) y Candida albicans (151) (tabla 1).
En esta revisión veremos cómo la presencia de la melanina en estos microorganismos puede actuar como un factor de virulencia, facilitarles la evasión a la respuesta inmune del huésped o, incluso, influenciar la resistencia a algunos antimicrobianos de uso frecuente.
Melanina como factor de virulencia
Es claro que la melanina hace parte del arsenal de factores de virulencia que los microorganismos poseen para defenderse de las agresiones cuando están en contacto con un huésped extraño diferente a su medio ambiente. Este tema ya ha sido revisado ampliamente por algunos autores (31,32,120,152), además de los muchos trabajos con mutantes para melanina o las enzimas que participan en su síntesis (20, 153-156). Sin embargo, también se ha dicho que las melaninas pueden proteger contra las agresiones del ambiente y del huésped, y que pueden actuar como componente antigénico y modular la respuesta inmune del hospedero; así mismo, pueden bloquear algunos de los mecanismo inmunes que el huésped utiliza para superar la agresión de estos microorganismos. Teniendo en cuenta que en casi todos los microorganismos está presente la melanina, veremos cómo este componente está interactuado con el sistema inmune.
Protección contra cambios en la osmolaridad, la temperatura y la desecación
Vibrio cholerae sintetiza melanina en respuesta a condiciones fisiológicas de estrés (hiperosmótico) unido con elevada temperatura (más de 30º C). Sin embargo, la cantidad de toxina detectada disminuyó en respuesta al estrés en condiciones de cultivo; por lo tanto, es posible que la melanogénesis sea una función específica de supervivencia de la bacteria en los estuarios durante las épocas de verano (1-3,83).
Las melaninas han mostrado proteger, no sólo contra el calor sino también contra el frío, a C. neoformans, manteniendo su integridad. Por tanto, esta protección podría estar implicada en la estabilidad térmica de muchos de los hongos (157). En M. fruticola también se ha observado protección contra la desecación (158-161).
Aunque las bases para este tipo de protección no están totalmente entendidas, es posible que las melaninas atrapen radicales del oxígeno que son liberados de sus membranas con el calentamiento o explicarse por la estrecha relación que existe entre la pared celular y la melanina (30).
Protección contra la luz ultravioleta
Las melaninas tipo DOPA absorben todo el espectro visible y el ultravioleta (162). La confirmación directa de las melaninas como escudos contra la luz ultravioleta se obtuvo de la experiencia humana que está llena de detalles y experiencias históricas que indican que la melanina DOPA de la piel humana protege contra la luz solar (163, 164).
En relación con la protección que ejerce la melanina contra la luz ultravioleta, en las bacterias es poco lo que se ha estudiado. Sin embargo, los estudios realizados con V. cholerae muestran que la capacidad de sintetizar melanina está asociada con la supervivencia en los estuarios, a altas temperaturas y a la radiación solar directa (1-3,82). A mutantes de B. thuringiensis capaces de producir melanina, les confiere resistencia a luz ultravioleta y a los plaguicidas (165).Bacillus subtillis. es una bacteria formadora de esporas que produce un pigmento café alrededor de la endospora (166). Este pigmento de las esporas les confiere resistencia contra la luz ultravioleta y el peróxido de hidrógeno; por lo tanto, las cepas pigmentadas son mucho más resistentes que aquéllas que no lo son (167,168).
Los cuerpos micóticos melánicos son más prevalentes en los hongos aéreos y en los que viven en las rocas (169,170). Las melaninas producidas por Cladospirium sp. y Oidiodendron sp. protegen contra la luz ultravioleta y la radiación gamma, e incluso, contra la irradiación solar artificial y la desecación (161,171).
Las conidias mutantes albinas de Monilinia fructicola fueron mucho más susceptibles a la luz ultravioleta que las conidias nativas (160).
Cepas melánicas y albinas de S. schenckii fueron sometidas a diferentes niveles y tiempos de radiación, y se encontró que las cepas melánicas son más resistentes a este tratamiento (20). De forma similar, las células melánicas de C. neoformans fueron menos susceptibles a los efectos de la luz ultravioleta cuando se compararon con las células no melánicas, lo cual indica que estos hongos patógenos están protegidos de la radiación ionizante (172). El grado de resistencia a la radiación es asociada con la cantidad de melanina que se produce (173,174).La protección contra la luz ultravioleta,la solar o la radiación gamma también se ha demostrado en Phaeococcomyces sp. (120), E. dermatitidis (175), A. alternata (176, 77) Cladosporium sp. (178, 179).
Existe una indicación más inquietante de los efectos protectores de las melaninas en los microorganismos contra la radiación en los estudios realizados en los pacientes (obreros expuestos a la radiación)y en los suelos de los alrededores del reactor nuclear de Chernobyl (180,181). La microflora del sitio del reactor provee una de las más fuertes asociaciones entre la melanogénesis de los hongos y su capacidad para sobrevivir en ambientes extremos, así como la producción de infección en humanos por cepas de microorganismos que generaron melanina (177, 182), hongos filamentosos como Alternaria alternata the reactor strains)parecen estar genéticamente adaptados a altas dosis de radiación y una de las características de estas cepas es la producción de melanina (177). En los lavados broncoalveolares y esputos de pacientes (obreros expuestos a la radiación) con patología crónica pulmonar, se encontraron muestras con hongos (Aspergillus niger, Aspergillus fumigatus, Aspergillus flavus, Penicillium sp. y Candida albicans) y melaninas extraídas de sus conidias. Estos autores proponen una hipótesis: "el polvo radiactivo y los micromicetos mutantes fueron inhalados por las personas durante su trabajo en el reactor; por lo tanto, esto generó una pérdida de la respuesta inmune en las personas y una infección por hongos mutantes resistentes " (182,183). Finalmente, y de hecho, las melaninas han sido usadas comercialmente en cremas de protección solar, o sus enzimas e intermediarios para incrementar la producción de melanina.
Relación: melanina Vs. sistema inmune
Los hongos han desarrollado estrategias de inhibición selectiva del estallido respiratorio, a través de la producción de quelantes específicos, como catalasas, manitol y melanina, contra los oxidantes mortales producidos por los macrófagos (30).
Las melaninas son moléculas inmunológicamente activas (12, 13); además, la melanina incrementa ligeramente la carga negativa de las células, como es el caso de C. neoformans (19), lo cual afecta su interacción con las células del huésped (184, 85).
Complemento
Se sabe también que la melanina puede activar la cascada del complemento (14,186). Es claro que la fagocitosis por opsonización contribuye a la eliminación de muchas conidias inhaladas, como es el caso de A. fumigatus, el cual es un proceso facilitado por la deposición del complemento en la superficie de las conidias. Sin embargo, las mutantes de A. fumigatus para arp1, gen que codifica para una enzima en la vía de la melanina DHN, eran de un color más claro que las nativas y exhibían un incremento significativo en su capacidad de unir complemento (C3), en comparación con las conidias de la cepa nativa (186). De forma similar, la melanina de C.neoformans puede activar la vía alterna del complemento e inducir una respuesta inflamatoria (14), incluso, las eumelaninas humanas tienen el potencial de activar complemento in vivo. Por tanto, esta capacidad podría dilucidar cómo las melaninas pueden contribuir a la patogénesis de muchas enfermedades autoinmunes en humanos y alteraciones degenerativas, al igual que tener un importante papel en la virulencia de algunos microorganismos (14,152).
Sin embargo, da Silva et al.(2006) encontraron que las levaduras melánicas de P. brasiliensis fueron pobremente fagocitadas, un en presencia de complemento (25) (tabla 2).
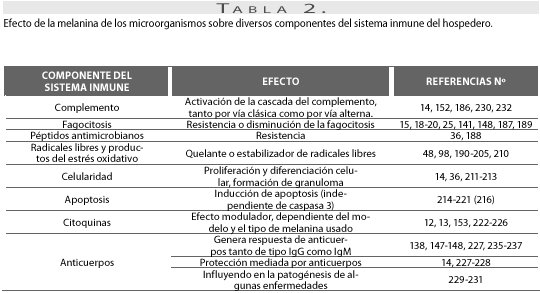
Fagocitosis
Se ha visto que las células melánicas son más resistentes a la fagocitosis en comparación con células no melánicas o mutantes para melanina. Esto se ha demostrado en C. neoformans 15,8,9), S. schenckii (20), Exophiala (Wangiella) dermatitidis (141), P. brasiliensis (25) y F. pedrosoi (148). Aunque la fagocitosis de E. dermatitidis por neutrófilos no fue afectada por la presencia o ausencia de melanina, las celulas melánicas estuvieron significativamente más protegidas contra la muerte (141, 87).
Además de las especies reactivas del oxígeno, las células fagocíticas pueden producir defensinas y otros péptidos antimicrobianos a los cuales las células melánicas de C. neoformans son menos susceptibles (188); el mecanismo de acción en este caso parece ser la absorción de los péptidos microbicidas que les impide alcanzar su blanco de acción (36).
En humanos, se ha visto que un incremento de la expresión de melanina en el epitelio pigmentado de la retina disminuye la fagocitosis de los ROS (rod outer segment)(189). Se considera que los mecanismos por los cuales la melanización puede disminuir la fagocitosis son la alteración del potencial Z de membrana,la reducción de eventos de fotoisomerización, la disminución de concentraciones subretinales de Ca+ y la reducción del consumo de oxígeno (189) (tabla 2).
Protección contra oxidantes, adicales libre y estrés oxidativo
Otro de los mecanismos es el de la protección que ejerce la melanina frente a agentes oxidantes; las melaninas tienen una fuerte afinidad por los metales, son quelantes con mucha afinidad por los radicales libres; además de sus propiedades de transferencia de electrones (190), estabilizan radicales libres en sistemas biológicos y atrapan electrones no apareados evitando su potencial dañino (191). Por resonancia paramagnética de electrones se encontró que las melaninas aumentan su señal cuando están en presencia de iones superóxido; es así como la transferencia de electrones libres del superóxido son estabilizados por la melanina (192, 193). Las melaninas unen muchos metales de transición. La utilidad de esta unión se ha interpreto de varias formas, como disminución de la concentración de metales libres en el caso de metales tóxicos o la creación de depósitos adyacentes en la célula en el caso de metales esenciales (194). Así, pues, se sabe que la melanina de C. neoformans está involucrada en la reducción de Fe(III) a Fe(II); estos datos soportan un modelo fisiológico de redox en las melaninas micóticas, por lo cual los electrones exportados por la levadura a formar Fe(II) mantienen la capacidad de reducción del tampón redox extracelular (195, 196).
La función como antioxidante de la melanina de C. neoformans puede ser particularmente importante a 37 °C, temperatura a la cual la actividad de la superóxido dismutasa es reducida (197). También se ha descrito una relación recíproca entre la cantidad de melanina celular y la actividad de superóxido dismutasa, en ranas (198); de manera similar, la melanina de B. cepacia protege el microorganismo contra el anión superóxido (98).
Células melánicas de C. neoformans mostraron ser menos susceptibles a la muerte por hipoclorito y permanganato (199); de igual forma sucede con las células de E. dermatitidis y A. alternata 200).
Por otro lado, las células melánicas de C. neoformans demostraron ser más resistentes a los radicales del nitrógeno y del oxígeno,a diferencia de las células no melánicas o las mutantes albinas (15,17).Estas observaciones también han estado presentes en trabajos realizados con otros hongos, como A. niger (201, 202), E. dermatitidis (141, 200), S. schenckii (20), A. fumigatus (140, 203), Azospirillum choococcum (110), Azobacter salinestris 110,204) Pycularia orizae (Magnaportha grisea)(205).
Otros experimentos han mostrado que la preincubación de macrófagos de ratón J774 con el ácido 5,6-dihidroxiindol-2 -carboxílico (DHICA), precursor de la melanina, resultó en un incremento de los niveles de óxido nítrico producido después de la estimulación con lipopolisacáridos; este efec- to es suprimido con inhibidores de la óxido nítrico sintasa inducible (NOS2). Estos resultados, que antes no eran reconocidos para DHICA como un mensajero que media la interacción entre melanocitos y macrófagos, podrían estar cumpliendo un papel importante en la respuesta inmune inflamatoria epidérmica (206).
En relación con las melaninas humanas,se ha indicado que el óxido nítrico (ON) inducido por la radiación ultravioleta estimula la melanogénesis en los queratinocitos, disminuyendo su crecimiento, incrementando las cantidades de tirosinasa y de proteína 1 relacionada con la tirosinasa (tyrosinase-related protein 1) y aumentando la generación de formas dendríticas de las células; por lo tanto, parece ser que el óxido nítrico juega un papel importante como mediador paracrino de la melanogénesis inducida por luz ultravioleta (207).
En la enfermedad de Parkinson se propone que la capacidad de la neuromelanina de quelar metales puede llevar a la sobrecarga de ésta con hierro y otros metales en las neuronas, disparando una respuesta inflamatoria por la posible producción de radicales libres y agravando el proceso patogénico degenerativo en esta enfermedad (48, 208, 209).
Sobre la etiología del melanoma y la degeneración macular se han propuesto muchas hipótesis que implican las melaninas en el papel de redox alterado, en el cual el equilibrio antioxidante y pro-oxidante de la melanina está perdido, lo cual resulta en un fenotipo alterado. Por lo tanto, se sugiere que una disminución en el grado de polimerización o peso molecular del polímero de melanina puede causar una alteración en el estatus redox, que lo lleva a un estado de pro-oxidación por la fuga de moléculas monoméricas fuera de las organelas, causando citotoxicidad y necrosis (210) (tabla 2).
Celularidad
Sin importar el origen de la melanina, ésta tiene efecto sobre la proliferación y diferenciación de queratinocitos y fibroblastos humanos in vitro, donde el efecto sobre los fibroblastos es más uniforme que sobre los queratinocitos. Sin embargo, la melanina sepia tuvo un efecto significativo sobre el estímulo en la proliferación de queratinocitos, mientras que la melanina sintética inhibió la proliferación de queratinocitos y fibroblastos humanos (211-213).
En relación con las melaninas micóticas, se ha observado que las partículas de melanina aisladas de C. neoformans e inyectadas en la cavidad peritoneal de ratones resultaron en la formación de granulomas en hígado, bazo y pulmón; la formación granulomatosa se dio alrededor de la partículas de melanina de forma muy parecida a las reacciones inflamatorias a cuerpo extraño (14). Estas observaciones sugieren que la melanina puede generar una vigorosa reacción inflamatoria, puesto que funciona como una sustancia extraña que no puede ser lisada por las enzimas del huésped. De hecho, muchas de las enfermedades micóticas están notoriamente asociadas con latencia y formación de granulomas y para muchos de estos agentes ya se ha descrito la presencia de melanina (36) (tabla 2).
Apoptosis
Hasta el momento los efectos que causa la melanina sobre la muerte celular sólo se han estudiado en modelos de enfermedad en humanos.
El proceso de fotosensibilización puede contribuir a las manifestaciones clínicas del cáncer de piel en humanos, el el cual los individuos pelirrojos o rubios son más susceptibles a las quemaduras por exposición a la luz solar y tienen un mayor riesgo de contraer cáncer de piel (aproximadamente, de 1,5 veces en los rubios y de 3 a 6 veces mayor en los pelirrojos), en comparación con controles caucásicos (214, 215). La feomelanina (presente en rubios o pelirrojos) contribuye tres veces más al daño celular por apoptosis que la eumelanina (presente en caucásicos), melanina irradiada, particularmente la feomelanina, fotosensibiliza queratinocitos a generar apoptosis independiente de la caspasa 3 y, por ende, la apoptosis inducida por la melanina puede contribuir al incremento de la sensibilidad de individuos albinos, blancos o pelirrojos a contraer cáncer de piel (216).
Las funciones de la neuromelanina en la patogénesis de la enfermedad de Parkinson hasta ahora se desconocen, al igual que su acumulación en el sistema nervioso; en estudios de espectroscopía se ha mostrado que la melaninadopamina sintética es idéntica al pigmento natural de la substancia nigra (217-219). Por consiguiente, los modelos in vitro que usan melanina-dopamina sintética y cultivos neuronales de rata o una línea celular (PC12) de feocromocitoma, mostraron que la fagocitosis de neuromelanina no es específica de neuronas dopaminérgicas y se puede encontrar en otro tipo de cultivos neuronales promoviendo neurodegeneración en la enfermedad de Parkinson (220, 221) (tabla 2).
Citocinas
El efecto de la melanina de los microorganismos sobre la modulación de las citocinas ha sido estudiada, principalmente en los modelos de C. neoformans, en los cuales, células deficientes de melanina (mutantes) fallaron en la producción de FNT-α por los macrófagos de ratón (153); tanto que, en un modelo de infección pulmonar en ratones que fueron inoculados tanto con células vivas completas no melánicas y melánicas de C. neoformans, como con la melanina purificada, este grupo presentó una mínima producción de citocinas y de inflamación en comparación con los animales infectados con las células vivas. Por lo tanto, se sugiere que estos fenómenos, presentados tanto en el reclutamiento celular como en la producción de citocinas, requieren de ambos componentes, la melanina y las células vivas (222).
Sin embargo, la gran mayoría de los datos encontrados sobre la modulación de las citocinas por la melanina están relacionados con su producción o su inhibición, en modelos in vitro con células humanas.
En estudios in vitro con melanina sintética a concentraciones no tóxicas, se suprime la producción de citocinas IL-1ß, IL-6,y FNT-α por monocitos humanos de sangre periférica, por la interferencia en los eventos postranscripcionales de éstas (13). Por otro lado, en estudios in vitro con líneas celulares humanas de queratinocitos, después de la estimulación con lipopolisacáridos o con luz ultravioleta, éstas son capaces de sintetizar y liberar FNT-a, el cual accede a la circulación; y, junto con otras citocinas derivadas de la epidermis, pueden mediar reacciones de inflamación local y sistémica por el huésped contra eventos perjudiciales causados por agentes microbianos o por radiación ultravioleta (223).
De igual manera, otros estudios in vitro han demostrado que las citocinas proinflamatorias disminuyen la melanización por efecto sobre la tirosina, y que la melanina de la piel, que protege contra la luz ultravioleta, produce una respuesta cutánea inflamatoria con participación de citocinas, incluyendo el FNT-α. Estos datos sugieren una doble vía de retroalimentación; mientras que la luz ultravioleta genera melanización, ésta a su vez induce la producción de citocinas proinflamatorias que deben estar regulando las células de esta zona de la piel (224-226) (tabla 2).
Por otro lado, se ha encontrado que la melanina de la uva, sintetizada por una tirosinasa, está provista de propiedades inmunomoduladoras, principalmente en la disminución de las citocinas de tipo pro inflamatorias. La administración de melanina de uva mostró un potente efecto inhibitorio en el modelo de la enfermedad inducida por adjuvante en ratas, suprimiendo significativamente la inflamación primaria y casi la totalidad de las lesiones artríticas secundarias. Las citocinas proinflamatorias en suero (IL-1β, IL-6 y FNT-α) fueron elevadas en ratas con enfermedad inducida por adjuvante, parámetros que fueron normalizados por la melanina; en contraste, la reducción de los niveles séricos de IL-2 no se afectó; la subpoblación Th1 (CD4+ o CD8+) de linfocitos es la principal responsable de este efecto inhibitorio y, por ende, la melanina puede llevar a una supresión del desarrollo de la enfermedad inducida por adjuvante en un modelo de inmunidad mediada por células (12, 13).
El efecto sobre las células T se muestra por la reducción de la respuesta mitogénica en el bazo y redujo los niveles séricos de IL-2 en ratas tratadas con melanina; además, la melanina en este modelo, no solo inhibió fuertemente la peroxidación de lípidos de membranas del microsoma del hígado de ratas in vitro, sino que también in vivo protegió contra la peoxidación hepática que ocurre en la enfermedad inducida por adjuvante; esto demuestra propiedades citoprotectoras y antioxidantes. En conclusión, la melanina de las uvas parece ser un producto natural interesante en la inmunomodulación y la respuesta inflamatoria, el cual parece tener múltiples blancos celulares dentro del sistema inmune (12, 3) (tabla 2).
Anticuerpos
La melanina actúa como un elemento inmune activo en la medida en que genera una respuesta efectiva de anticuerpos; la inyección de melanina purificada de C. neoformans en ratones resultó en una activa respuesta de anticuerpos (227); así mismo, los anticuerpos generados contra la melanina durante la infección pueden ser protectores (14,227,228), pero su asociación con la melanina es similar a lo que ocurre en enfermedades autoinmunes como el vitiligo, en la cual la respuesta de anticuerpos puede ser deletérea (229-231) (tabla 2).
El vitiligo es un desorden común de despigmentación de la piel, resultante de la destrucción de los melanocitos y casi siempre se asocia con la presencia de autoanticuerpos circulantes caracterizados como IgG, que activan el complemento por la vía clásica y que se unen a los melanocitos (230, 232). Sin embargo, muchos han sido los blancos encontrados como autoantígenos, puesto que el vitiligo puede asociarse a muchas enfermedades sistémicas, entre ellas la diabetes, la anemia, el hipotiroidismo, el hipertiroidismo, la enfermedad de Addison y la artritis reumatoide, entre muchas otras (233, 234).
En la actualidad, se reconoce que muchos de los hongos capaces de producir enfermedad en humanos tienen la capacidad de sintetizar melanina in vivo o in vitro, como se describió anteriormente, y que estas partículas son antigénicas por su capacidad de generar anticuerpos in vivo, como ha sido posible detectar niveles de anticuerpos antimelanina en modelos experimentales de enfermedades producidas por hongos (147, 236, 237).
En el modelo experimental con ratones, para la infección con C. neoformans se detectaron anticuerpos ti po IgM anti-melanina en el suero (227, 235); de igual manera, ratones infectados con P. marneffei también presentaron altos niveles de anticuerpos IgG anti-melanina en su suero (150). Estos hallazgos son similares a los presentes en los ratones infectados con conidias de P. brasiliensis, en los cuales se detectaron niveles altos de anticuerpos IgG anti-melanina, tanto en suero como en el lavado broncoalveolar (236).
De manera similar,se han podido detectar anticuerpos anti-melanina en sueros de pacientes enfermos de algunas de estas micosis; tal es el caso para la esporotricosis; los sueros de pacientes con esta entidad presentaron títulos de anticuerpos IgM anti-melanina (138); en casos de cromoblastomicosis y de infección por Fonsecaea pedrosoi, se presentaron títulos de anticuerpos IgG contra la melanina de este hongo (148). Se presentaron resultados similares en casos de paracoccidioidomicosis, cuyos títulos de anticuerpos anti-melanina presentes en el suero fueron de tipo IgG (237) (tabla 2).
Anticuerpos monoclonales anti-melanina
El uso de anticuerpos monoclonales es un mecanismo por el cual puede reconocerse, de modo indirecto y preliminar, la existencia de melanina en una determinada muestra, debido a que este compuesto posee una estructura y posibles factores determinantes antigénicos bastante conservados. Así mismo,l os anticuerpos monoclonales se han usado en el diagnóstico clínico o en el tratamiento del cáncer y otras enfermedades. En la actualidad se ha retornado a su estudio para el tratamiento de enfermedades infecciosas, considerando la teoría de la inmunidad mediada por anticuerpos.
Sin embargo, son muy pocos los anticuerpos monoclonales que se han reportado contra la melanina de estos hongos. En C. neoformans (235), este anticuerpo monoclonal ha servido para el estudio inicial de presencia de melanina en muchos otros hongos que hasta hoy se han estudiado (37-39, 142). Posteriormente, se generaron otros anticuerpos monoclonales como han sido los producidos contra la melanina de S. schenckii (138) y A. fumigatus (140). En el caso de P. brasiliensis , es la primera vez que se reporta la generación de anticuerpos monoclonales del isotipo IgG1 contra la melanina (238)(tabla 3), puesto que todos los anteriores anticuerpos monoclonales contra melanina de otros hongos han sido del isotipo IgM. En general, todos estos anticuerpos monoclonales, tanto los isotipo IgM como los IgG, reportados por nuestro grupo, tienen la capacidad de reconocer múltiples fuentes de melanina, a saber: melaninas comerciales (Sigma)sintética, Sepia officinalis, melaninas de conidias de A. fumigatus, S. schenckii, P. marneffei, A. niger y P. brasiliensis, y melaninas de levaduras de C. neoformans, C. albicans y P. brasiliensis (237, 238).

Sin embargo hasta el momento, el único de los anticuerpos monoclonales estudiado para la detección indirecta de melanina en otros hongos y su capacidad inmunomoduladora de la infección in vivo in vitro, ha sido el anticuerpo monoclonal 6D2 generado contra la melanina de C. neoformans (239), en el cual se encontró que el tratamiento con este anticuerpo monoclonal prolongaba la supervivencia de los animales y disminuía la carga micótica, lo cual siguiere que este anticuerpo estaría mediando un mecanismo de protección en este modelo.
Finalmente, los diferentes trabajos revisados sugieren la presencia de anticuerpos anti-melanina que pueden ser tanto de tipo IgG como IgM; en algunos casos, como en el modelo de C. neoformans, pueden proteger por un mecanismo de inmunidad mediada por anticuerpos o, de forma contraria, estos mismos anticuerpos anti-melanina pueden influenciar la patogénesis de otras enfermedades en su mayoría de tipo autoinmune, como es el caso del vitiligo (tabla 2).
Resistencia a los antimicrobianos
Por último, se ha visto que la presencia de melanina en muchos microorganismos genera mayor resistencia a los compuestos antimicrobianos y principalmente a los antimicóticos. El hecho de que, en general, los hongos dematiáceos presenten mayor resistencia a los antimicóticos disponibles condiciona que se haya suscitado un especial interés entre los otros hongos que sintetizan melaninas (240, 241). Se sabe que Scedosporium prolificans es uniformemente resistente a todos los antimicóticos de uso más común, como anfotericina B, fluocitosina, miconazol, ketoconazol, luconazol e itraconazol (242) (tabla 4).
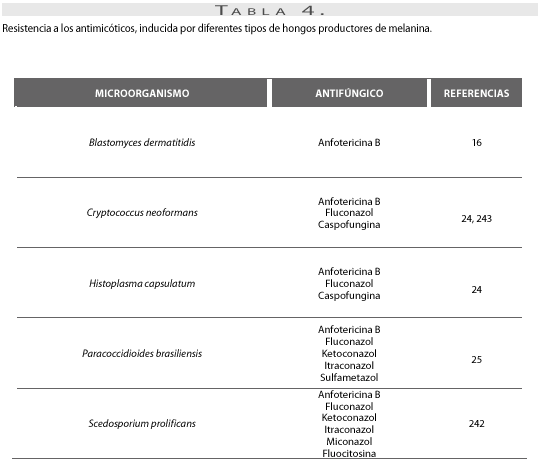
En la actualidad, se ha estudiado cuál es el papel de la melanina en este aspecto para muchos hongos, como es el caso de C. neoformans, el cual parece tener menor sensibilidad a la anfotericina B y a la caspofungina (24, 243); de igual manera, se ha observado para H. capsulatum (24). En P. brasiliensis se encontró que, en general, las células melánicas presentaban menor susceptibilidad que las células nativas (no melánicas) a antimicóticos como ketoconazol, fluconazol, itraconazol, sulfametazol y anfotericina B; esta última es el antimicótico menos efectivo sobre las células melánicas (25) (tabla 4).
Los autores ofrecen dos explicaciones para estos resultados: una, que la melanina disminuye la permeabilidad de la pared celular, o dos, que la melanina disminuye el daño de la membrana celular causado por los medicamentos. Sin embargo, no todos ellos parecen ser resistentes, como es el caso de E. dermatitidis en el que la presencia o ausencia de melanina no interfiere con la actividad antimicótica (244), aunque este tema aun no parece tener claridad (245).
Perspectivas
Finalmente, Eisenman y col.(2005) han propuesto un modelo de cómo la melanina presente en la pared de C. neoformans, uno de los hongos más estudiados en este aspecto, forma una especie de malla que puede presentar dos tipo de poros, unos pequeños que permitirían el paso de moléculas hasta del tamaño de los anticuerpos y otros que serían inaccesibles para moléculas de este tamaño o mayores. Se propone que a través de ella sólo podrían pasar pequeñas moléculas de nutrientes como azúcares o aminoácidos, y que la unión de los anticuerpos a la melanina puede prevenir el paso de nutrientes al bloquear estos espacios. Por lo tanto, los medicamentos antimicóticos, casi todas ellos de gran tamaño, no podrían ingresar entre los espacios de los gránulos de melanina (246).
Todas estas propiedades de la melanina se han propuesto para explicar su efecto patogénico, incluyendo su unión intima con la pared celular como un escudo contra enzimas hidrolíticas, el secuestro de proteínas de defensa del hospedero, el tampón redox, el atrapamiento de singletes de electrones, la dismutación del ion superóxido, la penetración en la pared celular de las plantas y la potencia inmunomoduladora durante la infección.De hecho, muchas de las enfermedades producidas por hongos están asociadas a formación de granulomas y latencia; la defensa contra los oxidantes derivados el hospedero y la resistencia a muchos de los actúales antimicóticos, entre otras, son la características hacen de la melanina uno de los componentes más interesante para su estudio, al determinar su controversial papel en la virulencia de muchos microorganismos, incluso en la patogénesis de la enfermedad en humanos; tal es es el caso en la enfermedad de Parkinson, el cáncer de piel y el vitiligo, en los cuales su papel aún está por dilucidar.
Conflicto de intereses
Los autores no tienen ningún conflicto de intereses que declarar.
Financiación y agradecimientos
Esta revisión hace parte de la tesis de Maestría en Ciencias Médicas, programa de Microbiología de la Universidad Pontificia Bolivariana de la estudiante Martha E.Urán J., con financiación del Centro Integrado para el Desarrollo de la Investigación, CIDI-UPB, y el convenio CIB - Fundación Bancolombia. La Dra. Cano recibe financiación de la Universidad de Antioquia. También se tuvo la financiación de COLCIENCIAS, proyecto código No.1115-04-11823 y, del CIDI, proyecto radicado: 04-05/06-52.
Correspondencia: Martha Eugenia Urán: estudiante de maestría en Ciencias Médicas, Programa de Microbiología, UPB; Corporación para Investigaciones Biológicas (CIB), Carrera 72 A Nº 78 B 141, Apartado aéreo 7378, Medellín, Colombia.Teléfono: (574) 441 08 55, Fax: 574) 41 55 14, muran@cib.org.co, meuj@hotmail.com
Referencias
1.Coyne VE, al-Harthi L. Induction of melanin biosynthesis in Vibrio cholerae. Appl Environ Microbiol. 1992;58:2861-5. [ Links ]
2. Ivins BE, Holmes RK. Factors affecting phaeomelanin production by a melanin-producing (mel) mutant of Vibrio cholerae. Infect Immun. 1981;34:895-9 [ Links ]
3. Kotob SI, Coon SL, Quintero EJ, Weiner RM. Homogentisic acid is the primary precursor of melanin synthesis in Vibrio cholerae, a Hyphomonas strain, and Shewanella colwelliana. Appl Environ Microbiol.1995;61:1620-2. [ Links ]
4. Lindholm P, Kortemaa H, Kokkola M, Haahtela K, Salkinojasalonen M, Valkonen J. Streptomyces spp. isolated from potato scab lesions under Nordic conditions in Finland. Plant Dis. 1997;81:1317-22. [ Links ]
5. Nellaiappan K, Devasundari AF, Dhandayuthapani S. Properties of phenol oxidase in Fasciola gigantica. Parasitology. 1989;99:403-7. [ Links ]
6. Srivastava M, Gupta SP. Polyphenol oxidase and scleroprotein/melanin pigments of Isoparorchis hypselobagri. Z. Parasitenkd. 1978;55:55-8. [ Links ]
7. Fetterer RH, Hill DE. The occurrence of phenol oxidase activity in female Trichuris suis. J Parasitol. 1993;79:155-9. [ Links ]
8. Hill DE, Fetterer RH. The effect of disulfiram on egg shell formation in adult Trichuris muris. J Parasitol. 1997;83:938-42. [ Links ]
9. Durrell LW. The composition and structure of walls of dark fungus spores. Mycopathol Mycol Appl. 1964;23:337-45. [ Links ]
10. Sussman AS, Lingappa Y, Bernstein IA. Effect of light and media upon growth and melanin formation in Cladosporium mansoni. Mycopathol Mycol Appl. 1963;20:307-14. [ Links ]
11. Wheeler MH, Bell AA. Melanins and their importance in pathogenic fungi. Curr Top Med Mycol. 1988;2:338-87. [ Links ]
12. Avramidis N, Kourounakis A, Hadjipetrou L, Senchuk V. Anti-inflammatory and immunomodulating properties of grape melanin. Inhibitory effects on paw edema and adjuvant induced disease. Arzneimittelforschung. 1998;48(7):764-71. [ Links ]
13. Mohagheghpour N, Waleh N, Garger SJ, Dousman L, Grill LK, Tuse D. Synthetic melanin suppresses production of proinflammatory cytokines. Cell Immunol. 2000;199:25-36. [ Links ]
14. Rosas AL, MacGill RS, Nosanchuk JD, Kozel TR, Casadevall A. Activation of the alternative complement pathway by fungal melanins. Clin Diagn Lab Immunol. 2002;9:144-8. [ Links ]
15. Wang Y, Aisen P, Casadevall A. Cryptococcus neoformans melanin and virulence: mechanism of action. Infect Immun. 1995;63:3131-6. [ Links ]
16. Wang Y, Casadevall A. Growth of Cryptococcus neoformans in presence of L-dopa decreases its susceptibility to amphotericin B. Antimicrob Agents Chemother. 1994;38:2648-50. [ Links ]
17. Wang Y, Casadevall A. Susceptibility of melanized and nonmelanized Cryptococcus neoformans to nitrogen and oxygen-derived oxidants. Infect Immun. 1994;62:3004-7. [ Links ]
18. Kozel TR. Dissociation of a hydrophobic surface from phagocytosis of encapsulated and non-encapsulated Cryptococcus neoformans. Infect Immun. 1983;39:1214-9. [ Links ]
19. Nosanchuk JD, Casadevall A. Cellular charge of Cryptococcus neoformans: contributions from the capsular polysaccharide, melaanin, and monoclonal antibody binding. Infect Immun. 1997;65:1836-41. [ Links ]
20. Romero-Martínez R, Wheeler M, Guerrero-Plata A, Rico G, Torres-Guerrero H. Biosynthesis and functions of melanin in Sporothrix schenckii. Infect Immun. 2000;68:3696-703. [ Links ]
21. Katz E, Thompson CJ, Hopwood DA. Cloning and expression of the tyrosinase gene from Streptomyces antibioticus in Streptomyces lividans. en Microbiol. 1983;129:2703-14. [ Links ]
22. Rosas AL, Nosanchuk JD, Gómez BL, Edens WA, Henson JM, Casadevall A. Isolation and serological analyses of fungal melanins. J Immunol Methods. 2000;244:69-80. [ Links ]
23. Kohler S, Wheat LJ, Connolly P, Schnizlein-Bick C, Durkin M, Smedema M, et al. Comparison of the echinocandin caspofungin with amphotericin B for treatment of histoplasmosis following pulmonary challenge in a murine model. Antimicrob Agents Chemother. 2000;44:1850-4. [ Links ]
24. van Duin D, Casadevall A, Nosanchuk JD. Melanization of Cryptococcus neoformans and Histoplasma capsulatum reduces their susceptibilities to amphotericin B and caspofungin. Antimicrob Agents Chemother. 2002;46:3394-400. [ Links ]
25. da Silva MB, Marques AF, Nosanchuk JD, Casadevall A, Travassos LR, Taborda CP. Melanin in the dimorphic fungal pathogen Paracoccidioides brasiliensis: effects on phagocytosis, intracellular resistance and drug susceptibility. Microbes Infect. 2006;8:197-205. [ Links ]
26. Pradel E, Ewbank JJ. Genetic models in pathogenesis. Annu Rev Genet. 2004;38:3347-63. [ Links ]
27. Mestas J, Hughes CC. Of mice and not men: differences between mouse and human immunology. J Immunol. 2004;172:2731-8. [ Links ]
28. Buer J, Balling R. Mice, microbes and models of infection. Nat Rev Genet. 2003;4:195-205. [ Links ]
29. Butler MJ, Gardiner RB, Day AW. Fungal melanin detection by the use of copper sulfide-silver. Mycologia. 2005;97:312-9. [ Links ]
30. Jacobson ES. Pathogenic roles for fungal melanins. Clin Microbiol Rev. 2000;13:708-17. [ Links ]
31. Langfelder K, Streibel M, Jahn B, Haase G, Brakhage AA. Biosynthesis of fungal melanins and their importance for human pathogenic fungi. Fungal Genet Biol. 2003;38:143-58. [ Links ]
32. Gomez BL, Nosanchuk JD. Melanin and fungi. Curr Opin Infect Dis. 2003;16:91-6. [ Links ]
33. Polak A. Melanin as a virulence factor in pathogenic fungi. Mycoses. 1990;33:215-22 [ Links ]
34. Enochs WS, Nilges MJ, Swartz HM. Purified human neuromelanin, synthetic dopamine melanin as a potential model pigment, and the normal human substantia nigra: characterization by electron paramagnetic resonance spectroscopy. J Neurochem. 1993;61:68-79. [ Links ]
35. Wakamatsu K, Ito S. Advanced chemical methods in melanin determination. Pigment Cell Res. 2002;15:174-83. [ Links ]
36. Nosanchuk JD, Casadevall A. The contribution of melanin to microbial pathogenesis. Cell Microbiol. 2003;5:203-23. [ Links ]
37. Nosanchuk JD, Yu JJ, Hung CY, Casadevall A, Cole GT. Coccidioides posadasii produces melanin in vitro and during infection. Fungal Genet Biol. 2007;44:517-20. [ Links ]
38. Gómez BL, Nosanchuk JD, Diez S, Youngchim S, Aisen P, Cano LE, et al. Detection of melanin-like pigments in the dimorphic fungal pathogen Paracoccidioides brasiliensis in vitro and during infection. Infect Immun. 2001;69:5760-7. [ Links ]
39. Nosanchuk JD, Gómez BL, Youngchim S, Diez S, Aisen P, Zancope-Oliveira RM, et al. Histoplasma capsulatum synthesizes mela anin-like pigments in vitro and during mammalian infection. Infect Immun. 2002;70:5124-31. [ Links ]
40. Woese CR. Bacterial evolution. Microbiol Rev. 1987;51:221-71. [ Links ]
41. Woese CR, Kandler O, Wheelis ML. Towards a natural system of organisms: proposal for the domains Archaea, Bacteria, and Eucarya. Proc Natl Acad Sci USA. 1990;87:4576-9. [ Links ]
42. Hill HZ. The function of melanin or six blind people examine an elephant. Bioessays. 1992;14:49-56. [ Links ]
43. Montefiori DC, Zhou JY. Selective antiviral activity of synthetic soluble L-tyrosine and L-dopa melanins against human immunodeficiency virus in vitro. antiviral Res. 1991;15:11-25. [ Links ]
44. Sidibe S, Saal F, Rhodes-Feuillette A, Lagaye S, Pelicano L, Canivet M, et al . Effects of serotonin and melanin on in vitro HIV-1 infection. J Biol Regul Homeost Agents. 1996;10:19-24. [ Links ]
45. Richman A, Kafatos FC. Immunity to eukaryotic parasites in vector insects. Curr Opin Immunol. 1996;8:14-9. [ Links ]
46. Marks MS, Seabra MC. The melanosome: membrane dynamics in black and white. Nat Rev Mol Cell Biol. 2001;2:738-48. [ Links ]
47. Hill HZ. The photobiology of melanin. Photochem Photobiol. 1997;65:471. [ Links ]
48. Zecca L, Tampellini D, Gatti A, Crippa R, Eisner M, Sulzer D, et al . The neuromelanin of human substantia nigra and its interaction with metals. J Neural Transm. 2002;109:663-72. [ Links ]
49. Zecca L, Tampellini D, Gerlach M, Riederer P, Fariello RG, Sulzer D. Substantia nigra neuromelanin: structure, synthesis, and molecular behaviour. Mol Pathol. 2001;54:414-8. [ Links ]
50. Britton G. The biochemistry os natural pigments. Cambridge: Cambridge University Press; 1983. [ Links ]
51. Thomas M. Modern methods of plant analysis. Paech K, Tracey MV, editors. Berlin: Springen Ferlag; 1955. [ Links ]
52. Kamei H, Hashimoto Y, Koide T, Kojima T. Anti-tumor effect of plant pigments including those with polyphenol groups. 2nd International Electronic Conference on Synthetic Organic Chemistry (ECSOC-2). Basel, witzerland, 1998. http://ecsoc2.hcc.ru/ecsoc-2g.htm [ Links ]
53. Henson JM, Butler MJ, Day AW. The dark side of the mycelium: Melanins of phytopathogenic fungi. Annu Rev Phytopathol. 1999;37:447-71. [ Links ]
54. H.D.S. Control of fungal diseases by compounds acting as antipenetrants. Crop Protection. 1986;5:306-13. [ Links ]
55. Kubo Y, Suzuki K, Furusawa I, Yamamoto M. Melanin biosynthesis as a prerequisite for penetration by appresoria of Colledotrichum lagenarium: site of inhibition by melanin-inhibiting fungicides and their action on appresoria. Pesticide Biochem Physiol. 1985;23:47-55. [ Links ]
56. Barr FE. Melanin: the organizing molecule. Med Hypotheses. 1983;11:1-139. [ Links ]
57. Zecca L, Mecacci C, Seraglia R, Parati E. The chemical characterization of melanin contained in substantia nigra of human brain. Biochim Biophys Acta. 1992;1138:6-10. [ Links ]
58. Faucheux BA, Hauw JJ, Agid Y, Hirsch EC. The density of (125I)- transferrin binding sites on perikarya of melanized neurons of the substantia nigra is decreased in Parkinsons disease. Brain Res. 1997;749:170-4. [ Links ]
59. Hirsch E, Graybiel AM, Agid YA. Melanized dopaminergic neurons are differentially susceptible to degeneration in Parkinson s disease. Nature. 1988;33 345-8. [ Links ]
60. Zecca L, Fariello R, Riederer P, Sulzer D, Gatti A, Tampellini D. The absolute concentration of nigral neuromelanin, assayed by a new sensitive method, increases throughout the life and is dramatically decreased in Parkinson s disease. FEBS Lett. 2002;510:216-20. [ Links ]
61. Taylor WO. Prenatal diagnosis in albinism. Lancet. 1987;1:1307-8. [ Links ]
62. Darwin CR. The origin of species by means of natural selection, or the preservation of favoured races in the struggle for life. London: Ed. John Murray; 1859. [ Links ]
63. Aurstad K, Dahle HK. Fine structure of melanin-producing aeromonads. Acta Pathol Microbiol Scand (B) Microbiol Immunol. 1972;80:1884-90 [ Links ]
64. Aurstad K, Dahle K. The production and some properties of the brown pigment of Aeromonas liquefaciens. Acta Vet Scand. 1972;13:251-9. [ Links ]
65. Hamilton-Miller JM, Ogunnariwo J. An improvement in the technique for the presumptive identification of Aeromonas salmonicida. J Appl Bacteriol. 1975;38:67-9. [ Links ]
66. Sanchez-Amat A, Solano F.A pluripotent polyphenol oxidase from the melanogenic marine Alteromonas sp. shares catalytic capabilities of tyrosinases and laccases. Biochem Biophys Res Commun. 1997;240:787-92. [ Links ]
67. Alexandre G, Zhulin IB. Laccases are widespread in bacteria. Trends Biotechnol. 2000;18:41-2. [ Links ]
68. Chatfield CH, Cianciotto NP. The secreted pyomelanin pigment of Legionella pneumophila confers ferric reductase activity. Infect Immun. 2007;75:4062-70. [ Links ]
69. Cutler RR, Wilson P, Clarke FV. Evaluation of modified BACTEC method to study the activity of disinfectants against Mycobacterium tuberculosis. Tuber Lung Dis. 1995;76:254-60. [ Links ]
70. Prabhakaran K, Harris EB. A possible metabolic role for -diphenoloxidase in Mycobacterium leprae. Experientia. 1985;41:1571-2. [ Links ]
71. Agodi A, Stefani S, Corsaro C, Campanile F, Gribaldo S, Sichel G. Study of a melanic pigment of Proteus mirabilis. Res Microbiol. 1996;1147:167-74. [ Links ]
72. Tanaka T. The decomposition of L-tyrosine and its derivatives by Proteus vulgaris. 2. Production of p-hydroxyphenylacetic acid, p-hydroxybenzaldehyde and melanin from L-tyrosine. Bull Pharm Res Inst. 1965;59:1-10. [ Links ]
73. Barshtein LA, Tydelskai a IL, Rozhavin MA. Experimental study of the pathogenicity of melanin-forming strains of Pseudomonas aeruginosa . Mikrobiol Zh. 1983;45:44-8. [ Links ]
74. Mann S. Melanin-forming strains of Pseudomonas aeruginosa . Arch Mikrobiol. 1969;65:359-79. [ Links ]
75. Ogunnariwo J, Hamilton-Miller JM. Brown- and red-pigmented Pseudomonas aeruginosa: differentiation between melanin and pyorubrin. J Med Microbiol. 1975;8:199-203. [ Links ]
76. Rozhavin MA. Biological properties of melanin Pseudomonas aeruginosa. Zh Mikrobiol Epidemiol Immunobiol. 1983;:45-7. [ Links ]
77. Rozhavin MA, Tydelskaia IL. Melanin-forming cultures of Pseudomonas aeruginosa . Zh Mikrobiol Epidemiol Immunobiol. 1979;21-3. [ Links ]
78. Arai T, Mikami Y. Chromogenicity of Streptomyces. Appl Microbiol. 1972;23:44 6. [ Links ]
79. Baumann R, Hutter R, Hopwood DA. Genetic analysis a in a melanin producing streptomycete, Streptomyces glaucescens. J Gen Microbiol. 1974;81:463-74. [ Links ]
80. Zhang H, Yao F, Sun L. Cloning and characterization of thr melanine biosynthesis genes from Streptomyces lincolnensis 78-11. Wei Sheng Wu Xue Bao. 1998;38:261-8. [ Links ]
81. Ruzafa C, Sanchez-Amat A, Solano F. Characterization of the melanogenic system in Vibrio cholerae, ATCC 14035. Pigment Cell Res. 1995;8:11 52. [ Links ]
82. Mekalanos JJ, Rubin EJ, Waldor MK. Cholera: molecular basis for emergence and pathogenesis. FEMS Immunol Med Microbiol. 1997;18:241-8. [ Links ]
83. Ivins BE, Holmes RK. Isolation and characterization of melanin-producing (mel) mutants of Vibrio cholerae. Infect Immun. 1980;27:721-9. [ Links ]
84. Bernan V, Filpula D, Herber W, Bibb M, Katz E. The nucleotide sequence of the tyrosinase gene from Streptomyces antibioticus and characterization of the gene product. Gene. 1985;37:101-10. [ Links ]
85. Lee YH, Chen BF, Wu SY, Leu WM, Lin JJ, Chen CW, et al. A trans-acting gene is required for the phenotypic expression of a tyrosinase gene in Streptomyces. Gene. 1988;65:71-81. [ Links ]
86. Tsai TY, Lee H. Roles of copper ligands in the activation and secretion of Streptomyces tyrosinase. J Biol Chem. 1998;273:19243-50. [ Links ]
87. Hasegawa M, Hintermann G, Simonet JM, Crameri R, Piret J, Hutter R. Certain chromosomal regions in Streptomyces glaucescens tend to carry amplifications and deletions. Mol Gen Genet. 1985;200:375-84. [ Links ]
88. Hintermann G, Zatchej M, Hutter R. Cloning and expression of the genetically unstable tyrosinase structural gene from Streptomyces glaucescens. Mol Gen Genet. 1985;200:422-32. [ Links ]
89. Kuznetsov VD, Filippova SN, Orlova TI, Rybakova AM. Regulation of the biosynthesis of secondary metabolites in Streptomyces galbus. Mikrobiologiia. 1984;53:357-63. [ Links ]
90. Kuznetsov VD, Filippova SN, Rybakova AM. Nature of the brown pigment and the composition of the phenol oxidases of Streptomyces galbus Mikrobiologiia. 1984;53:251-6. [ Links ]
91. Yabuuchi E, Ohyama, A. Characterization of pyomelanin producing strains of Pseudommonas aeruginosa. Int J Syst Bacteriol. 1972;222:53-64. [ Links ]
92. Ruetschi U, Odelhog B, Lindstedt S, Barros-Soderling J, Persson B, Jornvall H. Characterization of 4-hydroxyphenylpyru uvate dioxygenase. Primary structure of the Pseudommonas enzyme. Eur Biochem. 1992; 2005:459-66. [ Links ]
93. Elston HR. Melanogenic strains of Pseudomonas aeruginosa in biological specimens. Am J Med Technol. 1968;34:189-94. [ Links ]
94. Tydelskaia IL, Rozhavin MA, Sologub VV. Pathogenicity factors of melanin-forming strains of Pseudomonas aeruginosa. Zh Mikrobiol Epidemiol Immunobiol. 1981;73-6. [ Links ]
95. Ruan L, Huang Y, Zhang G, Yu D, Ping S. Expression of the mel gene from Pseudomonas maltophilia in Bacillus thuringiensis. Lett Appl Microbiol. 2002;34:244-8. [ Links ]
96. Wang G, Aazaz A, Peng Z, Shen P. Cloning and overexpression of a tyrosinase ene el from Pseudomonas maltophila. FEMS Microbiol Lett. 2000;185:23-7. [ Links ]
97. Nelson JW, Butler SL, Krieg D, Govan JR. Virulence factors of Burkholderia cepacia. FEMS Immunol Med Microbiol. 1994;8:89-97. [ Links ]
98. Zughaier SM, Ryley HC, Jackson SK. A melanin pigment purified from an epidemic strain of Burkholderia cepacia attenuates monocyte respiratory burst activity by scavenging superoxide anion. Infect Immun.1999;67:1908-11 [ Links ]
99. Bridelli MG. Self-assembly of melanin studied by laser light scattering. Biophys Chem. 1998;73:227-39. [ Links ]
100. Coon SL, Kotob S, Jarvis BB, Wang S, Fuqua WC, Weiner RM. Homogentisic acid is the product of MelA, which mediates melanogenesis in the marine bacterium Shewanella colwelliana J. Appl Environ Microbiol 1994;60:3006-11 [ Links ]
101. Fuqua WC, Coyne VE, Stein DC, Lin CM, Weiner RM. Characterization of melA: a gene encoding melanin biosynthesis from the marine bacterium Shewanella colwelliana. Gene. 1991;109:131-6. [ Links ]
102. Fuqua WC, Weiner RM. The melA gene is essential for melanin biosynthesis in the marine bacterium Shewanella colwelliana. J Gen Microbiol. 1993;139:1105-14. [ Links ]
103. Ruzafa C, Solano F, Sánchez-Amat A. The protein encoded by the Shewanella colwelliana melA gene is a p-hydroxyphenylpyruvate dioxygenase. FEMS Microbiol Lett. 1994;124:179-84. [ Links ]
104. Ellis DH, Griffiths DA. The location and analysis of melanins in cell walls of some soil fungi. Can J Microbiol. 1974;20:1379-86. [ Links ]
105. Fitt W, Lebare M, Fuqua WC, Walch M, Coon SL, Bonar D, Cowell R, Weiner RM. Factors influencing bacterial production of inducers of settlement behavior of larvae of the oyster Crassostrea gigas .Microb Ecol. 1989;17:287-98. [ Links ]
106. Turick CE, Tisa LS, Caccavo F, Jr. Melanin production and use as a soluble electron shuttle for Fe(III) oxide reduction and as a terminal electron acceptor by Shewanella algae BrY. Appl Environ Microbiol. 2002;68:2436-44. [ Links ]
107. Alexandre G, Bally R. Emergence of a laccase-positive variant of Azospirillum lipoferum occurs via a two-step phenotypic switching process. FEMS Microbiol Lett. 1999;174:371-8. [ Links ]
108. Newman DK, Kolter R. A role for excreted quinones in extracellular electron transfer. Nature. 2000;405:94-7. [ Links ] [ Links ]
110. Shivprasad S, Page WJ. Catechol formation and melanization by na-dependent Azotobacter chroococcum: a protective mechanism for aeroadaptation? Appl Environ Microbiol. 1989;55:1811-7. [ Links ]
111. Prabhakaran K. Unusual effects of reducing agents on 0-dipheno-loxidase of Mycobacterium leprae. J Bacteriol. 1971;107:787-9. [ Links ]
112. Prabhakaran K. Hypopigmentation of skin lesions in leprosy a hypothesis. Lepr India. 1977;49:462-3. [ Links ]
113. Prabhakaran K. Dopa metabolism by Mycobacterium leprae: its implications in culture of the Bacillus and chemotherapy of leprosy. Lepr Rev. 1973;44:112-9. [ Links ]
114. Amitai G, Adani R, Sod-Moriah G, Rabinovitz I, Vincze A, Leader H, et al .Oxidative biodegradation of phosphorothiolates by fungal laccase. FEBS Lett. 1998;438:195-200. [ Links ]
115. Xu F. Oxidation of phenoles, anilines and benzenethiols by fungal laccases: correlation between activity and redox potentials as well as halide inhibition. Biochemistry. 1996;35:7608-14. [ Links ]
116. Fernández E, Sánchez-Amat A, Solano F. Location and catalytic characteristics of a multipotent bacterial polyphenol oxidase. Pigment Cell Res. 1999;12:331-9. [ Links ]
117. Eshete F, LoVerde PT. Characteristics of phenol oxidase of Schistosoma mansoni and its functional implications in eggshell synthesis. J Parasitol. 1993;79:309-17. [ Links ]
118. Fetterer RH, Rhoads ML. Biochemistry of the nematode cuticle: relevance to parasitic nematodes of livestock. Vet Parasitol. 1993;46:103-11 [ Links ]
119. Hunt G, Fogel R. Fungal hyphal dynamics in western Oregon Douglas-fir stand. Soil Biol Biochem. 1983;15:641-9. [ Links ]
120. Butler M, Day AW. Fungal melanins: a review. Can J Microbiol. 1998;44:1115-36. [ Links ]
121. Rast D, Hollenstein G. Architecture of the Agaricus bisporus spore wall. Can J Bot. 1977;55:2251-62. [ Links ]
122. Revankar SG, Patterson JE, Sutton DA, Pullen R, Rinaldi MG. Disseminated phaeohyphomycosis: review of an emerging mycosis. Clin Infect Dis. 2002;34:467-76. [ Links ]
123. Silveira F, Nucci M. Emergence of black moulds in fungal disease: epidemiology and therapy. Curr Opin Infect Dis. 2001;14:679-84. [ Links ]
124. Shiotani H, Tsuge T. Efficient gene targeting in The filamentous fungus Alternaria alternata. Mol Gen Genet. 1995;248:142-50. [ Links ]
125. Kawamura C, Moriwaki J, Kimura N, Fujita Y, Fuji S, Hirano T, et al. The melanin biosynthesis genes of Alternaria alternata can restore pathogenicity of the melanin-deficient mutants of Magnaporthe grisea. Mol Plant Microbe Interact. 1997;10:446-53. [ Links ]
126. Jonsson L, Sjostrom K, Haggstrom I, Nyman PO. Characterization of a laccase gene from the white-rot fungus Trametes versicolor and structural features of basidiomycete laccases. Biochim Biophys Acta. 1995;1251:210-5. [ Links ]
127. Yaver DS, Golightly EJ. Cloning and characterization of three laccase genes from the white-rot basidiomycete Trametes villosa: genomic organization of the laccase gene family. Gene. 1996;181:95-102. [ Links ]
128. Yaver DS, Xu F, Golightly EJ, Brown KM, Brown SH, Rey MW, et al. Purification, characterization, molecular cloning, and expression of two laccase genes from the white rot basidiomycete Trametes villosa. Appl Environ Microbiol. 1996;62:834-41. [ Links ]
129. Fernández-Larrea J, Stahl U. Isolation and characterization of a laccase gene from Podospora anserina. Mol Gen Genet. 1996;252:539-51. [ Links ]
130. Wahleithner JA, Xu F, Brown KM, Brown SH, Golightly EJ, Halkier T, et al. The identification and characterization of four laccases from the plant pathogenic fungus Rhizoctonia solani. Curr Genet. 1996;29:395-403. [ Links ]
131. Smith M, Shnyreva A, Wood DA, Thurston CF. Tandem organization and highly disparate expression of the two laccase genes lcc1 and lcc2 in the cultivated mushroom Agaricus bisporus. Microbiology. 1998;1144:1063-9. [ Links ]
132. Giardina P, Palmieri G, Scaloni A, Fontanella B, Faraco V, Cennamo G, et al. Protein and gene structure of a blue laccase from Pleurotus ostreatus. Biochem J. 1999;341:655-63. [ Links ]
133. Edens WA, Goins TQ, Dooley D, Henson M. Purification and characterization of a secreted laccase of Gaeumannomyces graminis var. tritici. Appl Environ Microbiol. 1999;65:3071-4. [ Links ]
134. Litvintseva AP, Henson JM. Cloning, characterization, and transcription of three laccase genes from Gaeumannomyces graminis var.tritici, the take-all fungus. Appl Environ Microbiol. 2002;68:1305-11. [ Links ]
135. Staib F, Randhawa HS, Grosse G, Blisse A. Cryptococcosis. A contribution to the identification of Cryptococcus neoformans isolated from clinical specimens author s transl. Zentralbl Bakteriol Orig A. 1973;2225:211-22. [ Links ]
136. Staib F, Senska M. Brown pigmentation (brown colour effect, BCE) of Cryptococcus neoformans on Guizotia abyssinica-creatinine-agar as dependent on the initial pH value (author s transl). Zentralbl akte riol Orig A. 1973;225:113-24. [ Links ]
137. Frases S, Salazar A, Dadachova E, Casadevall A. Cryptococcus neoformans can utilize the bacterial melanin recursor homogentisic acid for fungal melanogenesis. Appl Environ Microbiol. 2007;73:615-21. [ Links ]
138. Morris-Jones R, Youngchim S, Gómez BL, Aisen P, Hay RJ, Nosanchuk JD, et al. Synthesis of melanin-like pigments by Sporothrix schenckii in vitro and during mammalian infection. Infect Immun. 2003;71:4026-33. [ Links ]
139. Tsai HF, Fujii I, Watanabe A, Wheeler MH, Chang YC, Yasuoka Y, et al. Pentaketide melanin biosynthesis in Aspergillus umigatus requires chain-length shortening of a heptaketide precursor. J Biol Chem. 2001;276:29292-8. [ Links ]
140. Youngchim S, Morris-Jones R, Hay RJ, Hamilton AJ. Production of melanin by Aspergillus fumigatus. J Med Microbiol. 2004;53:175-81. [ Links ]
141. Schnitzler N, Peltroche-Llacsahuanga H, Bestier N, Zundorf J, Lutticken R, Haase G. Effect of melanin and carotenoids of Exophiala (Wangiella)dermatitidis on phagocytosis, oxidative burst, and killing by human neutrophils. Infect Immun. 1999;67:94-101. [ Links ]
142. Nosanchuk JD,van Duin D, Mandal P, Aisen P, Legendre AM, Casadevall A. Blastomyces dermatitidis produces melanin in vitro and during infection. FEMS Microbiol Lett. 2004;239:187-93. [ Links ]
143. Morris-Jones R, Youngchim S, Hextall JM, Gómez BL, Morris-Jones SD, Hay RJ, et al. Scytalidium dimidiatum causing recalcitrant subcutaneous lesions produces melanin. J Clin Microbiol. 2004;42:3789-94 [ Links ]
144. van de Sande WW, de Kat J, Coppens J, Ahmed AO, Fahal A, Verbrugh H, et al. Melanin biosynthesis in Madurella mycetomatis and its effect on susceptibility to itraconazole and ketoconazole. Microbes Infect. 2007;9:1114-23. [ Links ]
145. van de Sande WW, Fahal AH, Riley TV, Verbrugh H, van Belkum A. in vitro susceptibility of Madurella mycetomatis, prime agent of Madura foot, to tea tree oil and artemisinin. J Antimicrob Chemother. 2007;59:553-5. [ Links ]
146. Icenhour CR, Kottom TJ, Limper AH. Evidence for a melanin cell wall component in Pneumocystis carinii. Infect Immun. 2003;71:5360-3. [ Links ]
147. Alviano CS, Farbiarz SR, De Souza W, Angluster J, Travassos LR. Characterization of Fonsecaea pedrosoi melanin. J Gen Microbiol. 1991;137:837-44. [ Links ]
148. Alviano DS, Franzen AJ, Travassos LR, Holandino C, Rozental S, Ejzemberg R, et al. Melanin from Fonsecaea pedrosoi induces production of human antifungal antibodies and enhances the antimicrobial efficacy of phagocytes. Infect Immun. 2004;72:229-37. [ Links ]
149. San-Blas G, Guanipa O, Moreno B, Pekerar S, San-Blas F. Cladosporium carrionii and Hormoconis resinae (C.resinae ): cell wall and melanin studies. Curr Microbiol. 1996;32:11-6 [ Links ]
150. Youngchim S, Hay RJ, Hamilton AJ. Melanization of Penicillium marneffei in vitro and in vivo. Microbiology. 2005;151:291-9. [ Links ]
151. Morris-Jones R, Gomez BL, Diez S, Uran M, Morris-Jones SD, Casadevall A, et al. Synthesis of melanin pigment by Candida albicans in vitro and during infection. Infect Immun. 2005;73:6147-50. [ Links ]
152. Plonka PM, Grabacka M. Melanin synthesis in microorganisms-biotechnological and medical aspects. Acta Biochim Pol. 2006;53:429-43. [ Links ]
153. Huffnagle GB, Chen GH, Curtis JL, McDonald RA, Strieter RM, Toews GB. Down-regulation of the afferent phase of T cell-mediated pulmonary inflammation and immunity by a high melanin-producing strain of Cryptococcus neoformans. Immunol. 1995;155:3507-16. [ Links ]
154. Noverr MC, Williamson PR, Fajardo RS, Huffnagle GB. CNLAC1 is required for extrapulmonary dissemination of Cryptococcus neoformans but not pulmonary persistence. Infect Immun. 2004;72:1693-9. [ Links ]
155. Salas SD, Bennett JE, Kwon-Chung KJ, Perfect JR, Williamson PR. Effect of the laccase gene CNLAC1, on virulence of Cryptococcus neoformans. J Exp Med. 1996;184:377-86. [ Links ]
156. Steenbergen JN, Casadevall A. The origin and maintenance of virulence for the human pathogenic fungus Cryptococcus neoformans. Microbes Infect. 2003;5:667-75. [ Links ]
157. Rosas AL, Casadevall A. Melanization affects susceptibility of Cryptococcus neoformans to heat and cold. FEMS Microbiol Lett. 1997;153:265-72. [ Links ]
158. Howard RJ, Valent B. Breaking and entering: host penetration by the fungal rice blast pathogen Magnaporthe grisea. Annu Rev Microbiol. 1996;50:491-512. [ Links ]
159. Kuo MJ, Alexander M. Inhibition of the lysis of fungi by melanins. J Bacteriol. 1967;94:624-9. [ Links ]
160. Rehnstrom A,Free S. The isolation and characterization of melanin deficient mutants of Monilinia fructicola. Physiol Mol Plant Pathol. 1997;49:321-30. [ Links ]
161. Zhdanova NN, Pokhodenko VD. Possible participation of melanin pigment in protecting the fungal cell from desiccation. Mikrobiologiia. 1973;42:848-53. [ Links ]
162. Kollias N, Sayre RM, Zeise L, Chedekel MR. Photoprotection by melanin. Photochem Photobiol B. 1991;9:135-60. [ Links ]
163. Kollias N, Baqer A. Spectroscopic characteristics of human melanin in vivo. Invest Dermatol. 1985;85:38-42. [ Links ]
164. Kollias N, Baqer AH. Absorption mechanisms of human melanin in the visible, 400-720 nm. J Invest Dermatol. 1987;89:384-8. [ Links ]
165. Patel KR, Wyman JA, Patel KA, Burden BJ. A mutant of Bacillus thuringiensis producing a dark brown pigment with increased resistence and insecticidal activity. Invertebr Pathol. 1996;67:120-4. [ Links ]
166. Schaeffer P. Sporulation and the production of antibiotics, exoenzymes, and exotonins. Bacteriol Rev. 1969;33:48-71. [ Links ]
167. Hullo MF, Moszer I, Danchin A, Martin-Verstraete I. CotA of Bacillus subtilis is a copper-dependent laccase. Bacteriol. 2001;183:5426-30. [ Links ]
168. Riesenman PJ, Nicholson WL. Role of the spore coat layers in Bacillus subtilis spore resistance to hydrogen peroxide, artificial UV-C, UV-B, and solar UV radiation. Appl Environ Microbiol. 2000;66:620-6. [ Links ]
169. Mirchink TG, Ashkina GB, Abaturov Iu D. Stability of pigmented fungi Stemphylium botryosum Wallr and Cladosporium cladosporivides (Freis) de Vries towards gamma-irradiation. Mikrobiologiia. 1968;37:865-9 [ Links ]
170. Ursi C, Wollenzien U, Criseo G, Krumbein WE. Biodiversity of the rock inhabiting microbiota with special reference to blak fungi and black yeast. In: Allosopp D, Colwell RR, Hawksworth DL, editors. Microbial diversity and ecosystem function. Wallingford, Oxon: CAB International; 1997. p. 289-302. [ Links ]
171. Zhdanova NN, Melezhik AV, Vasilevskaya AI. Thermostability of some melanin-containing fungi. Biol Bull Acad Sci USSR. 1980;7:305-10. [ Links ]
172. Wang Y, Casadevall A. Decreased susceptibility of melanized Cryptococcus neoformans to UV light. Appl Environ Microbiol. 1994;60:33 6. [ Links ]
173. Mirchink TG, Kashkina GB, Abaturov L. Resistance of fungi with different pigments to radiation. Mikrobiologiia. 1972;41:83-6. [ Links ]
174. Zhdanova NN, Pokhodenko VD, Gavriushina AI ,Golynskaia IS. Resistance of Dematiceae and their mutants to various types of irradiation. Izv Akad Nauk SSSR Biol. 1973;3:324-33. [ Links ]
175. Dixon DM, Polak A, Szaniszlo PJ. Pathogenicity and virulence of wild-type and melanin-deficient Wangiella dermatitidis. J Med Vet Mycol. 1987;25:97-106. [ Links ]
176. Kawamura C, Tsujimoto T, Tsuge T. Targeted disruption of a melanin biosynthesis gene affects conidial development and UV tolerance in the Japanese pear pathotype of Alternaria alternat. Mol Plant Microbe Interact. 1999;12:59-63. [ Links ]
177. Mironenko NV, Alekhina IA, Zhdanova NN, Bulat SA. Intraspecific variation in gamma-radiation resistance and genomic structure in the filamentous fungus Alternaria alternata: a case study of strains inhabiting Chernobyl reactor no. 4. Ecotoxicol Environ Saf. 2000;45:177-87. [ Links ]
178. Saleh YG, Mayo MS, Ahearn DG. Resistance of some common fungi to gamma irradiation. Appl Environ Microbiol. 1988;54:2134-5. [ Links ]
179. Zhdanova NN, Gavriushina AI, Vasilevskaia AI. Effect of gamma and UV irradiation on the survival of Cladosporium sp. and Oidiodendron cerealis. Mikrobiol Zh. 1973;35:449-52. [ Links ]
180. Zhdanova NN, Lashko TN, Redchits TI, Vasilevskaia AI, Borisiuk LG, Siniavskaia OI, et al. The interaction of soil micromycetes with hot particles in a model system. Mikrobiol Zh. 1991;53:9-17. [ Links ]
181. Zhdanova NN, Vasilevskaia AI, Artyshkova LV, Gavriliuk VI, Lashko TN, Sadovnikov Iu S.Complexes of soil micromycetes in the area of the influence of the Chernobyl Atomic Electric Power Station. Mikrobiol Zh. 1991;53:3-9. [ Links ]
182. Pulatova MK, Sharygin VL. Fungal infection of human organs by resistant melanin-synthesizing species is one of the pathogenic factors and one of the real consequences of the accident at Chernobyl power plant. Radiats Biol Radioecol. 1997;37:649-56. [ Links ]
183. Pulatova MK, Sharygin VL, Reva LP. Detection and nature of melanin containing centers in bronchoalveolar smears and blood of persons responsible for cleaning up after the accident at the Chernobyl Atomic Energy Station. Dokl Akad Nauk. 1995;345:130-4. [ Links ]
184. Blasi E, Barluzzi R, Mazzolla R, Tancini B, Saleppico S, Puliti M, et al. Role of nitric oxide and melanogenesis in the accomplishment of anticryptococcal activity by the BV-22 microglial cell line. J Neuroimmunol. 1995;58:111-6. [ Links ]
185. Stravs-Mombelli L, Willer H. Reinvestigation of the formation of dopa-melanin: new aspects of the autoxidation of dopa. In: Bargnara J, Klaus SN, Paul F, Schartl M, editors. Pigment cell: biological, molecular and clinical aspects of pigmentation. Tokyo: University of Tokyo Press; 1985. p.69. [ Links ]
186. Tsai HF, Washburn RG, Chang YC, Kwon-Chung KJ. Aspergillus fumigatus arp1 modulates conidial pigmentation and complement deposition. Mol Microbiol. 1997;26:175-83. [ Links ]
187. De Hoog GS, Queiroz-Telles F, Haase G, Fernandez-Zeppenfeldt G, Attili Angelis D, Gerrits Van Den Ende AH, et al. Black fungi: clinical and pathogenic approaches. Med Mycol. 2000; 38 (Suppl.1):243-50. [ Links ]
188. Doering TL, Nosanchuk JD, Roberts WK, Casadevall A. Melanin as a potential cryptococcal defence against microbicidal proteins. Med Mycol. 1999;37:175-81. [ Links ]
189. Sarangarajan R, Apte SP. Melanization and phagocytosis: implications for age related macular degeneration. Mol Vis. 2005;11:482-90. [ Links ]
190. Gan EV, Haberman HF, Menon IA. Electron transfer properties of melanin. Arch Biochem Biophys. 1976;173:666-72. [ Links ]
191. Commoner B, Townsend J, Pake GE. Free radicals in biological materials. Nature. 1954;174:689-91. [ Links ]
192. Korytowski W, Hintz P, Sealy RC, Kalyanaraman B. Mechanism of dismutation of superoxide produced during autoxidation of melanin pigments. Biochem Biophys Res Commun. 1985;131:659-65. [ Links ]
193. Korytowski W, Kalyanaraman B, Menon IA, Sarna T, Sealy RC. Reaction of superoxide anions with melanins: electron spin resonance and spin trapping studies. Biochim Biophys Acta. 1986;882:145-53. [ Links ]
194. Swartz HM, Sarna T, Zecca L. Modulation by neuromelanin of the availability and reactivity of metal ions. Ann Neurol. 1992;32(Suppl.): S69-75. [ Links ]
195. Jacobson ES, Hong JD. Redox buffering by melanin and Fe(II) in Cryptococcus neoformans. Bacteriol. 1997;179:5340-6. [ Links ]
196. Nyhus KJ, Wilborn AT, Jacobson ES. Ferric iron reduction by Cryptococcus neoformans. Infect Immun. 1997;65:434-8. [ Links ]
197. Jacobson ES, Jenkins ND, Todd JM. Relationship between superoxide dismutase and melanin in a pathogenic fungus. Infect Immun. 1994;62:4085-6. [ Links ]
198. Geremia E, Corsaro C, Bonomo, R, Giardinelli R, Pappalardo P, Vanella, A, Sichel, G. Eumelanins as free radicals trap and superoxide dismutase activities in amphhibia. Comp Biochem Physiol Ser B. 1984;79:67-9. [ Links ]
199. Jacobson ES, Tinnell SB. Antioxidant function of fungal melanin. J Bacteriol. 1993;175:7102-4. [ Links ]
200. Jacobson ES, Hove E, Emery HS. Antioxidant function of melanin in black fungi. Infect Immun. 1995;63:4944-5. [ Links ]
201. Lukiewicz S. The biological role of melanin. I. New concepts and methodical approaches. Folia Histochem Cytochem (Krakow). 1972;10:93-11 [ Links ]
202. Malama AA, Smirnova LA. Effect of cyclic compounds on pigment formation in Aspergillus niger cultures. Prikl Biokhim Mikrobiol. 1975;11:57-62. [ Links ]
203. Jahn B, Koch A, Schmidt A, Wanner G, Gehringer H, Bhakdi S, et al. Isolation and characterization of a pigmentless-conidium mutant of Aspergillus fumigatus with altered conidial surface and reduced virulence. Infect Immun. 1997;65:5110-7. [ Links ]
204. Page WJ, Shivprasad S. Iron binding to Azotobacter salinestris melanin, iron mobilization and uptake mediated by siderophores. Biometals. 1995;8:59-64 [ Links ]
205. Aver´yanov AA, Lapikova VP, Petelina GG, Dzhavakhiya VG. Increased sensitivity of pigment mutantas of Pyricularia oryzae to toxic excretions of rice leaves. Friziol Rast (Moscow). 1989;36:1088-95. [ Links ]
206. D Acquisto F, Carnuccio R, d Ischia M, Misuraca G. 5,6-Dihydroxyin- dole-2-carboxylic acid, a diffusible melanin precursor, is a potent stimulator of lipopolysaccharide-induced production of nitric oxide by J774 macrophages. Life Sci. 1995;57:PL401-6. [ Links ]
207. Romero-Graillet C, Aberdam E, Clement M, Ortonne JP, Ballotti R. Nitric oxide produced by ultraviolet-irradiated keratinocytes stimulates melanogenesis. J Clin Invest. 1997;99:635-42. [ Links ]
208. Double L, Halliday GM. New face of neuromelanin. J Neural Transm 2006(Suppl.):119-23. [ Links ]
209. Double KL, Ben-Shachar D, Youdim MB, Zecca L, Riederer P, Gerlach M. Influence of neuromelanin on oxidative pathways within the human substantia nigra. Neurotoxicol Teratol. 2002;24:621-8. [ Links ]
210. Sarangarajan R, Apte SP. The polymerization of melanin: a poorly understood phenomenon with egregious biological implications. Melanoma Res. 2006;16:3-10. [ Links ]
211. Blinova MI, Iudintseva NM, Kalmykova NV, Kuz minykh EV, Iurlova NA, Ovchinnikova OA. Effect of melanins from black yeast fungi on cultured human cells. I. Proliferation of keratinocytes and fibroblasts. Tsitologiia. 2002;44:780-7. [ Links ]
212. Blinova MI, Kalmykova NV, Iudintseva NM, Kuz minykh EV, Iurlova NA, Ovchinnikova OA, et al .Effect of melanins from black yeast fungi on cultured human cells. II. Differentiation of keratinocytes in vitro. Tsitologiia. 2002;44:788-91. [ Links ]
213. Blinova MI, Yudintseva NM, Kalmykova NV, Kuzminykh EV, Yurlova A, Ovchinnikova OA, et al . Effect of melanins from black yeast fungi on proliferation and differentiation of cultivated human keratinocytes and fibroblasts. Cell Biol Int. 2003;27:135-46. [ Links ]
214. Long CC, Marks R. Increased risk of skin cancer: another Celtic myth? A review of Celtic ancestry and other risk factors for malignant melanoma and nonmelanoma skin cancer. J Am Acad Dermatol. 1995;33:658-61. [ Links ]
215. Urbach F. Geographic distribution of skin cancer. J Surg Oncol. 1971;3:219-34. [ Links ]
216. Takeuchi S, Zhang W, Wakamatsu K, Ito S, Hearing VJ, Kraemer KH, et al . Melanin acts as a potent UVB photosensitizer to cause an atypical mode of cell death in murine skin. Proc Natl Acad Sci U S A. 2004;101:15076-81. [ Links ]
217. Aime S, Bergamasco B, Casu M, Digilio G, Fasano M, Giraudo S, et al. Isolation and 13C-NMR characterization of an insoluble proteinaceous fraction from substantia nigra of patients with Parkinsons disease. Mov Disord. 2000;15:977-81. [ Links ]
218. Aime S, Botta M, Camurati I. NMR studies of L-dopa melanin manganese(II)complex in water solution. J Inorg Biochem.1989;36:1-9. [ Links ]
219. Aime S, Fasano M, Terreno E, Groombridge CJ. NMR studies of melanins: characterization of a soluble melanin free acid from Sepia ink. Pigment Cell Res. 1991;4:216-21. [ Links ]
220. Offen D, Gorodin S, Melamed F, Hanania J, Malik Z. Dopamine-melanin is actively phagocytized by PC12 cells and cerebellar granular cells: possible implications for the etiology of Parkinsons disease. Neurosci Lett. 1999;260:101-4. [ Links ]
221. Offen D, Ziv I, Panet H, Wasserman L, Stein R, Melamed E, et al. Dopamine-induced apoptosis is inhibited in PC12 cells expressing Bcl-2. Cell Mol Neurobiol. 1997;17:289-304. [ Links ]
222. Mednick AJ, Nosanchuk JD, Casadevall A. Melanization of Cryptococcus neoformans affects lung inflammatory responses during cryptococcal infection. Infect Immun. 2005;73:2012-9. [ Links ]
223. Kock A, Schwarz T, Kirnbauer R, Urbanski A, Perry P, Ansel JC, et al. Human keratinocytes are a source for tumor necrosis factor alpha: evidence for synthesis and release upon stimulation with endotoxin or ultraviolet light. J Exp Med. 1990;172:1609-14. [ Links ]
224. Englaro W, Bahadoran P, Bertolotto C, Busca R, Derijard B, Livolsi A, et al. Tumor necrosis factor alpha-mediated inhibition of melanogenesis is dependent on nuclear factor kappa B activation. Oncogene. 1999;18:1553-9. [ Links ]
225. Martinez-Esparza M, Jimenez-Cervantes C, Solano F, Lozano JA, Garcia-Borron JC. Mechanisms of melanogenesis inhibition by tumor necrosis factor-alpha in B16/F10 mouse melanoma cells. Eur J Biochem. 1998;255:139-46. [ Links ]
226. Swope VB, Abdel-Malek Z, Kassem LM, Nordlund JJ. Interleukins 1 alpha and 6 and tumor necrosis factor-alpha are paracrine inhibitors of human melanocyte proliferation and melanogenesis. J Invest Dermatol. 1991;96:180-5. [ Links ]
227. Nosanchuk JD, Rosas AL, Casadevall A. The antibody response to fungal melanin in mice. J Immunol. 1998 Jun 15;160:6026-31. [ Links ]
228. Nosanchuk JD, Valadon P, Feldmesser M, Casadevall A. Melanization of Cryptococcus neoformans in murine infection. Mol Cell Biol. 1999;19:745-50. [ Links ]
229. Fishman P, Merimski O, Baharav E, Shoenfeld Y. Autoantibodies to tyrosinase: the bridge between melanoma and vitiligo. Cancer. 1997;77 1461-4. [ Links ]
230. Hertz KC, Gazze LA, Kirkpatrick CH, Katz SI. Autoimmune vitiligo: detection of antibodies to melanin-producing cells. N Engl J Med. 1977;297:634-7. [ Links ]
231. Vignale A, Lasalvia E, Borras A. Antimelanin antibodies in vitiligo. Med Cutan Ibero Lat Am. 1983;11:271-6. [ Links ]
232. Gottumukkala RV, Gavalas NG, Akhtar S, Metcalfe RA, Gawkrodger DJ, Haycock JW, et al. Function-blocking autoantibodies to the melanin-concentrating hormone receptor in vitiligo patients. Lab Invest. 2006;86:781-9. [ Links ]
233. Spritz RA. The genetics of generalized vitiligo and associated autoimmune diseases. Dermatol Sci. 2006;41:3-10. [ Links ]
234. Zhang J, Chen J, Liu JB. The genetic concept of vitiligo. J Dermatol Sci. 2005;39:137-46. [ Links ]
235. Rosas AL, Nosanchuk D, Feldmesser M, Cox GM, McDade HC, Casadevall A. Synthesis of polymerized melanin by Cryptococcus neoformans in infected rodents. Infect Immun. 2000;68:2845-53. [ Links ]
236. Uran ME, Gomez BL, Restrepo A, Cano LE. Antibody response against P. brasiliensis melanin in experimental model of Paracoccidioidomycosis. In: ISHAM, editor. 16th Congress of the International Society for Human and Animal Mycology. Paris: ISHAM; 2006. [ Links ]
237. Uran ME. Caracterización de la melanogénesis en el hongo dimórfico Paracoccidioides brasiliensis y análisis de su papel en la patogénesis (tesis). Medellín: Universidad Pontificia Bolivariana; 2007. [ Links ]
238. Uran ME, Gomez BL, Restrepo A, Cano LE, Hamilton A. Preparation and characterization of IgG and IgM monoclonal antibodies against Paracoccidioides brasiliensis melanin. In: FOCIS, editor. 12th International Congress of Immunology and 4th Annual Conference of FOCIS; Montreal: FOCIS; 2004. [ Links ]
239. Rosas AL, Nosanchuk JD, Casadevall A. Passive immunization with melanin-binding monoclonal antibodies prolongs survival of mice with lethal Cryptococcus neoformans infection. Infect Immun. 2001;69:33410-2. [ Links ]
240. Fothergill AW. Identification of dematiaceous fungi and their role in human disease. Clin Infect Dis. 1996;22(Suppl.2):S179-84. [ Links ]
241. Geis PA, Wheeler MH, Szaniszlo PJ. Pentaketide metabolites of melanin synthesis in the dematiaceous fungus Wangiella dermatitidis. Arch Microbiol. 1984;137:324-8. [ Links ]
242. Ruiz-Diez B, Martinez-Suarez JV. Isolation, characterization, and antifungal susceptibility of melanin-deficient mutants of Scedosporium prolificans. Curr Microbiol. 2003 Mar;46:228-32. [ Links ]
243. Ikeda R, Sugita T, Jacobson ES, Shinoda T. Effects of melanin upon susceptibility of Cryptococcus to antifungals. Microbiol Immunol. 2003;47:271-7. [ Links ]
244. Polak A, Dixon DM. Loss of melanin in Wangiella dermatitidis does not result in greater susceptibility to antifungal agents. Antimicrob Agents Chemother. 1989;33:1639-40. [ Links ]
245. Paolo WF, Jr., Dadachova E, Mandal P, Casadevall A, Szaniszlo PJ, Nosanchuk JD. Effects of disrupting the polyketide synthase gene WdPKS1 in Wangiella (Exophiala) dermatitidis on melanin production and resistance to killing by antifungal compounds, enzymatic degradation, and extremes in temperature. BMC Microbiol. 2006;6:55. [ Links ]
246. Eisenman HC, Nosanchuk JD, Webber JB, Emerson RJ, Camesano TA, Casadevall A. Microstructure of cell wall-associated melanin in the human pathogenic fungus Cryptococcus neoformans. Biochemistry. 2005;44:3683-93. [ Links ]














