Introducción
La infección de vías urinarias (IVU) es la infección que ocurre en alguna de las estructuras del tracto urinario, incluyendo uretra (uretritis), vejiga (cistitis), uréteres (ureteritis) y ríñones (pielonefritis); se define la IVU complicada como la infección que ocurre en pacientes con comorbilidades o con anomalías estructurales o funcionales del tracto urinario que pueden condicionar un mayor riesgo de desarrollar complicaciones, un curso clínico grave, fracaso terapéutico o recurrencia de la infección, la cual incluye un amplio grupo de pacientes y patologías (ej. mujeres posmenopáusicas, hombres adultos, pacientes con patología urológica, usuarios de catéter urinario, adultos mayores, pacientes con diagnóstico de diabetes, entre otros)1-4. Teniendo en cuenta la amplia gama de pacientes incluidos en la definición de IVU complicada, la información disponible sobre su incidencia puede variar según la comorbilidad o grupo poblacional en el que se realice la estimación, derivándose de estudios realizados en pacientes hospitalizados en la mayoría de oportunidades, los cuales han permitido documentar tasas significativas de ingreso hospitalario, morbilidad, mortalidad e incremento en costos asociadas a la IVU complicada4-7.
Adicional a este impacto en morbilidad y mortalidad, dado el uso de agentes antimicrobianos como parte del tratamiento de la IVU complicada, su adecuado diagnóstico y tratamiento tiene un impacto en el desarrollo de la resistencia a los antimicrobianos, situación considerada por la Organización Mundial de la Salud (OMS) desde el 2014 como un problema de salud pública, incluyendo en el listado de patógenos multirresistentes prioritarios especies como Escherichia coli y Klebsiella pneumoniae productores de betalactamasas de espectro extendido y/o con resistencia a carbapenémicos, los cuales son algunos de los principales agentes etiológicos de la IVU complicada8,9.
Por lo anterior resulta de importancia generar directrices que permitan orientar el tratamiento de este grupo de pacientes, con el objetivo de obtener mejores desenlaces clínicos y propender por un uso racional de antibióticos
Alcance de la guía de práctica clínica
Esta guía de práctica clínica (GPC) está dirigida al personal de la salud involucrado en la atención de pacientes adultos mayores de 18 años, con sospecha clínica o diagnóstico confirmado de infección de vías urinarias complicada, y a los tomadores de decisiones o entes involucrados en la generación de políticas en salud. Esta GPC incluye los temas de diagnóstico y tratamiento para la infección de vías urinarias complicada en el contexto colombiano. Se excluyen en estas recomendaciones las pacientes con infección urinaria en el contexto de la gestación.
Objetivo de la guía de práctica clínica
Desarrollar de manera sistemática recomendaciones clínicas basadas en la evidencia para el diagnóstico y tratamiento de pacientes adultos con sospecha clínica o diagnóstico confirmado de infección de vías urinarias complicada, con el fin de optimizar la calidad de la atención para obtener mejores desenlaces clínicos, y promover el uso adecuado y seguro de los antimicrobianos.
Pacientes considerados en la guía de práctica clínica
Las recomendaciones contenidas en esta GPC van dirigidas a los siguientes grupos de pacientes: Pacientes adultos (18 años), pacientes con sospecha clínica o diagnóstico confirmado de infección de vías urinarias complicada: (1) Mujeres posmenopáusicas, (2) Hombres adultos, (3) Adultos mayores, (4) Pacientes con anormalidad urológica, (5) Pacientes portadores de catéter urinario, (6) Pacientes con diagnóstico de diabetes mellitus o enfermedad renal crónica.
Pacientes no considerados en la guía de práctica clínica
Las recomendaciones contenidas en esta GPC no se dirigen a los siguientes grupos poblacionales: Población pediátrica (18 años), mujeres en gestación, pacientes con trasplante renal, pacientes con diagnóstico de neutropenia febril, pacientes con sospecha clínica o diagnóstico confirmado de infección de vías urinarias asociada a la atención en salud.
Usuarios a quienes se dirige la guía de práctica clínica
Las recomendaciones incluidas en la presente guía van dirigidas a los profesionales de la salud vinculados en el proceso de atención de pacientes con sospecha clínica o diagnóstico confirmado de infección de vías urinarias complicada en los diferentes niveles de atención del Sistema General de Seguridad Social en Salud (I, II, III y IV) entre los que se encuentran médicos generales, especialistas con formación en medicina de urgencias, medicina familiar, medicina interna, geriatría, urología, nefrología, infectología, enfermeras profesionales, personal de laboratorio clínico, químicos farmacéuticos y demás personal involucrado en el proceso de diagnóstico y de tratamiento de pacientes con infección de vías urinarias complicada.
Metodología
Para el desarrollo de la presente guía se siguieron los líneamientos presentados en la Guía Metodológica Adopción Adaptación de Guías de Práctica Clínica Basadas en Evidencia del ministerio de salud y protección social de Colombia (10), como se describe a continuación:
Conformación del grupo desarrollador de la guía
El grupo desarrollador (GDG) se conformó por cinco miembros entre expertos temáticos y metodológicos: un especialista con formación en enfermedades infecciosas de adultos (JAC), dos especialistas con formación en medicina interna (NCA, JDCB), un especialista con formación en urología (WDD), dos epidemiólogos clínicos con experiencia en el desarrollo de guías de práctica clínica, revisiones sistemáticas de la literatura, síntesis y calificación de la evidencia y procesos participativos (JAC, MCV). Cada uno de los miembros del GDG previo al inicio de actividades, realizó la declaración de conflictos de interés mediante el diligenciamiento del formulario diseñado para tal fin. En los casos en que se declaró algún conflicto, se realizó el respectivo análisis a fin de definir su implicación en la participación.
Búsqueda de guías de práctica clínica
A continuación, se realizó la búsqueda sistemática de GPC orientada a identificar guías relacionadas con el alcance de la presente guía, publicadas entre el 2016 y el 2021, sin restricción por idioma.
La búsqueda se realizó en los sitios web de los siguientes organismos compiladores y desarrolladores de GPC: Guidelines International Network, Agency for Healthcare Research and Quality/ National Guidelines Clearinghouse, CMA Infobase: Clinical Practice Guidelines, Catálogo de Guías de Práctica Clínica en el Sistema Nacional de Salud, National Institute for Clinical Excellence (NICE), Scottish Intercollegiate Guidelines Network (SING), New Zealand Guidelines Group y American College of Physicians (ACP).
También se realizó la búsqueda en las bases de datos Medli-ne, Embase y Lilacs mediante estrategias de búsqueda adaptadas para cada motor de búsqueda utilizando operadores booleanos, de truncamiento y de proximidad, términos en texto libre y vocabulario controlado, empleando términos clave como "urinary tract infections", "postmenopause", "ureteral obstruction" y "urinary catheters".
Tamización, evaluación de calidad y selección de las guías de práctica clínica a utilizar
Una vez obtenidos los resultados de la búsqueda, se realizó la tamización primaria de referencias por título y resumen, seleccionando aquellas correspondientes a GPC o recomendaciones basadas en la evidencia, que abordaran al menos uno de los aspectos definidos en el alcance de la presente guía. Posteriormente dos revisores de forma independiente realizaron la tamización secundaria en texto completo de las referencias seleccionadas en el paso anterior, resolviendo los desacuerdos por consenso, o con la ayuda de un tercer revisor en los casos en los que no se logró acuerdo entre los dos revisores. No se restringió la búsqueda por idioma, sin embargo, en la selección en texto completo se excluyeron las publicaciones en idiomas alemán, japonés o coreano.
Las GPC seleccionadas luego de la tamización descrita se presentaron al grupo desarrollador con el fin de realizar la evaluación de calidad con la herramienta AGREE II 11. Cada una de las guías se evaluó por dos revisores de forma independiente, siempre con la participación de un experto clínico y un experto metodológico, en los casos en los que se identificaron dudas en relación con la información disponible para la evaluación de la GPC, se realizó por correo electrónico la solicitud de información complementaria a los grupos desarrolladores. Como resultado del proceso de evaluación de calidad, se seleccionaron las GPC con un puntaje 60 % en los dominios de rigor metodológico y de independencia editorial. Finalmente, acorde a las recomendaciones de la Guía Metodológica Adopción Adaptación de Guías de Práctica Clínica Basadas en Evidencia del ministerio de salud y protección social de Colombia10, con el objetivo de seleccionar las GPC a utilizar en el proceso de adaptación, el GDG analizó las guías seleccionadas teniendo en cuenta: los temas abordados en la guía, el uso de la metodología GRADE (Grading of Recommendations, Assessment, Development and Evaluation), el año de publicación y la fecha de la última búsqueda.
Con la metodología descrita se seleccionaron tres guías de práctica clínica para el proceso de adaptación: las guías del Instituto Nacional de Salud y Excelencia Clínica del Reino Unido (NICE, por sus siglas en inglés), publicadas en el año 2018: Urinary tract infection (catheter-associated): antimicrobial prescribing12, Urinary tract infection (lower): antimicrobial prescribing13 y Pyelonephritis (acute): antimicrobial prescribing14.
Adaptación de las recomendaciones
El grupo desarrollador realizó el proceso de adaptación a través de la metodología GRADE, y los marcos GRADE de la evidencia a la recomendación (EtD, por sus siglas en inglés) 15,16 con base en la información proporcionada por las GPC seleccionadas, incluyendo los perfiles de evidencia GRADE con la evaluación de la certeza de la evidencia realizada mediante el análisis de cada uno de los dominios: número y diseño de los estudios, riesgo de sesgo, inconsistencia, evidencia indirecta, imprecisión y otras consideraciones; y teniendo en cuenta las consideraciones específicas del contexto colombiano, los beneficios y daños de las diferentes opciones, el uso de recursos, el impacto en equidad y la factibilidad de implementación.
Consenso de expertos
Finalmente, las recomendaciones adaptadas se llevaron a un consenso de expertos en el cual participaron representantes de diferentes disciplinas del área de la salud incluyendo cinco especialistas con formación en enfermedades infecciosas, dos especialistas con formación en urología, un especialista con formación en geriatra, un especialista con formación en nefrología, cinco especialistas con formación en medicina interna, y profesionales de las áreas de microbiología clínica, y auditoria entre otros. Algunos de los participantes del consenso como representantes de sociedades científicas colombianas como la Asociación Colombiana de Infectología [ACIN], la Sociedad Colombiana de Urología [SCU], y la Asociación Colombiana de Medicina Interna [ACMI], incluyendo de esta manera la perspectiva de diferentes partes interesadas. En el consenso teniendo en cuenta la información y evidencia proporcionada por las dos GPC seleccionadas y las consideraciones específicas del contexto colombiano aportadas por los asistentes, mediante un proceso participativo con metodología Delphi en tiempo real, se formularon las recomendaciones, la graduación de las mismas de acuerdo a la metodología GRADE 17 y se generaron puntos de buena práctica, orientados a brindar una mejor atención de los pacientes.
La votación durante el consenso fue de forma anónima, por medio electrónico. Se definió acuerdo como una votación mayor al 50 %, en los casos en los cuales no hubo acuerdo en la primera ronda, se realizó una sesión de discusión y una nueva ronda de votación, con un número máximo de rondas permitidas de tres.
Niveles de certeza en la evidencia
Alta: El grupo está muy seguro de que el verdadero efecto se acerca a la estimación del efecto.
Moderada: El grupo tiene una confianza moderada en la estimación del efecto. Es probable que el efecto real se acerque a la estimación del efecto, pero existe la posibilidad de que sea sustancialmente diferente
Baja: La confianza del grupo en la estimación del efecto es limitada. El efecto real puede ser sustancialmente diferente de la estimación del efecto.
Muy baja: El grupo tiene muy poca confianza en la estimación del efecto. Es probable que el efecto real sea sustancialmente diferente de la estimación del efecto.
Implicaciones de la fuerza de la recomendación
Las implicaciones de una recomendación fuerte son:
Para los pacientes: la mayoría de las personas en esta situación desearían el curso de acción recomendado y solo una pequeña proporción no lo haría; los pacientes solicitarían una discusión si no se ofrece la intervención.
Para los médicos: la mayoría de los pacientes deben recibir el curso de acción recomendado.
Para los responsables de la formulación de políticas: la recomendación se puede adoptar como política en la mayoría de las situaciones.
Las implicaciones de una recomendación (sugerencia) débil (condicional) son:
Para los pacientes: la mayoría de las personas en esta situación desearían el curso de acción recomendado, pero muchas no.
Para los médicos: debe reconocer que diferentes opciones serán apropiadas para diferentes pacientes y que debe ayudar a cada paciente a llegar a una decisión de manejo coherente con sus valores y preferencias.
Para los formuladores de políticas: la formulación de políticas requerirá un debate sustancial y la participación de muchas partes interesadas.
Preguntas abordadas en la guía
¿Cuáles son las estrategias diagnósticas más adecuadas para la IVU complicada en pacientes adultos?
¿Cuál es el tratamiento antimicrobiano empírico más adecuado en pacientes adultos con IVU complicada?
¿Cuál es la vía de administración del tratamiento antimicrobiano más adecuada en pacientes adultos con IVU complicada?
¿Cuál es la duración del tratamiento antimicrobiano más adecuada en pacientes adultos con IVU complicada?
¿Cuál es el manejo del catéter urinario más adecuado en pacientes adultos portadores de catéter urinario con IVU complicada?
Recomendaciones y revisión de la evidencia
Pregunta N° 1: ¿Cuáles son las estrategias diagnósticas más adecuadas para la IVU complicada en pacientes adultos?
Puntos de buena práctica:
Considerar la sospecha clínica de IVU en pacientes que presenten dos o más síntomas urinarios bajos (disuria, polaquiuria, urgencia, dolor suprapúbico, hematuria).
Considerar la sospecha clínica de IVU en pacientes con fiebre y dolor en flanco, incluso en ausencia de síntomas urinarios bajos.
En pacientes adultos mayores:
Con patología neurocognitiva, trastorno de la comunicación, o que no presenten síntomas típicos de IVU, considerar la IVU como un diagnóstico de exclusión.
Considerar el diagnostico de IVU aun en ausencia de fiebre.
Realizar la sospecha clínica de IVU teniendo en cuenta las manifestaciones atípicas de infección como la presencia de delirium, caída centinela, alteraciones en el patrón de incontinencia, y/o síntomas gastrointestinales.
Utilizar los parámetros de la tira reactiva y el Gram de orina sin centrifugar como herramientas para realizar el diagnóstico de IVU.
No usar la apariencia de la orina, ni el hallazgo de piuria, como herramientas únicas para realizar el diagnóstico de IVU, especialmente en pacientes portadores de catéter urinario.
En pacientes portadores de catéter urinario tomar la muestra de orina con las medidas de asepsia y antisepsia apropiadas o a partir del reservorio destinado para tal efecto.
Tomar urocultivo con antibiograma previo al inicio del tratamiento antimicrobiano.
No tomar urocultivo en pacientes con catéter urinario sin sospecha clínica de IVU.
Considerar la toma de imágenes diagnósticas del tracto urinario (ultrasonografía renal y de vías urinarias, uroTAC, o urografía por TAC) para identificar trastornos urológicos que requieran manejo complementario.
Considerar la toma de hemocultivos en pacientes con sepsis y sospecha clínica de IVU.
Justificación de la recomendación:
A pesar de que las guías seleccionadas no abordaron los aspectos sobre el diagnóstico de la IVU complicada, el consenso consideró pertinente establecer algunos puntos de buena práctica para el proceso diagnóstico.
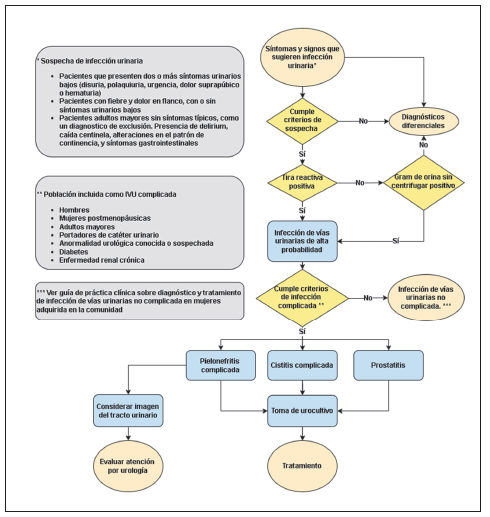
El diagnóstico de cistitis se basa principalmente en la presencia de al menos dos síntomas urinarios bajos (como disuria, poliaquiuria, tenesmo vesical, hematuria, entre otros). En hombres con estos síntomas se debe considerar el diagnóstico diferencial de prostatitis18. La presencia de fiebre y dolor en el flanco son sugestivos de pielonefritis, incluso en ausencia de síntomas urinarios bajos2 Figura 1.
En pacientes con disfunción vesical, portadores de catéteres, o adultos mayores que presentan fragilidad, deterioro cognitivo o alta carga de comorbilidad, es necesario tomar en consideración otros hallazgos clínicos al momento de considerar la sospecha clínica de IVU complicada, ya que pueden no manifestar síntomas típicos o localizadores19.
En adultos mayores que pueden no manifestar fiebre, se debe tener en cuenta la elevación de la temperatura con respecto a la basal20. Entre los síntomas atípicos descritos en estos pacientes se encuentran: anorexia, deterioro funcional, cambios en estado mental, síntomas gastrointestinales, cambios en la continencia urinaria y episodios de caída centinela21. Ante la presencia de estos síntomas atípicos, se puede considerar la IVU como diagnóstico de exclusión, habiendo evaluado y descartado otros focos infecciosos y otras causas. El examen de orina mediante el método de la tira reactiva es una herramienta de apoyo en el proceso diagnóstico. En conjunto, la detección de esterasa leucocitaria y la prueba de nitritos tienen una adecuada precisión diagnóstica, principalmente para predecir la ausencia de bacteriuria con respecto al urocultivo22. De la misma forma, el Gram de orina sin centrifugar tiene una buena sensibilidad para detectar la positividad del urocultivo con recuentos de colonias 105 UFC/mL, con la ventaja de que puede proveer información inicial rápida del tipo de microorganismo causante de la infección23,24. Un estudio realizado en Medellín, Colombia analizó 10.917 muestras de orina encontrando que el Gram de orina sin centrifugar presenta un valor predictivo negativo del 97% para bacteriuria significativa en el urocultivo25.
Es importante tener en cuenta que la bacteriuria y piuria en ausencia de infección es un hallazgo frecuente, sobre todo en adultos mayores y usuarios de dispositivos invasivos de la vía urinaria, de manera que los paraclínicos siempre se deben interpretar en el contexto de una probabilidad preprueba a partir de los datos clínicos26, siendo la tira reactiva y el Gram de orina sin centrifugar de mayor utilidad para descartar la IVU. El urocultivo y antibiograma son elementos claves en el diagnóstico de la infección urinaria, especialmente cuando hay duda. Además, permiten realizar ajustes en el tratamiento antimicrobiano empírico instaurado, en caso de ser necesario, por lo que se considera una buena práctica, realizarlos a todos los pacientes con sospecha clínica de IVU complicada20-28. En el caso que el paciente curse con sepsis también es mandatorio la realización de hemocultivos de acuerdo con las guías actuales29.
Adicionalmente, es necesario tener en cuenta las recomendaciones para la recolección adecuada de muestras de orina, con el fin de lograr un resultado confiable y realizar una interpretación adecuada 28-30:
En pacientes que pueden tener micción espontánea, se indica la toma de la muestra de chorro medio.
Sólo si el paciente no puede lograr micción espontánea sin contaminación se indica realizar cateterismo vesical para la toma de la muestra.
En pacientes portadores de catéter urinario la toma de la muestra de orina se debe realizar a través del puerto destinado para tal fin. Si al paciente le fue cambiado el catéter se debe tomar la muestra del nuevo dispositivo.
En cuanto a las ayudas diagnosticas imagenológicas, estas permiten la caracterización de anormalidades urológicas subyacentes a la infección urinaria complicada. De la misma forma, permiten excluir condiciones que requieren intervenciones adicionales como pielonefritis o cistitis enfisematosa, obstrucción del tracto urinario, litiasis y abscesos. De acuerdo con las guías del Colegio Americano de Radiología (ACR, por sus siglas en inglés) sobre criterios de idoneidad de procedimientos de imagen en pielonefritis complicada, y teniendo en cuenta la disponibilidad; pueden indicarse la ultrasonografía o la tomografía computarizada (TC) de abdomen y pelvis con y/o sin contraste27,31.
Pregunta N° 2: ¿Cuál es el tratamiento antimicrobiano empírico más adecuado en adultos con IVU complicada?
Recomendaciones:
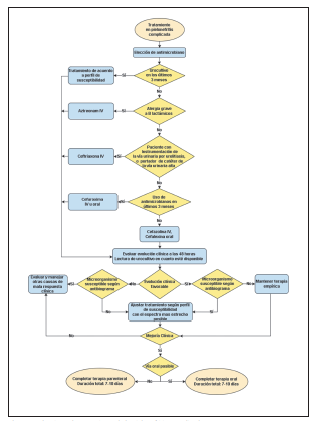
Pielonefritis complicada Tabla 2. Figura 2:
Se sugiere el uso de cefalosporina de primera generación (cefazolina IV, cefalexina oral) en pacientes sin uso previo de antibióticos, o sin instrumentación de la vía urinaria en los últimos 3 meses (recomendación débil, evidencia de muy baja calidad).
Se sugiere el uso de cefalosporina de segunda generación (cefuroxima IV u oral) en pacientes con uso previo de antibióticos en los últimos 3 meses (recomendación débil, evidencia de muy baja calidad).
Se sugiere el uso de cefalosporina de tercera generación (ceftriaxona IV) en pacientes con diagnóstico de urolitiasis e instrumentación de la vía urinaria, o en pacientes portadores de catéteres de la vía urinaria alta (nefrostomías, catéteres ureterales) (recomendación débil, evidencia de muy baja calidad).
Cistitis complicada Tabla 2. Figura 3:
Se sugiere el uso de nitrofurantoína como primera opción en pacientes con tasa de filtración glomerular estimada (TFGe) 45 ml/min (recomendación débil, evidencia de muy baja calidad)
Se sugiere el uso de fosfomicinatrometamol como alternativa (recomendación débil, evidencia de muy baja calidad).
Se sugiere el uso de cefalosporina de primera generación (cefazolina IV) como alternativa en pacientes con manejo intrahospitalario. (recomendación débil, evidencia de muy baja calidad).
Puntos de buena práctica:
Si se dispone del resultado de urocultivo y antibiograma tomado en los últimos 3 meses, se puede utilizar para decidir el tratamiento antimicrobiano a instaurar.
En caso de alergia a betalactámicos utilizar aztreonam para el tratamiento de la IVU alta.
Para la elección y ajuste de dosis de los antimicrobianos, estimar la TFG usando las ecuaciones basadas en creatinina sérica.
No usar nitrofurantoína ni fosfomicina trometamol para el tratamiento antimicrobiano de pacientes con sospecha clínica o diagnóstico confirmado de pielonefritis.
No usar como tratamiento antimicrobiano empírico amoxicilina, amoxicilina/clavulanato, ampicilina, ampicilina/subactam, trimetoprim/sulfametoxazol o fluoroquinolonas.
Realizar seguimiento de los eventos adversos de los antimicrobianos empleados incluyendo la resistencia bacteriana.
Revalorar a las 48 horas del inicio de la terapia antimicrobiana, y en caso de mala respuesta considerar posibles causas o diagnósticos adicionales.
En pacientes con evolución clínica favorable, mantener la terapia antimicrobiana empírica, independientemente del reporte del antibiograma aun cuando se presente resistencia al antimicrobiano instaurado.
Ajustar el tratamiento antimicrobiano de acuerdo con el resultado del urocultivo y el antibiograma, en cuanto esté disponible, usando el antibiótico de espectro más estrecho posible.
Justificación de la recomendación:
E. coli es el microorganismo causal más frecuente tanto en IVU complicada como en la no complicada. Sin embargo, algunos factores como la presencia de anormalidades urológicas, instrumentación del tracto urinario, presencia de catéter urinario y comorbilidades influyen en una mayor prevalencia de otros microorganismos e infección polimicrobiana, entre ellos Klebsiella spp., Proteus spp., Serratia spp., Enterobacter spp., Pseudomonas spp, Enterococcus spp., Staphylococcus spp. y Candida spp32.
Actualmente las cefalosporinas de primera, segunda o tercera generación se consideran antibióticos de primera línea para el tratamiento de pielonefritis3,7,12,14,33-37 mostrando un adecuado perfil de seguridad y caracterizándose por alcanzar altas concentración a nivel renal38,39. Los datos de susceptibilidad antimicrobiana en Colombia se tuvieron en cuenta durante la formulación de estas recomendaciones40-46 (ver tabla 1. En Colombia, la amplia disponibilidad de cefalosporinas de primera y segunda generación en formas orales permite el cambio de la vía de administración de endovenosa a oral para dar continuidad del tratamiento de forma ambulatoria, facilitando así un egreso temprano Tabla 2, Figura 2 y Figura 3.
Tabla 1 Frecuencia de microorganismos causantes de IVU en Colombia.
| Aislamientos (%) | |||||||
|---|---|---|---|---|---|---|---|
| Bogotá 20 | 200641 | 2011- 201242 | Cali 201443 | Risaralda 201544 | Cartagena 201645 | Bucaramanga 2017- 201846 | |
| Escherichia coli | 88.9 % | 85.47% | 68.9% | 61.8% | 72.6% | 64.63% | 83% |
| Klebsiella spp. | 3.7% | 1.75% | 8.1% | 15.4% | 10.9% | 14.66% | 15% |
| Proteus spp. | 5.1% | 5.29% | 3.3% | - | 4.9% | 2.78% | 1% |
| Pseudomonas aeruginosa | - | 0.34% | 1.8% | 4.5% | 3.3% | 10.86% | - |
| Grupo SPACE ** | 2 % | 4.32% | 1.2% | 5.2% | 5.4% | 7.33% | 1% |
| Enterococcus spp. | - | - | 10.7% | - | 1.2% | 3.28% | - |
Los estudios registrados analizaron pacientes con IVU complicada y no complicada
Se Incluye: Serratia spp., Providencia spp., Morganella spp., Acinetobacter spp., Citrobacter spp. y Enterobacter spp.
Tabla 2 Antimicrobianos y dosis para el manejo de la IVU complicada
| Antimicrobiano | Dosis | Intervalo | Ajuste renal |
|---|---|---|---|
| Intravenosos | |||
| Cefazolina | 2 g | 8 horas | TFG < 50 ml/min |
| Cefuroxima sódica | 750 mg | 8 horas | TFG < 30 ml/min |
| Ceftriaxona | 2 g | 24 horas | No |
| Aztreonam | 1 g | 8 horas | TFG < 30 ml/min |
| Orales | |||
| Cefalexina | 1 g | 8 horas | TFG < 50 ml/min |
| Cefuroxima axetil | 1 g | 12 horas | TFG < 30 ml/min |
| Nitrofurantoína macrocristales | 100 mg | 6 - 8 horas | Contraindicado en TFG < 45 ml/min |
| Fosfomicina-trometamol | 3 g | Dosis única | Precaución en TFG < 10 ml/min |
De acuerdo a recomendaciones de expertos, si la resistencia local a quinolonas es mayor al 10% se debería limitar su uso como terapia empírica en infecciones urinarias3,47 De la misma forma, en cuanto a trimetoprim, estudios y recomendaciones en guías soportan no usar este grupo farmacológico empíricamente si la resistencia en la población es mayor al 20%. En contraste, en la actualidad no se ha descrito un umbral de resistencia en la población que lleve a la recomendación de no usar cefalosporinas como terapia empírica en el contexto de infección de vías urinarias.
Estudios realizados en población colombiana reportan tasas de resistencia de E. coli a fluoroquinolonas, trimetoprim/sulfametoxazol y ampicilina/sulbactam que superan el 20%, lo cual puede limitar la utilidad de estos antimicrobianos40-46,48-52. En cuanto al uso de trimetoprim sulfametoxazol, múltiples estudios sugieren que este fármaco tiene una incidencia de efectos adversos de 2 a 3 veces mayor en relación con la ofloxacina y la ciprofloxacina para el tratamiento de infecciones similares, principalmente efectos secundarios gastrointestinales y cutáneos53. En relación con el grupo de las fluoroquinolonas, es importante tener en consideración su utilidad en el tratamiento de la tuberculosis multidrogo resistente, por lo que se tiene especial prudencia en su uso con fin de disminuir el impacto en la selección de resistencia. Así mismo teniendo en cuenta las alertas de agencias regulatorias sobre el riesgo de eventos adversos discapacitantes relacionados al uso de este grupo farmacológico54,55, el consenso considera como punto de buena práctica no usar las fluoroquinolonas ni TMP/SMX de forma empírica para el tratamiento de la IVU complicada.
En relación con el uso de aminoglucósidos, este grupo de medicamentos muestran en general un adecuado perfil de susceptibilidad en microorganismos Gram negativos, sin embargo, su utilidad como primera línea de tratamiento empírico está limitada principalmente por aspectos de seguridad, dado el potencial riesgo de ototoxicidad y nefrotoxicidad, eventos adversos que restringen su uso en pacientes con comorbilidades como enfermedad renal, edad avanzada, o uso concomitante de otros nefrotóxicos o neurotóxicos56.
La resistencia a cefalosporinas de tercera generación relacionada con el aislamiento de microorganismos productores de beta lactamasas de espectro extendido (BLEE) es un problema en incremento. Los factores más relacionados con infecciones urinarias por microorganismos productores de BLEE incluyen el uso previo de antimicrobianos u hospitalización reciente, el uso de dispositivos urinarios, y la presencia de comorbilidades57-59. Aunque algunos instrumentos como el puntaje de Tumbarello y otros se han sugerido, su real utilidad para predecir la presencia de dicha resistencia en IVU en nuestro medio es baja60,61.
Existen datos que sugieren que la bacteriemia por microorganismos productores de BLEE se puede relacionar con peores desenlaces clínicos62, sin embargo, en el escenario de IVU la presencia de BLEE no se ha relacionado de la misma forma63. Estudios realizados en pacientes con IVU complicada no han reportado que el uso de una terapia antimicrobiana empírica inapropiada según el reporte de perfil de susceptibilidad se relacione con desenlaces adversos en cuanto a falla terapéutica o mortalidad a 30 días64, reportándose hallazgos similares en IVU bacteriémica65. Una revisión sistemática reciente que incluyó estudios observacionales de pacientes adultos con pielonefritis aguda adquirida en la comunidad por microorganismos productores de BLEE no encontró diferencia en los desenlaces de falla clínica o microbiológica, recurrencia, recidiva, estancia hospitalaria, ni mortalidad entre el manejo empírico no activo (principalmente ceftriaxona y cefuroxima) comparado con un tratamiento empírico activo (piperacilina/tazobactam y carbapenémicos) 66,67.
En el caso de Enterobacterales productores de AmpC cromo-sómica inducible (Ej. Enterobacter cloacae complex, Citrobacter freundii, K. aerogenes, etc), aunque se conoce el potencial de las cefalosporinas de tercera generación para generar desrepresión y posiblemente falla en el tratamiento, en el caso de infecciones urinarias esto no está establecido completamente. Algunos estudios con ceftriaxona han demostrado efectividad clínica equivalente comparada con agentes antipseudomonas68,69. En este sentido, en el escenario de IVU la resistencia reportada en el cultivo no debería ser el único determinante en la respuesta clínica al antimicrobiano. Algunos pacientes pueden responder favorablemente a pesar de un tratamiento empírico inapropiado y en caso que no, el reconocimiento y cambio oportuno de antimicrobiano de acuerdo con el antibiograma permitiría obtener un buen desenlace clínico independiente del perfil de resistencia70.
Estos datos sugieren que en pacientes hospitalizados se justifica limitar el uso de antibióticos de mayor espectro como los carbapenémicos, siendo las cefalosporinas una terapia empírica razonable. Localmente se tiene experiencia en el uso de cefalosporinas de primera y segunda generación como manejo empírico en pielonefritis complicada. Un estudio observacional en un centro de tercer nivel en Bogotá evaluó la terapia empírica con cefuroxima en adultos con pielonefritis encontrando que la terapia empírica inapropiada de acuerdo al cultivo no se asoció con una mayor estancia hospitalaria, o reingreso por pielonefritis71.
Para el caso de pielonefritis complicada, de acuerdo con la evidencia disponible, el grupo de consenso acordó como primera elección, el uso de cefalosporinas de primera generación, tomando en consideración el uso de cefuroxima para los casos en los que se hayan usado previamente antibióticos. Debe tenerse en cuenta que la determinación microbiológica de susceptibilidad a cefuroxima no es una práctica frecuente en el contexto local. La susceptibilidad a cefazolina puede emplearse como subrogado de la susceptibilidad a las cefalosporinas de segunda y tercera generación, y debe tenerse en cuenta que todos los aislamientos productores de BLEE son resistentes a cefalosporinas de primera y segunda generación72,73.
Reconociendo la poca disponibilidad de datos locales, el consenso consideró que en la población con pielonefritis relacionada con urolitiasis que requirió instrumentación de la vía urinaria alta y en pacientes con catéteres ureterales o nefrostomía, existe la posibilidad de mayor carga polimicrobiana y de resistencia, por lo que se generó la recomendación de manejo empírico con ceftriaxona en este grupo de pacientes61. A pesar de que se conoce que el uso de cefalosporinas de tercera generación puede tener un impacto en la selección de cepas productoras de BLEE, este no parece ser diferente con el uso de cefuroxima74.
Por otro lado, si el paciente tiene urocultivo previo en los últimos tres meses se justificaría dirigir el antimicrobiano según este aislamiento, dada la posibilidad de recaída o reinfección. Ertapenem ha sido estudiado como tratamiento inicial en infecciones urinarias complicadas, demostrando una eficacia similar a ceftriaxona75-77. Por lo tanto, en el caso de aislamiento previo de microorganismos BLEE en los últimos 3 meses, este antimicrobiano se considera una alternativa terapéutica adecuada.
Como punto de buena práctica se resalta entonces la indicación de toma urocultivo en pacientes con IVU complicada, con seguimiento de la respuesta clínica a las 48 horas y revisión del antibiograma para evaluar la necesidad de ajustar el tratamiento en caso de evolución tórpida. Teniendo en cuenta la evidencia disponible en pacientes con infección urinaria y tratamiento inapropiado (resultado resistente en el antibiograma al antimicrobiano instaurado), no parece haber un beneficio de ajustar el esquema antibiótico en pacientes con evolución favorable, y éste, si puede prolongar la estancia y dificultar el tratamiento ambulatorio por la necesidad de uso de medicamentos intravenosos. Por eso, si la evolución clínica es favorable, la conducta es continuar con el tratamiento antimicrobiano que ha sido exitoso, sin cambios y poder ajustar a la vía de administración oral.
En caso de una contraindicación para el uso de cefalosporinas como antecedentes de alergia grave, estudios sugieren aztreonam como una estrategia adecuada de manejo empírico por lo cual se sugirió como punto de buena práctica su uso en este contexto78.
En cuanto a la cistitis complicada, como alternativa a los betalactámicos se encuentran disponibles antibióticos como nitrofurantoína y fosfomicina trometamol, los cuales tienen un espectro antimicrobiano más estrecho, con un buen perfil de susceptibilidad para Enterobacterales y bajas tasas de resistencia local. Teniendo en cuenta lo anterior, el hecho de que las cefalosporinas no se consideren de primera elección en estos casos permitiría potencialmente disminuir el impacto de la resistencia de estos antibióticos79.
Se enfatiza que la nitrofurantoína y la fosfomicinatrometamol son medicamentos con indicación para el manejo exclusivo de IVU baja, los cuales por su pobre penetración renal no se encuentran indicados en los casos que exista sospecha de pielonefritis3,12,13. Adicionalmente, la nitrofurantoína no tiene indicación si existe sospecha de prostatitis, y tiene limitación en cuanto a la resistencia natural en Proteus spp. y P. aeruginosa y en pacientes con TFGe 45 ml/min13,80.
Adicionalmente, es importante calcular la TFGe para el ajuste de dosis de antimicrobianos, históricamente se ha usado Cockroft Gault que es un cálculo estimado de depuración de creatinina con el cual se han realizado la mayor parte de estudios de ajuste de medicamentos, sin embargo, en la práctica clínica actual se han usado las fórmulas de TFG CKD-EPI y MDRD con alguna correlación81, aunque su validación en pacientes de cuidado crítico es limitada. Se hace énfasis en que, independientemente de la fórmula a usar, su cálculo no es confiable en la evolución de una lesión renal aguda, por lo cual el ajuste del antimicrobiano se debería realizar de acuerdo con la TFGe basal.
Resumen de la evidencia
Para esta recomendación el grupo de consenso evaluó estudios realizados en pacientes con IVU complicada en el escenario intrahospitalario y ambulatorio. Se reconoce la limitación dada por pocos estudios disponibles, y la baja calidad de la evidencia de manera general. Adicionalmente algunas de las comparaciones en estudios de superioridad o no inferioridad incluyen antimicrobianos de amplio espectro, lo cual no se correlaciona con la práctica clínica habitual en la que generalmente estos antimicrobianos no se consideran como terapia empírica.
En el caso de cefalosporinas de primera generación, una revisión sistemática de ensayos clínicos en adultos con pielonefritis complicada incluyo un total de 6 estudios. Los comparadores fueron cefamicinas, cefalosporinas de tercera generación y quinolonas. Algunos estudios reportaron un mayor riesgo de falla microbiológica con cefalosporinas de primera generación, sin embargo, se encontró que la eficacia clínica fue similar a los comparadores, sin diferencia en los desenlaces de cura clínica, recaída y reinfección37.
Un ensayo clínico realizado por Pasiechnikov y colaboradres comparó el uso de ceftazidima frente a ciprofloxacina en pacientes adultos con pielonefritis aguda obstructiva, demostrando superioridad con el uso de la cefalosporina en el desenlace de cura clínica (RR 1.14, IC 95% 1.01 a 1.29) y microbiológica (RR 1.16, IC 95% 1.0 a 1.35) en pacientes a los que se les realizó nefrostomía; sin encontrar diferencias en los desenlaces de cura clínica ni microbiológica en pacientes que recibieron manejo con catéter ureteral (RR 1.17, IC 95% 0.97 a 1.40; RR 1.19, IC 95% 0.95 a 1.49, respectivamente). Sin embargo, se encontraron mayores eventos adversos en el grupo de fluoroquinolona (RR 3.0, IC 95% 1.73 a 5.21) 14,82.
Park y colaboradores compararon el uso de ertapenem frente a ceftriaxona en pacientes adultos hospitalizados con pielonefritis u otra IVU complicada sin encontrar diferencia estadísticamente significativa en cuanto a respuesta microbiológica (RR 0.99, IC 95% 0.88 a 1.12), ni eventos adversos (RR 2.39, IC 95% 0.95 a 6.02) 14,83. Otro estudio comparó dos clases de fluoroquinolonas (levofloxacina y ciprofloxacina) en pacientes adultos hospitalizados y no hospitalizados con pielonefritis y/o IVU complicada, sin encontrar diferencias en los desenlaces de eficacia y seguridad84.
Wagenlehner y colaboradores compararon el uso de ceftolozano tazobactam frente a levofloxacina en pacientes adultos con pielonefritis o IVU complicada, encontrando un efecto favorecedor del uso de ceftolozano tazobactam para el desenlace compuesto de cura clínica y microbiológica, con similares eventos adversos entre ambos medicamentos85. De manera similar, el estudio de Vázquez y colaboradores comparó ceftazidima/avibactam frente a imipenem cilastatina en pacientes hospitalizados con IVU complicada incluyendo pielonefritis, sin encontrar diferencias significativas en términos de eficacia y seguridad de ambos antibióticos86.
Es importante mencionar que existe información limitada sobre la frecuencia de los diferentes uropatógenos y el perfil resistencia para IVU complicada en nuestro medio. Los estudios clínicos son heterogéneos, representan en su mayoría muestras pequeñas y algunos de ellos no aportan información clínica que permita diferenciar el tipo de infección. De igual manera, en varios estudios no se informan o no son vigentes los parámetros utilizados para definir la resistencia o los puntos de corte utilizados de acuerdo con las recomendaciones del Instituto Americano de Estándares Clínicos y de Laboratorio (CLSI, por sus iniciales en inglés), lo cual limita su interpretación72,73,87. Los puntos de corte vigentes para la interpretación de la resistencia a cefazolina son diferentes en aislamientos urinarios con respecto a otras infecciones y estos fueron actualizados en 2014, debiéndose interpretar sensible un aislamiento urinario con MIC 16 mcg/mL o halo de inhibición 15 mm y resistente si tiene MIC 32 mcg/mL o halo de inhibición 14 mm70,71,82.
En general, los estudios muestran que el porcentaje de sensibilidad de E. coli en aislamientos urinarios es bajo para ciprofloxacina (57.1% a 86.0%), al igual que para sulfametoxazol (5.7% - 60.8 %) y para ampicilina/sulbactam (27.9%-87.5%).La mayoría de los estudios muestran un perfil adecuado de susceptibilidad para nitrofurantoína con reportes entre 78.8% y 97.12%, así como un adecuado perfil de susceptibilidad in vitro para fosfomicina con reportes entre 88% y 97%. La sensibilidad a aminoglucósidos en el caso de amikacina se encuentra entre 88.2% y 100% y gentamicina entre 71.5% y 92 3%40-42,44-46,48-52,88
Pregunta N° 3: ¿Cuál es la vía de administración del tratamiento antimicrobiano más adecuada en pacientes adultos con IVU complicada?
Recomendaciones:
Se sugiere como primera línea el uso de antimicrobianos orales, teniendo en cuenta la tolerancia a la vía oral, y la severidad de la infección (recomendación débil, evidencia de muy baja calidad).
En pacientes con tratamiento intravenoso, se sugiere revalorar a las 48 horas de inicio de la terapia antimicrobiana, para considerar la posibilidad del cambio a antimicrobiano oral (recomendación débil, evidencia de muy baja calidad).
Justificación de la recomendación:
La evidencia disponible no ha demostrado que los esquemas antimicrobianos orales sean inferiores a los esquemas intravenosos en cuanto a desenlaces clínicos. Si bien en los estudios no se reportan mayores diferencias en eventos adversos, el tratamiento intravenoso puede relacionarse con prolongación de la estancia hospitalaria y mayores costos asociados a la atención en salud89. Por lo anterior, se favorece la elección del tratamiento antimicrobiano oral como primera posibilidad, siempre y cuando el estado clínico del paciente permita su administración adecuada, y tomando en consideración la biodisponibilidad de las opciones terapéuticas disponibles.
En caso de que se inicien esquemas de tratamiento antimicrobiano intravenosos, se debe reevaluar la evolución clínica del paciente con el fin de realizar oportunamente el cambio de vía de administración a oral y de esta manera favorecer un pronto egreso hospitalario. Así mismo la aplicación de los medicamentos intravenosos en casa ha mostrado una reducción en los costos asociados a la atención en salud con desenlaces clínicos similares comparado con la continuación de manera intrahospitalaria90.
Resumen de la evidencia:
Para esta recomendación el grupo de consenso evaluó la revisión sistemática y metaanálisis de Pohl y colaboradores91, que incluyo 15 ensayos clínicos comparando cuatro esquemas de administración del tratamiento antimicrobiano: todo el esquema de tratamiento con antibióticos parenterales; todo el tratamiento con antibióticos orales; inicio del tratamiento parenteral con cambio a vía oral; o dosis única parenteral para continuar con tratamiento vía oral. Los estudios incluían pacientes con IVU complicada en el escenario intrahospitalario y ambulatorio y la duración de los esquemas de tratamiento varió entre 4-14 días.
Los principales antimicrobianos incluidos en los esquemas parenterales fueron amoxicilina/ácido clavulánico, ciprofloxacino, cefalosporinas de tercera generación (cefotaxima, ceftriaxona y ceftazidima) y aminoglucósidos (netilmicina, amikacina y gentamicina). Los esquemas orales fueron amoxicilina/ácido clavulánico, ciprofloxacino, cefixima y ceftibuteno.
En cuanto al cambio secuencial de antibiótico endovenoso a oral contra esquema completo endovenoso, no se encontraron diferencias respecto a los desenlaces de cura clínica (RR 1.01, IC 95% 0.94 a 1.1), cura microbiológica (RR 1.05; IC 95% 0.95 a 1.17), o eventos adversos (RR 0.85, IC 95% 0.19 a 3.83). La comparación del cambio secuencial de antibiótico IV a vía oral contra el esquema completo vía oral tampoco mostró diferencias en cura clínica o microbiológica (RR 1.00, IC 95% 0,98 a 1.02), ni en eventos adversos (RR0,96, IC 95%0,06 a 15.02).
Sólo uno de los estudios incluidos en la revisión sistemática comparó la administración del esquema completo vía parenteral frente a vía oral (aztreonam IM frente a norfloxacino oral) 92, reportando mayor cura microbiológica en el grupo de pacientes con esquema inyectable (RR 1.37, IC 95% 1.02a 1.84).
En la comparación de una dosis única inicial intramuscular previo al tratamiento oral, frente a todo el tratamiento vía oral, (ceftriaxona dosis única más trimetoprim oral frente a trimetoprim oral únicamente) 93, no se encontró diferencia para el desenlace de cura clínica o microbiológica (RR 0.97, IC 95% 0.81 a 1.17) y los eventos adversos reportados fueron similares. En cuanto a la comparación de tratamiento secuencial de antibiótico endovenoso a oral contra esquema de dosis única parenteral con continuación oral (94, 95), tampoco se encontró diferencia en la cura clínica y microbiológica (RR 1.00, IC 95% 0.98 a 1.02) o eventos adversos (RR 0.96, IC 95% 0.06 a 15.02).
Pregunta N° 4: ¿Cuál es la duración del tratamiento antimicrobiano más adecuada en pacientes adultos con IVU complicada?
Cistitis complicada:
Se sugiere que la duración del tratamiento con nitrofurantoína o cefalosporina sea de 5 días en mujeres postmenopáusicas. (recomendación débil, evidencia de muy baja calidad)
Se sugiere que la duración del tratamiento sea de 7 días en pacientes hombres o en pacientes con IVU baja asociada a catéter (recomendación débil, evidencia de muy baja calidad).
Se sugiere que el tratamiento con fosfomicina Trometa
mol sea administrado en una dosis única (recomendación débil, evidencia de muy baja calidad).
Punto de buena práctica:
• Considere extender la duración del tratamiento antimicrobiano en pacientes:
- Inmunosuprimidos.
- Presencia de colecciones aún no drenadas.
- Usuarios de dispositivos urinarios.
• No realizar urocultivo posterior a la finalización del tratamiento antimicrobiano en pacientes con respuesta clínica adecuada.
Justificación de la recomendación:
En los estudios clínicos que han comparado el uso de esquemas de tratamiento antimicrobiano cortos frente a esquemas largos en el contexto de la IVU complicada, en general, no se han documentado diferencias significativas para los desenlaces clínicos96-99. Una mayor duración del tratamiento antimicrobiano puede llevar a una exposición innecesaria de estos medicamentos, favoreciendo el desarrollo de eventos adversos, dentro de los que se deben considerar la presión selectiva y los cambios en la microbiota100. De la misma forma, esquemas prolongados también pueden derivar en menor satisfacción para el paciente y mayores costos para el sistema de salud101,102.
De acuerdo con el análisis de la evidencia disponible, el panel consideró adecuada para la mayoría de los casos de pielonefritis complicada una duración del tratamiento antimicrobiano de 7 días. En algunas situaciones, de acuerdo con el juicio médico se puede considerar extender el tratamiento antimicrobiano hasta máximo 10 días, teniendo en cuenta características del paciente como la presencia de anormalidades urológicas, el estado inmunológico, la gravedad y evolución del cuadro clínico.
En el escenario de la cistitis complicada, para el caso de mujeres postmenopáusicas, se estableció como recomendación una duración de 5 días para nitrofurantoína y cefalosporinas, considerando que existe poca información de esquemas de menor duración. En hombres y en pacientes con catéter urinario, teniendo en cuenta que tienen mayor complejidad en la vía urinaria se justificaría una duración de 7 días.
Si se opta por el uso de fosfomicina trometamol, la dosis única muestra ser suficiente, sin embargo, se resalta la importancia de la educación al paciente en la adecuada toma del medicamento, el cual se debe diluir en medio vaso de agua y tomar inmediatamente con el estómago vacío (al menos 2 horas separado de alimentos), al momento de acostarse y después de haber vaciado la vejiga103.
Adicionalmente, es importante mencionar que existe una población de pacientes con IVU complicada la cual no se encuentra representada en los estudios, entre estos se resaltan los individuos inmunosuprimidos, pacientes con colecciones no drenadas, y aquellos portadores de catéteres urinarios en quienes no se ha realizado el cambio o éste no es posible. En estos escenarios se justifica considerar una duración mayor del tratamiento de acuerdo al juicio clínico.
Como punto de buena práctica se aclara que el seguimiento en pacientes con IVU complicada se debería basar en la respuesta clínica y no en la respuesta microbiológica por lo cual no se indica la realización de urocultivo de control.
Resumen de la evidencia:
Para esta recomendación el grupo de consenso evaluó los estudios identificados entre los cuales se incluían pacientes con pielonefritis, cistitis complicada e infección asociada a catéter en los escenarios intrahospitalario y ambulatorio, encontrando en general evidencia de baja calidad.
La revisión sistemática y metaanálisis de EliakimRaz, et al. incluyó 8 ensayos clínicos que compararon la duración de 7 o menos días frente a más de 7 días en pacientes con pielonefritis y sepsis urinaria, utilizando fluoroquinolonas, trimetoprim/sulfametoxazol y betalactámicos, sin encontrar diferencias en los desenlaces de falla clínica (RR 0.63, IC 95% 0.33 a 1.18) y falla microbiológica (RR 1.16, IC 95% 0.83 a 1.62). Evidenciando solo en uno de los estudios incluidos en el análisis (en el cual más de 20% de pacientes presentaban una anormalidad urológica), un mayor riesgo de falla microbiológica (RR 1.78, IC 95% 1.02 a 3.10). Tampoco encontraron diferencias en eventos adversos ni mortalidad96.
La revisión sistemática y metaanálisis de Kyriakidou, et al. incluyó 4 ensayos clínicos en pacientes adultos con pielonefritis comparando esquemas de tratamiento de 7 a 14 días contra esquemas de 14 a 42 días. Se usaron grupos de antibióticos como fluoroquinolonas, trimetoprim/sulfametoxazol y beta-lactámicos, sin encontrar diferencias en cura clínica (RR 1.04, IC 95% 0.91 a 1.19), cura microbiológica (RR 0.93, IC 95% 0.63 a 1.37), o eventos adversos (RR 0.71, IC 95% 0.42 a 1.20) 14,97.
En cuanto a IVU asociada a catéter urinario, el ensayo clínico de Darouiche, et al. evaluó 55 pacientes adultos con lesión de la médula espinal hospitalizados por infección urinaria que portaban catéter transuretral o suprapúbico, comparando duración de 5 días del esquema antimicrobiano y cambio de catéter, frente a 10 días con mantenimiento del catéter. Los resultados de este estudio, evidenciaron no inferioridad del esquema corto comparado con el esquema largo para los desenlaces de cura clínica y cura microbiológica (RR 1.0, IC 95% 0.93 a 1.07; RR 0.92, IC 95% 0.74 a 1.15, respectivamente) 12; y una menor frecuencia de recurrencia de la infección con el esquema largo (HR 0.76, IC 95% 0.56 a 0.99) 98.
En cuanto al escenario de IVU baja, el estudio de Lutters et al. incluyó 15 ensayos clínicos en los que se analizó la población de mujeres mayores de 60 años, comparando tres esquemas antibióticos: dosis única, ciclo corto de tres a seis días y ciclo prolongado de siete a 14 días. Los antimicrobianos utilizados fueron fosfomicina-trometamol, trimetoprim/sulfametoxazol, cefalexina y fluoroquinolonas99. La dosis única no tuvo diferencias en el desenlace de falla clínica con respecto al tratamiento corto (RR 1.69, IC 95% 0.08 a 3.26) o prolongado (RR 1.94, IC 95% 0.68 a 5.57). En los pacientes que recibieron dosis única se evidenció un mayor riesgo de IVU persistente a corto plazo en comparación con el esquema corto (RR 2.01, IC 95% 1.05 a 3.84) y esquema prolongado (RR 1.93, IC 95% 1.01 a 3.70). Por otro lado, se evidenció una mayor preferencia de los pacientes por los esquemas de tratamiento de dosis única en comparación con esquemas prolongados (RR 0.73, IC 95% 0.60 a 0.88). La comparación entre el esquema corto (3-6 días) y largo (7-14 días) no mostró diferencias en los diferentes desenlaces de falla clínica (RR 0.98, IC 95% 0.62 a 1.54), ni eventos adversos (RR 0.87, IC 95% 0.26 a 2.93).
No se identificaron estudios económicos que permitan evaluar la costo efectividad de las diferentes opciones en el escenario colombiano. Se espera que la utilización de tratamiento oral facilite el egreso hospitalario y tenga un impacto favorable sobre los costos de atención en salud, adicionales a la mejor aceptación por parte de los pacientes. Para la fecha de la publicación de esta guía las distintas opciones presentadas se encuentran disponibles en el plan de beneficios en salud (PBS), por lo que se considera que su utilización no afectaría la equidad de las recomendaciones planteadas.
Pregunta N° 5: ¿Cuál es el manejo más adecuado del catéter urinario en pacientes adultos portadores de catéter urinario con IVU complicada?
Recomendaciones:
• Se sugiere retirar o cambiar el catéter urinario tan pronto como sea posible en pacientes con IVU asociada a catéter si éste ha estado puesto por más de 7 días (recomendación débil, evidencia de muy baja calidad).
Punto de buena práctica:
• No retrasar el tratamiento antimicrobiano en caso de no ser posible el retiro o cambio inmediato del catéter.
Justificación de la recomendación:
Teniendo en cuenta la evidencia disponible, se favorece la recomendación de realizar el cambio del dispositivo urinario en pacientes con IVU asociada a catéter, en la medida de lo posible, previo al inicio del tratamiento antimicrobiano. De acuerdo a consensos internacionales se acoge la indicación de realizar el cambio si el dispositivo se encuentra insertado por más de 7 días12.
Se resalta además la importancia de la adherencia a las recomendaciones para la prevención de infecciones del tracto urinario asociadas a catéteres urinarios teniendo en cuenta: uso apropiado del catéter, técnica aséptica durante la inserción y mantenimiento, y procurar su retiro temprano104, siempre reevaluando si la indicación del dispositivo urinario persiste.
Resumen de la evidencia:
En el ensayo clínico realizado por Raz et al. que incluyó 54 pacientes adultos mayores con IVU complicada, residentes en centros de cuidado crónico, con indicación de catéter urinario permanente, los pacientes recibieron manejo antimicrobiano con fluoroquinolonas y se evaluó el impacto clínico del cambio del catéter previo inicio del tratamiento antimicrobiano frente a el no cambio de catéter105. Con el cambio del catéter se evidenció una mayor tasa de cura a las 72 horas (RR 2.27, IC 95% 1.42 a 3.63) y a los 28 días (RR 1.5, IC 95% 1.07 a 2.11) 12. En el grupo de no cambio de catéter se reportaron 2 fallecimientos por urosepsis y ningún caso en el grupo a quienes se les cambió el dispositivo. Globalmente se consideró baja calidad de la evidencia.
Este aspecto se considera importante por la frecuencia de utilización de este dispositivo. Como en otras preguntas, no se identificaron estudios económicos ni información para realizar una evaluación de costo efectividad y equidad de la recomendación.
Implementación y actualización de la guía de práctica clínica
En las instituciones con atención de pacientes con IVU complicada se propone la implementación de la presente guía con el fin de apoyar las actividades de atención y los programas de optimización de antimicrobianos (PROA), considerando para su gestión la medición de los indicadores que se presentan en la tabla 3, con la frecuencia y obligatoriedad de reporte que cada institución considere pertinente.
Con el objetivo de facilitar la implementación de la presente guía, se emplearán como herramientas de difusión que faciliten su acceso a los profesionales de la salud, la publicación de la guía en la revista Infectio de la Asociación Colombiana de Infectología.
La actualización de la presente guía se considera debe realizarse en un plazo no mayor de 5 años, siguiendo la misma metodología y rigurosidad que se empleó para el desarrollo de la misma. Los temas podrán ser replanteados según la necesidad o aparición de nuevas evidencias que se deseen incluir en la guía.