Introducción
La interacción corazón y riñón ha sido motivo de estudio desde hace muchos años, donde se ha encontrado que existen conexiones entre estos dos sistemas y no habían sido consideradas como una patología independiente, solamente por las manifestaciones cardiovasculares y la presencia de albuminuria [1]. En el 2004, el Instituto Nacional del Corazón definió el síndrome cardiorrenal (SRC) como la retención del volumen renal que es exacerbada por la disfunción de la bomba cardiovascular [2] y, en la actualidad, esta comprensión ha mejorado, en la Conferencia de Consenso sobre Síndromes Cardiorrenales, bajo el auspicio de la Acute Dialysis Quality Initiantive (ADQI), se definió como la coexistencia de desórdenes entre el corazón y el riñón en la que la alteración de uno causa disfunción del otro de forma aguda o crónica [3].
Este mismo Consenso (ADQI) postuló la clasificación del SRC, que consistió en 5 estadios [3] que incluyen: tipo I (síndrome cardiorrenal agudo), tipo II (síndrome cardiorrenal crónico), tipo III (síndrome renocardiaco agudo), tipo IV (síndrome renocardiaco crónico) y tipo V (síndrome renocardiaco secundario a alguna enfermedad sistémica que ocasiona falla cardiaca (FC) y renal) [3-5].
Según María Rosa Costanzo [6], el 50 % de los pacientes con insuficiencia cardiaca tienen algún estadio de enfermedad renal crónica o agudizada menor a 60 ml/min/1,73 m2 y, asimismo, Borja Quiroga et al. [7] resaltan que la presencia de estas dos enfermedades se relaciona con una mayor morbimortalidad y un peor pronóstico en los pacientes, aunque existen guías de manejo de insuficiencia cardiaca (IC) y enfermedad renal, tanto aguda como crónica [8-11], en la actualidad, no hay guías consensuadas de manejo para el SRC, por lo que el manejo debe ser óptimo para disminuir la congestión venosa y la sobrecarga hídrica mediante los diuréticos, medicamentos inotrópicos o vasodilatadores que potencien la función cardiaca, los inhibidores de la angiotensina (ARA2) o los inhibidores de la enzima convertidora angiotensina (IECA) y la neprilisina [12-14].
El objetivo del presente estudio es determinar la frecuencia de síndrome cardiorrenal tipo II junto con las características sociodemográficas y clínicas de los pacientes.
Materiales y métodos
Tipo de estudio y población: se realizó un estudio observacional, descriptivo y retrospectivo. La población que se incluyó fueron los pacientes con FC atendidos en el hospital San Rafael de Tunja, Colombia, en el periodo consistente entre el 06 de mayo del 2018 y el 21 de noviembre del 2021 (aprobado por el comité de investigación de la institución, acta N.° 9-2019-04).
Muestra: el cálculo del tamaño de la muestra se realizó con Epi-Info versión 7.2, donde se tomó una población de 3850 pacientes según los datos de esencia, prevalencia del 16,4 % de síndrome cardiorrenal, intervalo de confianza (IC) del 95 %, margen de error del 5 % y pérdidas estimadas del 10 % de las 357 historias, donde se obtuvo un cálculo del tamaño de la muestra de 347 historias clínicas en total, además, los pacientes fueron seleccionados mediante muestreo aleatorio simple.
Criterios de selección: se analizó a todos los pacientes hospitalizados con FC en historias clínicas completas que fueron atendidos entre los años 2018 y 2021, excluyendo a todas las personas con información faltante (variables incompletas).
Recolección de los datos: se hizo partícipe a los pacientes que presentaron la patología en estudio, los cuales fueron identificados mediante el código internacional de enfermedades (CIE-10). La valoración se realizó mediante la revisión de las historias clínicas, registrando la información en una base de datos integrada por las variables demográficas, clínicas y diagnósticas y los antecedentes, para la correspondiente evaluación y el análisis de las variables propuestas y así dar respuesta a los objetivos establecidos en este proyecto.
Diagnóstico del SRC en pacientes con FC: se presenta en un tercio de los hospitalizados por insuficiencia cardiaca (IC) aguda, donde puede ocurrir en el contexto de enfermedad crónica de uno o ambos órganos. La lesión renal aguda se define por los criterios KDIGO 2012 (elevación de creatinina sérica [CS] ≥ 0,3 mg/dl dentro de 48 h o ≥ 50 % del valor inicial dentro de siete días) [14].
Variables: se identifican las siguientes:
• Variables demográficas: sexo y procedencia.
• Variables antecedentes: hipertensión arterial (HTA), diabetes mellitus (DM), enfermedad pulmonar obstructiva crónica (EPOC), hipotiroidismo, antecedente familiar y personal de infarto agudo de miocardio (IAM), accidente isquémico transitorio (AIT), enfermedad cerebrovascular (ECV), síndrome de apnea obstructiva del sueño (SAHOS), tromboem-bolia pulmonar (TEP), trombosis venosa profunda (TVP), hiperlipidemia y obesidad.
• Variables clínicas: fracción de eyección del ventrículo izquierdo (FEVI), Stevenson y New York Heart Association (NYHA).
• Variables diagnosticas: hallazgos ecocardiográficos; hipertrofia del ventrículo izquierdo (HVI); hipertensión pulmonar; insuficiencia mitral, tricúspidea y aórtica; dilatación del ventrículo derecho; dilatación aurícula derecha e izquierda y hallazgos radiológicos: car-diomegalia; hipertensión pulmonar; edema pulmonar; derrame pleural; infiltrados alveolares bibasales; infiltrados intersticiales bibasales y borramiento de los hilios pulmonares.
Análisis estadístico: se creó la base de datos en formato Excel, versión 2013, y se analizó en el paquete estadístico SPSS versión 22, donde se incluyeron las variables descritas. El análisis univariado se realizó por medio de un estudio estadístico descriptivo a la población seleccionada, donde se determinaron frecuencias absolutas y relativas en las variables categóricas.
Sesgos: el sesgo de información que encontramos durante la ejecución de la investigación fue que había registros clínicos incompletos o ausentes, por lo que se incluyeron los pacientes con información completa.
Resultados
Características demográficas
Se incluyó a 347 pacientes, donde el 20,17 % eran procedentes de zonas urbanas, el 6,34 % de zonas rurales, el 16,13 % eran de sexo masculino y el 10,37 % de sexo femenino (tabla 1).
Antecedentes personales y familiares
HTA (21,61 %), DM (9,79 %), EPOC (8,64 %), hipotiroidismo (7,49 %) y antecedentes personales de IAM (4,03 %) fueron los antecedentes que predominaron (tabla 1).
Tabla 1 Caracterización demográfica y antecedentes de los pacientes con síndrome cardiorrenal
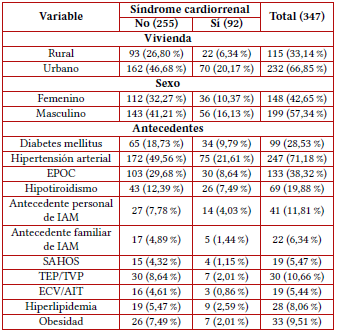
Notas aclaratorias: abreviaturas: EPOC: enfermedad pulmonar obstructiva crónica, IAM: infarto agudo de miocardio, Sahos: síndrome apnea obstructiva del sueño, TEP: tromboembolia pulmonar, TVP: trombosis venosa profunda, ECV: enfermedad cerebrovascular y AIT: accidente isquémico transitorio (AIT).
Fuente: elaboración propia.
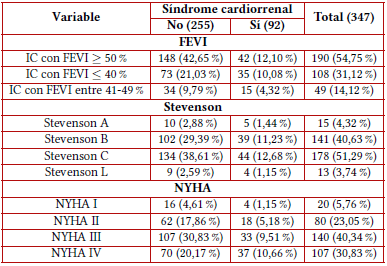
Variables clínicas en síndrome cardiorrenal
En cuanto a la caracterización clínica, el 12,10% de los pacientes cursaron IC con FEVI mayor o igual al 50 % y 10,08 casos con FEVI menor al 40 %. La estratificación según la clasificación de Stevenson mostró que el 12,68 % estaban en estadio C y el 10,66 % presentaron clase funcional NYHA IV, en comparación con las demás variables (tabla 2).
Diagnóstico: hallazgos imagenológicos
Basados en el criterio clínico y el requerimiento, a 21,32 % pacientes se les realizó un eco-cardiograma transtorácico y a 10,37 % una radiografía de tórax, donde los hallazgos ecocardiográficos más frecuentes fueron: valvulopatías (18,73 %) insuficiencia tricúspide (16,71 %), insuficiencia mitral (14,69 %), hipertensión pulmonar (14,69 %) y HVI (14,12 %). En la radiografía de tórax, 5,76 % pacientes presentaron cardiomegalia, 2,59 % infiltrado de alveolares bibasales, 2,30 % infiltrados intersticiales bibasales y 2,30 % derrame pleural (tabla 3).
Discusión
Este estudio observacional descriptivo y analítico evaluó algunas variables clínicas e imagenológicas encontradas en el SRC, estratificando los resultados en dos grupos, los que eran sometidos y a los que no se les realizaban ayudas diagnósticas, encontrando que las alteraciones de la pared o la función cardiaca fueron las más frecuentes y este hecho permite, en una vista general, estimar el pronóstico y la sobrevida de los pacientes con SRC para ser intervenidos oportunamente y así evitar peores desenlaces.
Tabla 3 Caracterización diagnóstica
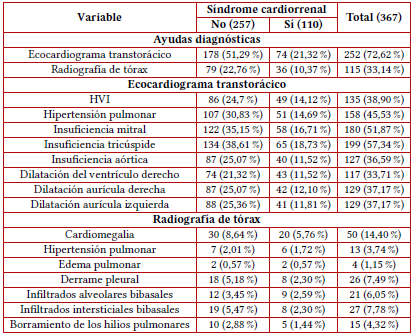
Nota aclaratoria: abreviatura: HVI: hipertrofia del ventrículo izquierdo.
Fuente: elaboración propia.
El SRC comprende una gama de alteraciones bidireccionales complejas entre el corazón y los riñones, el daño inicial de uno causa la disfunción y el deterioro del otro, donde alguno de estos órganos sistêmicos activa los mecanismos homeostáticos compensatorios que repercutirán en el consiguiente [13,14].
La enfermedad renal y la cardiaca son afecciones frecuentes, Hatamizadeh [15] describe que la prevalencia en el mundo de la enfermedad renal es de al menos un 9 % y que su incidencia es 2-3/1000 habitantes/año, mientras que la IC es más prevalente, se estiman 64 millones de casos en el mundo; mientras que para Bell et al. [16], la relación entre estas dos entidades patológicas aún no se ha comprendido complemente y continúa siendo un reto para los profesionales de la salud.
Se cree que el 30-50 % de los individuos con insuficiencia cardiaca crónica (ICC) desarrollan enfermedad renal crónica (ERC), dando un peor pronóstico en los pacientes. En una revisión realizada por House et al. [17], la incidencia de IC "de novo" en ERC es del 17-21 % y el desarrollo de la IC está influenciado por el estadio de la ERC, por tanto, esta relación aumenta la mortalidad por causa cardiovascular y por hospitalización en la FC con fracción de eyección ventricular preservada o reducida (HFpEF-HFrEF), sobre todo en aquellos sometidos a terapia dialítica. Un informe anual del año 2020 en Estados Unidos [18] encontró que el 44% de los individuos que estaban en terapia dialítica cursaban con IC, donde el 10 % tenían HFrEF, 13 % con HFpEF y 21 % de causa desconocida.
Es importante describir los múltiples procesos fisiopatológicos involucrados del SRC, así, se describen tres principales [18]: en hemodinámico comprenden la presión venosa intraabdominal (PIA) aumentada, la cual puede causar hipertensión intraabdominal (PIA > 12 mmHg) y, en casos graves, producir síndrome compartimental abdominal (PIA > 20 mmHg), exacerbando el daño cardiorrenal por influencia del gasto cardiaco disminuido que causa liberación de renina, retención de sodio, aumento de la congestión venosa y empeoramiento de la injuria renal [19].
La desregulación neurohormonal está dada por el sistema renina-angiotensina-aldosterona y la activación excesiva del sistema nervioso simpático, lo cual causa reabsorción de sodio y solutos, este último es secundario a cambios entre la presión oncótica e hidrostática de los túbulos renales [20] y, por último, los mediadores inflamatorios, si bien conocemos en la ICC y la ERC, existen estados inflamatorios crónicos mediados por citoquinas proinflamatorias como el factor de necrosis tumoral alfa y la interleucina-1 y 6 que causan muerte celular y fibrosis, deteriorando la función de estos dos órganos [21,22].
Los mêtodos diagnósticos imagenológicos más utilizados en el presente estudio fueron: radiografía de tórax y ecocardiograma transtorácico. El aumento de silueta cardiaca, infiltrados alveolares, derrame pleural e infiltrados intersticiales fueron los hallazgos radiológicos más frecuentes y entre los hallazgos principales del ecocardiograma transtorácico estaban: insuficiencia tricúspide y mitral, hipertensión pulmonar, HVI y dilatación del ventrículo derecho. Alprecht-Quiroz et al. [23] describen que las principales alteraciones del sistema cardiovascular por SRC son HVI (71 %), valvulopatías y cardiopatía isquêmica, a diferencia con lo encontrado en este estudio, donde el ventrículo izquierdo es el más comprometido.
El SRC es una entidad clínica que ha sido objeto de estudio para ayudar a comprender la relación patológica entre estos dos órganos, Damman et al. [24] reunieron 28 estudios que incluían un total de 49.890 individuos con IC aguda o crónica agudizada, donde el 23 % presentó empeoramiento de la función renal (EFR) y a los 1,5 años el EFR se asoció a una mayor mortalidad (OR: 1,75; IC 95 % 1,47-2,08; p < 0,001), sin embargo, el riesgo de mortalidad aumentó en quienes padecían ICC (OR: 1,96; IC 95% 1,48-2,61; p < 0,001). Al compararse con este estudio, la prevalencia es mayor en los pacientes con función sistólica conservada, donde se infiere que el SRC es una condición clínica heterogênea, influenciada por factores de riesgo como hipertensión arterial, diabetes mellitus, IAM y EPOC, que intervienen en el deterioro funcional de cada órgano [25-27], como también se evidencia en los resultados descritos.
Limitaciones
Al ser un estudio retrospectivo, se encontraron historias con falta de registros, lo cual se controló incluyendo a la población que tuviera información completa. Al tratarse de un estudio observacional no permite establecer asociaciones de causalidad o pronóstico, además que no se contaban con algunos biomarcadores de congestión por su característica retrospectiva.
Conclusión
El síndrome cardiorrenal es una afectación de origen multicausal, donde la presentación clínica dependerá del órgano causante de la disfunción, además, típicamente los pacientes con esta entidad han cursado con alguna descompensación que genera ingresos a hospitalización, cambios en su calidad de vida y un peor pronóstico, siendo la retención del volumen el principal proceso involucrado en el proceso fisiopatológico de la enfermedad, deteriorando las funciones del corazón y el riñón.