Introducción
La enfermedad renal en etapa terminal (ESRD, por sus siglas en inglés) es un problema de salud pública importante, cuya incidencia aumenta a una tasa del 5 % cada año. En 2011, la prevalencia de pacientes con ESRD en hemodiálisis (HD) fue de 388.000 en Estados Unidos, con un costo por persona calculado en 87.945 dólares estadounidenses [1]. Para el 2014, se reportaron al menos 400.000 pacientes con ESRD que requerían hemodiálisis más de tres veces por semana y que consumían anualmente más de 40 mil millones de dólares. Estas cifras cobran mayor importancia al considerar que, cuanto más tiempo están los pacientes en hemodiálisis, lograr y mantener el acceso vascular se vuelve más difícil y desafiante para los servicios de salud [2].
Para los pacientes con ESRD, la hemodiálisis es sin duda una terapia que salva vidas. Los métodos disponibles para su realización incluyen el uso de accesos arteriovenosos en extremidades (a través de fístula arteriovenosa o injerto arteriovenoso) y el uso de catéteres de diálisis tunelizados. La primera opción es una fístula arteriovenosa de vaso nativo en extremidad superior, la cual se asocia con mejores morbilidad y mortalidad [3,4], sin embargo, la presencia de vasos nativos deficientes o de enfermedad oclusiva venosa central condiciona a opciones limitadas y progresivamente reducidas en pacientes con ESRD de larga data [5].
Además, la obstrucción venosa central ocurre en más del 50 % de los pacientes en hemodiálisis y lleva a una morbilidad significativa para esta frágil población, que con frecuencia presentan obstrucción de las venas axilar, subclavia, innominada o vena cava superior [6], por lo que estos pacientes tienen también mayor riesgo de complicaciones como trombosis, bacteriemia y mayor mortalidad, además del alto costo que implica el manejo de estas complicaciones [7].
El dispositivo de injerto Hemodialysis Reliable Outflow, más conocido como HeRO® (Merit Medical), ha surgido como una posible solución para pacientes con opciones limitadas para diálisis. Es un sistema de acceso vascular permanente y de disposición subcutánea en el cual el radiólogo intervencionista juega un papel fundamental [5]. Dicho dispositivo, disponible en nuestro medio, puede ser usado para crear un nuevo acceso, "rescatar" un acceso fallido y también para tratar los síntomas asociados con hipertensión venosa severa del miembro superior [8].
Materiales y métodos
Se realizó una búsqueda sistemática en la literatura de los estudios publicados sin limitación de idioma, con el in de obtener una mayor sensibilidad y arrojar mayores resultados en la búsqueda, usando las bases de datos electrónicas de Medline, Lilacs y Europe PMC hasta el 25 de agosto del 2022.
Las palabras utilizadas para la búsqueda fueron: "Renal Insufficiency, Chronic", "Dialysis", "Renal Dialysis", "Hero Graft access Device" y "Hero graft". La estrategia de búsqueda fue realizada por dos autores (DJ y JJC), se revisaron los abstract de los artículos, se incluyeron artículos de revisión, metaanálisis, ensayos clínicos, reportes y series de caso. Cada autor analizó los artículos publicados disponibles para incluirlos dentro de la revisión de la literatura y en aquellos en los que hubo discrepancia para elegir, se realizó un consenso entre los autores para llegar al acuerdo de si incluirlos o no.
Fórmula de búsqueda: ((hero graft) OR (Hero Graft access Device)) AND (((("Hemodialysis, Home"[Mesh]) OR (Renal Dialysis"[Mesh])) OR ("Dialysis"[Mesh])) OR (Renal Insufficiency, Chronic"[Mesh])).
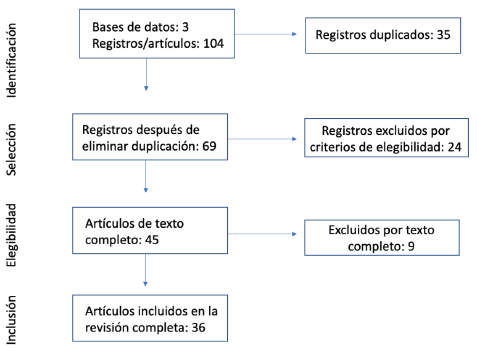
Los criterios de inclusión utilizados dentro de la revisión sistemática se basaron en metaanálisis, estudios de costo-efectividad y experiencia en el seguimiento de pacientes con el dispositivo. Los criterios de exclusión utilizados fueron: artículos involucrados con la técnica de inserción, artículos que no tuvieran relación con el tema de revisión y, por último, artículos basados en el diseño del dispositivo. Se incluyeron 36 artículos (figura 1) y, en la revisión exhaustiva de la literatura disponible, el grupo de autores se centró en tres ítems relacionados con el uso del injerto HeRO®:
Resultados
1. Primera pregunta: ¿cuáles son las indicaciones y el papel del injerto HeRO® en la práctica clínica?
El injerto HeRO® se introdujo en ensayos clínicos en 2004 [8,21] con la aprobación de la FDA (Food and Drug Administration) en 2008 para pacientes con enfermedad renal crónica en hemodiálisis catéter-dependientes y con estenosis venosa central u oclusión [9]. Este injerto permite un flujo de sangre arterial continuo hacia el sistema venoso central, haciendo un bypass en la estenosis, además, este dispositivo híbrido tiene dos componentes, un injerto y un componente de flujo venoso. El primero es anastomosado por cirugía vascular a la arteria braquial ipsilateral y tunelizado subcutáneamente. Por su parte, el componente venoso es puesto de manera percutánea por radiología intervencionista en la aurícula derecha a través de la vena subclavia o de la vena yugular interna, componente que posteriormente se tuneliza hacia el injerto con el fin de evitar la estenosis central [7,10] (figura 2).
En el estudio de Davis et al. [11], el injerto HeRO® se colocó preferentemente en el brazo derecho, esto debido a que el recorrido hacia la fosa supraclavicular y la vena cava superior es menos tortuoso en comparación con el lado izquierdo. El brazo izquierdo se usó cuando el pulso estaba disminuido en el derecho.
Recomendaciones en las guías de enfermedad renal crónica
El uso de este dispositivo ha venido en aumento durante la última década [12]. La National Kidney Foundation/Kidney Disease Outcomes Quality Initiative (Kdoqi) ha proporcionado pautas basadas en la evidencia para el acceso vascular para hemodiálisis desde 1996. En sus últimas guías de práctica clínica para el acceso vascular del 2019, recomienda el uso del HeRO® como alternativa en aquellos casos en los que se han agotado todas las opciones de acceso arteriovenoso en las extremidades superiores y la expectativa de vida del paciente incluye terapia con HD por más de 1 año [13].
El dispositivo HeRO® es una opción para el acceso de hemodiálisis en el paciente con oclusión de la vena central y puede ser en algunas ocasiones la única alternativa a la dependencia del catéter [11] (figura 3A y 3B).
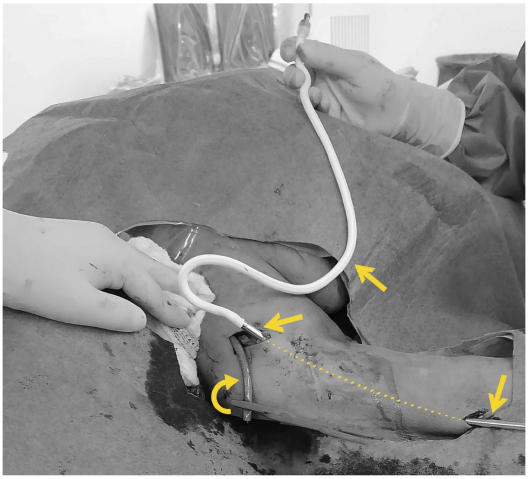
Notas aclaratorias: el injerto que se anastomosará a la arteria braquial (flechas rectas), tunelizado por el tejido celular subcutáneo del brazo (punteado) y el componente de flujo venoso con acceso percutáneo en el cuello a través de la vena yugular interna (flecha curva).
Fuente: elaboración propia.
Figura 2 Foto que muestra los dos componentes del injerto HeRo®
2. Segunda pregunta: ¿cuál es la evidencia relacionada con la costo-efectividad del uso del injerto HeRO®, además de su viabilidad en el contexto colombiano?
Dageforde et al. [5] realizaron un modelo de análisis de decisión para evaluar tres métodos distintos para accesos de diálisis en estadio terminal, en función de desenlaces y costos: el dispositivo de injerto HeRO®, catéteres de diálisis tunelizados y, por último, los injertos en extremidades inferiores. El dispositivo HeRO® fue el acceso menos costoso, con un valor promedio al año de 6521 dólares americanos, comparado con los catéteres de diálisis tunelizados (8477 dólares americanos) y con los injertos en miembro inferior (9567 dólares americanos) [5].
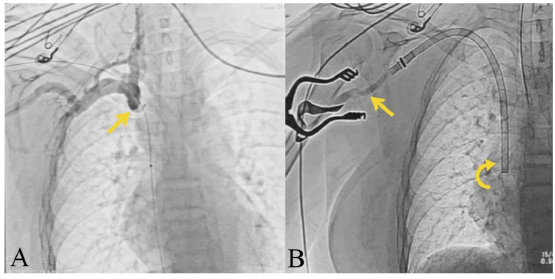
Notas aclaratorias: para la figura 3B: el injerto anastomosado a la arteria braquial (flecha recta) y el componente de flujo venoso con extremo distal en la aurícula derecha a través de la vena yugular interna (flecha curva).
Fuente: elaboración propia.
Figura 3 A. Cavografía que demuestra oclusión crónica de vena cava superior (flecha) y B. imagen de fluoroscopia que muestra los dos componentes del injerto HeRo®
Otros estudios han observado una disminución de costos en hasta un 23 % por año al comparar el uso de injertos HeRO® versus catéteres de diálisis tunelizados [2,8,14,15]. El costo bruto del dispositivo HeRO® es más alto que las otras alternativas, pero la baja incidencia de complicaciones y su mayor efectividad hacen que este sea sin duda más costo-efectivo [16]. El modelo de análisis de decisiones creado por Dageforde et al. [5] encontró que la inserción de catéteres de diálisis tunelizados era menos costosa en la población de pacientes si la tasa de infección era menor al 16 %, sin embargo, cuando la probabilidad de infección asociada al catéter de hemodiálisis era mayor, encontraron que HeRO® sería menos costoso.
En la búsqueda realizada, aún no hay información disponible sobre la costo- efectividad en países latinoamericanos. Una vez haya mayor experiencia en nuestra región, convendría realizar estudios de investigación que permitan obtener conclusiones claras acerca de la pertinencia de HeRO® en comparación con las demás alternativas de accesos vasculares para HD en términos de costos.
3. Tercera pregunta: ¿cuáles son las ventajas, las desventajas y las posibles complicaciones relacionadas con el uso de HeRO®?
Ventajas: tanto el HeRO® como el injerto arteriovenoso en miembro inferior han demostrado ser similares en permeabilidad, tasas de infección y mortalidad. Estos estudios se han diseñado para comparar la seguridad y la eficacia del injerto HeRO graft® en una cohorte de pacientes sin oclusiones de la vena central o estenosis, sin embargo, el HeRO® puede tener su mayor aplicabilidad en este subconjunto de pacientes [17]. La ventaja del HeRO® sobre el injerto arteriovenoso en miembro inferior está en la habilidad de mantener el acceso en miembro superior con un drenaje venoso de la vena cava superior [18-20]. Otros estudios han mostrado que las tasas de complicaciones (trombosis, infección, bacteriemia y mortalidad) con el dispositivo HeRO® han sido menores que con las otras técnicas [21, 22].
En un estudio hecho por Nassar et al., los investigadores argumentan que prefieren los injertos HeRO® sobre los injertos arteriovenosos del miembro inferior en sus pacientes dependientes de catéteres para preservar las opciones de acceso de las extremidades inferiores en el futuro. También argumentan que HeRO® es su acceso de diálisis preferido en pacientes con obesidad y enfermedad vascular periférica [17].
Debido a que HeRO® proporciona un acceso arteriovenoso totalmente subcutáneo a largo plazo que evita la oclusión, atraviesa la estenosis y además disminuye el riesgo de colonización de los demás dispositivos, podría considerarse como una solución a las altas tasas de infección en pacientes que dependen del catéter por estenosis del flujo de salida venoso [23]. En un estudio realizado por Kudlaty et al. [24], encontraron que la tasa de infección en los pacientes con injerto arteriovenoso en miembro inferior fue del 29 %, casi el doble de la reportada para HeRo®. Así, el injerto de miembro inferior tiene otras consideraciones importantes como el riesgo de isquemia y la amputación de la extremidad [5].
El injerto HeRO® también se puede anastomosar directamente a un injerto o fístula arteriovenosa con el in de salvar el acceso, lo que se ha visto que mejora el edema del brazo en presencia de una estenosis de la vena central. En estos pacientes que se presentan con una estenosis venosa central, tanto el despliegue del stent central como la conversión del acceso a un injerto HeRO® son alternativas para resolver la inflamación que se presenta en el brazo. Los datos del estudio de Cline et al. [25] sugieren que la conversión a un injerto HeRO® incurre en una menor incidencia de hinchazón recurrente y da como resultado tasas de permeabilidad de acceso más prolongadas, con menos intervenciones para mantener la permeabilidad secundaria [25].
El uso de una estrategia de implantación de HeRO® por etapas no resultó en un mayor riesgo de infección en comparación con la técnica de implantación primaria convencional de HeRO®, donde la técnica de implantación HeRO® por etapas se utilizó para pacientes con un catéter venoso central tunelizado preexistente, por lo tanto, el uso de un catéter de hemodiálisis tunelizado existente para el acceso venoso intraoperatorio para el injerto HeRO® es una estrategia eficiente y segura [26].
Torrent et al. [14] evaluaron retrospectivamente a 41 pacientes y mostraron una tasa de permeabilidad primaria a los 6 y 12 meses de 30,4 % y 8,4 %, respectivamente. La tasa de permeabilidad secundaria a los 6 y 12 meses fue del 81,6% y 53,7%, respectivamente, requiriendo 2,84 procedimientos por injerto HeRO®. Estas tasas de permeabilidad informadas son sustancialmente más bajas que las del ensayo multicéntrico de 164 pacientes, en el cual se observó una tasa de permeabilidad primaria y secundaria de 12 meses del 60 % y el 90,8 %, respectivamente, con 1,5 procedimientos requeridos por injerto HeRO® por año [19].
El síndrome de robo, caracterizado por una reducción del flujo de sangre arterial de la extremidad como resultado de un "robo" de flujo por parte del injerto o fístula, puede ocurrir hasta en un 20 % de los pacientes con injertos arteriovenosos, siendo más común en los accesos proximales que en los distales. Con el HeRO® se ha reportado una tasa de esta complicación en solo el 1,4 % de los pacientes portadores [19,27].
Kensinger et al. [2] destacan que los injertos HeRO® deben considerarse solo como opciones de hemodiálisis de rescate en pacientes con ESRD. Por otro lado, Glickman et al. [28] sugieren considerar este dispositivo en pacientes que se someterán a diálisis durante más de 3 o 5 años, ya que proporciona tasas de permeabilidad similares a los injertos de miembros superiores y mantiene la estructura de estos.
En cuanto a la calidad de vida de los pacientes, Wasse et al. [29] demostraron que los pacientes con injertos tenían una mejor calidad de vida que aquellos portadores de catéteres de diálisis tunelizados, sin embargo, no hay diferencias en términos de calidad de vida entre los injertos usados en miembro superior (incluyendo HeRO®) y aquellos localizados en extremidad inferior [5].
En otro escenario donde el HeRo® ha mostrado utilidad es en los pacientes con insuficiencia intestinal que dependen del acceso venoso central para recibir nutrición parenteral, se ha visto que los catéteres venosos centrales de larga duración se asocian con complicaciones potencialmente mortales, incluidas infecciones y trombosis que dan lugar a múltiples intercambios de líneas y al desarrollo de estenosis u oclusión venosa central progresiva, las cuales limitan el acceso venoso convencional o aumentan el riesgo de complicaciones relacionadas con el catéter y amenazan la vida. Por ello, se ha encontrado que intervenir más temprano, antes del desarrollo de la patología venosa central con la formación de un acceso periférico arteriovenoso, puede reducir las infecciones del torrente sanguíneo asociadas al catéter, ayuda a evitar la patología central y a preservar el acceso venoso, al tiempo que facilita la administración de nutrición parenteral de una manera más eficiente que catéteres centrales tunelizados tradicionales [30].
Riesgos y desventajas: a pesar de todas las ventajas presentadas, hay algunos inconvenientes del dispositivo HeRO®. Su inserción puede requerir, por ejemplo, un catéter de hemodiálisis puente mientras se logra la canulación del HeRO®, lo que puede llevar a una mayor carga de infección. Yoon et al. [31] describieron una técnica novedosa en la que se puede evitar tener que hacer ese puente con el catéter de hemodiálisis y realizar una canulación inmediata, disminuyendo así la tasa de infección y la mortalidad en estos pacientes [32].
La trombosis del injerto es una complicación reportada con alguna frecuencia, debido probablemente a hipotensión e hipovolemia posterior a la diálisis. Es por lo anterior que, para mantener un adecuado flujo del injerto, se debe tener una fracción de eyección mayor al 20 % y una presión arterial sistólica de al menos 100 mmHg [9]. De igual forma, suele prescribirse clopidogrel para los pacientes en riesgo como manejo antiagregante plaquetario [33].
Wallace et al. [8] reportaron un éxito técnico del 86 % (de 21 HeRO®) y las fallas reportadas estuvieron relacionadas con la ausencia de acceso venoso central secundario a la oclusión. De los implantes exitosos, el 38 % presentó algún tipo de complicación: 4 síndromes de robo, 1 hematoma en brazo, 2 muertes de causa no filiada y 2 casos de bacteriemias relacionadas al HeRO®. De igual forma, se requirieron aproximadamente 3 reintervenciones al año para mantener la permeabilidad del dispositivo [8].
Hay otro estudio donde se reportaron complicaciones en algunos dispositivos como estenosis y trombosis, esta última más frecuente que en las fístulas arteriovenosas. En este estudio, realizado por Gebhard et al. [34], se hicieron 73 intervenciones percutáneas en 26 dispositivos HeRO® que estaban disfuncionales con estenosis o trombosis, a los cuales se les realizaron trombectomías, teniendo como resultado un aumento en la permeabilidad primaria y permeabilidad secundaria de los mismos.
Cuando existe una estenosis venosa central bilateral de las extremidades superiores, las opciones de acceso arteriovenoso se vuelven mucho más limitadas. A veces, se puede tolerar una fístula distal si las colaterales venosas centrales son buenas, pero a menudo se deben considerar soluciones como un acceso arteriovenoso en las extremidades inferiores o el dispositivo HeRO®. Para algunos autores como Ladenheim et al. [35], en estos casos, la fístula arteriovenosa autógena transpuesta de arteria femoral superficial a vena femoral (SFA-tFV, por sus siglas en inglés) se ha convertido en el acceso de elección debido a los hallazgos encontrados en su estudio, donde no solo se encontró una permeabilidad primaria y secundaria significativamente mayor de la SFA-tFV en comparación con el injerto HeRO®, sino también cinco veces menos intervenciones para mantener la permeabilidad con la SFA-tVF, esto sugiere que para los pacientes más jóvenes con obstrucción venosa central, se debe considerar primero el SFA-tFV. Aunque los injertos HeRO® pueden extender el uso de la extremidad superior, los injertos de muslo brindan una opción más duradera para la hemodiálisis crónica, por lo que el injerto HeRO® puede ser una mejor opción para los pacientes con una expectativa de vida limitada, ya que se ven menos afectados por su menor permeabilidad y para aquellos reacios a aceptar la morbilidad del acceso a las extremidades inferiores [35,36].
Katzman et al. [22] sugieren algunas recomendaciones para reducir el riesgo de bacteriemia como posible complicación durante el periodo de puente del dispositivo HeRO®:
Realizar hemocultivos antes de la implantación del HeRO® para identificar infecciones asintomáticas.
Realizar un cultivo de la punta del catéter tunelizado de diálisis cuando sea removido y tratar de acuerdo con el aislamiento.
Evitar colocar el dispositivo HeRO® en lugares previamente infectados.
Iniciar antibióticos profilácticos durante el periodo perioperatorio, con base en la historia de bacteriemia del paciente.
Considerar la aplicación de antibiótico tópico en el sitio de salida del catéter tunelizado de diálisis.
Canular el dispositivo HeRO® y remover el catéter tunelizado de diálisis que está sirviendo como puente tan pronto como sea posible.
Discusión
Experiencia con el injerto HeRO® en Colombia
A la fecha se han realizado algunos casos en ciudades como Bogotá, Popayán, Cali y Medellín con resultados técnicos y clínicos satisfactorios, según informa Juan Serna, gerente de producto de Merit Medical. Muchas instituciones avanzan actualmente con los protocolos respectivos para que se avale la introducción de esta nueva alternativa como parte del arsenal terapéutico en los pacientes que tienen la indicación clínica adecuada.
Específicamente en la ciudad de Bogotá, instituciones como la Clínica Reina Sofía con el doctor Juan Agustín Varela, el Hospital San Carlos con el doctor Michael Ricardo y la Clínica Nogales con el doctor Juan Manuel Aguilar, han tenido éxito técnico, sin complicaciones asociadas al procedimiento en el corto plazo y una experiencia similar reportó el doctor Jorge Felipe Tobar en Popayán. Aún no se conoce el seguimiento a largo plazo de estos pacientes, sin embargo, el futuro del dispositivo es alentador según la experiencia observada en el último año, anota el señor Serna.
Conclusión
Los resultados de calidad a largo plazo del injerto HeRO® determinarán su importancia como acceso vascular. Este dispositivo ofrece una nueva forma de evitar los riesgos fatales asociados con la dependencia del catéter, a largo plazo, y requiere de una cuidadosa selección de pacientes, conocimientos y habilidades en cirugía e intervención endovascular, y de la gestión de expertos en diálisis para mejorar y mantener los resultados esperados con este nuevo dispositivo. La realización de ensayos clínicos adicionales, el mantenimiento de un registro de pacientes y la promoción para la actualización de equipos interdisciplinarios de acceso vascular son objetivos necesarios para obtener resultados de calidad adicionales para los pacientes. Así, serán ellos quienes tendrán la última palabra sobre el futuro del injerto HeRO® y su lugar en la historia del acceso vascular para hemodiálisis [29].