Introducción
La injuria renal aguda (IRA) que se desarrolla posterior a la exposición a un medio de contraste yodado (MCI) es un desorden iatrogénico de gran relevancia clínica, el cual se erige como la potencial complicación que genera mayor temor en el personal del área de salud que se desempeña en la práctica de imágenes médicas con fines diagnósticos y terapéuticos. A través del tiempo, se han utilizado diferentes términos para definirla, sin que exista uniformidad, asumiendo en su mayoría una relación causal no demostrable y sin excluir con certeza otras probables causas de IRA; esto ha llevado a que se prefiera, actualmente, usar términos que no impliquen causalidad y que tengan en cuenta todas las condiciones concomitantes, como el término "injuria renal aguda asociada al uso de medios de contraste yodado" (IRA-ACI).
Otro aspecto fundamental que presenta profundos cambios a través del tiempo es la determinación de la frecuencia real de presentación de esta entidad, ya que los primeros estudios ubicaban a los medios de contraste como la tercera causa de IRA en el contexto intrahospitalario, solo superada por la hipovolemia y la cirugía mayor; sin embargo, estos no contaban con diseños metodológicos que permitieran controlar adecuadamente los sesgos, por lo que no era posible establecer conclusiones derivadas de sus resultados. Por ello, y con el propósito de controlar las variables de confusión, se han desarrollado estudios de puntuaciones de propensión que permiten un mayor control de dichas variables y obtener datos más ajustados a la realidad. De igual forma, pese a que se han citado múltiples factores de riesgo para el desarrollo de la IRA-ACI, solo la reducción de la tasa de filtración glomerular estimada (TFGe) ha logrado demostrar ser un factor de riesgo independiente.
Son muchas las estrategias farmacológicas que se han utilizado con el objetivo de prevenir el desarrollo de IRA en pacientes que van a ser sometidos a procedimientos radiológicos con MCI. La mayoría de estas terapias se han derivado del conocimiento de mecanismos fisiopatológicos, ensayos clínicos no controlados y estudios con escasa población; con los nuevos ensayos con mayor rigor metodológico y un mayor tamaño de muestra, algunas estrategias que mostraron algún tipo de beneficio en estudios previos, pueden no mostrar alguno e incluso, de forma paradójica, efectos deletéreos sobre la función renal.
El presente documento consenso de la Asociación Colombiana de Nefrología e Hipertensión Arterial (Asocolnef) y la Asociación Colombiana de Radiología (ACR) sobre recomendaciones basadas en la evidencia de IRA-ACI es el primero, en toda la historia de Colombia, que logra congregar estas dos asociaciones científicas con el propósito de orientar a todo el personal del área de la salud que interviene en el manejo de pacientes que ameritan el uso de MCI, en procedimientos diagnósticos o terapéuticos, dando pautas y recomendaciones a implementar antes, durante y después de la aplicación del MCI, con el objetivo de reducir el riesgo de IRA-ACI.
Materiales y métodos
Objetivo
Generar recomendaciones basadas en la evidencia para el uso de MCI en pacientes sometidos a procedimientos radiológicos de tipo diagnóstico y terapéutico, a través de un consenso de expertos.
Población incluida
Pacientes sometidos a procedimientos diagnósticos o terapéuticos que requieren el uso de MCI, independientemente de su edad.
Aspectos clínicos
Recomendaciones referentes a la definición, la epidemiología y los factores de riesgo para el desarrollo de IRA-ACI, además, se evalúan estrategias de protección renal y escalas de riesgo que pueden ser usadas en la práctica clínica.
Usuarios
Médicos generales, especialistas en Medicina Interna, Nefrología, Radiología, Hemodinamia, entre otras y profesionales de la salud involucrados en la atención de los pacientes que requieren uso de medios de contraste.
Metodología
Las preguntas de interés fueron elaboradas por el grupo coordinador conformado por los presidentes de las asociaciones, un líder desarrollador de la guía y dos epidemiólogos expertos en la metodología; fueron seleccionados según las necesidades basadas en la experiencia de los profesionales expertos en el tema y soportados por la revisión de literatura.
Grupo desarrollador
Se elaboraron preguntas de interés por el grupo coordinador conformado por el presidente de la Asocolnef, el presidente de la ACR, un nefrólogo-epidemiólogo y dos metodólogos (epidemiólogos clínicos). Se convocaron 10 especialistas (5 nefrólogos, 4 radiólogos y 1 nefrólogo pediatra), teniendo en cuenta su experiencia clínica y su trayectoria académica y, finalmente, 9 especialistas (4 nefrólogos, 4 radiólogos y 1 nefrólogo pediatra) respondieron al llamado y culminaron el proceso de revisión. Se procuró una participación de las diferentes regiones de Colombia: Eje Cafetero, Oriental, Caribe, Pacífico y Centro. Todos los participantes manifestaron no tener conflictos de interés.
Tabla 1 Equipo desarrollador
| Papel en la elaboración de la guía | Participante | Perfil profesional | Agremiación/ Institución |
|---|---|---|---|
| Líder | Marcelo Aguirre Caicedo, Quibdó | Médico/internista/nefrólogo/ epidemiólogo/ultrasonido e intervencionismo/máster en Patología Renal/Gerencia en Seguridad Social y Proyectos de Salud | - Coordinador del Comité de Intervencionismo y Medios de Contraste - Miembro del comité de la Asociación Colombiana de Nefrología e Hipertensión Arterial (Asocolnef) - Miembro del Comité de Nefrología Intervencionista de la Sociedad Latinoamericana de Nefrología -SLANH - Miembro de ISN-ACP- ACMI - Director médico de Nefrochocó, Quibdó |
| Experto clínico | Luis Alberto Cruz Vásquez, Medellín | Médico/radiólogo/radiología intervencionista | - Presidente de la Asociación Colombiana de Radiología (ACR) - Radiólogo intervencionista Hospital General de Medellín - Clínica las Vegas - EMMSA - IN CARE - Centro Médico Buenos Aires |
| Experto clínico | Cesar Restrepo Valencia, Manizales | Médico/internista/nefrólogo | - Expresidente de la Asociación Colombiana de Nefrología e Hipertensión Arterial (Asocolnef) - Profesor titular de la Universidad de Caldas |
| Experto clínico | Amaury Ariza, Cartagena | Médico/internista/nefrólogo/estadística aplicada/: Maestría en Epidemiologia Clínica y Bioética | - Miembro de la junta directiva de la Asociación Colombiana de Nefrología e Hipertensión Arterial (Asocolnef) - Profesor de la Universidad de Cartagena |
| Experto clínico | Martha Edith Oyuela Mancera, Bogotá | Médica/radióloga/ bioética y epidemiología/: Maestría en Economía de la Salud y Farmacoeconomía | Miembro de la junta directiva nacional de la Asociación Colombiana de Radiología (ACR) - Profesor asociado de la Universidad de La Sabana - Profesor asociado de la Pontificia Universidad Javeriana - Profesor asociado de la Universidad del Norte - Profesor asociado de la Universidad del Rosario - Jefe del servicio de imágenes diagnósticas del Instituto Roosevelt |
| Experto clínico | Theo Martínez Mera, Popayán | Médico/internista/nefrólogo | Miembro de la Asociación Colombiana de Nefrología e Hipertensión Arterial (Asocolnef) |
| Experto clínico | Juan Manuel Pérez Hidalgo, Bogotá | Médico/radiólogo | Médico radiólogo de la Asociación Colombiana de Radiología (ACR) - Fundación Cardioinfantil - La Cardio |
| Experto clínico | Pedro Abad Díaz, Medellín | Médico/radiólogo/imagen cardiaca | - Médico radiólogo de la Asociación Colombiana de Radiología (ACR) - Línea de radiología cardiovascula r - SURA |
| Experto clínico | Richard Baquero, Medellín | Médico/pediatra/nefrólogo pediatra | - Expresidente de la Asociación Colombiana de Nefrología pediátrica (Asoconepe) - - Profesor de la Universidad de Antioquia |
| Líder metodológico | Anderson Bermón Angarita, Bucaramanga | Médico/: Epidemiología/PhD en Epidemiologia y Bioestadística | - Epidemiólogo de la Fundación Cardiovascular de Colombia (FCV) |
| Experto metodológico | José Arnoby Chacón, Manizales | Médico: Microbiología Médica | - Profesor de la Universidad de Caldas |
Fuente: elaboración propia.
Preguntas clínicas
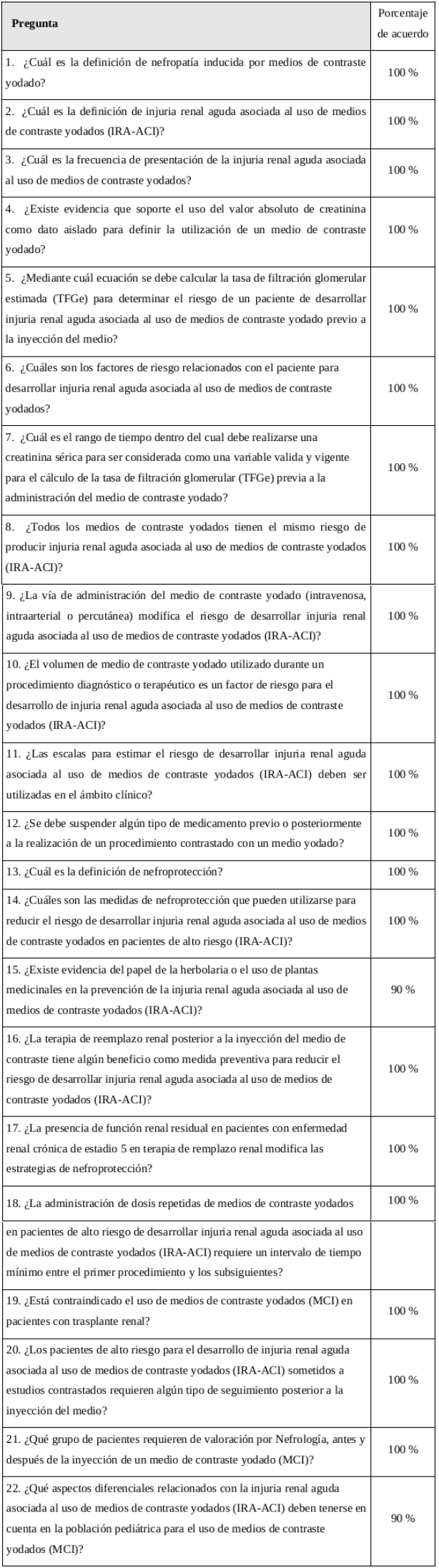
Fueron planteadas por el grupo de investigación teniendo en cuenta la disparidad de conceptos detectados en la experiencia, la relevancia clínica, las implicaciones en la seguridad del paciente, la existencia de barreras de acceso a intervenciones o procedimientos y la optimización de recursos del sistema de salud. Las preguntas con el resumen de las respuestas dadas en el consenso se describen en el anexo A.
Búsqueda de la evidencia
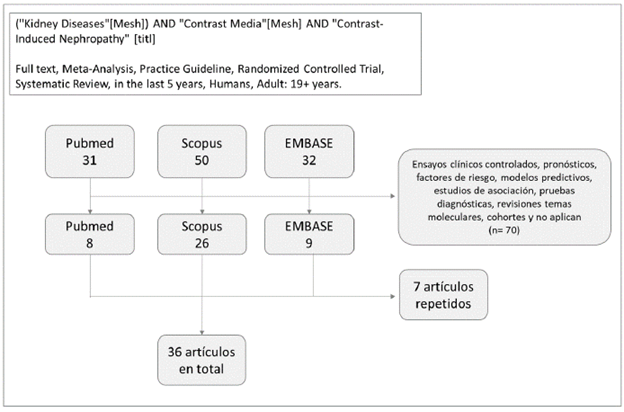
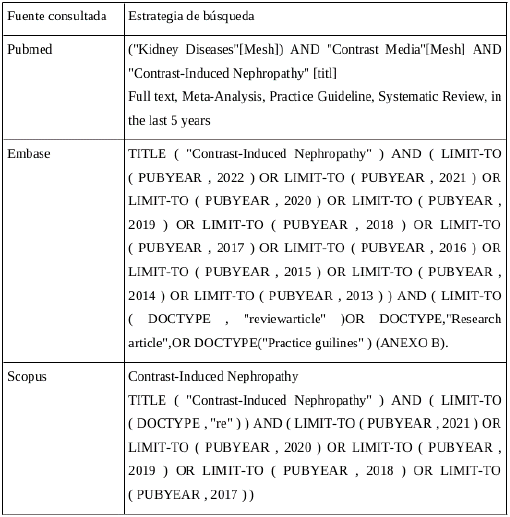
Se realizó una validación de las revisiones obtenidas en diferentes bases de búsqueda (anexo B), tales como PubMed, Scopus y Embase. Se utilizó como palabra clave principal o palabra incluida en el título: ("Kidney Diseases"[Mesh]) AND "Contrast Media"[Mesh] y se usaron como filtros: Full text, Meta-Analysis, Practice Guideline, Systematic Review, in the last 5 years, Humans, Adult: 19+ years. Para Scopus, Embase y Scielo se utilizó la siguiente estrategia de búsqueda: TITLE ( "Contrast-Induced Nephropathy" ) AND ( LIMIT-TO ( PUBYEAR, 2022 ) OR LIMIT- TO ( PUBYEAR , 2021 ) OR LIMIT-TO ( PUBYEAR , 2020 ) OR LIMIT-TO ( PUBYEAR , 2019 ) OR LIMIT-TO ( PUBYEAR , 2018 ) OR LIMIT-TO ( PUBYEAR , 2017 ) OR LIMIT- TO ( PUBYEAR , 2016 ) OR LIMIT-TO ( PUBYEAR , 2015 ) OR LIMIT-TO ( PUBYEAR , 2014 ) OR LIMIT-TO ( PUBYEAR, 2013 ) ) AND ( LIMIT-TO ( DOCTYPE , "review article" )OR DOCTYPE "Research article" OR DOCTYPE("Practice guidelines").
Tamización y selección de la evidencia
Un total de 113 artículos fueron identificados y evaluados desde el título y el resumen de manera independiente por dos revisores: un experto clínico y uno metodológico. Se descartaron 70 artículos por no cumplir con los criterios de inclusión para la revisión de revisiones basados en la Amstar-2 para revisiones sistemáticas de la literatura, donde 7 estaban repetidos entre las bases de datos. Finalmente, 36 artículos fueron distribuidos entre los evaluadores.
Los artículos revisados se presentan en el anexo C, discriminando su nivel de evidencia según la escala de Oxford (Ref).
Recomendaciones preliminares
Con los artículos recolectados y orientados por las preguntas de investigación se realizó una síntesis narrativa para cada pregunta y se plantearon recomendaciones basadas en las condiciones propias de la práctica clínica, según la experiencia de cada especialista clínico.
Consenso formal de expertos
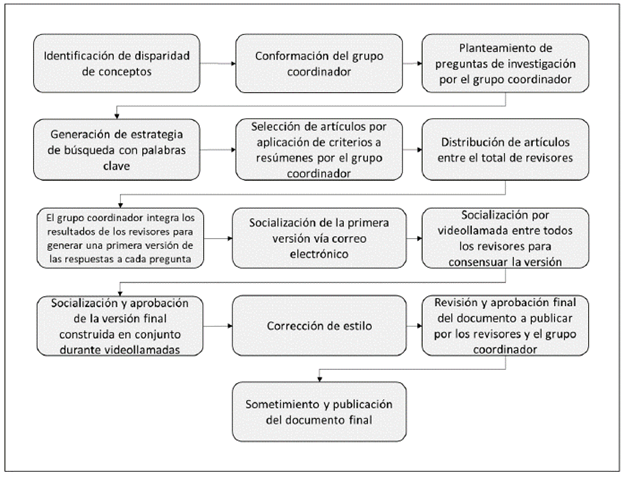
Los 36 artículos fueron distribuidos entre 8 revisores. Se identificaron 4 artículos con relevancia temática que fueron evaluados por todos los revisores, los 32 artículos restantes fueron distribuidos al azar. Una vez se contó con el total de respuestas, el comité coordinador las unificó y realizó una síntesis narrativa, la cual fue presentada inicialmente vía correo electrónico a todos los revisores y, posteriormente, se hicieron reuniones por medio de videollamadas para correcciones y revisiones al documento. Una vez se contó con el aval del total de especialistas, se realizó una versión que fue sometida a corrección gramatical y de estilo, para posteriormente ser revisada por los participantes del consenso y, luego de tener en cuenta las observaciones de los participantes, se realizó la revisión final del documento (figura 2) (anexo D).
Graduación de las recomendaciones
El grupo coordinador registró el acuerdo de los especialistas por cada una de las preguntas durante las discusiones del método Delphi, donde se evaluó y registró el nivel de acuerdo entre todos los participantes, siendo de 100 % el acuerdo entre todos los especialistas al finalizar las discusiones de cada pregunta (anexo E). Además, las recomendaciones fueron soportadas por la literatura encontrada y se categorizaron según el grado de recomendación usada en las guías del NHS.
Resultados
1. ¿Cuál es la definición de nefropatía inducida por medios de contraste yodados (NIC)?
La IRA en pacientes expuestos a MCI permitió inferir una relación causal: medio de contraste - desarrollo de IRA, debido a ello se acuño el término "Nefropatía inducida por medios de contraste" (NIC), sin embargo, dicha causalidad no estaba probada, por lo que esta definición no es acorde con la realidad; de igual forma, se utilizó el término "lesión" renal aguda sin que se contara con un biomarcador propiamente dicho de lesión (la creatinina no es un marcador de lesión renal) o evidencia histológica de la misma [1].
A través del tiempo se han utilizado diferentes términos (basados en múltiples criterios clínicos y de laboratorio) para definir la injuria renal que se desarrolla después del uso de MCI, valores absolutos o relativos (porcentuales) de creatinina y, en algunos casos, variables clínicas como cambios en el volumen urinario, al igual que una línea de temporalidad no uniforme. Por otro lado, en muchos casos se exigía la exclusión de otra causa de IRA, hecho que en la práctica clínica es poco probable.
Dentro de las definiciones más relevantes podemos contar:
Mehran et al. en 2004 la definieron como un incremento de la Crs > 0,5 mg/dL o > 25 % dentro de 48 h [2].
En 2004, la European Society of Urogenital Radiology (ESUR) lo definió como un incremento de la Crs > 0,5 mg/dl o > 25 % dentro de 72 h [3].
El Blue Cross Blue Shield of Michigan Cardiovascular Consortium (BMC2) lo catalogó como un incremento de la Crs ≥ 0,5 mg/dL [4].
Improving Global Outcomes (KDIGO) - Clinical practice guideline for acute kidney injury lo clasificó como un aumento de bajo grado, pero constante en la SCr en el transcurso de varios días (> 1,5 veces el valor inicial dentro de 7 días), un aumento repentino de la SCr en el periodo inmediato posterior a la exposición a MCI (> 0,3 mg/dl dentro de las 48 h) y el desarrollo de oliguria (volumen urinario < 0,5 ml/kg/h durante > 6 h) [5].
Esta heterogeneidad en las definiciones se refleja en los resultados tan disimiles en los estudios clínicos, en aspectos fundamentales como la frecuencia de presentación, la estimación del riesgo y la mortalidad asociada al uso de MCI.
Conclusión: el uso del término "Nefropatía inducida por medios de contraste yodado" debe restringirse solo a aquellos casos donde se excluya de forma exhaustiva cualquier otro factor de riesgo que pueda estar implicado en el desarrollo de IRA, hecho que en la práctica clínica no es fácilmente alcanzable, por lo que su uso es limitado.
2. ¿Cuál es la definición de IRA-ACI?
IRA posterior a la exposición a MCI en pacientes en los que coexisten factores a los cuales podría atribuirse, de forma independiente, el desarrollo de la IRA: relacionados con el paciente (edad, enfermedad renal crónica (ERC), diabetes mellitus y disfunción ventricular izquierda, entre otros) y factores relacionados con el procedimiento (por ejemplo, embolización de material ateromatoso de la aorta durante la manipulación del catéter, hipotensión y sangrado) [6].
El término "asociación" se refiere a la relación entre la exposición al medio de contraste y el desarrollo de IRA, sin que ello implique necesariamente causalidad. Este término podría aplicarse a aquellas situaciones en las que no se pueden excluir, de forma concluyente, otras causas de IRA.
Conclusión: recomendamos utilizar el término "Injuria renal aguda asociada al uso de medios de contraste yodado (IRA-ACI)" en aquellos escenarios clínicos donde coexista cualquier otro factor de riesgo que pueda estar implicado en el desarrollo de IRA.
Tabla 2 Definición de términos
| Término | Definición | Comentario |
|---|---|---|
| Nefropatía inducida por contraste (NIC) | Incremento en CrS absoluto (>0,5 mg/dl) o relativo (>25 %) de la CrS, con respecto a la basal después de la exposición al medio de contraste [2]. | Término acuñado en la literatura antigua que implica causalidad no probada y temporalidad no uniforme (24 - 72 h). |
| IRA | Incremento de Crs ≥ 50 % dentro de 7 días o un aumento repentino de la Crs (>0,3 mg/dl dentro de 48 h) y el desarrollo de oliguria (volumen urinario <0,5 ml/kg/h durante ≥ 6 h) [5]. | Definición global de IRA. |
| IRA poscontraste | IRA posterior a la exposición a MCI [7]. | Hace referencia a la cronología y no a una relación causa-efecto. |
| IRA inducida por contraste | IRA posterior a la realización de un estudio con medios de contraste, al cual podría atribuirse el desarrollo del daño renal. Se define como un aumento de bajo grado pero constante en la Crs en el transcurso de varios días (>1,5 veces el valor inicial dentro de 7 días), un aumento repentino de la Crs en el periodo inmediato posterior a la exposición a CM (>0,3 mg/dl dentro de 48 h) y el desarrollo de oliguria (volumen urinario <0,5 ml/kg/h durante ≥ 6 h) (5). | Se asume que el medio de contraste causó la injuria renal sin que se documente una relación de causalidad. Para establecer la presencia de un vínculo causal entre la exposición al medio de contraste y la IRA, es necesaria una evaluación detallada que descarte otras causas potenciales de IRA, sin embargo, el no encontrar una etiología alternativa a la exposición al MCI en el desarrollo de la IRA, no establece causalidad de manera inequívoca. |
| IRA-ACI | IRA posterior a la exposición a MC en pacientes en los que coexisten factores a los cuales podría atribuirse, de forma independiente, el desarrollo de la IRA: relacionados con el paciente (edad, ERC, diabetes mellitus y FEV, entre otros) y factores relacionados con el procedimiento (por ejemplo: embolización de material ateromatoso de la aorta durante la manipulación del catéter, hipotensión y sangrado) [6]. | El término "asociación" se refiere a la relación entre la exposición al medio de contraste y el desarrollo de la IRA, sin que ello implique necesariamente causalidad. Este término podría aplicarse a aquellas situaciones en las que no se pueden excluir, de forma concluyente, otras causas de IRA. |
Fuente: elaboración propia.
3. ¿Cuál es la frecuencia de presentación de la IRA-ACI?
Durante mucho tiempo se ha considerado de forma casi incuestionable el inherente potencial nefrotóxico de los medios de contaste yodados, sin embargo, una serie de recientes estudios observacionales, que cuentan cada vez con mayor rigor en sus diseños metodológicos y análisis estadísticos, no encontraron evidencia de una relación causal entre los MCI y la IRA. Esta considerable evidencia nos incita a cometer la osadía, por primera vez en la historia, de cuestionar la existencia de una IRA posterior a la exposición de MCI y, por ende, determinar su frecuencia.
Desde sus primeras descripciones, la incidencia de la IRA posterior a la exposición a MC ha sido difícil de determinar: la heterogeneidad en sus definiciones, las diferentes características fisicoquímicas de los MCI, la presencia de múltiples factores concomitantes con potencial nefrotóxicos y las distintas vías a través de las cuales son administrados los MCI a los pacientes, explican la gran variabilidad en dichos resultados.
Los primeros estudios ubicaban a los MC como la tercera causa de lesión renal aguda (LRA) en el contexto intrahospitalario, solo superada por la hipovolemia y la cirugía mayor. Estos datos derivaban de centros hospitalarios donde utilizaban MC de alta osmolalidad (hoy no utilizados), no tenían en cuenta otras condiciones concomitantes desencadenantes de IRA y la vía arterial era la más utilizada, por lo que su validez era cuestionable [8]. Paradójicamente, algunos estudios encontraron un menor riesgo de IRA en pacientes sometidos a procedimientos con contraste, en comparación con aquellos en los que las exploraciones se realizaban sin el empleo de MC, lo que refleja el sesgo de selección en lugar de cualquier efecto nefrotóxico derivado del MC [9]. Para hacer más difícil aún la determinación de la verdadera frecuencia de presentación de IRA-ACI, más de una cuarta parte de los pacientes hospitalizados pueden cursar con elevaciones de creatinina sérica (CrS) sin exponerse a un MCI [10]. En un estudio, Bruce et al. evidenciaron una alta incidencia de LRA entre los sujetos del grupo de control sometidos a una tomografía axial computarizada (TAC) sin medio de contraste y la incidencia de elevación de la CrS en este grupo fue estadísticamente similar a la del grupo que recibió MC iso-osmolal [11]. Otro aspecto que puede explicar el amplio espectro en los datos de incidencia de IRA-ACI es el hecho de que los pacientes que reciben MC están generalmente más enfermos que aquellos que no lo reciben; por el contrario, los pacientes con disminución de la TFGe o aquellos pacientes percibidos por sus médicos como con un mayor riesgo de IRA (personas mayores, ERC de base o diabetes mellitus) pueden tener menos probabilidades de ser sometidos a estudios con MCI [12]. En el estudio más grande realizado hasta la fecha (5.922.537 pacientes), Wilhelm-Lee et al. evaluaron la incidencia de IRA pos-administración de MCI: los pacientes a los que se les administró y no se les administró MCI desarrollaron IRA en 5,5 % vs. el 5,6 %, respectivamente, asociándose la administración de MCI a un OR para IRA de 0,93 (IC 95%, 0,88-0,97) [13]. En este estudio es muy poco probable concluir que el MCI "protege" a los pacientes expuestos a MCI de desarrollar IRA, más bien, esta paradoja podría explicarse por el hecho de que a aquellos pacientes cuyos médicos consideran que tienen el mayor riesgo de IRA, se les trata de tal manera que se minimiza el riesgo percibido.
Al utilizar las palabras claves "medio de contraste" e "insuficiencia renal", predeterminando como límite de tiempo los años de 1996 al 2004, Rao y Newhouse [12] evaluaron 3081 artículos, de los cuales dos hechos llamaron su atención: solo 40 artículos (1,3 %) incluían pacientes que recibieron MC intravenosos, en tanto que solamente 2 tenían grupos control de pacientes que no recibieron MC y eran relativamente pequeños [14, 15], por lo que los datos obtenidos de estos no derivaban de fuentes con un riguroso diseño metodológico.
Por razones éticas, se dificulta la realización de ensayos clínicos aleatorizados que permitan establecer una relación de causalidad entre exposición o intervención y resultado, por ello y con el propósito de controlar las variables de confusión, se han desarrollado estudios de puntuaciones de propensión. Las puntuaciones de propensión son una herramienta estadística que permite manejar el sesgo de confusión que inevitablemente surgirá en estudios epidemiológicos observacionales y, por lo tanto, posibilitan el obtener una identificación aproximable de los efectos causales (pero no igual) a la lograda con los Ensayos Clínicos Aleatorizados (ECA) [16]. Cabe recordar que estos estudios solo incluyen los sesgos conocidos y las covariables obtenidas de una base de datos, lo que los diferencia de los ECA, donde los sesgos y los factores de confusión desconocidos sí se tienen en cuenta; sin embargo, dicho tipo de estudios no ha logrado demostrar una relación causal concluyente entre el MC y el desarrollo de IRA y, de igual forma, tampoco demuestran una mayor incidencia de IRA en pacientes expuestos a MC con respecto a los que no [9,17].
Goulden et al. condujeron un estudio con el objetivo de determinar si la exposición intravenosa (IV) al MCI en pacientes sometidos a angiograma pulmonar tomográfico compu-tarizado en el servicio de urgencias estaba asociada con una insuficiencia renal a largo plazo clínicamente significativa, utilizando un diseño de estudio que permitiera una interpretación causal más fuerte que la investigación observacional existente hasta su culminación. Para el análisis de este estudio de cohorte se utilizó un diseño de discontinuidad de regresión difusa y no hubo evidencia de una asociación entre el uso del MCI con la reducción de la TFGe hasta seis meses después, con un cambio medio en el TFGe de -0,4 ml/min/1,73 m2 (IC 95 %, -4-4,0) posterior a la exposición al MCI. De manera similar, no hubo evidencia de una asociación con la necesidad de terapia de reemplazo renal (diferencia de riesgo (RD) de 0,07 %; IC 95 %, -0,47-0,61 %), mortalidad (RD de 0,3 %; IC 95 %, -2,9-3,2 %) y LRA (RD de 4,3 %; IC 95 % -2,7-12,9 %). Estos autores tampoco encontraron evidencia de un efecto dañino en la función renal de los MCI intravenoso administrado para angiograma pulmonar tomográfico computarizado en el servicio de urgencias [18].
Toda esta evidencia respalda el hecho de que la relación causal entre la MCI y el desarrollo de IRA no ha sido demostrada de forma consistente y que la percepción de este riesgo ha sido sobreestimada a lo largo de décadas. En el año 2020 y con base en estos hallazgos, el Colegio Estadounidense de Radiología (ACR) y la Fundación Nacional del Riñón (NKF) disminuyeron el nivel de precaución recomendado para la administración IV de MCI a pacientes con ERC preexistente (TFGe < 30 ml/min/1,73 m2) [19,20].
Conclusión: el riesgo de IRA posterior a la administración de MCI ha sido sobreestimado en la literatura y percibido de forma exagerada por el personal del área de la salud, ya que los datos derivan de estudios pequeños, no controlados ni aleatorizados, que no tenían en cuenta otras variables de confusión (características de los MCI, comorbilidades y fluctuaciones propias de la creatinina basal, etc.). Adicionalmente, una gran cantidad de ensayos retrospectivos y metaanálisis con un mejor diseño metodológico y análisis estadístico, que incluían un amplio número de individuos, en poblaciones seleccionadas y no seleccionadas, no han encontrado una asociación independiente entre la administración de MCI IV y el desarrollo de IRA-ACI, incluso en pacientes con ERC avanzada (TFGe < 30 ml/min/1,73 m2) e IRA en pacientes en estado crítico.
4. ¿Existe evidencia que soporte el uso del valor absoluto de creatinina como dato aislado para definir la utilización de un MCI?
La creatinina se deriva del metabolismo de la creatina en el músculo esquelético y de la ingesta dietética de la carne, la cual es liberada a la circulación a un ritmo relativamente constante. Los valores medios de CrS difieren entre hombres y mujeres, personas obesas, con baja masa muscular o con amputación de miembros (debido a las diferencias en la masa muscular y, por lo tanto, en la generación de creatinina) [21].
Estos factores conllevan a una gran variabilidad en los valores de creatinina sin que ellos se relacionen directamente con la tasa de filtración glomerular (TFG), por ello se deben utilizar ecuaciones de estimación de TFG a partir de la CrS en lugar de depender del valor sérico de creatinina. Las ecuaciones de estimación del TFG son más exactas y precisas que la valoración de esta a partir de la medida exclusiva de creatinina y, de igual forma, obvian la necesidad de mediciones de depuración de creatinina en orina de 24 horas. Se debe obtener la CrS utilizando un ensayo enzimático específico con calibración trazable a los materiales de referencia estándar internacionales y un sesgo mínimo en comparación con la metodología de referencia de espectrometría de masas por dilución de isótopos (IDMS) [22].
Conclusión: la CrS como dato aislado no debe utilizarse como referente para determinar el compromiso de la función renal, ella es solo una variable de la ecuación para estimar la TFG y, con base en esta última, se determinará el grado de compromiso de la función renal. No se recomienda la medición de depuración de creatinina en orina de 24 horas.
5. ¿Mediante cuál ecuación se debe calcular la TFGe para determinar el riesgo de un paciente de desarrollar IRA-ACI previo a su inyección?
La TFG es la mejor medida general de la capacidad de filtrado integrada de la nefrona, lo que equivale al total de unidades funcionales que conservan capacidad de filtración. Desde esta perspectiva, contar con su estimación numérica es de gran relevancia clínica, ya que nos aporta información más acorde a la realidad de la masa renal funcional que cualquier valor de otro biomarcador como dato aislado [23].
La ecuación de Cockcroft-Gault fue publicada en 1976 y ha sido usada de forma tradicional, especialmente para el ajuste de dosis de fármacos. Para la obtención de esta ecuación, se realizó un análisis de regresión en el que se incluyeron como variables la concentración sérica de creatinina, la edad y el peso, pero tiene como desventaja el método de laboratorio que se utilizó para la determinación de creatinina (Jaffé), además, esta ecuación es influenciada en gran medida por los valores extremos de las variables peso y edad, la asignación de un valor arbitrario como constante para el género femenino, no tener en cuenta la composición corporal y la sobreestimación del filtrado glomerular (FG) para valores inferiores a 15 ml/min/1,73m2 [24].
La ecuación de MDRD es el resultado de un análisis retrospectivo del estudio "Modification of Diet in Renal Disease", su propósito era mejorar la exactitud de la fórmula de Cockcroft-Gault a través de una estimación del FG y no del aclaramiento de creatinina. La muestra incluía pacientes adultos, de ambos sexos, con predominio de raza blanca y con ERC de base; se utilizó como medida del FG el aclaramiento con 125I-iotalamato y seis variables fueron analizadas: las concentraciones séricas de urea, creatinina y albúmina, la edad, el sexo y la etnia (MDRD-6) e incluía un análisis de regresión múltiple [25]. La versión abreviada de cuatro variables (MDRD-4) eliminaba la necesidad de utilizar la concentración sérica de urea y albúmina, manteniendo la misma eficacia diagnóstica que la fórmula original, pero de más fácil aplicación [26]. Algunas de sus limitaciones incluyen: mayor porcentaje de individuos de raza blanca, sin diabetes mellitus y con un filtrado glomerular menor a 60 ml/min/1,73 m2. Su exactitud disminuye de forma lineal con el aumento el filtrado glomerular, por lo que sobreestima la prevalencia de ERC, incrementando el número se falsos positivos de dicha enfermedad [27].
La ecuación CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) del 2009 se desarrolló utilizando datos agrupados de 10 estudios que posteriormente fueron validados con datos derivados de 16 estudios adicionales, en los que el patrón oro fue la medición directa de la TFG utilizando marcadores de filtración externos (-iothalamato). La muestra poblacional del estudio incluía a personas con y sin enfermedad renal con gran heterogeneidad de TFG. La ecuación CKD-EPI del 2009 fue tan precisa como la ecuación del estudio MDRD entre individuos con TFG inferior a 60 ml/min/1,73 m2 y algo más precisa en aquellos con TFG más altos [28].
La NKF y el grupo de trabajo sobre la reevaluación de la inclusión de la raza en el diagnóstico de enfermedades renales de la Sociedad Americana de Nefrología (ASN) han publicado su informe final, el cual describe un nuevo enfoque libre de raza para diagnosticar la enfermedad renal. En el informe, el grupo de trabajo NKF-ASN recomienda la adopción inmediata de la nueva ecuación de creatinina TFGe 2021 CKD-EPI que estima la función renal sin una variable de raza [29].
Por otra parte, algunas ecuaciones se basan en la cistatina C como biomarcador, al tener en cuenta algunas ventajas de esta molécula, como que sus niveles séricos no son modificados por masa muscular, dieta o raza, y son menos influenciados por el género y la edad que los de la creatinina [30]. Los limitantes más importantes para la utilización clínica de la cistatina C son su costo y la falta de estandarización internacional de los diferentes métodos de medición, este último aspecto viene siendo subsanado por la Federación Internacional de Química Clínica (IFCC) a través del desarrollo de materiales de referencia y la estandarización de ensayos [31].
Dharnidharka et al. [150] demostraron un mejor rendimiento de la cistatina C como bio-marcador de la TFG con respecto a la creatinina en la población general. En un metaanálisis que incluía estudios que comparaban los niveles de creatinina y cistatina C frente a algún método de medición de referencia de la TFG - clearance de inulina, iotalamato, iohexol, 51Cr-EDTA o 99mTc -DTPA, los investigadores encontraron que la correlación del recíproco de la cistatina C con la TFGm (tasa de filtración glomerular medida) fue superior al de la creatinina (r = 0,816; IC 95 %, 0,804-0,826) vs. (r = 0,742; IC 95 %, 0,726-0,758; P < 0,001), lo que evidencia de manera similar que los valores del área bajo la curva (AUC) de la gráfica de características operativas del receptor (ROC) para 1/Cys C tenían una mayor correlación con la prueba de referencia para TFGm (0,926; IC 95 %, 0,892-0,960) que los valores ROC para 1/Cr (0,837; IC 95 %, 0,796-0,878; P < 0,001) [30].
Existen diferentes fórmulas basadas en variables demográficas y antropométricas, además de la concentración plasmática de cistatina C, ya sea aislada o combinada con la concentración de creatinina plasmática.
Así, la CKD-EPI se compone de dos fórmulas, la primera basada en cistatina C aislada (CKD-EPICys) y la segunda combinada con creatinina (CKD-EPI crea-c ys ). Para su elaboración se incluyó a 5352 pacientes de 13 estudios y se validaron en una cohorte externa de 1119 pacientes de otros 5 estudios. La TFGm media por clearance de iotalamato fue de 47 ml/min/1,73 m2 en el grupo de formulación vs. 50 ml/min/1,73 m2 en el grupo de validación, incluyendo pacientes con un gran espectro de función renal (< 15 a > 120 ml/min/1,73 m2). Además, no se evidenció un mayor rendimiento de la ecuación CKD-EPICys al compararla con CKD-EPI, sin embargo, la ecuación combinada tuvo mayor exactitud y precisión, con lo que fue posible reclasificar el 16,9 % de pacientes que fueron asignados como ERC G3a a un estadio de ERC G2 [32].
Por su parte, el FAS (Full-age-spectrum) se trata de dos fórmulas: FAS basado en cistatina C sola (FASCysC) y el FAS basado en creatinina y cistatina C (FASCombi). Las ecuaciones se diseñaron al tener en cuenta los datos de cistatina C y creatinina obtenidos de 6870 sujetos y fueron validados en 6132 sujetos incluidos en 11 estudios, a los cuales se les había medido la TFG por algún método de referencia. En niños y adolescentes, la fórmula FAScysC presentó un mejor rendimiento que la fórmula de Schwartz basada en cistatina C, en tanto que FAS Combi presentó un mejor rendimiento que ambas ecuaciones. En adultos, la fórmula FAScysC tuvo un rendimiento similar a CKD-EPI y FAScombi tuvo similar rendimiento a CKD-EPIcrea-cysC. Por otra parte, FAScombi y FAScysC fueron superiores a sus similares de CKD-EPI en personas mayores de 70 años [33].
La TFGe de forma indirecta, a partir de la concentración plasmática de sustancias endógenas como la creatinina, puede arrojar diferencias de hasta un 30 % cuando es comparada con la TFGm [34]. La TFGm que utiliza un marcador exógeno es considerada el método óptimo de medición, sin embargo, su complejidad y sus costos limitan el uso de esta técnica en la práctica habitual, por lo que su utilización está indicada en cualquier situación clínica en la que se requiera una mayor precisión, especialmente si el resultado afectará las decisiones de tratamiento: evaluaciones de donante vivo de riñón, ajuste de dosis de drogas nefrotóxicas, pacientes en protocolos clínicos o como guía para decisiones terapéuticas basadas en la TFG: obesidad, masa muscular extrema, monorrenos e inicio de diálisis en situaciones no claramente definida [35].
El aclaramiento renal de la inulina de forma histórica ha sido considerado el "estándar de oro" para la determinación de la TFG, pero la complejidad para su medición y sus costos limitan su uso en la práctica clínica. Para simplificar la medición directa de la TFG se han utilizados otros métodos: marcadores radiactivos como el ácido etilendiaminotetraacético (51Cr-EDTA), el ácido dietilentriaminopentaacético (99mTc-DTPA) y el 125I-iotalamato, los cuales son fiables para determinar con precisión la TFG, con resultados comparables con la técnica de aclaramiento de inulina. Su desventaja es el requerimiento de sustancias radiactivas y que su uso no es permitido en cierto grupo de pacientes como embarazadas [36].
Por lo tanto, se han propuesto marcadores no isotópicos que utilizan el aclaramiento plasmático de los MC que cumplen con los criterios de los marcadores ideales, como iohexol, iotalamato, iopamidol e iopromida, como alternativas para medir la TFG. El aclaramiento plasmático de iohexol para la determinación de la función renal tiene una serie de ventajas: es un enfoque barato y muy simple que no es técnicamente exigente y es fácil de implementar en todos los centros. La elección de iohexol ofrece, tanto a los laboratorios como a los médicos, la oportunidad de seleccionar y ajustarse fácilmente al enfoque más adecuado para una medición fiable y precisa de la TFG [37], sin embargo, en situaciones particulares en las que aumenta el volumen extracelular (ascitis, edema o en unidades de cuidados intensivos), la evaluación del aclaramiento urinario puede considerarse un procedimiento más fiable [38]. Con relación al perfil de seguridad, independientemente de las condiciones de la enfermedad y el nivel de función renal, la tasa general de eventos relacionados con el iohexol es tan baja como el 0,006 % [39].
Conclusión: recomendamos utilizar la ecuación de CKD-EPI 20211 que no incluye una variable de raza, para calcular la TFGe para la población mayor de 18 años. Al tener en cuenta que la TFGe es el mejor índice general de función renal, en caso de no contar con calculadora específica para esta ecuación, puede utilizarse una fórmula alternativa (CKD-EPI 2009, MDRD o C&G), ya que sus resultados guardan una mayor correlación con el filtrado glomerular que un valor de creatinina como dato aislado.
6. ¿Cuáles son los factores de riesgo relacionados con el paciente para desarrollar IRA-ACI?
Estimar el riesgo de desarrollar IRA-ACI es fundamental para determinar qué pacientes son susceptibles de un deterioro prevenible de la función renal pos-exposición al MCI.
La función renal de base antes de la administración del MCI es el mayor predictor del deterioro de la TFG después de su administración, en este sentido, la presencia de ERC avanzada (TFGe < 30 ml/min/1,73 m2) y la IRA se constituyen en los factores de riesgo más relevantes. Características propias del paciente como la edad, comorbilidades como diabetes, hipertensión arterial, hiperuricemia, baja perfusión renal (fracción de eyección ventricular izquierda reducida, hipovolemia, uso de diuréticos, deshidratación), proteinuria, presencia de riñón único o de trasplante renal, no han podido demostrar ser factores de riesgo independientes de la TFGe [40].
En un estudio de puntuación de propensión se demostró que la IRA, posterior a la administración de MCI intravenoso de baja osmolalidad, generalmente no se produce en pacientes con un TFG ≥ 45 ml/min/1,73 m2, en tanto que en aquellos con TFGe de 30 a 44 ml/min/1,73 m2 se presentó en el 16 % de quienes fueron sometidos a una TAC con MC, frente a un 15 %, de aquellos a quienes se les realizo una TAC sin MC (OR 1,22, IC 95 % 0,88-1,71; P = 0,24). El panorama cambia drásticamente en los pacientes con TFGe < 30 ml/min/1,73 m2, ya que en estos se desarrolló IRA posterior al MC en el 35 % de los casos que fueron sometidos a una TAC con MC, frente a un 14 % en quienes que no se utilizó MCI (OR 3,96, IC 95 % 1,29-12,21; P = 0,016) [41]. Estos hallazgos son similares a lo evidenciado por Davenport et al., quienes demostraron un riesgo mayor de IRA cuando se estratificaba por TFGe (especialmente cuando TFGe ≤ 30 ml/min/1,73 m2) [17].
Conclusión: la reducción de la función renal de base, determinada a través de una ecuación para el cálculo de la TFGe antes de la administración de MCI, es el único factor de riesgo independiente para el desarrollo de IRA asociada a los medios de contraste; una TFGe < 30 ml/min/1,73 m2 (pacientes de alto riesgo) se constituye como el mayor predictor de desarrollo de IRA-ACI, en pacientes sometidos a estudios intravasculares con MCI.
7. ¿Cuál es el rango de tiempo dentro del cual debe realizarse una CrS para ser considerada como una variable valida y vigente para el cálculo de la TFGe, antes de la administración del MCI?
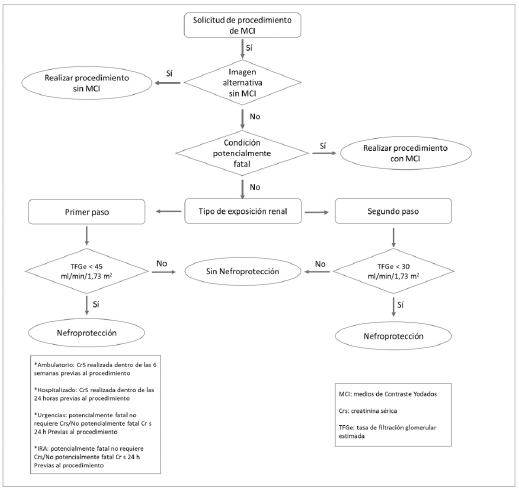
No existen estudios que evalúen el tiempo dentro del cual debe realizarse una CrS para ser considerada como una variable valida y vigente para el cálculo de la TFGe, antes de la administración del MCI, por lo que cualquier recomendación al respecto se deriva del conocimiento actual del comportamiento cinético de la creatinina, la existencia de ERC de base, la presencia de enfermedades intercurrentes y del horizonte clínico de la IRA-ACI. Dado que la reducción de la TFGe es < 30 ml/min/1,73 m2, se considera este como el único factor de riesgo independiente para el desarrollo de IRA-ACI y es necesario un compromiso avanzado de la función renal, situación que, por lo general en el contexto ambulatorio se asocia a síntomas o signos de ERC o a condiciones precursoras, motivo por el cual consideramos adecuado un lapso de semanas para su validez. La presencia de enfermedades intercurrentes modifican este criterio, ya que podrían asociarse a la agudización de una enfermedad de base, por lo que este periodo debe acortarse a días y esto explica las recomendaciones de excluir el requerimiento de practicar una CrS antes del estudio con contraste expresado en algunas guías, donde solo indican la realización de un interrogatorio para la identificación de factores de riesgo y, con base en estos, determinar la necesidad de CrS. Esta estrategia beneficia claramente al paciente, ya que no se retrasan, difieren o cancelan procedimientos con contraste, bajo el argumento de no disponer de una prueba de creatinina "reciente". En caso de hospitalización y en el ámbito de urgencias o la presencia de IRA, la necesidad de realizar un procedimiento con medios de contraste yodado será determinado por la condición clínica y el potencial riesgo de un desenlace fatal del paciente.
Ambulatorio
Para pacientes sin antecedentes de algún tipo de afectación renal o sin la presencia de condiciones intercurrentes que puedan modificar la TFGe (vómito, diarrea, fiebre, etc.), se considera aceptable una creatinina realizada dentro de las últimas seis semanas; sin embargo, si hay historial de algún tipo de daño renal o presencia de condiciones intercurrentes, entonces sería más apropiado reducir el intervalo a tres días (72 horas) después de resuelta la condición intercurrente.
Hospitalizado
Creatinina procesada dentro de las 24 horas previas a la exposición al MC para cálculo actualizado de la TFGe, sin embargo, si durante la hospitalización el paciente presenta una condición potencialmente fatal, no se debe retrasar la realización del estudio con MC en espera de una CrS y se debe realizar de forma inmediata.
Urgencias
En este escenario nos enfrentamos a condiciones potencialmente fatales, por lo que los estudios o las intervenciones deben realizarse de forma inmediata, independientemente de contar con creatinina. Si la situación no reviste una condición potencialmente mortal inmediata y permite la medición de la creatinina para la determinación de la TFGe, esta podría realizarse, sin embargo, una TFGe baja no deberá ser una limitante para realizar el procedimiento, si la condición clínica lo indica.
IRA
Para determinar el uso de un MCI IV o IA en pacientes con IRA, se debe realizar un estricto análisis del potencial balance beneficio/riesgo: si el beneficio de una mejor imagen diagnóstica o de una intervención terapéutica que limite o revierta una condición potencialmente fatal, compensa el riesgo de empeoramiento de la IRA o que esta se convierta en un daño renal permanente o irreversible, entonces la utilización del MCI está plenamente justificada.
Ehmann et al. diseñaron un estudio con el propósito determinar la asociación entre la administración de MCI IV y la LRA persistente en pacientes con LRA preexistente, ello conllevó a un análisis de cohorte observacional retrospectivo ponderado por propensión y balanceado por entropía de pacientes hospitalizados > 18 años de edad que cumplían con los criterios basados en la creatinina de Kidney Disease Improving Global Outcomes (Kdigo) para LRA al momento del ingreso a uno de tres servicios de emergencia, entre el 1 de julio del 2017 y el 30 de junio del 2021 que recibieron (o no) MCI intravenoso. Los desenlaces incluyeron IRA persistente al alta hospitalaria e inicio de diálisis dentro de los 180 días posteriores a la exposición al MCI [21]. Se incluyó a 14.449 pacientes, de ellos, el 12,8% fueron ingresados en la unidad de cuidados intensivos (UCI). El MCI se administró en el 18,4 % de los pacientes y la IRA se resolvió antes del alta hospitalaria en el 69,1 % de los casos. No se observó asociación entre la administración de MCI por vía IV y la LRA persistente después del modelo de regresión logística multivariable no ajustado (OR 1,0; IC 95% 0,89-1,11), ponderación de propensión (OR 0,93; IC 95 % 0,83-1,05) y equilibrio de entropía (OR 0,94; IC 95 % 0,83-1,05). El análisis de los subgrupos en los ingresados a la UCI arrojó resultados similares, además, no se observó una asociación entre la administración de MCI y un mayor riesgo de diálisis dentro de los 180 días (5,4 % de los pacientes de la cohorte). Adicionalmente, la administración de MCI no se asoció con LRA persistente en pacientes con LRA adquirida en la comunidad e insuficiencia renal grave (TFGe < 30 ml/min/1,73 m2) al momento de la llegada al servicio de urgencias (38 % de la cohorte).
De este estudio podemos concluir que entre los pacientes con LRA preexistente, la administración de MCI no se asocia con LRA persistente al alta hospitalaria, ni con un mayor riesgo de inicio de diálisis dentro de los 180 días posteriores. Estos hallazgos son consistentes para los pacientes del servicio de urgencias y para aquellos con TFGe baja (TFGe < 30 ml/min/1,73 m2), al igual que para aquellos ingresados en la UCI.
8. ¿Todos los MCI tienen el mismo riesgo de producir IRA-ACI?
Las propiedades fisicoquímicas más importantes de los MC son: la concentración de yodo (de la cual depende la radio-opacidad), la estructura molecular, la osmolalidad y la ionización.
La estructura molecular está determinada por el número de anillos de benceno: monomérico = 1 o dimérico= 2, en tanto que la ionización hace referencia a la capacidad de disociación, pudiendo ser iónicos o no iónicos. Con relación a la osmolalidad (mOsmol/kg), los primeros MCI denominados de alta osmolalidad (MCAO), tales como el iotalamato y el diatrizoato, consistían en preparaciones monoméricas iónicas con osmolalidades extremadamente altas (8002500 mOsmol/kg) con respecto al plasma (290 mOsm/kg). Debido a que fueron relacionados con un alto riesgo de injuria renal pos-administración de MC, se desarrollaron MCI diméricos iónicos (ioxaglato) o monómeros no iónicos (iopromida, iopamidol, iohexol, ioversol, iomeprol, etc.), cuyas osmolalidades se encontraban por debajo de los hiperosmolales (~400-800 mOsmol/kg), motivo por el cual fueron denominados MCI de baja osmolalidad (MCBO), pese a que su osmolalidad era superior a la del plasma. La tercera generación de MC (iodixanol e iotrolan) posee realmente una osmolalidad inferior a la del plasma, por lo que se añaden electrolitos a la solución utilizada clínicamente para alcanzar la osmolalidad plasmática y razón por la que se denominan isoosmolares (MCIO) [42,43] (tabla 3).
Tabla 3 Características de medios de contraste
| Compuesto | Ionicidad | Estructura | Osmolalidad | Viscosidad 20-25 | Viscosidad |
|---|---|---|---|---|---|
| (mOsm/kg) | °C (mPa.S) | 37 °C (mPa.S) | |||
| Alta osmolalidad | |||||
| Diatrizoato | Iónico | Monomérico | 1500 - 2000 | 3,3 - 16,4 | 1,4 - 19,5 |
| Metrizoato | Iónico | Monomérico | 2100 | 5-9 | 2,8-5 |
| Iotalamato | Iónico | Monomérico | 600 - 2400 | 2-9 | 1,5 - 5,0 |
| Baja osmolalidad | |||||
| Ioxaglato | Iónico | Dimérico | 600 | 12 - 15,7 | 6-7,5 |
| Iohexol | No iónico | Monomérico | 322 - 844 | 2,3 - 20,4 | 1,5 - 10,4 |
| Ioversol | No iónico | Monomérico | 350 - 792 | 4,6 - 14,3 | 3,0 - 9,0 |
| Iopamidol | No iónico | Monomérico | 300 - 832 | 2,3 - 20,9 | 1,5 - 9,5 |
| Iopromida | No iónico | Monomérico | 340 - 880 | 2,3 - 22 | 1,2 - 12,3 |
| Iopentol | No iónico | Monomérico | 310-810 | 2,7 - 26,6 | 1,7 - 12,0 |
| Iomeprol | No iónico | Monomérico | 301 - 730 | 1,9 - 27,5 | 1,4 -12,6 |
| Iso-omolales | |||||
| Iodixanol | No iónico | Dimérico | 290 | 12,7 - 26,6 | 6,3 - 11,8 |
| Iotrolan | No iónico | Dimérico | 270 - 320 | 6,8 - 16,4 | 3,9 - 8,1 |
Fuente: elaboración propia.
Lautin et al. demostraron un claro beneficio con el uso de agentes de osmolalidad más baja, en un estudio en el que el agente iónico de baja osmolalidad ioxaglato fue menos nefrotóxico que los agentes hiperosmolares iónicos [44]. Para resolver el interrogante sobre el mayor potencial nefrotóxico entre MCI iso-osmolales comparados con los de baja osmolalidad, Eng et al. condujeron un metaanálisis que incluyó 25 ensayos aleatorizados que comparaban el iodixanol (iso-osmolal) con un grupo de diversos agentes de baja osmolalidad (la mayoría de los pacientes con ERC o diabetes) y reportó una leve reducción del riesgo de IRA-ACI (riesgo relativo (RR) de 0,80, IC 95 % 0,65-0,99) con iodixanol [45]; sin embargo, pese a su mínima significancia estadística, estos hallazgos no se traducían en un claro beneficio clínico o en una diferencia en términos de riesgo de necesidad de terapia de reemplazo renal (TRR), resultados cardiovasculares o muerte, entre ambos grupos.
Por otra parte, la viscosidad de una MCI podría tener una importancia subestimada para la seguridad renal debido a que, al igual que la osmolalidad, una alta viscosidad ha sido implicada en la fisiopatología de la IRA-ACI. La viscosidad depende de varios factores: del disolvente (que en los MCI es agua), el peso, el tamaño molecular, la concentración molar y la temperatura, además que guarda una relación directa con el tamaño molecular (por eso los MCI monoméricos tienen una viscosidad menor que los diméricos), en tanto que la relación con la osmolalidad y la temperatura es inversa [46]. El aumento de la viscosidad de un MC favorece su concentración en los túbulos y los vasos medulares (debido al entorno hiperosmolar), comprometiendo el flujo sanguíneo y el suministro de oxígeno a la medula renal; además, la filtración glomerular disminuye debido a la congestión del fluido tubular altamente viscoso [47].
Conclusión: los datos actuales no soportan la teoría de que todos los medios iso-osmolales ofrecen mejores resultados que los medios de baja osmolalidad, en términos del riesgo de IRA-ACI, por lo que recomendamos utilizar medios iso-osmolales o de baja osmolalidad indistintamente de la condición del paciente. Dado el papel de la viscosidad en la fisiopatología de la IRA-ACI, recomendamos precalentar los MCI, antes de su administración.
9. ¿La vía de administración del MC (IV, IA o percutánea) modifica el riesgo de desarrollar IRA-ACI?
Con base en un sustrato anatómico (la proximidad a las arterias renales) y aspectos farmacocinéticos como la dilución que puede experimentar el MCI en el torrente sanguíneo previo a su contacto con la vasculatura renal, podemos clasificar la exposición renal al MCI en tres categorías: exposición renal de primer paso, de segundo paso e intervención percutánea [48].
Exposición renal de primer paso: hace referencia a la llegada del MCI a las arterias renales en una forma relativamente pura (sin diluir), debido a la corta distancia entre el sitio de inyección y las arterias renales. Ejemplos de esta categoría son los procedimientos que impliquen inyección de MCI en el ventrículo izquierdo, aorta torácica, aorta abdominal por encima del origen de las arterias renales y selectivamente en las arterias renales.
Exposición renal de segundo paso: hace referencia a la llegada del MCI a las arterias renales después de ser diluido por la circulación: a través del corazón derecho, la circulación pulmonar o un lecho capilar sistémico. Ejemplos de este tipo de exposición renal al MCI son la administración IV, la inyección del MCI en el ventrículo derecho y arterias pulmonares, al igual que la inyección directa del MCI en las arterias coronarias, carótida, subclavia, braquial y mesentérica, así como en la aorta infrarrenal y las arterias ilíaca, femoral y crural.
Procedimientos percutáneos: hace referencia a intervenciones mínimamente invasivas guiadas por imágenes, las cuales permiten la inyección del MCI mediante una punción cutánea. A través de esta vía puede accederse a estructuras vasculares (angioplastia trans luminal percutánea, intervenciones coronarias por vía percutánea y angioplastia coronaria transluminal percutánea); a la vía biliar (colangiografía transhepática percutánea, colangio-pancreatografía retrograda endoscópica o CPRE), a la vía urinaria (urografía anterógrada percutánea), al espacio intratecal (o espacio subaracnoideo), intraperitoneal e intraarticular, lo cual se considera un tipo de exposición renal de segundo paso.
La exposición renal de primer paso al MCI ha sido reportada en la literatura como de mayor riesgo para el desarrollo de IRA-ACI [49], sin embargo, existen controversias al respecto (especialmente por los múltiples factores de confusión derivados de las comorbilidades de base de los pacientes). En el contexto de una coronariografía terapéutica (no en el caso de la diagnóstica), especialmente por infarto agudo de miocardio, se ha informado un mayor riego de IRA-ACI, sin embargo, el mayor volumen del medio de contraste utilizado en este tipo de procedimientos y la inestabilidad hemodinámica asociada con el infarto agudo de miocardio podrían explicar este mayor riesgo [50]. En casos de administración venosa del MCI para la realización una TAC, la mayoría de los estudios han sugerido un riesgo bastante bajo de IRA-ACI, incluso en pacientes con ERC de base [51].
Por otra parte, el uso de la vía transfemoral (técnica de Seldinger) o transradial (técnica de Sones) para el cateterismo cardiaco podría afectar el riesgo de IRA posterior al procedimiento. Es fundamental tener en cuenta que la correcta selección de la zona de punción es determinante tanto para el éxito de un procedimiento diagnóstico o terapéutico, como para el riesgo de complicaciones (sangrado y ateroembolismo). Un sangrado abundante periprocedimiento (por ejemplo: retroperitoneal) en el contexto de un abordaje transfemoral es un factor de riesgo para el desarrollo de la IRA posprocedimiento, en tanto que el acceso transradial se ha asociado con una menor incidencia de complicaciones hemorrágicas relacionadas con el acceso vascular y la mortalidad por todas las causas [52], además de un menor riesgo de IRA posterior al procedimiento (OR 0,51 IC 95 % 0,39-0,67, p < 0,0001) [53].
A pesar de que el acceso transfemoral (arterial y venoso) hoy en día es el más utilizado por su menor curva de aprendizaje, porque permite el acceso a toda la anatomía vascular, así como el uso de catéteres de mayor calibre, esta evidencia indica que el uso de la vía transradial para el cateterismo cardiaco, cuando sea técnicamente factible, sería la recomendada.
Conclusión: el uso de MCI con exposición renal de primer paso podría estar asociado con un mayor riesgo de desarrollar IRA-ACI. Dadas las implicaciones en términos de morbilidad y mortalidad propias de la IRA, consideramos razonable establecer un punto de corte más alto (TFGe < 45 ml/min/1,73 m2) que el establecido para procedimientos arteriales de segundo paso e intravenosos (TFGe < 30 ml/min/1,73 m2), para clasificar a los pacientes como de alto riesgo de desarrollar IRA posterior a la exposición al MCI.
De igual forma, sugerimos en pacientes de alto riesgo utilizar métodos alternativos que no requieran exposición renal de primer paso a los medios de contraste (por ejemplo: ecocardio-grama en lugar de ventriculograma para evaluar la fracción de eyección ventricular - FEV), así como limitar los segmentos anatómicos a evaluar para aquellos estrictamente necesarios (circulación infrapoplítea si no hay clínica de compromiso proximal) y explorar otros segmentos con métodos que no ameriten contraste como registros segmentarios del volumen del pulso (pletismografía), ecografía Doppler, angiografía por resonancia magnética o angiografía con CO2.
10. ¿El volumen del MCI utilizado durante un procedimiento diagnóstico o terapéutico es un factor de riesgo para el desarrollo de IRA-ACI?
El volumen utilizado del MCI ha sido reconocido como un factor de riesgo modificable para el desarrollo de IRA-ACI, sin que hasta la fecha exista evidencia suficiente que le permita reconocerse como un factor de riesgo independiente para el desarrollo de IRA-ACI, especialmente cuando se inyectan por vía IV.
A través del tiempo, el volumen establecido como límite superior a partir del cual se le considera como factor de riesgo manifiesto para el desarrollo de IRA-ACI, ha variado desde un volumen fijo de 125 ml [54] hasta un volumen relativo determinado a través del peso de 3 ml/kg [55], sin embargo, estudios realizados en pacientes sometidos a angiografías coronarias, a principio de los años 90, ya evidenciaban que volúmenes por encima de los 30 ml podían conllevar a IRA-ACI, predominantemente en pacientes diabéticos e hiperazoémicos [56], siendo este volumen de especial consideración si tenemos en cuenta que el rango de volumen utilizado en procedimientos con MCI oscila entre 30 y 180 ml [57]. En pacientes sometidos a angiografía coronaria con compromiso de la TFGe, un volumen infundido < 125 ml se asoció a un incremento del 2 % del riesgo de desarrollar IRA, mientras que un volumen > 125 se asoció con un incremento del 19 % (p = 0,009) [38]. De igual forma, en la intervención coronaria percutánea (ICP) primaria para el infarto agudo de miocardio con elevación del segmento ST-AMCEST, un mayor volumen de contraste se asocia con un incremento en la tasa de IRA-ACI y la mortalidad [58].
Lee et al. condujeron un metaanálisis con el propósito de determinar si el volumen de contraste, su método de administración y la TFGe influían en la eficacia de la hidratación profiláctica para la prevención de la LRA después de la administración de contraste y encontraron que cuando el volumen del MCI administrado superó los 100 ml, la hidratación fue beneficiosa en la prevención de la IRA-ACI (OR 0,546), pero si el volumen era inferior a 100 ml, la hidratación no tuvo eficacia para prevenir la IRA-ACI (OR 0,917). La ruta de administración y la TFGe no ejercieron ningún efecto sobre la eficacia de la hidratación profiláctica, sin embargo, se necesitan más estudios para determinar si limitar el volumen de contraste mejoraría el resultado del paciente [59].
La dosis de contraste máxima permitida (MACD) es un concepto introducido por primera vez en 1989 por Cigarroa et al. [60], quienes pretendían determinar un límite superior de volumen de medio de contraste a utilizar, por lo que fue definida por la fórmula empírica: MACD = 5 ml X peso corporal (kg)/CrS (en mg/dL), con una dosis máxima del MCI de 300 ml. En su investigación, este grupo evidenció un incremento de 10 veces en la incidencia de IRA-ACI entre los pacientes que recibieron MCI en volúmenes que superaron a la MACD, en comparación con aquellos que no superaron la MACD (21 % vs. 2 %, p < 0,001). Entre los pacientes con diabetes, la incidencia de IA-ACI fue aún mayor cuando el volumen de contraste superó a MACD (38 % vs. 6 %, p < 0,001).
La MACD derivó de un estudio que presentaba como principales desventajas no poseer una base científica que explique la constante (K) de 5, además, fue realizada en un solo centro, con una baja muestra de pacientes (N = 115) con ERC presente antes del procedimiento con MCI (Cr ≥ 1,8 mg/dl) y definición de IRA con base en un incremento absoluto de la CrS en 1 mg/ml en los primeros 5 días posteriores a la exposición al MCI [60].
Con el objetivo de refinar la ecuación original de la MACD, Hattar et al. diseñaron un estudio de cohorte retrospectivo de un solo centro de adultos sometidos a ICP, donde utilizaron una curva ROC y el índice de Youden para identificar el valor de corte óptimo para el factor K en la predicción de IRA grave. El valor de corte óptimo para el factor K fue de 2,5, el cual predijo IRA-ACI en todas las etapas (ROC 0,649; IC 95% 0,611-0,686), con un mejor rendimiento para predecir la IRA grave (0,736; IC 95 % 0,674-0,800), por lo que este grupo plantea que la ecuación MACD debe revisarse para incorporar el coeficiente de 2,5 en lugar de 5. Con base en estas consideraciones, se puede concluir que no existe evidencia que apoye el uso rutinario de estas ecuaciones en la práctica clínica [61].
Kane et al. evaluaron volúmenes ultrabajos de un medio de contraste iso-osmolal (iodixanol) en pacientes sometidos a una angiografía coronaria diagnóstica y encontraron que los volúmenes fueron más altos en los pacientes que desarrollaron nefropatía inducida por contraste (CIN) (45 ± 18 ml) que en aquellos que no lo hicieron (31 ± 18 ml, p < 0,0005). Además, los pacientes que recibieron el cuartil más bajo de volumen de contraste tenían siete veces menos probabilidades de desarrollar CIN en comparación con aquellos con el cuartil más alto del volumen de contraste (4,4 % vs. 29,8 %, p = 0,005). En el análisis multivariable, el único factor significativo asociado con la CIN fue el volumen de contraste administrado, con cada 20 cc incremental de contraste se asociaba con un OR de 2,12 (IC 95 % 1,4-3,4, p = 0,002) [62].
La estrategia de limitar el volumen de MCI a máximo tres veces la TFGE (3x) ha sido implementada en muchos centros como estrategia para reducir el riesgo de desarrollar de IRAC-ACI [63], sin embargo, el valor predictivo de este algoritmo de dosificación ha sido motivo de debate y, por lo tanto, no es claro el beneficio real de esta estrategia para estimar la dosis de MC en pacientes con alto riesgo de complicaciones renales después de ser sometidos a intervenciones coronarias percutáneas (ICP).
Gurm et al. [65] desarrollaron un estudio observational multicéntrico de un solo brazo, en el cual se estableció como desenlace principal evaluar el porcentaje de volumen (VCM) del MCI ahorrado, usando un sistema de reducción de contraste (inyector) aprobado por la FDA (Food and Drugs Administration), en pacientes sometidos a procedimientos de angiografía coronaria de diagnóstico (CAG) o procedimientos de ICP comparado con aquellos realizados con inyecciones manuales. La magnitud general del VMC (volumen de medio de contraste) ahorrado fue tanto clínica como estadísticamente significativo (40,1 ± 8,8 % = IC 95 %: 38,4-41,8; P < 0,0001 por procedimiento), lo que se logró mediante una reducción de la relación VMC a TFGe, ya que en la mayoría de los casos el VCM administrado fue inferior al umbral de VMC predefinido. Un dato relevante fue que la calidad de la imagen se mantuvo en todos los estudios, menos en un caso en el que el sistema se apagó para una inyección. Adicionalmente, el volumen promedio de MCI administrado a los pacientes en este estudio (67 ml) se compara favorablemente con el volumen administrado en otros ensayos controlados aleatorios (mediana de 85 ml) [66] o en la práctica clínica habitual: media de 198 ml [67] y 168 ml [68]. Finalmente, la tasa de LRA observada en este estudio fue significativamente más baja de lo previsto.
Los estudios que buscan determinar si el volumen utilizado de MCI es un factor de riesgo modificable e independiente para el desarrollo de IRA-ACI no aportan evidencia robusta que permita emitir conclusiones sólidas al respecto, esto debido a la gran heterogeneidad en sus diseños metodológicos, su pobre tamaño muestral, el no tener en cuenta comorbilidades existentes, la no unificación de la definición de IRA, el no considerar las medidas profilácticas utilizadas y por presentar un sesgo por indicación, esto último teniendo en cuenta que los pacientes sometidos a ICP de emergencia en lugar de electivas tenían más probabilidades de ser hemodinámicamente inestables y requerir un mayor volumen de contraste (es decir, para la angioplastia coronaria y la inserción de stents) [69].
Si bien el umbral exacto para definir la seguridad renal no está establecido, los datos indican que los pacientes que reciben las dosis más altas de MCI tienen un mayor riesgo de IRA-ACI, en comparación con aquellos que reciben dosis más bajas. De igual forma, la disminución del VCM se ha asociado con una reducción en la incidencia de IRA-ACI (70). Con base en estos hallazgos, muchos protocolos sugieren el uso de las dosis más bajas posibles de MCI, sin que ello implique sacrificar la calidad de la imagen con MC.
Conclusión: no se puede minimizar el beneficio que aporta, desde el punto de vista diagnóstico y terapéutico, un procedimiento adecuadamente contrastado, por lo tanto, una vez se establezca la necesidad de realizar dicho estudio, se debe determinar el volumen a utilizar de MCI con base en el peso del paciente (1-2 ml/kg, con dosis máxima de 300 ml) y no a través de ecuaciones que incluyan la creatinina o la TFGe como variables, esto permite la obtención de imágenes de alta calidad a través de la TAC, con lo que se podría evitar la necesidad de repetir el procedimiento con MC, lo que finalmente implicaría la aplicación de un mayor volumen de MCI al paciente. Si la dosis requerida para un adecuado estudio con MCI supera la dosis recomendada, se debe utilizar el menor volumen posible que permita obtener una adecuada imagen. En el caso de procedimientos intervencionistas endovasculares, deberá primar el beneficio del paciente con dicha intervención en procura de evitar una mayor morbididad y mortalidad, por encima del potencial riesgo de IRA-ACI, por ejemplo, en un evento coronario agudo.
11. ¿Las escalas para estimar el riesgo de desarrollar IRA-ACI deben ser utilizadas en el ámbito clínico?
Con el propósito de mejorar la estratificación de los pacientes, se han hecho esfuerzos para desarrollar herramientas de predicción o escalas de riesgo que permitan identificar a los pacientes con más posibilidades de desarrollar IRA-ACI. Las variables incluidas en estos modelos derivan de los factores de riesgo ya conocidos (relacionados con el paciente, el procedimiento o el medio de contraste) y algunos de estos factores son comunes a todas las escalas (tabla 4).
Tabla 4 Evidencia de escalas de riesgo
| Autor | Población | Variables | Estadístico C / AUC |
|---|---|---|---|
| Mehran et al., 2004 [1] | (N = 5571) ICP | Sexo, edad, hematocrito, volumen de contraste, diabetes, hipotensión, uso de balón de contrapulsación intraaórtico, insuficiencia cardiaca y TFGe. | 0,67 |
| Bartholomew et al., 2004 [70] | (N = 20.479) ICP | TFGe <60 ml/min, uso de BCIAo, ICP urgente, diabetes, insuficiencia cardiaca, hipotensión, enfermedad vascular periférica y volumen de contraste >260 ml. | 0,589 |
| Gurm et al., 2013 [68] | (N = 68.773) ICP | Forma de presentación (indicación de la ICP, momento de la ICP, forma de presentación de la cardiopatía isquémica, shock cardiogénico, insuficiencia cardiaca en las dos últimas semanas, fracción de eyección de VI antes de la ICP), diabetes mellitus, características del paciente (edad, peso, altura), parámetros de laboratorio (CK-MB o creatinquinasa, creatinina, hemoglobina, troponina I, troponina T). | 0,84 |
| Gao et al., 2014 [72] | (N = 3945) Angiografía coronaria / ICP | Edad >60 años, hipertensión arterial, infarto agudo de miocardio, insuficiencia cardiaca, uso de BCIAo, TFGe y volumen de contraste (>100 ml) | 0,76 |
| Tziakas et al., 2014 [73] | (N = 52.882) ICP | Preexistencia de insuficiencia renal, uso de metformina, realización previa de la ICP, presencia de arteriopatía periférica y volumen de contraste >300. | 0,741 |
| Lin et al., 2017 [74] | (N = 692) ICP | Edad mayor de 75 años, CrS basal mayor de 1,5 mg/dl, hipotensión arterial y uso de BCIAo. | 0,773 |
Fuente: elaboración propia.
La capacidad discriminativa de estas escalas, medida a través del estadístico C o el AUC (cuanto más cerca esté el valor de 1, mejor será el modelo para clasificar correctamente los resultados), revela que algunas escalas han demostrado su superioridad: Hitinder (0,84), Liu (0,773) o Tziakas (eC 0,741), al compararlas con escalas más ampliamente conocidas y extensamente utilizadas como la de Mehran (0,67) o la de Bartholomew (0,589). Otro aspecto importante es que la mayoría de estos modelos tienen mayor capacidad predictiva para un requerimiento de diálisis que para estimar el desarrollo de IRA-ACI.
Una de las principales críticas a algunos de estos modelos es que no se pueden usar antes del procedimiento porque usan variables del propio procedimiento, por ejemplo: volumen de contraste, lo que es fundamental en un modelo de predicción. Adicionalmente, la complejidad de los algoritmos matemáticos de algunas de estas herramientas hace que se requiera de software o herramientas informáticas especializadas, e incluso, se debe tener presente que los datos con base en los que se realizaron estas escalas derivan de pacientes sometidos a procedimientos arteriales, por lo que no pueden ser extrapolados a la vía venosa; por último, se debe tener en consideración que no se incluyó población latina en dichos estudios.
Las características ideales de una escala predictiva para el desarrollo de IRA-ACI son: alta capacidad discriminativa en términos de estadístico C (eC) o AUC, variables clínicas o de laboratorio obtenibles previas al procedimiento, realizables a la cabecera del paciente, sin requerimientos de software o hardware especializado, que diferencien la vía venosa de la arterial en sus variables y ser validada con la población especifica en la que va a ser utilizada.
Conclusión: al tener en cuenta que las escalas predictivas se han desarrollado para procedimientos arteriales (procedimientos coronarios), no recomendamos el uso de este tipo de escalas para estimar el riesgo de desarrollar IRA-ACI en procedimientos con inyección de MC por vía IV. Recomendamos el uso de la BMC2 PCI Risk Calculator2 para estimar el riesgo de desarrollar IRA-ACI (la cual adicionalmente determina el riesgo de muerte, necesidad de transfusión sanguínea y requerimiento de diálisis) en el ámbito de estudios hemodinámicos. Reconocemos que esta escala requiere más variables que las demás escalas predictivas, sin embargo, permite realizar cálculos sin que se cuente con todas las variables. De igual forma, es fundamental recordar que este tipo de herramienta son una guía, por lo tanto, el análisis clínico de las características propias del paciente, sus comorbilidades, condiciones potencialmente fatales, etc. y del entorno (procedimientos programados vs. urgentes) deben primar a la hora de tomar la decisión de realizar o no el procedimiento con MC.
12. ¿Se debe suspender algún tipo de medicamento previo o posteriormente a la realización de un procedimiento con un MCI?
Un gran porcentaje de pacientes que son sometidos a estudios que utilizan MCI padecen múltiples patologías de base que los hacen tributarios de ingerir medicamentos de forma crónica e ininterrumpida. Es común el interrogante sobre la interrupción o la continuación de estos medicamentos antes de la inyección del MCI y sobre el impacto que estos puedan tener sobre su farmacocinética y farmacodinamia. Con relación a esta pregunta, debemos tener presente el potencial beneficio de estos medicamentos sobre las enfermedades subyacentes y el efecto en términos de morbilidad y mortalidad que podría derivarse en caso de suspenderlos, para llegar a una conclusión. Dentro de los diferentes fármacos, merecen un análisis especial los inhibidores del sistema renina-angiotensina-aldosterona (ISRAA) IECA/ARA II, la metformina y los diuréticos. Ningún otro medicamento cuenta con evidencia que soporte suspenderlos antes o después de la exposición al MCI.
Metformina
Desde hace algunos años, se ha informado en la literatura el riesgo de desarrollar acidosis láctica relacionada a metformina (ALRM), esta se puede presentar por tres mecanismos alteración del aclaramiento de metformina (falla renal aguda y crónica), alteración en la oxigenación en los tejidos (sepsis y choque séptico hipovolémico) y alteración del metabolismo del lactato (falla hepática y abuso de alcohol). Los MCI no poseen un efecto directo sobre el riesgo de ALRM y es la presencia de un episodio de IRA-ACI posterior a la administración intravascular del MC la que puede conducir a la acumulación de esta biguanida [75].
La incidencia de acidosis con hiperlactacidemia en pacientes tratados con metformina ha sido reportada como muy baja (frecuencia < 1/10.000) y se ha relacionado mayoritariamente con el deterioro renal agudo [76], sin embargo, algunos autores informan que esta incidencia puede ser mayor (4,3 eventos por cada 100.000 pacientes al año), con una letalidad que varía entre 30 y 50 %, siendo la falla renal aguda y los estados hipoxémicos crónicos los principales factores de riesgo [77]. Múltiples estudios y metaanálisis han demostrado que el riesgo de acidosis láctica está más relacionado con la enfermedad subyacente y las posibles comorbilidades que con el uso de metformina [78]. Es importante tener en cuenta que el uso de metformina en pacientes con TFGe 30-59 ml/min/1,73 m2 se considera seguro si las dosis se reducen adecuadamente [79,80].
Conclusión: recomendamos no suspender el uso de metformina y continuar su ingesta a la dosis ajustada a la TFGe y en el horario habitual, en pacientes no clasificados como de alto riego (TFGe > 30 ml/min/1,73 m2) o sin evidencia de IRA que reciben MCI IV o IA con exposición renal de segundo paso.
En pacientes con TFGe < 30 ml/min/1,73 m2 que reciben MCI intravenoso o MCI IA con exposición renal de primer y segundo paso o en presencia de IRA, recomendamos suspender la metformina antes de la inyección del MCI y reiniciarla mínimo después de 48 horas, solo si la función renal se mantiene estable (< 25 % de aumento con respecto con la creatinina inicial) y continuar su uso si la condición clínica lo amerita.
Inhibidores del sistema renina-angiotensina-aldosterona (ISRAA): inhibidores de la enzima convertidora de angiotensina (IECA) / antagonistas de los receptores de la angiotensina II (ARA II)
Los ISRAA, IECA y ARA-II fueron los primeros fármacos que demostraron eficacia para disminuir la proteinuria y retrasar la progresión de la ERC, por ello, se recomienda el uso de ISRAA como estrategia farmacológica de primera línea para pacientes con ERC, independientemente de sus etapas clínicas, y rango de proteinuria en las principales guías de práctica clínica; sin embargo, su uso es restringido en el mundo real en el contexto de una función renal gravemente reducida con o sin diabetes, debido a un potencial mayor riesgo de hiperkalemia y efectos hemodinámicos que conducen a IRA o agudización de la ERC de base [81].
Varios estudios observacionales investigaron el papel de continuar vs. suspender el tratamiento con ISRAA en pacientes con ERC avanzada que ya están recibiendo inhibición de RAS (sistema renina angiotensina), centrándose en los resultados renales y cardiovasculares [82].
Algunos autores han demostrado que la interrupción de un IECA o de un ARA-II en pacientes con ERC avanzada se asoció con un mayor riesgo de mortalidad y de enfermedad renal terminal (HR, 1,59; IC 95 %, 1,48-1,71) [83 - 85]. De igual forma, se ha demostrado que la terapia continua con ISRAA se asocia de manera significativa e independiente con una menor incidencia de inicio de diálisis no planificado [86]. Estos datos podrían ser extrapolables a la población con ERC que va a ser sometida a estudios con MCI.
En relación con los ISRAA y la exposición al MCI, Whiting et al. [87] en 1 revisión sistemática y 1 metaanálisis (N = 1663), 3 ensayos controlados aleatorizados (ECA) y 3 estudios prospectivos de cohortes analizaron el efecto de suspender los IECA/ARA II antes de la angiografía coronaria. Este metaanálisis informó que la interrupción de los IECA/ARA II no redujo el riesgo de IRA-ACI (RR 1,48, IC 95 %, 0,84-2,60). La evidencia actual sugiere que no hay un beneficio significativo de suspender los IECA/ARA II antes de la inyección del MC en pacientes con ERC, por lo que es razonable utilizar estos agentes en pacientes con ERC avanzada expuestos a MC. Adicionalmente, el avance de la terapia de unión al potasio ha provocado una mejor tolerabilidad de la inhibición del sistema renina-angiotensina-aldosterona en el contexto de la ERC avanzada.
Conclusión: no recomendamos suspender los IECA o ARA II antes ni después de la administración de un MCI para procedimientos diagnósticos o terapéuticos, si están plenamente indicados para la condición clínica del paciente.
Diuréticos
Los pacientes que requieren manejo con diuréticos de forma crónica tienen de base dificultades para mantener un adecuado equilibrio entre la ingesta y el egreso de líquidos que les permitan tener un estado euvolémico óptimo. En este escenario nos enfrentamos a dos caras de la moneda por un lado, la depleción de volumen en pacientes que reciben diuréticos teóricamente podría hacerlos más susceptibles de desarrollar IRA-ACI y, por otra parte, también existen riesgos evidentes al suspender los diuréticos en pacientes que los requieren para mantener la euvolemia, ya que se puede precipitar una sobrecarga de líquidos [88]. Aunque algunos estudios han relacionado el uso de diuréticos como un factor de riesgo de IRA-ACI [17], no se ha podido establecer de forma clara una relación causal.
Conclusión: no recomendamos suspender los diuréticos antes o después de la inyección de un MCI para procedimientos diagnósticos o terapéuticos, independientemente de la vía (venosa o arterial). Se debe determinar su requerimiento y guiar la dosis con base en los ingresos y los egresos de líquidos del paciente, en procura de alcanzar un estado euvolémico óptimo.
Otros medicamentos: no recomendamos suspender ningún otro medicamento de los que recibe un paciente en forma habitual para el manejo de sus patologías de base.
13. ¿Cuál es la definición de nefroprotección?
La demostración experimental de que el bloqueo de la angiotensina II con IECA retardaba la pérdida progresiva de la función renal en una serie de modelos animales de enfermedades renales, incluida la nefropatía diabética, ofreció la oportunidad, por primera vez, de diseñar una estrategia de tratamiento que no se limitara a acompañar al paciente y así ha surgido el concepto de nefroprotección [89]. La evidencia tanto de estudios experimentales como de ensayos clínicos sugieren que, en la práctica clínica y en el mejor de los casos, se logra posponer la enfermedad renal terminal durante unos años y no evitar la diálisis para la mayoría de los pacientes durante su vida útil [90].
La definición holística de nefroprotección, de forma ideal, debe abarcar todo el continuu m del horizonte clínico de la enfermedad renal, desde sus condiciones precursoras (antes de su aparición), cuando está plenamente establecida, cuando es tributaria de terapia de reemplazo renal (TRR) e incluso durante la presencia de complicaciones y desenlaces fatales. Desde esta perspectiva no se limita a estrategias encaminadas a evitar su inicio y progresión, ni al manejo de las complicaciones y evitar la muerte.
Conclusión: el término nefroprotección se define como: el conjunto de intervenciones colectivas e individuales de tipo preventivo y terapéutico que propenden identificar individuos susceptibles de algún tipo de afectación renal, evitar el inicio del deterioro de la función renal en la población de riesgo, limitar el daño renal y retardar su progresión a ERC establecida, aumentar los tiempos de llegada a la TRR o disminuir su necesidad, evitar las posibles complicaciones y secuelas, y evitar desenlaces fatales.
14. ¿Cuáles son las medidas de nefroprotección que pueden utilizarse para reducir el riesgo de desarrollar IRA-ACI en pacientes de alto riesgo?
Dado que la condición sine qua non para el desarrollo de IRAC-ACI es la exposición al MCI, parecería razonable que la no utilización de estos en pacientes de alto riego (TFGe < 30 ml/min/1,73 m2 por cualquier vía y TFGe < 45 ml/min/1,73 m2 para exposición renal de primer paso al MC) fuera la medida ideal para evitar la IRA-ACI. Con base en esta premisa, la primera pregunta que debemos responder es si la realización del estudio, si la intervención es estrictamente necesaria o si no existe un método alternativo que no utilice MCI (MC basado en gadolinio - MCBG) u otra modalidad diagnóstica que podamos ofrecer a los pacientes.
Son muchas las estrategias farmacológicas que se han utilizado con el objetivo de prevenir la IRA en pacientes que van a ser sometidos a procedimientos radiológicos con MCI y la mayoría de estas terapias se han derivado del conocimiento de los mecanismos fisiopatológicos obtenidos por medio del laboratorio.
Hidratación
La hidratación ha sido la estrategia profiláctica más utilizada en la prevención de la IRA-ACI. Esta propiedad es teóricamente debido a la capacidad de diluir las altas concentraciones de sustancias tóxicas a nivel tubular, lo que evita el contacto prolongado del MCI con el epitelio del túbulo y garantiza un adecuado flujo sanguíneo hacia la médula, sin embargo, se cuestiona su papel, ya que se ha evidenciado que el efecto nefroprotector puede haberse relacionado con una reducción de los episodios de hipotensión con líquidos intravenosos en lugar de reflejar un papel protector directo contra IRA-ACI en todos los grupos de alto riesgo [50].
No hay evidencia robusta a favor de la hidratación por vía oral, pese a que dos estudios sugieren algún beneficio con su uso [91, 92]. Con relación al tipo de hidratación (solución salina vs. bicarbonato), el bicarbonato no proporciona ningún beneficio adicional a la solución salina, además, necesita ser preparado, es más costoso y posee un mayor riesgo de efectos secundarios [66]. Mueller et al. encontraron que la IRA-ACI se redujo significativamente con la solución salina al 0,9% (0,7%, IC 95%, 0,1-1,4%) frente la solución salina al 0,45% (2,0%, IC 95%, 0,0-3,1%) (P = 0,04), sin embargo, dicho beneficio no fue tan evidente en pacientes con compromiso significativo en su TFGe, precisamente el grupo con mayor riesgo de IRA-ACI [93].
Conclusión: la evidencia actual no demuestra el beneficio de la hidratación IV en comparación con la ausencia de hidratación en pacientes con TFGe > 30 ml/min/1,73 m2. En este sentido, recomendamos la hidratación previa a la inyección del MCI vía IV o arterial con exposición renal de segundo paso en pacientes con TFGe < 30 ml/min/1,73 m2. Para los pacientes que van a ser sometidos a procedimientos con exposición renal de primer paso, consideramos razonable instaurar la hidratación con TFGe < 45 ml/min/1,73 m2, pese a no contar con evidencia concluyente, dado el potencial beneficio y el bajo riesgo de complicaciones.
Este consenso no sugiere fórmulas específicas para determinar el volumen de líquidos a utilizar, ya que lo que se busca es evitar que el paciente sea expuesto al MCI en condiciones de deshidratación (sin llegar a la sobrehidratación) y esto a su vez depende de las condiciones propias de cada paciente. Para el protocolo de hidratación, recomendamos el uso de la solución salina normal (SSN).
Un resumen de los estudios más relevantes puede ser visto en la tabla 5.
Tabla 5 Resumen artículos de medidas de nefroprotección
| Estudio | Diseño | Resultados | Análisis |
|---|---|---|---|
| Solomon et al., 1994 [94] | N = 78, pacientes con ERC de base sometidos a angiografía coronaria, quienes recibieron solución salina al 0,45 % vs. salina al 0,45 % + furosemida vs. salina al 0,45 % + manitol | Mayor incidencia de nefropatía en aquellos que recibieron manitol y furosemida con respecto a los que recibieron hidratación sola (28 %, 40 % y11 %, P = 0,05) | Sin grupo control |
| Mueller et al., 2002 [93] | N = 1620, pacientes sometidos a angiografía + stent, quienes recibieron SSN (0,9 %) vs. solución salina hipotónica (0,45 %) + glucosa al 5 %, infundidas a razón de 1 cc/kg/hora por 24 horas previas al procedimiento. | Menor elevación de los niveles de creatinina a las 48 horas en el grupo que recibió SSN (0,7 % vs. 2,0 %, P = 0,04) | Concentración media de creatinina muy parecida en los dos grupos (0,92 mg/dl 0,9 % vs. 0,93 mg/dl 0,45 %), además, al tener en cuenta la población de bajo riesgo incluida en el estudio, el impacto de las dos terapias no pudo ser valorado adecuadamente |
| Merten et al., 2004 [95] | N = 119, pacientes programados para procedimientos radiológicos con iopamidol (creatinina promedio de 1,8 mg/dl), en dos grupos para recibir 154 meq/l de bicarbonato vs. Solución salina al 0,9 % (SSN) a 3 ml/kg una hora antes de la aplicación del medio y 1 ml/kg/hr por seis horas pos-aplicación de este | Incremento de la CrS por encima de 25% (1,7% vs. 13,6 %) grupo bicarbonato vs. SSN 0,9 % (OR 0,88, IC 95 % 0,79-0,97) en el grupo de SSN (p = 0,02) | Concluyeron que la hidratación con bicarbonato de sodio es más efectiva que la hidratación con SSN, sin embargo, algunos aspectos del diseño metodológico del estudio y su finalización precoz no permiten obtener recomendaciones al respecto |
| Hiremath et al., 2013 [96] | N= 513, incluyeron 6 estudios: revisiones sistemáticas y metaanálisis de ensayos aleatorizados con un análisis estratificado y una metarregresión. Comparación de la expansión del volumen oral frente al IV | OR resumido fue de 1,19 (IC 95% 0,46-3,10, p = 0,73), lo que sugiere que no hay diferencia entre las dos rutas de expansión del volumen | La vía oral puede ser tan eficaz como la vía IV para la expansión del volumen para la prevención de lesiones renales agudas inducidas por contraste |
| Nijssen et (AMACI NG), 2017 [97] | N = 660, pacientes con TFGe de 30-59 ml por minuto/1,73 m2, de 18 años o más, sometidos a un procedimiento electivo que requirió de la administración de material de contraste yodado IA o IV y que fueron asignados al azar (1:1) para recibir NaCl al 0,9 % o ninguna profilaxis | Se registró nefropatía inducida por contraste en ocho (2,6 %) de 307 pacientes no hidratados y en ocho (2,7 %) de 296 pacientes hidratados (IC 95 %, -2,25-2,06; p = 0,4710) | No se encontraron diferencias entre hidratación y no hidratación. La población no era un de alto riesgo para IRA-ACI (TFGe >30 ml/min), solo el 48 % de los procedimientos implicaron la administración IA de contraste y el 65 % solo tenía ERC leve |
| Weisbord et al. (PRESER VE), 2018 [66] | N = 4993, pacientes con alto riesgo de complicaciones renales que estaban programados para una angiografía y recibir bicarbonato de sodio IV al 1,26 % o cloruro de sodio IV al 0,9 % | El criterio de valoración principal se produjo en 110 de 2511 pacientes (4,4 %) en el grupo de bicarbonato de sodio en comparación con 116 de 2482 (4,7%) en el grupo de cloruro de sodio (OR, 0,93; IC 95 %, 0,72-1,22; P = 0,62) | No hubo diferencias significativas entre grupos en las tasas de lesión renal aguda asociada al contraste: Bicarbonato no superior a solución salina. |
| Liu et al., 2019 [98] | N = 1074, de incluyeron tres ensayos de calidad moderada donde se comparaba hidratación vs. no hidratación | La hidratación IV redujo significativamente la incidencia de NIC en un 42 % (RR 0,58; IC 95 %, 0,45-0,74, p < 0,001). Los efectos estimados sobre la mortalidad por cualquier causa (RR 0,56; IC 95 %, 0,30-1,02, p = 0,057) y la necesidad de diálisis (RR 0,52, IC 95 %, 0,14-1,88, p=0.462) no fueron estadísticamente significativos | Es probable que la hidratación IV reduzca la incidencia de CIN en pacientes con STEMI (infarto de miocardio con elevación del segmento ST) sometidos a ICP primaria, sin embargo, para los resultados clínicos clave como la mortalidad, la insuficiencia cardiaca y la diálisis, las estimaciones del efecto fueron imprecisas |
| Timal et al. (KOMPAS), 2020 [99] | N = 523, pacientes con ERC en estadio 3 fueron aleatorizados en una proporción de 1:1 para no recibir prehidratación o prehidratación con 250 ml de bicarbonato de sodio al 1,4 %, administrado en una perfusión de una hora antes de someterse a una tomografía computarizada electiva con MC. | Se produjo una LRA poscontraste en 11 pacientes (2,1 %), de los cuales 7 de 262 (2,7 %) en el grupo sin prehidratación y 4 de 261 (1,5 %) en el grupo de prehidratación, lo que resultó en un RR de 1,7 (IC 95 %, 0,5-5,9; P = 0,36). | Al igual que Nijssen et al., 2017, soportan la no hidratación en pacientes con TFGe >30 ml/min |
Fuente: elaboración propia.
N-acetilcisteína (NAC)
Dado que las especies reactivas de oxígeno y los radicales libres han sido implicados dentro de la fisiopatología de la IRA-ACI, los agentes antioxidantes con capacidad de neutralizar estas moléculas se han vislumbrado como una opción preventiva. La N-acetilcisteína (NAC) tiene la capacidad de incrementar la actividad de la óxido nítrico sintetasa, aumentar los niveles de S- nitrosotiol (molécula que actúa como aceptor de radicales libres) y de amortiguar las metabolitos implicados en las vías metabólicas que conducen a la muerte celular mediada por isquemia y apoptosis [100].
Numerosos estudios han sido conducidos con el objetivo de evaluar la eficacia de este fármaco, mostrando resultados prometedores inicialmente, los cuales fueron diluyéndose a través del tiempo cuando se realizaban estudios con un diseño metodológico más riguroso y un mayor número de participantes. De hecho, los ensayos grandes (N > 500) han sido más homogéneos y no muestran un beneficio de la NAC en la prevención de la IRA-ACI [101].
Los metaanálisis muestran resultados contradictorios sobre el beneficio teórico del NAC en la prevención de la IRA-ACI; de igual forma, la marcada heterogeneidad entre los estudios incluidos en estos, los sesgos de publicación y los efectos de estudios pequeños, no permiten establecer conclusiones [44,102-104]. Adicionalmente, hay informes de que el NAC puede reducir artificialmente la CrS medida sin que ello refleje realmente una mejoría en la función renal, este fenómeno estaría relacionado directamente con su potencial capacidad de interferir con la técnica de medición in vitro [105], dicho fenómeno tendría un profundo efecto en los resultados clínicos, especialmente en los ensayos de IRA-ACI donde el potencial beneficio de la NAC como medida preventiva fue medido basados en un cambio en la creatinina como resultado y no en resultados clínicos como la necesidad de diálisis o la muerte. McCudden et al. evidenciaron que concentraciones muy altas (> 400 µg/ml) de NAC dan lugar a un sesgo negativo significativo (> 10%) para el método enzimático en la medición de la creatinina, además, no se observa ninguna interferencia con el método Jaffe, ni con otras medidas de la función renal como la cistatina-C y la proteína de traza beta [106]. Otro aspecto a considerar con relación a esta molécula es que puede asociarse con eventos adversos graves, como reacciones anafilactoides cuando es utilizada por vía IV [107].
Weisbord et al. condujeron el estudio controlado y aleatorizado con el mayor número de pacientes hasta el momento realizado, donde compararon NAC oral vs. placebo y hallaron tasas similares de IRA-ACI (9,1 vs. 8,7% (OR 1,06; IC 95 %, 0,87-1,28); P = 0,58), necesidad de diálisis a los 90 días (1,2 vs. 1,2 (OR 0,97; IC 95 %, 0,58-1,60; ); P = 0,90) o insuficiencia renal persistente a los 90 días (1,0 % frente a 1,1 % (OR 0,96, IC 95 %, 0,56-1,66); P = 0,89) y muerte (2,7 vs. 2,4% (OR 1,10, IC 95%, 0,78-1,57); P = 0,59). Los autores concluyeron que entre los pacientes con alto riesgo de complicaciones renales que se sometieron a una angiografía, no hubo ningún beneficio de la NAC oral sobre el placebo para la prevención de la muerte, la necesidad de diálisis o la disminución persistente de la función renal a los 90 días o para la prevención de LRA asociada al uso de MC [66].
Magner et al. elaboraron un metaanálisis de 101 ensayos clínicos aleatorizados, evidenciando que la NAC se asoció con la prevención de la IRA-ACI cuando todos los estudios se consideraron juntos, utilizando un modelo de regresión de efectos fijos o un análisis de efectos aleatorios; sin embargo, existió una heterogeneidad estadística sustancial y un sesgo de publicación, lo que socavó la validez de estas estimaciones agrupadas. Cuando se restringió el análisis a ensayos con un mayor tamaño muestral (es decir, ensayos con un tamaño de muestra superior a 500 o tasas de eventos superiores a 100), o analizaron los ensayos con resultados clínicos no bioquímicos, se redujeron estos problemas y se alcanzó un efecto nulo en la prevención de la IRA-ACI [101].
Conclusión: no existe evidencia que soporte la utilización de la NAC como medida profiláctica para la prevención de la IRA-ACI, por lo que este consenso no recomienda su uso.
Estatinas
No existe un mecanismo claro que explique el potencial papel nefroprotector de las estatinas para la prevención del desarrollo de IRA-ACI. La evidencia actual no es concluyente e incluso en algunos casos es contradictoria. Los ensayos que demostraron un probable papel en la reducción de la injuria renal posterior a la exposición al MC han sido realizados en pacientes sometidos a angiografía coronaria, los cuales son de alto riesgo cardiovascular y las estatinas hacen comúnmente parte de su manejo farmacológico de base [108-110]. De igual forma, otros autores como Toso et al. evidenciaron que una administración a corto plazo de altas dosis de atorvastatina antes y después de la exposición al MC, además de la hidratación IV estándar y la NAC oral, no disminuye la aparición de IRA-ACI en pacientes con ERC preexistente [111]. Estos hallazgos coinciden con los encontrados en un metaanálisis de ocho estudios (n = 5024) conducido por Subramaniam et al., donde no se estableció un beneficio concluyente de administrar estatinas más solución salina IV en comparación con la solución salina sola (RR, 0,68 IC 95 %, 0,39-1,20) [112].
Conclusión: no se recomienda el uso de estatina como medida preventiva para el desarrollo de IRA-ACI.
Otros fármacos
Son múltiples los fármacos que han sido postulados y evaluados a través de estudios como potenciales moléculas con capacidad de prevenir la IRA-ACI, aunque algunos de estos ensayos informan un pequeño beneficio, estos incluían un reducido número de participantes y un beneficio poco claro en los resultados clínicos. A menos de que se desarrollen ECA que incluyan muestras representativas y demuestren algún beneficio clínico, el uso de estos agentes para la prevención de la IRA-ACI no tendrán un nivel de evidencia sólida que permitan recomendarlos para su uso rutinario en los escenarios clínicos. Dentro de estas moléculas podríamos mencionar: teofilina [113], ácido ascórbico [114], trimetazidina [115], alopurinol [116], prostaglandina E1 [117], fenoldopam [118], alfa-tocoferol [119], nicorandil [120], péptidos natriuréticos [109], manitol o diuréticos [94,121] o dopamina [122].
Conclusión: la evidencia actual no soporta el uso de los siguientes fármacos como medida preventiva para el desarrollo de IRA-AC: teofilina, ácido ascórbico, trimetazidina, alopurinol, prostaglandina E1, fenoldopam, alfa-tocoferol, nicorandil, péptidos natriuréticos, manitol, diuréticos o dopamina. No recomendamos su uso como medida preventiva para el desarrollo de IRA-ACI.
15. ¿Existe evidencia del papel de la herbolaria o uso de plantas medicinales en la prevención de la IRA-ACI?
Fundamentados en el papel significativo del estrés oxidativo en la fisiopatología de la IRA-ACI, se han utilizado diferentes antioxidantes a base de hierbas tradicionales (los polifenoles y los carotenoides son los grupos más grandes de compuestos herbales antioxidantes) para la prevención de la IRA posterior al uso de MCI en diferentes estudios in vitro, modelos animales y humanos. Se han examinado plantas medicinales conocidas como: el jengibre (Zingiber officinale) [123], el té (Camellia sinensis) [124], la salvia roja asiática (Salvia miltiorrhiza) [125], la silimarina [126], la cúrcuma o turmérico (Curcuma longa) [127], el resveratrol [128] y la timoquinona [129]; sin embargo, la escasa representación de estos trabajos en humanos, su diseño in vitro y en modelos animales, no aportan un nivel de evidencia suficiente para recomendar su uso.
Conclusión: no existe en la actualidad evidencia que soporte el uso de preparados a base de plantas medicinales como medida preventiva para el desarrollo de IRA-ACI.
16. ¿La terapia de reemplazo renal posterior a la inyección del MC tiene algún beneficio como medida preventiva para reducir el riesgo de desarrollar IRA-ACI?
Técnicas de depuración extracorpóreas como la hemodiálisis (HD) y la hemofiltración (HF) han sido evaluadas como medidas preventivas para el desarrollo de IRA-ACI y dado que los MCI tienen un tamaño relativamente pequeño, lo que junto a su falta de unión a proteínas, los hacen susceptibles de ser extraídos de la circulación con estas técnicas. El uso de TRR para la prevención de IRA-ACI, desde un punto de vista teórico, se fundamenta precisamente en esta capacidad para eliminar el MC de la circulación y evitar así su interacción con el riñón, sin embargo, es poco probable que estas técnicas eviten dicho contacto con el parénquima renal, ya que se requieren pocos ciclos cardiacos para que el MCI sea distribuido por todo el organismo, una vez son inyectados en el torrente sanguíneo. Otra de las razones teóricas por las que las TRR podrían aportar un beneficio como mediada en la prevención de la IRA-ACI, se relaciona con la potencial carga de volumen asociada a los MCI, sin embargo, algunos estudios demuestran que el aumento del volumen extracelular después de una carga de contraste típica es mínimo [130].
Uno de los objetivos de instaurar medidas de nefroprotección en pacientes de alto riesgo de desarrollar IRA-ACI es precisamente evitar la necesidad de requerir una TRR, por lo que no resulta coherente utilizar este tipo de procedimientos como medida preventiva. Adicionalmente, este tipo de terapias extracorpóreas reducen los niveles de CrS, variable que es evaluada en la mayoría de los ensayos como desenlace para determinar el impacto de una estrategia de nefroprotección, por lo que podría aportar datos sobre un falso beneficio. Finalmente, las TRR no están exentas de complicaciones (sangrado, inestabilidad hemodinámica, infecciones, etc.), por lo que el riesgo supera el beneficio.
Para evaluar la eficacia de la TRR profiláctica después de la exposición al MC, Cruz et al. en una revisión sistemática y un metaanálisis agruparon los resultados de nueve ECA y dos no ECA (n = 1010), donde ocho estudios utilizaron la HD estándar, mientras que tres utilizaron modalidades continuas. Los autores no encontraron diferencias significativas en la incidencia de IRA-ACI entre los pacientes que se sometieron a HD y HF vs. aquellos con tratamiento médico estándar (RR 1,02I; IC 95 % 0,54-1,93). Además, la HD no ofreció ventajas significativas sobre el tratamiento estándar en cuanto a las necesidades de diálisis a largo plazo y la mortalidad [131]. Con relación a la diálisis peritoneal automatizada (APD) y la diálisis peritoneal ambulatoria continua (CAPD), se ha demostrado que también son efectivas para eliminar el MC (con menor eficiencia que la de la HD), pero sin que ello tenga un impacto sobre el desarrollo de IRA-ACI [132].
Finalmente, no se ha podido demostrar un beneficio claro de la realización de HD inmediatamente después de la inyección del MCI, ya que, pese a que la concentración del MC puede reducirse de manera efectiva mediante HD, esta no ofrece ninguna protección para el desarrollo de IRA-ACI [133].
Conclusión: no recomendamos el uso de TRR tipo HD, terapias lentas continuas o diálisis peritoneal en ninguna de sus modalidades (APD o CAPD), como estrategia para la prevención del desarrollo de IRA-ACI. Adicionalmente, en pacientes con ERC de base que se encuentran adscritos a un programa de HD crónica intermitente o de CAPD, el uso de la HD inmediatamente después de la inyección del MCI no está soportado por la evidencia actual, por lo que no se deben modificar los horarios programados para las sesiones de HD o para los recambios de líquido peritoneal previamente establecidos, excepto en aquellos pacientes que cursen con sobrecarga de volumen en el momento de la administración del medio de contraste.
17. ¿La presencia de función renal residual (FRR) en pacientes con enfermedad renal crónica estadio 5 en terapia de remplazo renal modifica las estrategias de nefroprotección?
Históricamente, se ha considerado que los MCI podrían reducir la FRR con la que cuentan algunos pacientes en TRR tipo HD o diálisis peritoneal (DP). Este hecho ha sido considerado de radical importancia, ya que en esta población (principalmente en HD) la FRR ha sido considerada un factor importante para la eliminación efectiva de moléculas pequeñas y medianas, el manejo de fluidos y la optimización del estado nutricional, incluido el manejo del fósforo y el potasio (independiente de la TFG que ya se ubica por debajo de los 15 ml/min). Adicionalmente, se ha asociado en algunos estudios con una mejor supervivencia del paciente y una mejor calidad de vida [134-136]. Este hecho ha conllevado a que, de manera tradicional, se utilice la presencia o no de volumen urinario residual (producción de orina > 100 ml/24 h) como criterio para la no utilización (si hay FRR) o utilización (si no hay FRR) de MCI en este grupo de pacientes.
En una revisión sistemática (9 estudios) y metaanálisis (7 estudios) que incluían a 434 pacientes, realizada por Oloko et al. [137], donde se analizó como desenlace principal el cambio de la función residual en pacientes en diálisis a los que se les ha administró un MCI intravas-cular, encontraron una diferencia ponderada en las medias de -0,16 ml/min/1,73 m2 (IC 95 % -0,66-0,34 ml/min; p = 0,53), lo que sugiere una pequeña reducción en la función residual después de la administración de un MC. Los autores concluyeron que los MCI administrados por vía intravascular pueden no dar lugar a una reducción significativa de la función residual en pacientes en diálisis, sin embargo, se observó una heterogeneidad significativa en los datos, con un Cochran Q de 35,83 y un I2 de 83,25 (p < 0,0001), lo que no permite emitir conceptos al respecto con base en estos resultados.
Cuando se opta por utilizar MCI en pacientes con ERC estadio 5 es porque nos enfrentamos a una situación donde no existe otra alternativa diagnóstica o terapéutica diferente a la que requiere MCI (por ejemplo: coronariografía) o existe un riesgo fatal inminente, por lo que su uso estaría plenamente justificado. En otros escenarios, donde los procedimientos son programados y la condición patológica no reviste una condición potencialmente fatal de forma inmediata, se debe tener en cuenta la importancia de la FRR y considerar otras alternativas diagnósticas que no utilicen MCI, con un buen rendimiento diagnóstico que permita una adecuada interpretación de los resultados.
Conclusión: la preservación de la FRR (volumen urinario > 100 ml/24 h) es un objetivo para tener en cuenta en pacientes con TRR tipo HD o diálisis peritoneal (DP), ya que mejora los resultados en términos de morbilidad y mortalidad, por lo tanto, se deben considerar otras alternativas diagnósticas que no utilicen MCI y no impliquen un riesgo de reducir la FRR en esta población (por ejemplo: ultrasonidos o resonancias magnéticas). En caso de que se decida usar el MCI debido a una condición potencialmente fatal o que no exista una modalidad diagnóstica alternativa, se deben utilizar las dosis recomendadas, en procura de evitar resultados con poca capacidad diagnóstica que no permitan tomar conductas terapéuticas o que obliguen a la repetición del procedimiento, conllevando a una mayor dosificación del MCI.
18. ¿La administración de dosis repetidas de MCI en pacientes de alto riesgo de desarrollar IRA-ACI requiere de un intervalo de tiempo mínimo entre el primer procedimiento y los subsiguientes?
Al tener en cuenta que el riesgo de IRA posterior a la exposición al MCI se relaciona de manera directa con la presencia de este en el torrente sanguíneo, se infiere que los estudios repetitivos confieren un mayor riesgo de desarrollar IRA-ACI. Dos estudios han demostrado la aparición de IRA-ACI en pacientes que recibieron una segunda dosis de MCI para la realización de imágenes con MC.
Abujudeh et al. [138] realizaron 328 TAC con medio de contraste (2 en cada paciente), con un intervalo promedio de separación de 11,4 horas, de los cuales 21 pacientes (12,8%) desarrollaron IRA-ACI. Al comparar a los pacientes con y sin IRA-ACI, el único factor de riesgo estadísticamente significativo fue un aumento de la CrS entre el primer y el segundo examen de la TAC, con un OR 18 (P < 0,0005). Posteriormente, Trivedi et al. [139] sometieron a 28 sujetos a una segunda TAC con MC después de un intervalo medio de 20 ± 13 días. Se evidenció un aumento significativo en la CrS antes vs. después de la aplicación del MCI (0,86 ± 0,15 vs. 0,93 ± 0,14 mg/dL, p = 0,027); y una disminución en TFGe (89,8 ± 13 vs. TFGe 83,9 ± 13,5 ml/min/1,73 m2, p = 0,028), donde cuatro sujetos (14,3 %) desarrollaron IRA-ACI, sugiriendo un mayor riesgo con estudios repetidos. Ninguno de estos estudios evaluó específicamente si el riesgo de IRA-ACI aumentó en relación con haber tenido una sola exposición al contraste o ninguna.
Conclusión: consideramos razonable evitar exposiciones repetidas a los MC durante un lapso menor a las 48 horas para procedimientos electivos en pacientes del alto riesgo de IRA-ACI (TFGe ≤ 30, IRA o administración IA de altos volúmenes de MCI). No se deben limitar las dosis repetidas en pacientes de menor riesgo (TFGe ≥ 30, sin IRA o vía IV) cuando exista una necesidad justificada de repetir el procedimiento. De igual forma, ante una enfermedad potencialmente fatal, está plenamente justificada la repetición de la dosis de MCI independiente del tiempo transcurrido entre un procedimiento y otro, para establecer un diagnóstico y una conducta terapéutica.
19. ¿Está contraindicado el uso de MCI en pacientes con trasplante renal?
Rong-Lee et al. [140] evaluaron 641 receptores de trasplante renal, encontrando una incidencia de IRA posterior al uso de MC de 2,8 % vs. el 0,9 % en pacientes sin trasplante de riñón (P = <0,01), adicionalmente, el uso de warfarina basal con un OR de 4,73 (IC 95 % 1,62-13,8, P = 0,03) y la mala función de aloinjerto (TFGe < 60 ml/min) con un OR de 4,04 (IC 95 % 1,12-14,5 P = < 0,01), se asociaron significativamente con un mayor riesgo de IRA-ACI. Con base en los puntajes de propensión, concluyeron que no encontraron un mayor riesgo de desarrollar IRA-ACI en receptores de trasplante renal sometidos a intervenciones vasculares periféricas en comparación con los pacientes sin trasplante de riñón, además, la incidencia fue muy baja (2,8 %) y sin impacto en la sobrevida.
Conclusión: los MCI pueden utilizarse en el paciente trasplantado renal en las dosis recomendadas para individuos no trasplantados, dado que el riesgo de IRA-ACI en receptores de trasplante renal no difiere de forma significativa con respecto a la población general. La TFGe continúa siendo el factor de riesgo más importante para el desarrollo de IRA-ACI en este grupo poblacional.
20. ¿Los pacientes de alto riesgo para el desarrollo de IRA-ACI sometidos a estudios con MC requieren algún tipo de seguimiento posterior a la inyección del medio?
No existen estudios que evalúen la necesidad de seguimiento de los pacientes expuestos a MCI, por lo que cualquier recomendación al respecto se deriva del conocimiento actual del comportamiento cinético de la creatinina y del horizonte clínico de la IRA-ACI. Para emitir cualquier recomendación sobre la medición de la CrS, es imprescindible tener en cuenta que la elevación de esta ocurre dentro de las 24-48 horas después de la exposición a un MCI y que el pico de creatinina ocurre dentro de los 3 a 5 días luego de la aplicación del MCI [141].
Conclusión: dado que los pacientes con TFGe < 30 ml/min/1,73 m2 o IRA son considerados de alto riesgo para desarrollar IRA-ACI, recomendamos realizar una medición de CrS de seguimiento a las 24 horas de la inyección del MCI, independientemente de la vía de administración (IV o IA). Esta misma recomendación aplica para pacientes sometidos a exposición renal de primer paso al MCI con TFGe < 45 ml/min/1,73 m2.
Dado que los pacientes con TFGe > 30 ml/min/1,73 m2 presentan un bajo riesgo de desarrollar IRA-ACI, no recomendamos la medición de una CrS de seguimiento en este grupo, sin embargo, se debe instruir a todos los pacientes que han sido expuestos a un MCI - independientemente de su TFGe para la realización de intervenciones diagnósticas o terapéuticas a través de cualquier vía, sobre la necesidad de consultar al servicio de emergencias en caso de presentar algún signo o síntoma que sugiera el desarrollo de una IRA en los días posteriores a la inyección del MCI: disminución del volumen de orina excretado, cambio en el aspecto o color de la orina, edema de miembros inferiores o disnea.
21. ¿Qué grupo de pacientes requieren valoración por Nefrología, previa y posteriormente a la inyección de un MCI?
Ante una enfermedad potencialmente fatal, donde el procedimiento diagnóstico o terapéutico con MCI sea la única opción por seguir, se debe realizar sin importar la condición renal de base o el riesgo de subsecuente daño renal y no amerita valoración previa por Nefrología.
En el contexto de procedimientos con MC programados, la primera pregunta que debemos resolver es si existe otra alternativa que no utilice MCI, sin que ello afecte el potencial beneficio que podría aportar la imagen con un MC basado en yodo. En casos de procedimientos diagnósticos o terapéuticos programados que requieran el uso de MCI como única alternativa, incluso en pacientes de alto riesgo (por ejemplo, con TFGe < 45 ml/min/1,73 m2 para exposición renal de primer paso y TFGe < 30 ml/min/1,73 m2 para exposición renal de segundo paso), con comorbilidades u otras condiciones asociadas que incrementen el riesgo de IRA-ACI, debe considerarse la valoración previa y posterior a la inyección del MC por Nefrología.
Conclusión: en el caso de una condición clínica potencialmente fatal, donde la realización de un procedimiento que implique el uso de un MCI sea obligatoria para establecer un diagnóstico o una conducta terapéutica que pueda resguardar la vida del paciente, no se debe retrasar su realización en espera de conceptos por alguna especialidad médica en particular.
Recomendamos la valoración por Nefrología previa y posterior al procedimiento con MC (con CrS realizada 24 horas después de la inyección del MCI), en pacientes de alto riesgo (TFGe < 30 ml/min/1,73 m2) indistintamente de la vía a través de la cual se inyecte el MCI (IV o IA) y en aquellos pacientes sometidos a exposición renal de primer paso al MCI, cuya TFGe sea < 45 ml/min/1,73 m2 programados para procedimientos no urgentes.
22. ¿Qué aspectos diferenciales relacionados con la IRA-ACI deben tenerse en cuenta en la población pediátrica para el uso de MCI?
Debido a que los pacientes pediátricos y en especial los recién nacidos son más propensos a desequilibrio hidroelectrolítico, en este grupo de edad se recomienda utilizar MC de baja osmolalidad, no iónicos, a una dosis que no exceda los 2 ml/kg. En los recién nacidos, la dosis máxima es de 4-6 ml/kg de peso corporal, particularmente en imágenes cardiacas.
En ausencia de insuficiencia renal conocida, los recién nacidos no parecen tener un mayor riesgo de desarrollar toxicidad renal debido a la administración IV de MC basado en yodo [142].
La IRA-ACI es una patología conocida en los pacientes adultos, pero hay poca información disponible sobre la incidencia, los factores de riesgo y el impacto pronóstico en la población pediátrica. Aunque se necesitan estudios adicionales en el entorno pediátrico, los datos sugieren que los médicos deben mantener un alto grado de sospecha hacia esta complicación entre los pacientes pediátricos [143].
La osmolalidad de los medios de contraste es de particular importancia en recién nacidos y en población pediátrica, debido a que son especialmente susceptibles a los cambios de fluidos y tienen una menor tolerancia a las cargas osmóticas intravasculares cuando se comparan con los adultos [144]. Si el volumen recibido de líquido es grande, puede producirse insuficiencia cardiaca y edema pulmonar; además, los niños con disfunción cardiaca significativa preexistente pueden correr un mayor riesgo [145].
La viscosidad es una propiedad física de los MCI especialmente importante para los pacientes pediátricos, debido al uso de angiocatéteres de pequeño calibre en pequeños vasos sanguíneos. Por otra parte, la viscosidad del MC y el tamaño del angiocatéter son factores importantes para determinar las velocidades máximas de inyección, si la viscosidad del medio es alta, pueden surgir dos problemas: primero, es posible que no se alcance el caudal de inyección deseado y, en segundo lugar, la alta presión puede provocar el fallo del catéter o la lesión del vaso [146].
En algunos casos, una tasa de inyección más lenta (en comparación con la que se usa en niños mayores y adultos) puede ser útil para prolongar el realce intravascular. En segundo lugar, los angiocatéteres de calibre pequeño (por ejemplo: de calibre 24) ubicados en pequeñas venas periféricas (en la mano o el pie) se utilizan comúnmente en recién nacidos y lactantes, pero cuando se cree que el acceso es tenue, se debe considerar seriamente la inyección manual de MC para minimizar el riesgo de lesión de los vasos y la extravasación [147].
Injuria renal asociada al uso de medios de contraste en niños
Los efectos de los MC en los riñones son similares entre niños y adultos.
Medición de la función renal en niños
La concentración sérica de creatinina refleja el equilibrio entre la producción y la excreción de creatinina. La creatinina es un producto de descomposición del músculo esquelético y su tasa de producción es proporcional a la masa muscular, la cual depende de una variedad de factores, incluyendo la edad del paciente, el sexo y el nivel de actividad física.
Las concentraciones de creatinina, por lo tanto, son bastante variables en pacientes pediátricos, incluso en presencia de un riñón preservado, por lo tanto, las concentraciones normales de creatinina en adultos no se pueden aplicar a la población pediátrica. Las concentraciones normales de CrS pediátrica aumentan con la edad.
La TFG es el método usado para definir la función renal previa a la administración de MC, utilizando la fórmula de Schwartz modificada [148].
Fórmula: Bedside Schwartz modificada
Tasa de filtración glomerular (ml/min/1,73 m2) = (0,413 * altura) / creatinina sérica.
• Talla en cms • Creatinina sérica en mg/dl [149].
La tabla 6 muestra los rangos normales para la TFG en población pediátrica según la edad en meses.
Tabla 6 TFG Según la edad
| Edad (meses) | FGR media ± DS (ml/min/1,73 m3) |
|---|---|
| ≥ 1,2 | 52 ± 9 |
| 1,2 - 3,6 | 61,7 ± 14,3 |
| 3,6 ± 7,9 | 71,7 ± 13,9 |
| 7,9 - 12 8 | 82,6 ± 17,3 |
| 12 - 18 | 91,5 ± 17,8 |
| 18-24 9 | 94,5 ± 18,1 |
| >24 | 104,4 ± 19,9 |
Fuente: [150].
Conclusión: no existe evidencia concluyente de que la población pediátrica tenga un mayor riesgo de desarrollar IRA-ACI con respecto a la población adulta. La osmolalidad de los MC es de particular importancia en recién nacidos y en población pediátrica, debido a que son especialmente susceptibles a los cambios de fluidos y tienen una menor tolerancia a las cargas osmóticas intravasculares cuando se comparan con los adultos, por lo que recomendamos utilizar MC de baja osmolalidad, no iónicos, a una dosis que no exceda los 2 ml/kg. En los recién nacidos, la dosis máxima es de 4-6 ml/kg de peso corporal, particularmente en imágenes cardiacas. Adicionalmente, el uso de angiocatéteres de pequeño calibre obligan a considerar la viscosidad y la velocidad de infusión cómo factores para tener en cuenta en la población pediátrica. Finalmente, la TFG es el método usado para definir la función renal previa a la administración de medios de contraste, utilizando la fórmula de Schwartz modificada.