Introducción
El mecanismo multiplicador de contracorriente (MMCC) ha significado un gran desafío para los fisiólogos y nefrólogos a lo largo de los años. Incluso, en la actualidad, sus mecanismos no están totalmente comprendidos en detalle y existen diversas hipótesis que intentan explicar la hiperosmolaridad de la médula interna y la papila renal.
La comprensión de los estudiantes de Medicina de pregrado y posgrado del MMCC es fundamental para el entendimiento de la concentración y dilución urinaria en humanos.
En el año 2023, en la asignatura "Biofísica y Fisiología Humana" de segundo año de la carrera de Medicina del Instituto Universitario Italiano de Rosario (IUNIR), un 36 % de los alumnos respondieron de manera incorrecta las preguntas referidas a los mecanismos de generación de un intersticio renal hiperosmótico y un 57 % de manera incorrecta a preguntas referidas a los conceptos básicos de mecanismo e intercambio por contracorriente (datos de los autores, no publicados a la fecha), habiendo adquirido los conocimientos a partir de la bibliografía "tradicionalmente" recomendada por la asignatura.
Debido a lo antedicho, se radicó un proyecto de investigación y docencia denominado "Mecanismo multiplicador por contracorriente del asa de Henle (AH). Impacto del cambio de bibliografía en estudiantes de fisiología de segundo año de la carrera Medicina" (CAI ININVI 07/24), en el cual se plantea la comparación del rendimiento académico de alumnos que adquirieron conocimientos de la bibliografía tradicional de la asignatura versus los que realizaron una revisión multibibliográfica.
Materiales y métodos
El presente trabajo es una revisión narrativa que sintetiza el funcionamiento y fundamento fisiológico del MMCC. La búsqueda bibliográfica se realizó en las siguientes bases de datos: Pudmed, Medline, Scopus, SciELO, Latindex y Google académico.
Resultados
Breve revisión histórica
Al final de la era mesozoica, los mamíferos migraron de la vida acuática a la terrestre. Como consecuencia, fueron privados del acceso libre al agua y al sodio, y la adaptación a esa nueva condición medioambiental fue conservar la capacidad excretora de "desechos", aunque por separado a la conservación y manejo fisiológico del sodio y agua libre, por el sistema renal [1]. Esta capacidad de producir orina hipertónica solo la han logrado algunas aves y mamíferos, para sobrevivir a condiciones de limitado acceso al agua [1].
El mecanismo por el que los riñones logran conservar agua libre es complejo y se explica por la especificidad de ciertos segmentos de la nefrona y su vasculatura especializada [1].
Evolución histórica del concepto
En el año 1842, William Bowman describió la similitud entre las células tubulares renales y el epitelio intestinal, desarrollando el concepto de la separación de la porción acuosa de la sangre y la excreción independiente de sales y agua [2, 3]. Esta teoría "excretora" de la formación del orina sería más tarde conocida como hipótesis de "Bowman-Heidenhain" (por el apoyo de Rudolf Heidenhain en 1874) o hipótesis "vitalista".
Simultáneamente, en 1842, Carl Ludwing, fisiólogo alemán, introdujo la hipótesis del glomérulo como filtro que producía un ultrafiltrado de la sangre, libre de células y proteínas, pero con el resto de los componentes sin modificaciones respecto al plasma. Ludwing también describió que el filtrado glomerular (FG) era influenciado por la presión hidrostática en la arteria renal y que, a su paso por los túbulos uriníferos, sufría procesos que alteraban las concentraciones finales de sustancias en la orina [4]. Esta teoría fue denominada "mecanicista".
La primera descripción, con similitud a la histología actual de los túbulos renales, se atribuyó a Friedrich Gustav Jakob Henle, quien en 1862 describió la porción tubular en "asa" que, desde entonces, lleva su nombre, en su monografía: "Zur Anatomie der Niere" [5, 6]. Mientras tanto, Homer William Smith se negaba a otorgarle un valor fisiológico a este segmento de la nefrona, ya que lo consideraba un remanente embrionario.
Smith, fisiólogo y escritor científico estadounidense, conocido por sus experimentos sobre el riñón, realizó importantes descubrimientos de la fisiología renal. Uno de sus hallazgos más importantes fue el rol crucial del flujo sanguíneo renal en la homeostasis. En sus trabajos, Smith demostró que los riñones podían autorregular su propio flujo sanguíneo, mediante la producción de sustancias vasoactivas y otros mecanismos de ajuste; además, describió a la nefrona como una estructura compleja, compuesta por un glomérulo y por la cápsula de Bowman, que funcionaban en conjunto para "filtrar" los componentes del plasma sanguíneo hacia los túbulos renales. En ese punto, comenzó la idea de que, a medida que el "líquido filtrado" se movilizaba a través de los túbulos renales, se eliminaban los desechos y se reabsorbían los nutrientes y las sustancias esenciales para la homeostasis corporal. Estos son los conceptos que hoy se conocen como "reabsorción" y "secreción" tubular [7,8].
Durante los años siguientes, coexistieron ambas teorías ("vitalista" y "mecanicista") en controversia y los conceptos de Henle fueron, inicialmente, negados.
Es por esta razón que, hasta el año 1950, la nefrona se esquematizaba de forma rectilínea, como se muestra en la figura 1, eliminando la idea del "asa" de Henle.
En el año 1922, Alfred Richards y Plant introdujeron un nuevo método de investigación de la función renal denominado: técnica de micropunción, mediante el cual, comprobaron que la hipótesis "mecanicista" era la que mejor explicaba el mecanismo de formación de orina [9].
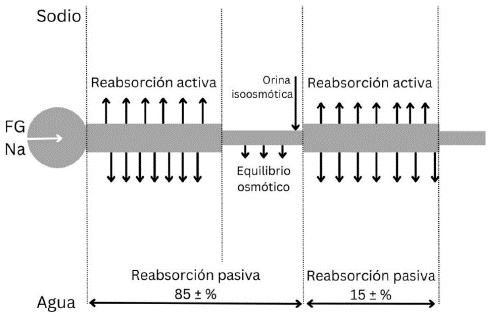
Fuente: modificado de [5].
Figura 1 Concepto "lineal" de la nefrona según Homer William Smith en 1950
En 1952, Gottschalk, con técnicas de micropunción y microosmómetro, demostró que, en roedores, los fluidos contenidos en el AH, túbulos colectores y vasos rectos eran hiperosmóticos en la médula renal y tenían igual presión osmótica al mismo nivel [10,11].
Al ampliar los experimentos, se demostró que la permeabilidad al agua de la rama delgada descendente (RDD) del AH superaba la de la rama delgada ascendente (RDA). Por último, estos experimentos demostraron que la permeabilidad al agua y la concentración de orina en la RDD del AH eran independientes de la presencia de hormona antidiurética (ADH, según sus siglas en inglés) y que la concentración final de la orina tenía lugar en el túbulo colector (TC) medular [10].
En el año 1967, el principio conocido como multiplicador por contracorriente fue planteado por Heinrich Wirz, mecanismo en que dos flujos opuestos de líquido tubular, (LT) en la rama descendente y en la rama ascendente del AH, jugaban un papel crítico [12].
Este concepto surgió de observaciones de que todos los vertebrados pueden eliminar orina isotónica y diluida, pero solo los mamíferos y algunas aves eran capaces de excretar orina concentrada y compensar un déficit de agua libre. Para que este concepto fuese posible, la nefrona no podía ser "lineal", por lo que se abandonó ese esquema y emergió el de "asa", como se conoce hoy en día (figura 2).
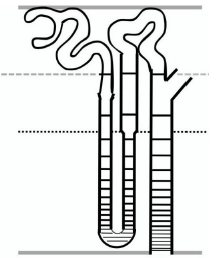
Nota. Se indicaba el aumento progresivo de la presión osmótica desde la corteza a la médula mediante las líneas transversales.
Fuente: modificado de [5].
Figura 2 Concepto de la nefrona según Wirz
Aspectos generales de la concentración y dilución de la orina a nivel tubular
En circunstancias fisiológicas, la excreción de agua se regula independientemente de la de solutos. Para que esto ocurra, los riñones deben ser capaces de excretar orina hipo o hiperosmótica con relación al plasma, lo que a su vez exige que los solutos se separen del agua en algún trayecto a lo largo de la nefrona [13-16].
La reabsorción de solutos en el túbulo proximal (TP) condiciona la reabsorción de una cantidad proporcional de agua (segmento de la nefrona permeable al agua y solutos); es decir que, en este segmento de la nefrona, no se produce separación de los procesos de reabsorción de agua y solutos. En cambio, en el AH, más especialmente en su rama gruesa ascendente (RGA) (segmento de la nefrona permeable a solutos, pero no al agua) del AH, es donde se produce la separación de la reabsorción de ambos compuestos. Como consecuencia de esta capacidad de separar agua y solutos, el AH cumple dos funciones básicas y fundamentales: i) diluir el LT, lo cual permite excretar orina diluida en ausencia de ADH y ii) lograr que el líquido intersticial (LI) de la médula renal a este nivel, sea hiperosmótico respecto al plasma, siendo el intersticio hiperosmótico fundamental para la excreción de orina concentrada, ya que establece un gradiente osmótico a través de la pared del TC y, por tanto, permite la reabsorción de agua, cuando la ADH aumenta la permeabilidad para el agua de las células que revisten el TC (mecanismo de acción de la ADH) [13-16]. La tabla 1 muestra las propiedades diferenciales de los distintos segmentos tubulares.
Tabla 1 Propiedades diferenciales de los distintos segmentos tubulares
| Segmento tubular | Permeabilidad a H2O | Permeabilidad a NaCl | Permeabilidad a urea | Trasporte activo de iones |
| RDD | Sí ++++ | Sí ± | Sí + | No |
| RDA | Sí ± | Sí +++ | Sí + | No |
| RGA | Sí ± | No? | No | Sí ++++ |
| TCD | Sí +++ | No ± | No? | ? |
| TCC | Sí +++ | No ± | No | Sí ++ |
| TCP | Sí +++ | No ± | No | Sí + |
Nota. RDA: rama delgada ascendente; RDD: rama delgada descendente; RGA: rama gruesa ascendente; TCC: túbulos colectores corticales; TCD: túbulo contorneado distal; TCP: túbulos colectores papilares.
Fuente: modificado de [5].
Características principales del sistema
El LT que ingresa a la RDD del AH desde el TP es isosmótico respecto al plasma, esto refleja la naturaleza isosmótica de la reabsorción de agua y de solutos en el TP.
La permeabilidad de la RDD del AH, en cambio, es muy alta al agua, pero mucho menor a la de solutos, NaCl y urea (lo que implica mayor posibilidad de reabsorción de agua que de solutos a este nivel). En consecuencia, al ir profundizando el LT en la médula hiperosmótica, se reabsorbe agua. En consecuencia, el LT tendrá, en la curva del asa, una osmolaridad igual a la del LI circundante. Aunque las osmolaridades de ambos líquidos (tubular e intersticial) son similares a este nivel, su composición química es muy diferente, la concentración relativa de NaCl es mayor en el LT, mientras que la de urea es mayor en el LI.
La RDA del AH es impermeable al agua, pero permeable a NaCl y urea. En consecuencia, al ascender el LT por el asa ascendente, se reabsorbe pasivamente NaCl y urea (ya que, por las características antes mencionadas del asa descendente, en el LT del asa ascendente, la concentración de NaCl y urea es mayor que la intersticial), aunque con mayor intensidad se produce reabsorción de NaCl que de urea. El efecto neto en el LT, a todo lo largo de la RDA, es, entonces, el siguiente: i) el volumen permanece sin cambios, ii) la concentración de NaCl disminuye y iii) la concentración de urea aumenta.
La RGA del AH es impermeable al agua y a la urea. Esta porción de la nefrona, en cambio, reabsorbe activamente NaCl y, por lo tanto, diluye el LT. Esa dilución es máxima en este punto de la nefrona (segmento dilutor) y el LT que egresa de la RGA tiene una osmolaridad aproximada de 150 mOsm/kg H2O.
El túbulo distal (TD) y el TC cortical reabsorben activamente NaCl y son impermeables a la urea. En ausencia de ADH, la permeabilidad de este segmento de la nefrona al agua es baja. Por lo tanto, cuando hay ausencia o niveles bajos de ADH (osmolaridad plasmática baja), el TD y el TC cortical son impermeables al agua. La osmolaridad del LT en estos segmentos disminuye aún más, al reabsorberse NaCl sin agua. Además, el LT que llega al TC cortical es hipoosmótico respecto al plasma, con una osmolaridad aproximada de 100 mOsm/kg de H2O.
El TC medular reabsorbe activamente NaCl e, incluso, en ausencia de ADH es ligeramente permeable al agua y a la urea. En consecuencia, cantidades escasas de urea pasan desde el intersticio medular al LT del TC y se reabsorbe un pequeño volumen de agua.
En este contexto de ausencia de ADH, se continúa la dilución urinaria y la orina finalmente excretada tendrá una osmolaridad aproximada de 50 mOsm/kg de H2O.
Por el contrario, a continuación, se considerará como excretan orina concentrada los riñones (antidiuresis) cuando la osmolaridad plasmática y los niveles de ADH son elevados:
1-4. Los pasos del 1 al 4 del apartado anterior son similares en situaciones en las que se produce una orina concentrada o diluida; mientras que la reabsorción de NaCl por la RGA del AH diluye el LT, por otro lado, el NaCl se acumula en el intersticio. El acúmulo de NaCl y urea en el intersticio medular es de fundamental importancia para la producción de orina hiperoosmótica respecto al plasma, ya que proporciona las condiciones necesarias para la reabsorción de agua desde el TC al intersticio.
5. La reabsorción de NaCl por la RGA del AH hace que el LT que ingresa al TC sea hipo-osmótico respecto al LI vecino (circundante), por lo tanto, existe un gradiente osmótico entre ambos compartimientos. En presencia de ADH, que aumenta la permeabilidad del TC para el agua, esta difunde fuera de la luz tubular, lo cual aumenta la osmolaridad del LT. Así comienza el proceso de concentración urinaria.
La máxima osmolaridad que puede alcanzar el LT en el TC es de aproximadamente 300 mOsm/kg H2O, igualando la osmolaridad del LI y del plasma circundante (en los vasos peritubulares). Aunque el LT en este segmento de la nefrona tiene la misma osmolaridad con la que ingresó a la RDD del AH, su composición cambia radicalmente. Debido a la reabsorción producida en los segmentos previos de la nefrona, el NaCl participa en una porción mucho menor en la osmolaridad total del LT. La osmolaridad del LT a este nivel refleja la presencia de urea (urea filtrada + urea añadida en las RDD y ascendente del AH) y los otros solutos no reabsorbidos (como, por ejemplo, la creatinina).
6. La osmolaridad del LI a nivel medular aumenta progresivamente a partir de la unión cortico-medular (donde es de 300 mOsm/kg de H2O) hasta la profundidad a nivel de la papila (donde es de 1200 mOsm/Kg de H2O). Existe entonces, a este nivel, un gradiente osmótico entre ambos compartimientos (TL y LI) a lo largo de todo el trayecto del TC. En presencia de ADH (que hace al TC permeable al agua, con reabsorción de esta hacia el LI), la osmolaridad del LT aumenta. Debido a que se ha reabsorbido la mayor parte del NaCl y que la porción inicial del TC es impermeable a la urea, incluso en presencia de ADH, la urea permanece en el LT y su concentración aumenta, debido a la reabsorción de agua. En presencia de ADH, la porción distal del TC se hace permeable a la urea. Dado que, como se había explicado previamente, la concentración de urea había aumentado por la reabsorción de agua, algo de urea difundirá desde el LT al LI, aumentando así la concentración de urea en el LI medular. La osmolaridad máxima que puede alcanzar el LT del TC medular es igual a la del LI circundante a este nivel. Los principales componentes del LT a este nivel son las sustancias que han escapado a la reabsorción o han sido secretadas al LT. La más abundante de ellas es la urea (principal determinante de la osmolaridad del LT a este nivel).
La orina tendrá una osmolaridad de 1200 mOsm/kg de H2O y contendrá concentraciones altas de urea y otros solutos no reabsorbibles. La urea del LT tiende a equilibrarse con la urea del LI, por lo que, su concentración urinaria sobrepasará la intersticial (de aproximadamente unos 600 mOsm/kg de H2O) [13-16] (figura 3).
La generación de un intersticio medular hiperosmótico (que depende de la reabsorción de NaCl por la RGA del AH) es de importancia crítica para la capacidad renal de excretar orina hiperosmótica con respecto al plasma. Como se describió anteriormente, los principales determinantes de la osmolaridad del LI son NaCl y urea, y la distribución de estos solutos no es uniforme a lo largo de la médula. En la unión entre la médula y la corteza, la osmolaridad es de 300 mOsm/kg de H2O (determinada prácticamente por NaCl). Posteriormente, hacia la profundidad de la médula, las concentraciones de NaCl y urea aumentan progresivamente hasta que, a nivel de la papila, es de aproximadamente 1200 mOsm/kg de H2O (600 mOsm/kg de H2O atribuibles al NaCl y 600 mOsm/kg de H2O atribuibles a la urea).
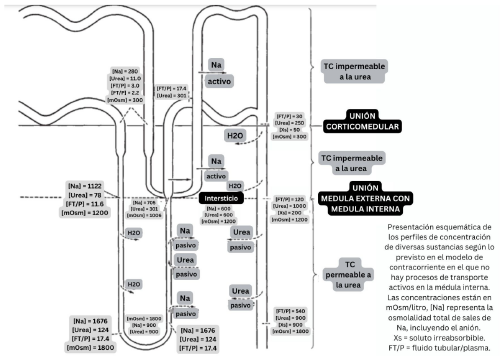
Fuente: modificado de [5].
Figura 3 Modelo de contracorriente en el que no hay transporte activo de solutos en la médula interna
El gradiente de NaCl medular es consecuencia del manejo tubular de este soluto en los distintos segmentos de la nefrona, como se explicó en los apartados anteriores. El acúmulo medular de urea es, sin embargo, más complejo y se produce con mayor eficacia cuando se genera orina hiperoosmótica, la permeabilidad de la mayoría de los segmentos de la nefrona a la urea es relativamente baja, con excepción del TC medular, especialmente en presencia de ADH. Al avanzar el LT a lo largo del interior de la nefrona, y especialmente al reabsorberse agua en el TC, aumenta la concentración de urea en el LT. Cuando el LT rico en contenido de urea llega al TC medular, donde la permeabilidad para la urea no es alta, sino que aumenta, especialmente en presencia de ADH, la urea difunde desde el LT al LI (a favor de gradiente de concentración), donde se acumula. Algo de urea entra a las asas ascendente y descendente de Henle (recirculación de la urea entre en TC y AH) y este proceso también sirve para atrapar y facilitar el acúmulo urea en la médula [13-16].
El intersticio hiperosmótico, como se comentó, es fundamental para la concentración del LT en el TC.
La reabsorción es un proceso pasivo que depende del gradiente osmótico, por lo que la concentración máxima que puede alcanzar la orina es igual a la del intersticio medular a nivel de la papila (aproximadamente 1200 mOsm/kg de H2O). Dado que para la concentración de la orina es fundamental un intersticio hiperoosmótico, cualquier variable que reduzca este gradiente (por ejemplo, una dieta hipoproteica) alterará la capacidad del riñón para concentrar la orina al máximo [13-16].
Función de los vasos rectos
Los vasos rectos, redes capilares que aportan sangre a la médula, son muy permeables al agua y a los solutos. Al igual que las asas de Henle, los vasos rectos forman una serie de asas paralelas en horquilla dentro de la médula, aportan nutrientes y O2 a los túbulos medulares y, lo que es más importante, eliminan el exceso de agua y solutos que pasan continuamente al intersticio medular desde los segmentos medulares de la nefrona, localizados en cada región. La capacidad de los vasos rectos para mantener el gradiente intersticial depende del flujo de sangre. A pesar de la disposición en contracorriente (opuesto al sentido del flujo del LT, ver detalle de "mecanismo de contracorriente", más adelante), un aumento importante del flujo sanguíneo a través de los vasos rectos acabará por disipar el gradiente medular [13-16].
La posibilidad de que el líquido en los vasos rectos ascendentes se vuelva relativamente hipotónico por la operación de gradientes de presión hidrostática, que fuerzan el agua desde los vasos rectos descendentes a los ascendentes, es poco probable por dos razones:
Los gradientes de presión hidrostática requeridos para generar gradientes osmóticos son mucho mayores de lo que se esperaría, razonablemente, en los "vasa recta".
Las mediciones directas realizadas por Jamison, Bennett y Berliner [17] mostraron que, en cualquier nivel dado de la médula, la sangre de los vasos rectos ascendentes estaba más concentrada que la sangre de los vasos rectos descendentes.
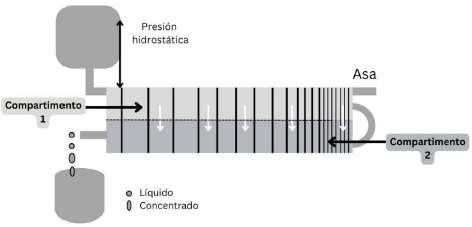
Mecanismo de contracorriente
El principio básico del mecanismo de contracorriente consiste en que dos corrientes que se mueven en dirección opuesta y que están yuxtapuestas intercambian entre sí energía o sustancias [13-16] (figura 4).
Multiplicación de contracorriente
Un sistema multiplicador de contracorriente puede aumentar enormemente la concentración mediante un simple intercambio osmótico. Un modelo de este tipo debe reunir las siguientes condiciones:
La presión hidrostática hace circular el líquido por el interior del tubo, pero también determina el pasaje de agua desde un compartimiento a otro, de manera que el líquido, a medida que circula en el compartimiento 1 (C1), se concentra progresivamente. De este modo, la presión osmótica aumenta en dirección al flujo de un extremo a otro del tubo (dentro del mismo C1) y ese aumento de presión osmótica se da, en paralelo, entre cada sección transversal de ambos tubos, pero en sentido opuesto entre los extremos de cada tubo, así: menor presión osmótica a la entrada del tubo 1, mayor presión osmótica a la salida del tubo 1, mayor presión osmótica a la entrada del tubo 2 y menor presión osmótica a la salida del tubo 1. Se generan, entonces, cambios transversales de osmolaridad en "capas" que se multiplican longitudinalmente desde la corteza a la médula (en el caso del riñón) (figura 4).
El AH, con la disposición de sus ramas ascendente y descendente, presenta las características de un sistema de contracorriente, aunque con algunas mínimas diferencias respecto al modelo descripto. La fuerza hidrostática es reemplazada por el transporte activo de NaCl en la rama ascendente gruesa y el intersticio medular separa a una rama de la otra. Cabe aclarar, además, que no todas las asas de Henle presentan la disposición descrita, ya que en el ser humano solo la sexta parte de las asas tienen ramas que llegan hasta el vértice de la papila [13-16].
Intercambio de contracorriente
El mantenimiento de la osmolaridad del intersticio medular depende de la particular disposición anatómica de los vasos rectos y de su alta permeabilidad. Su forma en U determina que la sangre que ingresa en la médula renal se encuentre en estrecho contacto con la que egresa de la zona. La alta permeabilidad de estos capilares da lugar a un rápido equilibrio de agua y solutos entre el plasma y el intersticio.
Por su parte, la sangre, al descender por los vasos rectos, pierde agua y gana NaCl y urea, de modo que en la parte extrema del asa capilar, la osmolaridad de la sangre del asa se equilibra con la del intersticio. Al ascender, el plasma gana nuevamente agua y pierde solutos, de esta forma se impide el "lavado" de los solutos acumulados en el intersticio por el mecanismo multiplicador del AH. A este fenómeno se le denomina intercambio de contracorriente (figura 4). La sangre que egresa de la médula lo hace con una ligera hiperosmolaridad (325 mOsm/kg de H2O), dado que el mecanismo intercambiador de contracorriente no es totalmente eficaz. Por esta razón, el "lavado" de solutos del intersticio es directamente proporcional al flujo sanguíneo de los vasos rectos que es, por otra parte, muy inferior al de la corteza. El flujo sanguíneo medular estaría regulado, en parte, por células contráctiles que rodean a los vasos rectos descendentes. Estas células son sensibles a la ADH y, posiblemente, a otros agentes humorales (angiotensina II, prostaglandinas) y al sistema nervioso simpático [13-16].
Integración de los mecanismos componentes del sistema
A nivel renal, este mecanismo es clave para la concentración/dilución de la orina. Durante la antidiuresis, la orina aparece diluida en el origen del túbulo distal, pero por la acción de la ADH se establece un equilibrio osmolar entre la orina y la sangre, comprendida en los vasos rectos que rodean a los túbulos que conforman la nefrona desde la mitad del túbulo distal, a partir del cual la orina permanece isosmótica hasta que ingresa al TC y, durante su trayecto, se concentra progresivamente [13-16].
En diuresis acuosa (ausencia de HAD), por el contrario, la orina permanece hipotónica desde que penetra al túbulo contorneado distal y se diluye aún más en el trayecto del túbulo colector, que es impermeable al agua y, además, le sustrae sodio a esta orina, ya de por sí diluida. Este proceso, hoy conocido y simplificado en la actualidad, que figura en los textos de fisiología humana, se explica por medio de la hipótesis del "mecanismo multiplicador por contracorriente del asa de Henle", un modelo matemático que contempla principios físicos y fisiológicos capaces de dar cuenta de casi la totalidad del proceso de concentración de orina en seres vivos, con excepción de ciertos mamíferos con capacidad de sobrevivir a condiciones extremas de deshidratación (hidropenia), por poder excretar orinas extremadamente concentradas [13-16].
Todo este sistema es posible por la existencia de los "vasa recta". Las reconstrucciones tridimensionales funcionales de los vasos rectos de la médula interna revelan varias relaciones espaciales que pueden ser significativas para el proceso de intercambio contracorriente vascular y el mecanismo de concentración urinaria. Estudios previos han demostrado que los grupos de conductos colectores forman el motivo organizador en la médula interna, con nefronas y vasos dispuestos dentro y alrededor de ellos, de manera organizada. Esta arquitectura conduce a dos compartimentos intersticiales distintos en la dimensión transversal: las regiones interclusión e intraclusión intersticial. Estos vasos podrían estar posicionados de manera única para participar en el intercambio contracorriente [13-16].
El flujo sanguíneo en la médula interna es un proceso dinámico que involucra múltiples mecanismos regulatorios dentro de una arquitectura fija. Las tasas y los patrones de flujo sanguíneo probablemente influyen en el grado en que los fluidos y solutos derivados de diferentes compartimentos endoteliales y epiteliales se mezclan entre sí y en la magnitud del intercambio a contracorriente de fluidos y solutos que ocurre dentro de cada haz vascular [13-16].
En líneas generales, el sistema opera para establecer un gradiente de concentración osmótica en el intersticio, que aumenta desde la unión cortico-medular hasta la punta del asa, y para concentrar la orina mediante la absorción pasiva de agua a través de los conductos colectores permeables al agua. Los "vasa recta" actúan como intercambiadores de contracorriente simples, promoviendo la eficiencia general y llevándose en las arterias ascendentes el agua extraída de la orina [13-16].
El LT que llega desde el TP es isosmótico, pero al penetrar en la médula pierde agua y se concentra progresivamente hasta alcanzar, en el vértice de la papila, la misma osmolaridad que existe en el intersticio (1200 mOsm/kg de H2O en el ser humano). Como se ha explicado, la contribución de la difusión de NaCl y de urea hacia el interior del asa es pequeña. El LT en el codo del asa tiene la misma osmolaridad que el intersticio, pero a expensas del aumento de la concentración de NaCl, mientras que hacia la punta de la papila, en el propio intersticio renal, la osmolaridad se debe, en situación de antidiuresis, en un 40 % a la acumulación de la urea [13-16].
El resultado final del mecanismo multiplicador de contracorriente es la producción de un intersticio hiperosmótico que proveerá el gradiente necesario para la reabsorción de agua en el TC. Este proceso es pasivo, pero depende en último término del transporte activo de NaCl a nivel de la rama ascendente gruesa [13-16].
Hipótesis para explicar la hiperosmolaridad de la médula interna y la papila. Teoría de Kokko y Rector
Describe un modelo (actualmente el más aceptado) de multiplicación contracorriente, donde tanto el AH descendente y el asa delgada ascendente operan puramente de forma pasiva, equilibrando los segmentos. Para que este modelo sea posible, deben coexistir ciertas características de cada segmento tubular, como se comentó en la sección "características principales del sistema". Los conceptos que se describieron previamente en este trabajo fueron basados en este modelo, el cual plantea que el proceso primario se genera por la salida de NaCl en la rama ascendente delgada, esto se expresa por la alta concentración de urea en el exterior de la médula del conducto distal que se transmite a la papila a través de la urea que difunde por su gradiente de concentración. A su vez, la urea intersticial papilar abstrae agua de la rama descendente delgada, generando altas concentraciones intraluminales de NaCl, lo que permite que todo el sistema funcione mediante la difusión pasiva de NaCl desde la rama ascendente delgada.
Para que este modelo se cumpla, es necesario que el asa ascendente delgada sea más permeable al NaCl que a la urea y relativamente impermeable al flujo osmótico del agua, así puede generar el fluido hipoosmótico de manera pasiva, permitiendo un flujo neto de NaCl del LT al intersticio mayor que el desplazamiento opuesto de la urea.
Entonces, el LT hipertónico con alta concentración de sal y baja concentración de urea asciende por la rama delgada ascendente del AH, hacia una región de hipertonicidad intersticial ligeramente menor. Además, existen tres fuerzas motrices importantes:
Una pequeña fuerza osmótica para el flujo de agua hacia el LT.
Un gran gradiente de concentración para la difusión de urea hacia el LT.
Un gran gradiente de concentración para la difusión de NaCl hacia el intersticio.
Si la permeabilidad al flujo osmótico de agua fuera relativamente baja y la permeabilidad a NaCl fuera mayor que la de la urea, habría relativamente poco movimiento de agua y el movimiento neto de NaCl al intersticio superaría al movimiento neto de urea hacia el LT. Como consecuencia de esta difusión pasiva de NaCl al hacia el intersticio, el LT se volvería hipotónico en relación con el líquido circundante.
Discusión
Perspectivas adicionales al modelo "clásico"
En el concepto del "clásico" MMCC anteriormente descripto, el LI hiperosmótico se genera por transporte activo de NaCl en la RGA (impermeable al agua), esto explicó la hiperosmolaridad en la médula externa, pero era insuficiente para elucidar el gradiente osmótico en la médula interna.
Posteriormente, fue descrito que, en este sector medular, el mecanismo era "pasivo", debido a la concentración de urea en el LI por reabsorción pasiva de NaCl y agua en los TC (impermeables a la urea) [18,19]. El descubrimiento de transportadores de urea (UT-A1, UT-A3), regulados por vía ADH, modificó algunos conceptos "clásicos" del MMCC. Dichos transportadores permiten el pasaje de urea desde los TC al LI, una acción de la ADH diferente a la clásicamente conocida del aumento de la permeabilidad al agua en los TC, a través de canales de acuaporinas (AQP1) [20].
Por último, importantes hallazgos fueron reportados por Dantzler et al., quienes obtuvieron reconstrucciones tridimensionales de RDD y RDA del AH y "vasa recta" en la médula interna de riñones de roedores [20]. En sus experimentos, demostraron que asumir que el conjunto de TC era altamente permeable al agua era incorrecto. Sus resultados mostraron que los TC de AH, que tienen sus bucles dentro del primer milímetro de la medular interna (aproximadamente un 40 % de las AH en la medular interna), no expresaban canales AQP1 en toda su longitud, mientras que los TC de bucles más largos (60 % restante), expresaban canales AQP1 solo en el 40 % inicial de su longitud [20].
La presencia del canal de cloruro ClC-K1 comienza en el segmento prebucle de la RDD y continúa a lo largo de la RDA, lo que explica la alta permeabilidad al cloruro del AH [20]. Otro de sus hallazgos de jerarquía, respecto al tema, fue la organización tridimensional del sistema tubular y de "vasa recta" en la medular interna. Estos autores reportaron que los TC tendían a converger en la medida que progresaban desde la corteza hacia la médula renal, formando clústeres. Las RDD y los "vasa recta" descendentes se encontraban en regiones periféricas de dichos clústeres (región denominada por los autores como interclústeres), mientras que las RDA y los "vasa recta" ascendentes se encontraban tanto en regiones periféricas como en regiones cercanas al eje de dichos clústeres (región denominada por los autores como intra-clústeres) [20]. La disposición de los "vasa recta" ascendentes, RDA y TC dentro de los clústeres forma espacios nodales intersticiales rodeados por células intersticiales laterales, creando así microdominios para la mezcla de solutos y agua [20].